Чужеродный сорняк: ваточник яркий угрожает полям и природе Европы
Биологические инвазии угрожают биоразнообразию и агроэкосистемам, а системы раннего оповещения позволяют минимизировать распространение чужеродных инвазионных видов при ограниченных ресурсах. В данном исследовании документируется присутствие чужеродного растения Asclepias speciosa Torr., произрастающего в Северной Америке, который был впервые обнаружен в 2022 году на горе Вронту, Центральная Македония, Северная Греция. Это вторая европейская находка данного чужеродного вида после Литвы, подтверждающая его способность адаптироваться к контрастным биогеографическим регионам Европы.
Аннотация
Для обеспечения будущего мониторинга в ходе этого исследования были получены новые данные о морфологических признаках вида (надземные части), климатической толерантности (режимы осадков и температур), местах произрастания с сопутствующими видами, опылителях, текущем репродуктивном потенциале и прорастании семян при контролируемых температурах (10 °C, 15 °C и 20 °C). Высокая вероятность ошибочной идентификации с высокоинвазивным видом A. syriaca в европейских учетах подтверждает теорию о том, что A. speciosa мог присутствовать в Европе задолго до его официального сообщения. Отсутствие обязательной по мандату ЕС переоценки мониторинга A. syriaca вызывает обеспокоенность относительно потенциального инвазионного риска A. speciosa для европейских природных и полуприродных территорий или сельскохозяйственных угодий. Поэтому механизмы инспекции, системы раннего оповещения и превентивные меры необходимы для защиты местного биоразнообразия и сельского хозяйства от потенциального вторжения A. speciosa — риска, который может усилиться из-за изменения климата.
1. Введение
Род Asclepias L. был первоначально описан Карлом Линнеем в 1753 году, который назвал его в честь Асклепия (Ἀσκληπιός по-гречески или лат. Aesculapius), бога медицины и врачевания в Древней Греции, вероятно, из-за долгой истории использования растений этого рода в лекарственных целях [1]. Линней описал обыкновенный ваточник как A. syriaca L., основываясь на ошибочном предположении, что этот вид, происходящий из Северной Америки, происходит из Сирии [2]. Род Asclepias L. s. str. (Apocynaceae, Asclepiadoideae) включает приблизительно 120 видов, произрастающих в Северной и Южной Америке и Южной Африке [3]. Большинство видов распространены в Северной Америке и Карибском бассейне, при этом десять видов встречаются в Южной Америке [4,5,6,7,8].
В Европе чужеродные представители рода Asclepias s. str. были зарегистрированы как чужеродные натурализовавшиеся виды, а именно: Asclepias curassavica L., A. incarnata L., A. syriaca L. [9,10] и A. speciosa Torr. [4], в то время как в нескольких странах Южной Европы также были отмечены виды близкородственного рода Gomphocarpus R. Br., например, Gomphocarpus fruticosus (L.) W.T.Aiton (Asclepias fruticosa L.) и Gomphocarpus physocarpus E.Mey. (Asclepias physocarpa (E.Mey.) Schltr.) [9,11,12,13]. Несомненно, A. syriaca является наиболее широко распространенным и инвазионным видом этого рода в странах Южной и Центральной Европы [14,15,16,17,18], в то время как A. curassavica и A. incarnata были зарегистрированы только как случайные или локально натурализовавшиеся чужеродные виды в различных регионах Европы [9,19,20]. В Греции A. curassavica с яркими оранжево-красными цветками, Gomphocarpus fruticosus и G. physocarpus были зарегистрированы как укоренившиеся чужеродные виды [9] (http://www.alienplants.gr, по состоянию на 25 октября 2024 г.), в то время как Asclepias speciosa Torr. был лишь недавно зарегистрирован как новое чужеродное растение в Северной Греции [21].
Asclepias speciosa разделяет несколько морфологических признаков с A. syriaca (обыкновенным ваточником), и было отмечено, что первый вид часто могут ошибочно идентифицировать как второй [4]. С момента интродукции A. syriaca в Европу в 1629 году [22] в декоративных и различных других целях, таких как его потенциал для производства волокна и латекса, A. syriaca укоренился во многих регионах Европы и за последние десятилетия все больше распространялся. Следует подчеркнуть, что присутствие A. speciosa в Европе было косвенно выявлено впервые только в южных частях Литвы [4] в ходе обширной оценки A. syriaca в стране в связи с выполнением требований Регламента ЕС по чужеродным инвазионным видам в национальном масштабе Литвы. Переоценка депонированных гербарных образцов в Литве выявила несколько случаев ошибочной идентификации A. syriaca вместо A. speciosa. Эти гербарные исследования показали, что A. speciosa был впервые собран в Литве в 1962 году [4]. Основываясь на информации с гербарных этикеток, последнее исследование показало, что A. speciosa встречался в дикой природе Литвы в течение почти 60 лет до официального сообщения, и, следовательно, его можно считать натурализовавшимся чужеродным растением в Литве [4]. Этот вид мог быть интродуцирован в Литву в конце XIX или начале XX века как декоративное растение, возможно, позже культивировался местными жителями в их садах или как медоносное растение, а затем одичал из культуры [4]. Репродуктивное поведение A. speciosa характеризуется высоким выходом распространяемых ветром семян в сочетании с бесполым размножением ползучими боковыми корневищами, что позволяет виду быстро распространяться и создавать колонии на новых территориях [23]. В своем чужеродном ареале в Европе A. syriaca внедряется в местообитания, которые уже были в некоторой степени нарушены антропогенным воздействием [24]. Это высококонкурентный чужеродный вид с высокорослым и теневыносливым габитусом, вегетативным распространением, засухоустойчивостью и аллелопатическим потенциалом [22,25], который может активно изменять свою локальную среду как вид-трансформер [26,27,28]. Хотя такие факты не известны в той же степени для сходного и близкородственного A. speciosa, оба вида демонстрируют значительное сходство с точки зрения габитуса растения, репродуктивных стратегий и экологии. Разнообразие естественных и антропогенных местообитаний, занимаемых A. speciosa в его нативном (США) и чужеродном (Литва) ареалах, включает различные типы луговых местообитаний и водно-болотные угодья, а также обочины дорог, нарушенные земли и пахотные земли, соответственно, что делает его колонизирующим луговым видом и/или сорняком пахотных земель [4], создавая тем самым потенциальную угрозу для сельского хозяйства. Последнее обстоятельство служит сигналом для детального изучения A. speciosa на самых ранних возможных стадиях в отношении его будущей натурализации и инвазии в Европе или для разработки видоспецифичных мер управления. В этом контексте геоинформационные системы (ГИС) широко применяются в исследованиях инвазионных видов. ГИС является эффективным вспомогательным инструментом для автоматизированного распознавания распространения инвазионных видов с помощью дистанционного зондирования [29], для прогнозирования потенциального пространственного распределения чужеродных видов [30] и для разработки оценок риска потенциального воздействия инвазионных видов на аборигенные виды в их экосистемах [31]. Кроме того, экологические предпочтения чужеродных видов могут быть получены с помощью применения ГИС аналогично случаям с редкими видами, находящимися под угрозой исчезновения [32].
Настоящее исследование было направлено на документирование экологических характеристик пилотной дикорастущей популяции A. speciosa (ваточника яркого), недавно впервые зарегистрированной в Северной Греции [21]; за этой популяцией велось тщательное наблюдение в течение последних двух лет, причем наблюдения предшествовали указанному исследованию. Нативный ареал A. speciosa включает части западной половины Северной Америки, от Калифорнии до Британской Колумбии и Центральной Канады и на юг до Техаса. В своем нативном ареале A. speciosa адаптирован к широкому спектру типов почв и условий увлажнения, от прибрежных до засушливых участков [33]. Однако мало что известно о климатических предпочтениях, которые формируют или ограничивают его естественное распространение. Хотя A. speciosa был зарегистрирован как укоренившееся чужеродное растение в Европе только несколько лет назад [4] и как новое чужеродное растение в Греции всего несколько месяцев назад [21], знания о его климатических предпочтениях и динамике интродуцированных популяций в Греции или Европе все еще ограничены, а статус его натурализации и инвазии остается в значительной степени неизвестным. Поскольку Греция является лишь второй страной после Литвы, сообщившей о присутствии A. speciosa [4], настоящее исследование ставило целью задокументировать присутствие A. speciosa на территории Греции как можно раньше и как можно полнее с точки зрения первых занимаемых местообитаний, переносимых локальных климатических режимов и текущего репродуктивного потенциала; такие характеристики могут облегчить первую оценку A. speciosa с точки зрения его текущего укоренения, натурализации и статуса инвазии [34]. Документация, предоставленная в этом исследовании, также представляет собой базовую оценку для будущих схем мониторинга и возвещает о начале усилий по раннему предупреждению, направленных на предотвращение потенциальной инвазии этого чужеродного вида в Греции и Европе.
2. Материалы и методы
2.1. Полевые исследования и идентификация целевого вида в полевых условиях
Полевые исследования по обнаружению A. speciosa начались в июле 2022 года после случайного обнаружения колонии этого вида недалеко от Капнофито, Серре (Северная Греция) Catherine Dijon. С тех пор проводились регулярные ботанические обследования в окрестностях, охватывающие площадь около 500 м² вокруг обнаруженной колонии, с целью регистрации любых других растений A. speciosa. В период с 2022 по 2024 год было совершено девять (9) выездов на участок (16 июля 2022 г., 21 июля 2022 г., 10 октября 2022 г., 16 февраля 2023 г., 10 июня 2023 г., 29 июня 2023 г., 8 июля 2023 г. и 26 июля 2024 г.) для оценки состояния дикорастущих популяций в период цветения или плодоношения A. speciosa. Во время полевых работ были зарегистрированы морфологические характеристики, время цветения и элементы местообитания A. speciosa, а также относительное обилие сосуществующих видов растений по шкале DAFOR, т.е., D: доминант >75%, A: обильно 51–75%, F: часто 26–50%, O: изредка 11–25%, и R: редко 1–10% [35]. Во время седьмого визита 8 июля 2023 года также были зарегистрированы высота стебля, количество пар листьев, длина и ширина листовой пластинки, длина черешка, количество соцветий на растение, диаметр соцветия, количество цветков в соцветии и диаметр цветка для семи репрезентативных дикорастущих особей A. speciosa.
Учитывая морфологическое сходство между A. syriaca и A. speciosa, было отмечено, что первый вид часто можно ошибочно принять за второй [4], что приводит к искаженным или запутанным результатам. Довольно надежным и заметным признаком для различения этих двух видов в природе является жилкование листьев. Боковые жилки на листовых пластинках средних стеблевых листьев A. speciosa в основном очередные и отходят от главной жилки под узким углом, тогда как у A. syriaca они обычно супротивные и отходят под более широким углом [4]. Отличительная крупная корона A. speciosa, а также густо бело-войлочные цветоножки также могут служить признаками, четко отличающими A. speciosa от A. syriaca.
2.2. Картирование нативного и чужеродного ареалов для видоспецифичного биоклиматического профилирования
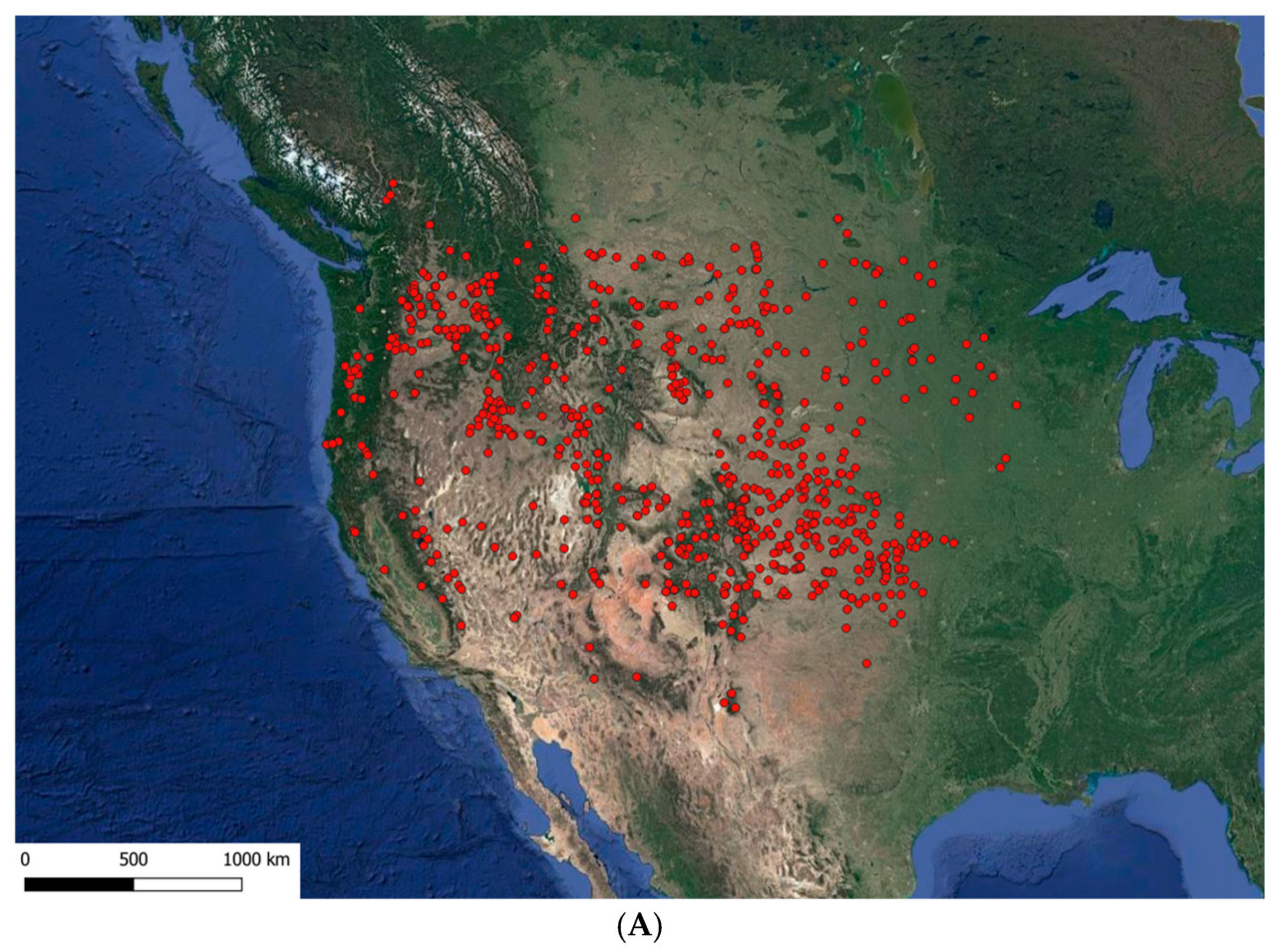
Нативный ареал A. speciosa был определен с использованием доступных данных из базы данных Global Biodiversity Information Facility (GBIF) [36]. Некоторые точки данных GBIF, полученные из iNaturalist.org и Pl@ntNet, были исключены для обеспечения надежности данных. Кроме того, были исключены записи с трех участков на востоке Соединенных Штатов, поскольку они не представляли естественный ареал вида согласно базе данных Plants of the World Online (POWO) [3] и, скорее всего, представляют A. speciosa как садовое декоративное растение или беглеца из сада. Первоначально из GBIF было получено 1173 точки распространения, и после фильтрации данных в окончательном наборе данных для построения карты было сохранено 1154 точки. Карты распространения были созданы с использованием QGIS Desktop 3.36.0 (Рисунок 1). Для разработки экологического профиля A. speciosa в пределах его нативного ареала (Рисунок 1A) из общего числа 1154 точек распространения была выбрана подвыборка из 100 точек. Этот выбор включал 20 наиболее экстремальных точек распространения в каждом кардинальном направлении (восток, запад, север и юг), с добавлением еще 20 более внутренних точек (центральная область распространения между крайними восточными, западными, северными и южными точками). Эти внутренние или более центральные точки были выбраны на основе таких факторов, как общая центральная картина распространения и изменение высотного диапазона (Рисунок 1B). Биоклиматический профиль был построен с использованием этой подвыборки точек. Исторические климатические данные были получены из базы данных WorldClim, которая предоставляет минимальные, максимальные и средние температуры, а также осадки и 19 биоклиматических переменных [36,37]. Климатические данные с пространственным разрешением 1 км² и размером пикселя 30 угловых секунд были интегрированы с выбранными точками распространения с помощью ArcMap 10.8.1.
Рисунок 1. (A) Точки распространения (n = 1154) Asclepias speciosa согласно базе данных Global Biodiversity Information Facility (GBIF) [36,37] после фильтрации записей, полученных с неэкспертных платформ, и (B) выбранные точки распространения (n = 100), охватывающие крайние точки его нативного ареала, использованные здесь для создания биоклиматического профиля в его нативном ареале.
Та же методология была использована для построения биоклиматического профиля для ненативного (чужеродного) ареала вида. В этом случае предыдущие исторические климатические данные были связаны с двумя известными на сегодняшний день местами распространения A. speciosa в Европе (Южная Литва и Северная Греция, как сообщается в этом исследовании) [4,21].
2.3. Сбор семян
Плоды A. speciosa (листовки), содержащие зрелые семена, были собраны 16 февраля 2023 года с трех оставшихся дикорастущих особей, растущих на целевом участке недалеко от Капнофито, Северная Греция. После сбора семена были очищены вручную, а затем разложены на фильтровальной бумаге в лабораторных условиях и высушены на воздухе в течение одной недели. Сухие семена хранились в стеклянном контейнере при температуре 3–5 °C до использования в эксперименте по проращиванию.
2.4. Тесты на прорастание семян
Эксперименты по проращиванию начались в конце июня 2023 года в Лаборатории цветоводства Школы сельского хозяйства Университета Аристотеля в Салониках (Терми, Греция). Для определения влияния температуры на прорастание семян использовались три климатические камеры с контролируемой температурой (CRW-500SD, Chryssagis, Афины, Греция). Семена инкубировали для проращивания при трех постоянных температурах: 10 °C, 15 °C и 20 °C с фотопериодом 12 часов света/12 часов темноты. Из-за ограниченного количества доступных семян при каждой температуре использовалось по 20 семян. Для каждого температурного режима семена помещали в стерильные пластиковые чашки Петри диаметром 9 см на фильтровальную бумагу (Рисунок 2A). Слой влажного стерильного песка был помещен под фильтровальную бумагу для поддержания влажности. Затем чашки Петри случайным образом размещали на полках климатических камер с фотопериодом 12 часов света/12 часов темноты, и субстрат (фильтровальная бумага и песок) поддерживали во влажном состоянии по мере необходимости в течение всего экспериментального периода. Проросшие семена (Рисунок 2B) подсчитывали и удаляли еженедельно в течение десяти недель. Семя считалось проросшим, когда через семенную оболочку появлялся корешок длиной не менее 2 мм (Рисунок 2B) [38].
Рисунок 2. (A) Семена Asclepias speciosa, помещенные в чашку Петри, и (B) проросшие семена с видимыми корешками (желтая масштабная линейка: 5 мм).
Проросшие семена были высеяны в пластиковые горшки (размером 6,5 см × 6,5 см × 8 см и объемом 260 мл), заполненные смесью обогащенного мелкого торфа и перлита в соотношении 3:1 (об./об.), использованной для приготовления субстрата, заполняющего горшки, а затем покрыты тонким слоем стерильного песка для поддержания влажности субстрата. Горшки были помещены на необогреваемый стеллаж в теплице. Полив горшков производился каждые два-три дня для обеспечения достаточной влажности для нормального роста сеянцев. Проросшие семена развились в нормальные сеянцы (с корнем, гипокотилем, семядолями, эпикотилем и первичными листьями) в течение двух месяцев (Рисунок 3A,B).
Рисунок 3. Двух- (A) и двенадцатимесячные (B) растения Asclepias speciosa, культивируемые в искусственных условиях в Греции (желтая масштабная линейка: 10 мм).
В эксперименте по проращиванию доля проросших семян при каждой температуре инкубации рассчитывалась путем деления числа проросших семян на общее количество семян, инкубированных при этой температуре (20 семян протестировано на обработку). Для сравнения этих долей прорастания между различными температурами инкубации мы использовали z-критерий для долей. Z-критерий для долей подходит при сравнении долей двух независимых групп, т.е. долей семян, проросших при разных температурах. Хотя z-критерий обычно идеален для больших размеров выборки из-за центральной предельной теоремы, меньшие размеры выборки все же могут позволить его использование при определенных условиях. Согласно статистическим руководствам, z-критерий можно использовать, когда размер выборки (n) и ожидаемое число успехов (np) и неудач (n(1 − p)) все больше пяти (5) [39,40]. В нашем исследовании каждая группа насчитывала 20 семян, и, учитывая наблюдаемые показатели прорастания, эти условия, вероятно, соблюдались. Z-критерий предполагает, что выборочные доли аппроксимируют нормальное распределение для больших размеров выборки. Несмотря на довольно малый размер выборки в 20 семян здесь, предыдущие исследования показали, что нормальная аппроксимация может оставаться разумной в аналогичных биологических контекстах [41]. Кроме того, z-критерий устойчив к отклонениям от нормальности, особенно при сравнении долей в пределах меньших размеров выборки, как это часто бывает в сельскохозяйственных и экологических исследованиях, где показатели прорастания имеют тенденцию стабилизироваться и следовать предсказуемым закономерностям [42]. Нашей основной целью было сравнение долей в различных температурных режимах, а не оценка средних с соответствующей вариабельностью, поэтому z-критерий для долей был выбран как прямой и подходящий.
3. Результаты
3.1. Первичная документация о наличии Asclepias speciosa в Греции
Дикорастущая популяция A. speciosa (Рисунок 4) была первоначально обнаружена в Северной Греции 16 июля 2022 года вторым автором этого исследования. Первые зарегистрированные особи этого чужеродного вида росли в 1,9–2,1 км к юго-востоку от центра деревни Капнофито, в муниципалитете Синтики, региональной единице Серре, Центральная Македония, Греция. Участок расположен в нижней части горы Врондус, на высоте 540 м над уровнем моря.
Рисунок 4. Asclepias speciosa возле деревни Капнофито, Северная Греция: (A) колония натурализовавшихся дикорастущих особей в цвету; (B,C) соцветия и характерное жилкование листьев (желтая линия: 1 см); (D,E) крупные планы соцветий и отдельного цветка (желтая линия: 1 см); (F) листовки со зрелыми семенами, несущими белые шелковистые волоски для распространения ветром; и (G) общий вид первоначального места сбора. Фотографии Catherine Dijon.
3.2. Морфологические признаки в инвазированной области
Обнаруженная колония дикорастущих растений, найденная в Капнофито, Северная Греция (Рисунок 4), была таксономически идентифицирована по нескольким характеристикам как Asclepias speciosa, травянистое многолетнее растение с обширными корневищами. Обычно войлочные стебли растений были крепкими, простыми и достигали высоты 67–123 см летом. Серовато-зеленые листья (всего было измерено 43 молодых и зрелых листа с 8-й по 11-ю пару от основания на семи растениях) были супротивными, короткочерешковыми (длиной 0,5–1,1 см), длиной 7,6–15 см и шириной 3,7–8,6 см, от овальных до довольно узкоэллиптических или яйцевидно-ланцетных, густо бело-войлочные до волосистых с нижней стороны и довольно голые с верхней стороны (Таблица 1). Стебли и листва при срезе выделяли млечный латексный сок. Крупные ароматные зонтичные соцветия (2–6 на растение, диаметром 7,3–9,9 см) развивались в рыхлых группах по 9–28 цветков с густо бело-войлочными цветоножками (Таблица 1).
Таблица 1. Морфологические параметры, изученные на семи особях Asclepias speciosa в полевых условиях.
Цветки (диаметром 2,1–2,5 см) были заметно крупными и яркими, с ланцетными долями чашечки длиной 4–8 мм; пурпурно-розовый венчик имел отогнутые бледно-розовые доли длиной 10–15 мм, а придаток (капюшон) был длинно-заостренным, шиловидным, загнутым внутрь над столбиком и голым. Пыльники были сросшимися, длиной 2,5–3 мм, с треугольными верхушечными придатками. Плоды (листовки) были мясистыми, яйцевидно-ланцетными, с заостренной верхушкой длиной 6–9(–12,5) см и развивались на изогнутых вверх цветоножках. Темно-красновато-коричневые, яйцевидные семена (ок. 6 мм × 3,5 мм) с краевой крылаткой и верхушечным пучком белых шелковистых волосков были многочисленны в каждой листовке (раскрывающейся с одной стороны осенью для рассеивания семян). Каждое семя имело пучок белых шелковистых волосков, что позволяло им эффективно распространяться ветром (Рисунок 4F). Эти признаки соответствуют ключевым характеристикам и попадают в диапазон описания A. speciosa [33]. Чтобы дать представление о морфологических характеристиках чужеродной колонии A. speciosa в Греции, девять морфологических параметров были изучены in situ на семи растениях, иллюстрируя их изменчивость (Таблица 1).
3.3. Размер популяции и местообитание
Чужеродные растения A. speciosa росли в диком виде в мелкой придорожной канаве на известковом субстрате. Дорога не была асфальтирована, имела небольшое движение и использовалась в основном местными фермерами. Наблюдаемая колония растений располагалась в 500 м к северу от искусственного озера Капнофито, которое служит источником воды для орошения близлежащих посевов, а также используется противопожарными вертолетами для предотвращения распространения лесных пожаров в окрестностях. В 150 м к северу от места обнаружения также находился водный резервуар. В радиусе 10 м вокруг особей A. speciosa мы зарегистрировали несколько местных греческих дикорастущих растений в качестве сосуществующих видов, которые характеризуют естественное состояние местообитания или нишу, занятую чужеродной колонией A. speciosa. Растения A. speciosa были найдены растущими близко к тени двух деревьев Quercus pubescens Willd. к западу и группы деревьев Fraxinus ornus L. к югу. Восточная сторона дороги в настоящее время выходит на овраг с густым древесным покровом из (относительное обилие в скобках) Quercus pubescens (D), Q. coccifera L. (A) и Acer heldreichii Orph. ex Boiss. (O). На холмистой западной стороне дороги растительность состояла в основном из низкорослых многолетников и некоторых кустарников. С северо-западной на юго-западную сторону от места произрастания A. speciosa мы заметили следующие виды растений: Quercus pubescens (F), Quercus coccifera (F), Fraxinus ornus (O), Cistus creticus L. (A), Daucus carota L. (A), Lonicera etrusca Santi (O), Cichorium intybus L. (F), Centaurea macedonica Boiss. (F), Xeranthemum annuum L. (F), Delphinium consolida L. (Consolida regalis Gray) (F), Lomelosia argentea (L.) Greuter & Burdet (F), Onosma heterophylla Griseb. (F), Achillea crithmifolia Waldst. & Kit. (F), Jasione heldreichi Boiss. & Orph. (F), Hypericum olympicum (O), Campanula scutellata (O) и Silene frivaldszkyana (R). Среди них только C. intybus можно считать местным рудеральным или синантропным растением [34], связанным с антропогенной деятельностью [43].
Популяция A. speciosa была обнаружена в единственном месте 16 июля 2022 года. Всего было насчитано 20 цветущих особей с несколькими листовками на площади примерно 2,5 м × 1 м (площадь занятости). Зрелые семена были собраны только с трех особей 16 февраля 2023 года, так как ветер, вероятно, рассеял семена с других плодоносящих особей, о чем свидетельствовали пустые листовки. 10 июня 2023 года мы повторно посетили это место, чтобы проверить колонию после обильных дождей и гроз весной. Колония была найдена в хорошем состоянии и сохранилась, несмотря на овражную эрозию, которая повредила дорогу и принесла много аллювиальных отложений в канавы. 29 июня 2023 года мы заметили, что некоторые растения (>10) наклонились из-за аллювия, который частично покрыл некоторые стебли. Однако дорога была частично отремонтирована. В этот день мы насчитали 36 растений на площади около 3 м × 1 м (площадь занятости). Несколько дней спустя строительная машина полностью выкопала траншею, уничтожив большую часть надземных частей растений. Вынутая из канавы почва была выброшена в более глубокую канаву на противоположной стороне дороги. 8 июля 2023 года мы нашли только одно цветущее растение в хорошем состоянии. Некоторые из других найденных живых растений были без верхушек или лежали, а у некоторых мелких растений не было цветков. Остальные живые растения росли все вблизи дороги, а не в канаве.
Следующий визит на участок состоялся 26 июля 2024 года. Колония была в хорошем состоянии и состояла из 50 растений высотой от 50 см до 123 см, причем 15 растений цвели, и по крайней мере пять из них несли листовки. Все растения находились в верхней части канавы и на обочине дороги, ни одно не присутствовало на дне канавы, будучи выкорчеванными во время работ по обслуживанию канавы в 2023 году. Из немногих оставшихся после нарушения 2023 года корней колония восстановилась на площади примерно 0,7 м × 3 м. На восточной стороне дороги растения не наблюдались, хотя часть почвы и некоторые выкорчеванные растения A. speciosa из канавы были перемещены туда строительной техникой в 2023 году. Несмотря на почти полное уничтожение растений в конце июня 2023 года, колония на том же участке, по-видимому, смогла восстановиться, вероятно, за счет вегетативного возобновления.
В греческой колонии A. speciosa не было зарегистрировано признаков поедания животными, вероятно, из-за содержания млечного латексного сока, который делает надземные части несъедобными для пасущихся животных [33].
3.4. Местные опылители для Asclepias speciosa в его чужеродном ареале
В этой недавно зарегистрированной популяции A. speciosa в Греции была отмечена привлекательность цветков A. speciosa для многих местных насекомых (Рисунок 5).
Рисунок 5. Местные аборигенные виды насекомых, посещающие цветки Asclepias speciosa в инвазированной области Северной Греции, такие как чешуекрылые Limenitis reducta (A1, A2, иллюстрирующие внешнюю и внутреннюю стороны крыльев) и Lycaena tityrus (B), перепончатокрылые Apis mellifera (C), Macroglossum stellatarum (D) и Camponotus sp. (I); жесткокрылые Cetonia aurata (D,G,H), полужесткокрылые Rhynocoris iracundus (E), Lygaeus sp. (нимфа) (F) и Aphis nerii (J). Фотографии Catherine Dijon.
Зарегистрированными посещающими видами насекомых были Apis mellifera (Linnaeus, 1758; Hymenoptera: Apidaea), Macroglossum stellatarum (Linnaeus, 1758; Hymenoptera: Sphingidae), Limenitis reducta (Staudinger, 1901; Lepidoptera: Nymphalidae), Lycaena tityrus (Poda, 1761; Lepidoptera: Lycaenidae), Cetonia aurata (Linnaeus, 1758; Coleoptera: Scarabaeidae), Sarcophaga carnaria (Linnaeus, 1758; Diptera: Sarcophaginae), Aphis nerii (Fonscolombe, 1841; Hemiptera: Aphididae), Camponotus sp. (Hymenoptera: Formicidae), Rhynocoris iracundus (Poda, 1761; Hemiptera: Reduviidae) и Lygaeus sp. (Hemiptera: Lygaeidae). Вероятно, поллинии (слипшаяся масса пыльцы) A. speciosa могут прикрепляться к ногам опылителей (по крайней мере, к некоторым из зарегистрированных видов насекомых) и переноситься на другие цветки.
3.5. Биоклиматические предпочтения Asclepias speciosa в нативном ареале
Основываясь на естественном распространении A. speciosa в Северной Америке (Рисунок 1), биоклиматический профиль выявил широкий диапазон экологической толерантности для A. speciosa (Рисунок 6). Нативные популяции A. speciosa процветают в районах и естественных местообитаниях, где наблюдаются низкие зимние температуры, со средней минимальной месячной температурой в январе (−3,63 °C ± 6,04 °C), в то время как средняя температура поднимается выше нуля к марту (3,38 °C ± 4,05 °C) и продолжает повышаться в летние месяцы, достигая пика в июле (20,91 °C ± 3,21 °C). После этого пика температуры постепенно снова снижаются к зимним месяцам. Данные свидетельствуют, что A. speciosa очень устойчив к холодовым режимам и естественно адаптирован к регионам с суровыми зимними условиями (среднее Tmin = −9,33 °C ± 6,45 °C в январе). Однако нативные популяции A. speciosa, по-видимому, избегают районов с высокими летними температурами (среднее Tmax = 28,78 °C ± 3,17 °C в июле). Этот факт подчеркивает предпочтение вида к умеренному климату с умеренным летним зноем, что, вероятно, определяет экстремальные границы естественного распространения в его нативном ареале. Что касается данных по осадкам, A. speciosa естественно встречается в местообитаниях в пределах своего нативного ареала, которые характеризуются умеренным уровнем осадков, как в самые холодные (154,74 мм ± 210,37 мм), так и в самые теплые (164,01 мм ± 88,50 мм) месяцы года. Как видно из характера выпадения осадков в самые засушливые периоды в его нативном ареале (56,14 мм ± 21,28 мм), количество осадков не падает до нуля (Рисунок 5); последнее указывает на то, что вид может сохраняться в средах, где в течение всего года имеется стабильное умеренное количество влаги. Общая биоклиматическая картина свидетельствует, что, хотя A. speciosa толерантен к различным режимам осадков в своем нативном ареале, он все же зависит от минимального количества осадков даже в самые засушливые сезоны (Рисунок 6).
Рисунок 6. Биоклиматический профиль в пределах нативного ареала дикорастущих популяций Asclepias speciosa [3] с использованием 100 выбранных точек распространения (см. Раздел 2), которые связаны в ГИС с геоданными (WorldClim версия 2.1) для предоставления значений минимальных, максимальных и среднемесячных температур (°C), месячного количества осадков (мм) и расчетных значений для 19 биоклиматических переменных (показаны минимум, максимум, среднее и стандартное отклонение на основе данных 1970–2000 гг.). Цвета нанесенных линий указывают на минимальные (синий), максимальные (оранжевый) и средние (серый) месячные значения температуры (°C) и осадков (мм).
3.6. Биоклиматические предпочтения Asclepias speciosa в его чужеродном ареале
Биоклиматический профиль A. speciosa в его ненативном (чужеродном) ареале в Европе в настоящее время представлен одним местонахождением в Южной Литве и другим в Северной Греции (Рисунок 7). Несмотря на ограниченное распространение, биоклиматическое профилирование показало, что чужеродные популяции этого вида могут процветать в регионах с относительно низкими зимними температурами. В январе среднемесячные температуры достигали −1,10 °C ± 2,90 °C, в то время как в марте температура поднималась выше нуля, достигая в среднем 3,40 °C ± 3,00 °C. Температура в этих районах постепенно повышалась, достигая максимума 19,70 °C ± 2,60 °C в июле. В августе температура оставалась относительно высокой, в среднем 19,25 °C ± 2,65 °C, перед постепенным снижением к зимним месяцам. На этих европейских участках чужеродные популяции этого вида, вероятно, испытывали постоянно низкие температуры (средняя температура самого холодного квартала составляет −0,22 °C ± 2,87 °C, с минимумом Tmin, достигающим −6,6 °C в январе). И наоборот, даже в самые теплые периоды температура не становилась чрезмерно высокой, о чем свидетельствует средняя температура самого теплого квартала (18,93 °C ± 2,48 °C) или наблюдение максимума Tmax, когда-либо зарегистрированного в июле (28,80 °C). Этот профиль предполагает возможность того, что чужеродные популяции A. speciosa могут переносить более прохладный климат и не предпочитают регионы с экстремальной жарой, даже в своем ненативном (чужеродном) ареале (Рисунок 6). Данные по осадкам также свидетельствуют, что чужеродные популяции A. speciosa могут процветать в регионах с относительно постоянным количеством осадков в течение года. В самый холодный сезон среднее количество осадков составляло 120 мм ± 9,5 мм (Bio 19), в то время как в самый теплый сезон оно увеличивалось до 166 мм ± 52 мм (Bio 18). Даже в самый засушливый сезон чужеродные популяции этого вида, по-видимому, все еще получали значительное количество осадков, в среднем 97 мм ± 3 мм (Bio 17). Это свидетельствует, что A. speciosa может адаптироваться к условиям со стабильной доступностью влаги в своем чужеродном ареале, даже в засушливые периоды (Рисунок 7).
Рисунок 7. Биоклиматический профиль пилотных диких популяций Asclepias speciosa в его текущем чужеродном ареале (Южная Литва и Северная Греция), связанных в ГИС с геоданными (WorldClim версия 2.1) со значениями минимальных, максимальных и среднемесячных температур (°C), месячного количества осадков (мм) и расчетными значениями для 19 биоклиматических переменных (показаны минимум, максимум, среднее и стандартное отклонение на основе данных с 1970 по 2000 г.). Цвета нанесенных линий указывают на минимальные (синий), максимальные (оранжевый) и средние (серый) месячные значения температуры (°C) и осадков (мм).
3.7. Прорастание семян Asclepias speciosa в чужеродном ареале
Количество проросших семян A. speciosa было значительно подвержено влиянию температуры (Таблица 2). При температуре инкубации 15 °C проросло значительно больше семян (9 из 20) по сравнению с 20 °C (2 из 20). Однако значительных различий в количестве проросших семян между температурами инкубации 10 °C и 15 °C (6 и 9 из 20 семян соответственно) или между 10 °C и 20 °C (6 и 2 из 20 семян соответственно) не наблюдалось.
Таблица 2. Сравнение количества проросших семян между температурами инкубации. Рассчитаны соотношения (доли) проросших семян при каждой температуре инкубации. Для сравнения соотношений используется z-критерий.
Семена, инкубированные при 15 °C, начали прорастать после первой недели (Рисунок 8), и прорастание завершилось через шесть недель после начала теста на прорастание. Напротив, семена, инкубированные при 10 °C и 20 °C, начали прорастать на две недели позже, чем при 15 °C. Прорастание семян, инкубированных при 10 °C, завершилось через восемь недель, тогда как инкубированные при 20 °C завершили прорастание через шесть недель.
Рисунок 8. Диаграмма, иллюстрирующая совокупное количество проросших семян Asclepias speciosa, инкубированных при 10 °C, 15 °C и 20 °C (○ 10 °C, □ 15 °C и ∆ 20 °C).
4. Обсуждение
4.1. Время и способ первичной интродукции
Весьма вероятно, что район вокруг деревни Капнофито и точное место, где A. speciosa был первоначально найден в Северной Греции в 2022 году, не подвергались ботаническому исследованию в течение многих лет. Например, известно, что в мае 2006 года Eckhard Willing проводил систематический сбор ботанических образцов вдоль дорог и прилегающих местообитаний в Северной Греции, включая район к юго-западу от деревни Капнофито в Серре, останавливаясь каждые 5 км для сбора образцов, но в то время не было зарегистрировано ни одной находки A. speciosa [21]. Кроме того, были ретроспективно просмотрены несколько визитов, сделанных Kit Tan в конце 1990-х и начале 2020-х годов по дороге в Ахладохори на северо-востоке Греции, но записей о A. speciosa не было [21]. Дикая популяция A. speciosa, обнаруженная в Северной Греции 16 июля 2022 года, подтверждает предположения Kit и Sister Pachomia о недавнем появлении этого вида в Греции [21]. Таким образом, можно заключить, что вид появился в Греции в начале 2020-х годов. Последующие тщательные осмотры этого района, проведенные вторым автором этого исследования, а также другими коллекторами [21], не выявили дополнительных дикорастущих популяций A. speciosa в этом районе. То самое место, откуда A. speciosa был недавно зарегистрирован как новая находка для флоры Греции [21], безусловно, страдает отсутствием описательной точности и геопространственной достоверности; первоначальное место сбора A. speciosa в Греции, как сообщается здесь, находится в 1,9–2,1 км к юго-востоку от центра деревни Капнофито (в зависимости от того, рассчитывается ли расстояние от центра деревни или ее окраины).
Можно только строить догадки о том, как A. speciosa был интродуцирован в греческое местонахождение, где он был обнаружен. Учитывая, что A. speciosa уже продается по всему миру как высоко ценимое декоративное садовое растение (например, https://www.beanplace.co.uk/products/asclepias-speciosa, и др., по состоянию на 24 октября 2024 г.), вполне вероятно, что A. speciosa был интродуцирован в Грецию как декоративное растение (например, в близлежащую деревню Капнофито) и, возможно, позже был выброшен на обочине дороги, где и укоренилась чужеродная колония. Такой способ интродукции также известен для A. syriaca в Болгарии и Литве [44], где жизнеспособные семена или корневища чаще всего выбрасываются с садовыми отходами на свалки и берега рек, что позволяет им укореняться и в дальнейшем колонизировать подходящие близлежащие местообитания. Близкородственный и сходный A. syriaca был впервые выращен в Европе в декоративных и медоносных целях, как потенциальное волокнистое растение, для производства биотоплива и латекса [45]. В XVIII и XIX веках было проведено множество исследований его потенциального использования, например, в Германии и России, причем его культивирование время от времени то прекращалось, то возобновлялось [46]. Весьма вероятно, что та же цель интродукции может относиться и к греческому A. speciosa, или даже к другим соседним районам, таким как Южная Болгария; однако этот последний вид мог быть не замечен или ошибочно идентифицирован как A. syriaca, по крайней мере, в ряде случаев, как это произошло в Литве [4].
4.2. Проблемы обнаружения и мониторинга
Asclepias syriaca является наиболее широко распространенным и инвазионным видом рода Asclepias в некоторых странах Южной и Центральной Европы [14,15,16,17,18]. Asclepias syriaca наблюдался в Адриатико-Ионическом регионе, и его появления участились за последние два десятилетия [47]. Из-за своей инвазивности и значительного негативного воздействия на аборигенные европейские (включая балканские) местообитания и агроэкосистемы, A. syriaca был включен в список чужеродных видов, вызывающих озабоченность Европейского Союза (EU 2016/1142, EU 2017/1263) согласно положениям Регламента Европейского парламента и Совета от 22 октября 2014 года об инвазионных чужеродных видах (Регламент ЕС 1143/2014). Согласно полевому исследованию, проведенному в Словакии, A. syriaca не влияет на видовое разнообразие, но значительно снижает покрытие аборигенных видов растений. В том же исследовании утверждается, что A. syriaca не представляет угрозы для сообществ почвенных нематод, но оказывает негативное воздействие на аборигенные растения [48]. Хотя A. syriaca встречается в нескольких странах Балканского полуострова, и его болгарские находки находятся очень близко к близлежащей границе с Северной Грецией [23,44], где был впервые найден A. speciosa, как задокументировано в настоящей работе, первый вид (A. syriaca) официально не зарегистрирован в Греции. Тем не менее, сходство A. syriaca с довольно изменчивым, но сходным по габитусу A. speciosa связано с проблемами ошибочной идентификации [4], подчеркивая, что последний вид (A. speciosa) долгое время оставался незамеченным или ошибочно идентифицировался из-за сходства с A. syriaca, особенно когда растения исследуются или регистрируются на вегетативной стадии. Согласно последнему исследованию [4], возможное наличие A. speciosa в других регионах Европы не может быть исключено, и обнаружение A. speciosa в Северной Греции согласуется с этой гипотезой.
Первоначальное событие интродукции A. speciosa в Грецию пока неизвестно. Возможное декоративное культивирование вида в близлежащих городских районах (например, в деревне Капнофито) в недавнем прошлом могло бы частично ответить на этот вопрос, поскольку семена довольно легко распространяются животными, с одеждой, транспортом и ветром, что позволяет предположить, что первые особи могли сбежать из сада. Однако, учитывая задокументированные случаи ошибочной идентификации в Литве [4], другая возможность, которую нельзя легко исключить и следует дополнительно изучить, заключается в том, что A. speciosa укоренился в Болгарии давно, но не был распознан местными учеными; это означает, что по крайней мере некоторые из записей A. syriaca, за которым регулярно ведется мониторинг в Болгарии [23,44], могут на самом деле относиться к A. speciosa, подобно тому, что было доказано в случае Литвы [4]. В таком неудачном случае (A. speciosa все еще не распознан, не задокументирован или скрывается под видом A. syriaca) семена A. speciosa могли быть случайно занесены в Капнофито в Северной Греции (где было найдено это новое чужеродное растение) сильными потоками ветра или посредством антропохории и зоохории (прикрепившись к одежде человека или шерсти животных) непосредственно из прилегающего пограничного района Болгарии, где образцы ваточника были ошибочно идентифицированы как A. syriaca [23,44] вместо A. speciosa. Однако для проверки или опровержения этого сценария требуется дальнейшая инспекция и верификация собранных образцов, как это было сделано, например, в Литве [4].
4.3. Последствия, касающиеся Регламента ЕС
Согласно требованиям Регламента ЕС 1143/2014, инвазия A. syriaca в аборигенные растительные сообщества Европы должна регулярно контролироваться из-за фрагментарности доступной информации; однако путаницу с близкородственным и сходным A. speciosa также следует тщательно оценивать, чтобы избежать необъективных оценок [4]. Как видно на примере чужеродного ареала вида (Литва и Греция), A. syriaca легче всего отличить от A. speciosa по форме и размеру цветков во время цветения, по морфологии капюшонов на стадиях плодоношения или даже наблюдая листья и цветоножки на вегетативной стадии. На стадии цветения два вида различаются по количеству цветков в соцветии. Хотя диаметр соцветия почти одинаков у обоих видов, у A. speciosa в чужеродном ареале (Европа) они более рыхлые и содержат почти вдвое меньше цветков (в среднем 36,2 ± 7,2), чем у A. syriaca (61,2 ± 19,5) [4]. Во время плодоношения капюшоны A. speciosa, как видно в чужеродном ареале вида (Европа), имеют длину 10–13 мм, с удлиненной язычковидной верхушкой, а рожки длиннее и заметно изогнуты внутрь, в то время как капюшоны A. syriaca имеют длину 3,5–5,0 мм, с округлой верхушкой, а рожки короткие и лишь слегка изогнуты внутрь [4]. На вегетативной стадии другим надежным ключевым признаком, который можно использовать в программах мониторинга, является опушение цветоножек: цветоножки A. speciosa густо покрыты короткими белыми волосками, как видно в чужеродном ареале вида (Европа), тогда как у A. syriaca они голые или имеют лишь несколько таких волосков [4]. Кроме того, несколько характеристик листьев столь же надежны для различения A. speciosa и A. syriaca, т.е. листовая пластинка средних стеблевых листьев A. speciosa широко яйцевидная или эллиптическая и наиболее широкая у своего слегка сердцевидного основания (как видно в чужеродном ареале вида в Европе), тогда как листовая пластинка A. syriaca яйцевидная или эллиптическая с округлым или слегка клиновидным основанием, наиболее широкая около середины [4]. Кроме того, листья A. speciosa значительно длиннее и шире, чем у A. syriaca [4]. Эти ключевые признаки цветения или вегетативные характеристики следует тщательно учитывать в протоколах мониторинга A. syriaca по всей Европе, особенно во время полевых работ, поскольку такие ключевые признаки могут обеспечить информированную и точную таксономическую идентификацию [4, таксономический ключ для диагностики], а также объективные результаты по инвазии/распространению.
4.4. Биоклиматическое профилирование в нативном и чужеродном ареалах
ГИС уже давно используется для анализа потенциального и текущего пространственного распределения целевых видов, оценки популяций и ареалов, или для измерения и мониторинга паттернов биоразнообразия в попытках определить приоритеты управления [49,50,51,52]. ГИС также использовался как инструмент для конкретных сравнений экологических паттернов между локальным и региональным масштабами в исследованиях пригодности местообитаний или для анализа воздействия чужеродных видов на аборигенные растения [53] с использованием статической информации из ботанических коллекций для оценки ареалов распространения видов или для выявления экологических предпочтений в отношении местных климатических режимов [32,54] или для инвазионных чужеродных видов, таких как Solanum elaegnifolium Cav. в Греции [55]. Впервые построенный здесь биоклиматический профиль для A. speciosa в соответствии с его нативным ареалом выявил, что вид процветает в условиях умеренного климата, проявляя толерантность к относительно низким зимним температурам, но менее приспособлен к режимам умеренно-высокой летней жары. Постоянное количество осадков в течение года, по-видимому, является критическим фактором для сохранения популяций вида в его нативных местообитаниях. Большие стандартные отклонения, наблюдаемые в этом биоклиматическом профиле, были скорее ожидаемы, отражая широкое географическое и высотное распространение вида [33], которое охватывает широкий диапазон долгот (от 92° з.д. до 124° з.д.), широт (от 32° с.ш. до 50° с.ш.) и высот от уровня моря до 5443 м над уровнем моря.
Биоклиматический профиль ненативного (чужеродного) ареала распространения A. speciosa в Европе близко соответствует климатическим условиям его нативного ареала в Северной Америке, предполагая, что европейские участки, инвазированные на сегодняшний день, находятся в пределах предпочтительного экологического диапазона вида. Климатические условия на ненативных европейских участках, по-видимому, находятся в пределах экологической толерантности вида и могут представлять возможные экстремумы (Южная Литва, Северная Греция), в пределах которых вид может продолжать распространяться как инвазионный чужеродный вид. Последнее может иметь важные последствия для большой части европейских территорий, особенно в связи с климатическим кризисом.
4.5. Репродуктивный потенциал и опылители
В Северной Америке ароматные цветки нативных популяций A. speciosa привлекают бабочек, пчел и других насекомых [33]. В общей сложности 128 полезных насекомых было зарегистрировано для A. speciosa в центральной части штата Вашингтон, США [56]. В своем нативном ареале A. speciosa известен как одно из основных кормовых растений для гусениц бабочки-монарха (Danaus plexippus Linnaeus, 1758; Lepidoptera: Nymphalidae), представляя собой пример специализированных растительно-насекомых отношений, когда гусеница бабочки-монарха питается исключительно представителями рода Asclepias. В результате программы восстановления с участием A. speciosa специально предпринимаются в его нативном ареале для поддержки и увеличения популяций Danaus plexippus [56]. В своем чужеродном ареале в Северной Греции было зарегистрировано почти дюжина местных видов насекомых, посещающих цветки A. speciosa, вероятно, обеспечивающих эффективные услуги по опылению и способствующих развитию плодов и семян. Среди них был примечателен аборигенный вид семенных клопов (Lygaeus sp.; Hymenoptera: Lygaeidae). Принимая во внимание, что обыкновенный семенной клоп, Lygaeus kalmii (Stål, 1874; Hymenoptera: Lygaeidae), питается почти исключительно нектаром цветков и семенами A. speciosa в пределах его нативного ареала [57], становится очевидным, что соответствующий родственный вид семенных клопов из энтомофауны Греции уже положительно отреагировал на интродукцию чужеродного ваточника яркого.
В случае чужеродных декоративных растений отсутствие производства семян из-за стерильности пыльцы или отсутствия совместимой пыльцы, как известно, действует как начальный барьер для их инвазионного успеха, давая представление о том, почему некоторые декоративные виды не становятся инвазионными [58]. Кроме того, сообщалось, что в некоторых случаях недостаточные услуги опылителей могут препятствовать успеху инвазии [58]. В настоящем исследовании обнаруженные in situ услуги опыления и образование семян, а также ex situ проращивание A. speciosa были впервые продемонстрированы как возможные и были признаны эффективными, что предоставляет доказательства полностью завершенной натурализации A. speciosa в Северной Греции. Предыдущие исследования [45] упоминали, что дороги и связанные с ними режимы антропогенных нарушений могут стимулировать распространение близкородственного и сходного A. syriaca, подчеркивая, что меры управления и профилактики должны применяться вдоль обочин дорог. Поскольку это справедливо и для других многолетних чужеродных инвазионных растений американского происхождения [55], и из-за сходных предпочтений в местообитаниях и репродуктивных стратегий A. syriaca и A. speciosa, такие меры управления и профилактики, вероятно, также следует применять к A. speciosa.
Настоящее исследование является первым, подтверждающим потенциал полового размножения чужеродного A. speciosa в Северной Греции. В ближайшем районе Капнофито мы заметили, что колония A. speciosa расширилась в период между 2022 и 2023 годами за счет вегетативного возобновления, вероятно, распространяясь с помощью длинных корневищ. Однако мы не нашли каких-либо новых популяций, которые укоренились бы вокруг первичного участка в результате рассеивания семян и последующего прорастания. Утверждалось, что основным препятствием для распространения этого вида в его чужеродном ареале является очевидное отсутствие полового размножения в изученных популяциях в Литве [4], поскольку отсутствие полового размножения значительно снижает возможность распространения и занятия новых местообитаний. Однако это не относится к греческому местонахождению A. speciosa, так как хорошо развитые плоды и спелые семена регулярно наблюдались in situ, а проведенные ex situ тесты с семенами доказали, что семена способны хорошо прорастать при 15 °C без холодной стратификации для преодоления механизмов покоя. Это полевое исследование в Северной Греции выявило, что A. speciosa может создавать колонии, которые распространяются через длинные подземные корневища, и может завязывать спелые плоды с жизнеспособными семенами, в то время как проведенные нами ex situ эксперименты по проращиванию показали, что его жизнеспособные семена способны соответствующим образом прорастать без врожденных ограничений. Этот двойной способ размножения — как половой, так и бесполый — впервые задокументированный здесь в его чужеродном ареале, делает A. speciosa потенциально сильным инвайдером в Греции. Поэтому системы раннего предупреждения должны быть задействованы для мониторинга его будущей инвазии, прежде чем будет слишком поздно действовать.
4.6. Прорастание семян Asclepias speciosa в его инвазированном ареале
Настоящее исследование задокументировало, что A. speciosa может регулярно завязывать плоды в Северной Греции и что его семена созревают в листовках к началу осени, ожидая распространения ветром в течение осени и зимы, в отличие от сообщений из Литвы [4].
Согласно Baskin и Baskin [59], семена Asclepias могут проявлять физиологический покой, который можно нарушить с помощью холодной стратификации. Однако было обнаружено, что покой семян значительно варьирует как внутри, так и между разными видами и популяциями Asclepias, и продолжительность холодной стратификации, необходимой для нарушения покоя, также может варьировать [60]. Предыдущее исследование сообщало, что у большинства популяций A. speciosa [60] показатели прорастания могут превышать 80% при переменных температурах 15/25 °C со значительной вариабельностью в покое семян между популяциями (половина без покоя, половина требует периода холодной стратификации в 2–4 недели для полного нарушения покоя). Примечательно, что в популяциях, где покой присутствовал, показатель прорастания семян без холодной стратификации все же мог достигать приблизительно 55% [60]. Другое исследование сообщало, что семена A. speciosa часто находятся в состоянии покоя, требуя холодной стратификации для прорастания, причем между популяциями наблюдается значительная изменчивость [33]. Следовательно, предложенные на сегодняшний день протоколы проращивания A. speciosa четко указывают на то, что холодная стратификация не всегда необходима для прорастания семян [61,62].
В настоящем исследовании прорастание семян A. speciosa, созревших в его чужеродном ареале, было исследовано впервые, и собранные семена не подвергались холодной стратификации. Тем не менее, 9 из 20 семян (45%) проросли при температуре инкубации 15 °C. Вероятно, что холодная стратификация могла бы еще больше улучшить показатели прорастания семян A. speciosa. Температура инкубации оказала значительное влияние на прорастание семян. Повышение контролируемой температуры с 15 °C до 20 °C привело к значительному снижению количества проросших семян. Аналогичная тенденция наблюдалась в предыдущем исследовании [60], где можно наблюдать снижение прорастания примерно на 30% при повышении переменной температуры инкубации с 15/25 °C до 20/30 °C. Таким образом, возможно, что холодная стратификация может смягчить влияние температуры на прорастание A. speciosa, позволяя семенам прорастать в более широком диапазоне температур. Несомненно, необходимы дальнейшие исследования прорастания семян A. speciosa в его чужеродном ареале с дополнительными экспериментами для полного определения требований к прорастанию вида, а также точного типа покоя семян в его чужеродном ареале. В ненативном ареале распространения в Европе зрелые семена естественным образом рассеиваются осенью или зимой, и прорастание их части без покоя, вероятно, происходит в октябре-ноябре, когда климатические условия, такие как температура (около 10 °C) и достаточная влажность почвы из-за осадков, благоприятны для выживания сеянцев, что, однако, зависит от того, насколько низки зимние температуры. Физиологически покоящиеся семена, вероятно, сначала подвергаются воздействию низких зимних температур, при этом прорастание происходит, возможно, позже, ранней весной. Как только новая колония укореняется, она может распространяться вегетативно с помощью длинных корневищ. Этот двойной способ размножения следует учитывать в будущих программах мониторинга, ориентированных на A. speciosa.
4.7. Потенциальная инвазия и необходимость систем раннего предупреждения
Хотя A. speciosa был зарегистрирован в Европе лишь недавно [4], а в Греции еще позднее [21], воздействие инвазии в пределах его чужеродного ареала еще не было детально оценено, поскольку оно может быть замаскировано A. syriaca [4]. В этом контексте несколько европейских исследований A. syriaca, предоставляющих соответствующие сведения о потенциальном экологическом воздействии этого вида, особенно важны и могут относиться к A. speciosa, поскольку A. syriaca и A. speciosa имеют сходную морфологию, репродуктивный потенциал и экологию [4]. Например, несколько исследований показали влияние A. syriaca на аборигенную флору [17] и фауну [48] или сельскохозяйственные культуры [63,64,65,66,67], включая аллелопатические эффекты экстрактов корней на три сельскохозяйственные культуры с негативными последствиями как для прорастания семян, так и для роста проростков культур [64,67], тем самым влияя на сельскохозяйственное производство. Помимо того, что A. syriaca является видом-трансформером, его распространение, по-видимому, не ограничивается сухими почвами и антропогенным нарушением почвы, что может дополнительно стимулировать его инвазию как в сельскохозяйственных угодьях, так и в природных ландшафтах [65]; он также может играть причинную роль в возникновении глубоких почвенных засух на инвазированных территориях, главным образом из-за своей глубокой и обширной подземной системы [66,68]. Учитывая, что A. syriaca считается важным и проблемным чужеродным инвазионным видом в Европе [23,47], особенно в Центральной и Северной Европе [14,16,17,44,63,64,65,66], а A. speciosa, вероятно, является столь же проблемным и, возможно, скрывается под видом A. syriaca, в настоящей работе предлагается тщательно обследовать и контролировать оба вида, в то время как предыдущие записи о распространении и депонированные гербарные образцы следует пересмотреть и перепроверить [4].
Планы мониторинга и управления для A. syriaca изучались на нескольких уровнях, с использованием как обычных [65,68], так и современных средств и методов, таких как технология гиперспектрального дистанционного зондирования и соответствующие данные [69,70]. С течением времени также тестировались обычные методы борьбы с помощью гербицидов [71] или агентов биологической борьбы [72,73] для контроля его инвазии. Результаты в большинстве случаев были краткосрочными [69,70] и не очень обнадеживающими, поскольку A. syriaca продолжал внедряться на новые территории, иногда даже приводя к новым вторичным инвазиям [69]. Asclepias syriaca остается основной угрозой для сельского хозяйства, аборигенного биоразнообразия и функционирования экосистем, особенно в свете изменения климата. Учитывая, что некоторые исследования сообщали, что дым от растений может усиливать прорастание семян A. syriaca [74], инвазия этого вида в средиземноморские местообитания также может быть успешной из-за повышенной вероятности местных лесных пожаров в южноевропейских странах в жаркие летние месяцы во времена климатического кризиса [75]. Принимая это во внимание, и несмотря на отсутствие соответствующей информации для A. speciosa, планы управления для A. speciosa следует предпочтительно сосредоточить на механизмах раннего предупреждения и обнаружения на самой ранней возможной стадии в сочетании с мерами искоренения в локальных масштабах.
5. Выводы
Недавно обнаруженная дикая популяция A. speciosa в Греции является второй в Европе после Литвы и первой на Балканах и в Южной Европе. Последняя находка подтверждает способность этого североамериканского вида адаптироваться к различным биогеографическим регионам Европы. С этой целью и с целью содействия будущим программам мониторинга настоящее исследование впервые задокументировало исходную чужеродную популяцию A. speciosa с точки зрения морфологических признаков, экологических (климатических и местообитаний) предпочтений, динамики популяции, опылителей, способности к прорастанию семян и инвазионного потенциала на юго-восточной границе его европейского (ненативного) ареала. Хотя A. speciosa был зарегистрирован в Европе лишь недавно, предполагается, что A. speciosa мог присутствовать на европейских территориях задолго до этих официальных сообщений в национальных или региональных реестрах, из-за задокументированного потенциала ошибочной идентификации с высокоинвазионным A. syriaca. Поэтому к этому вопросу следует отнестись внимательно, поскольку A. speciosa может представлять собой новый случай инвазии криптической природы с последствиями для сельскохозяйственных земель и (полу)естественных ландшафтов. В настоящее время нет исследований, посвященных инвазионности A. speciosa в Европе, и никакая процедура перепроверки не планируется или не применяется в схемах мониторинга A. syriaca, в настоящее время предписанных Регламентом ЕС по всей Европе. Учитывая сильное морфологическое сходство, экологическое родство и сходные репродуктивные стратегии A. speciosa и A. syriaca, в настоящей работе предлагается, что A. speciosa может представлять важный новый риск инвазии для европейских территорий. Таким образом, механизмы инспекции, системы раннего оповещения и превентивные меры являются важнейшими для защиты местного биоразнообразия и сельского хозяйства от потенциальной инвазии A. speciosa — риска, который может усилиться из-за изменения климата.
Ссылки
1. Ilieva, I. Names of botanical genera inspired by mythology. GSC Biol. Pharm. Sci. 2021, 14, 8–18. [Google Scholar] [CrossRef]
2. Darlington, W.; Thurber, G. American Weeds and Useful Plants: Being a Second and Illustrated Edition of Agricultural Botany; Rev.; A.O. Moore & company: New York, NY, USA, 1859. [Google Scholar]
3. POWO Plants of the World Online. 2024. Available online: https://powo.science.kew.org/taxon/urn:lsid:ipni.org:names:94654-1 (accessed on 30 September 2024).
4. Gudžinskas, Z.; Petrulaitis, L.; Žalneravičius, E. Asclepias speciosa (Apocynaceae, Asclepiadoideae): A rare or unrecognized alien species in Europe? PhytoKeys 2019, 121, 29–41. [Google Scholar] [CrossRef] [PubMed]
5. Woodson, R.E. The North American species of Asclepias L. Ann. Mo. Bot. Gard. 1954, 41, 1–211. [Google Scholar] [CrossRef]
6. Wilbur, H.M. Life history evolution in seven milkweeds of the genus Asclepias. J. Ecol. 1976, 64, 223–240. [Google Scholar] [CrossRef]
7. Endress, M.E.; Bruyns, P.V. A revised classification of the Apocynaceae s.l. Bot. Rev. 2000, 66, 1–56. [Google Scholar] [CrossRef]
8. Agrawal, A.A.; Fishbein, M.; Jetter, R.; Salminen, J.-P.; Goldstein, J.B.; Freitag, A.E.; Sparks, J.P. Phylogenetic ecology of leaf surface traits in the milkweeds (Asclepias spp.): Chemistry, ecophysiology, and insect behavior. New Phytol. 2009, 183, 848–867. [Google Scholar] [CrossRef]
9. Arianoutsou, M.; Bazos, I.; Delipetrou, P.; Kokkoris, Y. The alien flora of Greece: Taxonomy, life traits and habitat preferences. Biol. Invasions 2010, 12, 3525–3549. [Google Scholar] [CrossRef]
10. Pyšek, P.; Chytry, M.; Pergl, J.; Sádlo, J.; Wild, J. Plant invasions in the Czech Republic. In Flora and Vegetation of the Czech Republic. Plant and Vegetation; Chytrý, M., Danihelka, J., Kaplan, Z., Pyšek, P., Eds.; Springer: Cham, Switzerland, 2017; Volume 14, pp. 339–399. [Google Scholar] [CrossRef]
11. Greuter, W.; Raus, T. Med-Checklist Notulae, 19. Willdenowia 2000, 30, 229–243. [Google Scholar] [CrossRef]
12. Knees, S.G. Asclepias Linnaeus. In The European Garden Flora. A Manual for the Identification of Plants Cultivated in Europe, Both Out-of-Doors and Under Glass; Cullen, J., Alexander, J., Brickell, C., Edmondson, J., Green, P., Heywood, V., Jørgensen, P.-M., Jury, S., Knees, S., Maxwell, H., et al., Eds.; Cambridge University Press: Cambridge, UK, 2000; Volume 6, pp. 51–53. [Google Scholar]
13. Haeger, J.F.; Jordano, D.; Meléndez, M.L. Status and conservation of Asclepiadaceae and Danaus in southern Spain. J. Insect Conserv. 2011, 15, 361–365. [Google Scholar] [CrossRef]
14. Botta-Dukát, Z.; Balogh, L. The Most Important Invasive Plants in Hungary; Botta-Dukát, Z., Balogh, L., Eds.; HAS Institute of Ecology and Botany: Vácrátót, Hungary, 2008. [Google Scholar]
15. Konstantinović, B.; Meseldžija, M.; Mandić, N. Distribution of Asclepias syriaca L. on the territory of Vojvodina and possibilities of its control. Herbologia 2008, 9, 39–46. [Google Scholar]
16. Medvecká, J.; Kliment, J.; Májeková, J.; Halada, L.; Zaliberová, M.; Gojdičová, E.; Feráková, V.; Jarolímek, I. Inventory of the alien flora of Slovakia. Preslia 2012, 84, 257–309. [Google Scholar]
17. Kelemen, A.; Valkó, O.; Kröel-Dulay, G.; Deák, B.; Török, P.; Tóth, K.; Miglécz, T.; Tóthmérész, B. The invasion of common milkweed (Asclepias syriaca) in sandy old-fields—Is it a threat to the native flora? Appl. Veg. Sci. 2016, 19, 218–224. [Google Scholar] [CrossRef]
18. Pergl, J.; Sádlo, J.; Petrusek, A.; Laštůvka, Z.; Musil, J.; Perglová, I.; Šanda, R.; Šefrová, H.; Šíma, J.; Vohralík, V.; et al. Black, grey and watch lists of alien species in the Czech Republic based on environmental impacts and management strategy. NeoBiota 2016, 8, 1–37. [Google Scholar] [CrossRef]
19. Verloove, F. Catalogue of neophytes in Belgium (1800–2005). Scr. Bot. Belg. 2006, 39, 1–89. [Google Scholar]
20. DAISIE. Handbook of Alien Species in Europe; Springer: Dordrecht, The Netherlands, 2009. [Google Scholar]
21. Tan, K.; Pachomia, S. A first report of Asclepias speciosa (Asclepiadaceae) for Greece and the Balkan Peninsula. Phytol. Balk. 2024, 30, 183–188. [Google Scholar] [CrossRef]
22. Bagi, I. Common milkweed (Asclepias syriaca L.). In The Most Important Invasive Plants in Hungary; Botta-Dukát, Z., Balogh, L., Feher, A., Eds.; Institute of Ecology and Botany, Hungarian Academy of Sciences: Vácrátót, Hungary, 2008; pp. 151–159. [Google Scholar]
23. Follak, S.; Bakacsy, L.; Essl, F.; Hochfellner, L.; Lapin, K.; Schwarz, M.; Tokarska-Guzik, B.; Wołkowycki, D. Monograph of invasive plants in Europe N°6: Asclepias syriaca L. Bot. Lett. 2021, 168, 422–451. [Google Scholar] [CrossRef]
24. Szilassi, P.; Szatmári, G.; Pásztor, L.; Árvai, M.; Szatmári, J.; Szitár, K.; Papp, L. Understanding the environmental background of an invasive plant species (Asclepias syriaca) for the future: An application of LUCAS field photographs and machine learning algorithm methods. Plants 2019, 8, 593. [Google Scholar] [CrossRef]
25. Tokarska-Guzik, B.; Pisarczyk, E. Risk Assessment of Asclepias syriaca. 2015. Available online: https://circabc.europa.eu/sd/a/8dbd637b-6d8b-4608-b2b1-b51dd21cacde/Asclepias%20syriaca%20RA.pdf (accessed on 20 December 2024).
26. Török, K.; Botta-Dukát, Z.; Dancza, I.; Németh, I.; Kiss, J.; Mihály, B.; Magyar, D. Invasion gateways and corridors in the Carpathian basin: Biological invasions in Hungary. Biol. Invasions 2003, 5, 349–356. [Google Scholar] [CrossRef]
27. Balogh, L.; Dancza, I.; Király, G. Actual list of neophytes in Hungary and their classification according to their success. In Biological Invasions in Hungary: Invasive Plants; Mihály, B., Botta-Dukát, Z., Eds.; Természet BÚVÁR Alapítvány Kiadó: Budapest, Hungary, 2004; pp. 61–92. [Google Scholar]
28. Szitár, K.; Kröel-Dulay, G.; Török, K. Invasive Asclepias syriaca can have facilitative effects on native grass establishment in a water-stressed ecosystem. Appl. Veg. Sci. 2018, 21, 607–614. [Google Scholar] [CrossRef]
29. Somodi, I.; Čarni, A.; Ribeiro, D.; Podobnikar, T. Recognition of the invasive species Robinia pseudacacia from combined remote sensing and GIS sources. Biol. Conserv. 2012, 150, 59–67. [Google Scholar] [CrossRef]
30. Zhu, L.; Sun, O.J.; Sang, W.; Li, Z.; Ma, K. Predicting the spatial distribution of an invasive plant species (Eupatorium adenophorum) in China. Landsc. Ecol. 2007, 22, 1143–1154. [Google Scholar] [CrossRef]
31. Miller, T.K.; Allen, C.R.; Landis, W.G.; Merchant, J.W. Risk assessment: Simultaneously prioritizing the control of invasive plant species and the conservation of rare plant species. Biol. Conserv. 2010, 143, 2070–2079. [Google Scholar] [CrossRef]
32. Hatzilazarou, S.; El Haissoufi, M.; Pipinis, E.; Kostas, S.; Libiad, M.; Khabbach, A.; Lamchouri, F.; Bourgou, S.; Megdiche-Ksouri, W.; Ghrabi-Gammar, Z.; et al. GIS-Facilitated seed germination and multifaceted evaluation of the endangered Abies marocana Trab. (Pinaceae) enabling conservation and sustainable exploitation. Plants 2021, 10, 2606. [Google Scholar] [CrossRef] [PubMed]
33. Stevens, M. Plant guide for showy milkweed (Asclepias speciosa); USDA-Natural Resources Conservation Service, National Plant Data Center: Greensboro, NC, USA, 2000; Available online: https://www.westernnativeseed.com/plant%20guides/ascspepg.pdf (accessed on 20 December 2024).
34. Krigas, N.; Dardiotis, G. Plants and human activities: Terminological chaos, current approachesand suggested terminology in the Greek language. Bot. Chron. 2008, 19, 325–366. Available online: https://www.researchgate.net/publication/236021710_Phyta_kai_anthropines_drasteriotetes_ennoiologiko_chaos_synchrones_prosengiseis_kai_proteinomene_orologia_sten_Ellenike_glossa_Plants_and_human_activities_terminological_chaos_current_approaches_and_s (accessed on 20 December 2024).
35. Walker, K.J.; Pearman, D.A.; Ellis, R.W.; McIntosh, J.W.; Lockton, A. Recording the British and Irish flora, 2010–2020; Botanical Society of the British Isles: London, UK, 2010. [Google Scholar]
36. GBIF. Secretariat: GBIF Backbone Taxonomy. In GBIF Occurrence Download for Asclepias speciosa in USA; GBIF: Copenhagen, Denmark, 2024. [Google Scholar] [CrossRef]
37. Fick, S.E.; Hijmans, R.J. WorldClim 2: New 1-km spatial resolution climate surfaces for global land areas. Int. J. Climatol. 2017, 37, 4302–4315. [Google Scholar] [CrossRef]
38. I.S.T.A. International Rules for Seed Testing. 2025. Available online: https://www.seedtest.org/en/publications/international-rules-seed-testing.html (accessed on 20 December 2024).
39. Cochran, W.G. The χ2 Test of Goodness of Fit. Ann. Math. Stat. 1952, 23, 315–345. [Google Scholar] [CrossRef]
40. Agresti, A. An Introduction to Categorical Data Analysis; John Wiley & Sons: Hoboken, NJ, USA, 2018. [Google Scholar]
41. Fleiss, J.L.; Levin, B.; Paik, M.C. Statistical Methods for Rates and Proportions; John Wiley & Sons: Hoboken, NJ, USA, 2013. [Google Scholar]
42. Moore, D.S.; McCabe, G.P. Introduction to the practice of statistics. Technometrics 2004, 46, 118–119. [Google Scholar] [CrossRef]
43. Krigas, N. Flora and Human Activities in the Area of Thessaloniki: Biological Approach and Historical Considerations; Aristotle University of Thessaloniki: Thessaloniki, Greece, 2004. [Google Scholar] [CrossRef]
44. Vladimirov, V.; Georgiev, V. National reporting of Bulgaria about the invasive alien plants of EU concern in relation to regulation (EU) 1143/2014. Phytol. Balk. 2019, 25, 407–415. [Google Scholar]
45. Follak, S.; Schleicher, C.; Schwarz, M. Roads support the spread of invasive Asclepias syriaca in Austria. Bodenkultur 2018, 69, 257–265. [Google Scholar] [CrossRef]
46. Whittening, A. A summary of the literature on Milkweeds (Asclepias spp.) and their utilization. Bibliogr. Bull. 1943, 2, 41. [Google Scholar]
47. Gazoulis, I.; Antonopoulos, N.; Kanatas, P.; Karavas, N.; Bertoncelj, I.; Travlos, I. Invasive alien plant species—Raising awareness of a threat to biodiversity and ecological connectivity (EC) in the Adriatic-Ionian region. Diversity 2022, 14, 387. [Google Scholar] [CrossRef]
48. Jurová, J.; Renčo, M.; Gömöryová, E.; Čerevková, A. Effects of the invasive common milkweed (Asclepias syriaca) on nematode communities in natural grasslands. Nematology 2020, 22, 423–438. [Google Scholar] [CrossRef]
49. Iverson, L.R.; Prasad, A. Estimating regional plant biodiversity with GIS modelling. Divers. Distrib. 1998, 4, 49–61. [Google Scholar] [CrossRef]
50. Salem, B. Application of GIS to biodiversity monitoring. J. Arid Environ. 2003, 54, 91–114. [Google Scholar] [CrossRef]
51. Powell, M.; Accad, A.; Shapcott, A. Geographic information system (GIS) predictions of past, present habitat distribution and areas for re-introduction of the endangered subtropical rainforest shrub Triunia robusta (Proteaceae) from south-east Queensland Australia. Biol. Conserv. 2005, 123, 165–175. [Google Scholar] [CrossRef]
52. Pedersen, Å.Ø.; Nyhuus, S.; Blindheim, T.; Krog, O.M.W. Implementation of a GIS-based management tool for conservation of biodiversity within the municipality of Oslo, Norway. Landsc. Urban Plan. 2004, 68, 429–438. [Google Scholar] [CrossRef]
53. Draper, D.; Rosselló-Graell, A.; Garcia, C.; Tauleigne Gomes, C.; Sérgio, C. Application of GIS in plant conservation programmes in Portugal. Biol. Conserv. 2003, 113, 337–349. [Google Scholar] [CrossRef]
54. Grigoriadou, K.; Sarropoulou, V.; Krigas, N.; Maloupa, E.; Tsoktouridis, G. GIS-Facilitated effective propagation protocols of the endangered local endemic of Crete Carlina diae (Rech. f.) Meusel and A. Kástner (Asteraceae): Serving ex situ conservation needs and its future sustainable utilization as an ornamental. Plants 2020, 9, 1465. [Google Scholar] [CrossRef]
55. Krigas, N.; Tsiafouli, M.A.; Katsoulis, G.; Votsi, N.-E.; van Kleunen, M. Investigating the invasion pattern of the alien plant Solanum elaeagnifolium Cav. (Silverleaf Nightshade): Environmental and human-induced drivers. Plants 2021, 10, 805. [Google Scholar] [CrossRef]
56. James, D.G.; Seymour, L.; Lauby, G.; Buckley, K. Beneficial insect attraction to milkweeds (Asclepias speciosa, Asclepias fascicularis) in Washington State, USA. Insects 2016, 7, 30. [Google Scholar] [CrossRef]
57. Wheeler, A.G. The small milkweed bug, Lygaeus kalmii (Hemiptera: Lygaeidae): Milkweed specialist or opportunist? J. N. Y. Entomol. Soc. 1983, 91, 57–62. [Google Scholar]
58. Bufford, J.L.; Daehler, C.C. Sterility and lack of pollinator services explain reproductive failure in non-invasive ornamental plants. Divers. Distrib. 2014, 20, 975–985. [Google Scholar] [CrossRef]
59. Baskin, C.; Baskin, J.M. Seed Ecology, Biogeography, and Evolution of Dormancy and Germination; Academic Press: San Diego, CA, USA, 2014. [Google Scholar]
60. Kaye, T.N.; Sandlin, I.J.; Bahm, M.A. Seed dormancy and germination vary within and among species of milkweeds. AoB Plants 2018, 10, ply018. [Google Scholar] [CrossRef] [PubMed]
61. Skinner, D.M. Propagation protocol for production of container (plug) Asclepias speciosa Torr. plants 10 cu. In USDA NRCS—Pullman Plant Materials Center Pullman; US Department of Agriculture, Forest Service, National Center for Reforestation, Nurseries, and Genetic Resources: Washington, DC, USA, 2008. [Google Scholar]
62. Tilley, D. Propagation protocol for production of container (plug) Asclepias speciosa Torr. Plants 10 cubic inch container. In USDA NRCS—Aberdeen Plant Materials Center Aberdeen; US Department of Agriculture, Forest Service, National Center for Reforestation, Nurseries, and Genetic Resources: Boise, ID, USA, 2016. [Google Scholar]
63. Balogh, M.B.; Kertész, M.; Török, K.; Visztra, G.V.; Szilassi, P. Changes in the occurrence of five invasive plant species in different ecosystem types between 2009–2018 in Hungary. Land 2023, 12, 1784. [Google Scholar] [CrossRef]
64. Avramov, S.; Miljković, D.; Barišić Klisarić, N.; Živković, U.; Tarasjev, A. Multi-year monitoring of Asclepias syriaca L. spread in the Deliblato Sands protected reserve in Serbia. Forests 2024, 15, 347. [Google Scholar] [CrossRef]
65. Gudžinskas, Z.; Petrulaitis, L.; Taura, L. Asclepias syriaca L. (Apocynaceae) and its invasiveness in the southern part of the boreal region of Europe—Evidence from Lithuania. BioInvasions Rec. 2021, 10, 436–452. [Google Scholar] [CrossRef]
66. Shuvar, I.; Korpita, H.; Balkovskyi, V.; Shuvar, A. Asclepias syriaca L. is a threat to biodiversity and agriculture of Ukraine. BIO Web Conf. 2021, 07010, 1–6. [Google Scholar] [CrossRef]
67. Popov, M.; Prvulović, D.; Šućur, J.; Vidović, S.; Samardžić, N.; Stojanović, T.; Konstantinović, B. Chemical characterization of common milkweed (Asclepias syriaca L.) root extracts and their influence on maize (Zea mays L.), soybean (Glycine max (L.) Merr.) and sunflower (Helianthus annuus L.) seed germination and seedling growth. Appl. Ecol. Environ. Res. 2021, 19, 4219–4230. [Google Scholar] [CrossRef]
68. Tölgyesi, C.; Tóth, V.; Hábenczyus, A.A.; Frei, K.; Tóth, B.; Erdős, L.; Török, P.; Bátori, Z. Suppressing the invasive common milkweed (Asclepias syriaca L.) saves soil moisture reserves. Biol. Invasions 2024, 26, 2791–2799. [Google Scholar] [CrossRef]
69. Berki, B.; Botta-Dukát, Z.; Csákvári, E.; Gyalus, A.; Halassy, M.; Mártonffy, A.; Rédei, T.; Csecserits, A. Short-term effects of the control of the invasive plant Asclepias syriaca: Secondary invasion of other neophytes instead of recovery of the native species. Appl. Veg. Sci. 2023, 26, 1–12. [Google Scholar] [CrossRef]
70. Papp, L.; van Leeuwen, B.; Szilassi, P.; Tobak, Z.; Szatmári, J.; Árvai, M.; Mészáros, J.; Pásztor, L. Monitoring invasive plant species using hyperspectral remote sensing data. Land 2021, 10, 29. [Google Scholar] [CrossRef]
71. Bakacsy, L.; Bagi, I. Survival and regeneration ability of clonal common milkweed (Asclepias syriaca L.) after a single herbicide treatment in natural open sand grasslands. Sci. Rep. 2020, 10, 1–10. [Google Scholar] [CrossRef] [PubMed]
72. Ducs, A.; Kazi, A.; Bilkó, Á.; Altbäcker, V. Milkweed control by food imprinted rabbits. Behav. Process. 2016, 130, 75–80. [Google Scholar] [CrossRef] [PubMed]
73. Csákvári, E.; Sáradi, N.; Berki, B.; Csecserits, A.; Csonka, A.C.; Reis, B.P.; Török, K.; Valkó, O.; Vörös, M.; Halassy, M. Native species can reduce the establishment of invasive alien species if sown in high density and using competitive species. Restor. Ecol. 2023, 31, 1–10. [Google Scholar] [CrossRef]
74. Mojzes, A.; Kalapos, T. Plant-derived smoke enhances germination of the invasive common milkweed (Asclepias syriaca L.). Pol. J. Ecol. 2015, 63, 280–285. [Google Scholar] [CrossRef]
75. Ruffault, J.; Curt, T.; Moron, V.; Trigo, R.M.; Mouillot, F.; Koutsias, N.; Pimont, F.; Martin-StPaul, N.K.; Barbero, R.; Dupuy, J.; et al. Increased likelihood of heat-induced large wildfires in the Mediterranean Basin. Sci. Rep. 2020, 10, 13790. [Google Scholar] [CrossRef]
Krigas N, Dijon C, Samartza I, Avtzis DN, Anestis I, Pipinis E, Gudžinskas Z. Forewarned Is Forearmed: Documentation on the Invasion Risk of Asclepias speciosa in Greece and Europe. Agriculture. 2025; 15(3):324. https://doi.org/10.3390/agriculture15030324
Перевод статьи «Forewarned Is Forearmed: Documentation on the Invasion Risk ofAsclepias speciosain Greece and Europe» авторов Krigas N, Dijon C, Samartza I, Avtzis DN, Anestis I, Pipinis E, Gudžinskas Z., оригинал доступен по ссылке. Лицензия: CC BY. Изменения: переведено на русский язык


























































































































Комментарии (0)