Виноградные выжимки в корме ягнят помогают сдерживать размножение опасных паразитов
Целью данного исследования была оценка потенциальных преимуществ и целесообразности добавления высушенных и измельченных виноградных выжимок в концентрат, скармливаемый ягнятам при экспериментальном заражении Haemonchus contortus.
Аннотация
Восемнадцать недавно отнятых от матерей ягнят породы Санта-Инес мужского пола содержались в индивидуальных загонах и были распределены на две группы в зависимости от живой массы. Ягнята опытной группы (n = 9) первоначально получали рацион, состоящий из 50% измельченного сена и 50% концентрата. Впоследствии животных постепенно адаптировали к виноградным выжимкам, пока их окончательное включение в концентрат не достигло 20%. Ягнята контрольной группы получали концентрат без добавления виноградных выжимок. Обе группы ягнят были искусственно заражены 4000 инвазионных личинок H. contortus, и через 28 дней ягнят подвергли эвтаназии для количественного учета нематод в сычуге. Следующие показатели не показали статистически значимых различий (p > 0,05) между группами: общее количество паразитов, гематокрит, общий белок плазмы, количество эозинофилов в крови и среднесуточный прирост массы. Что касается уровня IgG в плазме к H. contortus, было отмечено значимое взаимодействие времени и обработки (p = 0,0099) с более высокими значениями в опытной группе. В двух последних пробах опытная группа показала значительно более низкие значения количества яиц в грамме фекалий по сравнению с контрольной группой (p < 0,05). У самок паразитов из опытной группы длина тела была меньше и количество яиц в матке было ниже, чем у самок из контрольной группы, с достоверной разницей по этим показателям (p < 0,05). В заключение, виноградные выжимки могут быть включены в рацион, так как это способствует более устойчивому ведению животноводства и, кроме того, может привести к снижению плодовитости H. contortus, что полезно для профилактики гемонхоза.
1. Введение
Значительные экономические потери в овцеводстве являются результатом инфекций, вызванных желудочно-кишечными нематодами (ЖКН). Период отъема ягнят считается одним из самых критических этапов, так как он включает не только стресс, связанный с переходом на новый рацион, но и отделение от матери, а также увеличение активности выпаса. Эти факторы приводят к большему заглатыванию инвазионных личинок [1,2,3]. Следовательно, развитие животных нарушается, и в некоторых случаях наблюдается повышенный уровень смертности [1,4,5,6].
Среди ЖКН Haemonchus contortus выделяется как наиболее значимый вид из-за своей гематофаговой природы и высокого биотического потенциала, что обусловливает его высокую патогенность. Этот вид отличается высокой плодовитостью, способен производить от 5000 до 15 000 яиц в день, которые выделяются в окружающую среду, где из них развиваются инвазионные личинки третьей стадии [7,8].
Контроль этих гельминтозов в основном осуществляется путем применения антигельминтных препаратов, таких как альбендазол, клозантел, левамизол, макроциклические лактоны и монепантел [9,10]. Однако из-за бессистемного использования устойчивость к антигельминтикам возросла за последние десятилетия, и во всем мире часто регистрируются случаи наличия в отарах популяций нематод, устойчивых к нескольким классам антигельминтных соединений [11,12,13,14,15].
Генетическое разнообразие и быстрый жизненный цикл _H. contortus_ облегчают отбор и распространение резистентных генотипов, что еще больше осложняет меры борьбы [16]. Эта резистентность не только снижает эффективность лечения, но и увеличивает экономические потери фермеров из-за снижения продуктивности и необходимости применения альтернативных стратегий управления. Решение этой проблемы требует комплексных подходов, включающих целенаправленное выборочное лечение, управление пастбищами и разработку новых антигельминтиков или вакцин [17].
Таким образом, необходимы альтернативные меры контроля для снижения использования антигельминтиков, минимизации сброса остаточных веществ в окружающую среду, а также усиления или стимуляции иммунного ответа [17,18,19]. Текущее состояние исследований других природных антигельминтных методов включает в себя множество инновационных стратегий, направленных на борьбу с желудочно-кишечными нематодами. Эти методы включают использование фитотерапии [20], агентов биологического контроля [21,22] и комплексных методов ведения хозяйства [22], которые в совокупности предоставляют перспективные альтернативы традиционным химическим методам лечения. В этом контексте были изучены подходы, включающие улучшение питания для повышения резистентности и устойчивости животных к инфекциям ЖКН.
Виноградные выжимки, побочный продукт винодельческой промышленности, привлекают все больше внимания в качестве альтернативного ингредиента в кормовых рецептурах для жвачных. Их использование является перспективным не только для снижения затрат на кормление, но и для содействия устойчивому развитию путем повторного использования отходов, которые в противном случае были бы выброшены [23,24]. Включение высушенных и измельченных виноградных выжимок в корма и рационы является жизнеспособной стратегией для снижения воздействия на окружающую среду и добавления стоимости этому побочному продукту [25]. В одном исследовании сообщается о применении виноградных выжимок в кормлении животных, где было обнаружено, что виноградные выжимки безопасны и могут добавляться в корм для жвачных в количестве до 100 г/кг/день в качестве хорошего источника питательных веществ [26].
Виноградные выжимки состоят из семян, остаточной мякоти и гребней, которые богаты пищевыми волокнами (49,37%) и фенольными соединениями (35,35 мг эквивалента галловой кислоты на грамм (ЭГК/г)) [25]. Кроме того, они являются богатым источником биоактивных соединений с антиоксидантными свойствами, включая каротиноиды и полифенолы [27]. Было обнаружено, что виноградные выжимки сорта IAC 138-22 'Máximo', произведенные в штате Сан-Паулу, богаты фенольными соединениями: общее содержание составило 3,95 мг/г (в эквиваленте таниновой кислоты) на 100 мг сухих выжимок, что соответствует 4,2% общего содержания фенолов в сухом веществе, и танины с общим содержанием 1,92 мг/г (в эквиваленте таниновой кислоты) на 100 мг сухих выжимок, что соответствует 2,03% общего содержания танинов в сухом веществе. Гидроалкогольный экстракт этих виноградных выжимок продемонстрировал _in vitro_ антигельминтную активность, успешно ингибируя вылупление, развитие и подвижность свободноживущих стадий _H. contortus_ [28].
Учитывая необходимость выявления альтернатив, снижающих зависимость от обычных антигельминтиков для предотвращения резистентности и содействия устойчивому развитию животноводства, настоящее исследование было направлено на оценку потенциальных преимуществ добавления измельченных виноградных выжимок в корм недавно отнятых ягнят, искусственно зараженных H. contortus. Изучая потенциальное использование виноградных выжимок, это исследование стремится не только улучшить здоровье, благополучие и показатели мелких жвачных, но и добавить стоимость побочному продукту агропромышленности, который часто утилизируется.
2. Материалы и методы
2.1. Место проведения, животные и дизайн эксперимента
Все процедуры с участием животных в этом исследовании соответствуют международным этическим стандартам и были одобрены Комитетом по этике животных FMVZ/UNESP (0542/2023).
Эксперимент был проведен на экспериментальной территории Лаборатории ветеринарной гельминтологии Института биологических наук (IBB), Университета штата Сан-Паулу (UNESP), расположенного в городе Ботукату, штат Сан-Паулу, Бразилия (22°53′16″ ю.ш. и 48°29′57″ з.д., высота над уровнем моря 884 м), в период с октября 2023 по декабрь 2023 года (весна/лето).
Восемнадцать ягнят мужского пола породы Санта-Инес, использованных в этом исследовании, находились с матерями от рождения до отъема в загонах с пастбищами, состоящими из Urochloa decumbens и Cynodon spp. Загоны были оборудованы поилками и кормушками для свободного доступа к минеральной соли и концентрату, который овцематки получали ежедневно в количестве, эквивалентном 2% их живой массы. Ягнята имели доступ к кормушкам вместе с матерями и начинали потреблять небольшие количества корма по мере приближения отъема. В возрасте 60 дней ягнят отняли от матерей и поместили в индивидуальные загоны, где они находились на протяжении всего эксперимента. Загоны были оборудованы поилками и кормушками для ежедневного добавления концентрата и измельченного сена.
Первоначально все животные получали одинаковый рацион в течение 10 дней, рассчитанный на основе их живой массы и состоящий из 2% измельченного сена и 2% концентрата. Кроме того, животные имели свободный доступ к минеральной соли, предоставляемой в отдельной кормушке. Концентрат состоял из 70% молотой кукурузы и 30% соевого шрота, и суточный рацион делился на две порции, одну утром и другую днем, в соответствии с рекомендациями Nutrient Requirements of Small Ruminants (NRC) [29].
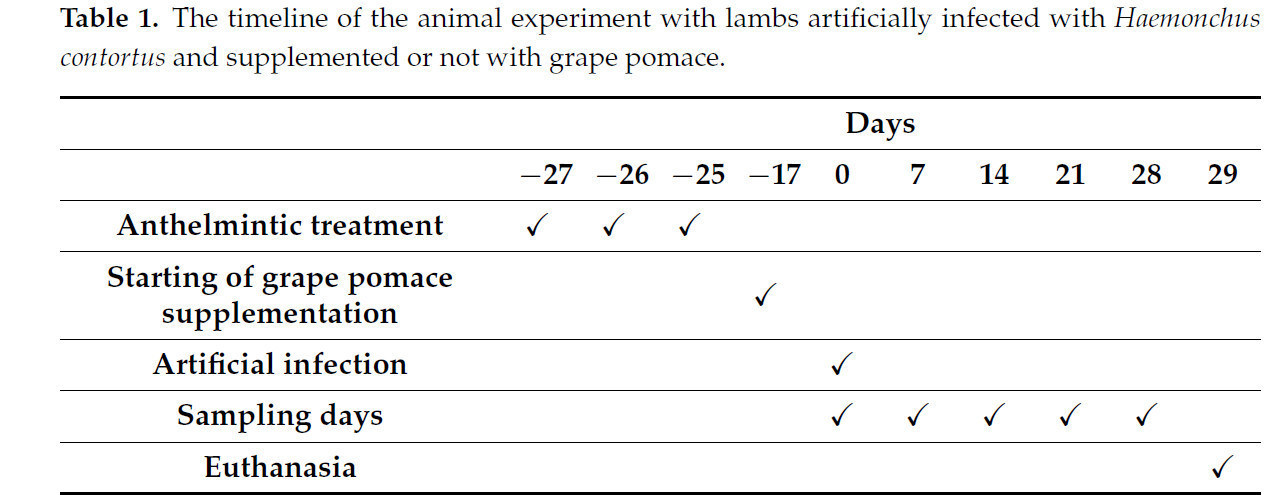
Ягнята были равномерно распределены на две группы по 9 животных в каждой, на основе живой массы, в полностью рандомизированном дизайне. На день −27 (Д−27) все животные были размещены и получили лечение левамизолом (10 мг/кг; Ripercol® L раствор; Zoetis, Кампинас, Бразилия) и альбендазолом (20 мг/кг; Valbazen® 10; Zoetis, Кампинас, Бразилия) в течение трех последовательных дней для устранения естественной инфекции нематодами (Таблица 1).
Таблица 1. Временная шкала эксперимента на ягнятах, искусственно зараженных Haemonchus contortus и получавших или не получавших добавку с виноградными выжимками.
Через восемь дней после последнего введения антигельминтиков (Д−17) группа, получавшая добавку, была постепенно адаптирована к виноградным выжимкам, пока конечное количество не составило 20% концентрата. Высушенные и измельченные виноградные выжимки смешивали с концентратом (Таблица 2) и скармливали животным. Ягнята контрольной группы получали концентрат (Таблица 2) без виноградных выжимок. Рационы были составлены с различными пропорциями разных ингредиентов, чтобы обеспечить сходное потребление белка и энергии среди животных.
Таблица 2. Состав концентрата, скармливаемого ягнятам в группе, получавшей добавку с виноградными выжимками, и в контрольной группе.
После периода адаптации к рациону (Д0) все ягнята были искусственно заражены 4000 личинками L3 изолята _H. contortus_ перорально.
С нулевого дня (Д0) животные обеих групп получали измельченное сено вволю (ad libitum). Добровольное потребление корма и измельченного сена для каждого животного измерялось ежедневно путем расчета разницы между массой предложенного рациона и массой остатков, собранных на следующее утро.
2.2. Приготовление высушенных и измельченных виноградных выжимок
Виноград сорта Сира (Vitis vinifera L.), предназначенный для производства вина, был собран в сентябре 2022 года. Виноградные выжимки были получены от винодельни в Сан-Роке, штат Сан-Паулу, Бразилия (23°35′41.2″ ю.ш. и 47°09′41.6″ з.д., высота 880 м). Выжимки сушили в печи с циркуляцией воздуха (50 °C) в течение приблизительно 24 часов, измельчали и хранили в морозильной камере (−20 °C) до использования.
2.3. Получение инвазионных личинок Haemonchus contortus
Два ягненка породы Санта-Инес содержались в загоне без доступа к пастбищу и получали концентрат и измельченное сено. Для устранения естественной инфекции нематодами обоим вводили левамизол (10 мг/кг; Ripercol® L раствор; Zoetis, Кампинас, Бразилия) и альбендазол (20 мг/кг; Valbazen® 10; Zoetis, Кампинас, Бразилия) в течение трех последовательных дней. Через четырнадцать дней после последнего введения антигельминтиков элиминация нематод была подтверждена подсчетом яиц в грамме фекалий (ЯГФ) с использованием камеры МакМастера [30]. Ягнята были экспериментально заражены пероральным введением 4000 личинок третьей стадии (L3) изолята _H. contortus_, восприимчивого к альбендазолу, ивермектину и левамизолу [31]. Через 21 день фекалии культивировали [32] при 26 °C в течение 7 дней, личинки L3 были извлечены, сохранены при комнатной температуре и использованы для искусственного заражения.
2.4. Измерение содержания общих фенолов и танинов
Концентрации общих фенолов (ОФ) измеряли с использованием реактива Фолина–Чоколтеу по методу, описанному Маккаром [33]. Общее содержание танинов (ОТ) определяли путем расчета разницы между концентрациями ОФ до и после обработки нерастворимым поливинилполипирролидоном, следуя протоколу Маккара [33,34], с использованием таниновой кислоты в качестве стандарта. Уровни конденсированных танинов (КТ) оценивали с использованием бутанол-НСl метода, также описанного Маккаром [33], с лейкоцианидином в качестве эталонного стандарта.
2.5. Сбор фекалий
Первый образец фекалий был собран на Д−17, а последующие сборы проводились каждые 7 дней, начиная с Д0. Образцы получали непосредственно из прямой кишки каждого животного для подсчета яиц в фекалиях (ЯГФ) в соответствии с Уэно и Гонсалвесом [30].
2.6. Гематологические исследования
Образцы крови собирали на Д−17 и каждые 7 дней после этого путем пункции яремной вены в вакуумные пробирки с ЭДТА. Гематокрит (ГТ) определяли центрифугированием в микро-гематокритных трубках. Общий белок плазмы (ОБП) измеряли с помощью рефрактометрии (SPR-Atago). Подсчет эозинофилов проводили в камере Нойбауэра после окрашивания раствором Карпентьера [35] и выражали как количество эозинофилов на мкл крови. Образцы плазмы хранили при −20 °C для дальнейшего анализа.
2.7. Иммуноферментный анализ (ELISA)
Специфический иммуноглобулин G (IgG) против L3 _H. contortus_ был количественно определен в сохраненных образцах плазмы с использованием растворимого экстракта из личинок L3, как описано Амаранте и др. [36]. Процедуры ELISA проводились в соответствии с Албукерке и др. [37]. Отрицательные контрольные образцы были получены от свободных от гельминтов животных [38], а положительные контроли — от овец, естественно инфицированных _H. contortus_ и _T. colubriformis_. Результаты выражали как отношение оптической плотности (ОП) образца к положительному контролю [39].
2.8. Зоотехнический анализ
Образцы (500 г) измельченного сена, концентрата и виноградных выжимок были собраны и хранились в морозильной камере до анализа. Анализ состава включал сухое вещество (СВ), органическое вещество (ОВ), сырой протеин (СП), сырой жир (СЖ), нейтрально-детергентную клетчатку (НДК), кислотно-детергентную клетчатку (КДК) и содержание золы, следуя процедурам Ассоциации официальных аналитических химиков [40].
2.9. Прирост живой массы
Животных взвешивали на Д−17 и каждые 7 дней утром, до кормления, для контроля производительности и расчета среднесуточного прироста живой массы до окончания исследования.
2.10. Определение паразитарной нагрузки и измерение гельминтов
Все животные были гуманно забиты на Д29 на бойне. Сычуг извлекали, вскрывали, и его содержимое собирали в градуированные ведра. Десятипроцентные аликвоты общего содержимого консервировали 5% формальдегидом. Гельминтов подсчитывали и идентифицировали на основе стадии их развития [30].
От каждого животного случайным образом отбирали по пять самок и пять самцов _H. contortus_ для измерения длины взрослых паразитов и подсчета яиц у самок. Измерение взрослых паразитов проводили с использованием стереомикроскопа и линейки. Для подсчета яиц внутри самок каждый экземпляр помещали в полиэтиленовую микропробирку, содержащую 800 мкл деионизированной воды и 200 мкл раствора гипохлорита натрия с 0,25% активного хлора. Пробирку дважды встряхивали в течение 30 секунд на вортекс-миксере с 2-минутным интервалом между встряхиваниями. Количество яиц на мл оценивали путем наблюдения 10 капель по 10 мкл каждая, распределенных на предметном стекле, и исследовали под микроскопом при 100-кратном увеличении. Общее количество рассчитывали на основе этого наблюдения.
2.11. Статистический анализ
Статистический анализ выполняли с использованием системы статистического анализа версии 9.4 (SAS Institute, Inc., Cary, NC, USA). Переменные с повторными измерениями анализировали с использованием процедуры PROC MIXED. Средние значения считались значительно различными при p < 0,05. Данные проверяли на нормальность и при необходимости трансформировали (log10 (x + 1)) (ЯГФ, количество эозинофилов в крови, данные ELISA). Средние значения переменных с единичным измерением (количество гельминтов, длина гельминтов и количество яиц на самку) сравнивали с использованием Т-теста при 5% уровне значимости. Для упрощения интерпретации в разделе «Результаты» представлены средние арифметические значения нетрансформированных данных (±стандартная ошибка). Представлены только значимые взаимодействия времени и обработки.
3. Результаты
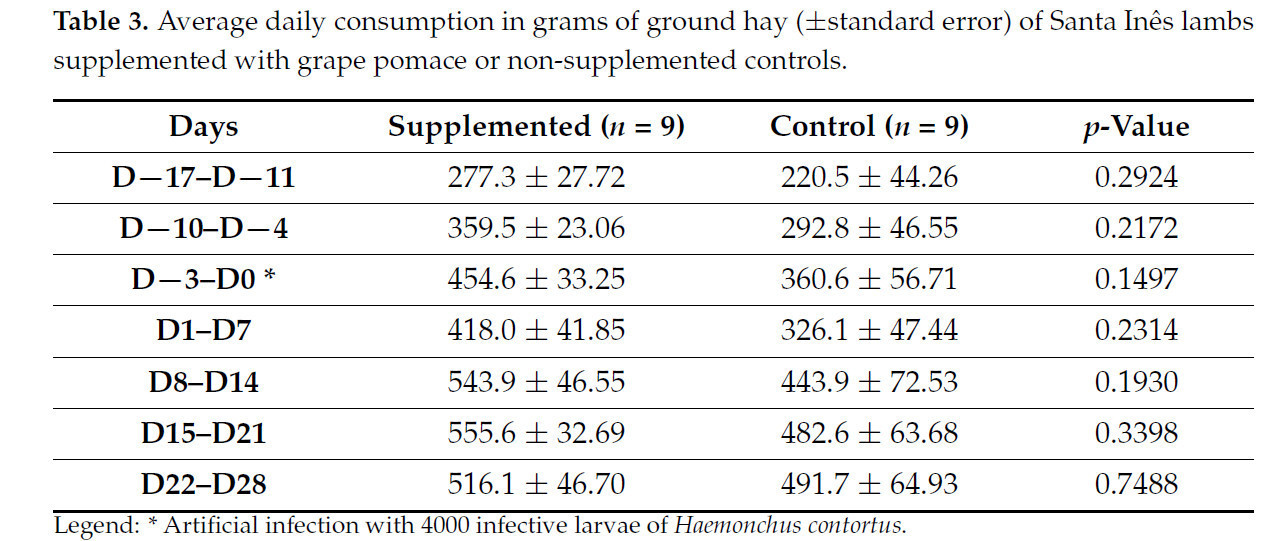
Было получено в общей сложности 91 кг влажных виноградных выжимок, которые после сушки уменьшились до 28 кг, что представляет собой 31% потерю веса. Что касается потребления виноградных выжимок, только один ягненок (№ 9) из группы, получавшей добавку, не съел весь концентрат, смешанный с виноградными выжимками, в течение первых двух дней. В первый день в кормушке осталось 57% (0,235 кг) смеси (концентрат + виноградные выжимки), а на второй день осталось 25% (0,105 кг). Хотя группа, получавшая добавку, потребляла больше измельченного сена еженедельно по сравнению с контрольной группой, значимой разницы не наблюдалось (Таблица 3 и Таблица S1, Дополнительные материалы).
Таблица 3. Среднее суточное потребление измельченного сена в граммах (±стандартная ошибка) ягнятами породы Санта-Инес, получавшими добавку с виноградными выжимками, и контрольными животными, не получавшими добавку.
Несмотря на обработку антигельминтиками, некоторые животные продолжали выделять яйца с фекалиями, хотя и с низкими значениями ЯГФ. На Д−17 у двух животных в группе с добавкой было 100 ЯГФ; по одному животному из каждой группы имели 100 ЯГФ на Д7; а на Д14 у двух животных в контрольной группе было 100 ЯГФ.
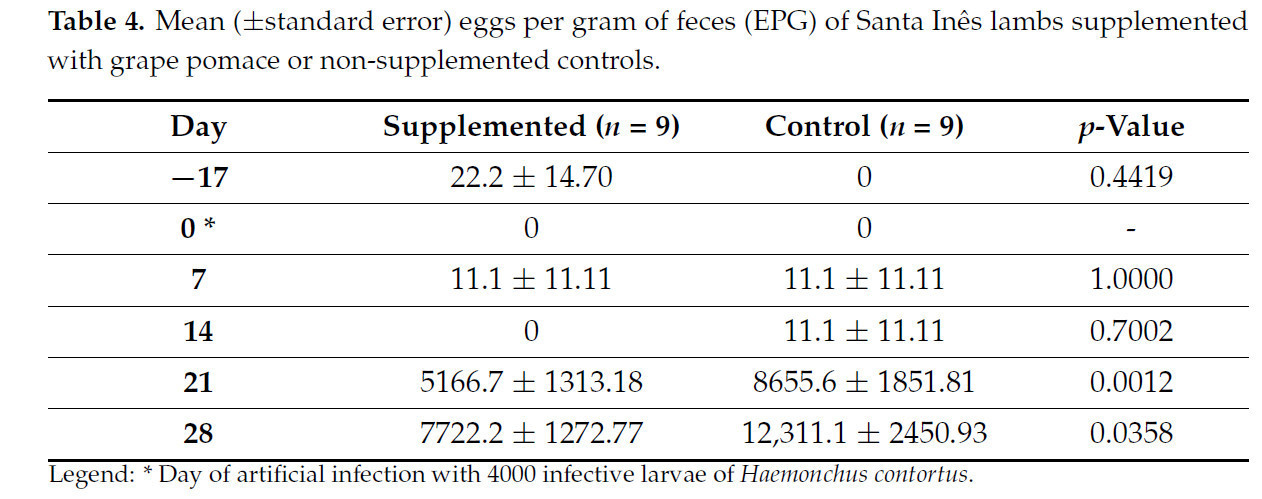
В первой пробе, соответствующей началу периода выделения яиц при искусственном заражении (День 21), все животные выделяли яйца с фекалиями, со средним значением 5167 (±1313,18) в группе с добавкой и 8656 (±1851,81) в контрольной группе (p = 0,0012). Аналогичный результат наблюдался на 28-й день: среднее значение в группе с добавкой было ниже (7722 ± 1272,77), чем в контрольной группе (12 311 (±2450,93) (p = 0,0358) (Таблица 4). Наблюдалось значимое взаимодействие времени обработки (p = 0,0384), с более выраженным увеличением значений ЯГФ в контрольной группе.
Таблица 4. Среднее значение (±стандартная ошибка) яиц в грамме фекалий (ЯГФ) ягнят породы Санта-Инес, получавших добавку с виноградными выжимками, и контрольных животных, не получавших добавку.
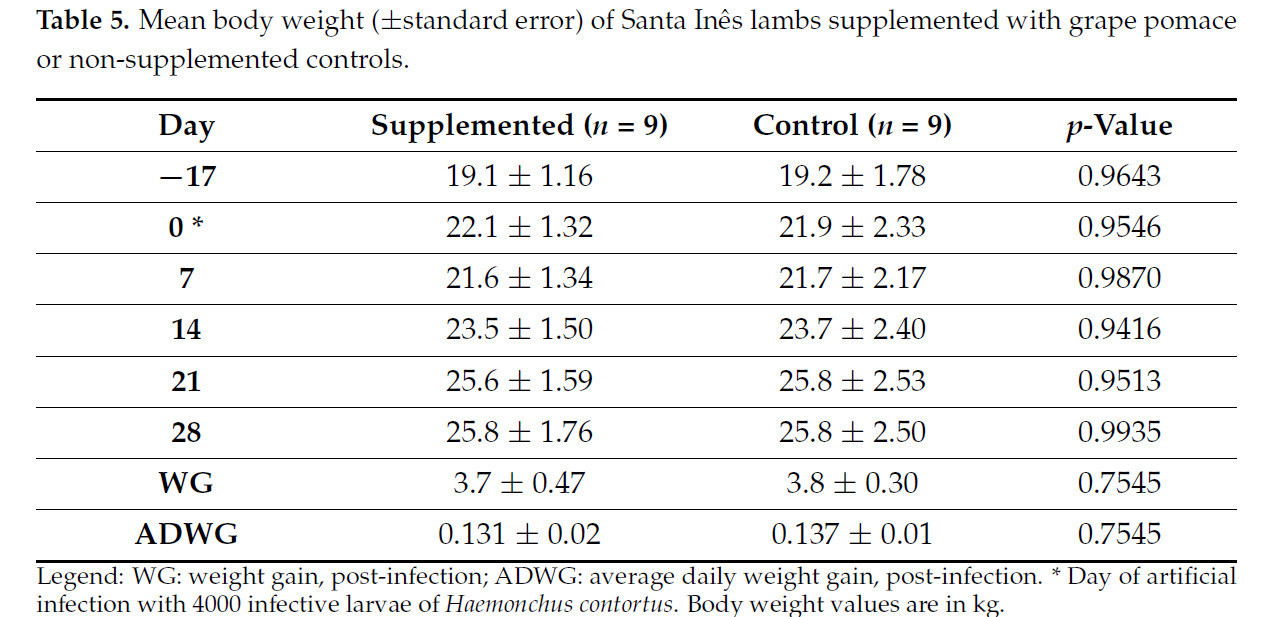
Прирост массы у ягнят, получавших добавку с виноградными выжимками, не показал значимых различий (p > 0,05) по сравнению с контрольной группой ни в одной из точек сбора данных. Средний прирост массы после заражения (с Д0 по Д28) для ягнят, получавших добавку, составил 3,7 кг (±0,47), в то время как для контрольной группы он составил 3,8 кг (±0,30). Среднесуточный прирост массы составил 0,131 кг (±0,02) в группе с добавкой и 0,137 кг (±0,01) в контрольной группе (p > 0,05) (Таблица 5).
Таблица 5. Средняя живая масса (±стандартная ошибка) ягнят породы Санта-Инес, получавших добавку с виноградными выжимками, и контрольных животных, не получавших добавку.
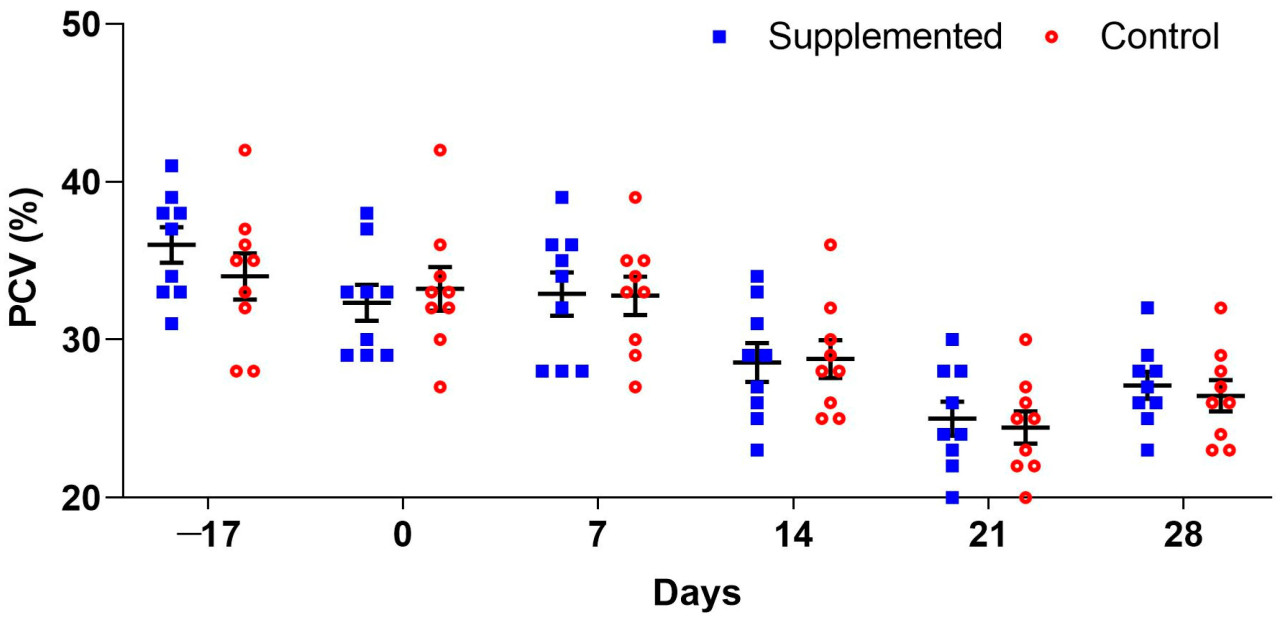
Первоначальные средние значения ГТ составили 36% (±1,12) в группе с добавкой и 34% (±1,47) в контрольной группе. С Д7 эти средние значения показали прогрессивное снижение до Д21, когда были зарегистрированы самые низкие значения: 25% (±1,08) в группе с добавкой и 24% (±1,02) в контрольной группе.
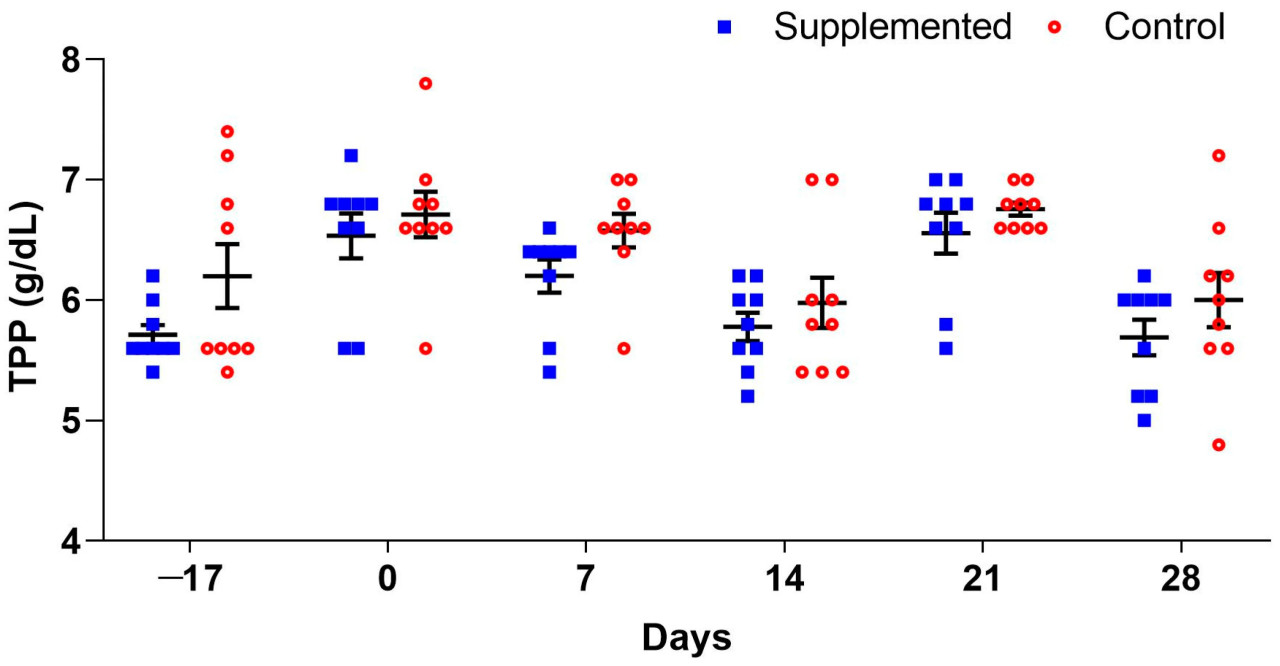
Концентрации общего белка плазмы колебались на протяжении эксперимента, но оставались в пределах нормы для овец (6,0–7,9 г/дл) [41]. Самые высокие средние значения, наблюдаемые в группе с добавкой, составили 6,6 г/дл (±0,17) на Д21, и в тот же день самое высокое среднее значение в контрольной группе составило 6,8 г/дл (±0,06). Влияния добавления виноградных выжимок на средние значения ГТ или концентрации ОБП не наблюдалось (p > 0,05) ни в одной из точек сбора (Рисунок 1 и Рисунок 2). Тем не менее, было обнаружено значимое взаимодействие времени обработки для ОБП (p = 0,0089).
Рисунок 1. Среднее значение (±стандартная ошибка) гематокрита (ГТ) ягнят породы Санта-Инес, получавших добавку с виноградными выжимками, и контрольных животных, не получавших добавку.
Рисунок 2. Среднее значение (±стандартная ошибка) концентраций общего белка плазмы (ОБП) (г/дл) ягнят породы Санта-Инес, получавших добавку с виноградными выжимками, и контрольных животных, не получавших добавку.
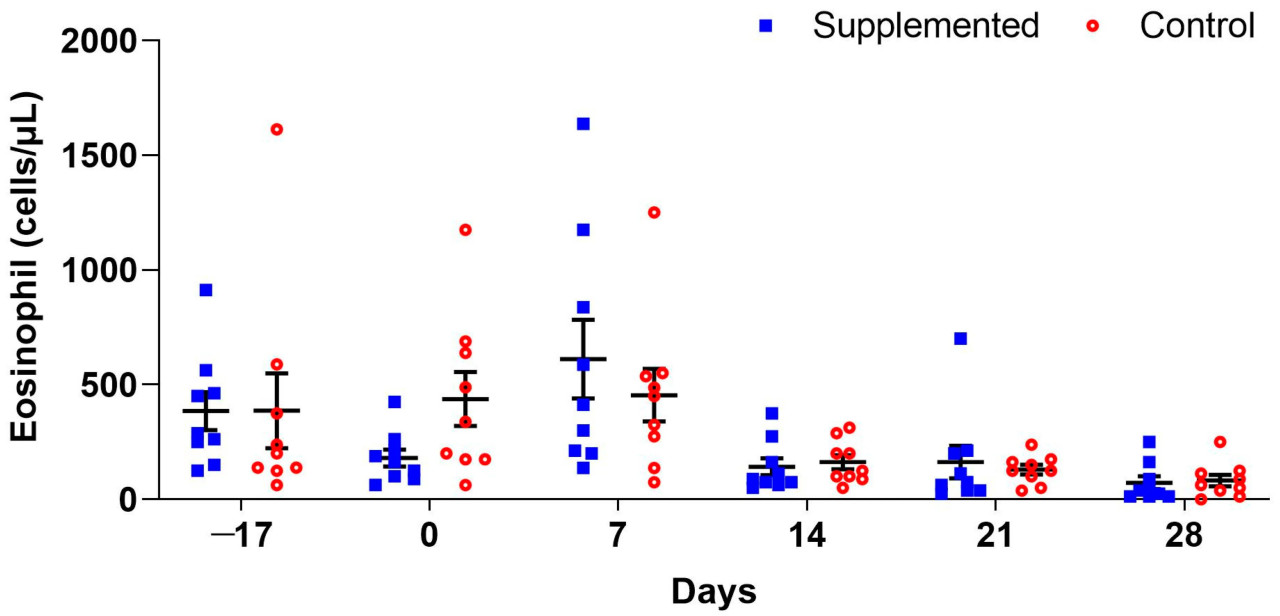
Количество эозинофилов в крови варьировало на протяжении эксперимента, достигнув пика через семь дней после заражения, со средними значениями 611 (±171,26) и 454 (±114,47) в группах с добавкой и контрольной соответственно (p > 0,05). Последующие сборы показали заметное снижение средних значений в обеих группах (Рисунок 3).
Рисунок 3. Среднее значение (±стандартная ошибка) количества эозинофилов (клеток/мкл) ягнят породы Санта-Инес, получавших добавку с виноградными выжимками, и контрольных животных, не получавших добавку.
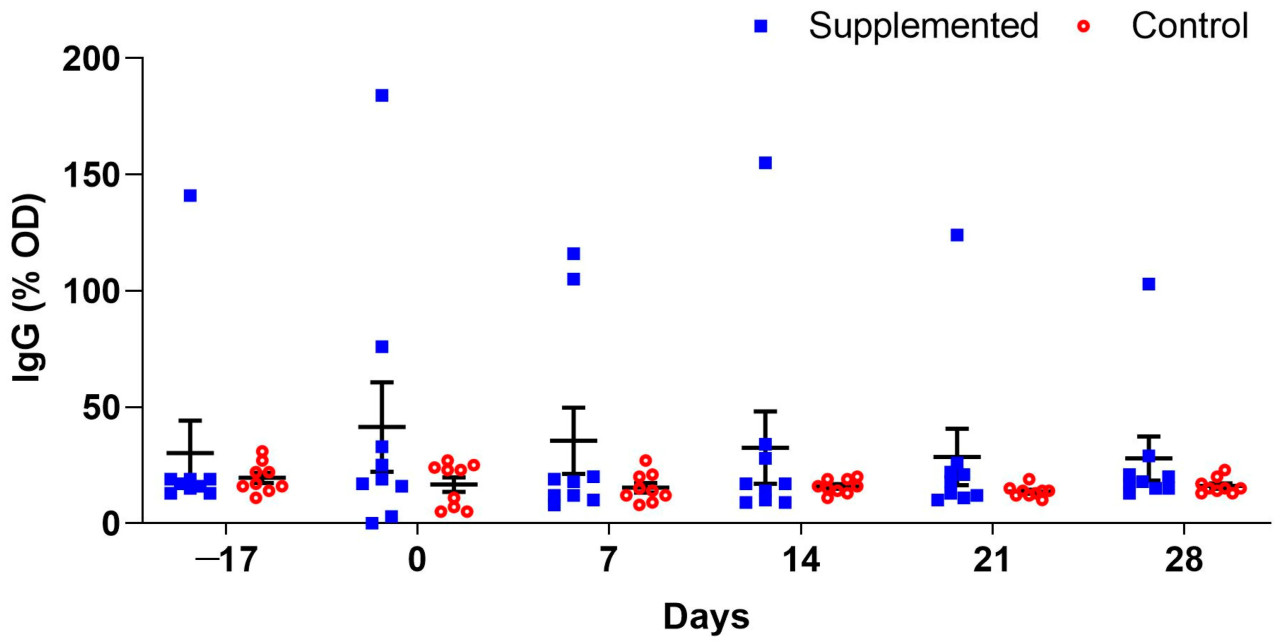
Анализы ELISA показали значимое взаимодействие времени обработки (p = 0,0099), при этом уровни IgG были стабильно выше в группе, получавшей добавку. На Д0 группа с добавкой показала свое самое высокое среднее значение 41,5 (±19,33), а контрольная группа — 16,5 (±3,11), но без значимой разницы (p = 0,0596) (Рисунок 4).
Рисунок 4. Средний уровень IgG (±стандартная ошибка) (ОП: процент оптической плотности относительно контроля) против L3 _H. contortus_ у ягнят породы Санта-Инес, получавших добавку с виноградными выжимками, и контрольных животных, не получавших добавку.
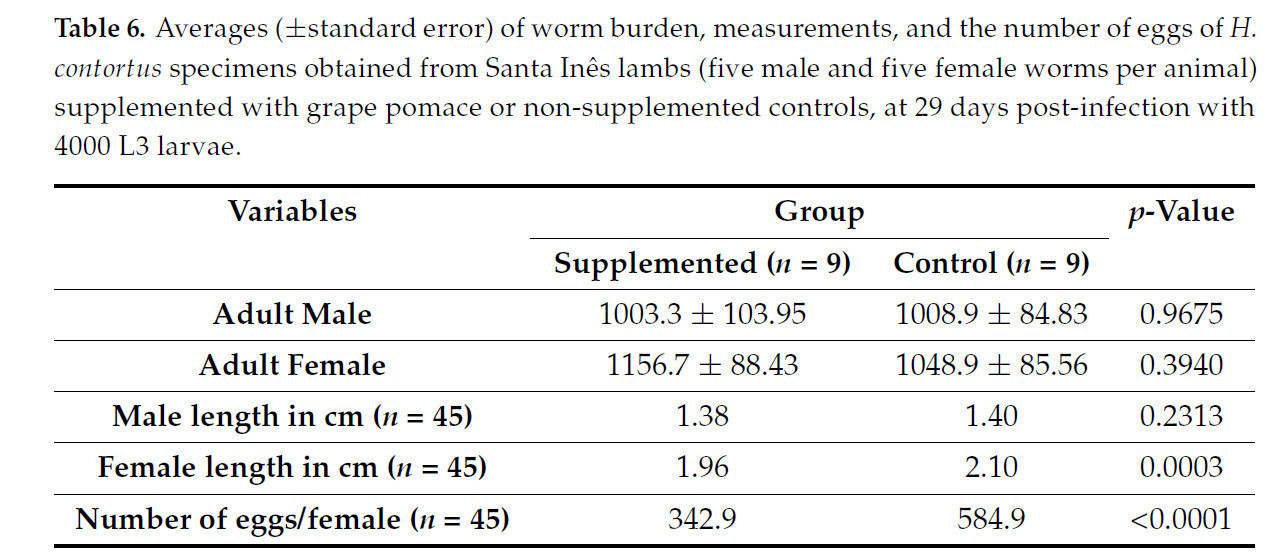
Что касается взрослых особей _H. contortus_, средняя нагрузка самок составила 1157 (±88,43) в группе с добавкой и 1049 (±85,56) в контрольной группе, без значимой разницы (p = 0,3940). Аналогично, нагрузка самцами составила 1003 (±103,95) в группе с добавкой и 1009 (±84,83) в контрольной группе (p = 0,9675).
Всего три неполовозрелых _H. contortus_ (ранняя стадия L5) были обнаружены у двух ягнят контрольной группы. Кроме того, было найдено два мужских экземпляра _Trichostrongylus colubriformis_ — один у ягненка 9 (с добавкой) и другой у ягненка 18 (контроль).
Что касается измерений длины, паразиты-самцы и самки из группы, получавшей добавку, были меньше по размеру по сравнению с контрольной группой; при этом значимая разница между группами (p = 0,0003) наблюдалась в измерениях самок. Среднее количество яиц, подсчитанных в матке каждой самки, составило 343 для группы с добавкой и 585 для контрольной группы (p < 0,0001) (Таблица 6).
Таблица 6. Средние значения (±стандартная ошибка) количества гельминтов, их размеров и количества яиц у особей _H. contortus_, полученных от ягнят породы Санта-Инес (пять самцов и пять самок на животное), получавших добавку с виноградными выжимками, и контрольных животных, не получавших добавку, через 29 дней после заражения 4000 личинок L3.
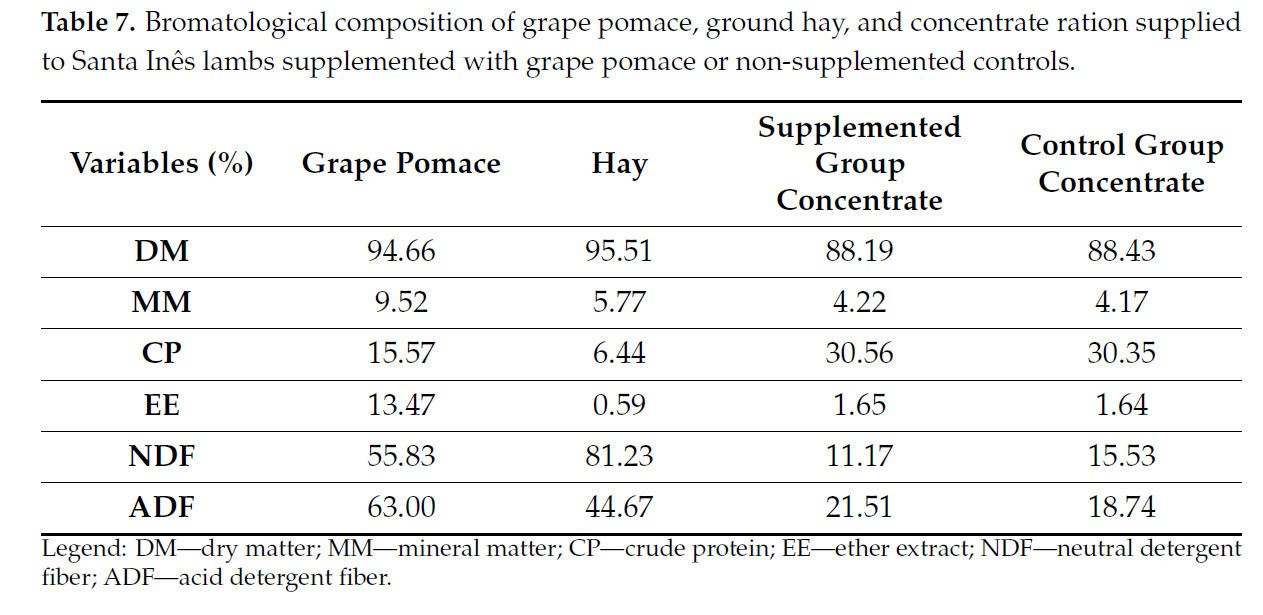
Зоотехнический состав виноградных выжимок, измельченного сена и концентрата, предоставленного ягнятам двух групп, показан в Таблице 7.
Таблица 7. Зоотехнический состав виноградных выжимок, измельченного сена и концентрата, скармливаемых ягнятам породы Санта-Инес, получавшим добавку с виноградными выжимками, и контрольным животным, не получавшим добавку.
Виноградные выжимки показали значение общих фенольных соединений 42,21 в эквивалентных граммах таниновой кислоты/кг сухого вещества; значение общих танинов 39,06 в эквивалентных граммах таниновой кислоты/кг сухого вещества; и значение конденсированных танинов 2,89 в эквивалентных граммах лейкоцианидина/кг сухого вещества. Среднее количество, потребляемое в день на одно животное, можно увидеть в Дополнительных материалах, Таблица S2.
4. Обсуждение
В настоящем исследовании виноградные выжимки, вводимые ежедневно ягнятам, продемонстрировали эффект против инфекции _H. contortus_. Группа, получавшая добавку, показала значительно более низкие показатели ЯГФ, более коротких гельминтов и самок гельминтов с меньшим количеством яиц в матке по сравнению с контрольной группой. Эффект виноградных выжимок на плодовитость паразита мог быть прямым действием соединений против гельминтов и/или косвенным эффектом, обусловленным улучшенным иммунным ответом. Метаболиты, образующиеся при ферментации фенольных соединений в рубце, могут создавать неблагоприятную среду для паразитических нематод. Считается, что метаболиты, такие как короткоцепочечные жирные кислоты и другие бактериальные метаболиты, являются важными медиаторами воздействия микробиоты на здоровье [42,43]. Было продемонстрировано, что полифенолы и танины в виноградных выжимках препятствуют репродуктивным процессам _H. contortus_, нарушая развитие и вылупление яиц. Танины, в частности, могут связываться с белками и гликопротеинами в репродуктивном тракте паразита, ингибируя ключевые ферментативные активности, необходимые для производства яиц и эмбриогенеза [44]. Это связывание также может нарушать структурную целостность кутикулы паразита и репродуктивных органов, что приводит к снижению производства яиц [45]. Снижая плодовитость, выделение яиц соответственно уменьшается, что приводит к меньшему количеству личинок третьей стадии (инвазионных) на пастбище. Это, в свою очередь, способствует снижению частоты повторных заражений и уменьшению паразитарной нагрузки.
Известно, что конденсированные танины способны связывать белки корма, защищая их от распада в рубце. Этот процесс увеличивает поток белков и улучшает всасывание аминокислот в тонком кишечнике, тем самым усиливая иммунный ответ против желудочно-кишечных нематод [44]. В настоящем исследовании такое преимущество было подтверждено более высокими уровнями IgG-анти-H. contortus в группе, получавшей добавку. Более высокие уровни пищевого белка у естественно инфицированных овец связаны с увеличением уровней эозинофилов, IgE, IgA и IgG, что приводит к более сильному иммунному ответу против нематод [46]. Несмотря на более высокие уровни IgG-анти-H. contortus в группе с добавкой, мы не наблюдали значимой разницы в количестве эозинофилов, поскольку этот параметр связан с врожденным иммунным ответом на проникающих личинок. Поскольку заражение было однократным, а эозинофилия не была интенсивной, значимых различий не обнаружено.
Виноградные выжимки богаты биоактивными соединениями, такими как фенольные кислоты, проантоцианидины, антоцианы и стильбены, обладающими значительным потенциалом для укрепления здоровья, включая антиоксидантную активность, противовоспалительные свойства, противоопухолевые эффекты, нейропротекцию и пользу для здоровья кишечника. Эти функции в значительной степени приписываются метаболитам, образующимся при деградации фенольных соединений в пищеварительном тракте, наряду с трансформациями, опосредованными ферментами фазы II метаболизма, которые инактивируют токсины для эффективного выведения [47]. Фенольные соединения, содержащиеся в виноградных выжимках, значительно влияют как на желудочно-кишечную микробиоту, так и на иммунную систему. Эти соединения взаимодействуют с кишечными бактериями, способствуя развитию полезных микробных популяций и генерируя биоактивные метаболиты, которые улучшают результаты для здоровья. Кишечная микробиота метаболизирует фенольные соединения, что приводит к продукции биоактивных метаболитов, которые могут легче всасываться и оказывать системное оздоровительное действие [42,43]. Было показано, что фенольные соединения обладают противовоспалительными эффектами, которые могут усиливать иммунные реакции [43]. Естественно инфицированные ягнята на выпасе, получавшие добавку с органическим экстрактом винограда Пино Нуар (Vitis vinifera), содержащим концентрацию конденсированных танинов 0,20 мг/мл и уровень суммарных процианидинов и продельфинидинов 0,0007 мг/мл с 15,5% галлоилированных танинов, показали более низкие значения ЯГФ по сравнению с контрольной группой [48]. Галлоилированные танины — это тип гидролизуемых танинов, состоящих в основном из единиц галловой кислоты, которые представляют собой структурно разнообразные вторичные метаболиты растений с потенциальным применением в фармацевтике и фитомедицине. Они включают галлотанины и эллагитанины, которые в избытке содержатся во фруктах и лекарственных растениях. Известные своей способностью хелатировать железо и ингибировать такие ферменты, как фермент репарации ДНК ALKBH2, галлоилированные танины также предлагают значительные преимущества для здоровья [49,50,51].
Согласуясь с нашими результатами, у шестимесячных ягнят породы Санта-Инес, искусственно зараженных и подвергнутых обработке водным экстрактом листьев банана (_Musa_ spp.), наблюдалось 33% снижение ЯГФ. Фитохимические анализы выявили наличие флавоноидов, сапонинов, катехинов, а также конденсированных и галловых танинов [52]. Сообщалось, что общее содержание полифенолов в листве банана (Musa x paradisiaca) было высоким (80 г/кг СВ), тогда как содержание конденсированных танинов было незначительным (0,007 г/кг СВ), что свидетельствует о том, что другие соединения вносят вклад в наблюдаемую нематицидную активность при скармливании ягнятам [53]. Исследование Лимы [54] продемонстрировало, что у ягнят, инфицированных нематодами и получавших экстракт _Acacia mearnsii_ (15 г/животное/день в течение 50 дней), содержащий 577 г/кг СВ общих танинов и 279 г/кг СВ конденсированных танинов, наблюдалось снижение ЯГФ.
Значительные снижения паразитарной нагрузки _T. colubriformis_ и _Cooperia_ sp. наблюдались у естественно инфицированных ягнят, получавших добавку с 18 г порошка коры черной акации (A. mearnsii), содержащего 18% конденсированных танинов (18 г экстракта или 3,24 г конденсированных танинов), один раз в неделю в течение 13 недель [55]. Экстракт, использованный в настоящем эксперименте, также содержал танины, хотя и в меньших количествах, чем сообщалось для A. mearnsii. Это предполагает, что для снижения количества гельминтов могут потребоваться относительно высокие уровни танинов. Одной из возможных причин более низкого содержания танинов может быть обработка виноградных выжимок, поскольку процессы сушки и измельчения значительно влияют на сохранение биоактивных соединений в этом побочном продукте виноделия. Эти процессы могут влиять на стабильность, растворимость и общую биодоступность фитохимических веществ, особенно фенольных соединений, известных своей пользой для здоровья. Более высокие температуры сушки могут приводить к деградации чувствительных биоактивных соединений [56]; уровень влажности во время сушки влияет на стабильность этих соединений, при этом более низкое содержание влаги обычно способствует их сохранению [57,58]. Измельчение может увеличить площадь поверхности виноградных выжимок, потенциально улучшая извлечение биоактивных соединений во время последующей обработки. Однако чрезмерное измельчение может привести к потере летучих соединений [58]. Хотя сушка и измельчение могут улучшить извлечение и сохранение биоактивных соединений, крайне важно сбалансировать эти процессы для предотвращения деградации. И наоборот, неправильное обращение может привести к значительным потерям этих ценных соединений, что подчеркивает необходимость оптимизированных методов обработки.
Несмотря на ожидаемое снижение после искусственного заражения H. contortus (гематофаговой нематодой), значения ГТ и ОБП оставались соответственно выше 20% и 5 г/дл, без необходимости профилактического применения антигельминтиков в ходе исследования. Изменения этих гематологических показателей часто связаны с паразитарными инфекциями и дефицитом питательных веществ. Наши результаты указывают на то, что добавление виноградных выжимок в рацион не оказало негативного влияния на здоровье ягнят, согласно этим индикаторам. Это согласуется с другими исследованиями, использующими побочные продукты в рационах ягнят без изменения гематологических параметров [59,60,61].
Что касается производительности животных, виноградные выжимки не повлияли отрицательно на среднесуточный прирост массы ягнят. Эти результаты подтверждают данные Ченга и др. [62], которые использовали виноградные выжимки в количестве 8% от сухого вещества рациона, не влияя на среднесуточный прирост массы ягнят. Другие исследования сообщают, что сельскохозяйственные побочные продукты, такие как кукурузные кочерыжки и шелуха арахиса, могут эффективно заменять слоновую траву (Pennisetum purpureum) в рационах ягнят, повышая прирост массы без ущерба для роста и развития [63]. Однако более высокие уровни включения виноградных выжимок (150, 300 и 500 г/кг СВ) снижали среднесуточный прирост массы из-за более медленной скорости прохождения, вызванной увеличением НДК и лигнина. Это привело к более низкому потреблению энергии и белка, может ограничивать доступность питательных веществ и подчеркивает необходимость сбалансированных рецептур рационов [64]. Несмотря на значительные различия в количестве ЯГФ, не было значимой разницы в приросте живой массы из-за малой продолжительности эксперимента. Если бы период был длительнее, мы могли бы наблюдать некоторые различия. По этой причине следует провести новые исследования для оценки более длительных периодов действия виноградных выжимок в рационе овец.
В нашем исследовании включение виноградных выжимок в пропорции 20% в концентрат было приемлемым для ягнят, так как только один ягненок из группы, получавшей добавку, не съел весь концентрат, смешанный с виноградными выжимками, в течение первых двух дней. Впоследствии этот ягненок съедал весь предоставленный корм. Большинство остатков урожая и агропромышленных побочных продуктов являются довольно приемлемыми на основе шкалы классификации приемлемости (1 = низкая; 2 = средняя; 3 = хорошая; 4 = очень хорошая). Приемлемые и высокоприемлемые остатки (со средними баллами 3 и 4 соответственно) составляют 56%, в то время как неприемлемые остатки составляют только 8% из 14 изученных остатков урожая и 11 агропромышленных побочных продуктов [65].
Неправильная утилизация сотен миллионов тонн агропромышленных побочных продуктов, образующихся ежегодно, может привести к значительным воздействиям на окружающую среду [66]. Повторное использование и включение этого побочного продукта, таким образом, может быть жизнеспособной стратегией для повышения эффективности кормления, особенно в производственных системах, сталкивающихся с проблемами затрат, одновременно способствуя устойчивому производству животных. Отчет ЮНЕП о пищевых отходах за 2024 год [67] подчеркивает значительные потери продовольствия, и включение таких побочных продуктов, как виноградные выжимки, может смягчить проблему отходов и их воздействие на окружающую среду.
Глобальная тенденция к сокращению промышленных отходов стимулировала исследования по использованию этих материалов в кормлении животных [68]. Эти результаты подчеркивают сложность взаимодействий между диетой и инфекциями желудочно-кишечных нематод, акцентируя важность учета как пищевых эффектов, так и общего состояния здоровья животных при оценке новых ингредиентов корма.
5. Выводы
Виноградные выжимки могут быть добавлены в рацион ягнят, так как это способствует более устойчивым практикам в животноводстве. Кроме того, это может вызвать снижение плодовитости _H. contortus_, что может быть полезно для профилактики гемонхоза у овец.
Дополнительные материалы
Следующие вспомогательные материалы можно загрузить по адресу: https://www.mdpi.com/article/10.3390/agriculture15030341/s1, Таблица S1: Среднее суточное потребление компонентов корма и соответствующие уровни питательности; Таблица S2: Среднее суточное потребление виноградных выжимок и общих фенолов ягнятами, получавшими добавку.
Ссылки
1. Alessandro Francisco Talamini do Amarante. Os Parasitas de Ovinos, 1st ed.; Editora da UNESP, Ed.; Alessandro Francisco Talamini do Amarante: São Paulo, Brazil, 2014. [Google Scholar]
2. Campbell, B.J.; McCutcheon, J.S.; Marsh, A.E.; Fluharty, F.L.; Parker, A.J. Delayed Weaning Improves the Growth of Lambs Grazing Chicory (Cichorium intybus) Pastures. Small Rumin. Res. 2021, 204, 106517. [Google Scholar] [CrossRef]
3. Högberg, N.; Hessle, A.; Lidfors, L.; Höglund, J. The Effect of Weaning Age on Animal Performance in Lambs Exposed to Naturally Acquired Nematode Infections. Vet. Parasitol. 2023, 316, 109900. [Google Scholar] [CrossRef] [PubMed]
4. Idris, A.; Moors, E.; Sohnrey, B.; Gauly, M. Gastrointestinal Nematode Infections in German Sheep. Parasitol. Res. 2012, 110, 1453–1459. [Google Scholar] [CrossRef] [PubMed]
5. Chagas, A.C.S.; Katiki, L.M.; Silva, I.C.; Giglioti, R.; Esteves, S.N.; Oliveira, M.C.S.; Barioni, W. Haemonchus contortus: A Multiple-Resistant Brazilian Isolate and the Costs for Its Characterization and Maintenance for Research Use. Parasitol. Int. 2013, 62, 1–6. [Google Scholar] [CrossRef] [PubMed]
6. Toscano, J.H.B.; Lopes, L.G.; Giraldelo, L.A.; da Silva, M.H.; Okino, C.H.; de Souza Chagas, A.C. Identification of Appropriate Reference Genes for Local Immune-Related Studies in Morada Nova Sheep Infected with Haemonchus contortus. Mol. Biol. Rep. 2018, 45, 1253–1262. [Google Scholar] [CrossRef]
7. Urquhart, G.M.; Armour, J.; Duncan, J.L.; Dunn, A.M.; Jennings, F.W. Parasitologia Veterinária, 2nd ed.; Guanabara Koogan, Ed.; Blackwell Publishing: Rio de Janeiro, Brazil, 1998. [Google Scholar]
8. Emery, D.L.; Hunt, P.W.; Le Jambre, L.F. Haemonchus contortus: The Then and Now, and Where to from Here? Int. J. Parasitol. 2016, 46, 755–769. [Google Scholar] [CrossRef]
9. Almeida, F.A.; Garcia, K.C.O.D.; Torgerson, P.R.; Amarante, A.F.T. Multiple Resistance to Anthelmintics by Haemonchus contortus and Trichostrongylus colubriformis in Sheep in Brazil. Parasitol. Int. 2010, 59, 622–625. [Google Scholar] [CrossRef]
10. Martins, A.C.; Bergamasco, P.L.F.; Felippelli, G.; Tebaldi, J.H.; Moraes, M.F.D.; Testi, A.J.P.; Lapera, I.M.; Hoppe, E.G.L. Haemonchus contortus Resistance to Monepantel in Sheep: Fecal Egg Count Reduction Tests and Randomized Controlled Trials. Semin. Cienc. Agrar. 2017, 38, 231. [Google Scholar] [CrossRef]
11. Bhagat, V.; Bhong, C.; Khillare, B.; Jadhav, N.; Narawade, M.; Khandekar, G.; Gaikwad, S.; Katkade, B.; Sharma, A.K.; Chigure, G. Prevalence Status and Detection of Benzimidazole Resistance Using AS-PCR in Haemonchus contortus of Goats from Marathwada Region, Maharashtra, India. Vet. Parasitol. Reg. Stud. Rep. 2024, 55, 101119. [Google Scholar] [CrossRef]
12. Macedo, L.O.; Silva, S.S.; Alves, L.C.; Carvalho, G.A.; Ramos, R.A.N. An Overview of Anthelmintic Resistance in Domestic Ruminants in Brazil. Ruminants 2023, 3, 214–232. [Google Scholar] [CrossRef]
13. Van den Brom, R.; Moll, L.; Borgsteede, F.H.M.; Van Doorn, D.C.K.; Lievaart-Peterson, K.; Dercksen, D.P.; Vellema, P. Multiple Anthelmintic Resistance of Haemonchus contortus, Including a Case of Moxidectin Resistance, in a Dutch Sheep Flock. Vet. Rec. 2013, 173, 552. [Google Scholar] [CrossRef] [PubMed]
14. Bassetto, C.C.; Albuquerque, A.C.A.; Lins, J.G.G.; Marinho-Silva, N.M.; Chocobar, M.L.E.; Bello, H.J.S.; Mena, M.O.; Niciura, S.C.M.; Amarante, A.F.T.; Chagas, A.C.S. Revisiting Anthelmintic Resistance in Sheep Flocks from São Paulo State, Brazil. Int. J. Parasitol. Drugs Drug Resist. 2024, 24, 100527. [Google Scholar] [CrossRef] [PubMed]
15. Babják, M.; Königová, A.; Komáromyová, M.; Kuzmina, T.; Nosal, P.; Várady, M. Multidrug Resistance in Haemonchus contortus in Sheep—Can It Be Overcome? J. Vet. Res. 2023, 67, 575–581. [Google Scholar] [CrossRef] [PubMed]
16. Chaudhry, U.; Redman, E.M.; Raman, M.; Gilleard, J.S. Genetic Evidence for the Spread of a Benzimidazole Resistance Mutation across Southern India from a Single Origin in the Parasitic Nematode Haemonchus contortus. Int. J. Parasitol. 2015, 45, 721–728. [Google Scholar] [CrossRef]
17. Knox, M.R.; Torres-Acosta, J.F.J.; Aguilar-Caballero, A.J. Exploiting the Effect of Dietary Supplementation of Small Ruminants on Resilience and Resistance against Gastrointestinal Nematodes. Vet. Parasitol. 2006, 139, 385–393. [Google Scholar] [CrossRef] [PubMed]
18. Sykes, A.; Coop, R.L. Interaction between Nutrition and Gastrointestinal Parasitism in Sheep. N. Z. Vet. J. 2001, 49, 222–226. [Google Scholar] [CrossRef] [PubMed]
19. Torres-Acosta, J.F.J.; Hoste, H. Alternative or Improved Methods to Limit Gastro-Intestinal Parasitism in Grazing Sheep and Goats. Small Rumin. Res. 2008, 77, 159–173. [Google Scholar] [CrossRef]
20. Castagna, F.; Bava, R.; Musolino, V.; Piras, C.; Cardamone, A.; Carresi, C.; Lupia, C.; Bosco, A.; Rinaldi, L.; Cringoli, G.; et al. Potential New Therapeutic Approaches Based on Punica Granatum Fruits Compared to Synthetic Anthelmintics for the Sustainable Control of Gastrointestinal Nematodes in Sheep. Animals 2022, 12, 2883. [Google Scholar] [CrossRef] [PubMed]
21. Holsback, L.; Lima, H.E.; Porto, P.P.; Marquez, E.d.S.; Zacarias, F.G.d.S.; Porto, E.d.P. Biological Control of Nematodes by Nematode-Trapping Fungi Duddingtonia Flagrans in Naturally Infected Sheep in Southern Brazil. Ger. J. Vet. Res. 2021, 1, 17–26. [Google Scholar] [CrossRef]
22. Haenlein, G.F.W.; Park, Y.W. Fighting the Deadly Helminthiasis without Drug Resistance. Dairy 2020, 1, 177–186. [Google Scholar] [CrossRef]
23. Kalli, E.; Lappa, I.; Bouchagier, P.; Tarantilis, P.A.; Skotti, E. Novel Application and Industrial Exploitation of Winery By-Products. Bioresour. Bioprocess. 2018, 5, 46. [Google Scholar] [CrossRef]
24. Tayengwa, T.; Mapiye, C. Citrus and Winery Wastes: Promising Dietary Supplements for Sustainable Ruminant Animal Nutrition, Health, Production, and Meat Quality. Sustainability 2018, 10, 3718. [Google Scholar] [CrossRef]
25. Machado, A.R.; Voss, G.B.; Machado, M.; Paiva, J.A.P.; Nunes, J.; Pintado, M. Chemical Characterization of the Cultivar ‘Vinhão’ (Vitis vinifera L.) Grape Pomace towards Its Circular Valorisation and Its Health Benefits. Meas. Food 2024, 15, 100175. [Google Scholar] [CrossRef]
26. Eleonora, N.; Dobrei, A.; Alina, D.; Bampidis, V.; Valeria, C. Grape Pomace in Sheep and Dairy Cows Feeding. J. Hortic. For. Biotechnol. 2014, 18, 146–150. [Google Scholar]
27. Popovici, V.; Boldianu, A.-B.; Pintea, A.; Caraus, V.; Ghendov-Mosanu, A.; Subotin, I.; Druta, R.; Sturza, R. In Vitro Antioxidant Activity of Liposomal Formulations of Sea Buckthorn and Grape Pomace. Foods 2024, 13, 2478. [Google Scholar] [CrossRef] [PubMed]
28. Silva Soares, S.C.; de Lima, G.C.; Carlos Laurentiz, A.; Féboli, A.; dos Anjos, L.A.; de Paula Carlis, M.S.; da Silva Filardi, R.; da Silva de Laurentiz, R. In Vitro Anthelmintic Activity of Grape Pomace Extract against Gastrointestinal Nematodes of Naturally Infected Sheep. Int. J. Vet. Sci. Med. 2018, 6, 243–247. [Google Scholar] [CrossRef] [PubMed]
29. Nutrient Requirements of Small Ruminants; National Academies Press: Washington, DC, USA, 2007. [CrossRef]
30. Ueno, H.; Gonçalves, P.C. Manual Para Diagnóstico Das Helmintoses de Ruminantes, 4th ed.; JICA: Tokyo, Japan, 1998. [Google Scholar]
31. Echevarria, F.A.M.; Armour, J.L.; Duncan, J.L. Efficacy of Some Anthelmintics on an Ivermectin-Resistant Strain of Haemonchus contortus in Sheep. Vet. Parasitol. 1991, 39, 279–284. [Google Scholar] [CrossRef] [PubMed]
32. Roberts, F.; O’Sullivan, P. Methods for Egg Counts and Larval Cultures for Strongyles Infesting the Gastro-Intestinal Tract of Cattle. Aust. J. Agric. Res. 1950, 1, 99. [Google Scholar] [CrossRef]
33. Makkar, H.P.S. Quantification of Tannins in Tree and Shrub Foliage; Springer: Dordrecht, The Netherlands, 2003. [Google Scholar] [CrossRef]
34. Makkar, H.P.S.; Blümmel, M.; Borowy, N.K.; Becker, K. Gravimetric Determination of Tannins and Their Correlations with Chemical and Protein Precipitation Methods. J. Sci. Food Agric. 1993, 61, 161–165. [Google Scholar] [CrossRef]
35. Dawkins, H.J.S.; Windon, R.G.; Eagleson, G.K. Eosinophil Responses in Sheep Selected for High and Low Responsiveness to Trichostrongylus colubriformis. Int. J. Parasitol. 1989, 19, 199–205. [Google Scholar] [CrossRef] [PubMed]
36. Amarante, A.F.T.; Susin, I.; Rocha, R.A.; Silva, M.B.; Mendes, C.Q.; Pires, A.V. Resistance of Santa Ines and Crossbred Ewes to Naturally Acquired Gastrointestinal Nematode Infections. Vet. Parasitol. 2009, 165, 273–280. [Google Scholar] [CrossRef] [PubMed]
37. Albuquerque, A.C.A.; Bassetto, C.C.; Almeida, F.A.; Hildersley, K.A.; McNeilly, T.N.; Britton, C.; Amarante, A.F.T. Differences in Immune Responses to Haemonchus contortus Infection in the Susceptible Ile de France and the Resistant Santa Ines Sheep under Different Anthelmintic Treatments Regimens. Vet. Res. 2019, 50, 104. [Google Scholar] [CrossRef] [PubMed]
38. Santos, M.C.; Xavier, J.K.; Amarante, M.R.V.; Bassetto, C.C.; Amarante, A.F.T. Immune Response to Haemonchus contortus and Haemonchus Placei in Sheep and Its Role on Parasite Specificity. Vet. Parasitol. 2014, 203, 127–138. [Google Scholar] [CrossRef] [PubMed]
39. Kanobana, K.; Vervelde, L.; Van Der Veer, M.; Eysker, M.; Ploeger, H.W. Characterization of Host Responder Types after a Single Cooperia oncophora Infection: Kinetics of the Systemic Immune Response. Parasite Immunol. 2001, 23, 641–653. [Google Scholar] [CrossRef]
40. Official Methods of Analysis, 16th ed.; AOAC Association of Official Analytical Chemists: Washington, DC, USA, 1995.
41. Diaz Gonzalez, F.H.; Silva, S.C.D. Introdução à Bioquímica Clínica Veterinária, 3rd ed.; UFRGS: Porto Alegre, Brazil, 2017. [Google Scholar]
42. Cueva, C.; Gil-Sánchez, I.; Ayuda-Durán, B.; González-Manzano, S.; González-Paramás, A.; Santos-Buelga, C.; Bartolomé, B.; Moreno-Arribas, M. An Integrated View of the Effects of Wine Polyphenols and Their Relevant Metabolites on Gut and Host Health. Molecules 2017, 22, 99. [Google Scholar] [CrossRef] [PubMed]
43. Domínguez-Avila, J.A.; Villa-Rodriguez, J.A.; Montiel-Herrera, M.; Pacheco-Ordaz, R.; Roopchand, D.E.; Venema, K.; González-Aguilar, G.A. Phenolic Compounds Promote Diversity of Gut Microbiota and Maintain Colonic Health. Dig. Dis. Sci. 2021, 66, 3270–3289. [Google Scholar] [CrossRef]
44. Hoste, H.; Jackson, F.; Athanasiadou, S.; Thamsborg, S.M.; Hoskin, S.O. The Effects of Tannin-Rich Plants on Parasitic Nematodes in Ruminants. Trends Parasitol. 2006, 22, 253–261. [Google Scholar] [CrossRef] [PubMed]
45. Athanasiadou, S.; Kyriazakis, I.; Jackson, F.; Coop, R.L. Direct Anthelmintic Effects of Condensed Tannins towards Different Gastrointestinal Nematodes of Sheep: In Vitro and in Vivo Studies. Vet. Parasitol. 2001, 99, 205–219. [Google Scholar] [CrossRef]
46. Toscan, G.; Cadore, G.C.; Limana, J.F.T.; Weber, A.; Palma, H.H.; Duarte, M.M.F.; Sangioni, L.A.; Vogel, F.S.F. Immune Response of Sheep Naturally Infected with Haemonchus Spp. on Pastures with Two Different Nutritional Conditions. Semin. Cienc. Agrar. 2017, 38, 809. [Google Scholar] [CrossRef]
47. Yang, C.; Han, Y.; Tian, X.; Sajid, M.; Mehmood, S.; Wang, H.; Li, H. Phenolic Composition of Grape Pomace and Its Metabolism. Crit. Rev. Food Sci. Nutr. 2024, 64, 4865–4881. [Google Scholar] [CrossRef]
48. Cash, K.A.; Shanks, B.C.; Caldwell, J.D.; Naumann, H.D.; Bax, A.L.; Wilbers, L.S.; Drane, T.N.; Basinger, K.L.; Clark, J.K.; Bartimus, H. The Use of Organic Pinot Noir Grape Extract as a Natural Anthelmintic in Katahdin Lambs. Sheep Goat Res. J. 2016, 31, 38–44. [Google Scholar]
49. Jourdes, M.; Pouységu, L.; Deffieux, D.; Teissedre, P.-L.; Quideau, S. Hydrolyzable Tannins: Gallotannins and Ellagitannins. In Natural Products; Springer: Berlin/Heidelberg, Germany, 2013; pp. 1975–2010. [Google Scholar] [CrossRef]
50. Ma, H.; Liu, W.; Frost, L.; Wang, L.; Kong, L.; Dain, J.A.; Seeram, N.P. The Hydrolyzable Gallotannin, Penta-O-Galloyl-β-d-Glucopyranoside, Inhibits the Formation of Advanced Glycation Endproducts by Protecting Protein Structure. Mol. Biosyst. 2015, 11, 1338–1347. [Google Scholar] [CrossRef]
51. Chen, F.; Tang, Q.; Ma, H.; Bian, K.; Seeram, N.P.; Li, D. Hydrolyzable Tannins Are Iron Chelators That Inhibit DNA Repair Enzyme ALKBH2. Chem. Res. Toxicol. 2019, 32, 1082–1086. [Google Scholar] [CrossRef] [PubMed]
52. Nogueira, F.A.; Oliveira, L.N.; da Silva, R.B.; Nery, P.S.; Virgínio, G.F.; Geraseev, L.C.; Duarte, E.R. Anthelminthic Efficacy of Banana Crop Residues on Gastrointestinal Nematodes of Sheep: In Vitro and in Vivo Tests. Parasitol. Res. 2012, 111, 317–323. [Google Scholar] [CrossRef] [PubMed]
53. Marie-Magdeleine, C.; Boval, M.; Philibert, L.; Borde, A.; Archimède, H. Effect of Banana Foliage (Musa x Paradisiaca) on Nutrition, Parasite Infection and Growth of Lambs. Livest. Sci. 2010, 131, 234–239. [Google Scholar] [CrossRef]
54. Lima, P.d.M.T.; Crouzoulon, P.; Sanches, T.P.; Zabré, G.; Kabore, A.; Niderkorn, V.; Hoste, H.; Amarante, A.F.T.d.; Costa-Júnior, L.M.; Abdalla, A.L.; et al. Effects of Acacia Mearnsii Supplementation on Nutrition, Parasitological, Blood Parameters and Methane Emissions in Santa Inês Sheep Infected with Trichostrongylus colubriformis and Haemonchus contortus. Exp. Parasitol. 2019, 207, 107777. [Google Scholar] [CrossRef] [PubMed]
55. Cenci, F.B.; Louvandini, H.; McManus, C.M.; DelľPorto, A.; Costa, D.M.; Araújo, S.C.; Minho, A.P.; Abdalla, A.L. Effects of Condensed Tannin from Acacia Mearnsii on Sheep Infected Naturally with Gastrointestinal Helminthes. Vet. Parasitol. 2007, 144, 132–137. [Google Scholar] [CrossRef] [PubMed]
56. Armonavičius, D.; Stankevičius, M.; Maruška, A. Extraction of Bioactive Compounds and Influence of Storage Conditions of Raw Material Chamaenerion angustifolium (L.) Holub Using Different Strategies. Molecules 2024, 29, 5530. [Google Scholar] [CrossRef] [PubMed]
57. Peron, G.; Ferrarese, I.; Carmo Dos Santos, N.; Rizzo, F.; Gargari, G.; Bertoli, N.; Gobbi, E.; Perosa, A.; Selva, M.; Dall’Acqua, S. Sustainable Extraction of Bioactive Compounds and Nutrients from Agri-Food Wastes: Potential Reutilization of Berry, Honey, and Chicory Byproducts. Appl. Sci. 2024, 14, 10785. [Google Scholar] [CrossRef]
58. Lavelli, V.; Sri Harsha, P.S.C. Grape Pomace as a Source of Phenolics for Inhibition of Starch Digestion Enzymes: Comparative Study and Standardization of the Efficacy. Preprints 2024. [Google Scholar] [CrossRef]
59. Aruwayo, A.; Maigandi, S.; Malami, B.; Daneji, A. Haematological and Biochemical Indices of Growing Lambs Fed Fore-Stomach Digesta and Poultry Litter Waste. Niger. J. Basic. Appl. Sci. 2010, 17, 223–228. [Google Scholar] [CrossRef][Green Version]
60. de Evan, T.; Cabezas, A.; de la Fuente, J.; Carro, M.D. Feeding Agroindustrial Byproducts to Light Lambs: Influence on Growth Performance, Diet Digestibility, Nitrogen Balance, Ruminal Fermentation, and Plasma Metabolites. Animals 2020, 10, 600. [Google Scholar] [CrossRef]
61. Nascimento, C.d.O.; Pina, D.d.S.; Santos, S.A.; de Araújo, M.L.G.M.L.; Cirne, L.G.A.; Alba, H.D.R.; Rodrigues, T.C.G.C.; Silva, W.P.; Rodrigues, C.S.; Tosto, M.S.L.; et al. Whole Corn Germ as an Energy Source in the Feeding of Feedlot Lambs: Metabolic and Productive Performance. Animals 2022, 12, 1261. [Google Scholar] [CrossRef]
62. Cheng, X.; Du, X.; Liang, Y.; Degen, A.A.; Wu, X.; Ji, K.; Gao, Q.; Xin, G.; Cong, H.; Yang, G. Effect of Grape Pomace Supplement on Growth Performance, Gastrointestinal Microbiota, and Methane Production in Tan Lambs. Front. Microbiol. 2023, 14, 1264840. [Google Scholar] [CrossRef]
63. Adiwinarti, R.; Lestari, C.M.S.; Purbowati, E.; Restitrisnani, V.; Purnomoadi, A.; Rianto, E. Agricultural Byproducts in Lamb’s Diet Can Substitute Napier Grass without Decreasing Lambs Products. In AIP Conference Proceedings; AIP Publishing: Melville, NY, USA, 2023; p. 040001. [Google Scholar] [CrossRef]
64. Maciel, M.B.; Pires, C.C.; Mello, R.d.O.; Fagundes, M.B.; Wagner, R.; de Vargas, D.P. Performance and Meat Quality of Lambs Fed with Grape Pomace Silage. Res. Sq. 2023. [Google Scholar] [CrossRef]
65. Onyeonagu, C.; Njoku, O. Crop Residues and Agro-Industrial by-Products Used in Traditional Sheep and Goat Production in Rural Communities of Markudi LGA. Agro-Science 2011, 9. [Google Scholar] [CrossRef]
66. García-Rodríguez, J.; Ranilla, M.J.; France, J.; Alaiz-Moretón, H.; Carro, M.D.; López, S. Chemical Composition, In Vitro Digestibility and Rumen Fermentation Kinetics of Agro-Industrial By-Products. Animals 2019, 9, 861. [Google Scholar] [CrossRef] [PubMed]
67. Food Waste Index Report 2024; United Nations Environment Programme: Nairobi, Kenya, 2024; p. 173.
68. de Castro, V.C.G.; Budel, J.C.d.C.; Rodrigues, T.C.G.d.C.; Silva, B.A.; de Lima, A.C.S.; de Souza, S.M.; da Silva, J.A.R.; Joele, M.R.S.P.; Silva, A.G.M.e.; Lourenço-Junior, J.d.B. Nutrient Intake, Digestibility, Performance, Carcass Traits and Sensory Analysis of Meat from Lambs Fed with Co-Products of Amazon Oilseeds. Front. Vet. Sci. 2023, 10, 1181765. [Google Scholar] [CrossRef] [PubMed]
Mena MO, Trevise GGO, Silva TNR, Moellmann VM, Bassetto CC, Gatti BS, Louvandini H, Soutello RVG, Albuquerque ACA, Amarante AFT. Evaluation of Grape Pomace Supplementation in Lamb Diets to Mitigate Haemonchus contortus Infection. Agriculture. 2025; 15(3):341. https://doi.org/10.3390/agriculture15030341
Перевод статьи «Evaluation of Grape Pomace Supplementation in Lamb Diets to Mitigate Haemonchus contortusInfection» авторов Mena MO, Trevise GGO, Silva TNR, Moellmann VM, Bassetto CC, Gatti BS, Louvandini H, Soutello RVG, Albuquerque ACA, Amarante AFT., оригинал доступен по ссылке. Лицензия: CC BY. Изменения: переведено на русский язык
Фото: freepik











































































































Комментарии (0)