Нуг абиссинский (Guizotia abyssinica): использование скрытого потенциала малораспространенной масличной культуры с помощью селекции и биотехнологий
В данном обзоре рассматривается применение традиционных методов селекции и генетических инструментов для улучшения нуга абиссинского , с акцентом на культуру растительных тканей, молекулярные маркеры и выявление перспективных генов-мишеней для получения желаемых признаков. Передовые технологии, такие как CRISPR/Cas, включая редактирование оснований и прайм-редактирование, открывают большие перспективы для революционных изменений в селекции этой культуры и исследованиях функциональной геномики.
Аннотация
Нуг (гвизотия абиссинская, Guizotia abyssinica (L. f.) Cass.), масличная культура семейства Астровые (Сложноцветные), произрастает в регионах с умеренным и тропическим климатом. Его мелкие семена, богатые маслом (50–60% биосырья), широко используются для производства биодизеля, мыла, а также в качестве приправы в кулинарии. Кроме того, убранные растения нуга служат сидеральным удобрением, способствуя улучшению здоровья почвы. Однако за последнее десятилетие выращивание этой культуры в Индии значительно сократилось из-за низкой урожайности, плохого завязывания семян, самостерильности, низкого индекса урожайности и осыпаемости семян. Недостаток генетического разнообразия дополнительно ограничивает возможности селекционеров по созданию высокоурожайных сортов. Открытие наследственной мужской стерильности в Индии позволило использовать явление гетерозиса и заложило основу для выведения улучшенных сортов. В данном обзоре рассматривается применение традиционных методов селекции и генетических инструментов для улучшения нуга, с акцентом на культуру растительных тканей, молекулярные маркеры и выявление перспективных генов-мишеней для получения желаемых признаков. Передовые технологии, такие как CRISPR/Cas, включая редактирование оснований и прайм-редактирование, открывают большие перспективы для революционных изменений в селекции этой культуры и исследованиях функциональной геномики. Выводы, представленные в этой статье, подчеркивают острую необходимость генетического улучшения нуга и других малоиспользуемых масличных культур для удовлетворения растущего мирового спроса на устойчивые и разнообразные источники масличного сырья. Такие меры позволят трансформировать возделывание нуга, обеспечив его роль в мировом сельском хозяйстве.
1. Введение
Нуг (гвизотия абиссинская, Guizotia abyssinica (L. f.) Cass.) является диплоидным видом с 2n = 30 и размером генома около 3,8 пг [1]. Нуг — важная второстепенная масличная культура в Индии, Кении, Уганде, Судане, Малави и других странах Африканского континента и Индийского субконтинента. Это двудольное травянистое растение, умеренно или хорошо ветвящееся, достигающее в высоту до 2 м. Семена содержат около 40% масла с жирнокислотным составом: 75–80% линолевой кислоты, 7–8% пальмитиновой и стеариновой кислот, а также 5–8% олеиновой кислоты [2]. Индийские разновидности содержат 25% олеиновой и 55% линолевой кислот [3]. Масло нуга также используется как заменитель оливкового масла. Масло нуга обладает хорошей сохраняемостью, содержит <70% ненасыщенных жирных кислот и не содержит токсинов, поэтому считается полезным для здоровья [2]. Нуг признан «забытой и малоиспользуемой» культурой [4], и вследствие этого он получил мало внимания со стороны исследователей. Нуг обладает потенциалом для достижения самообеспеченности производством растительного масла в Индии. Масло нуга может использоваться в качестве краски, смазочного материала или корма для животных, а также вносится в поле в качестве удобрения. Низкоурожайные сорта, самостерильность, проблемы полегания и осыпаемости, восприимчивость к вредителям и т. д. являются основными ограничениями для создания высокоурожайных сортов с помощью традиционных программ селекции растений [4]. Биотехнологические культуры, которые включают трансгенные, генетически модифицированные культуры или нетрансгенные культуры, созданные с помощью редактирования генов без использования ДНК, помогают создать или модифицировать продукт для практической цели. Эта культура может помочь решить проблемы производства сельскохозяйственных культур, которые традиционные технологии не смогли решить, и может быть использована для повышения урожайности и производства с помощью биотехнологии, геномики и маркер-ориентированных методов селекции [5].
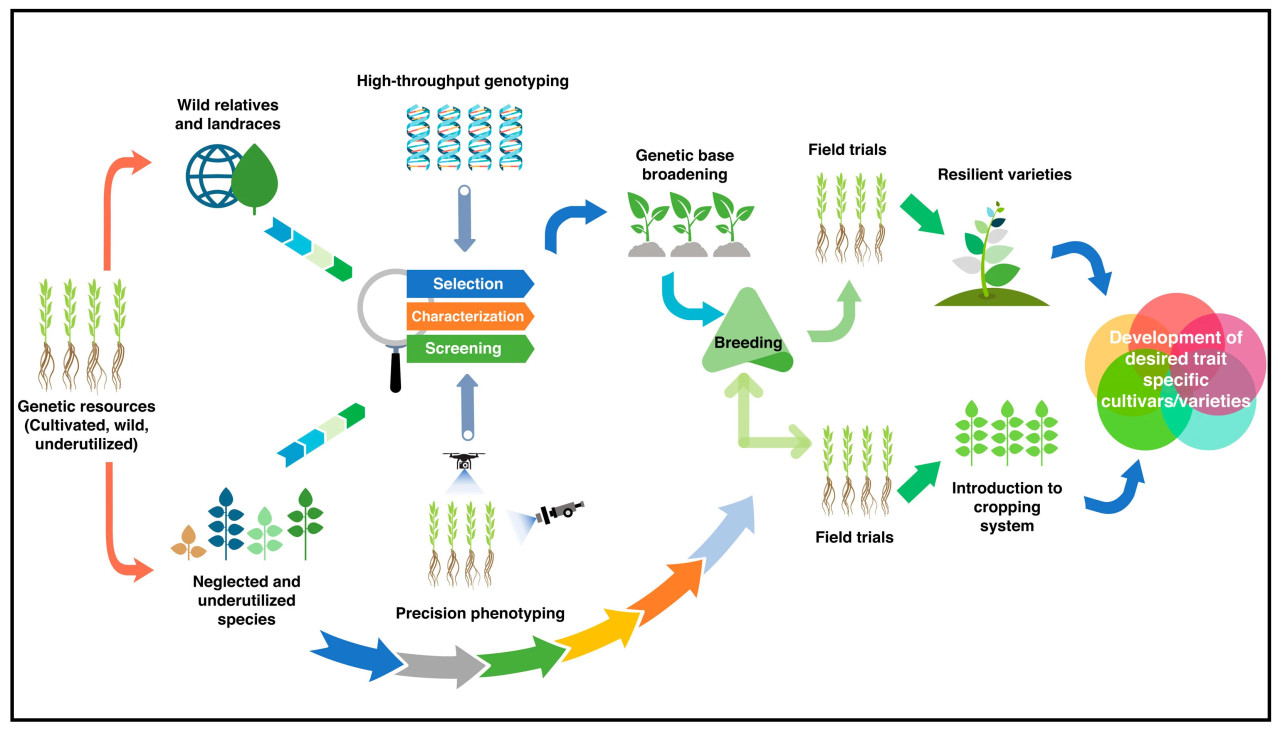
В данном обзоре рассматривается применение традиционной селекции, геномики и биотехнологических инструментов для малоиспользуемой культуры нуга с целью создания сортов с желаемыми признаками. Инструменты редактирования генома CRISPR/Cas были использованы для некоторых масличных культур для улучшения их признаков [6]. В данном обзоре также подчеркивается, насколько важны геномные методы для поиска, идентификации и использования желаемых признаков у диких родичей культурных растений (Рисунок 1).
Рисунок 1. Стратегии селекции и молекулярные стратегии для создания сортов нуга с желаемыми признаками. Отбор, характеристика и скрининг генетических ресурсов, таких как культурные и дикие виды, местные сорта и забытые малоиспользуемые культуры, осуществляются с помощью традиционных и современных методов селекции и биотехнологических подходов для создания устойчивых сортов/разновидностей нуга с желаемыми признаками. Точное фенотипирование может быть использовано для понимания физиологии и генетики селекционного гермплазмы, а затем преобразовано в методы высокопроизводительного фенотипирования и потенциально в молекулярные маркеры для быстрого скрининга нуга. Высокопроизводительное генотипирование идентифицирует генетические вариации среди лучших линий. Геномная селекция, передовой метод маркер-ориентированной селекции в методах селекции растений, является одним из нескольких подходов, отвечающих этим требованиям. Она использует полногеномные маркеры, информацию о фенотипе, полевые испытания и идентификацию лучших линий. Идентифицированные гены-кандидаты и маркеры, связанные с желаемыми признаками, обнаруженные в результате высокопроизводительного секвенирования и анализа данных фенотипирования, позволят проводить рекомбинацию превосходных генотипов растений, внедряемых в систему севооборота, для создания сортов/разновидностей нуга с желаемыми признаками.
2. Объем производства семян нуга в Индии
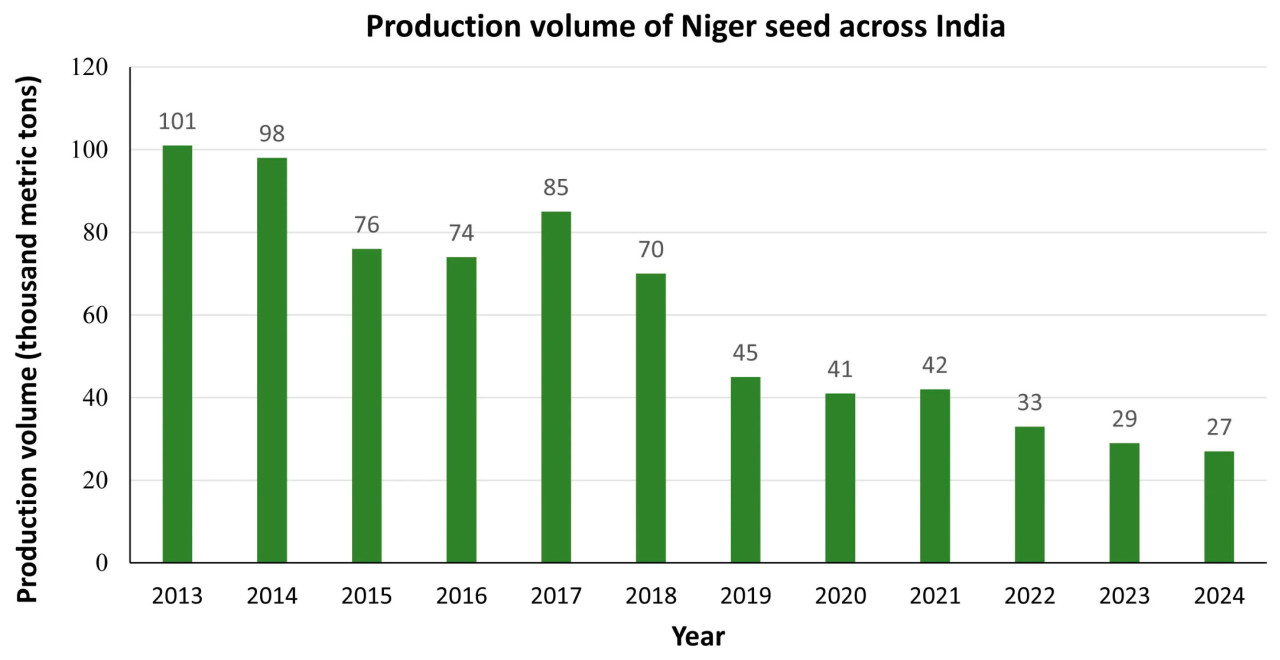
Индия занимает первое место по производству и экспорту семян нуга [7]. Он возделывается в штатах Андхра-Прадеш, Мадхья-Прадеш, Орисса, Махараштра, Бихар, Карнатака, Нагар-Хавели и Западная Бенгалия, из которых Мадхья-Прадеш является крупнейшим производителем. График на Рисунке 2 показывает самый высокий объем производства в финансовом году 2013 (101 000 метрических тонн) и самый низкий объем производства в 2024 году — 27 000 метрических тонн. Начиная с 2013 года производство нуга снижалось, но в 2017 году производство немного увеличилось, а затем снова снизилось. Нуг имеет высокое содержание масла около 40% с ценным составом жирных кислот. Однако высокое содержание ненасыщенных жирных кислот приводит к плохой сохраняемости, что ограничивает его более широкое использование. Такие факторы, как отсутствие государственного интереса к традиционной кухне племен, ограниченная генетическая изменчивость, восприимчивость к болезням, отсутствие разнообразных сортов, осыпаемость, самостерильность, низкая или слабая отзывчивость на агротехнические мероприятия [8] и малое внимание со стороны исследователей, в основном способствовали снижению производства, и нуг в основном остался малоиспользуемой масличной культурой [9]. Существует необходимость увеличить производство нуга.
Рисунок 2. Объем производства семян нуга в Индии с 2013 по 2024 год (в тысячах метрических тонн) (источник: https://www.statista.com/statistics/769707/india-niger-seed-production-volume).
В Африке семена нуга в основном выращиваются в Эфиопии, а также в меньших масштабах в Судане, Уганде, Танзании, Малави и Зимбабве [10]. Семена нуга (Guizotia abyssinica) являются ключевым источником пищевого масла в Эфиопии, в основном выращиваются мелкими фермерами. Они обеспечивают около 30% производства масличных культур в стране, причем 26% оставляется для домашнего использования. Хотя нуг выращивается по всей Эфиопии, более 90% производится в высокогорьях Амхары и Оромии. Ключевые районы производства включают Волегга и Шева в Оромии, а также Годжам и Гондар в Амхаре. Основными возделываемыми сортами являются Абат, Месно и Бунегне [10].
Объем производства семян нуга в Эфиопии
Производство семян нуга имеет долгую историю в Эфиопии и остается значимой культурой, составляя 50–60% от объема производства масличных культур в стране. По данным Центрального статистического агентства (CSA) Эфиопии, за последние 18 лет его производство удвоилось, увеличившись с 1,04 млн квинталов до примерно 3 млн квинталов. Это улучшение, вероятно, обусловлено внедрением улучшенных сортов и совершенствованием агротехнических приемов, таких как внесение удобрений, своевременная посадка, выбор участка и эффективное управление полями [11]. Это свидетельствует о потенциале увеличения производства и продуктивности путем создания подходящих сортов и совершенствования агротехнических приемов с использованием методов селекции и биотехнологий.
3. Ограничения культуры
Нуг имеет недетерминантный характер роста и чрезвычайно низкий индекс урожайности [12]. Склонность к полеганию и осыпаемость семян напрямую влияют на урожайность семян. Из-за его самостерильной природы трудно создать инбредную линию, и традиционная селекционная работа с нугом является очень сложной для проведения [13]. Однако использование методов улучшения популяций должно привести к стабильному генетическому прогрессу, а самофертильные типы, встречающиеся в Эфиопии, могут быть использованы для создания высокоурожайных синтетических популяций или даже гибридов. Сибсовое спаривание играет важную роль в создании инбредных линий; следовательно, оно может помочь в развитии самоопыленных семян (самофертильные типы). Насекомые и вредители, такие как нигрная муха, атакуют цветки нуга, питаются соцветиями и препятствуют завязыванию семян и опылению, вызывая прямое снижение завязываемости семян, что было отмечено [14,15,16]. Насекомые — черные пыльцевые жуки — питаются соцветиями, тем самым снижая завязываемость семян [16]. По сравнению с другими масличными культурами нуг менее подвержен возникновению болезней. Такие заболевания, как стеблевая и листовая пятнистость нуга, могут быть проблемой для современных сортов. Семена нуга имеют высокое содержание клетчатки, и производители масел сообщают, что они имеют более низкий процент извлечения масла по сравнению с другими масличными семенами. Согласно отчету, животные, которых кормили жмыхом нуга, набирают меньший вес, чем те, которых кормили жмыхом из других масличных семян, хотя в нуге не известно о наличии токсичных или антипитательных факторов [7].
4. Сохранение гермплазмы нуга
Национальное бюро генетических ресурсов растений (NBPGR), Индия, обеспечило долгосрочное сохранение гермплазмы ex situ в Индии. Базовая коллекция хранится для долгосрочного хранения при –20 °C, тогда как среднесрочное хранение осуществляется при 4 °C. Крайне важно определить процент генетического разнообразия, представленного в этих сохраняемых коллекциях, выявить то, что остается несохраненным, и разработать стратегии использования доступных ресурсов. NBPGR хранит 1807 образцов гермплазмы нуга [17]. Приоритет следует отдавать находящимся под угрозой ресурсам, особенно диким видам. Из-за своей самостерильности нуг является перекрестноопыляемым растением. Чтобы сохранить его гермплазму в безопасности, ее содержат в нескольких местах, группируя растения для предотвращения перекрестного скрещивания между образцами (Рисунок 3).
Рисунок 3. Снимок с дрона участка размножения/регенерации семян для селекции нуга на кампусе Индийского совета сельскохозяйственных исследований — Национального бюро генетических ресурсов растений (ICAR-NBPGR), Акола, Индия, датированный 15 декабря 2020 года. Здесь представлены 1700 различных образцов нуга вместе со стандартами, используемыми для размножения семян. С левой границы: 2 ряда — стандарты JNS 28 и JNS 30; средние 9 рядов — 1700 образцов для размножения семян; с правой границы: 2 ряда — стандарты JNS 9 и IGPN 2004-1.
В Индии генетическое разнообразие было использовано путем прямого отбора местного адаптированного материала. До сих пор улучшенные методы селекции растений использовались для нуга в наименьшей степени. Генетическая основа сортов ограничена. Поэтому использование гермплазмы должно быть расширено для генетического улучшения нуга. Дикие родичи культурных растений или гермплазма служат ресурсами для улучшения генетических показателей культурных растений, предоставляя всестороннюю справку о генетическом разнообразии для улучшения определенных признаков. Таким образом, дикие виды могут быть использованы для улучшения признаков культурных растений [18]. Использование селекции и биотехнологии оказало большое влияние на расширение генетической базы гермплазмы нуга для широкого спектра агрономических признаков и сделало возможным создание новых сортов с улучшенными качественными и количественными признаками [19].
5. Селекция и улучшение культуры
Гетерогенная популяция семян нуга в Индии предоставляет значительный потенциал для повышения урожайности с помощью различных селекционных программ. Ключевые цели включают увеличение урожайности и содержания масла при одновременном снижении осыпаемости. Снижение высоты растений улучшает индекс урожайности за счет уменьшения количества листьев и повышения эффективности использования удобрений, что тем самым увеличивает урожайность семян. Из-за своей самостерильности нуг подходит для создания гибридных сортов, подобно подсолнечнику. Открытие генетической мужской стерильности в Индии [20] позволило использовать гетерозис у нуга.
Мутационная селекция с использованием химического и физического мутагенеза создала генетическую изменчивость для создания сортов с желаемыми признаками [21,22]. Были выделены мутанты с такими признаками, как высокое содержание олеиновой кислоты и масла, и четыре лучшие линии (OY-155, OY-325, HO-308 и OO-309) были разработаны для использования в сельском хозяйстве. Повышенный уровень олеиновой кислоты стал результатом индуцированных мутаций, влияющих на десатурацию олеиновой кислоты, что привело к снижению содержания полиненасыщенных жирных кислот [23]. Дикие виды Guizotia (G. scabra subsp. Schimperi) предоставляют гены устойчивости к болезням для интрогрессии в культивируемые виды [2]. Мутационная и трансгенная селекция образуют ключевые основы современных программ селекции нуга [24,25]. Misal и др. 2021 [25] изучили и пришли к выводу, что возвратная селекция имеет потенциал для создания высокоурожайных сортов нуга, подчеркивая ее важность для устойчивой продовольственной безопасности. В 2020 году Amsalu [26] показал, что наличие значительной изменчивости среди различных генотипов нуга по всем изученным признакам может быть использовано в селекционной программе для создания сортов с высоким выходом масла, высокой урожайностью семян и ранним созреванием. Аналогично, генетическая дивергенция среди протестированных генотипов свидетельствует о потенциале выявления разнообразного материала с желаемыми агрономическими признаками, позволяя создавать превосходные сорта нуга путем гибридизации и отбора образцов из разных кластеров [8].
Приоритетом программы улучшения нуга является увеличение содержания масла в семенах и преодоление проблем растрескивания стручков и самостерильности. Гермплазма с разнообразным содержанием масла доступна в Эфиопии и Индии, и она может быть включена в селекционную программу для значительного увеличения содержания масла. Характер опыления благоприятствует программе генетического улучшения нуга. Метод рекуррентной селекции используется в качестве стандартной процедуры селекции для создания сортов со свободным опылением из-за их самостерильности. Таким образом, нуг является кандидатом для создания гибридов. Идентификация генетической мужской стерильности в Индии и недавно в Эфиопии проложила путь к использованию гетерозиса у нуга.
6. Биотехнологические подходы к улучшению нуга
Использование биотехнологии для улучшения культур является очень важным, поскольку оно помогает в пирамидировании генов, оценке генетического разнообразия, ускоренной селекции с помощью геномики и генетических модификациях, которые увеличивают питательную ценность, содержание масла и устойчивость к биотическим и абиотическим стрессам. Проблема самостерильности у нуга усложняет создание и поддержание инбредных линий, как отметили Getinet и Teklewold [2]. Этот биологический барьер предотвращает самооплодотворение, которое является критически важным для достижения генетической однородности в селекционных программах. Однако in vitro технологии предлагают перспективную альтернативу для генетического улучшения. Эти методы включают такие техники, как культивирование in vitro, соматический эмбриогенез и прямую регенерацию, которые позволяют размножать и манипулировать растениями в контролируемых условиях [2]. Надежная система регенерации растений является ключевой для успеха in vitro подходов. Она обеспечивает стабильное и эффективное развитие растений из эксплантов, соматических клеток или тканей, тем самым способствуя генетическому улучшению нуга, обходя ограничения, налагаемые его самостерильностью. In vitro технологии, такие как культура растительных тканей, играют важную роль в системе регенерации растений [18]. Соматический эмбриогенез является успешным методом, используемым для регенерации растений нуга из суспензионных культур [27]. Agrobacterium-опосредованная генетическая трансформация играет значительную роль в переносе специфических желаемых генов в культуры. Биотехнологические подходы к изучению и улучшению нуга подробно рассматриваются ниже.
6.1. Культура растительных тканей
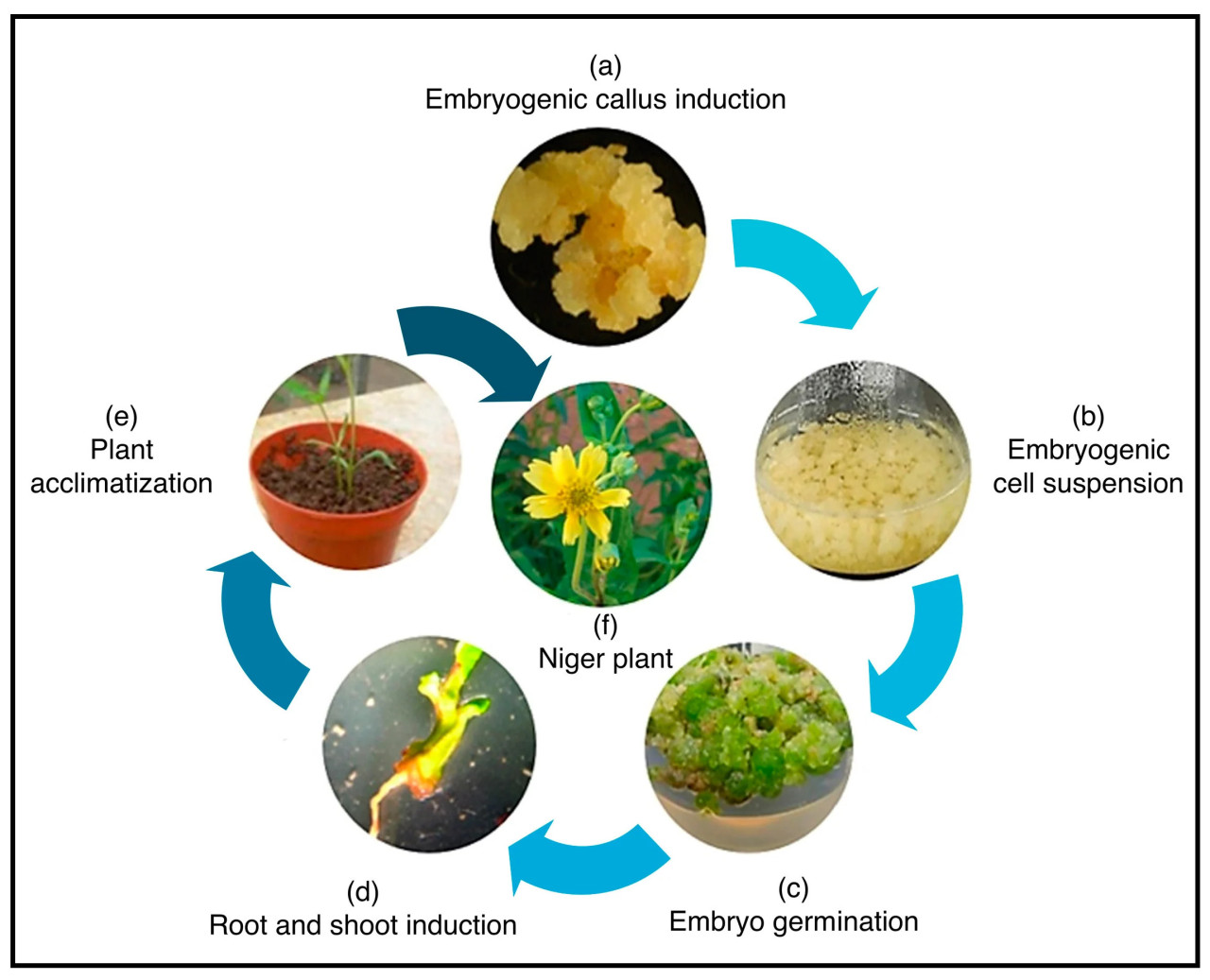
Культура растительных тканей нуга предлагает перспективное направление для развития сельского хозяйства. Этот метод позволяет осуществлять быстрое размножение элитных сортов, производство безболезненных растений и генетическое улучшение ключевых признаков культур [28,29]. Нуг был широко изучен в клеточных и тканевых культурах, причем регенерация была зарегистрирована из различных эксплантов, включая листья [30,31,32], пыльники [33,34,35], семядоли и гипокотили [36,37,38]. Tiwari и др. [5] подчеркнули полезность культуры пыльников для создания гомозиготных линий, которые могут быть включены в селекционные программы для гибридизации. Было обнаружено, что соматический эмбриогенез (Рисунок 4) с использованием суспензионных культур имеет большой потенциал. Он может помочь в проведении отбора in vitro вариантов и улучшении культур, устойчивых к биотическим и абиотическим стрессам [27].
Рисунок 4. Применение соматического эмбриогенеза у малоиспользуемой культуры нуга. (a) Эмбриогенный нодулярный каллюс, индуцированный из эксплантов незрелых зародышей. (b) Эмбриогенные клетки суспензионной культуры, которые подверглись делению и образовали клеточные кластеры. (c) Прорастание соматических зародышей. (d) Развитие побега и корня. (e) Растение, регенерированное из соматического зародыша, и пересаженное в теплицу для акклиматизации. (f) Созревшее растение нуга с цветением.
Было сообщено, что с помощью культуры пыльников были получены гаплоиды и созданы растения с крупными соцветиями, карликовые и самофертильные растения, которые полезны для улучшения нуга, в частности для преодоления проблем самостерильности и низкой урожайности [34]. Jadimath и др. [32] эффективно поддерживали мужскостерильные растения с помощью метода тканевой культуры и использовали экспланты листьев мужскостерильного растения, которые были получены с помощью гамма-облучения. Культура пыльников используется для создания дигаплоидных растений и самофертильных линий, таких как карликовые и односоцветные дигаплоидные растения. Дигаплоидные растения, полученные из культуры пыльников, могут быть использованы для создания гомозиготных инбредных линий в течение короткого времени [19]. Нуг был в центре различных исследований клеточных и тканевых культур, подчеркивающих его потенциал для улучшения и сохранения культуры. Регенерация растений через тканевую культуру была успешно зарегистрирована с использованием специфических эксплантов, таких как семядоли и гипокотили [33,36,37]. Развитие методов тканевой культуры может решить некоторые из присущих культуре проблем, таких как низкая урожайность, восприимчивость к болезням и проблемы адаптации, тем самым раскрывая ее полный потенциал для сельскохозяйственного и промышленного применения [39]. Использование культуры пыльников и методов тканевой культуры у нуга является перспективным для дальнейших достижений. Эти методы могут повысить эффективность селекции за счет быстрого создания гомозиготных инбредных линий, улучшая урожайность и признаки самофертильности.
In vitro методы являются важными инструментами для улучшения культур и привели к индукции сомаклональных вариаций [40]. Несколько методов, включая кариотипирование и изоферментное профилирование, используются для оценки генетической подлинности клонов, полученных in vitro. Однако эти подходы имеют присущие им ограничения. Кариотипирование не выявляет хромосомные перестройки и изменения в генах, тогда как изоферментное профилирование подвержено онтогенетическим вариациям [41]. Поэтому крайне важно использовать молекулярные маркеры для обнаружения вариаций в генах или генетических взаимосвязей между особями внутри и между видами. Интеграция с методами генетической трансформации может позволить внедрять такие признаки, как устойчивость к болезням и толерантность к абиотическим стрессам. В целом, эти биотехнологические инструменты могут привести к значительным улучшениям в продуктивности и устойчивости возделывания нуга.
6.2. Технология молекулярных маркеров
Молекулярные маркеры предоставляют огромную поддержку селекции растений и значительно ускоряют усилия по улучшению культур [42,43]. Эти маркеры играют ключевую роль в характеристике и оценке доступной гермплазмы с помощью ДНК-фингерпринтинга, оценке генетической изменчивости и генетического разнообразия [43]. Потенциал улучшения культуры с помощью селекции зависит от величины генетического разнообразия и генетической изменчивости. Крайне важно охарактеризовать и оценить внутреннюю ценность сохраняемой гермплазмы. Доступные коллекции разнообразных образцов дикой и культивируемой гермплазмы значительно способствовали улучшению культур [5]. Молекулярные маркеры обладают огромным потенциалом для изучения генетического разнообразия и изменчивости и для интерпретации в полиморфной форме [44,45,46]. RAPD-маркеры в основном использовались для изучения филогенетических взаимосвязей у нуга и его диких родичей. Geleta и др. [47] исследовали генетическое разнообразие и изменчивость 70 популяций эфиопского нуга с помощью RAPD-маркеров и обнаружили 97% полиморфизма. Это исследование показало, что генетически отдаленные популяции, которые были ограничены различными кластерами, являются уникальными и могут быть включены в программу маркер-ориентированной селекции для улучшения культуры. Nagella и др. [48] изучили генетическое разнообразие нескольких образцов индийской гермплазмы нуга с использованием RAPD-маркеров. Это была первая попытка использовать молекулярные маркеры для количественной оценки генетического разнообразия среди сортов индийского нуга. Dempewolf и др. [49] разработали библиотеку EST и сконструировали 43 SSR с использованием последовательностей EST и последовательности хлоропластного генома. Эти микросателлитные маркеры были использованы для оценки генетического разнообразия и генетической изменчивости среди различных генотипов, что привело к лучшему пониманию филогеографических паттернов. Секвенирование по Сэнгеру было использовано для получения полной последовательности хлоропластного генома, которая была представлена в Genebank (идентификатор GeneBank EU549769/Refseq NC 010601) после аннотации. Аналогичным образом, Tsehay и др. [1] идентифицировали SNP-маркеры с помощью секвенирования транскриптома двух генотипов, что привело к созданию KASP-анализов для 554 SNP для генотипирования у нуга. В настоящее время отсутствуют глобальные сообщения о картировании признаков или маркер-ориентированной селекции у нуга, которые могли бы нацеливаться на такие признаки, как устойчивость к абиотическому стрессу, устойчивость к болезням, урожайность и качество [50].
Будущие исследования должны быть сосредоточены на создании высокоплотных генетических карт, которые интегрируют различные типы маркеров (SNP, SSR и т. д.) для точного QTL-картирования ключевых агрономических признаков, таких как выход масла, устойчивость к болезням и толерантность к стрессам. Эта интегрированная карта в сочетании с фенотипическими данными из разнообразной гермплазмы будет поддерживать надежные стратегии маркер-ориентированной селекции для ускорения улучшения нуга. Кроме того, полная последовательность хлоропластного генома открывает возможности для хлоропластной трансформации в генетической инженерии. Исследования должны нацеливаться на объединение этих молекулярных ресурсов с передовыми методами селекции для эффективного внедрения желаемых признаков в сорта нуга, повышения продуктивности и решения проблем продовольственной безопасности.
6.3. Генетическая трансформация
Генетическая трансформация предоставляет средство для решения многих проблем и улучшения ключевых признаков в культурах. Но разработка эффективных протоколов трансформации остается ключевой для успешной реализации стратегий генетической инженерии в культурах, включая нуг. Для улучшения ключевых признаков нуга и его масла необходимо создать эффективные протоколы трансформации для генетического улучшения. Чтобы преодолеть такие ограничения, как самостерильность, осыпаемость и восприимчивость к болезням, генетическое улучшение нуга является необходимым [4,39]. Успех таких генетических улучшений зависит от создания надежного и эффективного протокола трансформации [39]. Генетическая трансформация — это метод, при котором ген, представляющий интерес, переносится или вставляется в желаемый генотип.
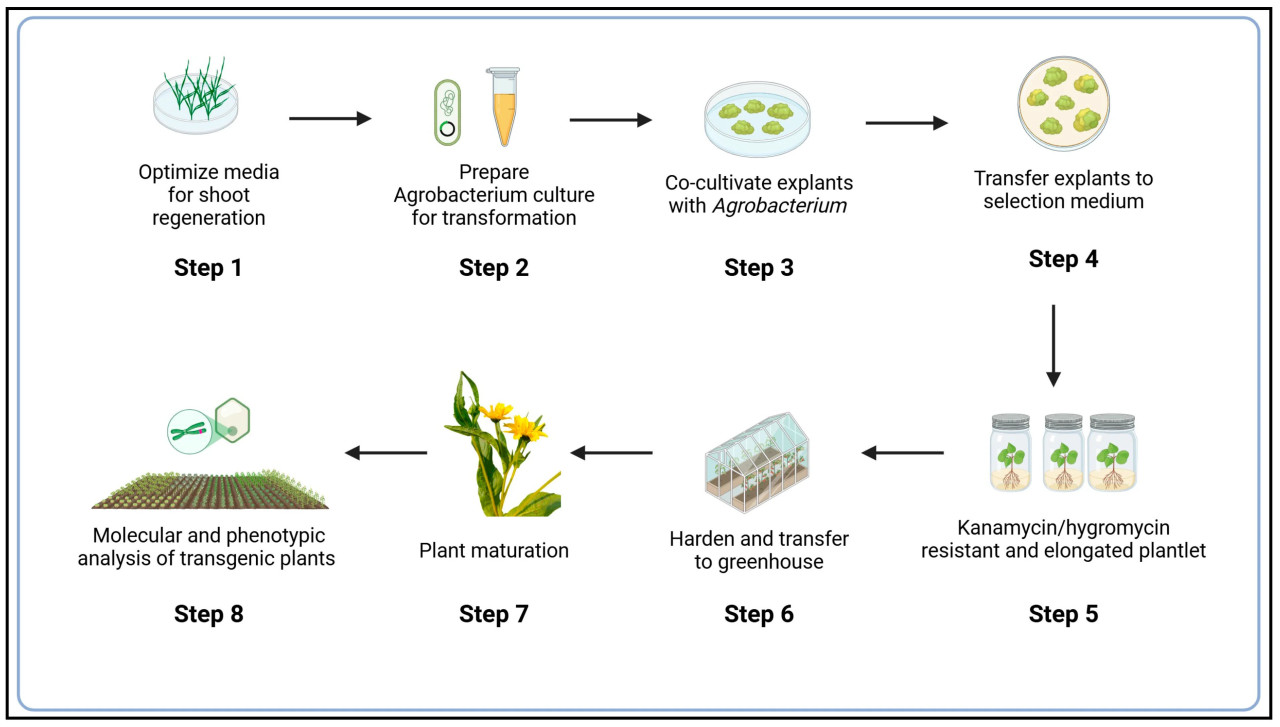
На сегодняшний день доступен только один отчет об Agrobacterium-опосредованной генетической трансформации нуга. Murthy и др. [39] сообщили о протоколе Agrobacterium-опосредованной генетической трансформации нуга с использованием эксплантов гипокотилей и семядолей сорта UNS-4. Семидневные проростки использовались в качестве эксплантов для трансформации. Экспланты культивировали на среде MS с различными концентрациями 6-бензиламинопурина (BA) для регенерации побегов. Штамм Agrobacterium tumefaciens EHA101 с бинарным вектором pIG121Hm использовался для трансформации. T-ДНК-область содержала гены nptII и hpt в качестве селективных маркеров и ген GUS в качестве репортерного гена, находящиеся под контролем промотора CaMV 35S [39]. Совместное культивирование происходило в течение 3 дней при 22 °C. После совместного культивирования экспланты переносили на селекционную и регенерационную среды. После успешной регенерации растения акклиматизировали в теплице [39]. Agrobacterium-опосредованная трансформация нуга с использованием эксплантов проростков изображена на Рисунке 5.
Рисунок 5. Протокол Agrobacterium-опосредованной трансформации нуга. Этап (1): оптимизация среды для регенерации побегов; этап (2): приготовление штамма Agrobacterium tumefaciens (например, EHA101) для генетической трансформации; этап (3): совместное культивирование эксплантов с Agrobacterium; этап (4): перенос на селекционную среду (среда MS, содержащая 1 мг/л BA, 50 мг/л канамицина и 50 мг/л гигромицина); этап (5): отделение устойчивых удлиненных корней (длиной 3–4 см) и перенос на среду для укоренения; этап (6): закаливание и перенос в теплицу; этап (7): созревание растений; этап (8): молекулярный и фенотипический анализ трансгенных растений (создано в https://BioRender.com).
В этом исследовании частота трансформации семядолей составила 15%, тогда как частота трансформации гипокотилей составила только 3% [39]. В настоящее время нет других сообщений о трансформации нуга. Будущие исследования должны быть сосредоточены на разработке высокопроизводительных, эффективных и экономически эффективных систем трансформации. Это требует оптимизации существующих протоколов, изучения новых технологий редактирования генов, таких как CRISPR/Cas9, и исследования альтернативных источников эксплантов. Для повышения эффективности генетической трансформации нуга необходим многосторонний подход. Расширение спектра протестированных эксплантов за пределы тех, что использовались Murthy и др. [39], является ключевым. Различные ткани могут иметь различные реакции на трансформацию, что требует оптимизации условий тканевой культуры для регенерации. Это включает улучшение состава среды, концентраций гормонов и параметров культивирования для улучшения развития побегов и корней из трансформированных эксплантов. Сравнительный анализ штаммов Agrobacterium является важным из-за их различной вирулентности и эффективности трансформации. Изучение различных плазмид с различными селективными маркерами и точками начала репликации повысит успех трансформации. Кроме того, тестирование различных промоторов для экспрессии трансгенов является ключевым для последовательности. Систематическое исследование этих факторов поможет выявить оптимальные условия для эффективной и надежной трансформации нуга.
7. Обзор редактирования генома и его применение у нуга
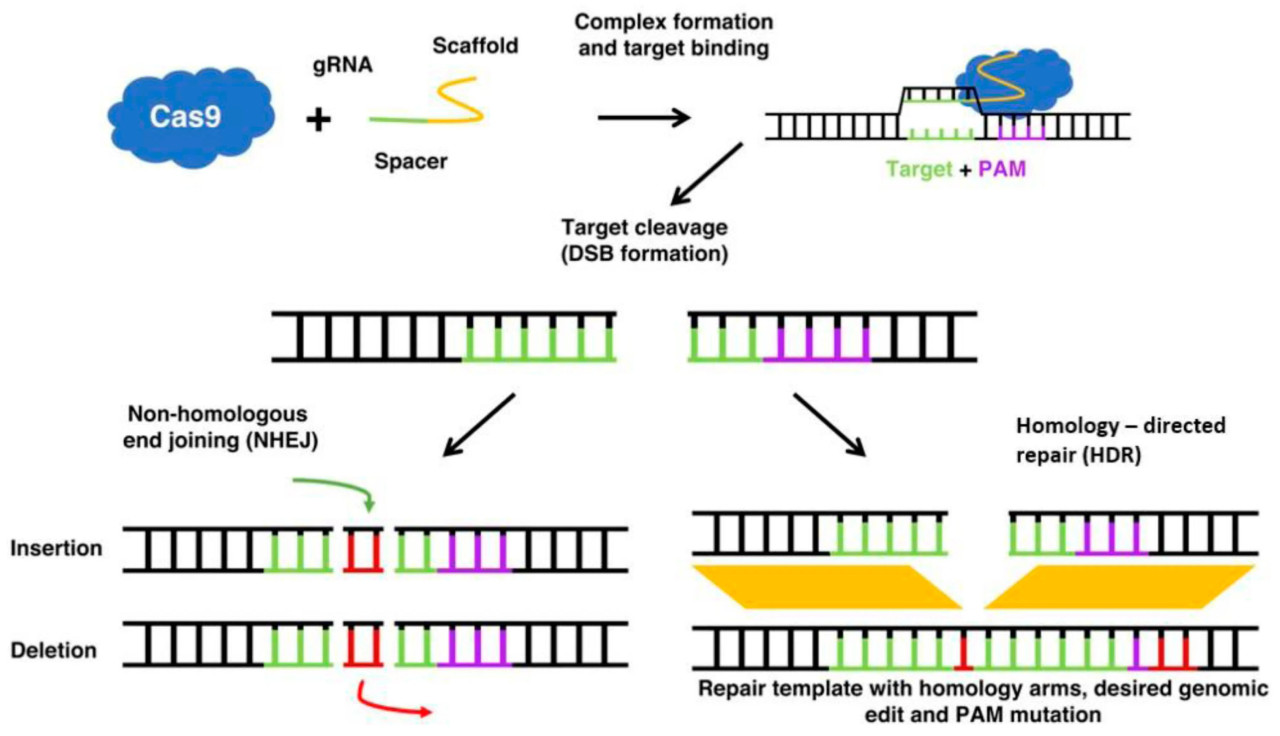
Методы редактирования генома на основе CRISPR, включая CRISPR/Cas9, CRISPR/Cpf1, редактирование оснований и прайм-редактирование, показали перспективность в улучшении генетики и элитных характеристик культур [51]. CRISPR-Cas-белки, включая fCas9, Cas12, Cas13a и Cas13b, предлагают новые возможности для улучшения исследований культур [52,53,54,55,56,57]. Системы CRISPR/Cas модифицируют эукариотическую ДНК путем создания направляющей РНК (гРНК), которая соответствует целевой последовательности. Эта гРНК имеет протоспейсерный мотив размером около 20 пар оснований, окруженный сайт-специфическими гомологичными последовательностями. В системе CRISPR-Cas9 Cas9 связывается с протоспейсерным мотивом в гРНК и образует комплекс с сайтом-мишенью. Cas9 взаимодействует с прилегающим мотивом протоспейсера (PAM). PAM катализирует двухцепочечный разрыв (DSB) в ДНК хозяина, на три пары оснований выше [58]. Механизмы репарации ДНК клетки-хозяина могут восстановить разрыв либо с помощью гомологично-направленной репарации (HDR), либо с помощью негомологичного соединения концов (NHEJ) [59]. Репарация NHEJ может приводить к небольшим делециям, а вставки могут вызывать полную потерю или снижение функции гена, тогда как HDR может приводить к модификациям последовательности ДНК, включая встраивание генов или их замену (Рисунок 6).
Рисунок 6. CRISPR/Cas9 для создания DSB и репарация либо путем негомологичного соединения концов, либо гомологично-направленной репарации. Cas9 — это белок, который действует как молекулярные ножницы, связываясь с направляющей РНК. Направляющая РНК имеет основания РНК, комплементарные основаниям целевой последовательности ДНК в геноме. Прилегающий мотив протоспейсера (PAM) — это короткая последовательность ДНК (обычно длиной 2–6 пар оснований), которая следует за областью ДНК, нацеленной для разрезания Cas9. PAM необходим для разрезания нуклеазой Cas. Cas9 разрезает обе цепи ДНК в определенном сайте генома. Этот разрез создает двухцепочечный разрыв (DSB), который клетка затем пытается восстановить. В зависимости от механизма репарации, используемого клеткой, могут быть внесены новые последовательности (через HDR, гомологично-направленную репарацию) или внесены мутации (через NHEJ, негомологичное соединение концов). NHEJ вносит полу-случайные мутации вставки-делеции (инделы), тогда как HDR (гомологично-направленная репарация) обеспечивает точную вставку, делецию или замену нуклеотидов с использованием донорных шаблонов.
Другие системы на основе CRISPR-Cas, такие как редактирование оснований и прайм-редактирование, могут модифицировать последовательности ДНК через структуру хроматина или редактирование оснований, устраняя необходимость в разрезании цепей ДНК [57]. Благодаря своей адаптивности технология CRISPR-Cas9 стала ценным инструментом в редактировании генома и может играть важную роль в изучении функций генов и улучшении нуга и других масличных культур (Рисунок 7). Существует необходимость в понимании или расшифровке генов, участвующих в растрескивании стручков, так как это вызывает серьезные потери у масличных культур [60]. Растрескивание стручков значительно снижает урожайность масличных культур, включая сою, кунжут и рапс, как до, так и после уборки урожая. Селекция масличных культур нацелена на минимизацию потерь от осыпаемости. Исследования мутантов выявили гены, ответственные за устойчивость к осыпаемости. Минимизация растрескивания стручков с помощью биотехнологии является главной целью. Идентификация генов, участвующих в растрескивании стручков, необходима для развития устойчивости или толерантности растений к растрескиванию стручков. Например, у Brassica napus комплексный подход привел к открытию BnTCP8.C09 как гена, ответственного за растрескивание стручков [61]. Удаление гена растрескивания стручков 1 (PDH1) привело к снижению растрескивания стручков у сои [62]. Самостерильность является еще одним ограничением, которое ограничивает производство и продуктивность масличных культур. Опыление и оплодотворение приводят к образованию семян, что является экономически ценной частью масличных культур. Наличие самостерильности препятствует созданию инбредных линий, и преодоление самостерильности является ключевой целью селекции масличных культур, таких как нуг. Исследователи успешно достигли самофертильности, модифицируя такие важные гены, как S-рецепторная киназа и M-локусная протеинкиназа у рапса [63].
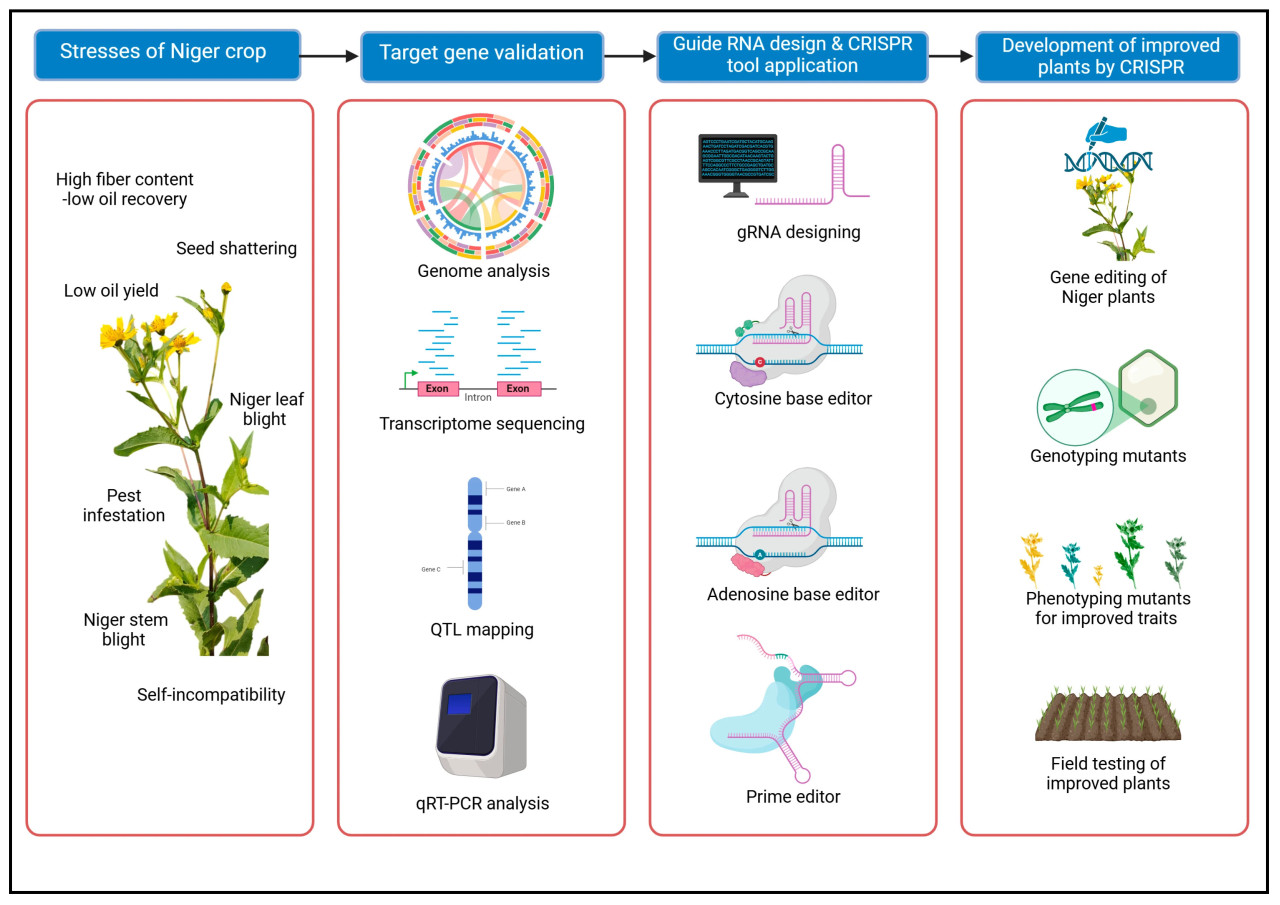
Рисунок 7. Применение инструментов на основе CRISPR/Cas для улучшения нуга. Основные биотические и абиотические факторы, препятствующие росту и урожайности нуга, включают нашествия вредителей, грибковые заболевания (например, пирикуляриоз), низкий выход масла, осыпаемость семян, высокое содержание клетчатки с низким содержанием масла и самостерильность. Вторая панель описывает комплексную стратегию, используемую для подтверждения роли гена-мишени у нуга. Подход объединяет полногеномные ассоциативные исследования (GWAS), транскриптомный анализ, картирование количественных локусов признаков (QTL) и количественную ПЦР в реальном времени (qRT-PCR) для идентификации и характеристики функции гена. Третья панель изображает применение передовых методов редактирования генома, в частности подходов на основе CRISPR-Cas, для модификации гена-мишени у нуга. Тремя основными используемыми стратегиями являются редактирование оснований на основе аденозина (ABE) и редактирование оснований на основе цитозина (CBE), которые точно преобразуют определенные пары оснований ДНК без внесения двухцепочечных разрывов. Прайм-редактирование позволяет осуществлять широкий спектр генетических модификаций, включая вставки, делеции и замены оснований. Последняя панель иллюстрирует рабочий процесс создания и характеристики растений нуга с отредактированным геномом. Процесс включает редактирование генома, генотипирование для выявления желаемых мутаций, фенотипирование для оценки влияния редактирования на признаки растений, полевые испытания для оценки эффективности в реальных условиях и, в конечном итоге, выпуск улучшенных сортов нуга (рисунок создан в https://BioRender.com).
Использование технологии редактирования генома привело к значительному развитию масличных культур с улучшенной урожайностью и продуктивностью, тем самым способствуя продовольственной безопасности и устойчивому сельскому хозяйству. Комбинация этих результатов убедительно свидетельствует о том, что методы редактирования генома создали перспективные возможности для улучшения масличных культур, и мы ожидаем, что это исследование принесет значительные выгоды в будущем [64]. Однако существуют также несколько проблем в применении технологии редактирования генома на основе CRISPR у масличных культур. Сложность генома и устойчивость к трансформации, а также полиплоидная природа привели к большой проблеме эффективного получения нокаутных линий на основе CRISPR у некоторых масличных культур, особенно кунжута, подсолнечника и арахиса. Таким образом, необходимо разработать новые системы доставки генетических элементов для этих устойчивых к трансформации масличных культур в будущем [64].
Технология таргетинга генов у растений в основном использует гомологично-направленную репарацию (HDR) для достижения точного редактирования генома. Это включает введение специфических вставок, замен последовательностей или замен нуклеотидов. Однако низкая эффективность HDR ограничила ее более широкое применение в генетике растений [65,66]. Чтобы преодолеть эти ограничения, альтернативные технологии редактирования генома, такие как редактирование оснований с помощью деаминаз и прайм-редактирование с помощью обратной транскриптазы, стали перспективными методами. В отличие от традиционных методов HDR, эти подходы на основе CRISPR–Cas не создают двухцепочечных разрывов (DSB) и не требуют включения донорной ДНК. Эта характеристика не только повышает их эффективность по сравнению с HDR, но и позволяет проводить точное редактирование без осложнений, связанных с образованием DSB. В результате эти инновационные технологии становятся все более ценными для улучшения генетической инженерии растений, предоставляя более надежные и эффективные средства достижения желаемых генетических модификаций [51]. В следующих разделах обсуждаются редактор оснований на основе цитозина (CBE), редактор оснований на основе аденина (ABE) и прайм-редактирование.
7.1. Редактирование оснований на основе цитозина (CBE)
Редактирование оснований на основе цитозина (CBE) — это передовая технология редактирования генома, которая использует модифицированную форму системы CRISPR-Cas9 для достижения точных редактирований в геномах растений. В частности, CBE использует никаз Cas9 (nCas9) с мутацией D10A, которая инактивирует один из нуклеазных доменов, RuvC, позволяя создавать одноцепочечные разрывы (или ники) вместо двухцепочечных разрывов (DSB). Эта модификация минимизирует потенциал нежелательных повреждений генома, которые могут возникнуть в результате активности традиционной нуклеазы Cas9 [67].
В CBE nCas9 слит с двумя ключевыми белками: цитидиндеаминазой, которая отвечает за преобразование цитидина (C) в уридин (U), и ингибитором урацил-ДНК-гликозилазы (UDG) (UGI), который предотвращает репарацию образовавшегося урацила. В результате, когда пара оснований C:G нацелена специфической однонаправляющей РНК (sgRNA), деаминаза эффективно превращает цитозин в урацил, и впоследствии, во время репликации ДНК или процессов репарации, урацил может быть заменен на тимин (T). Это обеспечивает преобразование пар оснований C:G в пары T:A, достигая точных переходов оснований без необходимости использования донорной ДНК и обходя ограничения, связанные с гомологичной рекомбинацией [51].
Эффективность и точность CBE делают его мощным инструментом в редактировании генома растений, расширяя возможности для создания генетически модифицированных растений с желаемыми признаками. CBE может быть использован для внесения полезных мутаций в гены нуга, связанные с содержанием масла, устойчивостью к болезням и толерантностью к абиотическим стрессам, улучшая его общую продуктивность и устойчивость (Рисунок 7). Эта технология может помочь преодолеть ограничения традиционной селекции, обеспечивая точные модификации в специфических генах без необходимости обширных возвратных скрещиваний.
7.2. Редактирование оснований на основе аденина (ABE)
Редакторы оснований на основе аденина (ABE) представляют собой значительный прогресс в точности редактирования генома, в частности для достижения замен A:T на G:C в геномах растений. Это новшество использует сконструированную версию аденозиндеаминазы, в частности полученную из специфичной к тРНК Escherichia coli аденозиндеаминазы (ecTadA), которая была оптимизирована для эффективного функционирования в CRISPR/Cas9 [68]. В структуре ABE аденозиндеаминаза слита с каталитически неактивным вариантом Cas9 (nCas9 с мутацией D10A), что позволяет проводить таргетное редактирование без создания двухцепочечных разрывов (DSB) в ДНК. Когда комплекс ABE связывается с определенной геномной мишенью, компонент аденозиндеаминазы способствует преобразованию аденозинов в инозины. Во время последующих процессов репарации и репликации ДНК инозины интерпретируются ДНК-полимеразами как гуанозины. Это приводит к желаемому переходу A:T на G:C, позволяя проводить точную замену нуклеотидов без необходимости использования донорной ДНК или дополнительных механизмов репарации [51]. Разработка ABE решила некоторые ограничения, связанные с гомологично-направленной репарацией (HDR), поскольку они могут достигать высоких уровней эффективности редактирования с меньшим потенциалом для нецелевых эффектов.
ABE представляет ценный инструмент для улучшения агрономических признаков нуга, обеспечивая точные замены A на G в генах, связанных с урожайностью, качеством и устойчивостью к стрессам. Эта технология может быть особенно полезна для устранения мутаций, вызывающих нежелательные признаки у нуга, что приводит к улучшению показателей культуры (Рисунок 7).
7.3. Прайм-редактирование
Прайм-редактирование — это передовая технология редактирования генома, которая объединяет технологию CRISPR с обратной транскрипцией для точных генетических модификаций. Она использует модифицированный белок Cas9, nCas9 (H840A), который создает одноцепочечный разрыв в ДНК без разрезания обеих цепей, обеспечивая точное редактирование. Направляющая РНК прайм-редактирования (pegRNA) направляет nCas9 к сайту-мишени и включает шаблон обратной транскриптазы, который содержит желаемые мутации, и сайт связывания праймера, который спаривается с одноцепочечной ДНК для инициации обратной транскрипции. Этот процесс синтезирует ДНК с использованием РНК-шаблона, включая генетические правки непосредственно в геном [51,69]. Таким образом, прайм-редактирование предоставляет универсальный и точный метод для внесения таргетных генетических изменений с меньшим количеством нецелевых эффектов. Прайм-редактирование предоставляет универсальную платформу для разнообразных генетических модификаций у нуга, включая вставки, делеции и точные замены нуклеотидов, обеспечивая создание новых и улучшенных сортов. Эта технология предлагает потенциал для решения сложных генетических признаков и внедрения более сложных генетических модификаций, чем это было возможно ранее у нуга (Рисунок 7).
Заглядывая вперед, будущее направление редактирования генома у масличных культур должно быть сосредоточено на улучшении систем доставки и методологий для преодоления проблем устойчивости к трансформации и сложности генома. Достижения в области методов доставки на основе наночастиц и вирусных векторов могли бы предложить более эффективные средства введения CRISPR-компонентов в клетки-мишени, тем самым повышая эффективность трансформации. Интеграция мультиомиксных подходов, таких как геномный, транскриптомный и протеомный анализы, поможет в понимании основных механизмов регуляции генов и паттернов экспрессии у этих культур. Решая эти проблемы и улучшая механизмы доставки, мы можем раскрыть полный потенциал технологии CRISPR, прокладывая путь для создания сортов масличных культур с улучшенными признаками, что в конечном итоге будет способствовать глобальной продовольственной безопасности и устойчивым методам ведения сельского хозяйства.
8. Будущие стратегии
Эфиопские и индийские популяции нуга являются генетически разнообразными, что предлагает потенциал для селекционных программ по улучшению производства и продуктивности. Ключевые цели селекции включают улучшение урожайности семян, содержания масла, преодоление самостерильности, устойчивость к болезням и осыпаемость. Чтобы решить проблему самостерильности, селекционеры в Эфиопии и Индии используют массовый отбор и сибсовое спаривание, одновременно проводя скрининг линий с минимальной инбредной депрессией. Дикие виды Guizotia могут предоставить гены устойчивости к болезням для интрогрессии в культивируемый нуг [4]. Использование гетерозиса вскоре станет возможным благодаря созданию мужскостерильных линий и инбредов. Это открыло новое измерение в селекции на гетерозис при улучшении нуга [9]. Основными ограничениями нуга являются самостерильность, осыпаемость, создание высокоурожайных сортов, сортов с высоким содержанием масла и устойчивость к болезням. Они могут быть преодолены с помощью подходов тканевой культуры, таких как соматический эмбриогенез, а также с использованием маркер-ориентированной селекции и технологий редактирования генома. Редактирование генома на основе CRISPR может ускорить доместикацию диких масличных культур и улучшить культивируемые для удовлетворения растущего спроса. Однако его применение в масличных культурах сталкивается с проблемами, включая трудности в создании нокаутных линий на основе CRISPR в таких культурах, как кунжут, подсолнечник и арахис, из-за сложных геномов и низкой частоты трансформации. Получение полностью мутантных линий у полиплоидных культур, таких как рапс, также является значительной проблемой [64]. Редактирование оснований и прайм-редактирование предлагают мощные инструменты для точной генетической модификации нуга [64]. CBE и ABE могут быть использованы для исправления специфических точечных мутаций, связанных с нежелательными признаками, такими как восприимчивость к болезням или сниженная урожайность. Точное редактирование гена BnALS1 в положении P197 у рапса было достигнуто с использованием системы CBE, которая эффективно ввела преобразование C в T в мишени sgRNA. Эффективность редактирования составила 1,8%, что привело к замене P197S в BnALS1, создав новый мутант, устойчивый к гербицидам, у рапса, что способствовало борьбе с сорняками [70]. Такие исследования могут быть проведены на нуге с мощными инструментами CRISPR/Cas для улучшения признаков и содержания масла в будущем.
Точность прайм-редактирования позволяет внедрять полезные аллели или модифицировать регуляторные последовательности для усиления экспрессии генов, улучшая ключевые агрономические признаки (Рисунок 7). Эти технологии могут ускорить создание устойчивых, высокоурожайных сортов нуга. Применения включают повышение урожайности, улучшение устойчивости к болезням и гербицидам, индукцию гаплоидов, создание мужскостерильных линий, закрепление гибридной силы, манипулирование самостерильностью и содействие de novo доместикации. Эта технология готова преобразовать возделывание масличных культур и методы селекции [64]. Технология CRISPR обладает огромным потенциалом для преобразования нуга. Путем точного редактирования геномов культур она может повысить устойчивость к засухе и болезням, увеличить содержание масла и улучшить толерантность к гербицидам, что приведет к созданию более устойчивых и продуктивных культур нуга.
9. Выводы
Нуг является масличной культурой в Индии, на которую приходится более 50% мировых площадей и производства нуга. Нуг считается забытой малоиспользуемой культурой, несмотря на его питательную ценность, медицинскую важность и экономическое значение для средств к существованию мелких и маргинальных фермеров в засушливых и полузасушливых районах страны. Нуг является важной второстепенной масличной культурой, которая может быть использована для улучшения качества масла и высокой урожайности семян у сортов нуга. Стратегия молекулярной селекции помогает преодолеть такие ограничения, как низкоурожайные сорта, самостерильность, проблемы полегания и осыпаемости, восприимчивость к вредителям и т. д. В течение длительного времени нуг оставался забытой и малоиспользуемой культурой, и из-за этого он получил мало внимания со стороны научного сообщества. Микроклональное размножение in vitro и метод тканевой культуры действительно являются краеугольной технологией в селекции растений, предлагая контролируемый и эффективный метод производства больших количеств генетически однородных растений. Однако в этом процессе сомаклональная вариабельность играет важную роль в улучшении культур. Интегрируя сомаклональную вариабельность в современные селекционные конвейеры и комбинируя ее с геномными инструментами, селекционеры могут выявлять и стабилизировать новое генетическое разнообразие для решения растущих проблем сельского хозяйства. Изучение гермплазмы с помощью коллекций не только предоставляет возможность расширить генетическую базу этих культур в коллекциях генбанков. Правительство инициировало несколько программ для повышения урожайности с помощью лучших сортов, с соответствующими выгодами для фермеров и для страны за счет увеличения предложения семян, доступных для экспорта. Отсутствие всесторонних исследований, омиксных подходов и исследований по генетической трансформации и QTL-картированию представляет собой основные пробелы в исследованиях. Чтобы преодолеть эти пробелы, Департамент биотехнологии правительства Индии [71] предпринял программный режим под названием «Второстепенные масличные культуры индийского происхождения» для использования их преимуществ для сообществ с помощью вмешательства передовых геномных технологий. Такие инициативы способствуют исследованиям малоиспользуемых второстепенных масличных культур, таких как нуг, в области омиксных и маркер-ориентированных подходов селекции, которые являются поздними участниками эры геномики. Экологически нейтральный подход, такой как методы молекулярных маркеров, представляется лучшим вариантом для включения в программы улучшения нуга. Предпринимаются усилия по использованию молекулярных маркеров у нуга для изучения его генетического разнообразия и реакций на абиотические стрессы. Спрос на промышленное применение и потребление масла увеличивается с каждым днем. Поэтому урожайность нуга, его качество, содержание масла и признаки, связанные с биотическими и абиотическими стрессами, должны быть улучшены. Однако культура сталкивается с различными проблемами производства и селекции. Расширение биотехнологических инструментов и наличие высокого генетического разнообразия создают возможность улучшить культуру с помощью доступных ресурсов. Биотехнологические инструменты могут быть очень полезны для селекции нуга и его улучшения путем добавления желаемых признаков с использованием геномики и методов in vitro. Ожидается, что геномика вскоре принесет быстрый прогресс в исследованиях нуга.
Ссылки
1. Tsehay, S.; Ortiz, R.; Johansson, E.; Bekele, E.; Tesfaye, K.; Hammenhag, C.; Geleta, M. New transcriptome-based SNP markers for noug (Guizotia abyssinica) and their conversion to KASP markers for population genetics analyses. Genes 2020, 11, 1373. [Google Scholar] [CrossRef] [PubMed]
2. Getinet, A.; Teklewold, A. An agronomic and seed-quality evaluation of niger (Guizotia abyssinica Cass.) germplasm grown in Ethiopia. Plant Breed. 1995, 114, 375–376. [Google Scholar]
3. Nasirullah, K.; Mallika, T.; Rajalakshmi, S.; Pashupathi, K.S.; Ankaiah, K.N.; Vibhakar, S.; Krishnamurthy, M.N.; Nagaraja, K.V.; Kapur, O.P. Studies on niger seed oil (Guizotia abyssinica) Seed Oil. J. Food Sci. Technol. 1982, 19, 147–149. [Google Scholar]
4. Getinet, A.; Sharma, S.M. Niger. Guizotia abyssinica (L. f.) Cass. Promoting the Conservation and Use of Underutilized and Neglected Crops; Institute of Plant Genetics and Crop Plant Research: Gatersleben, Germany, 1996; pp. 1–59. [Google Scholar]
5. Tiwari, S.; Kumar, S.; Gontia, I. Minireview: Biotechnological approaches for sesame (Sesamum indicum L.) and Niger (Guizotia abyssinica L.f. Cass). AsPac J. Mol. Biol. Biotechnol. 2011, 19, 2–9. [Google Scholar]
6. Barrangou, R.; Fremaux, C.; Deveau, H.; Richards, M.; Boyaval, P.; Moineau, S.; Romero, D.A.; Horvath, P. CRISPR provides acquired resistance against viruses in prokaryotes. Science 2007, 315, 1709–1712. [Google Scholar] [CrossRef] [PubMed]
7. Ranganatha, A.R.G.; Jyotishi, A.; Deshmukh, M.R.; Bisen, R.; Pandey, A.K.; Gupta, K.N.; Jain, S.; Paroha, S. Improved Technology for Maximizing Production of Niger; All India Coordinated Research Project on Sesame and Niger, Indian Council of Agricultural Research: Jabalpur, India, 2013. [Google Scholar]
8. Aboye, B.M. Cluster, diveregence and principal component analysis of niger seed (Guizotia abyssinica (L. f.) Cass) genotypes. Int. J. Res. Stud. Agri. Sci. 2021, 2, 17–22. [Google Scholar]
9. Terefe, M.; Girma, D. Development of molecular resources for the genetic improvement of noug (Guizotia abyssinica (L. f) Cass): A mini review. CABI Agric. Biosci. 2022, 3, 52. [Google Scholar] [CrossRef]
10. Kurenkova, E.M.; Zapilov, S.A.; Tolkacheva, A.N. Introduction of Guizotia abyssinica (L. f.) Cass. in agroecological conditions of the central region of the Russian federation. Bio Web Conf. 2024, 82, 02017. [Google Scholar] [CrossRef]
11. Merga, M. Niger improvement and production in Ethiopia: Progress and major challenges. J. Innov. Agric. 2022, 9, 1–9. [Google Scholar] [CrossRef]
12. Belayneh, H. Oilcrop germplasm: A vital resource for the plant breeder. In Plant Genetic Resources of Ethiopia; Engels, J.M.M., Hawkes, J.G., Worede, M., Eds.; Cambridge University Press: Cambridge, UK, 1991; pp. 344–354. [Google Scholar]
13. Patil, H.S.; Duhoon, S.S. Self incompatibility, male sterility and pollination mechanism In: Niger {Guizotia abyssinica (L.f.) Cass.}—A review. Agric. Rev. 2006, 27, 113–121. [Google Scholar]
14. Schmutterer, H. Contribution to the knowledge of the crop pest fauna in Ethiopia. Angew. Entomol. 1971, 67, 371–389. [Google Scholar] [CrossRef]
15. Jakhmola, S.S. Niger grain fly, Diozina sororcula (Wiedemann), a serious pest of niger in central India. J. Bombay Nat. Hist. Soc. 1981, 80, 439–440. [Google Scholar]
16. Bayeh, M.; Medhin, T.G. Insect pests of niger, linseed and Brassica. In Oilseed Research and Development in Ethiopia; Proceedings of the First National Oilseed Workshop: Addis Ababa, Ethiopia, 1991; pp. 174–177. [Google Scholar]
17. Radhamani, J.; Pushpa, H.D.; Gomshe, S.S.; Choudhary, S.B.; Kumar, V.; Bisen, R.; Sujatha, M. Early maturing niger germplasm accessions. Indian J. Plant Genet. Resour. 2021, 34, 495–498. [Google Scholar] [CrossRef]
18. Thakur, N.R.; Ingle, K.P.; Sargar, P.R.; Baraskar, S.S.; Kasanaboina, K.; Awio, B.; Pranati, J.; Abdi, G. Sustainable utilization of wild germplasm Resources. In Sustainable Utilization and Conservation of Plant Genetic Diversity; Al-Khayri, J.M., Jain, S.M., Penna, S., Eds.; Springer: Singapore, 2024; Volume 35, pp. 1–22. [Google Scholar]
19. Ranganatha, A.R.G.; Panday, A.K.; Bisen, R.; Jain, S.; Sharma, S. Niger. In Breeding Oilseed Crops for Sustainable Production; Academic Press: Cambridge, MA, USA, 2016; pp. 169–199. [Google Scholar]
20. Trivedi, H.B.P.; Sinha, P.K. Gynomonoecism in niger. J. Oilseeds Res. 1986, 3, 93–94. [Google Scholar]
21. Phanindra, K.S.; Toprope, V.N.; Thakur, N.R. Mutation studies in confectionary sunflower (Helianthus annuus L.). J. Res. ANGRAU 2018, 46, 15–20. [Google Scholar]
22. Shinde, A.V.; Thakur, N.R.; Deshmukh, A.S. Allele mining: An approach for crop improvement. In Advances in Agricultural and Horticultural Sciences; Shinde, Y.A., Ed.; Department of Agricultural Entomology, Shri Vaishnav Institute of Agriculture: Indore, India, 2022; pp. 235–245. [Google Scholar]
23. Shabnam, A.D.J.; Sarkar, C.; Phulara, R.; Pawar, S.E. Evaluation of gamma rays-induced changes in oil yield and oleic acid content of niger. Curr. Sci. 2011, 101, 490–491. [Google Scholar]
24. Oladosu, Y.; Rafii, M.Y.; Abdullah, N.; Hussin, G.; Rahim, H.A.; Miah, G.; Usman, M. Principle and application of plant mutagenesis in crop improvement: A Review. Biotechnol. Biotechnol. Equip. 2016, 30, 1–16. [Google Scholar] [CrossRef]
25. Misal, V.D.; Davane, S.S.; Mane, S.B. Improvement of yield in Guizotia abyssinica (L. f.) Cass. by using backcross method. World J. Adv. Res. Rev. 2021, 12, 261–266. [Google Scholar]
26. Amsalu, F. Genetic variability correlation and path coefficient analysis of Niger seed (Guizotia abyssinica [L. f.] Cass.) genotypes. Int. J. Res. Stud. Agric. Sci. 2020, 6, 8–16. [Google Scholar]
27. Naik, P.M.; Murthy, H.N. Somatic embryogenesis and plant regeneration from cell suspension culture of niger (Guizotia abyssinica Cass.). Acta Physiol. Plant 2010, 32, 75–79. [Google Scholar] [CrossRef]
28. Long, Y.; Yang, Y.; Pan, G.; Shen, Y. New insights into tissue culture plant-regeneration mechanisms. Front. Plant Sci. 2022, 13, 926752. [Google Scholar] [CrossRef]
29. Mineo, L. Plant tissue culture techniques. Test. Stud. Lab. Teach. 1990, 11, 151–174. [Google Scholar]
30. Sujatha, M. In vitro adventitious shoot regeneration for effective maintenance of male sterile niger Guizotia abyssinica (L. f) Cass. Euphytica 1997, 9, 89–95. [Google Scholar] [CrossRef]
31. Baghel, S.; Bansal, Y.K. Micropropagation and flowering of a biodiesel plant niger (Guizotia abyssinica Cass.). Asian J. Exp. Biol. Sci. 2013, 4, 532–539. [Google Scholar]
32. Jadimath, V.; Murthy, H.; Pyati, A.; Kumar, H.A.; Ravishankar, B. Plant regeneration from leaf cultures of Guizotia abyssinica (niger) and Guizotia scabra. Phytomorphology 1998, 48, 131–135. [Google Scholar]
33. Sarvesh, A.; Reddy, T.; Kishor, P.K. Embryogenesis and organogenesis in cultured anthers of an oil-yielding crop niger (Guizotia abyssinica. Cass). Plant Cell Tissue Organ Cult. 1993, 35, 75–80. [Google Scholar] [CrossRef]
34. Adda, S.; Reddy, T.; Kishor, P.K. Androclonal variation in niger (Guizotia abyssinica Cass). Euphytica 1994, 79, 59–64. [Google Scholar] [CrossRef]
35. Murthy, H.N.; Kumar, H.G.A.; Paek, K.Y. Anther culture of niger. Korean J. Plant Tissue Cult. 2000, 27, 353–358. [Google Scholar]
36. Nikam, T.; Shitole, M. Regeneration of niger (Guizotia abyssinica Cass.) CV sahyadri from seedling explants. Plant Cell Tissue Organ Cult. 1993, 32, 345–349. [Google Scholar] [CrossRef]
37. Ganapathi, T.; Nataraja, K. Effect of auxins and cytokinins on plant regeneration from hypocotyls and cotyledons in niger (Guizotia abyssinica Cass.). Biol. Plant. 1993, 35, 209–215. [Google Scholar] [CrossRef]
38. Bhandari, H.R.; Sujatha, M.; Dangi, K.S.; Sivasankar, A. Efficient plantlet regeneration from seedling explants of niger (Guizotia abyssinica Cass). Int. J. Agric. Environ. Biotechnol. 2009, 2, 438–444. [Google Scholar]
39. Murthy, H.N.; Jeong, J.H.; Choi, Y.E.; Paek, K.Y. Agrobacterium-mediated transformation of niger [Guizotia abyssinica (L. f.) Cass.] Using Seedling Explants. Plant Cell Rep. 2003, 21, 1183–1187. [Google Scholar] [CrossRef] [PubMed]
40. Baghel, S.; Bansal, Y.K. In vitro regeneration of Guizotia abyssinica Cass. and evaluation of genetic fidelity through RAPD markers. S. Afr. J. Bot. 2017, 109, 294–307. [Google Scholar] [CrossRef]
41. Isabel, N.; Tremblay, L.; Michaud, M. RAPDs as an aid to evaluate the genetic integrity of somatic embryogenesis-derived populations of Picea mariana (Mill.) B.S.P. Theoret. Appl. Genet. 1993, 86, 81–87. [Google Scholar] [CrossRef] [PubMed]
42. Ingle, K.; Thakur, N.; Moharil, M.P.; Suprasanna, P.; Awio, B.; Narkhede, B.; Kumar, P.; Ceasar, S.A.; Abdi, G. Current status and future prospects of molecular marker assisted selection (MAS) in millets. In Nutriomics of Millet Crops, 1st ed.; Pudake, R.N., Solanke, A.U., Kole, C., Eds.; CRC Press: Boca Raton, FL, USA, 2023. [Google Scholar]
43. Jadhav, Y.; Thakur, N.R.; Ingle, K.P.; Ceasar, S.A. The role of phenomics and genomics in delineating the genetic basis of complex traits in millets. Physiol. Plant. 2024, 176, e14349. [Google Scholar] [CrossRef]
44. Thakur, N.R.; Gorthy, S.; Vemula, A.; Odeny, D.A.; Ruperao, P.; Sargar, P.R.; Mehtre, S.P.; Kalpande, H.V.; Habyarimana, E. Genome-wide association study and expression of candidate genes for Fe and Zn concentration in sorghum grains. Sci. Rep. 2024, 14, 1. [Google Scholar] [CrossRef]
45. Melchinger, A.; Messmer, M.; Lee, M.; Woodman, W.; Lamkey, K. Diversity and relationships among US maize inbreds revealed by Restriction Fragment Length Polymorphisms. Crop Sci. 1991, 31, 669–678. [Google Scholar] [CrossRef]
46. Melchinger, A. Use of RFLP markers for analysis of genetic relationships among breeding materials and prediction of hybrid performance. Int. Crop Sci. 1993, 1, 621–628. [Google Scholar]
47. Geleta, M.; Bryngelsson, T.; Bekele, E.; Dagne, K. Genetic diversity of Guizotia abyssinica (L. f.) Cass. (Asteraceae) from Ethiopia as revealed by random amplified polymorphic DNA (RAPD). Genet. Resour. Crop Evol. 2007, 54, 601–614. [Google Scholar] [CrossRef]
48. Nagella, P.; Murthy, H.N.; Ravishankar, K.V.; Hahn, E.; Paek, K. Analysis of genetic diversity among Indian niger [Guizotia abyssinica (L. f.) Cass.] cultivars based on Randomly Amplified Polymorphic DNA Markers. Electron. J. Biotechnol. 2008, 11, 1–5. [Google Scholar] [CrossRef]
49. Dempewolf, H.; Kane, N.C.; Ostevik, K.L.; Geleta, M.; Barker, M.S.; Lai, Z.; Stewart, M.L.; Bekele, E.; Engels, J.M.; Cronk, Q.B.; et al. Establishing genomic tools and resources for Guizotia abyssinica (L. f.) Cass.—The development of a library of expressed sequence tags, microsatellite loci, and the sequencing of its chloroplast genome. Mol. Ecol. Resour. 2010, 10, 1048–1058. [Google Scholar] [CrossRef] [PubMed]
50. Janila, P.; Variath, M.T.; Pandey, M.K.; Desmae, H.; Motagi, B.N. Genomic tools in groundnut breeding program: Status and perspectives. Front. Plant Sci. 2016, 7, 289. [Google Scholar] [CrossRef]
51. Zhu, H.; Li, C.; Gao, C. Applications of CRISPR-Cas in agriculture and plant biotechnology. Nat. Rev. Mol. Cell Biol. 2020, 21, 661–677. [Google Scholar]
52. Ingle, K.P.; Thakur, N.R.; Papade, J.N.; Kasanaboina, K.; Deshmukh, S.S.; Abdi, G.; Bhalerao, J.B. Genome Editing: Revolutionizing horticultural crops improvement. In Innovative Methods in Horticultural Crop Improvement; Advances in Plant Breeding Strategies; Al-Khayri, J.M., Alnaddaf, L.M., Jain, S.M., Penna, S., Eds.; Springer: Cham, Switzerland, 2024; Volume 1. [Google Scholar]
53. Zafar, K.; Sedeek, K.E.M.; Rao, G.S.; Khan, M.Z.; Amin, I.; Kamel, R.; Mahfouz, M.M. Genome editing technologies for rice improvement: Progress, prospects, and safety concerns. Front. Genome Edit. 2020, 2, 5. [Google Scholar] [CrossRef] [PubMed]
54. Aman, R.; Ali, Z.; Butt, H.; Mahas, A.; Aljedaani, F.; Khan, M.Z.; Mahfouz, M. RNA virus interference via CRISPR-Cas13a system in plants. Genome Biol. 2018, 19, 1. [Google Scholar] [CrossRef]
55. Abudayyeh, O.O.; Gootenberg, J.S.; Essletzbichler, P.; Han, S.; Joung, J.; Belanto, J.J.; Zhang, F. RNA targeting with CRISPR–Cas13. Nature 2017, 550, 280–284. [Google Scholar] [CrossRef] [PubMed]
56. Sirba, H.; Chimdessa, T. Review of impact of climate change on food security in Africa. Int. J. Res. Innov. Earth Sci. 2021, 8, 40–66. [Google Scholar]
57. Hillary, V.E.; Ceasar, S.A. A review on the mechanism and applications of CRISPR/Cas9/Cas12/Cas13/Cas14 proteins utilized for genome engineering. Mol. Biotechnol. 2023, 65, 311–325. [Google Scholar] [CrossRef] [PubMed]
58. Tripathi, L.; Dhugga, K.S.; Ntui, V.O.; Runo, S.; Syombua, E.D.; Muiruri, S.; Tripathi, J.N. Genome editing for sustainable agriculture in Africa. Front. Genome Edit. 2022, 4, 876697. [Google Scholar] [CrossRef] [PubMed]
59. Sun, X.; Hu, Z.; Chen, R.; Jiang, Q.; Song, G.; Zhang, H.; Xi, Y. Targeted mutagenesis in soybean using the CRISPR-Cas9 system. Sci. Rep. 2015, 5, 10342. [Google Scholar] [CrossRef] [PubMed]
60. Vaikuntapu, P.R.; Kumar, V.D. Applications and challenges of harnessing genome editing in oilseed crops. J. Plant Biochem. Biotechnol. 2022, 32, 751–772. [Google Scholar] [CrossRef]
61. Chu, W.; Liu, J.; Cheng, H.; Li, C.; Fu, L.; Wang, W.; Wang, H.; Hao, M.; Mei, D.; Liu, K.; et al. A lignified-layer bridge controlled by a single recessive gene is associated with high pod-shatter resistance in Brassica napus L. Crop J. 2021, 10, 638–646. [Google Scholar] [CrossRef]
62. Zhang, Z.; Wang, J.; Kuang, H. Elimination of an unfavorable allele conferring pod shattering in an elite soybean cultivar by CRISPR/Cas9. aBIOTECH 2022, 3, 110–114. [Google Scholar] [CrossRef]
63. Chen, F.; Yang, Y.; Li, B.; Liu, Z.; Khan, F.; Zhang, T.; Zhou, G.; Tu, J.; Shen, J.; Yi, B.; et al. Functional analysis of M-Locus protein kinase revealed a novel regulatory mechanism of self-incompatibility in Brassica napus L. Int. J. Mol. Sci. 2019, 20, 3303. [Google Scholar] [CrossRef] [PubMed]
64. He, J.; Zhang, K.; Tang, M.; Zhou, W.; Chen, L.; Chen, Z.; Li, M. CRISPR-based genome editing technology and its applications in oil crops. Oil Crop Sci. 2021, 6, 105–113. [Google Scholar] [CrossRef]
65. Atkins, P.A.; Voytas, D.F. Overcoming bottlenecks in plant gene editing. Curr. Opin. Plant Biol. 2020, 54, 79–84. [Google Scholar] [CrossRef]
66. Huang, T.K.; Puchta, H. CRISPR/Cas-mediated gene targeting in plants: Finally a turn for the better for homologous recombination. Plant Cell Rep. 2019, 38, 443–449. [Google Scholar] [CrossRef]
67. Komor, A.C.; Kim, Y.B.; Packer, M.S.; Zuris, J.A.; Liu, D.R. Programmable editing of a target base in genomic DNA without double-stranded DNA cleavage. Nature 2016, 533, 420–424. [Google Scholar] [CrossRef] [PubMed]
68. Gaudelli, N.M.; Komor, C.A.; Rees, H.A.; Packer, M.S.; Badran, A.H.; Bryson, D.I.; Liu, D.R. Programmable base editing of A•T to G•C in genomic DNA without DNA cleavage. Nature 2017, 551, 464–471. [Google Scholar] [CrossRef] [PubMed]
69. Anzalone, A.V.; Randolph, P.B.; Davis, J.R.; Sousa, A.A.; Koblan, L.W.; Levy, J.M.; Chen, P.J.; Wilson, C.; Newby, G.A.; Raguram, A.; et al. Search-and-replace genome editing without double-strand breaks or donor DNA. Nature 2019, 576, 149–157. [Google Scholar] [CrossRef] [PubMed]
70. Wu, J.; Chen, C.; Xian, G.; Liu, D.; Lin, L.; Yin, S.; Sun, Q.; Fang, Y.; Zhang, H.; Wang, Y. Engineering herbicide-resistant oilseed rape by CRISPR/Cas9-mediated cytosine base editing. Plant Biotechnol. J. 2020, 18, 1857–1859. [Google Scholar] [CrossRef]
71. Duraimurugan, P.; Reddy, A.V. ICAR-Indian Institute of Oilseeds Research, Rajendranagar, Hyderabad, India. Newsletter 2020, 26, 12–13. [Google Scholar]
Papade JN, Ingle KP, Thakur NR, Gomashe SS, Padmavathy M, Ceasar SA. Tapping into the Potential of Underutilized Niger (Guizotia abyssinica (L. f.) Cass.) Through Breeding and Biotechnological Tools. Agriculture. 2025; 15(3):350. https://doi.org/10.3390/agriculture15030350
Перевод статьи «Tapping into the Potential of Underutilized Niger (Guizotia abyssinica(L. f.) Cass.) Through Breeding and Biotechnological Tools» авторов Papade JN, Ingle KP, Thakur NR, Gomashe SS, Padmavathy M, Ceasar SA., оригинал доступен по ссылке. Лицензия: CC BY. Изменения: переведено на русский язык











































































































Комментарии (0)