Окислительный удар по семенам: как экстракт гриба Diaporthe подавляет прорастание ежовника
В данном исследовании изучается ингибирующее действие экстракта изолята Diaporthe sp. EC010 на прорастание и рост семян ежовника обыкновенного (Echinochloa crus-galli). Применение методов последовательной экстракции к мицелию Diaporthe sp. позволило частично разделить фитотоксические соединения.
Аннотация
Фракция этилацетата (EtOAc) наиболее сильно снижала прорастание семян (на 81,01%), длину корней (на 89,18%) и длину побегов (на 84,74%) по сравнению с контрольными значениями. Химическая характеристика с использованием газовой хроматографии-масс-спектрометрии выявила основные компоненты: линолевую кислоту, бутиловый эфир (9,69%), гексадекановую кислоту (7,99%) и 14-пентадеценовую кислоту (7,86%). Что касается физиологических и биохимических показателей, обработанные семена демонстрировали более низкое набухание, значительно сниженную активность α-амилазы (EC 3.2.1.1) (p<0,05) и повышенное накопление малонового диальдегида (на 85,52%) и пероксида водорода (на 141,10%). Кроме того, активность антиоксидантных ферментов супероксиддисмутазы (EC 1.15.1.1) и гваяколпероксидазы (EC 1.11.1.7) была повышена (на 67,24% и 61,62% соответственно), в то время как активность каталазы (EC 1.11.1.6) была снижена (на –33,75%). Предполагается, что дисбаланс уровней активных форм кислорода (АФК) в сочетании со сниженным антиоксидантным потенциалом приводит к постепенному накоплению окислительных повреждений в клетках семян и последующей потере жизнеспособности семян. В целом, эти результаты подтверждают, что экстракт Diaporthe индуцирует окислительный стресс и ингибирует антиоксидантные ферменты. Данное исследование наглядно демонстрирует окислительное повреждение, связанное с аллелохимическими веществами Diaporthe.
1 Введение
Гербициды представляются экономически эффективным способом борьбы с сорняками и способствуют продуктивности сельскохозяйственных культур. Однако чрезмерное использование синтетических гербицидов привело к распространению устойчивых к гербицидам биотипов (Saini and Singh, 2019). Эта устойчивость снижает эффективность существующих гербицидов, что требует изучения альтернативных стратегий борьбы с сорняками. Подходы интегрированной борьбы с сорняками (ИБС), которые объединяют различные методы борьбы с сорняками, предоставляют стратегический способ снижения зависимости от синтетических гербицидов (Nazarkov and Gerasimova, 2023). В этом контексте натуральные гербициды, полученные из аллелохимических веществ, представляют интерес как потенциальные дополнительные инструменты в ИБС (Saini and Singh, 2019; Gao and Su, 2024). Эти натуральные продукты могут быть интегрированы с другими методами борьбы с сорняками для достижения широкого спектра борьбы с сорняками (Bailey, 2014) и, благодаря своим множественным механизмам действия, могут помочь предотвратить устойчивость к гербицидам (Hazrati et al., 2017). По сравнению с синтетическими вариантами, натуральные гербициды обычно имеют более низкую токсичность и меньшую продолжительность воздействия на окружающую среду (Gao and Su, 2024). Расширяя исследования в этой области, текущее исследование направлено на изучение и открытие новых источников, содержащих токсичные соединения, которые могли бы улучшить борьбу с сорняками, в конечном итоге способствуя разработке эффективных натуральных гербицидов. Diaporthe — это крупный род грибов, относящийся к порядку Diaporthales и отделу Ascomycota, для которого постоянно сообщается о новых видах (Huang et al., 2021; Sun et al., 2021). Примечательно, что грибы Diaporthe являются важными источниками активных природных продуктов, причем из этого рода были идентифицированы многочисленные сообщения о терпенах (Luo et al., 2021; Zhang et al., 2021), алкалоидах, антрахинонах (Tian et al., 2018; Xu et al., 2021) и других метаболитах с уникальными структурами. За последние 20 лет было показано, что более 200 таких соединений обладают значительной противоопухолевой, антибактериальной, гербицидной и другой биологической активностью. Следовательно, снижение использования химических продуктов может быть достигнуто путем использования натуральных гербицидов, содержащих натуральные грибные соединения или грибные активные компоненты. Экологически чистые гербициды были разработаны с использованием этих химических веществ в качестве потенциальных кандидатов.
Физиология сорняков во время воздействия аллелохимических веществ в последнее время стала областью исследовательского интереса, причем проведенные на сегодняшний день исследования подчеркивают воздействие на важные метаболические процессы, такие как процессы, связанные с делением клеток, поглощением питательных веществ, антиоксидантами, стресс-опосредованными гормонами и другими метаболитами, которые контролируют прорастание и рост семян (Radhakrishnan et al., 2018). Сообщалось, что применение гербицидов индуцирует генерацию активных форм кислорода (АФК) в растениях, включая супероксидные радикалы (O2•−), гидроксильные радикалы (OH•) и пероксид водорода (H2O2) (Wu et al., 2021; Dmitrieva et al., 2024). Это накопление АФК может индуцировать окислительный стресс, который имеет неблагоприятные последствия для белков, ДНК и липидов (Choudhary et al., 2020). Особенно действие АФК на мембранные липиды приводит к перекисному окислению липидов, что, в свою очередь, вызывает повреждение клеточных мембран (Laosinwattana et al., 2018). Соответственно, растения имеют механизм защиты от окислительного стресса посредством антиоксидантной ферментной системы. Антиоксидантные ферменты удаляют или элиминируют различные свободные радикалы, включая те, которые генерируются во время биологических процессов. Основными антиоксидантными ферментами являются супероксиддисмутаза (СОД), каталаза (КАТ) и гваяколпероксидазы (ПО) (Mishra et al., 2023). СОД поддерживает клеточные уровни O2•− в физиологических концентрациях, превращая O2•− в H2O2. Поскольку H2O2 может затем окислять клеточные мембраны и клеточные компоненты до OH•, его удаление является ключевой задачей. КАТ является ферментом, разлагающим H2O2, который метаболизирует H2O2 до O2 и H2O (Fujita and Hasanuzzaman, 2022). ПО затем обеспечивает дополнительные механизмы для поддержания окислительно-восстановительного баланса и удаления токсичных метаболитов (Zhu et al., 2023).
В предыдущем исследовании мы собрали 21 гриб с пораженных сорняками тканей и протестировали их на гербицидную активность. Среди них изолят Diaporthe sp. EC010 (номер доступа GenBank OR143425) показал гербицидные эффекты своих вторичных метаболитов на целевые растения, включая довсходовые гербицидные эффекты в виде ингибирования прорастания семян Amaranthus tricolor (двудольный сорняк). Мы предположили, что экстракт Diaporthe индуцирует осмотический стресс и тем самым ограничивает как активность амилазы, которая необходима для энергообеспечения роста корней и побегов, так и митотическую активность (Manichart et al., 2023a). В этом исследовании мы изучили окислительное повреждение, вызванное экстрактом Diaporthe sp., на однодольном сорняке ежовнике обыкновенном (Echinochloa crus-galli), и изучили, как обработанные растения реагируют через систему антиоксидантных ферментов. Кроме того, мы идентифицировали химические компоненты экстракта.
2 Материалы и методы
2.1 Культивирование гриба и выделение грибных аллелохимических веществ
Грибы, использованные в этом исследовании (Diaporthe sp. EC010), были первоначально собраны Manichart, Laosinwattana (Manichart et al., 2023a) в сентябре 2021 года в районе Ладкрабанг Бангкока, Таиланд. Выделенные грибы культивировали с помощью глубинной ферментации в картофельно-декстрозном бульоне. После периода культивирования биомассу собрали и инкубировали в сушильном шкафу с горячим воздухом (45°C). Полученный мицелий подвергли последовательной экстракции органическими растворителями с возрастающей полярностью в соответствии с Poonpaiboonpipat, Krumsri (Poonpaiboonpipat et al., 2021). Кратко, высушенный мицелий замачивали в гексане на 24 часа, затем полученную смесь фильтровали через фильтровальную бумагу, а оставшийся остаток реэкстрагировали. Далее растворы объединяли и выпаривали для получения фракции сырого гексанового экстракта. Оставшийся остаток затем экстрагировали этилацетатом (EtOAc) и этанолом (EtOH) в том же процессе, получая фракции экстрактов EtOAc и EtOH. Фитотоксичность всех фракций экстрактов оценивали с помощью анализа прорастания семян.
2.2 Анализ прорастания семян
Во-первых, каждый сырой экстракт липкого гриба растворяли в соответствующем растворителе (гексан, EtOAc или EtOH) в концентрациях 0,625, 1,25 и 2,50 мг/мл. Концентрации были выбраны на основе предварительных экспериментов, которые показали, что эти концентрации влияют на прорастание семян. Поддерживали четыре повторности на обработку для каждого из органических растворителей в полностью рандомизированном дизайне (ПРД); обработки дистиллированной водой использовали в качестве отрицательных контролей. Для тестов на прорастание, согласно Teerarak, Laosinwattana (Teerarak et al., 2010), 5 мл каждого раствора экстракта добавляли в чашку Петри (диаметром 9 см), содержащую двойной слой бумаги для проращивания, и оставляли испаряться до полного высыхания при комнатной температуре. Затем бумагу для проращивания в чашке Петри увлажняли 5 мл дистиллированной воды. Двадцать здоровых семян ежовника помещали в каждую чашку. Чашки помещали в климатическую камеру (LAC-1075-N, Longyue, Шанхай) с температурой 27 ± 2°C, фотопериодом 12/12 ч свет/темнота и относительной влажностью около 80%. Скорость прорастания семян сорняка и длину корней и побегов проростков (см) оценивали через семь дней обработки. Оптимальную сырую фракцию с наиболее высокой ингибирующей эффективностью в отношении прорастания и роста проростков отобрали для дальнейших экспериментов.
2.3 Химическая характеристика с помощью ГХ-МС
Компоненты сырого экстракта Diaporthe в EtOAc были идентифицированы с помощью ГХ-МС. Экстракт разбавляли в этилацетате перед анализом на газовом хроматографе Agilent 6890 N, оснащенном масс-детектором Agilent 5973 и капиллярной колонкой HP-5 с кремнеземом (30 м x 0,25 мм ID, толщина пленки 0,25 м). Температурная программа колонки начиналась с 40°C в течение 3 минут, затем повышалась до 100°C со скоростью 10°C/мин, а затем дальнейше до 260°C со скоростью 5°C/мин, которая удерживалась в течение 5 минут. Скорость потока составляла 1 мл/мин, в качестве газа-носителя использовали гелий. МС-анализ проводили с диапазоном обнаружения 30-500 а.е.м. Образец (0,2 мкл) вводили с соотношением разделения потока 50:1. Температуры инжектора и детектора поддерживали на уровне 250°C и 270°C соответственно. Индивидуальные соединения идентифицировали путем сравнения МС-профилей с эталонной библиотекой (Национальный институт стандартов и технологий, NIST, 2014). Относительное содержание различных компонентов общего сырого экстракта выражали в процентах площади пика относительно общей площади пика. Пики площадью менее 0,1% исключали, тогда как все пики площадью более 0,1% включали.
2.4 Набухание семян и активность α-амилазы
Сырой экстракт EtOAc был оценен на его влияние на набухание семян. Набухание семян проводили в соответствии с Turk and Tawaha (2003) с модификацией. Кратко, исходную массу семян сорняка (W1) регистрировали, а затем семена погружали в грибной экстракт на установленный период инкубации 12, 24 или 36 часов. Поскольку ежовнику требуется приблизительно 36 часов для завершения процесса прорастания (Takao et al., 2011), эти временные точки были выбраны для мониторинга физиологической реакции на каждой стадии прорастания. После инкубации семена промывали и снова взвешивали (W2), а значения водопоглощения определяли с использованием формулы:
Активность α-амилазы (EC 3.2.1.1) определяли с помощью теста с 3,5-динитросалициловой кислотой (ДНСК). Активность α-амилазы измеряли, как сообщалось Sadasivam and Manickam (1996). Для экстракции фермента обработанные семена измельчали с 0,1 M CaCl2 (4 мл) в ледяной бане и центрифугировали при 9600 × g в течение 20 минут при температуре 4°C. Это давало сырой фермент. Впоследствии реакцию проводили путем добавления 1,0 мл сырого фермента к 1,0 мл 0,5% растворимого крахмала. Смесь инкубировали, а затем добавляли 1,0 мл реактива ДНСК, после чего раствор реакции немедленно помещали в кипящую водяную баню на 5 минут. Наконец, измеряли светопоглощение при 560 нм и использовали его для расчета активности α-амилазы, выраженной в мкмоль мальтозы/мин/г (свежая масса, СМ).
2.5 Измерение содержания MDA и H2O2
Анализ тиобарбитуровой кислоты реактивных веществ (ТБК-РВ) использовали для определения перекисного окисления липидов на основе оценки содержания малонового диальдегида (MDA). Образец (0,5 г СМ) растирали с 6,0 мл 3,0% трихлоруксусной кислоты (ТХУК) и центрифугировали в течение 20 минут при 4°C при 9600 × g. Затем супернатант (1,0 мл) смешивали с 2,0 мл 0,5% тиобарбитуровой кислоты (ТБК) в 20% ТХУК. Эту реакционную смесь нагревали в кипящей водяной бане в течение 20 минут перед охлаждением на льду в течение 5 минут (He et al., 2014). Наконец, измеряли поглощение при 532 и 600 нм, и для расчета содержания MDA использовали коэффициент экстинкции 155 мМ/см·м. Содержание пероксида водорода (H2O2) рассчитывали согласно Velikova, Yordanov (Velikova et al., 2000). Обработанные семена (0,5 г СМ) гомогенизировали с 6,0 мл 3,0% ТХУК и центрифугировали (9600 × g) в течение 20 минут. Затем к 1,0 мл супернатанта добавляли 3,0 мл реакционной смеси (10 мМ фосфатный буфер pH 7,0 и 500 мМ йодида калия). Через 15 минут измеряли поглощение при 390 нм.
2.6 Экстракция и определение активности антиоксидантных ферментов
Сырой экстракт фермента готовили в соответствии с процедурой, описанной Mir, John (Mir et al., 2018). Кратко, 6,0 мл 50 мМ фосфатного буфера, содержащего поливинилполипирролидон (ПВПП) и 0,5 мМ этилендиаминтетрауксусную кислоту (ЭДТА), использовали для экстракции обработанных семян ежовника (1,0 г СМ). Гомогенаты центрифугировали, и полученные сырые экстракты фермента использовали для тестирования активности ферментов. Значения поглощения растворимых белков определяли колориметрически при 595 нм с использованием метода Брэдфорда (Bradford, 1976). Все полученные биохимические показатели определяли в четырех повторностях. Активность супероксиддисмутазы (СОД), каталазы (КАТ) и гваяколпероксидаз (ПО) определяли с помощью колориметрического анализа, следуя методу, описанному Chen and Zhang (2016). Активность СОД (EC 1.15.1.1) определяли при 560 нм с использованием фоторедукции нитросинего тетразолия (НСТ). Реакционная смесь состояла из 100 мМ фосфата калия (pH 7,8), содержащего 130 мМ метионина, 750 мкМ НСТ, 100 мкМ ЭДТА и 20 мкМ рибофлавина. Экстракт фермента (1,0 мл) добавляли к реакционной смеси, за исключением случая контроля. Затем смесь инкубировали на свету в течение 30 минут и определяли удельную активность, выраженную в единицах СОД/мг белка. Одна единица СОД определяется как количество, которое ингибирует фоторедукцию НСТ на 50%. Аналогично, для определения активности КАТ (EC 1.11.1.6), сырой экстракт фермента (1,0 мл) добавляли к реакционной смеси КАТ, которая включала фосфатный буфер (100 мМ, pH 7,0) и H2O2 (10 мМ). Изменение поглощения из-за потребления H2O2 немедленно регистрировали при 240 нм каждые 15 секунд в течение 1 минуты, отслеживая устойчивое среднее изменение. Затем активность фермента рассчитывали и выражали как единицы/мг белка. Одна единица КАТ определяется как количество фермента, которое уменьшает поглощение при 240 нм на 0,1 в минуту. Наконец, гваякол использовали для измерения активности ПО (EC 1.11.1.7). В этом анализе 1,0 мл экстракта фермента добавляли к смеси фосфатного буфера (100 мМ, pH 7,0), ЭДТА (0,1 мМ), гваякола (0,5%) и H2O2 (1,0 мМ). Увеличение поглощения, вызванное окислением гваякола, немедленно измеряли при 470 нм каждые 15 секунд в течение 1 минуты. Определенную активность фермента выражали как единицы/мг белка. Одна единица ПО определяется как количество фермента, которое увеличивает поглощение при 470 нм на 0,01 в минуту.
2.7 Статистический анализ
Эксперимент был организован в полностью рандомизированном дизайне с четырьмя повторностями и был повторен дважды. Каждый образец был собран в четырех повторностях для биохимического анализа. Результаты представлены как средние значения. Все данные были проанализированы с использованием программного обеспечения SAS и подвергнуты дисперсионному анализу (ANOVA) и сравнению средних с помощью множественного рангового критерия Тьюки (p≤0,05). Средние значения, за которыми следуют одинаковые буквы, не различаются.
3 Результаты и обсуждение
3.1 Влияние на прорастание и ранний рост E. crus-galli
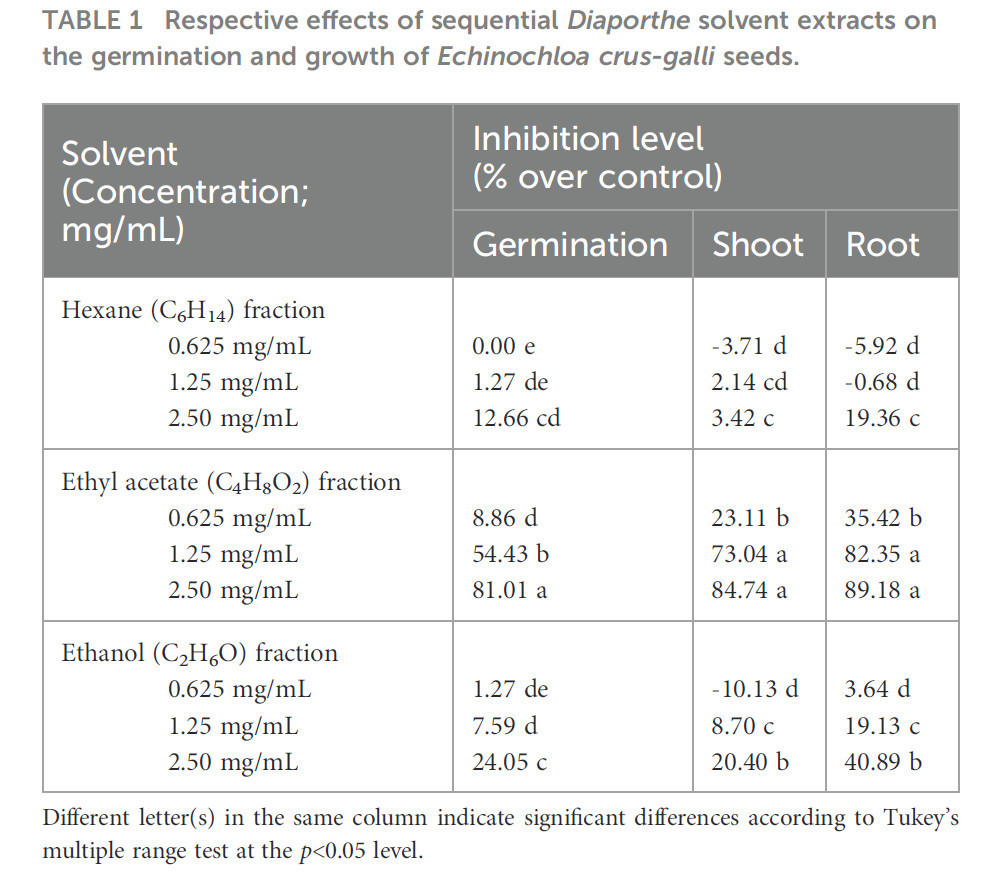
Измельченный мицелий Diaporthe sp. EC010 взвешивали и подвергали последовательной экстракции. Наиболее высокий выход экстракции был получен из фракции EtOH, за которой следовали фракции EtOAc и гексана соответственно (данные не показаны). В таблице 1 показано влияние этих экстрактов на прорастание и рост проростков E. crus-galli. Для всех экстрактов процент прорастания снижался по мере увеличения концентрации экстракта. Фракция EtOAc оказывала значительно большее влияние на прорастание ежовника по сравнению с другими растворителями; при наиболее высокой протестированной концентрации 2,50 мг/мл соответствующие проценты ингибирования составили 81,01%, 24,05% и 12,66% для фракций EtOAc, EtOH и гексана соответственно (Рисунок 1). Помимо влияния на прорастание семян, фракция EtOAc также оказывала влияние на рост проростков E. crus-galli. Физический осмотр длины побегов и корней показал, что обработка фракцией EtOAc уменьшала их во всем диапазоне концентраций. Примечательно, что корни проростков сорняка были чрезвычайно ограничены по сравнению с побегами (Laosinwattana et al., 2018; Somala et al., 2022). Поскольку корень проростков E. crus-galli погружался в чашки Петри, содержащие экстракт, ингибирующий эффект экстракта на корень проростков оказался больше, чем на побег. Teerarak, Charoenying (Teerarak et al., 2012) аналогично изучали влияние экстракта Aglaia odorata в EtOAc в смачивающейся порошковой формуле на прорастание и начальный рост E. crus-galli, в котором обработанные семена показали более низкое набухание и активность α-амилазы. Что касается различных результатов трех протестированных здесь экстрактов, различия в ингибирующей эффективности могут быть вызваны несколькими факторами, такими как состав, растворимость в растворителе и полярность растворителя. Таким образом, хорошо установлено, что ингибирующая активность различается в различных экстрактах, полученных с использованием разных растворителей (Li et al., 2006; Luthria et al., 2007; Garcia et al., 2010). Эти сообщения подтверждают, что настоятельно необходимо использовать подходящие растворы растворителей при проведении селективной экстракции из природных источников, чтобы получить фракции с высоким аллелопатическим потенциалом и высоким выходом сырого экстракта. Поскольку результаты анализа показали, что фракция EtOAc обладает наиболее мощной ингибирующей эффективностью, эта фракция была использована в последующих экспериментах.
Таблица 1 Соответствующие эффекты последовательных растворительных экстрактов Diaporthe на прорастание и рост семян Echinochloa crus-galli.
Разные буквы в одном столбце указывают на значительные различия согласно множественному ранговому критерию Тьюки при уровне p<0,05.
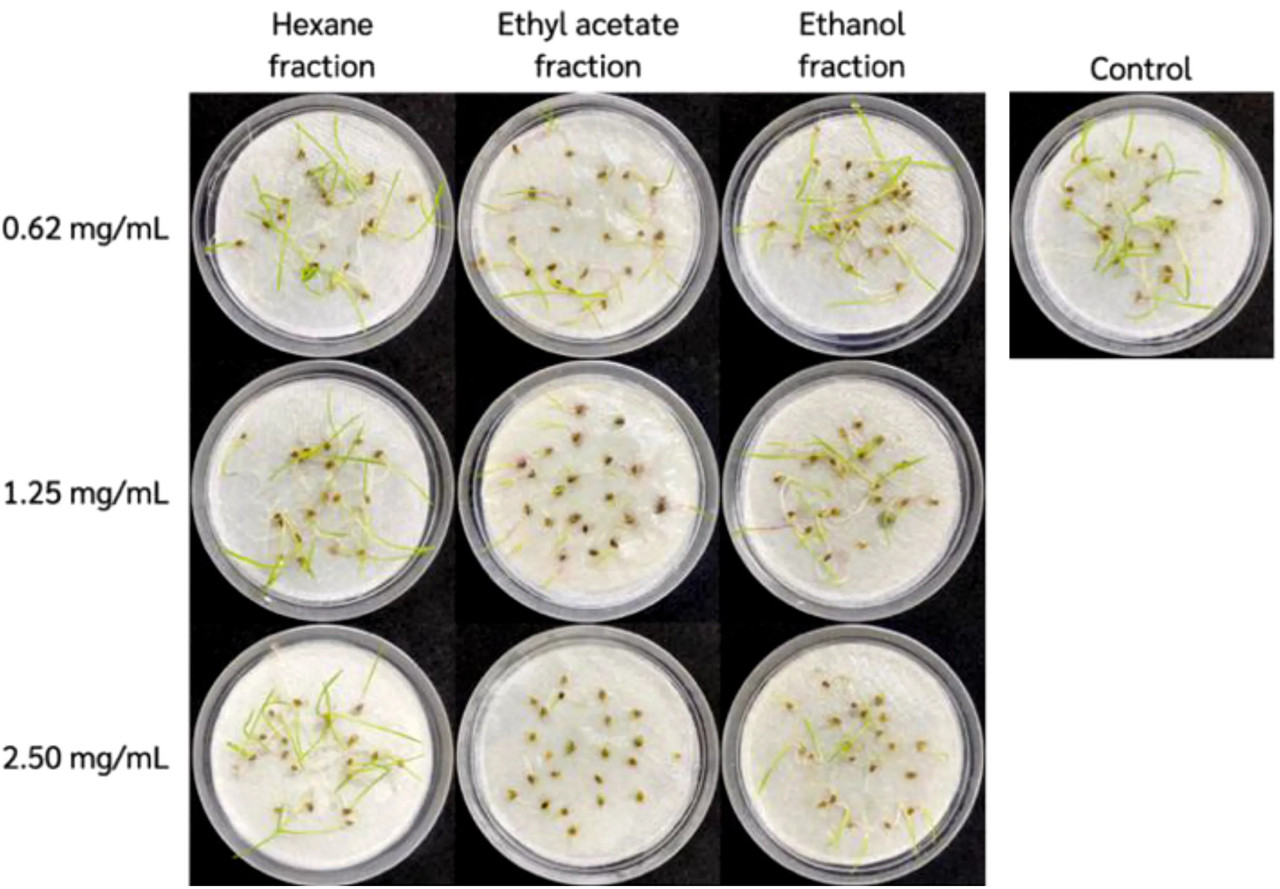
Рисунок 1 Ингибирующие эффекты, наблюдаемые во время биоиспытаний с последовательными растворительными экстрактами мицелия Diaporthe sp.
3.2 Химические компоненты сырого экстракта Diaporthe в EtOAc
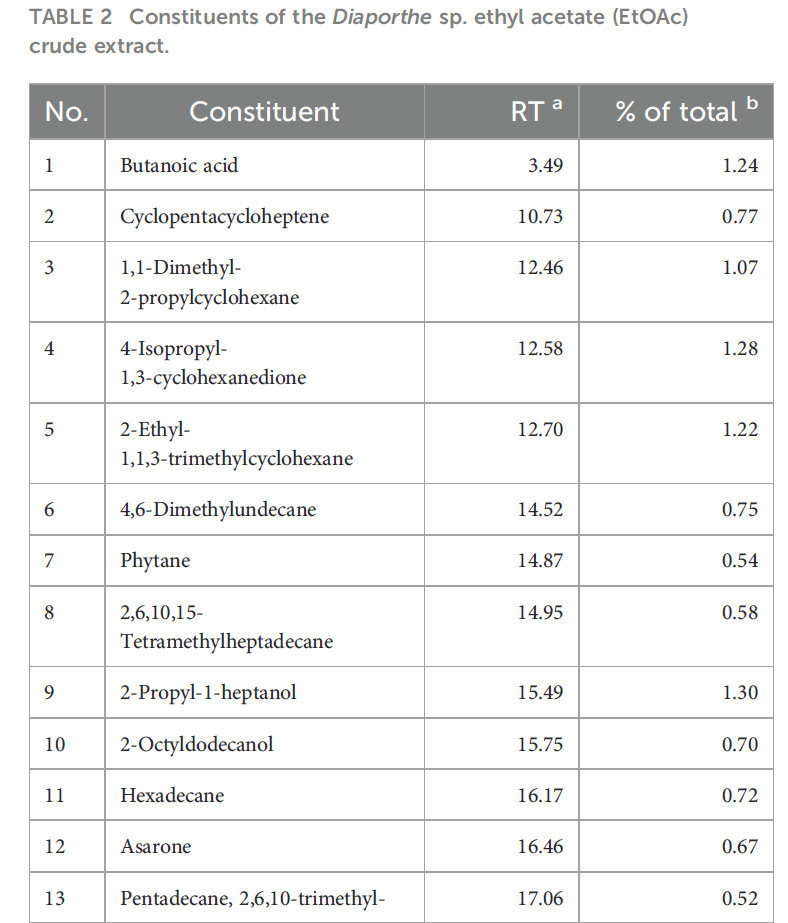
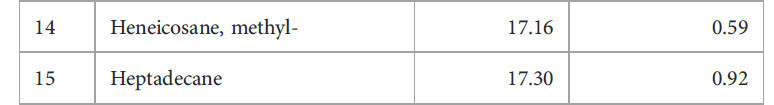
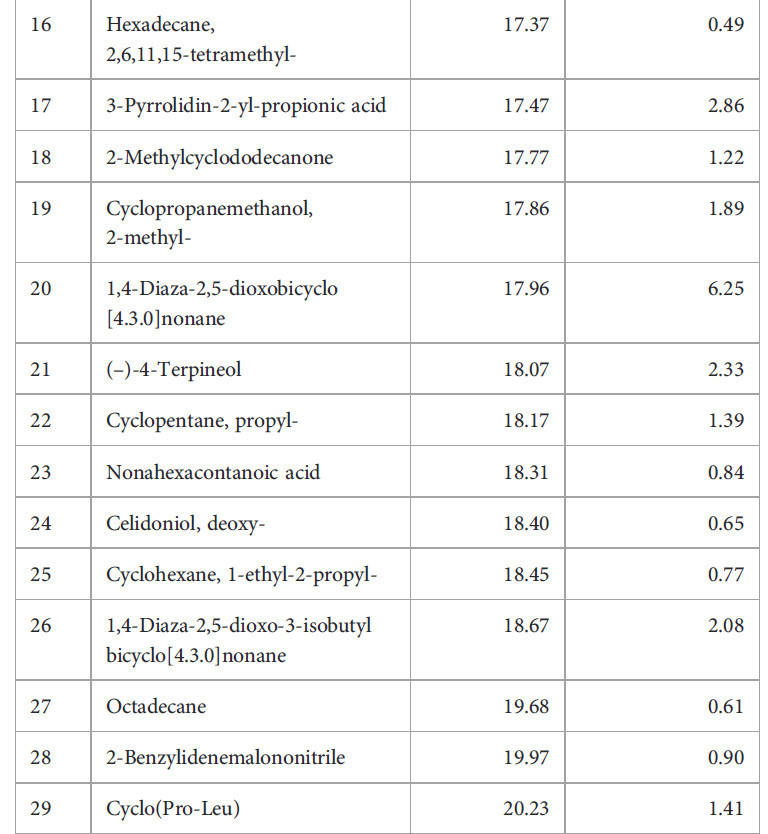
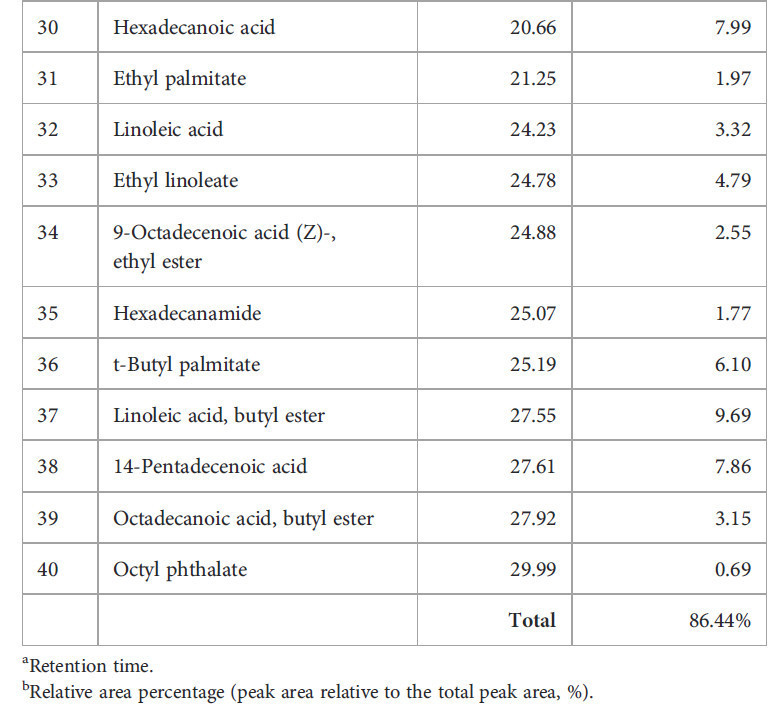
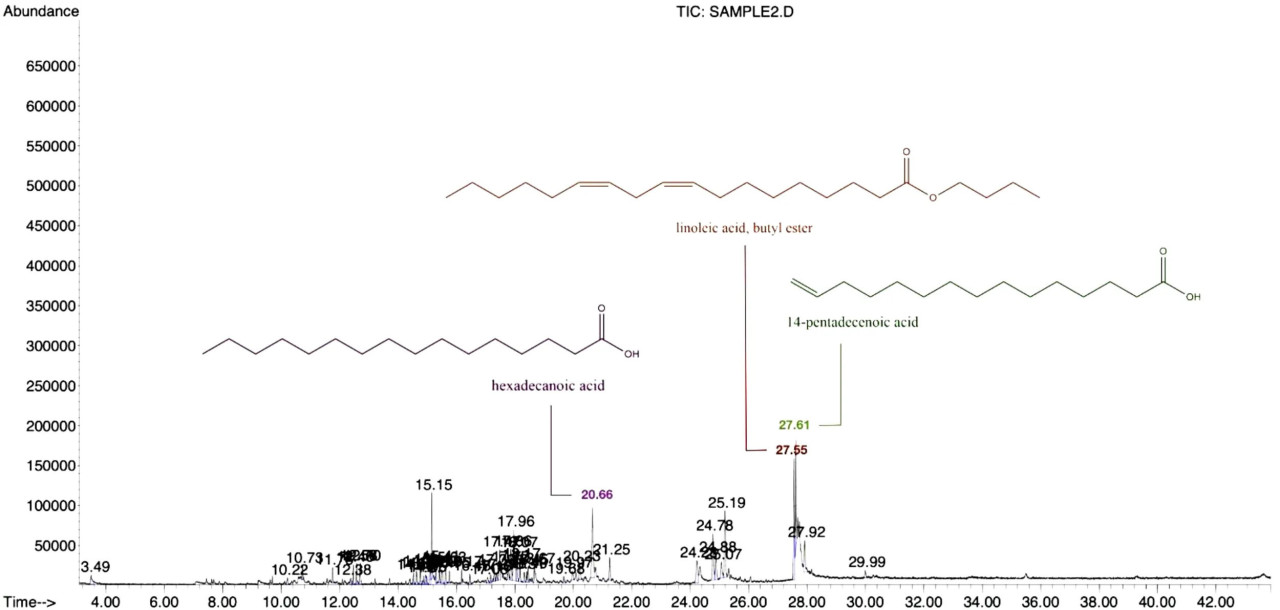
В таблице 2 перечислены химические компоненты, идентифицированные с помощью ГХ-МС в сыром экстракте мицелия Diaporthe в EtOAc. Этот анализ показал, что экстракт содержит множество фитосоединений (Рисунок 2), причем 40 идентифицированных компонентов в совокупности составляли 86,44% от общего сырого экстракта. Основными компонентами (Рисунок 3) были линолевая кислота, бутиловый эфир (9,69%), гексадеценовая кислота (7,99%) и 14-пентадеценовая кислота (7,86%). Эти результаты согласуются с предыдущими сообщениями da Rosa, Sauzem (da Rosa et al., 2021) и dos Reis, da Rosa (dos Reis et al., 2019), которые нашли сложные эфиры жирных кислот и диазосоединения в качестве основных химических компонентов экстрактов Diaporthe schini. Примечательно, что специфические активности метаболических ферментов (Winter et al., 2011; Tanapichatsakul et al., 2019) и видовое разнообразие могут приводить к дифференциации химических компонентов. Фитотоксичность, наблюдаемая в этом исследовании, может быть связана с этими идентифицированными химическими веществами и возможным синергизмом между ними.
Таблица 2 Компоненты сырого экстракта этилацетата (EtOAc) Diaporthe sp.
Рисунок 2 ГХ-МС хроматограмма и химическая структура основных соединений сырого экстракта Diaporthe sp. в EtOAc, показывающие время удерживания (мин) пиков.
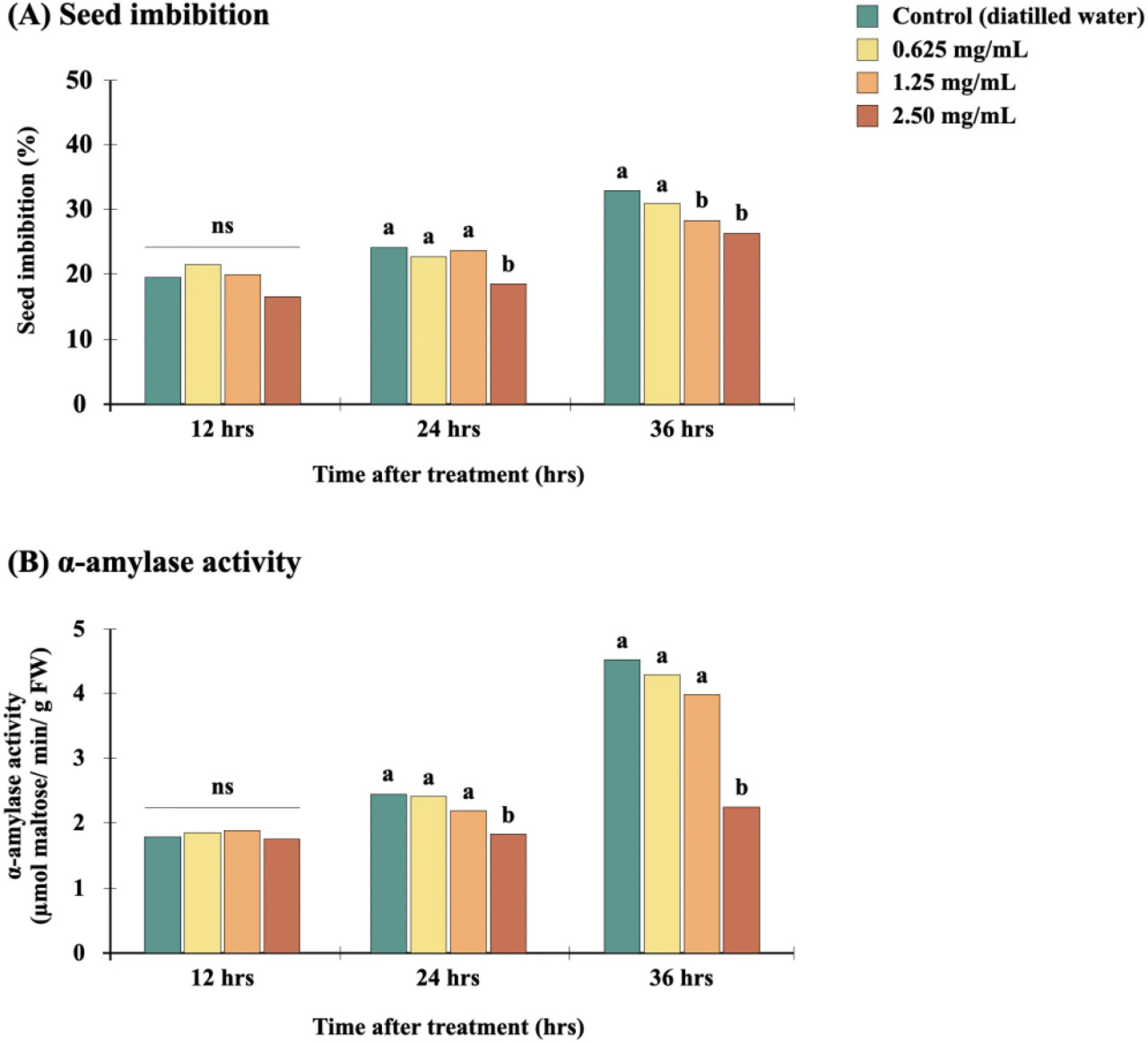
Рисунок 3 Влияние сырого экстракта Diaporthe sp. в EtOAc на набухание (A) и активность α-амилазы (B) семян E. crus-galli. Для данного времени воздействия столбцы с разными буквами (a, b) между обработками значительно различаются при p<0,05 согласно множественному ранговому критерию Тьюки. «ns» указывает на отсутствие значимого различия. Данные представляют собой средние значения (n=4).
3.3 Влияние на набухание семян и активность α-амилазы
Сначала мы исследовали, нарушается ли набухание семян, начальная фаза процесса прорастания семян, сырым экстрактом Diaporthe в EtOAc. В первые 12 часов после погружения семян сорняка в экстракт или дистиллированную воду скорость поглощения была высокой и значимо не отличалась (p>0,05) от контроля. С 12 до 24 часов семена поглотили больше воды, чем на первой стадии. Затем, с 24 до 36 часов, экстракт Diaporthe явно нарушал набухание семян в зависимости от концентрации обработки и продолжительности (Рисунок 3A). Это может быть attributed к тому, что экстракт изменяет водный потенциал, что вызывает осмотический стресс (Manichart et al., 2023a). Сниженное набухание предполагает, что поглощение воды и минеральных питательных веществ ограничено, что ограничивает рост проростков (Kamran et al., 2020), что подтверждается ранее опубликованными исследованиями (Teerarak et al., 2012; Laosinwattana et al., 2018; Manichart et al., 2023b).
Мы дополнительно исследовали влияние экстракта Diaporthe на активность α-амилазы, показанную на Рисунке 3B. Во время прорастания семян основным источником энергии является крахмал эндосперма и его расщепление. Этот процесс зависит от нескольких ферментов, включая α-глюкозидазу, деветвящий фермент и α- и β-амилазы (Amato et al., 2023), из которых α-амилаза функционирует на протяжении всего процесса прорастания, расщепляя крахмал на более мелкие молекулы, тем самым обеспечивая питательные вещества и энергию, необходимые для прорастания (Li et al., 2019). После обработки семян сорняка экстрактом Diaporthe, α-амилазу экстрагировали из семян, и ее активность определяли путем продукции мальтозы in vitro. В результате деградация активности α-амилазы ингибировалась всеми концентрациями экстракта, что коррелирует с прорастанием (Таблица 1). В целом, активность α-амилазы была снижена в обработанных экстрактом семенах сорняка по сравнению с контролями. Более того, экстракт ингибировал активность α-амилазы дозозависимым образом, при этом наиболее высокая протестированная концентрация (2,50 мг/мл) показала заметно обширное снижение активности α-амилазы через 36 часов после обработки (p<0,05). Этот вывод совместим с результатами анализа набухания семян и согласуется с литературой о гербицидных эффектах грибных экстрактов из Alternaria brassicicola и изолята Diaporthe sp. EC010 на амаранте, двудольном сорном растении (Manichart et al., 2023a; Manichart et al., 2023b). Согласно результатам текущего исследования, одним из гербицидных свойств этого экстракта является ингибирование активности α-амилазы. Поскольку крахмал не расщепляется на крошечные молекулы для поддержки роста и развития, это воздействие может, в свою очередь, привести к ингибированию прорастания семян и роста проростков.
3.4 Влияние на MDA, генерацию ROS и активность антиоксидантных ферментов
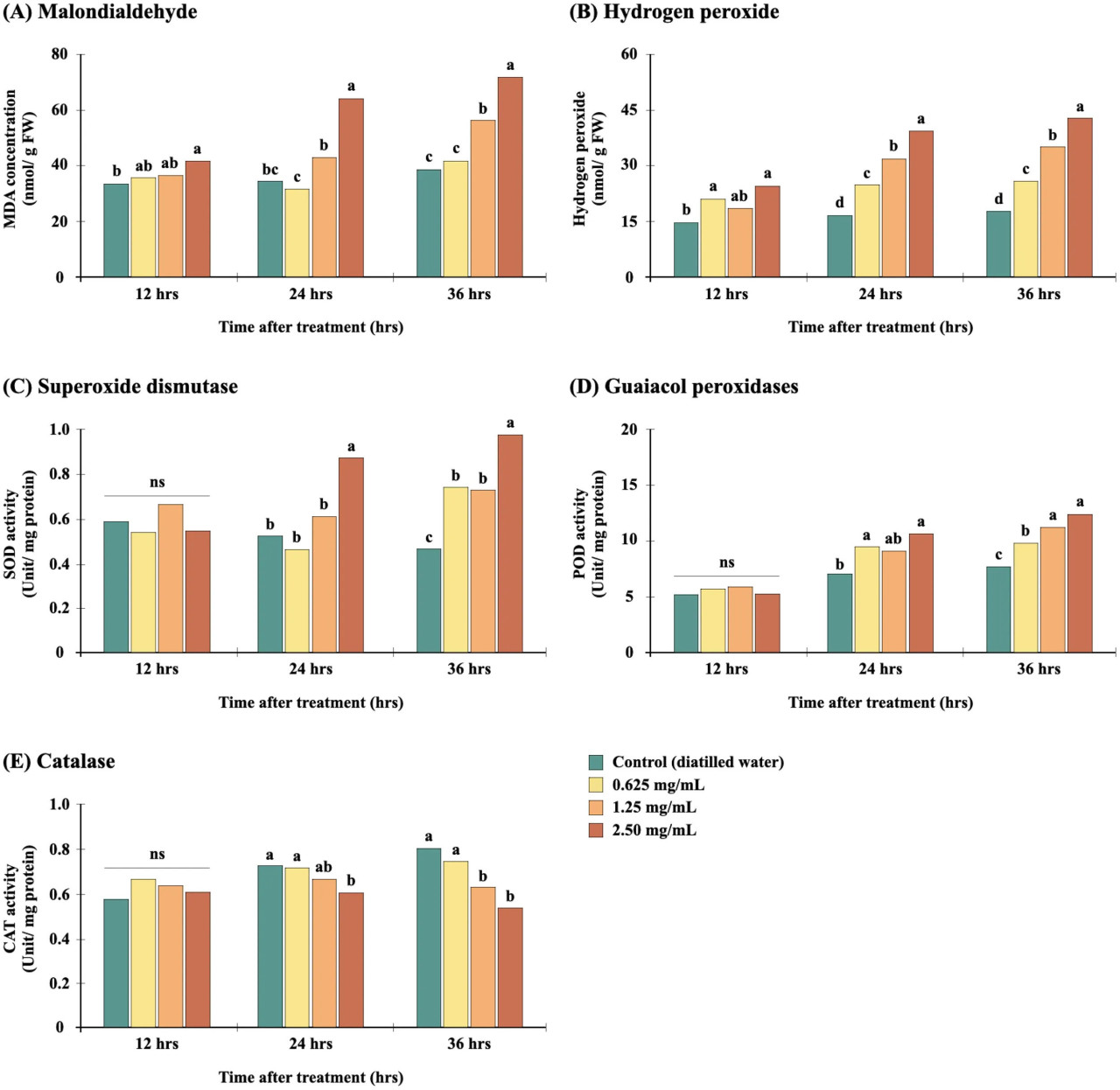
Степень активности АФК в растительных клетках зависит от способности АФК перемещаться через клеточные мембраны. Среди АФК H2O2 является наиболее стабильным и легко перемещается через мембраны на относительно большие расстояния, даже в сухих семенах. Ratajczak, Małecka (Ratajczak et al., 2015) и Kurek, Plitta-Michalak (Kurek et al., 2019) показали значительную корреляцию между уровнями H2O2 и сниженным прорастанием (r = -0,9471, p = 0,004139). Соответственно, в этом исследовании мы фокусируемся на накоплении H2O2 в семенах E. crus-galli как окне в роль окислительного стресса в механизме действия фракции Diaporthe sp. в EtOAc (Рисунки 4A, B). Клеточные мембраны растений состоят из жирных кислот и других липидов, и, таким образом, свободные липиды могут высвобождаться из деградированных клеточных мембран в результате окислительного действия (Scrivanti et al., 2003). Перекисное окисление липидов жирных кислот в конечном итоге приводит к накоплению MDA (Marnett, 1999). В настоящем исследовании было обнаружено, что содержание MDA и H2O2 в семенах значительно повышается через 24 и 36 часов воздействия 2,50 мг/мл грибного экстракта, с увеличением MDA на 84,47% и 85,52% и увеличением концентрации H2O2 на 137,17% и 141,10% соответственно. Таким образом, обработка экстрактом значительно увеличивала продукцию H2O2 и вызывала перекисное окисление липидов, что приводило к индуцированному окислительному повреждению семян E. crus-galli (Oracz et al., 2009; Ma et al., 2016). H2O2 считался как благоприятным (Oracz et al., 2009; Bahin et al., 2011), так и вредным фактором в отношении клеточных событий при прорастании семян. Поскольку он регулирует экспрессию генов и передачу сигналов фитогормонов (абсцизовая кислота, гиббереллины, ауксины и этилен) (Bailly, 2019), умеренный уровень H2O2 полезен и способствует прорастанию, тогда как чрезмерное содержание H2O2 индуцирует окислительное повреждение, которое предотвращает или задерживает прорастание (Kurek et al., 2019). Эта двойная роль наблюдалась в семенах хлопчатника, для которых более высокие уровни H2O2 и перекисного окисления липидов коррелировали со сниженным прорастанием (Goel and Sheoran, 2003), и в стареющих семенах подсолнечника Kibinza, Vinel (Kibinza et al., 2006), которые установили линейную ассоциацию между содержанием H2O2 и прорастанием. Аналогично, было обнаружено, что снижающаяся жизнеспособность семян пшеницы зависит как от продукции H2O2, так и от уровня перекисного окисления липидов (Kong et al., 2015), которое изменяет проницаемость мембраны и тем самым снижает жизнеспособность семян.
Рисунок 4 Влияние сырого экстракта Diaporthe sp. в EtOAc на содержание MDA (A) и H2O2 (B) и активность СОД (C), ПО (D) и КАТ (E) в E. crus-galli. Для данного времени воздействия разные буквы (a, b) над столбцами указывают на значительные различия при p<0,05. «ns» указывает на отсутствие значимого различия. Данные представляют собой средние значения (n=4).
Антиоксидантные ферменты играют важную роль в регуляции окислительно-восстановительного статуса, балансируя уровни АФК. Мы обнаружили, что активность СОД значительно повышалась в семенах E. crus-galli, подвергшихся воздействию экстракта Diaporthe sp. (Рисунок 4C), достигая 67,24% сверх контроля (p<0,05) через 36 часов после прорастания. Активность ПО также стабильно увеличивалась по мере прогрессирования периода прорастания (Рисунок 4D), причем максимальная доза давала увеличение на 49,87% и 61,62% через 24 и 36 часов соответственно. Между тем, в отличие от СОД и ПО, активность КАТ показала тенденцию к снижению дозозависимым образом (Рисунок 4E), что указывает на то, что экстракт снижает регуляцию ферментативной активности КАТ. Поскольку СОД и ПО участвуют в удалении АФК (Shuai et al., 2011; Bhardwaj et al., 2021), их более высокая активность в обработанных семенах E. crus-galli может указывать на индукцию этих антиоксидантных ферментов, чтобы помочь клеткам справиться с вызванным экстрактом окислительным стрессом и минимизировать развитие свободных радикалов (Narayan et al., 2024). Предыдущее исследование предположило более высокую активность пролина в Amaranthus tricolor, обработанном экстрактом Diaporthe (Manichart et al., 2023a). Пролин также служит поглотителем свободных радикалов, защищая от денатурации белков и деградации мембран (Kumar et al., 2018; Kamran et al., 2020). Тем не менее, поскольку экстракт Diaporthe в этом исследовании показал негативные эффекты на прорастание семян независимо от применяемой концентрации, индуцированных СОД и ПО было недостаточно для ингибирования пролиферации АФК и MDA. Значительное снижение активности КАТ, вероятно, усугубляло окислительные всплески. В аналогичном исследовании семян подсолнечника наблюдалось снижение ферментативной активности КАТ в условиях ускоренного окислительного стресса (Kibinza et al., 2011). Более того, Ratajczak, Małecka (Ratajczak et al., 2015) сообщили о сниженной активности КАТ в семенах бука и сильной отрицательной корреляции (r = -0,9177) активности КАТ с уровнем H2O2. В нашей гипотетической модели, показанной на Рисунке 5, снижение активности КАТ могло привести к накоплению АФК, что приводит к перекисному окислению липидов и инактивации ферментов, что, в свою очередь, могло бы способствовать структурному и функциональному повреждению белков и углеводов и модификации или нарушению структуры ДНК (Sharma et al., 2012). Такие события объяснили бы сниженный процент прорастания, наблюдаемый в обработанных экстрактом семенах.
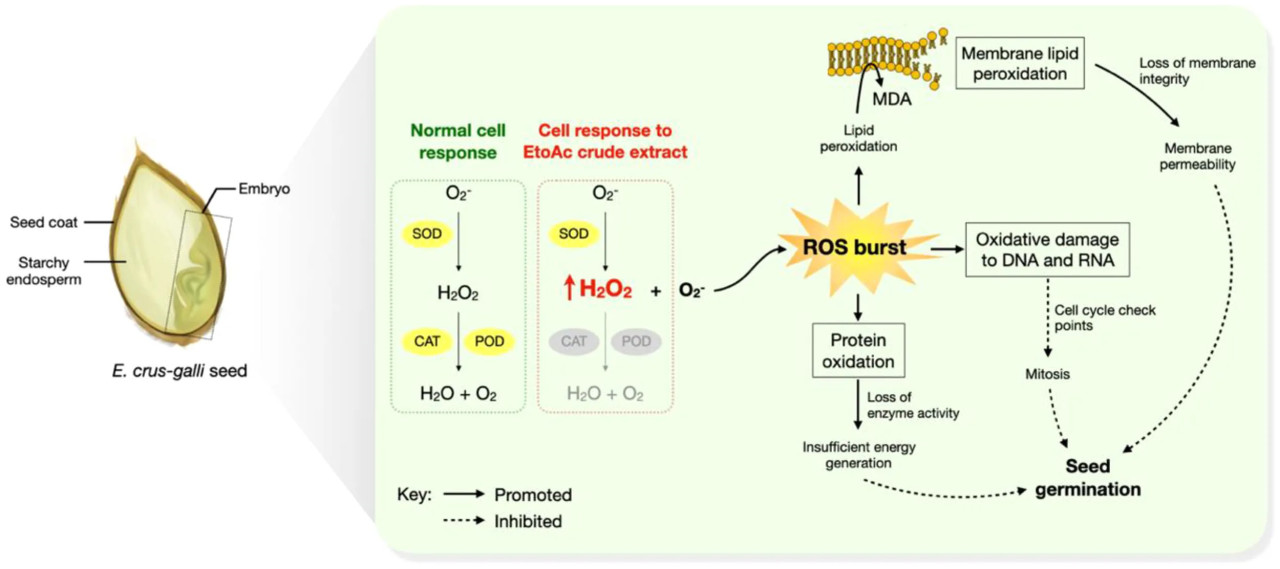
Рисунок 5 Гипотетическая модель механизма ингибирования прорастания семян сырым экстрактом Diaporthe sp. в EtOAc.
Наше исследование продемонстрировало потенциал грибных аллелохимических веществ в ингибировании роста сорняков через окислительное повреждение, внося ценные идеи в ограниченную литературу по этой теме. Будущая работа будет сосредоточена на оптимизации формулы экстракта, исследовании его избирательности и проведении полевых испытаний. Мы также оценим потенциальные воздействия на окружающую среду, чтобы обеспечить безопасность и устойчивость этого подхода. Это новаторское исследование служит основой для разработки гербицидов грибного происхождения в качестве альтернативной стратегии борьбы с сорняками.
4 Заключение
Это исследование изучает ингибирующие эффекты сырых экстрактов штамма Diaporthe sp. EC010 на прорастание и рост ежовника. Фракция этилацетата наиболее сильно снижала прорастание семян и развитие сорняка. ГХ-МС этой фракции идентифицировала ее основные компоненты, включающие линолевую кислоту, бутиловый эфир (9,69%), гексадекановую кислоту (7,99%) и 14-пентадеценовую кислоту (7,86%). Обработанные семена E. crus-galli показали более низкое набухание, сниженную активность α-амилазы, повышенное содержание MDA и накопление H2O2. Они также продемонстрировали более высокую активность СОД и ПО, но более низкую активность КАТ, что может коррелировать с задержкой прорастания и роста проростков. В целом, это исследование представляет собой изучение окислительного повреждения, вызванного экстрактом Diaporthe. Это исследование подчеркивает потенциал экстракта Diaporthe в качестве кандидата для довсходовых гербицидных продуктов. Хотя результаты являются перспективными, они основаны на лабораторных анализах и фокусируются на одном виде сорняков. Дополнительные исследования необходимы для определения эффективности экстрактов Diaporthe в полевых условиях, оценки их воздействия на сельскохозяйственные культуры, здоровье почвы и экологические факторы, а также для понимания их роли в стратегиях интегрированной борьбы с сорняками.
Ссылки
1. Amato G., Caputo L., Francolino R., Martino M., De Feo V., De Martino L. (2023). Origanum heracleoticum essential oils: chemical composition, phytotoxic and alpha-amylase inhibitory activities. Plants. 12, 866. doi: 10.3390/plants12040866. CrossRef Google Scholar
2. Bahin E., Bailly C., Sotta B., Kranner I., Corbineau F., Leymarie J. (2011). Crosstalk between reactive oxygen species and hormonal signalling pathways regulates grain dormancy in barley. Plant Cell Environ. 34, 980–993. doi: 10.1111/j.1365-3040.2011.02298.x. CrossRef Google Scholar
3. Bailey K. L. (2014). The bioherbicide approach to weed control using plant pathogens. Integrated Pest Management: Elsevier; p, 245. doi: 10.1016/B978-0-12-398529-3.00014-2. CrossRef Google Scholar
4. Bailly C. (2019). The signalling role of ROS in the regulation of seed germination and dormancy. Biochem. J. 476, 3019–3032. doi: 10.1042/BCJ20190159. CrossRef Google Scholar
5. Bhardwaj R. D., Singh N., Sharma A., Joshi R., Srivastava P. (2021). Hydrogen peroxide regulates antioxidant responses and redox related proteins in drought stressed wheat seedlings. Physiol. Mol. Biol. Plants 27, 151–163. doi: 10.1007/s12298-021-00937-z. CrossRef Google Scholar
6. Bradford M. M. (1976). A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing the principle of protein-dye binding. Analytical Biochem. 72, 248–254. doi: 10.1016/0003-2697(76)90527-3. CrossRef Google Scholar
7. Chen T., Zhang B. (2016). Measurements of proline and malondialdehyde content and antioxidant enzyme activities in leaves of drought stressed cotton. Bio-protocol. 6, e1913. doi: 10.21769/BioProtoc.1913. CrossRef Google Scholar
8. Choudhary A., Kumar A., Kaur N. (2020). ROS and oxidative burst: Roots in plant development. Plant Diversity. 42, 33–43. doi: 10.1016/j.pld.2019.10.002. CrossRef Google Scholar
9. da Rosa B. V., Sauzem G. D. S., Kuhn R. C. (2021). Obtaining antioxidant compounds from the endophytic fungus Diaporthe schini using heat- and ultrasound-assisted extraction. Braz. J. Chem. Engineering. 38, 189–195. doi: 10.1007/s43153-021-00089-3. CrossRef Google Scholar
10. Dmitrieva V. A., Tyutereva E. V., Voitsekhovskaja O. V. (2024). What can reactive oxygen species (ROS) tell us about the action mechanism of herbicides and other phytotoxins? Free Radical Biol. Med. 220, 92–110. doi: 10.1016/j.freeradbiomed.2024.04.233. CrossRef Google Scholar
11. dos Reis C. M., da Rosa B. V., da Rosa G. P., do Carmo G., Morandini L. M. B., Ugalde G. A. et al. (2019). Antifungal and antibacterial activity of extracts produced from Diaporthe schini. J. Biotechnol. 294, 30–37. doi: 10.1016/j.jbiotec.2019.01.022. CrossRef Google Scholar
12. Fujita M., Hasanuzzaman M. (2022). Approaches to enhancing antioxidant defense in plants. Antioxidants (Basel). 11 (5), 925. doi: 10.3390/antiox11050925. CrossRef Google Scholar
13. Gao W. T., Su W. H. (2024). Weed management methods for herbaceous field crops: A review. Agronomy. 14, 486. doi: 10.3390/agronomy14030486. CrossRef Google Scholar
14. Garcia L. M. Z., de Oliveira T. F., Soares P. K., Bruns R. E., Scarminio I. S. (2010). Statistical mixture design—Principal component determination of synergic solvent interactions for natural product extractions. Chemometrics Intelligent Lab. Systems. 103, 1–7. doi: 10.1016/j.chemolab.2010.04.016. CrossRef Google Scholar
15. Goel A., Sheoran I. (2003). Lipid peroxidation and peroxide-scavenging enzymes in cotton seeds under natural ageing. Biol. Plantarum. 46, 429–434. doi: 10.1023/A:1024398724076. CrossRef Google Scholar
16. Hazrati H., Saharkhiz M. J., Niakousari M., Moein M. (2017). Natural herbicide activity of Satureja hortensis L. essential oil nanoemulsion on the seed germination and morphophysiological features of two important weed species. Ecotoxicology Environ. Safety. 142, 423–430. doi: 10.1016/j.ecoenv.2017.04.041. CrossRef Google Scholar
17. He J., Ren Y., Chen X., Chen H. (2014). Protective roles of nitric oxide on seed germination and seedling growth of rice (Oryza sativa L.) under cadmium stress. Ecotoxicology Environ. Saf. 108, 114–119. doi: 10.1016/j.ecoenv.2014.05.021. CrossRef Google Scholar
18. Huang L., Zhang X., Yang Y., Zou H., Fang B., Liu W. (2021). High-quality genome resource of Diaporthe destruens causing foot rot disease of sweet potato. Plant Disease. 105, 3279–3281. doi: 10.1094/PDIS-07-20-1473-A. CrossRef Google Scholar
19. Kamran M., Xie K., Sun J., Wang D., Shi C., Lu Y. et al. (2020). Modulation of growth performance and coordinated induction of ascorbate-glutathione and methylglyoxal detoxification systems by salicylic acid mitigates salt toxicity in choysum (Brassica parachinensis L.). Ecotoxicology Environ. Saf. 188, 109877. doi: 10.1016/j.ecoenv.2019.109877. CrossRef Google Scholar
20. Kibinza S., Bazin J., Bailly C., Farrant J. M., Corbineau F., Bouteau H. (2011). Catalase is a key enzyme in seed recovery from ageing during priming. Plant Science. 181, 309–315. doi: 10.1016/j.plantsci.2011.06.003. CrossRef Google Scholar
21. Kibinza S., Vinel D., Côme D., Bailly C., Corbineau F. (2006). Sunflower seed deterioration as related to moisture content during ageing, energy metabolism and active oxygen species scavenging. Physiologia Plantarum. 128, 496–506. doi: 10.1111/j.1399-3054.2006.00771.x. CrossRef Google Scholar
22. Kong L., Huo H., Mao P. (2015). Antioxidant response and related gene expression in aged oat seed. Front. Plant Science. 6, 158. doi: 10.3389/fpls.2015.00158. CrossRef Google Scholar
23. Kumar A., Kumar A., Kumar P., Lata C., Kumar S. (2018). Effect of individual and interactive alkalinity and salinity on physiological, biochemical and nutritional traits of marvel grass. Indian J. Exp. Biol. 56, 573–581. Google Scholar
24. Kurek K., Plitta-Michalak B., Ratajczak E. (2019). Reactive oxygen species as potential drivers of the seed aging process. Plants. 8, 174. doi: 10.3390/plants8060174. CrossRef Google Scholar
25. Laosinwattana C., Wichittrakarn P., Teerarak M. (2018). Chemical composition and herbicidal action of essential oil from Tagetes erecta L. Leaves Ind. Crops Products. 126, 129–134. doi: 10.1016/j.indcrop.2018.10.013. CrossRef Google Scholar
26. Li B., Smith B., Hossain M. M. (2006). Extraction of phenolics from citrus peels: I. Solvent extraction method. Separation Purification Technology. 48, 182–188. doi: 10.1016/j.seppur.2005.07.005. CrossRef Google Scholar
27. Li Q., Yang A., Zhang W.-H. (2019). Higher endogenous bioactive gibberellins and α-amylase activity confer greater tolerance of rice seed germination to saline-alkaline stress. Environ. Exp. Botany. 162, 357–363. doi: 10.1016/j.envexpbot.2019.03.015. CrossRef Google Scholar
28. Luo X. W., Chen C. M., Li K. L., Lin X. P., Gao C. H., Zhou X. F. et al. (2021). Sesquiterpenoids and meroterpenoids from a mangrove derived fungus Diaporthe sp. SCSIO 41011. Natural product Res. 35, 282–288. doi: 10.1080/14786419.2019.1627355. CrossRef Google Scholar
29. Luthria D. L., Biswas R., Natarajan S. (2007). Comparison of extraction solvents and techniques used for the assay of isoflavones from soybean. Food Chem. 105, 325–333. doi: 10.1016/j.foodchem.2006.11.047. CrossRef Google Scholar
30. Ma Z., Marsolais F., Bykova N. V., Igamberdiev A. U. (2016). Nitric oxide and reactive oxygen species mediate metabolic changes in barley seed embryo during germination. Front. Plant Sci. 7. doi: 10.3389/fpls.2016.00138. CrossRef Google Scholar
31. Manichart N., Laosinwattana C., Somala N., Teerarak M., Chotsaeng N. (2023a). Physiological mechanism of action and partial separation of herbicide-active compounds from the Diaporthe sp. extract on Amaranthus tricolor L. Sci. Rep. 13, 18693. doi: 10.1038/s41598-023-46201-0. CrossRef Google Scholar
32. Manichart N., Somala N., Laosinwattana C. (2023b). Allelopathic potential of secondary metabolites produced by Alternaria brassicicola and physiological mechanisms on Amaranthus tricolor. Int. J. Agric. Technol. 19, 1115–1126. Google Scholar
33. Marnett L. J. (1999). Lipid peroxidation-DNA damage by malondialdehyde. Mutat. Research/Fundamental Mol. Mech. Mutagenesis 424, 83–95. doi: 10.1016/s0027-5107(99)00010-x. CrossRef Google Scholar
34. Mir M. A., John R., AlYemeni M. N., Alam P., Ahmad P. (2018). Jasmonic acid ameliorates alkaline stress by improving growth performance, ascorbate glutathione cycle and glyoxylase system in maize seedlings. Sci. Rep. 8, 2831. doi: 10.1038/s41598-018-21097-3. CrossRef Google Scholar
35. Mishra N., Jiang C., Chen L., Paul A., Chatterjee A., Shen G. (2023). Achieving abiotic stress tolerance in plants through antioxidative defense mechanisms. Front. Plant Sci. 14. doi: 10.3389/fpls.2023.1110622. CrossRef Google Scholar
36. Narayan H., Kumar U., Chowdhury T., Swain P., Barik M., Nayak A. K. (2024). Effect of salinity stress on growth, chlorophyll, antioxidant enzymes and nutrient content in Azolla spp. Aquat. Botany. 192, 103750. doi: 10.1016/j.aquabot.2024.103750. CrossRef Google Scholar
37. Nazarkov M., Gerasimova I. (2023). Dynamics of weeds and integrated weed control in crop rotation with cereals. Bulgarian J. Crop Science/Rastenievdni Nauki. 60 (2), 17–25. Google Scholar
38. Oracz K., Hayat E. M. B., Kranner I., Bogatek R., Corbineau F., Bailly C. (2009). The mechanisms involved in seed dormancy alleviation by hydrogen cyanide unravel the role of reactive oxygen species as key factors of cellular signaling during germination. Plant Physiol. 150, 494–505. doi: 10.1104/pp.109.138107. CrossRef Google Scholar
39. Poonpaiboonpipat T., Krumsri R., Kato-Noguchi H. (2021). Allelopathic and Herbicidal Effects of Crude Extract from Chromolaena odorata (L.) RM King and H. Rob. on Echinochloa crus-galli and Amaranthus viridis. Plants 10, 1609. doi: 10.3390/plants10081609. CrossRef Google Scholar
40. Radhakrishnan R., Alqarawi A. A., Allah E. F. (2018). Bioherbicides: Current knowledge on weed control mechanism. Ecotoxicology Environ. Safety. 158, 131–138. doi: 10.1016/j.ecoenv.2018.04.018. CrossRef Google Scholar
41. Ratajczak E., Małecka A., Agnieszka B. Z., Kalemba E. M. (2015). The production, localization and spreading of reactive oxygen species contributes to the low vitality of long-term stored common beech (Fagus sylvatica L.) seeds. J. Plant Physiol. 174, 147–156. doi: 10.1016/j.jplph.2014.08.021. CrossRef Google Scholar
42. Sadasivam S., Manickam A. (1996). Biochemical Methods New Age International (P) Ltd (New Delhi: Publishers). Google Scholar
43. Saini R., Singh S. (2019). Use of natural products for weed management in high-value crops: An overview. Am. J. Agric. Res. 25 (4), 1–13. Google Scholar
44. Scrivanti L. R., Zunino M. P., Zygadlo J. A. (2003). Tagetes minuta and Schinus areira essential oils as allelopathic agents. Biochem. Systematics Ecology. 31, 563–572. doi: 10.1016/S0305-1978(02)00202-8. CrossRef Google Scholar
45. Sharma P., Jha A. B., Dubey R. S., Pessarakli M. (2012). Reactive oxygen species, oxidative damage, and antioxidative defense mechanism in plants under stressful conditions. J. Bot. 2012, 217037. doi: 10.1155/2012/217037. CrossRef Google Scholar
46. Shuai L., Yuan Y., Chen P., Lin S. (2011). Correlation between H~2~O~2~ scavenging system and flavonoids accumulation of Scutellaria baicalensis. Zhongguo Zhong Yao Za Zhi 36, 1707–1710. Google Scholar
47. Somala N., Laosinwattana C., Teerarak M. (2022). Formulation process, physical stability and herbicidal activities of Cymbopogon nardus essential oil-based nanoemulsion. Sci. Rep. 12, 10280. doi: 10.1038/s41598-022-14591-2. CrossRef Google Scholar
48. Sun W., Huang S., Xia J., Zhang X., Li Z. (2021). Morphological and molecular identification of Diaporthe species in south-western China, with description of eight new species. MycoKeys. 77, 65–95. doi: 10.3897/mycokeys.77.59852. CrossRef Google Scholar
49. Takao L. K., Ribeiro J. P. N., Lima M. I. S. (2011). Allelopathic effects of Ipomoea cairica (L.) Sweet Crop weeds. Acta Botanica Brasilica 25, 858–864. doi: 10.1590/S0102-33062011000400012. CrossRef Google Scholar
50. Tanapichatsakul C., Khruengsai S., Monggoot S., Pripdeevech P. (2019). Production of eugenol from fungal endophytes Neopestalotiopsis sp. and Diaporthe sp. isolated from Cinnamomum loureiroi leaves. PeerJ. 7, e6427. doi: 10.7717/peerj.6427. CrossRef Google Scholar
51. Teerarak M., Charoenying P., Laosinwattana C. (2012). Physiological and cellular mechanisms of natural herbicide resource from Aglaia odorata Lour. on bioassay plants. Acta Physiologiae Plantarum. 34, 1277–1285. doi: 10.1007/s11738-011-0923-5. CrossRef Google Scholar
52. Teerarak M., Laosinwattana C., Charoenying P. (2010). Evaluation of allelopathic, decomposition and cytogenetic activities of Jasminum officinale L. f. var. grandiflorum (L.) Kob. on bioassay plants. Bioresource Technology. 101, 5677–5684. doi: 10.1016/j.biortech.2010.02.038. CrossRef Google Scholar
53. Tian W., Liao Z., Zhou M., Wang G., Wu Y., Gao S. et al. (2018). An unusual asymmetric bisanthraquinone with cage-like skeleton from the endophytic fungus Diaporthe sp. Fitoterapia. 128, 253–257. doi: 10.1016/j.fitote.2018.05.032. CrossRef Google Scholar
54. Turk M. A., Tawaha A. (2003). Allelopathic effect of black mustard (Brassica nigra L.) on germination and growth of wild oat (Avena fatua L.). Crop Prot. 22, 673–677. doi: 10.1016/S0261-2194(02)00241-7. CrossRef Google Scholar
55. Velikova V., Yordanov I., Edreva A. (2000). Oxidative stress and some antioxidant systems in acid rain-treated bean plants: Protective role of exogenous polyamines. Plant Science. 151, 59–66. doi: 10.1016/S0168-9452(99)00197-1. CrossRef Google Scholar
56. Winter J. M., Behnken S., Hertweck C. (2011). Genomics-inspired discovery of natural products. Curr. Opin. Chem. Biol. 15, 22–31. doi: 10.1016/j.cbpa.2010.10.020. CrossRef Google Scholar
57. Wu J., Zhai Y., Monikh F. A., Daniel A. L., Grillo R., Vijver M. G. et al. (2021). The Differences between the effects of a nanoformulation and a conventional form of atrazine to lettuce: physiological responses, defense mechanisms, and nutrient displacement. J. Agric. Food Chem. 69, 12527–12540. doi: 10.1021/acs.jafc.1c01382. CrossRef Google Scholar
58. Xu T. C., Lu Y. H., Wang J. F., Song Z. Q., Hou Y. G., Liu S. S. et al. (2021). Bioactive secondary metabolites of the genus Diaporthe and anamorph Phomopsis from terrestrial and marine habitats and endophytes: 2010–2019. Microorganisms. 9, 217. doi: 10.3390/microorganisms9020217. CrossRef Google Scholar
59. Zhang Q., Ma W. G., Zhao Q., Zhao Y. Y., Huang Z. P., Xu Y. X. et al. (2021). α-Pyrone derivatives from endophytic fungus Diaporthe sp. *RJ-41. Biochem. Systematics Ecology.* 94, 104198. doi: 10.1016/j.bse.2020.104198. CrossRef Google Scholar
60. Zhu J., Cai Y., Wakisaka M., Yang Z., Yin Y., Fang W. et al. (2023). Mitigation of oxidative stress damage caused by abiotic stress to improve biomass yield of microalgae: A review. Sci. Total Environment. 896, 165200. doi: 10.1016/j.scitotenv.2023.165200. CrossRef Google Scholar
Somala N, Manichart N, Laosinwattana C, Wichittrakarn P, Yoneyama K, Teerarak M and Chotsaeng N (2024) Oxidative damage in Echinochloa crus−galli seeds exposed to Diaporthe sp. (Diaporthales, Ascomycota) fungal extract during germination. Front. Agron. 6:1456168. doi: 10.3389/fagro.2024.1456168
Перевод статьи «Oxidative damage inEchinochloa crus−galliseeds exposed toDiaporthesp. (Diaporthales, Ascomycota) fungal extract during germination» авторов Somala N, Manichart N, Laosinwattana C, Wichittrakarn P, Yoneyama K, Teerarak M and Chotsaeng N., оригинал доступен по ссылке. Лицензия: CC BY. Изменения: переведено на русский язык
Фото: wikipedia
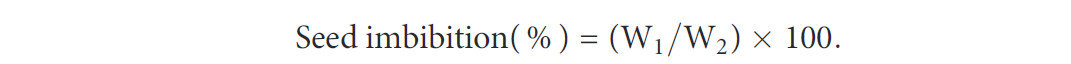















































































































Комментарии (0)