Как патогены картофеля и свеклы выживают в остатках культур и сорняках в севооборотах Нидерландов
Растительные остатки, сапрофитно колонизированные некротрофными фитопатогенами, являются важным источником первичного инокулюма для эпидемий листовых болезней. В ходе эксперимента со сложным севооборотом были проведены систематические пробы остатков культурных растений, сорняков и опада.
Аннотация
Концентрации ДНК основных патогенов выращиваемых культур — Alternaria solani на картофеле, а также Cercospora beticola, Ramularia beticola и Stemphylium beticola на сахарной свекле — были количественно определены в остатках с использованием вновь разработанных ПЦР-анализов в реальном времени. Дополнительные полевые испытания позволили получить данные о динамике A. solani в остатках ботвы картофеля в течение двух лет. Общие результаты показывают, что A. solani и C. beticola колонизируют растительные остатки своих растений-хозяев в высокой плотности сразу после уборки урожая, тогда как R. beticola и S. beticola в поле практически отсутствовали. В течение нескольких месяцев количество доступных остатков хозяина значительно сокращалось, а концентрация патогенов в оставшихся остатках резко снижалась. Альтернативные субстраты — остатки нехозяев, включая покровные культуры и сорняки — сапрофитно колонизировались некротрофными патогенами A. solani и C. beticola. Можно сделать вывод, что остатки нехозяев потенциально могут служить важным мостом для популяций патогенов в безхозяинные вегетационные периоды в системах севооборота. Эти результаты способствуют разработке рациональных стратегий управления растительными остатками, направленных на профилактику болезней за счет снижения инокуляционного потенциала в системах севооборота.
1 Введение
Листовые болезни картофеля, вызываемые Alternaria solani Sorauer, и сахарной свеклы, вызываемые Cercospora beticola Sacc., Ramularia beticola Fautr. & Lamb, или Stemphylium beticola Woudenb. & Hanse, регулярно приводят к значительным потерям урожая (Abuley и др., 2018; Shane and Teng, 1992; Hanse и др., 2015). Для борьбы с этими болезнями обычно применяют несколько обработок фунгицидами за сезон (Jindo и др., 2021; Khan and Smith, 2005; Vereijssen и др., 2007). Описано, что A. solani поражает растения семейства пасленовых (Solanaceae), включая распространенные сорняки, такие как Solanum nigrum, а также непасленовые растения-хозяева из семейств астровых (Asteraceae) и бобовых (Fabaceae) (Woudenberg и др., 2014), дикую капусту (Brassica oleracea), огурец (Cucumis sativus) и циннию (Zinnia elegans) (обзор van der Waals и др., 2001). Спектр растений-хозяев для патогенов C. beticola, R. beticola и S. beticola также узок: сахарная свекла и другие маревые (Chenopodiaceae), включая распространенный сорняк Chenopodium album, однако для C. beticola и S. beticola в качестве хозяев описаны также несколько других родов растений (Hanse и др., 2015; Knight и др., 2019). Общим для всех четырех патогенов является их некротрофный образ жизни и жизненные циклы, которые включают выживание на растительных остатках в почве и на ее поверхности в периоды отсутствия растений-хозяев.
Роль остатков растений-хозяев в выживании популяций патогенов и как потенциальных источников инокулюма для последующих растений-хозяев была изучена для многих комбинаций патоген–хозяин. Примерами являются Venturia inaequalis на яблоне (MacHardy и др., 2001), токсигенные Fusarium spp. на кукурузе и пшенице (Cotton and Munkvold, 1998; Köhl и др., 2007; Mourelos и др., 2024), а также A. brassicicola, A. brassicae, Mycosphaerella brassicicola и Xanthomonas campestris pv. campestris на капусте (Humpherson-Jones, 1989; Köhl и др., 2011). Эти знания можно использовать для разработки стратегий управления растительными остатками с целью снижения выживаемости инокулюма и, следовательно, уменьшения количества первичного инокулюма патогенов в последующие вегетационные сезоны. Например, в яблоневых садах изучались физические, химические или биологические обработки перезимовавших яблоневых листьев для снижения выживаемости V. inaequalis в листовых остатках в течение зимы и для задержки начала эпидемий парши яблони весной (Gomez и др., 2007).
Растительные остатки зараженных культур можно рассматривать как основной субстрат для популяций патогенов, обеспечивающий их выживание в периоды отсутствия хозяина. Однако другие сапрофитные микроорганизмы будут конкурировать с патогенами за питательные вещества и пространство в остатках, и со временем остатки будут разлагаться. Сапрофитная колонизация остатков нехозяев или сорняков, присутствующих в поле, может обеспечить дополнительный путь для выживания патогена. Примером такой стратегии выживания является колонизация остатков нехозяев (сорняков и злаков) патогеном груши S. vesicarium, что приводит к значительному вкладу таких альтернативных источников инокулюма в эпидемии бурой пятнистости в грушевых садах (Rossi и др., 2008; Köhl и др., 2013). Mourelos и др. (2024) также наблюдали, что остатки сои служат резервуаром инокулюма для Fusarium graminearum, вызывающего фузариоз колоса пшеницы. Они обнаружили корреляции между количеством ДНК патогена, определенным в остатках сои, и количеством инокулюма, обнаруженным в предшествующей зерновой культуре, что предполагает сохранение инокулюма в полях и повышение вероятности развития инфекции.
Целью нашего исследования была задача внести вклад в разработку рациональных стратегий управления растительными остатками, направленных на профилактику болезней в системах севооборота. Колонизация остатков растений-хозяев A. solani, C. beticola, R. beticola и S. beticola была количественно оценена с использованием видеспецифичных ПЦР-анализов в реальном времени. Остатки нехозяев и покровных культур, выращиваемых в севообороте, а также сорняков и органического опада на поверхности почвы также были оценены для выяснения их роли в динамике популяций патогенов в периоды отсутствия хозяина в пахотных системах с севооборотом. Популяции патогенов измеряли на делянках поля с различными последовательностями культур в течение трех зимних сезонов, когда не выращивались основные культуры (за исключением озимого ячменя), с перерывами на отбор проб в течение двух соответствующих вегетационных сезонов. Это было выполнено на повторных делянках полевого опыта по севообороту с картофелем (1), озимым или яровым ячменем, сахарной свеклой (поздний сбор), морковью, картофелем (2), кукурузой, сахарной свеклой (ранний сбор) и луком, высеваемым весной, в севообороте в двух различных системах управления культурами: сравнивалась обычная практика в южных регионах Нидерландов с интегрированной стратегией управления культурами (ICM), основанной на минимизации химической защиты растений (Riemens и др., 2022).
2 Материалы и методы
2.1 Изоляты грибов
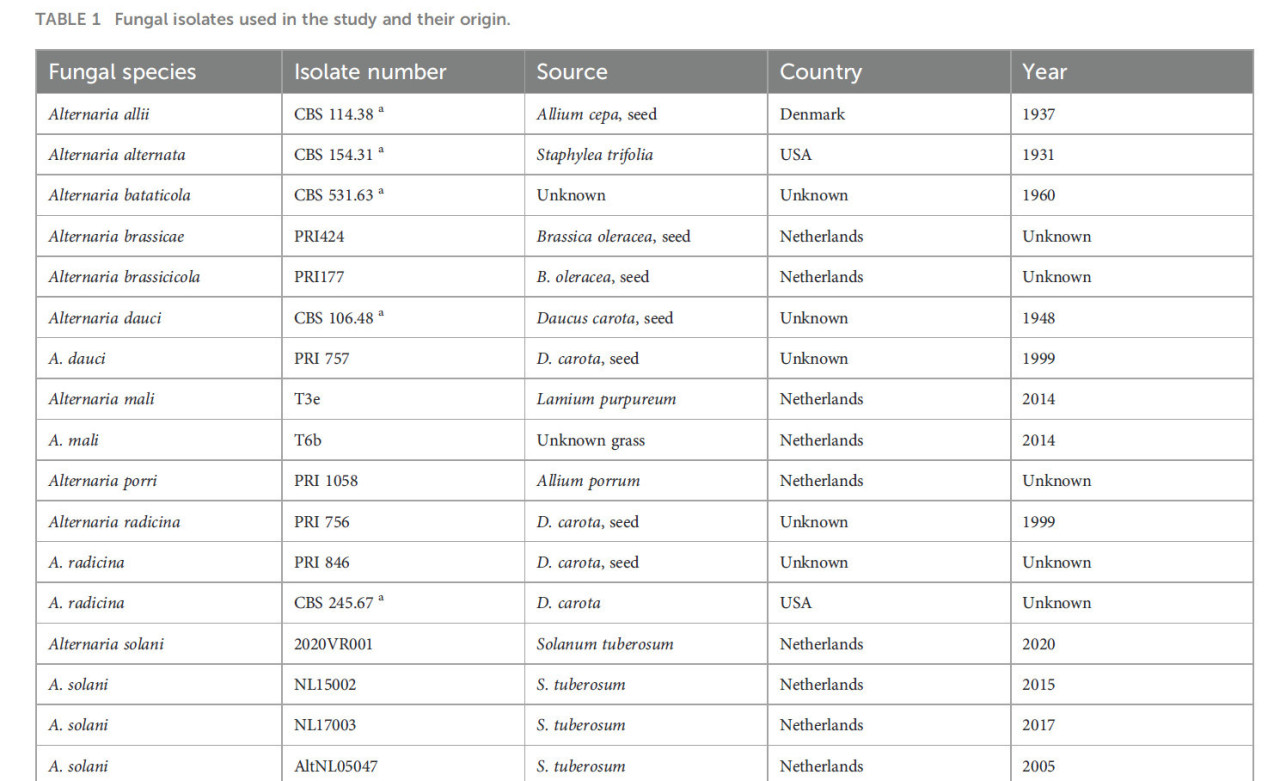
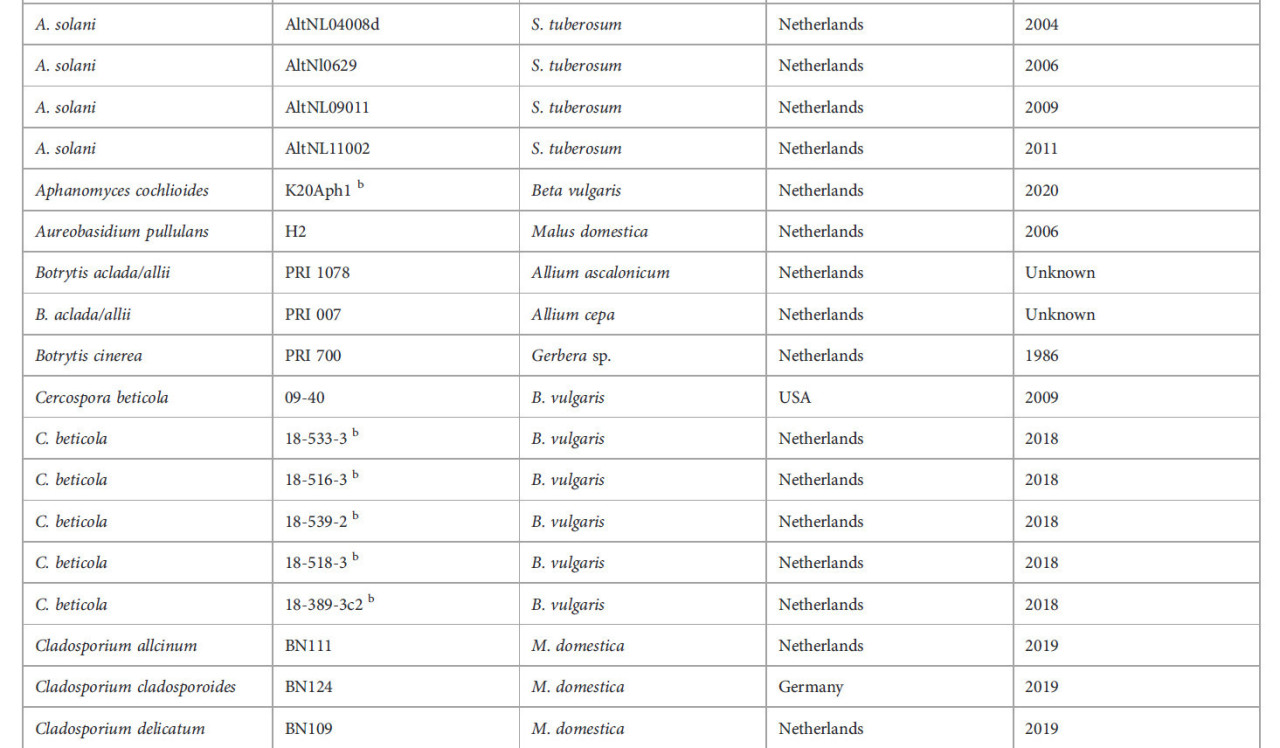
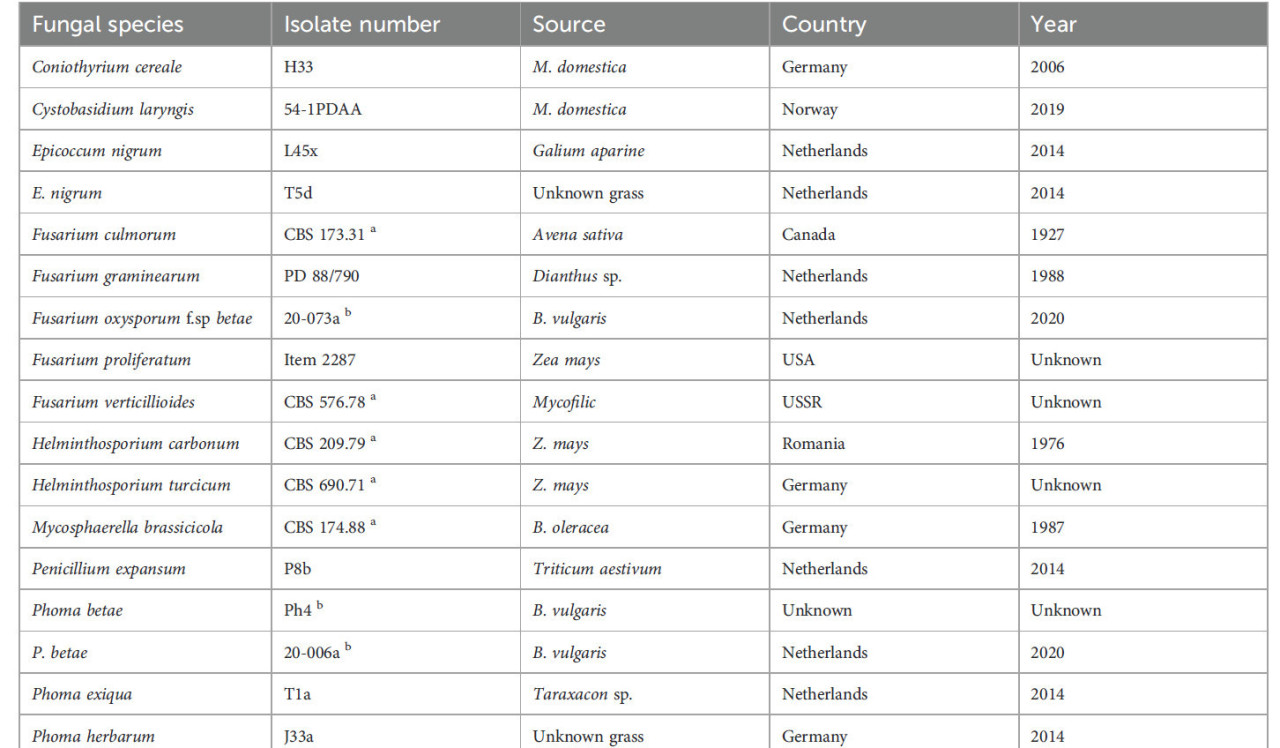
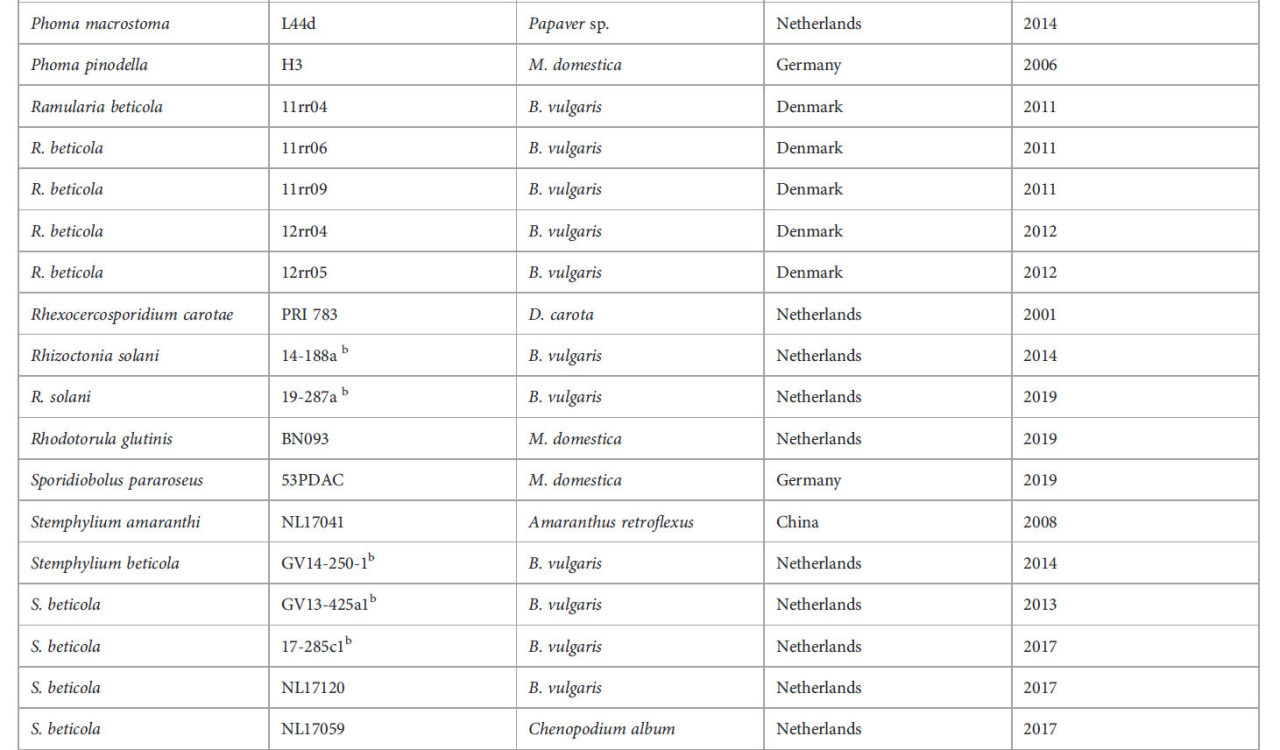
Изоляты грибов, использованные в исследовании, перечислены в Таблице 1. Если не указано иное, изоляты взяты из коллекции Университета Вагенингена и Исследовательского центра.
Таблица 1 – Изоляты грибов, использованные в исследовании, и их происхождение.
2.2 Эксперимент по севообороту
2.2.1 Дизайн эксперимента
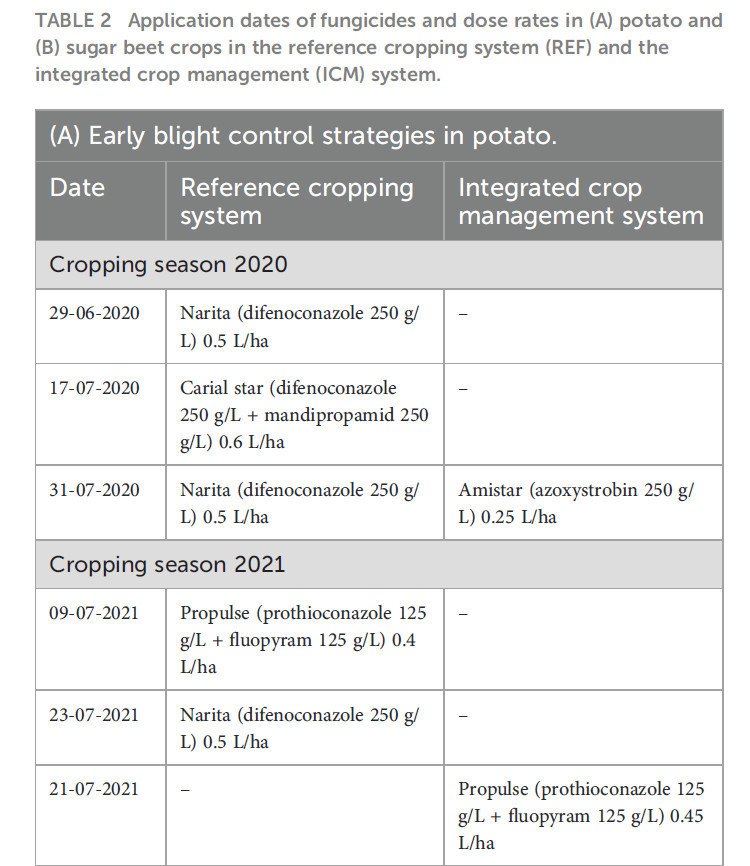
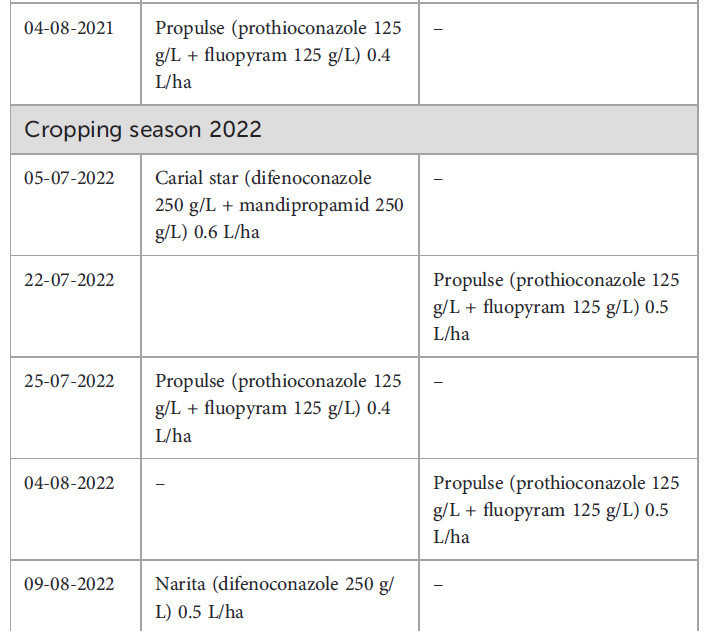
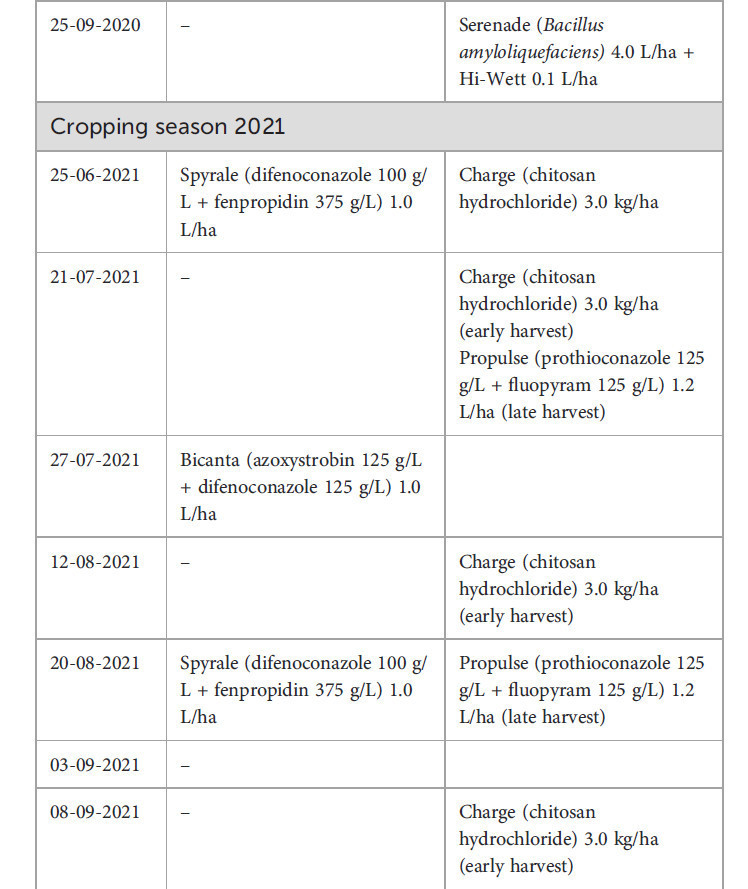
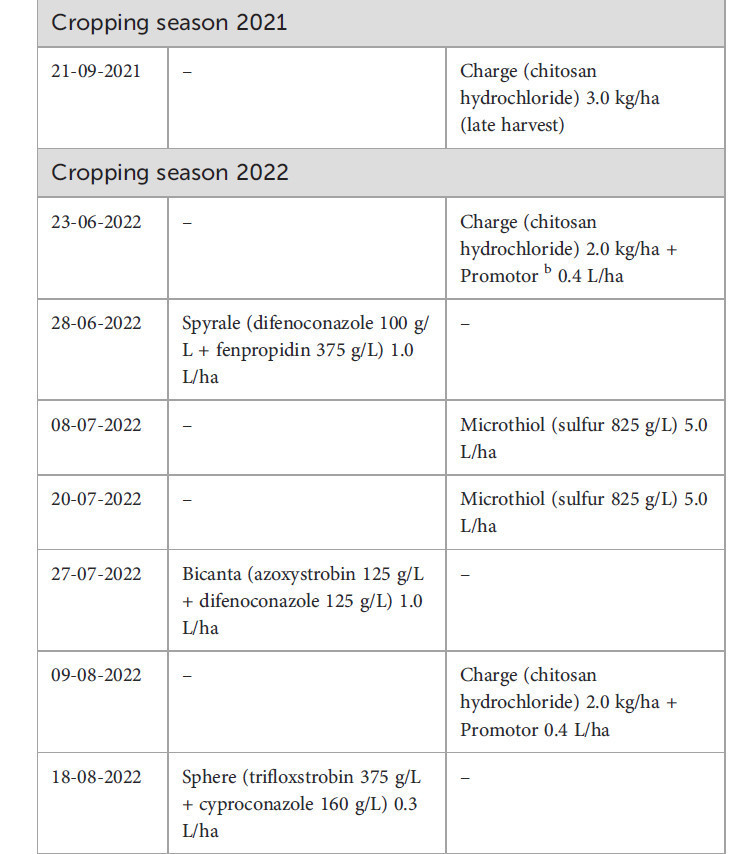
Полевой эксперимент начался в 2020 году в Университете Вагенингена и Исследовательском центре, Вредепел (51.54 с.ш.; 5.85 в.д.) на песчаной почве с содержанием органического вещества от 4.4% до 4.8%. Культуры выращивались в соответствии с двумя стратегиями защиты растений. Эталонная стратегия (REF) контролирует сорняки, вредителей и болезни в соответствии с обычной практикой в юго-восточном регионе Нидерландов. Стратегия ICM была основана на минимизации химической защиты растений и отказе от пестицидов, которые Европейским союзом перечислены как кандидаты на замену (CfS) (European Commission, 2015). Например, в системе ICM выращивались сорта картофеля с лучшей устойчивостью против фитофтороза (Phytophthora infestans) для минимизации применения пестицидов и отказа от флуопиколида (CfS). Поскольку дифеноконазол как CfS был недоступен для борьбы с альтернариозом, варианты были ограничены в первые годы. Для борьбы с церкоспорозом свеклы синтетические фунгициды были недоступны, так как все они содержали действующее вещество, включенное в список CfS. Подробная информация о применении фунгицидов на картофеле, направленном на борьбу с альтернариозом, и на сахарной свекле, направленном на борьбу с листовыми болезнями, приведена в Таблице 2.
Таблица 2 – Даты применения фунгицидов и нормы расхода на (A) картофеле и (B) сахарной свекле в эталонной системе земледелия (REF) и системе интегрированного управления культурами (ICM).
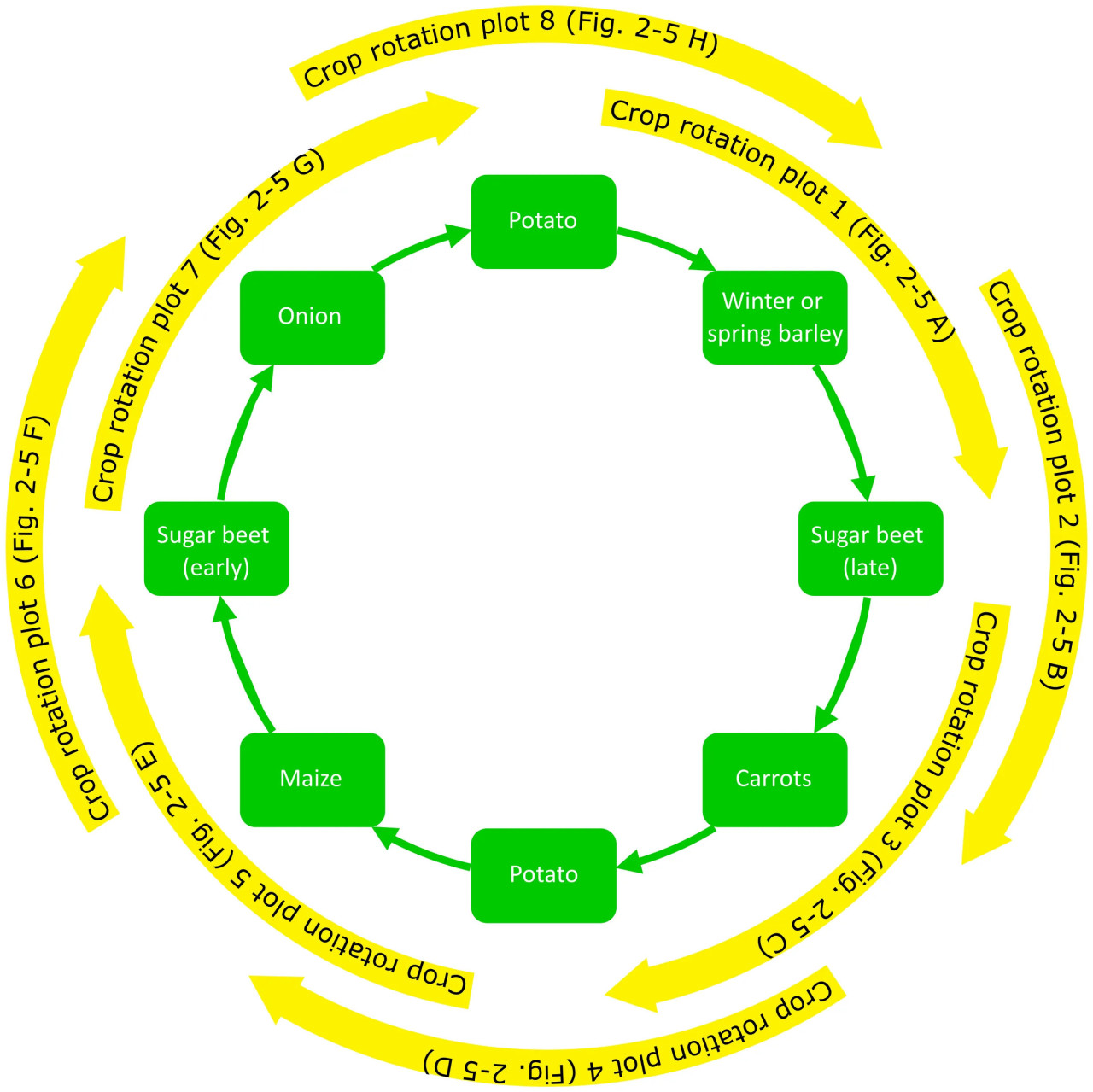
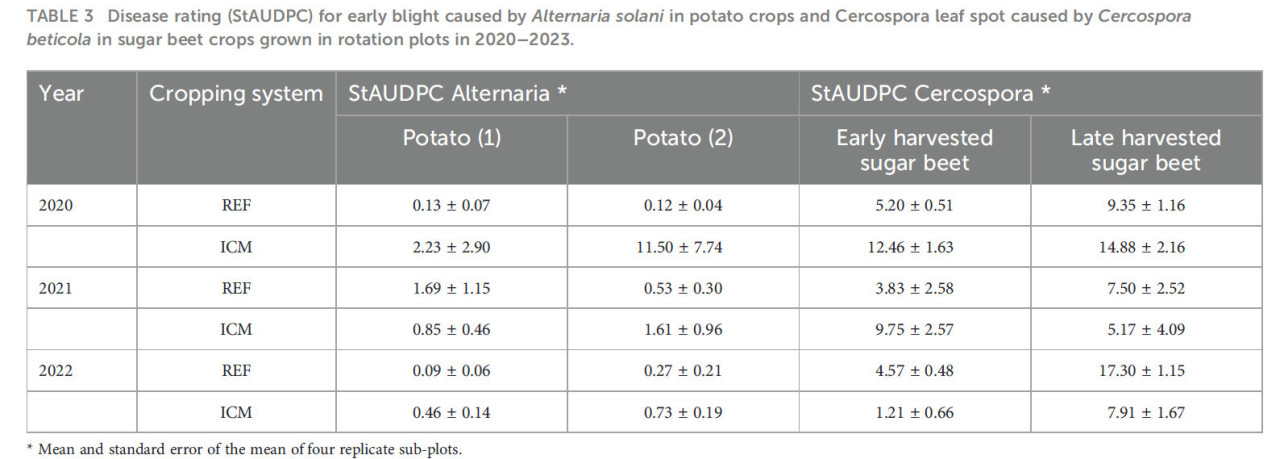
Выращиваемыми культурами были картофель, озимый или яровой ячмень, сахарная свекла, морковь, кукуруза и лук весеннего сева. Севооборот был восьмипольным, за исключением картофеля и сахарной свеклы, которые возделывались один раз в четыре года. Порядок чередования культур в обеих стратегиях был: картофель (1), озимый или яровой ячмень, сахарная свекла (поздний сбор), морковь, картофель (2), кукуруза, сахарная свекла (ранний сбор) и лук весеннего сева (Рисунок 1; Дополнительная таблица 1). Покровные культуры зависели от основных культур и стратегии защиты растений (Дополнительная таблица 1). Всего эксперимент состоял из четырех главных блоков (повторностей), каждый из которых был разделен на две делянки с различными системами земледелия, причем каждая делянка имела восемь субделянок для случайно распределенных культур (REF1–REF8; ICM1–ICM8). Размер субделянки составлял 24 м × 24 м. Степень развития альтернариоза картофеля и церкоспороза сахарной свеклы еженедельно оценивали визуально по шкале от 0% до 100% пораженной площади листьев. Площадь под кривой развития болезни (AUDPC) была рассчитана в соответствии с Madden и др. (2007) и стандартизирована путем деления на продолжительность эпидемии (дни). Полученные значения StAUDPC для картофеля и сахарной свеклы, выращенных в различных системах севооборота, показывает Таблица 3. Симптомы инфекций, вызванных R. beticola, не наблюдались на делянках с сахарной свеклой, и было обнаружено лишь несколько симптомов, типичных для инфекций S. beticola.
Рисунок 1 – Диаграмма, показывающая севооборот и периоды отбора проб на восьми делянках севооборота. Соответствующие результаты показаны на Рисунках 2–5.
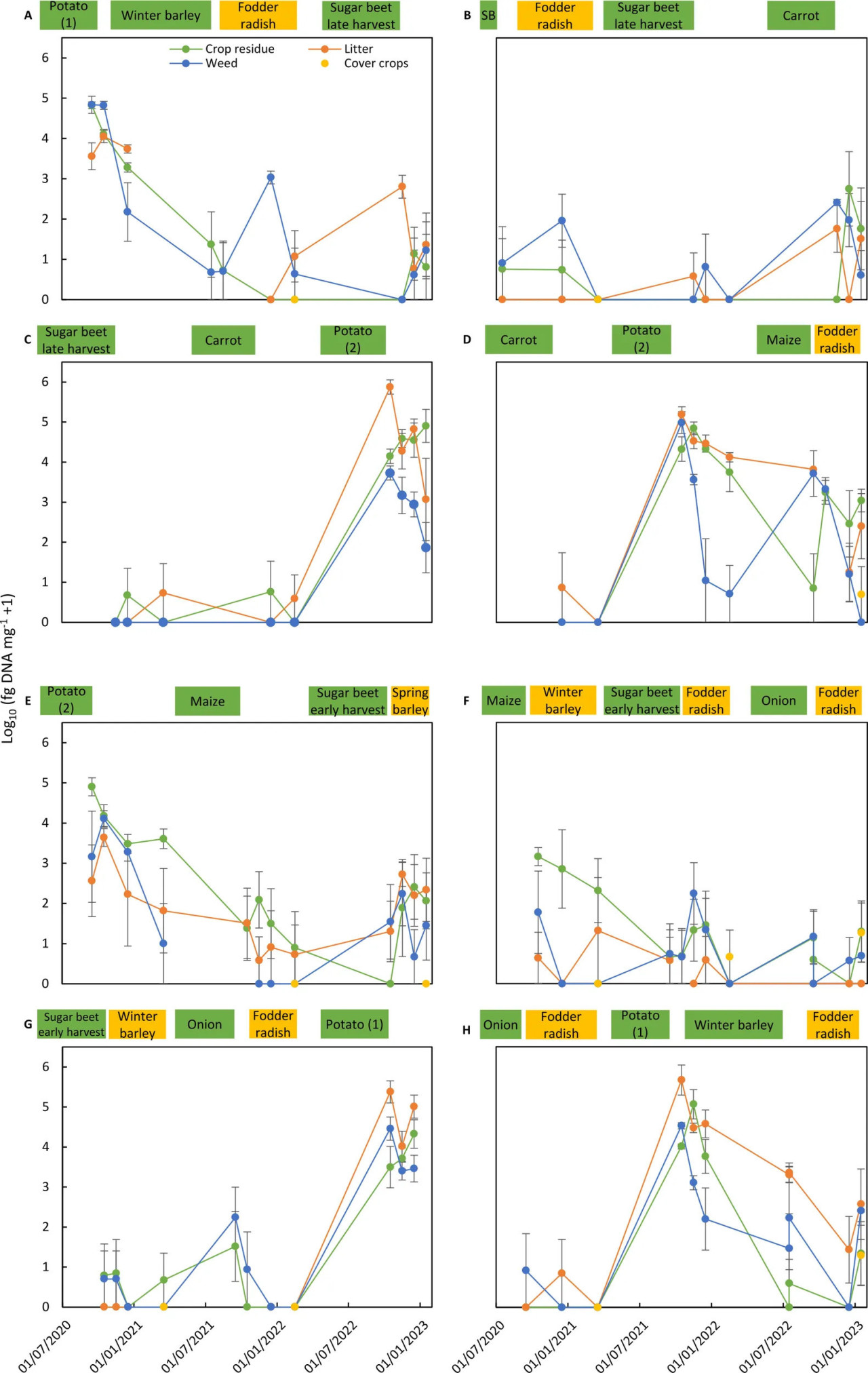
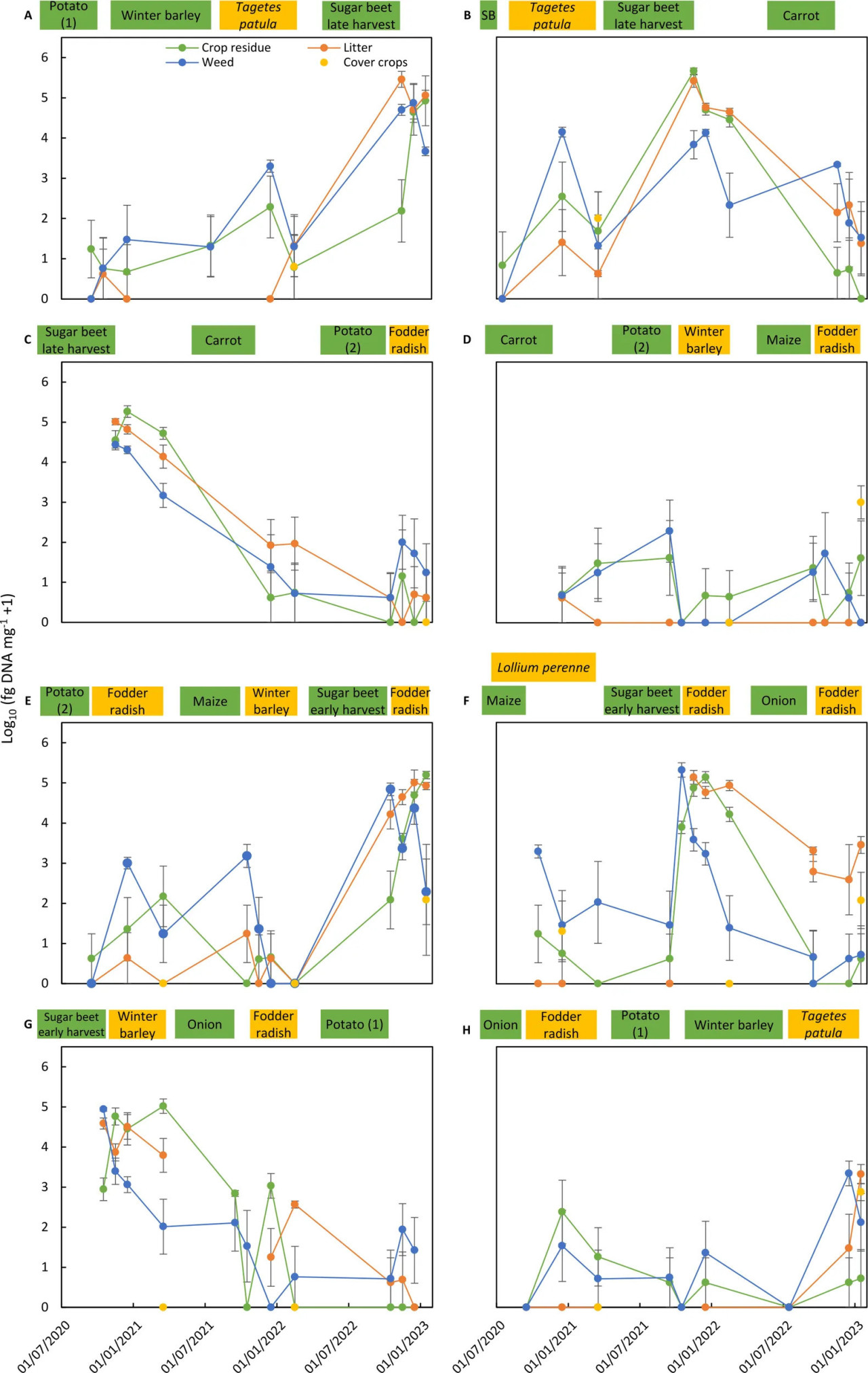
Рисунок 2 – Колонизация остатков основных культур, покровных культур, сорняков и опада грибом Alternaria solani на восьми делянках севооборота (A–H) эталонной системы земледелия (REF). Колонизация Alternaria solani выражена как среднее log10-преобразованных данных из четырех повторных субделянок (фг ДНК A. solani мг⁻¹ сухого материала – 1). Столбики соответствуют стандартной ошибке среднего. Периоды вегетации основных культур (зеленым цветом) и покровных культур (желтым цветом) на делянке севооборота показаны в верхней части каждого графика. SB на графике B означает яровой ячмень.
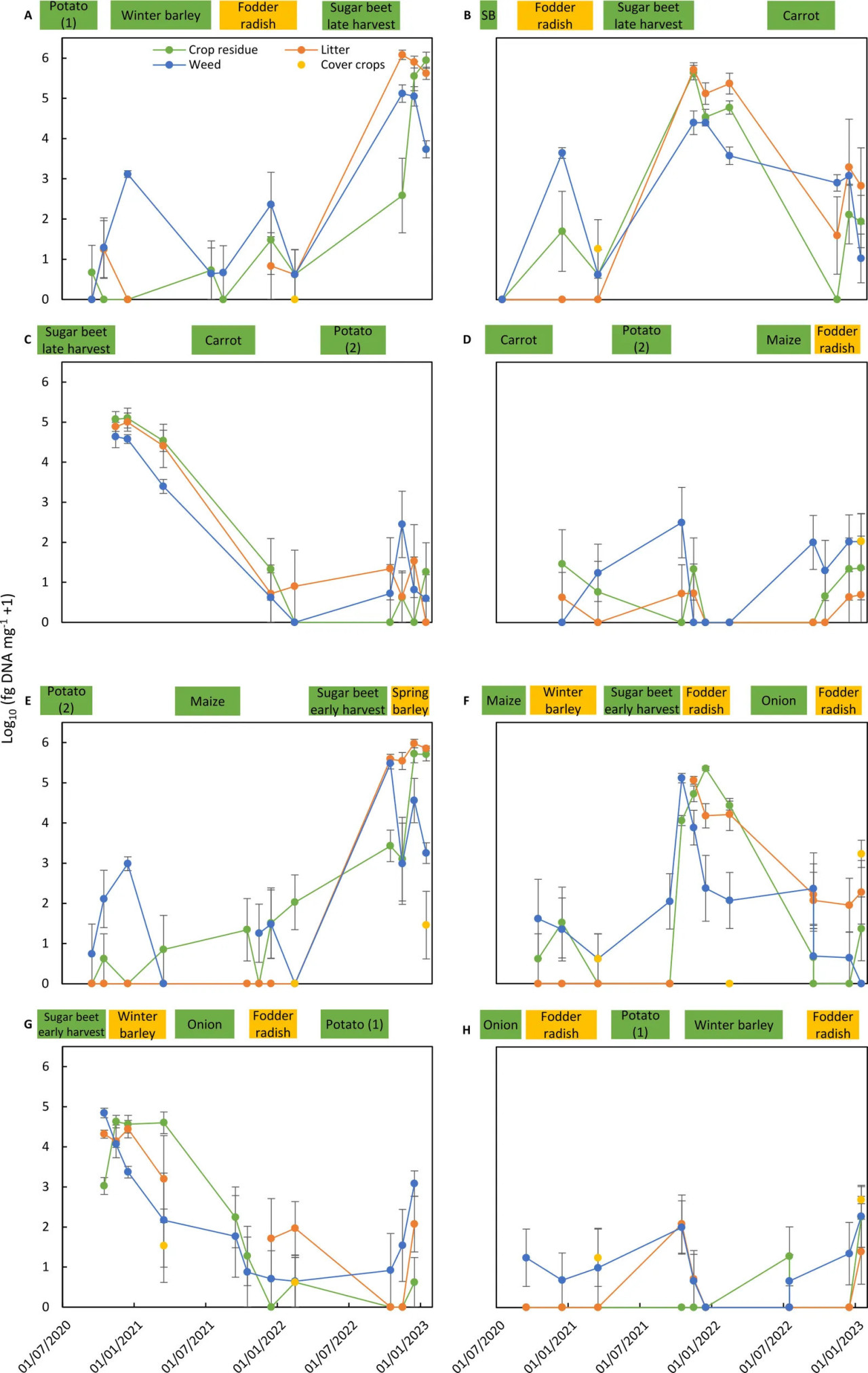
Рисунок 3 – Колонизация остатков основных культур, покровных культур, сорняков и опада грибом Cercospora beticola на восьми делянках севооборота (A–H) эталонной системы земледелия (REF). Колонизация Cercospora beticola выражена как среднее log10-преобразованных данных из четырех повторных субделянок (log10 фг ДНК C. beticola мг⁻¹ сухого материала + 1). Столбики соответствуют стандартной ошибке среднего. Периоды вегетации основных культур (зеленым цветом) и покровных культур (желтым цветом) на делянке севооборота показаны в верхней части каждого графика. SB на графике B означает яровой ячмень.
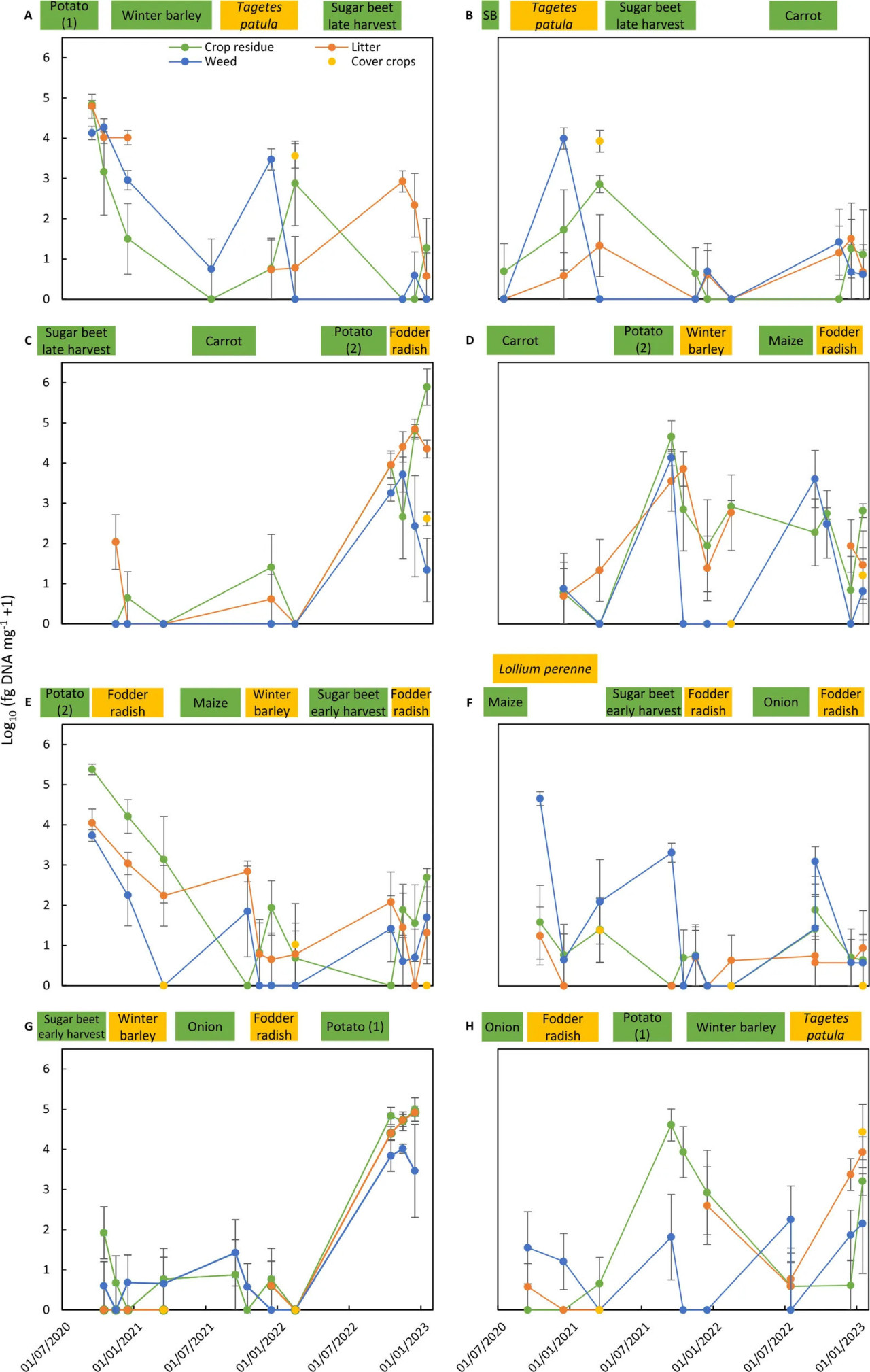
Рисунок 4 – Колонизация остатков основных культур, покровных культур, сорняков и опада грибом Alternaria solani на восьми делянках севооборота (A–H) системы интегрированного управления культурами (ICM). Колонизация Alternaria solani выражена как среднее log10-преобразованных данных из четырех повторных субделянок (log10 фг ДНК A. solani мг⁻¹ сухого материала + 1). Столбики соответствуют стандартной ошибке среднего. Период вегетации основных культур (зеленым цветом) и покровных культур (желтым цветом) на делянке севооборота показаны в верхней части каждого графика. SB на графике B означает яровой ячмень.
Рисунок 5 – Колонизация остатков основных культур, покровных культур, сорняков и опада грибом Cercospora beticola на восьми делянках севооборота (A–H) системы интегрированного управления культурами (ICM). Колонизация Cercospora beticola выражена как среднее log10-преобразованных данных из четырех повторных субделянок (log10 фг ДНК C. beticola мг⁻¹ сухого материала + 1). Столбики соответствуют стандартной ошибке среднего. Периоды вегетации основных культур (зеленым цветом) и покровных культур (желтым цветом) на делянке севооборота показаны в верхней части каждого графика. SB на графике B означает яровой ячмень.
Таблица 3 – Оценка болезни (StAUDPC) для альтернариоза (ранней гнили), вызываемого Alternaria solani на картофеле, и церкоспороза, вызываемого Cercospora beticola на сахарной свекле, выращенных на делянках севооборота в 2020–2023 гг.
Сорняки контролировались на различных культурах комбинацией механической борьбы и использования гербицидов, в зависимости от культуры, стадии развития культуры и стратегии борьбы (REF или ICM). Тем не менее, развитие сорняков никогда не контролировалось полностью, так что всегда была возможность отобрать образцы отмирающих сорняков.
2.2.2 Отбор проб растительных остатков
Остатки отбирали три или четыре раза за сезон в зависимости от выращиваемой культуры. Образцы отбирали: (1) сразу после уборки урожая; (2) примерно через 3 недели после уборки урожая, но до обработки почвы или посева последующей культуры; (3) в конце года, непосредственно перед наступлением зимы (если возможно); и (4) весной перед обработкой почвы, посадкой или посевом последующей культуры. В некоторых случаях 3 недели после уборки урожая совпадали с концом года. В этом случае на делянке в это время отбирали только один образец. Рисунок 1 иллюстрирует севооборот и периоды отбора проб на восьми различных делянках севооборота, а Дополнительная таблица 1 предоставляет обзор дат посева, дат уборки урожая и дат отбора проб на различных культурах.
Три различных типа растительных остатков отбирали с поверхности почвы в каждый период отбора проб: (1) легко узнаваемые остатки выращенной основной культуры или покровной культуры, (2) остатки сорняков и (3) опад, соскобленный небольшим лезвием вместе с небольшим количеством верхнего слоя почвы с поверхности земли. Отбирали только уже отмирающий растительный материал. Живой растительный материал не отбирали. Образцы отбирали с каждой делянки примерно на 20 различных участках, случайным образом распределенных по делянке. Между отборами проб на делянках использованные ножницы, ножи и маленькие лопатки очищали и дезинфицировали 70%-м спиртом для предотвращения загрязнения образцов между делянками. Размер образца с делянки варьировал, но обычно составлял не менее 10 г сырого веса. Образцы хранили при температуре −18°C в пластиковых пакетах.
2.2.3 Эксперимент по управлению растительными остатками
Растение картофеля сорта Фонтане (cv. Fontane), показывающее симптомы альтернариоза в конце сезона, было выбрано в качестве источника остатков листового аппарата картофеля для эксперимента. Процент пораженной поверхности листьев альтернариозом (степень развития болезни) составлял 7.5%. Остатки листового аппарата картофеля были собраны на стадии развития BBCH 95-97 19 августа 2020 г. Остатки были обработаны следующим образом: без обработки, нарезка на кусочки по 2 см секатором и нарезка на кусочки по 10 см. Для четвертой обработки остатки листового аппарата были собраны на полосе того же поля, где листовой аппарат был обработан измельчительной машиной Grimme KS 3000 (Damme, Germany) за 30 минут до сбора образцов. Сетчатые мешки (размером 25 × 30 см) заполняли subsamples остатков каждой из четырех обработок примерно по 250 г сырого веса на мешок. Всего было приготовлено 40 мешков на обработку, и они были помещены в поле, не занятое сельскохозяйственными культурами, в Университете Вагенингена и Исследовательском центре, Вредепел.
Было две основные делянки размером 3.1 × 4.8 м: одна с сетчатыми мешками, зарытыми горизонтально в почву на глубину 10 см, и одна с сетчатыми мешками, помещенными на поверхность почвы. Внутри каждой основной делянки было пять блоков (повторностей), каждый из которых состоял из четырех делянок с сетчатыми мешками, относящимися к четырем различным обработкам, полностью рандомизированным внутри блока. На каждой из делянок было размещено по четыре мешка с одинаковой обработкой на расстоянии 0.1 м между мешками. Один мешок случайным образом выбирался для каждого периода отбора проб: примерно каждые 6 месяцев, 15 апреля 2021 г., 23 сентября 2021 г., 29 апреля 2022 г. и 23 сентября 2022 г. Десять дополнительных образцов, каждый примерно по 250 г сырого веса, были взяты в начале экспериментов 19 августа 2020 г. из остатков листового аппарата, использованных для обработок 1–3, и 10 образцов с полосы поля, обработанной измельчителем. Все образцы хранились при температуре −20°C перед обработкой.
Эксперимент был повторен на том же поле. Образцы остатков листового аппарата были собраны 23 сентября 2021 г. с растения картофеля сорта Каммео (cv. Cammeo) на стадии развития BBCH 99. Симптомы альтернариоза были обнаружены на 5% поверхности листового аппарата 15 сентября 2021 г. Даты отбора проб мешков, содержащих остатки листового аппарата: 23 апреля 2022 г., 29 сентября 2022 г., 1 мая 2023 г. и 20 сентября 2023 г.
2.3 Обработка образцов
Замороженные полевые образцы растительных остатков основных культур, покровных культур и остатков сорняков, собранные в эксперименте по севообороту, были измельчены, и subsamples объемом примерно 150 мл были лиофилизированы с использованием установки Alpha 1-4 LSC basic (Martin Christ, Osterode am Harz, Germany). После этого высушенный материал был измельчен в порошок с использованием лабораторной мельницы CT 293 Cyclotec с ситом с ячейками 1 мм (Foss, Hillerød, Denmark) и хранился при температуре −20°C.
Замороженные образцы опада переносили в пластиковые стаканы объемом 1 л и добавляли 600 мл водопроводной воды. После полного оттаивания воду с образцом интенсивно перемешивали дезинфицированной металлической ложкой для создания водной смеси и оставляли на 1 час для полного насыщения и осаждения песка на дно. Надосадочную жидкость, содержащую большую часть опада, осторожно выливали через воронку, содержащую моно дурный фильтр (200 мкм). Выливание надосадочной жидкости прекращали до того, как частицы песка могли вытечь. Для увеличения выхода опада этот процесс повторяли один раз, на этот раз со временем осаждения 10 с. Остатки опада в моно дурном фильтре осторожно промывали водопроводной водой для удаления всех мелких частиц. Оставшийся опад собирали в пробирку Precellys объемом 15 мл (Bertin Technologies, Montigny-le-Bretonneux, France) и добавляли две бусины из нержавеющей стали размером 6.35 мм (Vanem, Hoek van Holland, The Netherlands). Пробирки с образцами опада лиофилизировали с использованием установки Epsilon 1-4 LSC plus (Martin Christ, Osterorde am Harz, Germany). Лиофилизированные образцы измельчали в порошок с использованием гомогенизатора Precellys Evolution Homogenizer (Bertin Technologies, Montigny-le-Bretonneux, France) при 6000 об/мин в течение 2 × 15 с с паузой 10 с. Измельченные образцы хранили при температуре −20°C.
Замороженные образцы остатков листового аппарата картофеля, собранные в экспериментах по управлению растительными остатками, переносили в пластиковые стаканы объемом 1 л и добавляли 600 мл водопроводной воды. После полного оттаивания воду с образцом интенсивно перемешивали дезинфицированной металлической ложкой для создания водной смеси. Всю смесь выливали на металлическое сито (размер ячейки 2.8 мм) и осторожно промывали водопроводной водой для удаления всех мелких частиц. Остатки сортировали, удаляя загрязнения, такие как сорняки, насекомые или материал, отличный от остатков картофеля. Оставшиеся остатки картофеля собирали, лиофилизировали с использованием Alpha 1-4 LSC basic и отмечали общий сухой вес. Наконец, образцы измельчали в порошок в лабораторной мельнице CT 293 Cycloteca с ситом с ячейками 1 мм и хранили при температуре −20°C.
2.4 Экстракция ДНК
2.4.1 Экстракция ДНК из изолятов грибов
Изоляты грибов выращивали на картофельно-декстрозном агаре (PDA) в течение 2 недель при 20°C в темноте, за исключением изолятов R. beticola, которые выращивали в течение 4 недель (Таблица 1). Мицелий и споры выращенных изолятов соскабливали с поверхности агара, лиофилизировали и разрушали с использованием TissueLyser II (Qiagen) и одной стальной бусины (диаметр 3.2 мм) в течение 30 с при 30 Гц. После разрушения к каждому образцу добавляли 200 мкл лизирующего буфера из набора Sbeadex maxi plant kit (LGC, 175 Teddington, UK), и дальнейшую экстракцию ДНК проводили автоматически в соответствии с протоколом, предоставленным производителем, с использованием робота-пипетера KingFisher™ Flex Purification System (Thermo Fisher Scientific, Waltham, MA, USA). Концентрацию ДНК измеряли с использованием PicoGreen в планшетном ридере для флуоресценции (TECAN).
2.4.2 Экстракция ДНК из образцов растительных остатков
ДНК экстрагировали из взвешенных лиофилизированных и измельченных образцов растительных остатков (примерно 50 мг) с использованием набора Sbeadex maxi plant kit в соответствии с протоколом производителя со следующими модификациями: лизис проводили при 65°C в течение 1 часа с 700 мкл лизирующего буфера, и после центрифугирования 200 мкл супернатанта использовали в последующем протоколе. Для автоматизации экстракции использовали робота-пипетера KingFisher™ Flex Purification System. Экстракты ДНК хранили при температуре −20°C.
2.5 Разработка видоспецифичных Taqman ПЦР-анализов в реальном времени
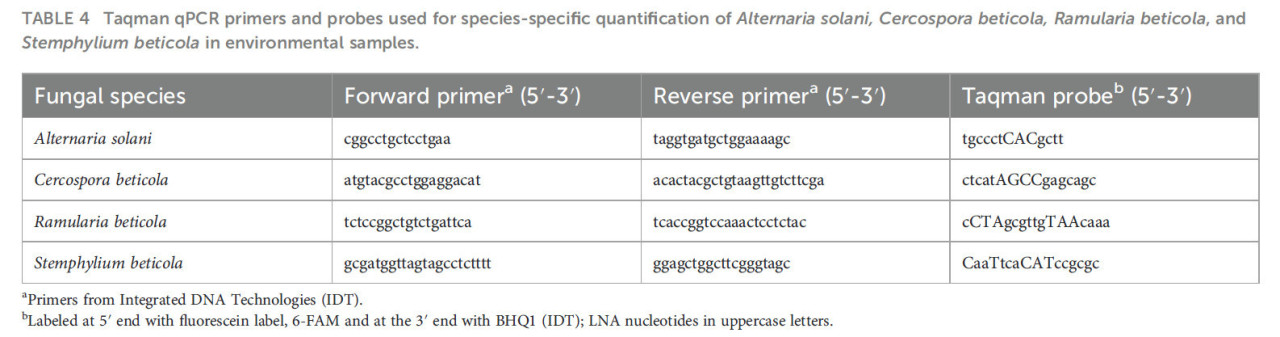
Было разработано четыре различных Taqman ПЦР-анализа в реальном времени для обнаружения и количественного определения A. solani, C. beticola, R. beticola и S. beticola. Для дизайна праймеров и зондов были выполнены выравнивания с помощью CLC genomics workbench 12.0 (CLC bio, Denmark) на основе последовательностей целевых и нецелевых Alt a 1 от Woudenberg и др. (2014) для A. solani, последовательностей gapdh от Bakhshi и др. (2018) для C. beticola, последовательностей ITS от Videira и др. (2016) для R. beticola и последовательностей cmdA от Woudenberg и др. (2017) для S. beticola. Видоспецифичные праймеры и зонд были разработаны с использованием CLC genomic workbench и primer express v.3.0 (Thermo Fisher Scientific, USA).
Специфичность разработанных Taqman ПЦР-анализов in silico была сначала протестирована с использованием поиска blastn в NCBI и, в случае специфичности, разработанные праймеры и зонд были оценены с синтетической ДНК и с 1 нг ДНК всех целевых и нецелевых грибов, перечисленных в Таблице 1. Анализ считался специфичным, если для нецелевых грибов не было реакций или значения Ct были выше, чем значение Ct для целевого гриба при самой низкой концентрации динамического диапазона TaqMan ПЦР. Чувствительность была определена с помощью 10-кратных серийных разведений от 1 нг до 10 фг для пяти повторностей изолята A. solani 2020Vr001, C. beticola 18-539-2, R. beticola 11rr04 и S. beticola 14-250-1.
2.6 Taqman ПЦР-анализы в реальном времени
Отдельные ПЦР-анализы в реальном времени проводили в 384-луночном формате в системе детекции ПЦР в реальном времени CFX 384 (Bio-Rad) для количественного определения A. solani, C. beticola, R. beticola, S. beticola и зеленого флуоресцентного белка (GFP), служащего контролем амплификации (AC) (Klerks и др., 2004). Для каждой TaqMan ПЦР 1 мкл образца смешивали с 9 мкл реакционной смеси, содержащей 5 мкл 2× PerfeCTa Toughmix no ROX (Quantabio), 100 нМ зонда и 300 нМ каждого прямого и обратного праймера (Таблица 4). Для C. beticola использовали 150 нМ зонда. Условия реакции были следующими: 95°C в течение 2 мин, 40 циклов: 95°C в течение 15 с, затем 60°C в течение 60 с.
Таблица 4 – Праймеры и зонды Taqman ПЦР в реальном времени, используемые для видоспецифичного количественного определения Alternaria solani, Cercospora beticola, Ramularia beticola и Stemphylium beticola в образцах окружающей среды.
10-кратная серийная разбавленная серия геномной ДНК была включена в каждую 384-луночную пластину для калибровки. Концентрации экстрагированной ДНК патогена в образцах были рассчитаны по пороговым значениям производного цикла (значения Ct) TaqMan ПЦР для серий разведения ДНК и для экстрактов ДНК растительных образцов и выражены как фг ДНК патогена на мг растительного остатка (сухой вес).
2.7 Статистический анализ
Для эксперимента по севообороту были рассчитаны средние значения и стандартные ошибки средних для четырех повторностей для log10-преобразованных концентраций ДНК [фг ДНК патогена на мг растительного остатка (сухой вес)] A. solani, C. beticola, R. beticola и S. beticola для каждой даты отбора проб для различных типов растительных остатков, полученных для каждой комбинации культура–система земледелия в эксперименте по севообороту.
Для эксперимента по управлению растительными остатками были рассчитаны средние значения и стандартные ошибки средних для повторностей (10 повторностей в начале экспериментов и 5 повторностей для каждой даты отбора проб) для log10-преобразованных концентраций ДНК A. solani (выраженных как log10 фг ДНК A. solani мг⁻¹ сухого материала +1) в каждом эксперименте для каждой даты отбора проб, обработки и размещения (на поверхности почвы/зарыто в почву). ДНК A. solani также была рассчитана как log10-преобразованные концентрации ДНК, оставшиеся в исходных образцах, помещенных в мешок (выраженные как пг ДНК A. solani в остатках 1 г сухого материала в начале эксперимента + 1). Разложение было выражено как средние значения и стандартные ошибки средних процента разложившегося сухого веса на каждую дату отбора проб по сравнению с началом экспериментов.
Статистический анализ для эксперимента по управлению растительными остатками был выполнен с использованием программного обеспечения R версии 4.0.3 (R Core Team, 2020). Для анализа использовали линейные смешанные модели, реализованные в пакете R версии 3.1-3 lmerTest (Kuznetsova и др., 2017). Откликами в анализе были соответственно процент разложившегося сухого веса, log10-преобразование ДНК A. solani (фг ДНК A. solani мг⁻¹ сухого материала +1) и log10-преобразование ДНК A. solani, присутствующей в остатках исходных образцов, помещенных в мешки [выраженное как пг исходной ДНК A.s. г⁻¹ листового остатка (сухой вес)]. Допущения базовой модели были проверены с помощью диагностических графиков. Чтобы включить исходное количество обоих откликов ДНК в начале экспериментов, отклики были преобразованы в разницу между средним количеством в начале и фактически измеренным количеством в четыре даты отбора проб. Процент разложившегося сухого веса анализировался как есть. Модель включала обработку, а также размещение как номинальные переменные в фиксированной части модели. Кроме того, четыре времени отбора проб были включены как фактор в модель. Изначально модель(и) также включали взаимодействия между этими тремя факторами. Однако они были сокращены до более экономной модели, когда (некоторые или все) взаимодействия значительно не вносили вклад в модель. Случайная часть модели(ей) учитывает коррекции для экспериментального дизайна и контролирует вариацию, связанную с экспериментами и блоками, вложенными в эксперименты.
3 Результаты
3.1 Специфичность и чувствительность Taqman ПЦР-анализов в реальном времени
Праймеры и зонды, разработанные для количественного определения A. solani, C. beticola, R. beticola или S. beticola, приведены в Таблице 4. Специфичность четырех ПЦР-анализов в реальном времени была оценена in silico с помощью поиска blastn (https://www.ncbi.nlm.nih.gov/BLAST). ДНК растений-хозяев Solanum tuberosum (биосэмпл SAMN02981305) и Beta vulgaris subsp. vulgaris (биосэмпл SAMN23167344) не могла быть обнаружена различными праймерами и зондами. Поиск BLAST видоспецифичных праймеров и зондов R. beticola и S. beticola дал 100% совпадение с соответствующей целью и отсутствие совпадений с наиболее близкородственными видами. В отличие от этого, праймеры и зонд для обнаружения A. solani не были специфичны к целевому виду, но также обнаруживали A. alternariacida sp. nov, A. catananches sp. nov., A. cichorii, A. conidiophora, A. dichondrae, A. grandis, A. linicola и A. protenta. Для C. beticola также было 100% совпадение с C. plantaginis.
Специфичность четырех разработанных Taqman ПЦР-анализов в реальном времени была подтверждена с использованием синтетической ДНК целей и филогенетически наиболее близких нецелевых объектов и геномной ДНК (1 нг) изолятов, перечисленных в Таблице 1. Положительные результаты Taqman ПЦР были получены для соответствующего анализа со всеми восемью целевыми изолятами A. solani, шестью C. beticola, пятью R. beticola или пятью S. beticola. Для нецелевых гифальных грибов и дрожжей, перечисленных в Таблице 1, значения Ct были выше 40 или выше значений Ct самой низкой концентрации цели (см. ниже). Калибровочные кривые, каждая из которых состояла из пяти повторных серий разведений ДНК своей цели, использовались для определения чувствительности. Линейность, эффективность и предел обнаружения были оценены по стандартным кривым для A. solani 2020VR001, C. beticola 18-539-2 и S. beticola GV14-250-1 в диапазоне от 1000 до 0.1 пг геномной ДНК на реакцию и от 1000 до 0.01 пг для R. beticola 11rr04 (Дополнительный рисунок 1).
3.2 Популяционная динамика Alternaria solani, Cercospora beticola, Ramularia beticola и Stemphylium beticola в растительных остатках в системах севооборота
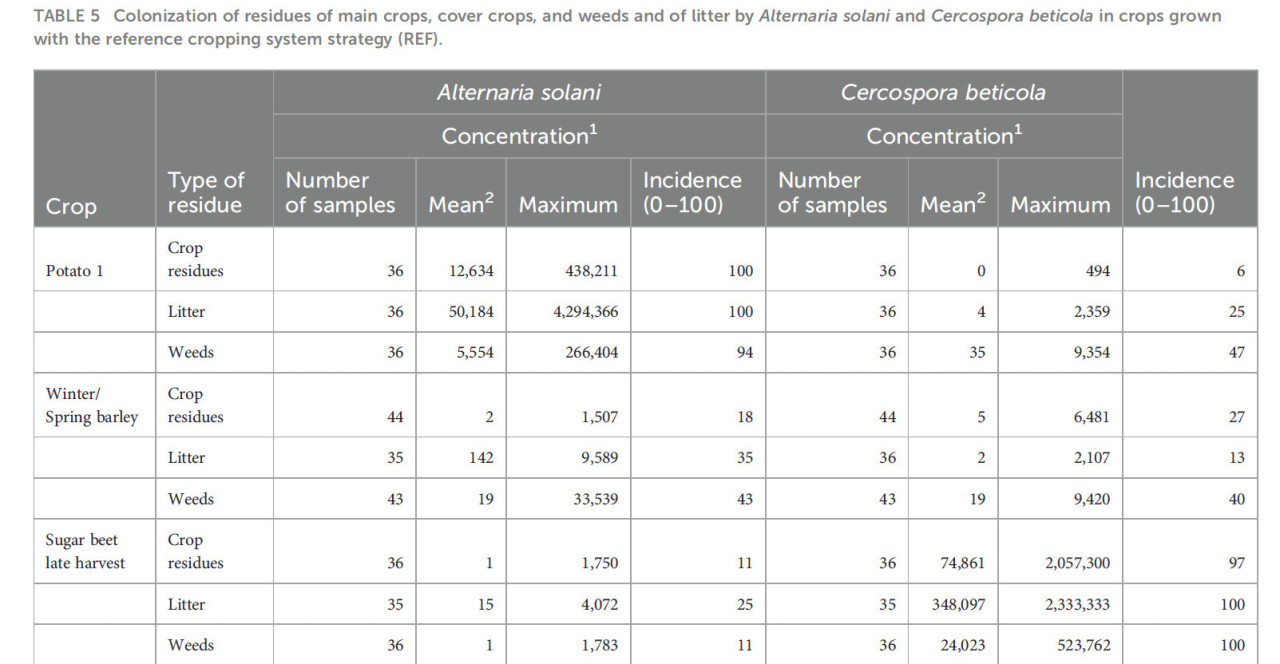
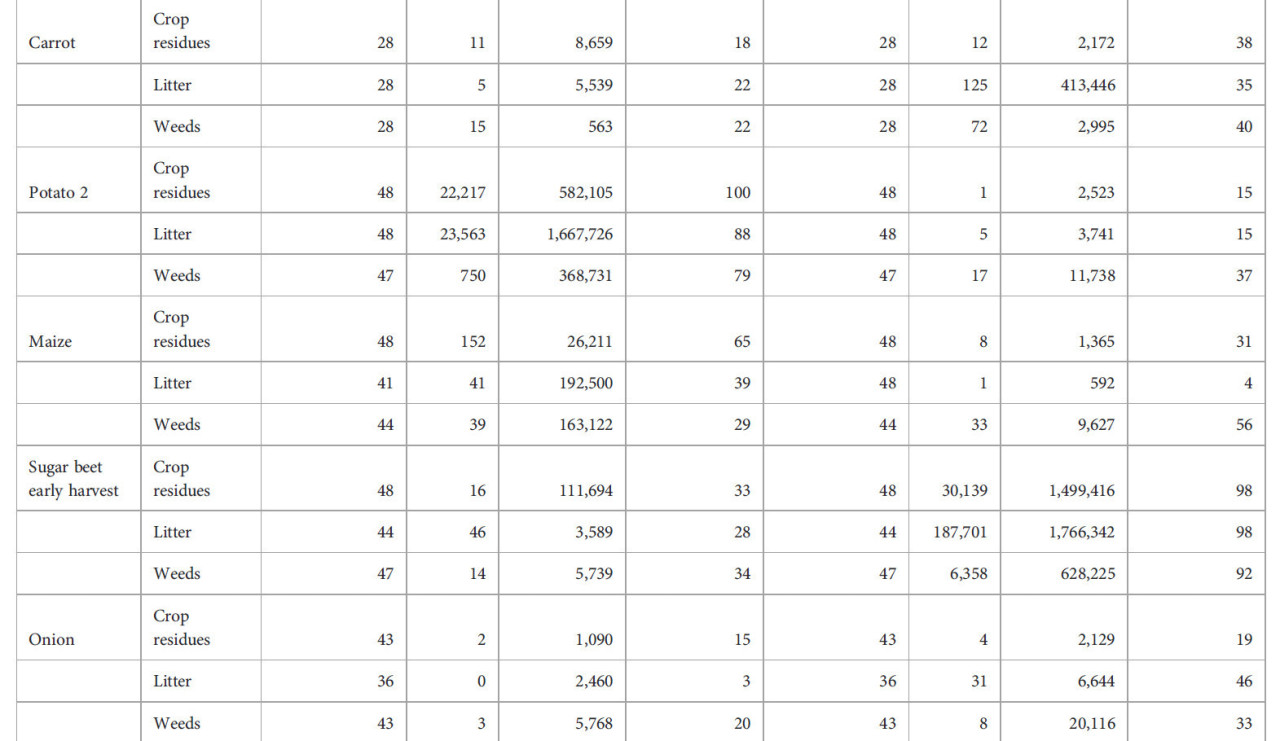
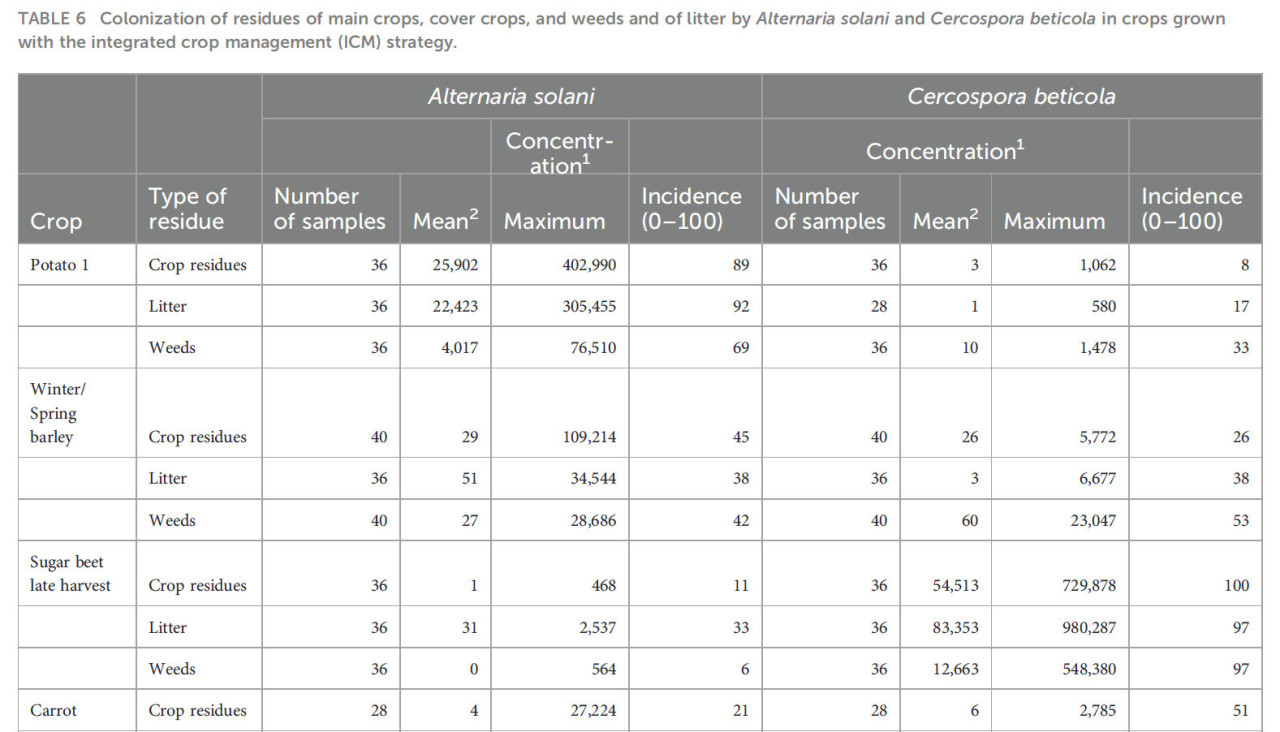
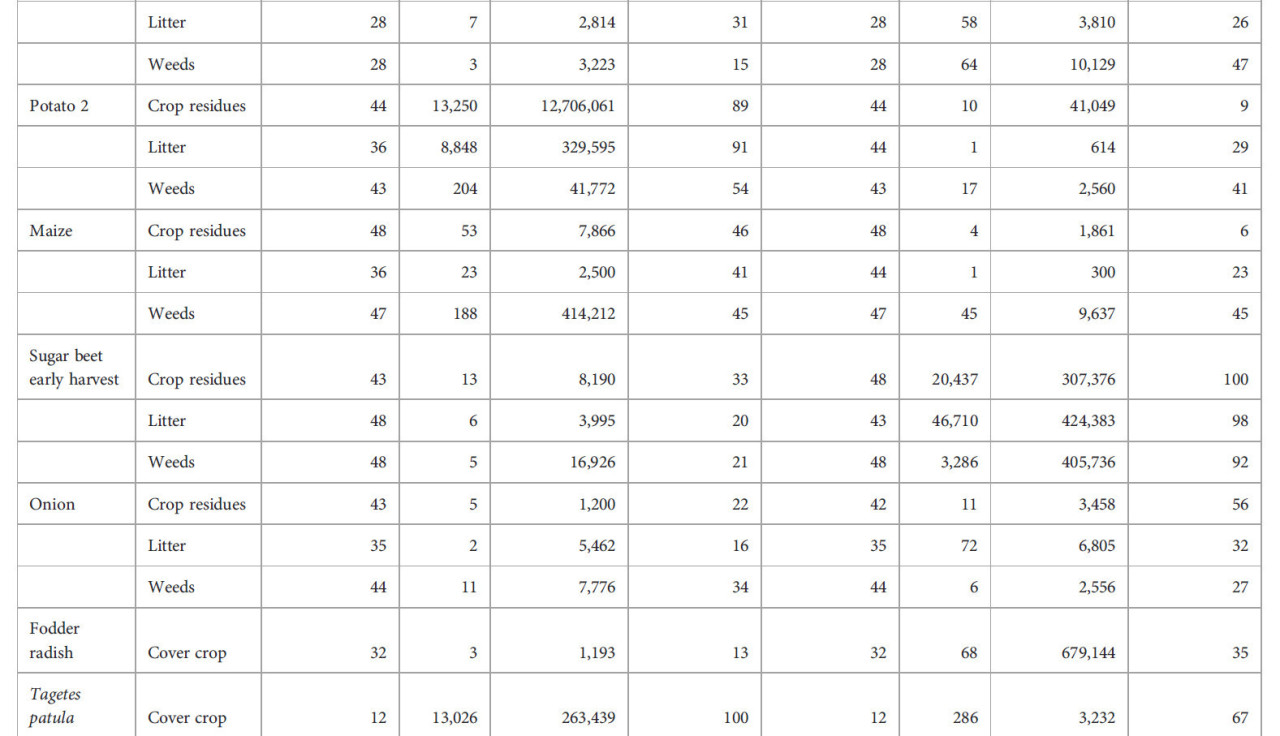
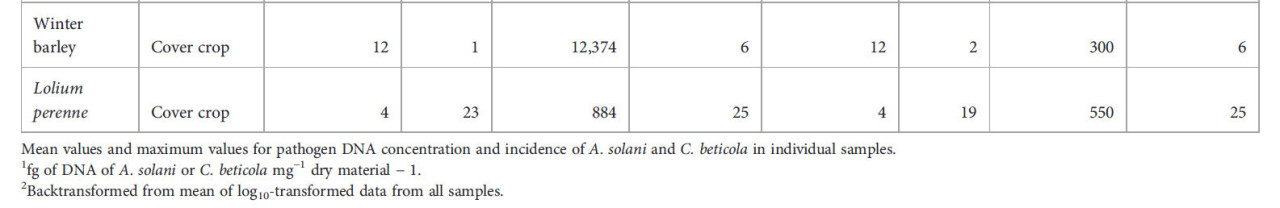
Alternaria solani стабильно обнаруживалась в 80%–100% оцененных образцов остатков двух картофельных культур в высоких концентрациях выше 10 000 фг ДНК A.s. мг⁻¹ (Таблицы 5, 6). Патоген также стабильно обнаруживался в опаде на поверхности почвы после картофеля. Образцы остатков сорняков, собранные после картофеля, на 50%–80% содержали A. solani, но колонизация была ниже по сравнению с концентрациями патогена, присутствующими в остатках картофеля. Частота встречаемости A. solani, определяемая как процент образцов с положительным обнаружением целевого патогена, в образцах растительных остатков ячменя, сахарной свеклы, моркови, кукурузы или лука составляла от 10% до 60%, а средние концентрации патогена были на три-четыре порядка ниже по сравнению с концентрациями в остатках картофеля, собранных в течение первых месяцев после уборки картофеля. Аналогичная картина наблюдалась в остатках сорняков и образцах опада, полученных с тех же делянок. Максимальные концентрации указывают на то, что в исключительных случаях растительные остатки, остатки сорняков или опад с делянок, на которых выращивался не картофель, а другие культуры, содержали A. solani в высоких концентрациях от 1000 до 100 000 фг ДНК A.s. мг⁻¹. В остатках редьки масличной, озимого ячменя и Lolium perenne, выращенных в качестве покровных культур, частота встречаемости A. solani в образцах составляла 25% или ниже, лишь в нескольких случаях концентрации превышали 100 фг ДНК A.s. мг⁻¹. Ярким исключением были остатки Tagetes patula, выращенной в качестве покровной культуры после озимого или ярового ячменя в системе ICM. A. solani была обнаружена во всех образцах остатков T. patula с высокой средней концентрацией 13 000 фг ДНК A.s. мг⁻¹, аналогичной концентрациям, измеренным в остатках картофеля.
Таблица 5 – Колонизация остатков основных культур, покровных культур, сорняков и опада грибами Alternaria solani и Cercospora beticola на культурах, выращенных по стратегии эталонной системы земледелия (REF).
Таблица 6 – Колонизация остатков основных культур, покровных культур, сорняков и опада грибами Alternaria solani и Cercospora beticola на культурах, выращенных по стратегии интегрированного управления культурами (ICM).
Аналогичная картина, как для A. solani на картофеле, была обнаружена для C. beticola на сахарной свекле раннего или позднего сбора (Таблицы 5, 6). Частота встречаемости C. beticola составляла >90% в остатках сахарной свеклы, остатках сорняков и опаде, собранных на делянках после уборки сахарной свеклы. Концентрации ДНК патогена обычно были в два раза выше на делянках, где сахарная свекла была убрана поздно, по сравнению с ранней уборкой сахарной свеклы. Концентрации в опаде достигали уровней, аналогичных или превышающих уровни в остатках сахарной свеклы. В образцах, полученных с делянок с ячменем, морковью, картофелем, кукурузой или луком, частота встречаемости C. beticola составляла от 4% до 56%, а концентрации были на три-четыре порядка ниже по сравнению с концентрациями, измеренными в остатках с делянок сахарной свеклы. Исключительно высокие концентрации ДНК C. beticola были обнаружены в отдельных образцах сорняков, собранных на культурах, выращиваемых в севообороте с сахарной свеклой. Концентрации выше 10 000 фг ДНК C. beticola мг⁻¹ сухого материала также были обнаружены в отдельных образцах растительных остатков, собранных на делянках с редькой масличной в качестве покровной культуры.
Ramularia beticola была обнаружена в 64 из 168 образцов остатков сахарной свеклы при средних концентрациях 94 фг ДНК R.b. мг⁻¹ (обратно преобразованные значения) и в 60 из 577 образцов остатков других культур в среднем 1 фг ДНК R.b. мг⁻¹. Stemphylium beticola была обнаружена в 39 из 168 образцов остатков сахарной свеклы при средней концентрации 14 фг ДНК S.b. мг⁻¹ и в 25 из 612 образцов остатков других культур при средней концентрации 3 фг ДНК S.b. мг⁻¹. В опаде R. beticola была обнаружена в 65 из 659 образцов (средняя концентрация 28 фг ДНК R.b. мг⁻¹), а S. beticola была обнаружена в 64 из 659 образцов (средняя концентрация 35 фг ДНК S.b. мг⁻¹). В сорняках R. beticola была обнаружена в 66 из 701 образца (средняя концентрация 13 фг ДНК R.b. мг⁻¹), а S. beticola была обнаружена в 39 из 701 образца (средняя концентрация 2 фг ДНК S.b. мг⁻¹).
Динамика колонизации патогенами в течение 2.5 лет в остатках основных культур, покровных культур и сорняков, а также в опаде, присутствующем на четырех повторных субделянках, показана для всех делянок севооборота обеих систем управления культурами для A. solani (Рисунки 2, 4) и C. beticola (Рисунки 3, 5). Рисунки также включают информацию о периодах вегетации основных культур и покровных культур до и в течение 2.5-летнего периода отбора проб и временных точках отбора проб остатков (подробности см. в Дополнительной таблице 1).
Основные тенденции, обобщенные в Таблицах 5, 6, показаны, такие как высокие концентрации патогенов в остатках их растений-хозяев, сорняков и опаде, собранных на делянках в течение месяцев после уборки урожая растения-хозяина. Снижение концентрации A. solani до двух порядков в течение нескольких месяцев после уборки картофеля было обнаружено в большинстве случаев, тогда как отсутствие снижения или даже увеличение колонизации на один-два порядка в течение месяцев после уборки наблюдалось в двух случаях (Рисунки 2C, G). Эти закономерности на делянках после возделывания картофеля были аналогичны для остатков картофеля, а также для остатков сорняков и опада. Аналогичное быстрое снижение было также обнаружено для C. beticola в остатках сахарной свеклы, сорняков и опаде, собранных на делянках в течение месяцев после уборки растения-хозяина.
В периоды отбора проб, следующие за нехозяевами, концентрации A. solani были на порядки ниже, чем обнаруженные в образцах, собранных после возделывания картофеля, и наблюдаемая картина была непостоянной. Значения колебались между датами отбора проб, между повторными делянками (что приводило к большей стандартной ошибке средних) и между типами субстрата. Несмотря на противоречивые результаты для различных отдельных оценок, общая закономерность наблюдалась для всех периодов отбора проб, следующих за периодами возделывания культур-нехозяев: A. solani присутствовала на всех делянках (на низких уровнях) в периоды отсутствия растений-хозяев. Наибольшая вариабельность, включая偶尔 более высокие значения концентраций A. solani, была обнаружена в остатках сорняков, что указывает на то, что некоторые сорняки, присутствующие на культурах-нехозяевах, могут функционировать как хозяева для A. solani. Аналогичная картина была обнаружена для концентраций C. beticola на делянках без хозяина с колеблющимися значениями между датами отбора проб, повторными делянками и типами субстрата, с наибольшей вариабельностью и наиболее высокими значениями в образцах сорняков.
Патогены показывали одинаковое поведение в обеих системах управления культурами (Рисунки 2–5). Аналогичные уровни колонизации и аналогичные закономерности в популяционной динамике были обнаружены за исключением периодов с ростом T. patula в системе ICM. A. solani достигала высоких концентраций не только в остатках этой покровной культуры, но также в остатках предшествующей основной культуры, сорняков и опаде, присутствующих на делянках с покровными культурами T. patula.
3.3 Влияние обработки растительных остатков на разложение и динамику Alternaria solani в остатках картофеля
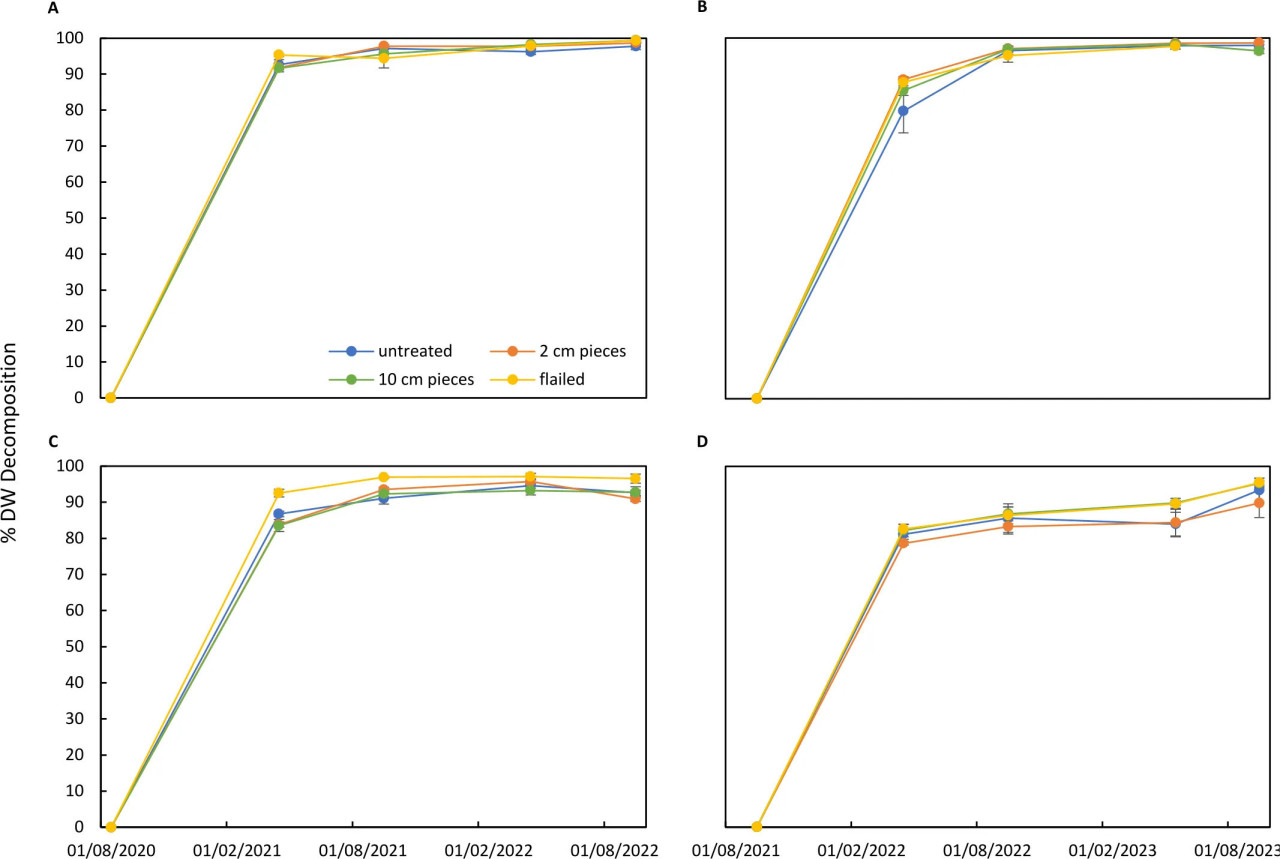
Измельченные остатки листового аппарата картофеля, зарытые в почву, разложились на 95% за 6 месяцев в первом эксперименте, начавшемся после уборки картофеля в 2020 г. (Рисунок 6A). Остатки листового аппарата, оставленные без обработки или нарезанные на кусочки по 10 см или 2 см, разложились на 92%–93%. После быстрого разложения в течение первых 6 месяцев эксперимента дальнейшее разложение было медленнее. Через 24 месяца было восстановлено 1%–2% исходных остатков листового аппарата. Остатки были обнаружены в 75% зарытых мешков (представляющих все четыре обработки), а в остальных 25% мешков остатки не были обнаружены. Остатки листового аппарата, которые были выдержаны в поле на поверхности почвы, разлагались медленнее (Рисунок 6C). В течение 6 месяцев 93% измельченных остатков разложились, тогда как необработанные остатки или остатки, нарезанные на кусочки по 10 см или 2 см, разложились меньше — на 84%–87%. Через 24 месяца 3% измельченных остатков и 7%–9% остатков, нарезанных на кусочки по 10 см или 2 см, все еще присутствовали. Во втором эксперименте, начавшемся после уборки урожая в 2021 г., разложение остатков листового аппарата картофеля в почве было изначально медленнее (Рисунок 6B), чем в первом эксперименте. Через 6 месяцев 80% необработанных остатков разложились. Более высокое разложение было обнаружено для трех других обработок: 85%–88% разложения. Дальнейшее разложение было медленнее без значительных различий между обработками, и через 24 месяца в зарытых мешках все еще присутствовало только 1%–4% остатков. Кроме того, остатки, помещенные на поверхность почвы, разлагались медленнее по сравнению с первым экспериментом (Рисунок 6D). Через 6 месяцев 80% остатков разложились без различий между обработками. Дальнейшее разложение было медленным, но измельченные остатки имели тенденцию разлагаться быстрее, чем необработанные или нарезанные остатки. Через 24 месяца присутствовало 4% измельченных остатков, тогда как более высокая доля — 10% остатков, нарезанных на кусочки по 2 см, все еще обнаруживалась. Статистически значимые эффекты обработки были обнаружены только в нескольких случаях для двух экспериментов. Измельченные остатки разлагались значительно быстрее по сравнению с необработанными остатками (p = 0.0045) и остатками, нарезанными на кусочки по 2 см (p = 0.0090). Однако было значительное различие между мешками, зарытыми в почву, и мешками, помещенными на поверхность почвы (p < 2.2e-16). Разложение было значительно выше в течение первых двух дат отбора проб (p < 0.0001) по сравнению со скоростями разложения после первого года. Таким образом, разложение остатков листового аппарата картофеля показывало аналогичную картину в обоих экспериментах для всех обработок «нарезкой».
Рисунок 6 – Разложение (%) остатков листового аппарата картофеля, обработанных измельчением или нарезкой тканей на кусочки по 2 см или 10 см, в сравнении с необработанными остатками. Остатки были зарыты в почву (A, B) или оставлены на поверхности почвы (C, D). Два эксперимента начались после уборки картофеля в 2020 г. (A, C) и в 2021 г. (B, D). Разложение было выражено как процент разложившегося сухого веса на каждую дату отбора проб по сравнению с началом экспериментов.
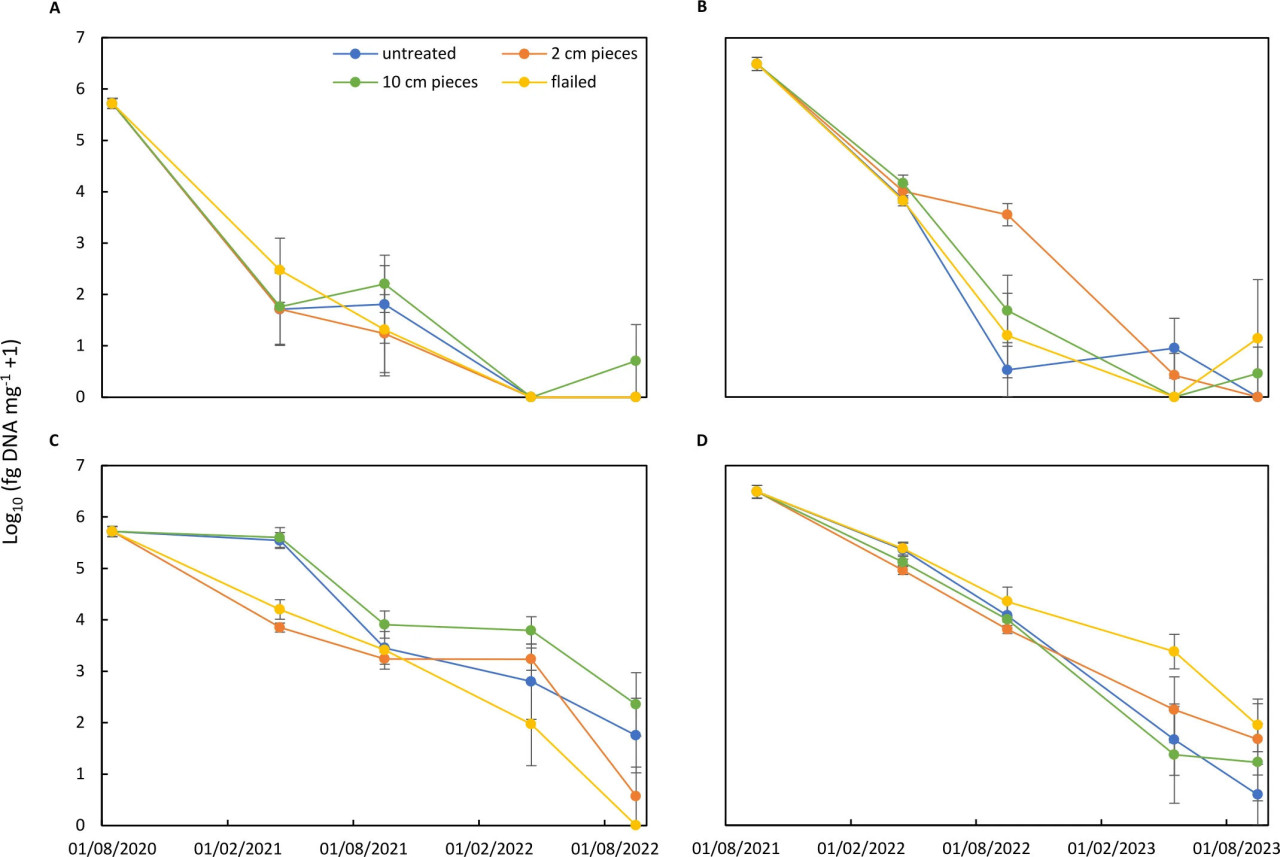
Концентрация ДНК A. solani резко снижалась в остатках листового аппарата, зарытых в почву, в течение первых 6 месяцев на три-четыре порядка без различий между обработками в первом эксперименте (Рисунок 7A). Концентрация ДНК A. solani дальше снижалась в течение следующих месяцев, и A. solani не могла быть обнаружена на оставшихся остатках через 24 месяца. Аналогичные закономерности были обнаружены во втором эксперименте (Рисунок 7B). Однако более высокие концентрации ДНК A. solani были обнаружены в остатках, нарезанных на кусочки по 2 см, после 12-месячной полевой экспозиции: 3 568 фг ДНК A.s. мг⁻¹ (сухой вес) (обратно преобразованные значения) по сравнению с <50 фг ДНК A.s. мг⁻¹ (сухой вес) в других обработках. В конце эксперимента через 24 месяца следы ДНК A. solani были обнаружены в немногих образцах остатков. Для остатков на поверхности поля наблюдались различные закономерности по сравнению с остатками, зарытыми в почву, и между двумя экспериментами (Рисунки 7C, D). В первом эксперименте концентрация ДНК A. solani снизилась на два порядка в измельченных остатках и остатках, нарезанных на кусочки по 2 см, тогда как для других обработок такого снижения концентрации в течение первых 6 месяцев не наблюдалось. Концентрация ДНК снижалась в измельченных остатках в течение следующих месяцев, и через 24 месяца A. solani не могла быть обнаружена в таких остатках. В необработанных остатках и остатках, нарезанных на кусочки по 10 см, были обнаружены более высокие концентрации в последующие даты отбора проб, и, наконец, через 24 месяца были обнаружены низкие концентрации 55–225 фг ДНК A.s. мг⁻¹ (сухой вес). Во втором эксперименте эффекта обработки не наблюдалось в течение первого года (Рисунок 7D). Измельченные остатки все еще содержали 3 568 фг ДНК A.s. мг⁻¹ (сухой вес) через 18 месяцев полевой экспозиции на поверхности почвы и 87 фг ДНК A.s. мг⁻¹ (сухой вес) через 24 месяца. В конце эксперимента следы A. solani все еще обнаруживались в остатках других обработок. Статистический анализ обоих экспериментов не показал значительных различий ни в одной из обработок (p = 0.2338). Однако разложение образцов листового аппарата, оставленных на поверхности почвы, было значительно медленнее во все периоды отбора проб по сравнению с образцами, зарытыми в почву (p = 2.369e−08). Таким образом, концентрации ДНК A. solani снижались во всех обработках на два-четыре порядка в течение первых 6 месяцев и до следовых или необнаруживаемых концентраций через 24 месяца в оставшихся остатках. Снижение концентраций в остатках на поверхности почвы обычно было медленнее, но достигало аналогичных низких уровней через 24 месяца, как и в зарытых остатках.
Рисунок 7 – Концентрация Alternaria solani (log10 фг ДНК A. solani мг⁻¹ сухого материала + 1) в остатках листового аппарата картофеля, обработанных измельчением или нарезкой тканей на кусочки по 2 см или 10 см, в сравнении с необработанными остатками. Остатки были зарыты в почву (A, B) или оставлены на поверхности почвы (C, D). Два эксперимента начались после уборки картофеля в 2020 г. (A, C) и в 2021 г. (B, D). Концентрация ДНК Alternaria solani выражена как среднее log10-преобразованных данных из 10 повторностей в начале экспериментов и пяти повторностей для каждой даты отбора проб. Столбики соответствуют стандартной ошибке среднего.
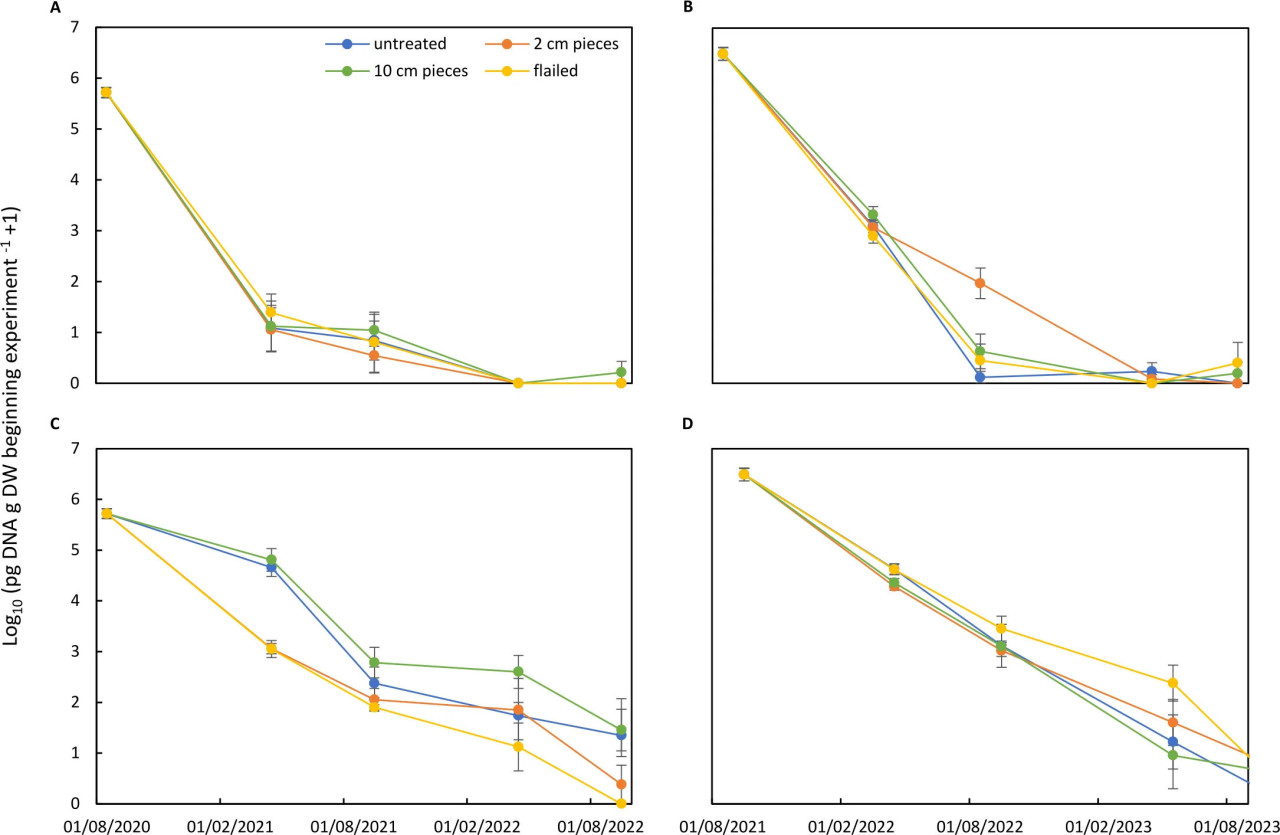
Объединение данных о разложении остатков и концентрации ДНК A. solani в оставшихся остатках дало количество ДНК A. solani, присутствующей в остатках исходных образцов, помещенных в мешки (выраженное как пг ДНК A. solani в остатках 1 г сухого материала в начале эксперимента – 1) (Рисунок 8). Количество ДНК A. solani, присутствующей в остатках листового аппарата, уменьшалось в течение первых 6 месяцев на пять порядков в остатках, зарытых в почву, в первом эксперименте и на два порядка во втором эксперименте (Рисунки 8A, B) без последовательных эффектов обработки. В остатках, выдержанных на поверхности поля, эффект обработки был обнаружен в первом эксперименте, что было в основном вызвано эффектами обработки на концентрацию ДНК A. solani, а не эффектами обработки на разложение (Рисунок 8C). Во втором эксперименте снижение количества ДНК A. solani следовало той же закономерности (Рисунок 8D). Статистический анализ не показал значительных различий между любыми из обработок (p = 0.5428). Значительные различия были обнаружены между размещением на поверхности почвы/зарыто в почву (p < 2e-16) и между периодами отбора проб (p < 2e-16).
Рисунок 8 – Количество Alternaria solani (log10 пг ДНК A. solani в остатках 1 г сухого материала в начале эксперимента +1) в остатках листового аппарата картофеля, обработанных измельчением или нарезкой тканей на кусочки по 2 см или 10 см, в сравнении с необработанными остатками. Остатки были зарыты в почву (A, B) или оставлены на поверхности почвы (C, D). Два эксперимента начались после уборки картофеля в 2020 г. (A, C) и в 2021 г. (B, D). Значения были рассчитаны с учетом разложения остатков (Рисунок 6) и концентрации A. solani (Рисунок 7).
4 Обсуждение
Остатки культур, сорняков и опада были систематически отобраны в сложном эксперименте по севообороту. Концентрации ДНК основных патогенов выращиваемых культур — A. solani, C. beticola, R. beticola и S. beticola — были количественно определены в остатках с использованием вновь разработанных ПЦР-анализов в реальном времени. Alternaria solani и C. beticola стабильно обнаруживались, тогда как R. beticola и S. beticola были обнаружены только в немногих образцах при низких концентрациях. Повторные полевые испытания дали дополнительные сведения о динамике A. solani в остатках листового аппарата картофеля в течение 2 лет. Общие результаты продемонстрировали, что A. solani и C. beticola колонизировали растительные остатки своих растений-хозяев сразу после уборки урожая в высокой плотности. В течение нескольких месяцев количество доступных остатков хозяина значительно уменьшалось (как было обнаружено для остатков листового аппарата картофеля), а концентрации патогенов в оставшихся остатках хозяина резко снижались. Альтернативные субстраты — остатки нехозяев, включая покровные культуры и сорняки — сапрофитно колонизировались некротрофными патогенами. Можно сделать вывод, что такие остатки потенциально могут служить мостом для популяций патогенов в безхозяинные вегетационные сезоны в системах севооборота.
Количественные ПЦР-анализы Taqman являются мощными инструментами для таких оценок, поскольку они могут потенциально надежно количественно определять концентрацию целевой ДНК в образцах окружающей среды в широком динамическом диапазоне. Исходные образцы и экстракты ДНК могут храниться, что позволяет организовать рабочие процессы с большим количеством оценок в экономически эффективных форматах, например, автоматизированная экстракция ДНК в сочетании с 384-луночным форматом для измерений ПЦР в реальном времени. Кроме того, хранение образцов ДНК позволяет в будущем измерять дополнительные важные патогены, например, токсигенные Fusarium spp. как патогены кукурузы и ячменя, A. dauci и A. radicina как патогены моркови, Botrytis squamosa и B. aclada/allii как патогены лука, а также C. apii как патоген сахарной свеклы, чтобы расширить представление о роли растительных остатков в динамике популяций патогенов.
Было описано несколько ПЦР-анализов для количественного определения A. solani. Ранее описанный ПЦР-анализ в реальном времени Leiminger и др. (2015) показал слабую перекрестную реактивность с P. infestans и несколькими другими патогенами картофеля, а также с грибами, не патогенными для картофеля. Анализ, о котором сообщили Lees и др. (2019), показывает перекрестную реакцию с A. dauci, который является патогеном моркови, присутствующим в нашем ротационном эксперименте. Анализ на основе Syber green, разработанный Khan и др. (2018) для обнаружения A. solani, требует дополнительного времени на проведение и анализ для анализа кривых плавления. Наш новый ПЦР-анализ в реальном времени включает Taqman-зонд, что исключает использование анализа кривых плавления. Он также имеет более высокую чувствительность: 100 фг на реакцию по сравнению с Khan и др. (2018), у которого чувствительность составляет 1 000 фг на реакцию. Однако наш Taqman-ПЦР-анализ, разработанный для количественного определения A. solani, также обнаруживает близкородственные A. alternariacida sp. nov, A. catananches sp. nov., A. cichorii, A. conidiophora, A. dichondrae, A. grandis, A. linicola и A. protenta. A. grandis и A. protenta вызывают раннюю гниль картофеля и являются членами европейской популяции Alternaria на картофеле (Landschoot и др., 2017). Кроме того, A. alternariacida sp. nov., недавно описанный Woudenberg и др. (2014) для изолята из плода Solanum lycopersicum в Великобритании, недавно был описан как возбудитель фитофтороза листьев картофеля в России (Kokaeva and Elansky, 2023). Другие виды Alternaria имеют различные спектры хозяев и не были ассоциированы с картофелем или другими культурами, выращиваемыми в ротационном эксперименте. Недавно описанный вид A. catananches sp. nov. был обнаружен на Catananche caerulea (астеровые) в Нидерландах, а A. conidiophora был обнаружен на неустановленном хозяине (Woudenberg и др., 2014). A. cichorii вызывает пятнистость листьев эндивия и других астровых (Barreto и др., 2008). A. dichondrae является возбудителем пятнистости листьев Dichondra repens (вьюнковые) (Cardin и др., 2005). A. linicola вызывает корневую гниль проростков льна (Corlett and Corlett, 1999). Таким образом, маловероятно, что ДНК A. catananches, A. conidiophore, A. cichorii, A. dichondrae или A. linicola присутствовала в исследованных образцах остатков в количествах, влияющих на результаты, полученные для A. solani. Для представителей комплекса Alternaria на картофеле, вызывающих раннюю гниль, A. grandis и A. protenta, а возможно, и A. alternariacida, ожидается, что они присутствуют в Нидерландах, но это еще не подтверждено.
Неожиданно высокие концентрации ДНК A. solani были обнаружены в остатках покровных культур Tagetes patula. Бархатцы не являются известным хозяином A. solani. Однако A. tagetica был описан как патоген T. patula, вызывающий некротические поражения листьев (Tomioka и др., 2000). Информация о последовательности A. tagetica показывает, что этот патоген не обнаруживается применяемым Taqman-ПЦР-анализом. Другой патоген T. patula, A. patula, был описан как новый вид в 2005 году (Wu and Wu, 2005, 2019). Опубликованная информация об этом виде, близкородственном A. tagetica, ограничена, и информация о последовательности недоступна. Alternaria spp. часто выделялись из остатков T. patula в трех образцах, собранных в феврале 2023 года в ротационном эксперименте (данные не представлены). Большинство изолятов, идентифицированных по информации о последовательностях ДНК alta 1 и gpd1, принадлежали к A. alternata — виду, который не обнаруживается применяемым Taqman-ПЦР-анализом. Изоляты A. solani также были выделены из двух из трех образцов. Только один из полученных различных изолятов Alternaria spp. принадлежал к другому виду — A. cinerariae.
Taqman-ПЦР, разработанный для количественного определения C. beticola Knight и Pethybridge (2020), также обнаруживает C. cf. flagellaris, хотя и с низкой чувствительностью. Присутствие C. cf. flagellaris на B. vulgaris было сообщено Groenewald и др. (2006) и Vaghefi и др. (2018). Наш недавно разработанный Taqman-ПЦР не обнаруживает C. cf. flagellaris и достигает 10-кратного повышения чувствительности по сравнению с qPCR, описанным Knight и Pethybridge (2020). Однако наш Taqman-ПЦР-анализ, разработанный для количественного определения C. beticola, также обнаруживает C. plantaginis. C. plantaginis был связан с Plantago (Groenewald и др., 2006) и описан на Plantago lanceolata (Bakhshi и др., 2018). P. lanceolata (подорожник ланцетный) является вездесущим видом в Нидерландах, который обычно не растет на пахотных полях. Нет сообщений о C. plantaginis на сахарной свекле или других культурах, выращиваемых в ротационном эксперименте, или других родах растений. Таким образом, маловероятно, что ДНК C. plantaginis присутствовала в исследованных образцах остатков в количествах, мешающих количественному определению C. beticola. Помимо C. beticola, C. apii вызывает церкоспороз сахарной свеклы (Groenewald и др., 2006). Этот вид не обнаруживается используемым Taqman-ПЦР-анализом. C. apii недавно был выделен из пятнистостей листьев сахарной свеклы на полях в Нидерландах, включая экспериментальное поле во Вредепеле. В 2021 году C. beticola в основном выделяли из листовых пятен, и только немного изолятов C. apii были получены от cv. Reforma KWS. Однако в 2022 году примерно 50% изолятов, полученных от cv. Reforma KWS, выращенного на экспериментальном поле, или от различных сортов, выращенных в разных местах в Нидерландах, принадлежали к C. apii (Hanse, 2023). Таким образом, необходим новый анализ для количественного определения C. apii, чтобы завершить исследование роли растительных остатков в развитии церкоспороза.
Количественное определение концентрации ДНК целевого грибного патогена в образцах окружающей среды в течение определенного времени дает представление о его популяционной динамике. Однако при тщательной интерпретации следует учитывать, что такие измерения не различают ДНК, происходящую из живых или мертвых клеток. Особенно в ситуациях, когда популяции сокращаются, снижение может быть недооценено, поскольку ДНК мертвых клеток может обнаруживаться в течение определенного времени. Кроме того, грибы могут продуцировать различные типы клеток, имеющие разное значение для выживания популяции, например, мицелиальные клетки, споры, покоящиеся споры, такие как хламидоспоры, склероции и плодовые тела. Таким образом, знание биологии патогена необходимо для адекватных выводов. Alternaria solani обычно выживает в виде мицелия и конидий, защищенных темной пигментацией от факторов окружающей среды. Хламидоспоры были описаны, но встречаются редко (Kemmit, 2002). Для C. beticola сообщается, что патоген выживает в зараженных растительных остатках путем формирования псевдостром, и что патоген также может выживать на мертвой растительной ткани как некротроф, независимо от статуса хозяина (Sharma и др., 2022).
Оценки ДНК патогена в растительных остатках, включая опад, присутствующий в верхнем слое почвы, в ротационном эксперименте выявили общую закономерность для обоих патогенов A. solani и C. beticola. Концентрации ДНК патогена были высокими в растительных остатках, остатках сорняков и остатках опада после уборки растения-хозяина. Концентрации значительно снижались в течение следующих месяцев. ДНК патогена была обнаружена при низкой концентрации в растительных остатках с делянок, на которых выращивались нехозяева. Однако такие результаты варьировали во времени и между повторными делянками. Специфическая вариабельность и иногда высокие концентрации были измерены в остатках сорняков, скорее всего, потому, что определенные сорняки, встречающиеся на делянках севооборота, действовали как хозяева, например, C. album для C. beticola или S. nigrum для A. solani. Риск того, что остатки сорняков, действующих как хозяева изучаемых патогенов, будут способствовать выживанию патогенов в системе севооборота, может возрасти в будущих системах земледелия с меньшим использованием гербицидов. Хотя это еще не наблюдалось при сравнении эталонной системы земледелия и системы ICM в течение первых лет эксперимента, ожидается, что встречаемость определенных сорняков увеличится после нескольких лет внедрения систем ICM с меньшим использованием гербицидов.
Наши результаты предполагают, что остатки нехозяев могут играть важную роль, позволяя патогенам переживать периоды в поле без культур-хозяев и быстро разлагающихся остатков хозяев. Количество конкретных типов остатков не было количественно определено при отборе проб остатков в эксперименте по севообороту в нашем исследовании. Относительная важность остатков для колонизации патогенами зависит от количества и концентрации патогенов в конкретном субстрате. Остатки будут присутствовать при уборке урожая в больших количествах и уменьшаться в последующие месяцы, как было продемонстрировано для остатков листового аппарата картофеля в дополнительных экспериментах по обработке остатков. Это колебание доступности субстрата приведет к значительным колебаниям популяций патогенов. Покровные культуры, включенные в схемы севооборота, могут играть особую роль, поскольку они производят биомассу, которая полностью остается в поле и превращается в растительные остатки. Различия в колонизации патогенами между покровными культурами были обнаружены в нашем исследовании: неожиданно высокие концентрации A. solani были обнаружены в остатках бархатцев. Остатки бархатцев могут быть особенно подходящим субстратом для A. solani. Возможно, отмирание культуры бархатцев совпало в определенные периоды с высокой плотностью A. solani на других остатках, что привело к быстрой и интенсивной колонизации остатков бархатцев. Поскольку покровные культуры производят огромное количество остатков, их особая роль в динамике популяций патогенов требует внимания в дальнейших исследованиях.
Гипотеза нашего полевого испытания с обработками остатков листового аппарата картофеля заключалась в том, что концентрации A. solani снижаются быстрее в меньших кусочках листового аппарата, поскольку меньшие кусочки могут быть быстрее колонизированы сапрофитами, вытесняющими патоген. Эффектов обработки остатков листового аппарата на A. solani с течением времени обнаружено не было. Необходимы дальнейшие эксперименты, чтобы лучше понять колонизацию кусочков остатков сапрофитами и как поддерживать такие функции микробиома. В экспериментах был продемонстрирован четкий основной эффект. Остатки листового аппарата, зарытые в почву, разлагались значительно быстрее, и концентрация A. solani также снижалась быстрее по сравнению с остатками на поверхности почвы. Это может быть связано с различными условиями окружающей среды: более высокой и более постоянной доступностью воды в зарытых субстратах в сочетании с различным составом вторгающегося микробиома, развивающегося в остатках. Закапывание растительных остатков, например, путем вспашки, может не только усилить разложение и снизить колонизацию патогенами, но также предотвратит перенос патогена от остатков хозяина к остаткам, присутствующим после уборки последующей культуры-нехозяина. Это возможное преимущество обработки почвы в управлении патогенами требует дальнейшего внимания в будущих исследованиях систем обработки почвы (Kerdraon и др., 2019; Wang и др., 2020).
Различные источники инокулюма потенциально могут инициировать новые эпидемии, как только восприимчивая культура-хозяин будет создана в поле. Популяции патогенов могут присутствовать, колонизируя некротические ткани растений сапрофитно, как было оценено в нашем исследовании. Другим источником в пределах поля могут быть растения-добровольцы хозяина и сорняки-хозяева, которые выжили в последующих культурах и служат местом активного заражения патогеном (Thompson и др., 2015). Источники из-за пределов поля также могут играть роль, например, споры патогена, присутствующие на семенах, или воздушно-капельные споры, происходящие из полей, где эпидемии уже происходят, или из сапрофитно колонизированных растений и зараженных растений-добровольцев в окрестностях поля. Относительная важность различных потенциальных источников зависит от биологии патогена, а также от региональных систем земледелия и управления культурами. Экспериментальные данные об источнике спор, инициирующих эпидемии, ограничены и их трудно получить в полевых исследованиях (Suffert and Sache, 2011). Экспериментальные манипуляции, например, удаление известных источников инокулюма, которые приводят к задержке эпидемий, дают представление о роли определенных источников (Köhl и др., 1995).
Будущие системы с уменьшенной обработкой почвы и без обработки почвы, направленные на снижение выбросов CO₂, увеличение содержания органического вещества в почве и улучшение структуры почвы, приведут к увеличению количества растительных остатков. Однако есть данные, включая результаты этого исследования, что растительные остатки в поле являются основным источником инокулюма патогенов, например, при производстве зерновых (Kerdraon и др., 2019). Таким образом, управление растительными остатками, не мешающее общим целям увеличения органического вещества в пахотных системах, является вариантом снижения инокуляционного потенциала и последующей задержки или даже предотвращения вспышек болезней. Обработки растительных остатков, такие как измельчение, внесение мочевины или физическое удаление, были описаны для плодоводства (Gomez и др., 2007). Для профилактики альтернариоза, вызываемого A. solani, рассматривается удаление потенциально инфицированного материала, такого как ботва и плоды (в случае томата) (Kemmit, 2002). Научные сообщения о последствиях таких санитарных мер для полевых культур ограничены, и отсутствуют сообщения, рассматривающие динамику патогенов в остатках последующих выращиваемых культур, включая нехозяева, в системах севооборота. Понимание временной динамики количества и качества субстрата откроет возможности для профилактики болезней с помощью управления растительными остатками в пахотных ротационных системах. Будет важно понять биотические механизмы. Растительные остатки колонизируются различными типами организмов в порядке преемственности, в зависимости от доступности питательных веществ в разлагающихся тканях, потребностей потенциальных колонизаторов в питательных веществах и их способности использовать оставшиеся более сложные органические соединения (Hudson, 1971; Hudson and Webster, 1958; Köhl and Fokkema, 1998; Kerdraon и др., 2019). Патогены, уже присутствующие во время отмирания тканей, имеют преимущество на ранних стадиях разложения в ходе конкурентной колонизации субстрата. Изменение состава субстрата, вызванное потреблением питательных веществ начальными колонизаторами, приводит к появлению более сложных органических субстратов, что благоприятствует специалистам с соответствующими физиологическими свойствами и приводит к типичным микробным сукцессиям при колонизации субстрата. Патогены в этой ситуации могут быть вытеснены из конкуренции и нуждаться в выживании посредством формирования покоящихся структур или колонизации альтернативных растительных остатков.
Таким образом, управление растительными остатками, направленное на профилактику болезней, должно быть сосредоточено на ранней стадии колонизации субстрата. Сбор и физическое удаление растительных остатков с поля является реалистичным вариантом, если такие остатки, как солома, могут использоваться как побочные продукты, имеющие экономическую ценность. Управление полями всегда будет сосредоточено на вытеснении патогенов на ранних стадиях разложения, усилении раннего разложения или закапывании остатков в почву, чтобы заблокировать перенос на альтернативные субстраты и дополнительно создать микробный буфер, предотвращающий колонизацию субстрата патогенами на более поздних стадиях. Процессы разложения являются результатом микробной активности, определяемой микробиомом, присутствующим в начале процесса разложения, и динамикой микробиома в процессе разложения (Kerdraon и др., 2019). Знание функций микробиома и возможности формирования микробиомов в «сфере остатков», определяемой как микроместообитание, состоящее из всех растительных остатков на почве и в почве (Kerdraon и др., 2019), необходимо для разработки рациональных стратегий управления растительными остатками, включая решения для биоконтроля на основе микробиома. Кроме того, роль мезофауны в раннем разложении некротических тканей растений, часто игнорируемая фитопатологами, требует особого внимания.
Растительные остатки нехозяев, выращиваемых в севообороте, как альтернативные пути для патогенов делают жизненные циклы патогенов более сложными, а рассмотрение вопросов санитарии — более трудным. С другой стороны, санитарные меры, направленные на растительные остатки вскоре после уборки урожая, не только предотвратят развитие популяций патогенов данной конкретной культуры, но и повлияют на патогенов других культур, выращиваемых в севообороте. Это повышает ценность целенаправленного управления растительными остатками и может позволить провести комплексную санитарию системы севооборота, а не санитарию, направленную на одного патогена.
Дополнительные материалы
Дополнительные материалы к этой статье можно найти в интернете по адресу: https://www.frontiersin.org/articles/10.3389/fagro.2024.1470598/full#supplementary-material
Ссылки
1. Abuley I. K., Nielsen B. J., Hansen H. H. (2018). The influence of crop rotation on the onset of early blight (Alternaria solani). J. Phytopathol. 167, 35–40. doi: 10.1111/jph.12771. CrossRef Google Scholar
2. Bakhshi M., Arzanlou M., Babai-ahari A., Groenewald J. Z., Crous P. W. (2018). Novel primers improve species delimitation in Cercospora. IMA FUNGUS 9, 299–332. doi: 10.5598/imafungus.2018.09.02.06. CrossRef Google Scholar
3. Barreto R. W., Santin A. M., Vieira B. S. (2008). Alternaria cichorii in Brazil on Cichorium spp. seeds and cultivated and weedy hosts. J. Phytopathol. 156, 425–430. doi: 10.1111/j.1439-0434.2007.01380.x. CrossRef Google Scholar
4. Cardin L., Delecolle B., Moury B. (2005). Occurrence of Alternaria dichondrae, Cercospora sp., and Puccinia sp. on Dichondra repens in France and Italy. Plant Dis. 89, 1012. doi: 10.1094/PD-89-1012A. CrossRef Google Scholar
5. Corlett M., Corlett M. E. (1999). Alternaria linicola. Can. J. Plant Pathol. 21, 55–57. doi: 10.1080/07060661.1999.10600134. CrossRef Google Scholar
6. Cotton T. K., Munkvold G. P. (1998). Survival of Fusarium moniliforme, F. proliferatum, and F. subglutinans in maize stalk residue. Phytopathology 88, 550–555. doi: 10.1094/PHYTO.1998.88.6.550. CrossRef Google Scholar
7. European Commission (2015). Commission Implementing Regulation (EU) No. 2015/408 of 11 March 2015 implementing Article 80(7) of Regulation (EC) No 1107/2009 of the European Parliament and of the Council concerning the placing of plant protection products on the market and establishing a list of candidates for substitution. O.J.E.U. L 67, 18–22. Google Scholar
8. Gomez C., Brun L., Chauffour D., Vallée D. D. L. (2007). Effect of leaf litter management on scab development in an organic apple orchard. Agric. Ecosyst. Environ. 118, 249–255. doi: 10.1016/j.agee.2006.05.025. CrossRef Google Scholar
9. Groenewald M., Groenewald J. Z., Braun U., Crous P. W. (2006). Host range of Cercospora apii and C. beticola and description of C. apiicola, a novel species from celery. Mycologia 98, 275–285. doi: 10.3852/mycologia.98.2.27. CrossRef Google Scholar
10. Hanse B. (2023). IRS project 12-14 stemphylium en cercospora in suikerbieten. In: IRS jaarverslag 2022 (Stichting IRS, Dinteloord, NL), 107–111. Google Scholar
11. Hanse B., Raaijmakers E. E. M., Schoone A. H. L., van Oorschot P. M. S. (2015). Stemphylium sp., the cause of yellow leaf spot disease in sugar beet (Beta vulgaris L.) in the Netherlands. Eur. J. Plant Pathol. 142, 319–330. doi: 10.1007/s10658-015-0617-8. CrossRef Google Scholar
12. Hudson H. J. (1971). The development of the saprophytic fungal flora as leaves senesce and fall. In: Ecology of Leaf Surface Microorganisms (Preece T. F., Dickinson C. H. eds.), Academic Press, London, pp. 447-455. Google Scholar
13. Hudson H. J., Webster J. (1958). Sucession of fungi on decaying stems of Agropyron repens. Trans. Br. Myco. Soc. 41, 165-177. Google Scholar
14. Humpherson-Jones F. M. (1989). Survival of Alternaria brassicae and Alternaria brassicicola on crop debris of oilseed rape and cabbage. Ann. Appl. Biol. 115, 45–50. doi: 10.1111/j.1744-7348.1989.tb06810.x. CrossRef Google Scholar
15. Jindo K., Evenhuis A., Kempenaar C., Pombo Sudré C., Zhan X., Goitom Teklu M., et al. (2021). Review: Holistic pest management against early blight disease towards sustainable agriculture. Pest Manage. Sci. 77, 3871–3880. doi: 10.1002/ps.6320. CrossRef Google Scholar
16. Kemmit G. (2002). Early blight of potato and tomato. In: The Plant Health Instructor. The American Phytopathological Society (APS). Vol. 2. doi: 10.1094/PHI-I-2002-0809-01. CrossRef Google Scholar
17. Kerdraon L., Laval V., Suffert F. (2019). Microbiomes and pathogen survival in crop residues, an ecotone between plant and soil. Phytobiomes J. 3, 246–255. doi: 10.1094/PBIOMES-02-19-0010-RVW. CrossRef Google Scholar
18. Khan M. F. R., Smith L. J. (2005). Evaluating fungicides for controlling Cercospora leaf spot on sugar beet. Crop Prot. 24, 79–86. doi: 10.1016/j.cropro.2004.06.010. CrossRef Google Scholar
19. Khan M., Wang R., Li B., Liu P., Weng Q., Chen Q. (2018). Comparative evaluation of the LAMP assay and PCR-based assays for the rapid detection of Alternaria solani. Front. Microbiol. 9, 2089. doi: 10.3389/fmicb.2018.02089. CrossRef Google Scholar
20. Klerks M. M., Zijlstra C., van Bruggen A. H. C. (2004). Comparison of realtime PCR methods for detection of Salmonella enterica and Escherichia coli O157:H7, and introduction of a general internal amplification control. J. Microbiol. Methods 59, 337–349. doi: 10.1016/j.mimet.2004.07.011. CrossRef Google Scholar
21. Knight N. L., Pethybridge S. J. (2020). An improved PCR assay for species-specific detection and quantification of Cercospora beticola. Can. J. Plant Pathol. 42, 72–83. doi: 10.1080/07060661.2019.1621380. CrossRef Google Scholar
22. Knight N. L., Vaghefi N., Kikkert J. R., Pethybridge S. J. (2019). Alternative hosts of Cercospora beticola in field surveys and inoculation trials. Plant Dis. 103, 1983–1990. doi: 10.1094/PDIS-01-19-0229-RE. CrossRef Google Scholar
23. Köhl J., de Jong P.-F., Kastelein P., Groenenboom-de Haas B. H., Anbergen R. H. N., Balkhoven H., et al. (2013). Dynamics of pear-pathogenic Stemphylium vesicarium in plant residues in Dutch pear orchards. Eur. J. Plant Pathol. 137, 609–619. doi: 10.1007/s10658-013-0274-8. CrossRef Google Scholar
24. Köhl J., Fokkema N. J. (1998). Biological control of necrotrophic foliar fungal pathogens. In: Plant-Microbe Interactions and Biological control. Eds. Boland G. J., Kuykendall L. V. (Marcel Dekker, New York), 49–88. Google Scholar
25. Köhl J., Haas B. H., Kastelein P., Burgers S. L. G. E., Waalwijk C. (2007). Population dynamics of Fusarium spp. and Microdochium nivale in crops and crop residues of winter wheat. Phytopathology 97, 971–978. doi: 10.1094/PHYTO-97-8-0971. CrossRef Google Scholar
26. Köhl J., van der Plas C. H., Molhoek W. M. L., Fokkema N. J. (1995). Suppression of sporulation of Botrytis spp. as a valid biocontrol strategy. Eur. J. Plant Pathol. 101, 251–259. doi: 10.1007/BF01874781. CrossRef Google Scholar
27. Köhl J., Vlaswinkel M., Groenenboom-de Haas B. H., Kastelein P., van Hoof R. A., van der Wolf J. M., et al. (2011). Survival of pathogens of Brussels sprouts (Brassica oleracea Gemmifera group) in crop residues. Plant Pathol. 60, 661–670. doi: 10.1111/j.1365-3059.2010.02422.x. CrossRef Google Scholar
28. Kokaeva L. Y., Elansky S. N. (2023). First report of Alternaria alternariacida causing potato leaf blight in the Far East, Russia. Plant Dis. 107, 938. doi: 10.1094/PDIS-02-22-0291-PDN. CrossRef Google Scholar
29. Kuznetsova A., Brockhoff P., Christensen R. H. B. (2017). lmerTest package: tests in linear mixed effects models. J. Stat. Software 82, 1–26. doi: 10.18637/jss.v082.i13. CrossRef Google Scholar
30. Landschoot S., Vandecasteele M., De Baets B., Höfte M., Audenaert K., Haesaert G. (2017). Identification of A. arborescens, A. grandis, and A. protenta as new members of the European Alternaria population on potato. Fungal Biol. 121, 172–188. doi: 10.1016/j.funbio.2016.11.005. CrossRef Google Scholar
31. Lees A. K., Roberts D. M., Lynott J., Sullivan L., Brierley J. L. (2019). Real-Time PCR and LAMP assays for the detection of spores of Alternaria solani and sporangia of Phytophthora infestans to inform disease risk forecasting. Plant Dis. 103, 3172–3180. doi: 10.1094/PDIS-04-19-0765-RE. CrossRef Google Scholar
32. Leiminger J. H., Bäßler E., Knappe C., Bahnweg G., Hausladen H. (2015). Quantification of disease progression of Alternaria spp. on potato using real-time PCR. Eur. J. Plant Pathol. 141, 295–309. doi: 10.1007/s10658-014-0542-2. CrossRef Google Scholar
33. MacHardy W. E., Gadoury D. M., Gessler C. (2001). Parasitic and biological fitness of Venturia inaequalis: Relationship to disease management strategies. Plant Dis. 85, 1036–1051. doi: 10.1094/PDIS.2001.85.10.1036. CrossRef Google Scholar
34. Madden L. V., Hughes G., van den Bosch F. (2007). The Study of Plant Disease Epidemics (St. Paul, MN: American Phytopathological Society). Google Scholar
35. Mourelos C. A., Malbrán I., Mengual Gómez D., Ghiringhelli P. D., Lori G. A. (2024). Dynamics of Fusarium graminearum inoculum on residues of naturally infected winter and summer crops. Eur. J. Plant Pathol. 169, 543–553. doi: 10.1007/s10658-024-02850-z. CrossRef Google Scholar
36. R Core Team (2020). R: A language and environment for statistical computing (Vienna, Austria: R Foundation for Statistical Computing). Available at: https://www.R-project.org/. Google Scholar
37. Riemens M., Sønderskov M., Moonen A. C., Storkey J., Kudsk P. (2022). An Integrated Weed framework: A pan-European perspective. Eur. J. Agron. 133, 126443. doi: 10.1016/j.eja.2021.126443. CrossRef Google Scholar
38. Rossi V., Pattori E., Bugiani R. (2008). Sources and seasonal dynamics of inoculum for brown spot disease of pear. Eur. J. Plant Pathol. 121, 147–159. doi: 10.1007/s10658-007-9258-x. CrossRef Google Scholar
39. Shane W. W., Teng P. S. (1992). Impact of Cercospora leaf spot on root weight, sugar yield, and purity of Beta vulgaris. Plant Dis. 76, 812–820. doi: 10.1094/PD-76-0812. CrossRef Google Scholar
40. Sharma S., Heck D. W., Branch E., Kikkert J. E., Pethybridge S. J. (2022). Cercospora leaf spot of table beet. In: The Plant Health Instructor. The American Phytopathological Society (APS). Vol. 22. doi: 10.1094/PHI-P-2022-020101. CrossRef Google Scholar
41. Suffert F., Sache I. (2011). Relative importance of different types of inoculum to the establishment of Mycosphaerella graminicola in wheat crops in north-west Europe: Wheat debris as local source of M. graminicola inoculum. Plant Pathol. 60, 878–889. doi: 10.1111/j.1365-3059.2011.02455.x. CrossRef Google Scholar
42. Thompson S., Tan Y., Shivas R., Neate S., Morin L., Bissett A., et al. (2015). Green and brown bridges between weeds and crops reveal novel Diaporthe species in Australia. Persoonia Mol. Phylogeny Evol. Fungi 35, 39–49. doi: 10.3767/003158515X687506. CrossRef Google Scholar
43. Tomioka K., Sato T., Koganezawa H. (2000). Marigold leaf spot caused by Alternaria tagetica new to Japan. J. Gen. Plant Pathol. 66, 294–298. doi: 10.1007/PL00012967. CrossRef Google Scholar
44. Vaghefi N., Kikkert J. R., Hay F. S., Carver G. D., Koenick L. B., Bolton M. D., et al. (2018). Cryptic diversity, pathogenicity, and evolutionary species boundaries in Cercospora populations associated with Cercospora leaf spot of Beta vulgaris. Fungal Biol. 122, 264–282. doi: 10.1016/j.funbio.2018.01.008. CrossRef Google Scholar
45. Vereijssen J., Schneider J. H. M., Jeger M. J. (2007). Supervised control of Cercospora leaf spot in sugar beet. Crop Prot. 26, 19–28. doi: 10.1016/j.cropro.2006.03.012. CrossRef Google Scholar
46. Videira S. I. R., Groenewald J. Z., Braun U., Shin H. D., Crous P. W. (2016). All that glitters is not Ramularia. Stud. Mycol. 83, 49–163. doi: 10.1016/j.simyco.2016.06.001. CrossRef Google Scholar
47. van der Waals J. E., Korsten L., Aveling T. A. S. (2001). A review of early blight of potato. Afr Plant Prot. 7, 91–102. Google Scholar
48. Wang H., Li X., Li X., Wang J., Li X., Guo Q., et al. (2020). Long-term no-tillage and different residue amounts alter soil microbial community composition and increase the risk of maize root rot in northeast China. Soil Tillage Res. 196. doi: 10.1016/j.still.2019.104452. CrossRef Google Scholar
49. Woudenberg J. H. C., Hanse B., van Leeuwen G. C. M., Groenewald J. Z., Crous P. W. (2017). Stemphylium revisited. Stud. Mycol. 87, 77–103. doi: 10.1016/j.simyco.2017.06.001. CrossRef Google Scholar
50. Woudenberg J. H. C., Truter M., Groenewald J. Z., Crous P. W. (2014). Large-spored Alternaria in section Porri disentangled. Stud. Mycol. 79, 1–47. doi: 10.1016/j.simyco.2014.07.003. CrossRef Google Scholar
51. Wu W.-S., Wu H.-C. (2005). A new species of Alternaria on seeds of French marigold. Mycotaxon 91, 21–25. doi: 10.1111/ppa.12982. CrossRef Google Scholar
52. Wu W.-S., Wu H.-C. (2019). Evaluation of virulence and pathogenicity of Alternaria patula on French marigold (Tagetes patula). Plant Pathol. 68, 678–688. doi: 10.1111/ppa.12982. CrossRef Google Scholar
Köhl J, Elena G, Hanse B, Houwers I, Groenenboom-de Haas L, de Lange E, Verstegen H and Evenhuis A (2024) Population dynamics of Alternaria solani, Cercospora beticola, Ramularia beticola, and Stemphylium beticola in residues of host crops, non-host crops, and weeds in Dutch rotation systems. Front. Agron. 6:1470598. doi: 10.3389/fagro.2024.1470598
Перевод статьи «Population dynamics ofAlternaria solani,Cercospora beticola,Ramularia beticola, andStemphylium beticolain residues of host crops, non-host crops, and weeds in Dutch rotation systems» авторов Köhl J, Elena G, Hanse B, Houwers I, Groenenboom-de Haas L, de Lange E, Verstegen H and Evenhuis A., оригинал доступен по ссылке. Лицензия: CC BY. Изменения: переведено на русский язык
Фото: freepik















































































































Комментарии (0)