Биоуголь против стеблевой гнили арахиса: простое решение серьезной проблемы
Из-за способности патогена выживать в почве в течение длительного времени, почвенные заболевания часто трудно поддаются контролю. В данном исследовании изучается многогранное влияние биоугля на борьбу со стеблевой гнилью арахиса, а также его воздействие на свойства почвы и микробные сообщества.
Аннотация
Было тщательно оценено влияние биоугля в различных концентрациях (0%, 1%, 3% и 5%) на стеблевую гниль арахиса, вызываемую Sclerotium rolfsii. В лабораторных условиях биоуголь не оказывал прямого ингибирующего действия на S. rolfsii в различных концентрациях, но продемонстрировал косвенное подавление образования склероциев, что указывает на зависимое от концентрации влияние на покоящиеся структуры патогена. Кроме того, было обнаружено, что обработка биоуглем эффективно задерживала появление симптомов и снижала развитие болезни у растений арахиса, при этом наблюдалась значительная вариабельность между генотипами и концентрациями биоугля. Особо следует отметить, что взаимодействия с участием генотипов ICGV 171002 и ICGV 181035 при обработке BC2 + Sr (3% биоугля + S. rolfsii) и BC3 + Sr (5% биоугля + S. rolfsii) показали высокую эффективность в снижении заболеваемости в контролируемых условиях. Полевые оценки подтвердили эти результаты, выявив генотипспецифичные реакции на обработку биоуглем. Однако при сравнении с контролями не было обнаружено значительной разницы между обработками BC2 + Sr (3%) и BC3 + Sr (5%) в борьбе со стеблевой гнилью. Внесение биоугля значительно повысило уровень питательных веществ в почве, включая азот, фосфор и калий, а также увеличило содержание органического вещества почвы, электропроводность (EC) и pH, что подчеркивает его потенциал для улучшения плодородия почвы. В целом, эти результаты демонстрируют потенциальные преимущества биоугля для устойчивого сельского хозяйства через борьбу с болезнями, обогащение почвы питательными веществами и модуляцию микробиома, что требует дальнейшего изучения оптимальных стратегий его применения в различных агроэкологических условиях.
1 Введение
Sclerotium rolfsii, почвенный гриб, является серьезным препятствием для различных культур в теплом и влажном климате. Он вызывает стеблевую и коробочковую гниль арахиса, что оказывает серьезное воздействие на продуктивность. Стеблевая гниль, также известная как склеротиниоз, южный фитофтороз или белая плесень, представляет собой серьезную проблему в выращивании арахиса, приводящую к значительным потерям урожая, несмотря на профилактические меры. Стеблевая гниль обычно снижает урожайность арахиса на 10–40%, но на сильно пораженных полях сокращение может достигать 80% (Bera и др., 2014). Коробочковая и столоновая гнили, вызываемые S. rolfsii, широко распространены в различных странах, вызывая значительные потери коробочек при сборе урожая. Стеблевая гниль активно развивается в теплых и влажных условиях, тогда как коробочковые гнили более распространены в более сухих почвах. На плотных почвах гриб повреждает растения на уровне поверхности, тогда как на более легких почвах он может глубоко повреждать столоны и коробочки (Mehan и др., 1994). Гриб сохраняется в почве в виде склероциев и в растительных остатках в виде мицелия, причем склероции сохраняются годами без растения-хозяина. В настоящее время эффективные профилактические меры и меры борьбы недостаточны для обеспечения устойчивой защиты всех культур. Традиционные подходы к борьбе, такие как устойчивые сорта, севооборот, методы почвенной солнечной стерилизации и т.д., не всегда могут стабильно эффективно бороться с S. rolfsii, который может процветать в неблагоприятных почвенных условиях и поражать различные виды растений-хозяев (Tian и др., 2021). Хотя для борьбы с болезнями используется множество химических и биологических методов, они сталкиваются с многочисленными ограничениями (Wang и др., 2024). Кроме того, постоянное применение химических пестицидов способствует значительному загрязнению окружающей среды и способствует появлению устойчивых к пестицидам патогенов (Chen и др., 2020). Следовательно, существует настоятельная необходимость в поиске альтернативных экологически безопасных подходов для эффективного контроля этого заболевания. Использование почвенных мелиорантов, таких как биоуголь, может быть перспективным подходом, поскольку их подавляющая активность была показана для широкого спектра почвенных болезней (Akhter и др., 2015).
Использование биоугля в качестве почвенного мелиоранта значительно возросло и имеет различные применения в сельском хозяйстве, энергетике, промышленности и охране окружающей среды (Wang и др., 2024). Биоуголь, богатый углеродом материал, получаемый путем пиролиза органических отходов, таких как навоз, древесина и растительные остатки, в условиях низкого содержания кислорода (Pasumarthi и др., 2024; Akhter и др., 2015; Chen и др., 2020; Tian и др., 2021). Биоуголь состоит из различных питательных веществ, включая углерод, азот, фосфор, калий, кальций и магний, а его физические и химические свойства, такие как насыпная плотность (BD), влагоемкость (WHC), удержание питательных веществ, кислотность почвы, электропроводность (EC) и катионообменная способность (CEC) и т.д., определяются типом органического материала, температурой пиролиза и используемым временем удерживания (Antal and Gronli, 2003; Gaskin et al., 2008). Помимо улучшения свойств почвы, биоуголь может связывать углерод, снижать выбросы парниковых газов, адсорбировать тяжелые металлы и органические загрязнители (Zhang и др., 2013) и улучшать рост растений (Kumar и др., 2024; Zhang и др., 2016). Он также способствует обильности, разнообразию и составу почвенных микробов (Elad и др., 2010; Graber и др., 2010; Lehmann и др., 2011).
Биоуголь показывает замечательную стабильность в почве с длительным сроком службы, достигающим тысяч лет. Несколько последних исследований показали, что биоуголь эффективно подавляет различные почвенные заболевания растений, вызываемые разными патогенами, и может даже укреплять защиту растений против листовых патогенов, таких как Botrytis cinerea и Leveillula taurica, на таких культурах, как томат и перец, а также на клубнике против Botrytis cinerea, Colletotrichum acutatum и Podosphaera aphanis (Elad и др., 2010; Meller Harel и др., 2012). Дополнительно, биоуголь может влиять на прогрессирование болезней, вызываемых почвенными патогенами, посредством нескольких механизмов, включая индукцию защитных реакций растений, изменения в почвенной микросреде, увеличение популяций полезных микробов, прямое ингибирование роста патогена токсичными соединениями и изменения в химизме корневых экссудатов (Graber and Elad, 2013; Graber и др., 2014). Например, внесение биоугля из рисовой соломы снизило частоту и тяжесть бактериального увядания табака, вызываемого Ralstonia solanacearum, что было связано с улучшением условий почвы и бактериального разнообразия (Zhang и др., 2017). Более того, внесение биоугля подавляет болезни, непосредственно адсорбируя патогены и косвенно адсорбируя корневые экссудаты (Gu и др., 2017). Следовательно, внесение биоугля становится интригующим подходом к борьбе с болезнями растений (Jaiswal и др., 2017). Однако большинство исследований по внесению биоугля были проведены в лабораторных условиях в течение коротких периодов времени. Долгосрочные последствия, особенно превышающие 12 месяцев после внесения биоугля, для почвенных микробных сообществ, почвенных биохимических свойств и болезней остаются слабо изученными в полевых экспериментах. Эффективность биоугля в подавлении болезней варьируется в зависимости от внесенной дозы (Jaiswal и др., 2014, Jaiswal и др., 2015). Выдвигается гипотеза, что внесение биоугля изменит свойства почвы и увеличит микробную популяцию, в частности полезных бактерий, тем самым снижая заболеваемость стеблевой гнилью. Дальнейшим предположением было то, что различные дозировки биоугля будут в разной степени эффективны в борьбе с болезнью. Цель этого исследования направлена на определение оптимальной дозировки биоугля для эффективного контроля стеблевой гнили арахиса.
2 Материалы и методы
2.1 Детали эксперимента
Эксперимент был проведен в сезон дождей (июнь/июль – сентябрь/октябрь) 2023 года в полевых условиях и условиях теплицы в ICRISAT (17°5' с.ш.; 78°2' в.д.), Патанчеру, Индия. Четыре генотипа арахиса, а именно ICGV 171025, 181035, 171002 и 211107, были включены в исследование на основе их умеренно устойчивой реакции на стеблевую гниль в искусственных эпифитотийных условиях в поле и теплице (данные не показаны). Два стандартных контроля, один толерантный (CS 319) (Mahatma и др., 2018; Nogiya и др., 2021) и один восприимчивый (TMV 2) (Rani и др., 2022; Sunkad и др., 2016), также были включены.
2.2 Источник патогена
Патоген стеблевой гнили, S. rolfsii, использованный в этом исследовании, был получен из коллекции культур Лаборатории патологии арахиса ICRISAT, Патанчеру. Патоген был первоначально выделен из зараженных растений арахиса с характерными симптомами стеблевой гнили на полях Патанчеру и поддерживался при 25°C на картофельно-декстрозном агаре (PDA; HiMedia). До этого для подтверждения патогенности грибной культуры использовались постулаты Коха. Склероции были собраны с пластинок с питательной средой, культивированы в течение 14 дней и сохранены при 4°C для дальнейших исследований.
2.3 Массовое размножение патогена
После поддержания на среде PDA гриб массово размножали на стерилизованном и автоклавированном сорго для инокуляции горшков в тепличных и полевых условиях. Зерна сорго, замоченные на ночь, стерилизовали в стеклянных колбах (по 100 г в каждой) и полиэтиленовых пакетах (примерно по 500 г каждый) и инокулировали мицелиальными дисками (с использованием бура диаметром 10 мм), взятыми с краев активно растущих культур на среде PDA. Инокулированные колбы и полиэтиленовые пакеты инкубировали в течение 10–15 дней при 28 ± 2°C (Bera и др., 2016; Jacob и др., 2018). Через 30 дней после посева (DAS) для обоих условий полевую почву и стерилизованную почву в горшках искусственно инокулировали инокулюмом патогена, который затем второй раз добавляли в полевую почву через 45 дней.
2.4 Приготовление биоугля
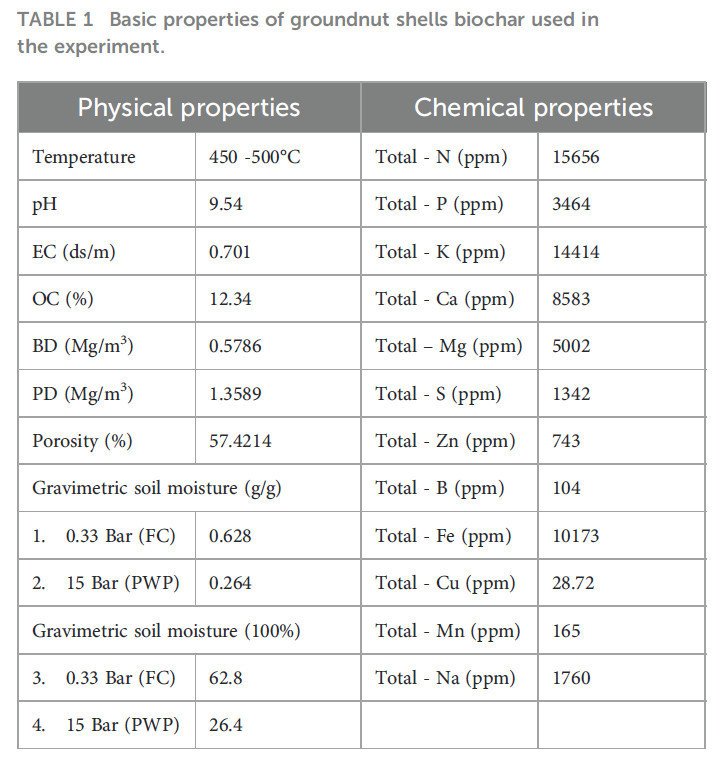
Для приготовления биоугля использовалась экономически эффективная, locally made portable kiln с одним барабаном. Размеры печи: длина 88 см, окружность 81 см, диаметр 58 см. Она имеет отверстие на верхней поверхности с крышкой для загрузки сырья размером 31×31 см. Для облегчения процесса горения на дне печи имеется около 20 отверстий диаметром 3,2 ± 0,1 см. На дно была помещена проволочная сетка, а скорлупа арахиса была взвешена и помещена в печь. Для производства биоугля использовалась скорлупа арахиса путем (медленного) пиролиза при 450–500°C в течение 60 минут. После производства биоуголь измельчается в мелкий порошок и хранится в герметичном контейнере до дальнейшего использования (Рисунок 1). Анализ образцов биоугля включал определение различных физико-химических параметров, включая органический углерод (OC) (метод Уокли-Блэка), (Nelson and Sommers, 1982), общий азот (N), фосфор (P) (Setter et al., 2020), калий (K) (Olsen and Sommers, 1982; Helmke and Sparks, 1996), серу (S) (Sparks et al., 1996), влагоемкость (WHC) (Klute, 1986), pH (Thomas, 1996), электропроводность (EC) (Rhoades, 1996), насыпную плотность (BD), плотность частиц (PD) и обменные катионы, такие как кальций (Ca), магний (Mg), натрий (Na) (Okalebo et al., 2002) (Таблица 1).
Рисунок 1 Биоуголь из скорлупы арахиса, приготовленный при 450–500°C путем медленного пиролиза. (A) Чистая скорлупа арахиса (B) Биоугленная скорлупа арахиса (C) Измельченный в порошок биоуголь.
Таблица 1 Основные свойства биоугля из скорлупы арахиса, использованного в эксперименте.
2.5 Выбор концентраций биоугля
В этом исследовании биоуголь вносился в концентрациях 1%, 3% и 5%. Эти концентрации были выбраны на основе предыдущих исследований, которые продемонстрировали их эффективность в борьбе с почвенными болезнями и улучшении здоровья растений. Wang et al. (2024) использовали концентрации биоугля до 3%, Jin et al. (2023) применяли концентрации в диапазоне от 1% до 5%, а Luigi et al. (2022) использовали концентрации биоугля от 1% до 5% для борьбы с бактериальными почвенными болезнями, фузариозным увяданием томатов и вирусными инфекциями рассады томатов соответственно. Основываясь на этих исследованиях, концентрация 3% была определена как оптимальный уровень, с дополнительными 1% и 5% концентрациями, включенными для оценки более широкого диапазона эффектов.
2.6 Морфология поверхности с помощью сканирующей электронной микроскопии
Образцы биоугля, полученные из скорлупы арахиса, были проанализированы с помощью SEM. Модель SEM Quanta FEG 250 из Эйндховена, Нидерланды, с диапазоном разрешающей способности минимум 1 нм использовалась для изучения морфологии поверхности образцов биоугля. Прибор, поддерживаемый программным обеспечением xT microscope control V6 2.8, использовался для изучения размера пор образцов биоугля. Морфология поверхности и микропоры биоугля, приготовленного в условиях пиролиза, показаны на Рисунке 2. Повышенная распространенность взаимосвязанных микропор свидетельствует об улучшении пористости биоугля.
Рисунок 2 Сканирующая электронная микроскопия (SEM) образцов биоугля из скорлупы арахиса при температуре 450°C. Показанная структура немного более плотная с несколькими видимыми полостями и комбинацией овальных и слегка неправильных форм макропор.
2.7 Оценка in vitro различных концентраций биоугля из скорлупы арахиса против патогена стеблевой гнили
Биоанализ биоугля проводился с использованием метода отравленной пищи в лаборатории для оценки эффективности различных концентраций биоугля против патогена. Среда картофельно-декстрозный агар (PDA) была приготовлена и отравлена биоуглем на уровнях 1%, 3% и 5% (1 г, 3 г и 5 г биоугля добавляли к 100 мл PDA в колбу объемом 250 мл, которую затем автоклавировали), а неотравленная среда PDA служила контролем (0%). Примерно 20 мл отравленной среды разливали в стерильные чашки Петри диаметром 90 мм и давали остыть, и все чашки инокулировали 5-миллиметровым мицелиальным диском активно растущего S. rolfsii. Каждая обработка была повторена трижды. Затем эти чашки помещали в инкубатор при 26 ± 1°C на пять дней, диаметр колонии измеряли, регистрировали и сравнивали с контролем (Schmitz, 1930).
2.8 Почвенные условия в контролируемых и полевых условиях
Эксперимент был заложен в полностью рандомизированном дизайне (CRD) для контролируемых условий и в дизайне расщепленных делянок для полевых условий. В этих экспериментах было оценено четыре обработки. Каждая обработка была повторена трижды, охватывая внесение 0% (без биоугля + инокуляция патогена стеблевой гнили -Sr), 1% (биоуголь + инокуляция патогена стеблевой гнили – BC1 + Sr), 3% (биоуголь + инокуляция патогена стеблевой гнили – BC2 + Sr) и 5% (биоуголь + инокуляция патогена стеблевой гнили – BC3 + Sr) биоугля с инокуляцией патогена. Биоуголь добавляли в почву за два дня и за тридцать дней до посева в контролируемых и полевых условиях соответственно. В контролируемых условиях тестируемые растения выращивали в шестидюймовых пластиковых горшках, заполненных стерилизованной почвой (2 кг на горшок), состоящей из смеси одной части песка и двух частей глинистой почвы, дополненной указанными концентрациями биоугля. Температура поддерживалась на уровне 26 ± 2°C. Семена каждой линии (9 семян) высевали в три горшка (по три семени в каждом горшке), что составляло три повторности. Горшки инокулировали инокулюмом патогена из расчета 8–10 г на растение. Заболеваемость (DI) регистрировали с 15-дневным интервалом после инокуляции и выражали в процентах. Горшки поливали по мере необходимости.
В полевых условиях основная делянка была разделена на четыре субделянки. Каждую перспективную селекционную линию (ABL) высевали в три ряда шириной 3 метра с расстоянием 0,5 метра между рядами и 10 см между растениями в каждой субделянке. Поддерживали три блока, и каждый блок содержал шесть основных делянок (длина 12 метров x ширина 3 метра) с тремя одинарными рядами. Блоки орошали до внесения инокулюма и инокулировали на следующий день из расчета 1,3 кг на делянку 12 м². DI регистрировали с 30-дневным интервалом после инокуляции и выражали в процентах.
Степень тяжести стеблевой гнили измеряли в тепличных условиях и выражали в процентах на 60 DAI на основе шкалы от 1 до 5, где: 1 = Здоровое растение; 2 = Поражения только на стебле; 3 = До 25% растения имеет симптомы (увядшее, мертвое или гниющее); 4 = 26–50% растения имеет симптомы; 5 = >50% растения имеет симптомы (Divya Rani et al., 2018) (Рисунок 3).
Рисунок 3 Оценка инокулированных растений после внесения биоугля в контролируемых условиях. Стрелки указывают на уровень распространения инфекции на растении. 1 = Здоровое растение; 2 = Поражения только на стебле; 3 = До 25% растения имеет симптомы (увядшее, мертвое или гниющее); 4 = 26–50% растения имеет симптомы; 5 = >50% растения имеет симптомы (Divya Rani et al., 2018).
Где: a = количество заболевших растений с одинаковой степенью заражения, b = степень заражения, A = общее количество растений, K = наивысшая степень заражения.
2.9 Отбор и анализ почвы
По окончании эксперимента почву отбирали из ризосферной области каждой обработки в поле и анализировали для определения pH почвы, OC, EC, доступного азота, доступного фосфора, доступного калия и активности ферментов, таких как дегидрогеназа, уреаза и сахараза, следуя стандартным протоколам. Активность уреазы оценивали с использованием мочевины в качестве субстрата по методу Yao et al. (2006). Пять граммов влажной почвы инкубировали с 1 мл метилбензола, 10 мл 10% раствора мочевины и 20 мл цитратного буфера (pH 6,7) при 37°C в течение 24 часов. После инкубации добавляли 1 мл фильтрованного почвенного экстракта, 1 мл фенолята натрия и 3 мл гипохлорита натрия, и смесь разбавляли до 50 мл. Абсорбцию затем измеряли при 578 нм с помощью спектрофотометра (Shimadzu corp. УФ-спектрофотометр), и активность уреазы выражали как NH3-N г⁻¹ ч⁻¹ при 37°C.
Активность дегидрогеназы оценивали с использованием хлорида трифенилтетразолия (TTC) в качестве субстрата по Thalmann (1968). Раствор TTC (0,3–0,4 г/100 мл) смешивали с 5 г влажной почвы и инкубировали в течение 24 часов при 30°C. После инкубации добавляли 40 мл ацетона, и абсорбцию измеряли при 546 нм с помощью спектрофотометра (Shimadzu corp. УФ-спектрофотометр). Активность дегидрогеназы выражали как мкг TTC г⁻¹ ч⁻¹.
Активность сахаразы определяли путем измерения содержания глюкозы после инкубации в течение 24 часов при 37°C с сахарозой в качестве субстрата. Для определения активности сахаразы 5 г высушенной на воздухе почвы инкубировали в течение 24 часов при 37°C с 15 мл 8% сахарозы, 5 мл фосфатного буфера при pH 5,5 и 0,1 мл толуола. Раствор фильтровали, затем добавляли раствор 3,5-динитросалициловой кислоты моногидрата. Высвобожденная сахаразой глюкоза реагировала с 3,5-динитросалициловой кислотой, и затем ее измеряли на основе абсорбции при 508 нм с помощью спектрофотометра (Shimadzu corp. УФ-спектрофотометр). Результаты выражали как мг глюкозы г⁻¹ ч⁻¹ (Wu et al., 2020).
Четыре повторности каждой субпробы для трех ферментов были проанализированы. Более того, для каждой пробы были добавлены контроли без субстрата и без почвы для учета неферментативного гидролиза субстрата.
2.10 Определение обилия S. rolfsii в почве
Количество S. rolfsii, присутствующего в почве, оценивали с использованием метода, адаптированного из Wang et al., 2013. Через 30 дней после инокуляции патогена 10 граммов свежесобранной почвы добавляли в колбы с 90 мл стерильной воды, затем разбавляли до концентрации 10⁻⁶. Почвенную суспензию наносили на среду PDA и инкубировали в инкубаторе в течение двух дней. Для определения количества S. rolfsii в почве использовали метод подсчета колоний на пластинках. Аналогично, почву отбирали во время сбора урожая и следовали той же процедуре, чтобы узнать процент снижения популяции S. rolfsii в почве.
2.11 Определение плотности микробных популяций в почве
Плотность популяций бактерий и грибов оценивали с использованием метода разведения Мартина (Martin, 1950). PDA использовали в качестве питательной среды для бактерий и грибов. 10 граммов свежей почвы собирали и добавляли в колбы с 90 мл стерильной воды, затем встряхивали в течение 30 минут при 150 об/мин на шейкере. После этого 100 мкл супернатанта из каждой пробы смешивали с 900 мкл стерильной воды в 2-мл стерильной центрифужной пробирке. Центрифужную пробирку встряхивали на вортексе для тщательного перемешивания раствора. Затем раствор разбавляли до концентраций 10⁻³ и 10⁻⁷ для анализа бактерий и грибов соответственно. Эти разведения наносили на соответствующие питательные среды и затем помещали в инкубатор, поддерживаемый при 30°C. Бактериальные культуры инкубировали в течение 2 дней, а грибные культуры – в течение 5 дней. После периода инкубации регистрировали количество колоний для определения плотности различных микробных популяций.
2.12 Статистический анализ
Двухфакторный полностью рандомизированный дизайн (CRD) и дизайн расщепленных делянок были использованы для лабораторных и полевых экспериментов соответственно. В обоих случаях было включено три повторности. Данные были статистически проанализированы с использованием программного обеспечения SPSS 16. Перед проведением ANOVA предположения о нормальности и однородности дисперсии были проверены с помощью критерия Шапиро-Уилка и критерия Бартлетта соответственно. Пост-хок анализ проводился с использованием множественного рангового критерия Дункана (DMRT) и непараметрического критерия Краскела-Уоллиса для выявления значимых различий между средними значениями обработок, с дальнейшим разделением средних, проведенным с использованием метода критической разницы (CD).
3 Результаты
3.1 Эффективность различных концентраций биоугля против патогена стеблевой гнили при оценке in vitro
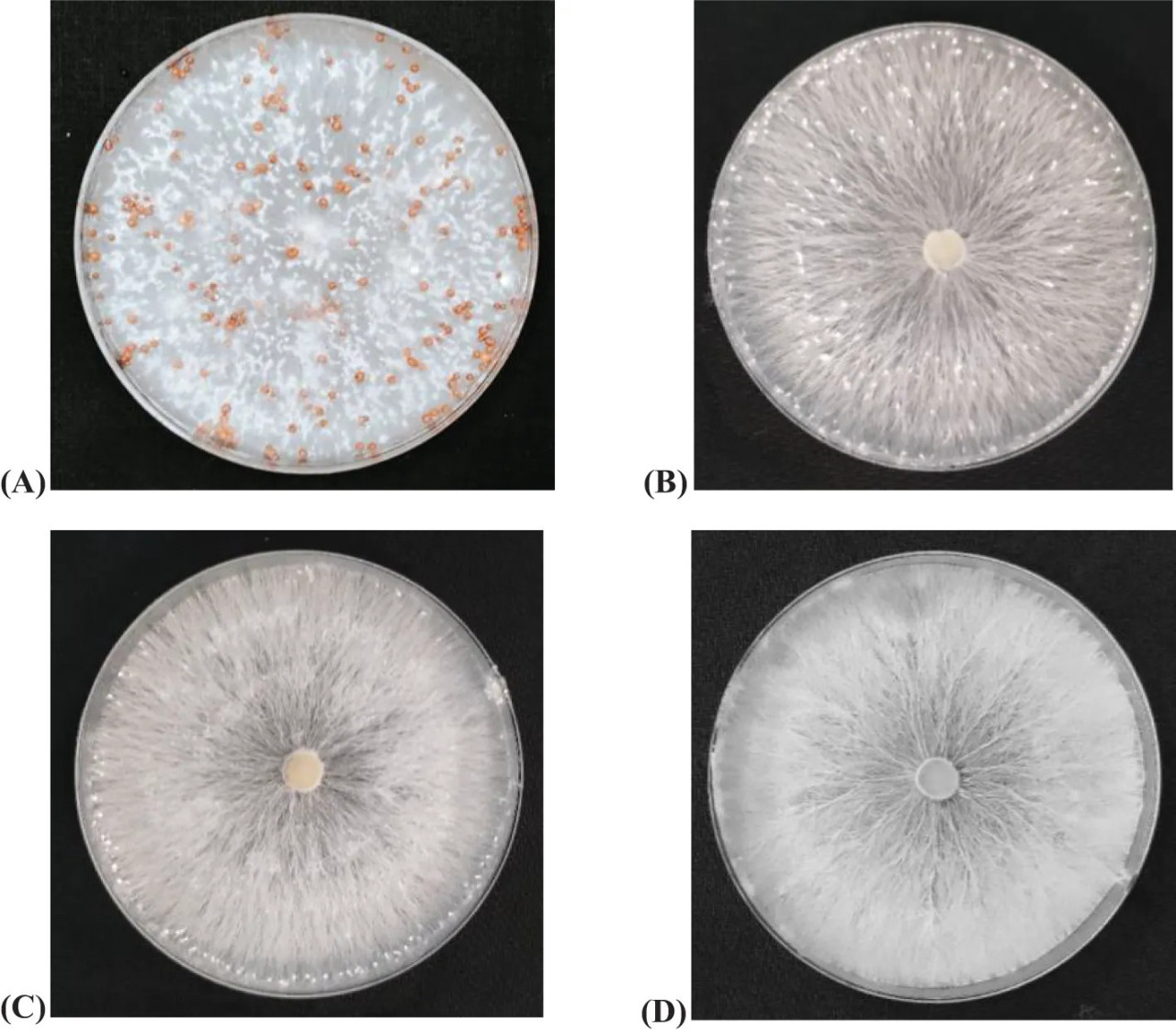
В методе отравленной пищи, проведенном в лабораторных условиях, были исследованы различные концентрации биоугля (0%, 1%, 3% и 5%) против патогена стеблевой гнили. Интересно, что не наблюдалось явных прямых ингибирующих эффектов биоугля ни на одном уровне концентрации против патогена стеблевой гнили по сравнению с контролем (0% конц.). Однако при более тщательном рассмотрении стало очевидным косвенное подавление образования склероциев с увеличением концентрации биоугля по сравнению с контролем. Эти результаты свидетельствуют о сложном взаимодействии между концентрацией биоугля и его влиянием на формирование склероциев патогена стеблевой гнили (Рисунок 4).
Рисунок 4 Эффективность различных концентраций биоугля против патогена стеблевой гнили при оценке in vitro (A) Контроль (B) 1% конц. (C) 3% конц. (D) 5% конц. Фотографии были сделаны через 14 дней после наблюдений.
3.2 Влияние внесения биоугля на заболеваемость
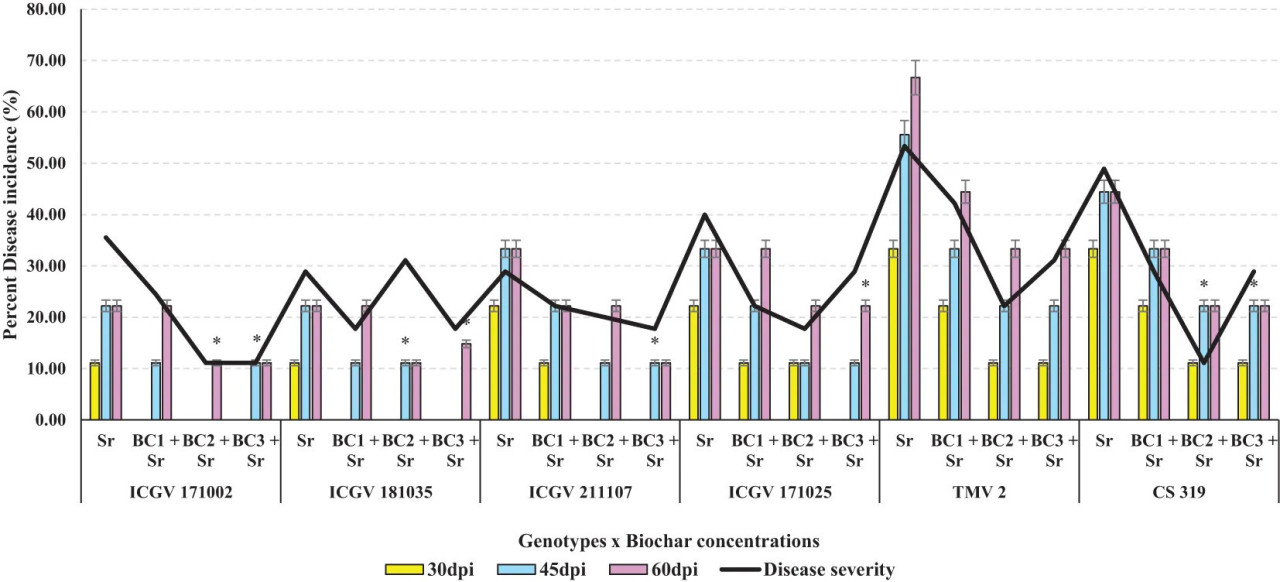
Симптомы стеблевой гнили проявились в группе, инокулированной S. rolfsii (Sr), через семь дней после инокуляции (dpi). Однако в группе, обработанной биоуглем, эти симптомы были отсрочены до десяти дней после инокуляции, что указывает на замедление пролиферации патогена, вызванное биоуглем. Обе обработки биоуглем эффективно сдерживали прогрессирование болезни и повышали устойчивость растений арахиса к заболеванию. Из 4 оцененных ABL ICGV 171002 показал наименьший PDI, за ним следовали ICGV 181035, ICGV 211107 и ICGV 171025 по сравнению с контролями (критерий DMRT, p < 0,05). Из четырех примененных различных концентраций биоугля обработка BC3 + Sr оказалась эффективной, за ней следовали BC2 + Sr, BC1 + Sr по сравнению с одним Sr. Среди взаимодействий между генотипами и BC, ICGV 171002 x BC2 + Sr и BC3 + Sr, ICGV 181035 x BC2 + Sr и ICGV 211107 x BC3 + Sr показали 11,11% заболеваемости, за ними следовали ICGV 181035 x BC2+ Sr с 14,81% заболеваемости, ICGV 171002 x BC1 + Sr, ICGV 181035 x BC2+ Sr, ICGV 211107 x BC2+ Sr и BC3 + Sr, ICGV 171025 и CS 319 x BC2 + Sr и BC3 + Sr с 22,22% заболеваемости на 60 dpi. Эти результаты свидетельствуют о том, что генотипы испанского и вирджинского типов с длительным периодом вегетации (ICGV 181035 и ICGV 171002 соответственно) и с взаимодействиями BC2 + Sr и BC3 + Sr более эффективны, чем другие взаимодействия, в значительном снижении заболеваемости стеблевой гнилью арахиса в контролируемых условиях (Рисунки 5, 6). Фотографии инокулированных контрольных горшков не включены на Рисунок 6.
Рисунок 5 Показатели перспективных селекционных линий (ABL) арахиса и различных норм внесения биоугля против S. rolfsii, оцененные в контролируемых условиях в 2023 году. (p < 0,05 – значительно).
Рисунок 6 Показатели различных концентраций биоугля из скорлупы арахиса на выбранных ABL: (A) ICGV 171002, (B) ICGV 181035, (C) CS 319 и (D) TMV 2 против патогена стеблевой гнили. Здоровое растение, без биоугля и без инокуляции S. rolfsii (Sr); 1% концентрация, 1% концентрация биоугля и инокуляция S. rolfsii (BC1+Sr); 3% концентрация, 3% концентрация биоугля и инокуляция S. rolfsii (BC2+Sr); 5% концентрация, 5% концентрация биоугля и инокуляция S. rolfsii (BC3+Sr). Фотографии были сделаны по окончании эксперимента (120 DAS).
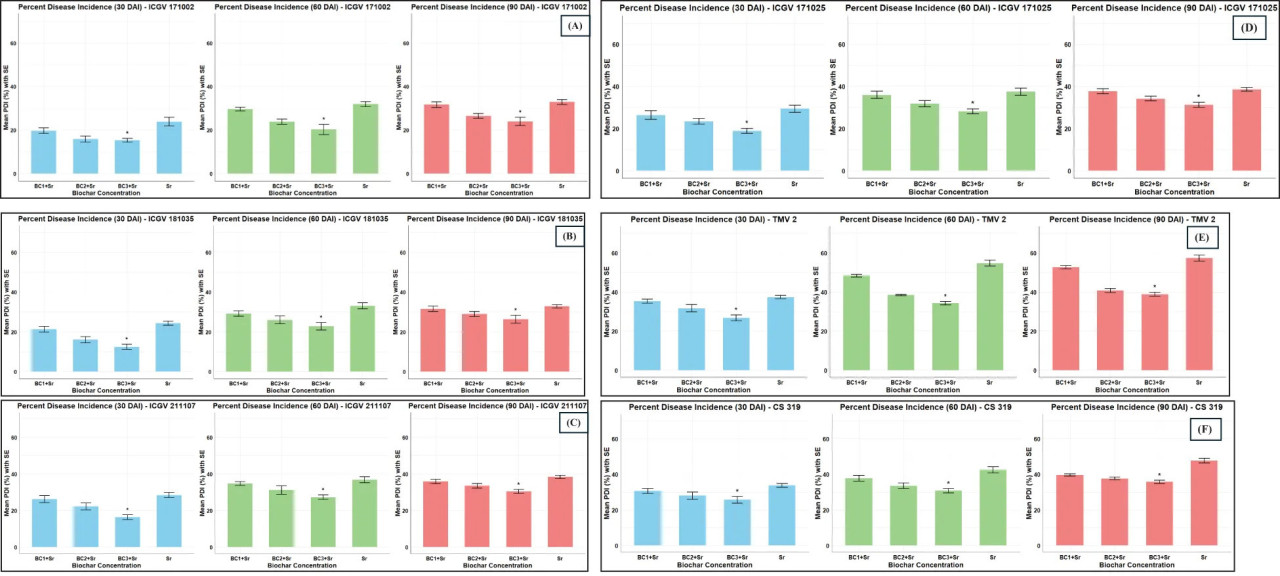
В полевых условиях среди четырех оцененных ABL ICGV 171002 показал самый низкий PDI, за ним следовали ICGV 181035, ICGV 171025 и ICGV 211107 по сравнению с контролями. Среди протестированных вариантов BC не было заметной разницы между эффективностью обработок BC2 + Sr и BC3 + Sr в борьбе со стеблевой гнилью по сравнению с одним Sr. Что касается взаимодействий генотип-BC, заболеваемость составила 16,62% для ICGV 171002 x BC3+ Sr, 19,79% для ICGV 181035 x BC3 + Sr, 19,91% для ICGV 171002 x BC2 + Sr, 23,51% для ICGV 181035 x BC2 + Sr, 27,51% для ICGV 171002 x BC1 + Sr и 27,46% для ICGV 181035 x BC1 + Sr по сравнению с контролями и инокулированными контролями на 90 dpi (Рисунок 7).
Рисунок 7 Прогрессирование заболевания во времени для различных ABL: (A) ICGV 171002, (B) ICGV 181035, (C) ICGV 211107, (D) ICGV 171025, (E) TMV 2, (F) CS 319. Подавляющие эффекты внесения биоугля (при четырех разных концентрациях, а именно: Sr – без биоугля и без внесения S. rolfsii; BC1+Sr – 1% концентрация биоугля и инокуляция S. rolfsii; BC2+Sr – 3% концентрация биоугля и внесение S. rolfsii; BC3+Sr – 5% концентрация биоугля и инокуляция S. rolfsii) на S. rolfsii на ABL арахиса через три разных интервала после инокуляции. (p < 0,05 – значительно).
3.3 Влияние биоугля на свойства почвы
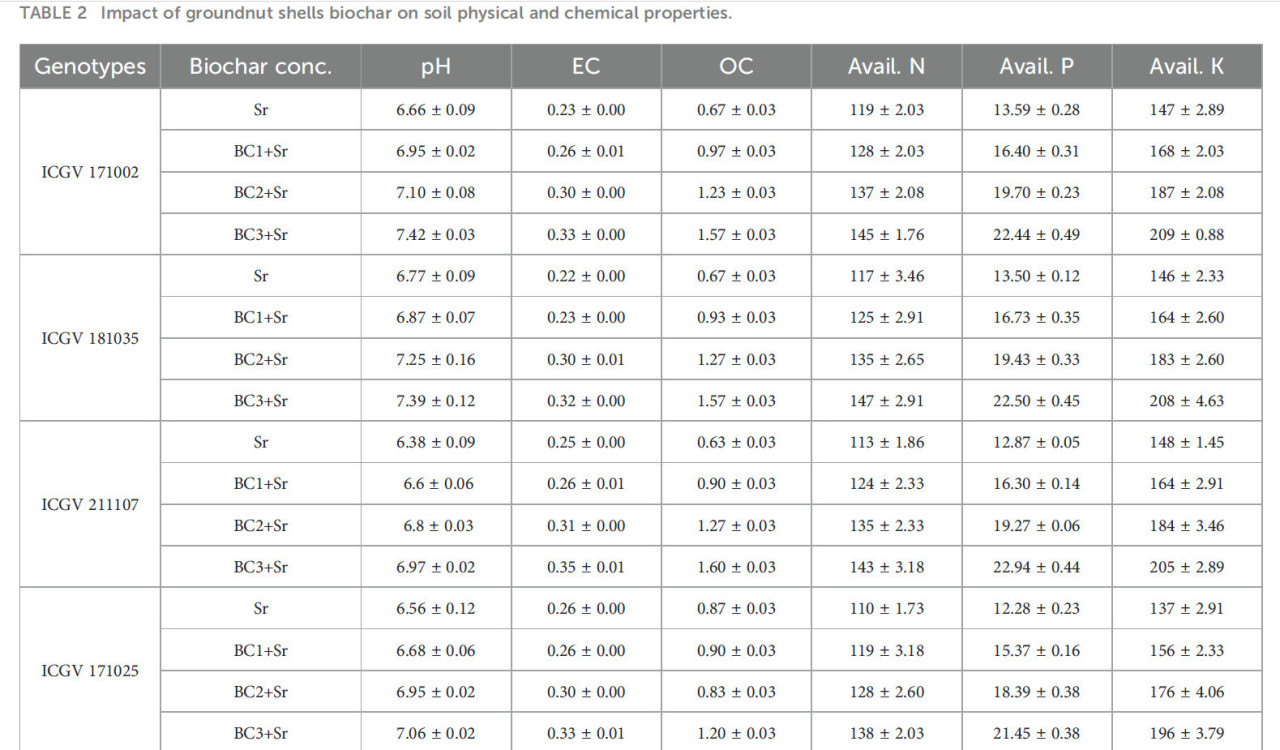
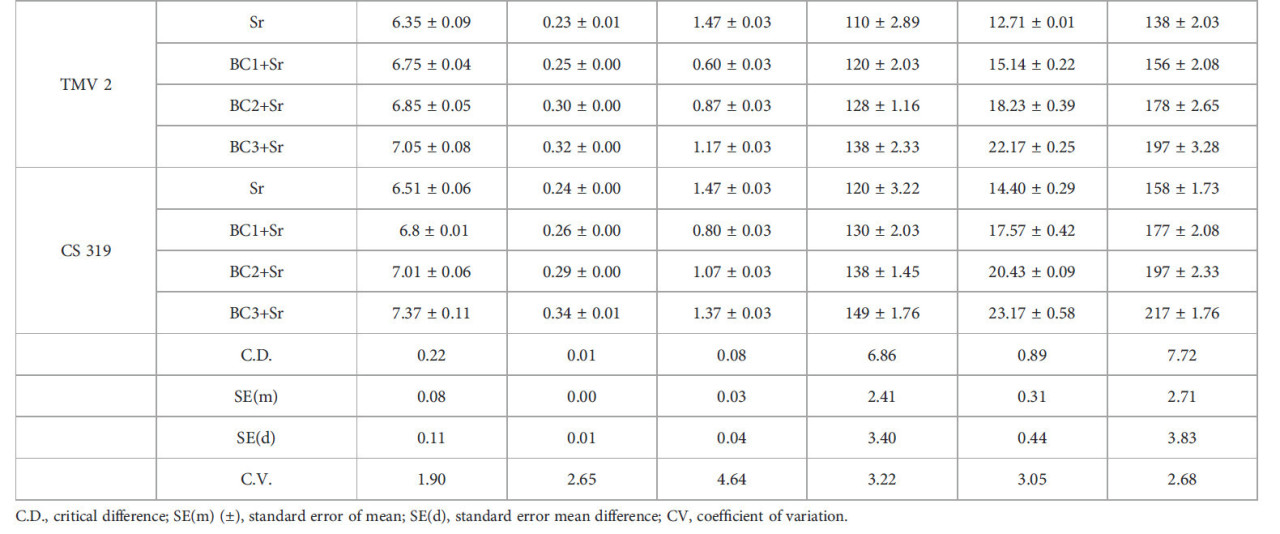
На физические и химические параметры почвы значительно (P < 0,05) повлияло внесение биоугля. Результаты недвусмысленно показывают, что добавление биоугля значительно улучшает физические и химические характеристики почвы у различных генотипов арахиса, в частности при более высоких концентрациях (BC3+Sr). Повышение pH, электропроводности, органического углерода и доступных питательных веществ (N, P и K) являются некоторыми из этих улучшений. Эти изменения предполагают, что биоуголь может быть полезной почвенной добавкой для повышения продуктивности сельскохозяйственных культур и плодородия почвы, особенно в почвах с низким содержанием органического вещества или дефицитом питательных веществ. Более того, хотя существуют генотипспецифичные реакции на биоуголь, общая закономерность свидетельствует о том, что преимущества биоугля универсальны для многих типов арахиса. За счет повышения pH внесение биоугля снижает кислотность почв у всех генотипов. Повышение pH варьируется в зависимости от генотипа и уровня биоугля примерно от 0,2 до 1,0 единицы. Более высокие концентрации биоугля показывают устойчивое увеличение EC, что указывает на повышенную ионную активность в почве, которая может влиять на засоление и доступность питательных веществ. Поскольку биоуголь содержит много углерода и может улучшать органическое вещество почвы, его содержание драматически растет с увеличением содержания биоугля. Биоуголь улучшает доступность азота, что полезно для роста растений. Это может быть результатом улучшенных условий для азотфиксирующих бактерий и более высокого удержания азота. Повышенная доступность фосфора предполагает, что биоуголь либо высвобождает фосфор, либо улучшает свойства почвы, которые облегчают поглощение и растворение фосфора. Прямой вклад биоугля или лучшее удержание питательных веществ предполагается повышенной доступностью калия с биоуглем. Это свидетельствует о том, что добавление биоугля в почву в количестве 3–5% может улучшить ее химические и физические характеристики (Таблица 2).
Таблица 2 Влияние биоугля из скорлупы арахиса на физические и химические свойства почвы.
C.D. – критическая разница; SE(m) (±) – стандартная ошибка среднего; SE(d) – стандартная ошибка разности средних; CV – коэффициент вариации.
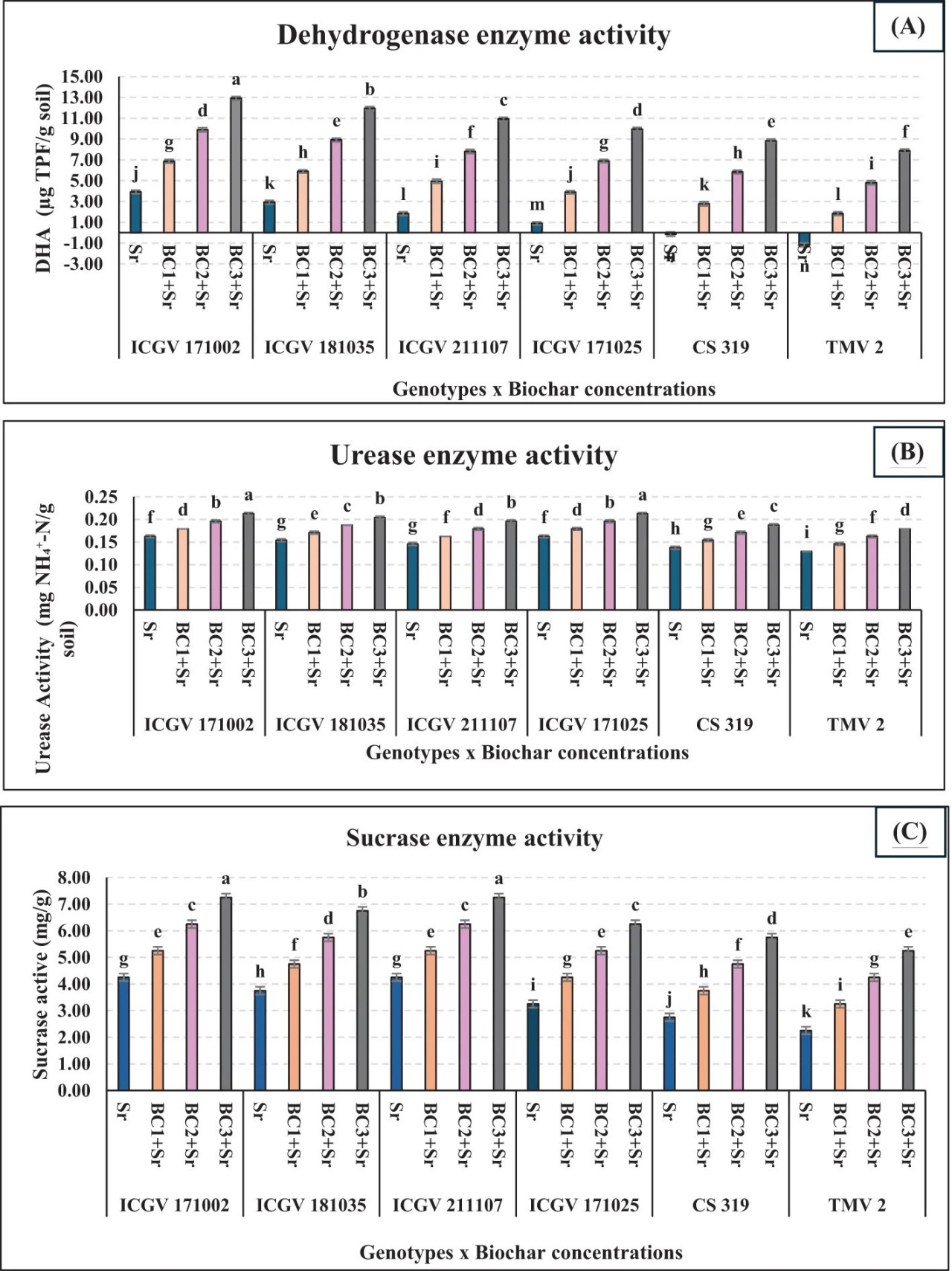
Что касается активности почвенных ферментов, активность уреазы, сахаразы и дегидрогеназы в почве, обработанной биоуглем (BC2 и BC3), у всех генотипов значительно увеличилась (P < 0,05), что свидетельствует о том, что внесение биоугля в диапазоне 3–5% может улучшить активность почвенной уреазы, сахаразы и дегидрогеназы по сравнению с 1% и контролем. Активность этих ферментов является прямым индикатором почвенной микробной активности. Высокая активность этих ферментов означает активный микробный метаболизм, отражая здоровые и плодородные почвенные условия. Мониторинг этих ферментативных активностей предоставляет ценную информацию о здоровье почвы, эффективности практик управления почвой и прогрессе работ по восстановлению почвы. Таким образом, ферменты служат ключевым связующим звеном в понимании и оценке почвенной микробной динамики (Рисунок 8).
Рисунок 8 Эффективность биоугля из скорлупы арахиса на активность почвенных ферментов: (A) Активность дегидрогеназы, (B) Активность уреазы, (C) Активность сахаразы. На графике буквы (a–d и т.д.), присвоенные каждому столбцу, представляют результаты статистических сравнений, обычно из ANOVA с последующим пост-хок анализом. Каждая буква обозначает группы, которые значительно не отличаются друг от друга; столбцы, имеющие одинаковую букву, указывают на отсутствие значимой разницы в измеряемом параметре между этими группами, в то время как столбцы с разными буквами обозначают статистически значимые различия.
3.4 Обилие микроорганизмов в почве
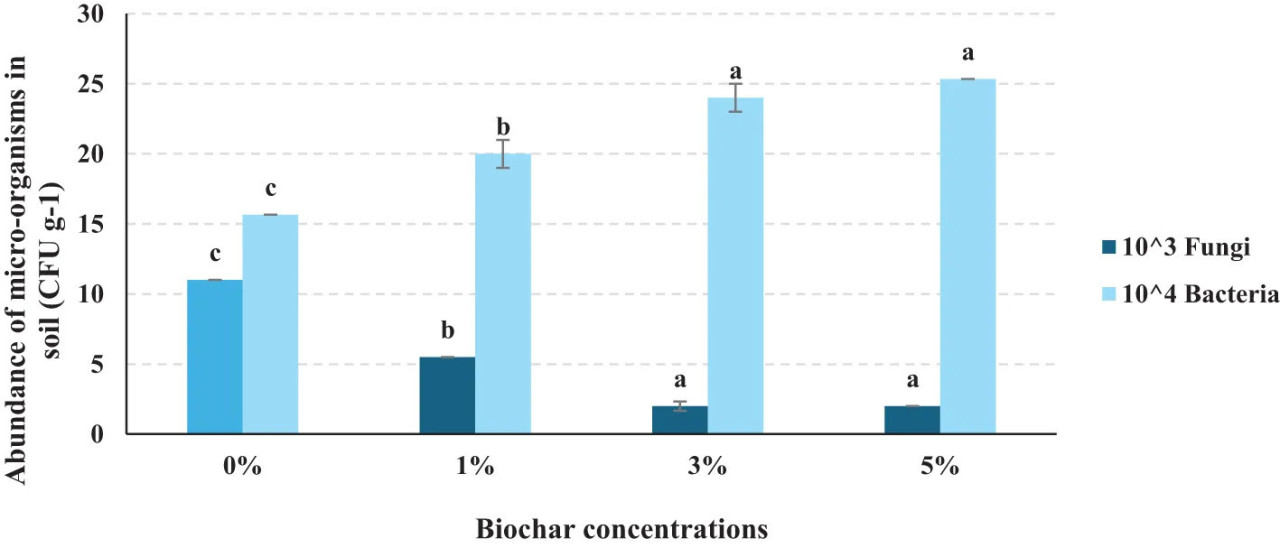
Этот анализ подчеркивает влияние биоугля на обилие грибов и бактерий в почве, обработанной S. rolfsii. Данные свидетельствуют о том, что внесение биоугля смещает микробный баланс, значительно увеличивая бактериальные популяции в почве, потенциально улучшая здоровье почвы и снижая грибковые популяции, что может помочь бороться с такими грибными патогенами, как S. rolfsii. Бактерии процветают в почве с более высокими концентрациями биоугля, показывая значительное увеличение от 0% до 3% и стабилизируясь на уровне 5% (критерий DMRT, p < 0,05). Рекомендуются дальнейшие исследования для изучения долгосрочных эффектов биоугля на почвенную микробную динамику и оптимизации концентраций биоугля для различных типов почв и культур (Рисунок 9).
Рисунок 9 Обилие микробных популяций в почве после внесения биоугля и инокуляции S. rolfsii в почву. 10³ и 10⁴ указывают, при каких разведениях грибные и бактериальные популяции были обильны в разных концентрациях биоугля. На графике буквы (a–c), присвоенные каждому столбцу, представляют результаты статистических сравнений, обычно из ANOVA с последующим пост-хок анализом. Каждая буква обозначает группы, которые значительно не отличаются друг от друга; столбцы, имеющие одинаковую букву, указывают на отсутствие значимой разницы в измеряемом параметре между этими группами, в то время как столбцы с разными буквами обозначают статистически значимые различия.
3.5 Популяции Sclerotium rolfsii в почве
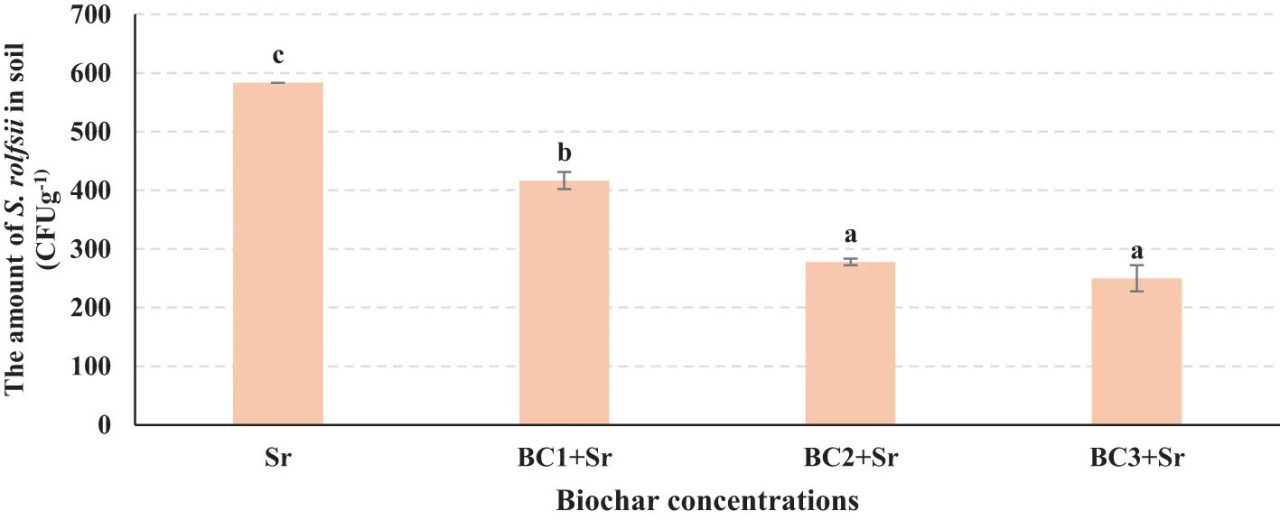
Внесение инокулюма S. rolfsii значительно увеличило популяции S. rolfsii в почве на 58,33%. Однако в почвах, обработанных биоуглем, количество S. rolfsii было значительно ниже по сравнению с контролем (Sr). Популяции S. rolfsii в почве были снижены на 28,57% в BC1+Sr, на 52,38% в BC2+Sr и на 57,14% в BC3+Sr. Патоген подавляется в почве с увеличением концентраций биоугля, показывая значительное снижение от 0% до 3% и стабилизируясь на уровне 5% (критерий DMRT, p < 0,05) (Рисунок 10).
Рисунок 10 Популяция Sclerotium rolfsii в почве, обработанной биоуглем. Серийное разведение объединенных образцов почвы из шести генотипов арахиса, смешанных в соответствии с концентрацией биоугля (0%, 1%, 2% и 4%). Образцы были приготовлены путем объединения почвы из всех генотипов на каждом уровне концентрации. На графике буквы (a–c), присвоенные каждому столбцу, представляют результаты статистических сравнений, обычно из ANOVA с последующим пост-хок анализом. Каждая буква обозначает группы, которые значаще не отличаются друг от друга; столбцы, имеющие одинаковую букву, указывают на отсутствие значимой разницы в измеряемом параметре между этими группами, в то время как столбцы с разными буквами обозначают статистически значимые различия.
4 Обсуждение
Борьба с патогеном стеблевой гнили арахиса является ключевой проблемой для устойчивого сельского хозяйства. Обычные методы включают севооборот, химические фунгициды и биологические агенты борьбы для управления этим почвенным патогеном. Тем не менее, эти методы часто имеют ограничения, такие как их воздействие на окружающую среду, развитие устойчивости и стоимость. Поэтому необходимы инновационные и экологически безопасные подходы для улучшения борьбы с болезнями и продуктивности сельскохозяйственных культур. В последние годы биоуголь привлек внимание благодаря своим многогранным преимуществам. Исследования показали, что биоуголь, богатый углеродом продукт, получаемый из органических материалов путем пиролиза, улучшает здоровье почвы, повышает удержание питательных веществ и влияет на почвенные микробные сообщества. Основываясь на недавних исследованиях, биоуголь может косвенно подавлять почвенные патогены, изменяя pH почвы, увеличивая популяции полезных микробов и улучшая структуру почвы. В этом контексте наше исследование изучило использование биоугля из скорлупы арахиса в качестве нового подхода для борьбы со стеблевой гнилью растений арахиса. Скорлупа арахиса, обильный сельскохозяйственный побочный продукт, предоставляет ценный ресурс для производства биоугля. Использование биоугля из скорлупы арахиса перерабатывает отходы и обеспечивает устойчивое решение для борьбы с болезнями.
Наши оценки in vitro концентраций биоугля (0%, 1%, 3% и 5%) против патогена стеблевой гнили, проведенные с использованием метода отравленной пищи, выявили интригующую закономерность. Вопреки первоначальным ожиданиям, не было прямого ингибирующего эффекта на патоген во всех концентрациях биоугля по сравнению с контролем. Этот результат подразумевает, что основной механизм действия биоугля может не включать прямую антимикробную активность. Вместо этого наше исследование выявило, что по мере увеличения концентраций биоугля производство склероциев косвенно подавлялось. SEM-анализ биоугля в нашем исследовании выявил высокопористую поверхность с взаимосвязанными микропорами. Эта морфология, вероятно, играет ключевую роль в косвенном подавлении патогена за счет увеличения поверхности для микробной колонизации. Микропоры не только удерживают влагу и питательные вещества, но и становятся средой обитания для полезных микробов, которые могут конкурировать с популяциями патогенов. Это подавление указывает на сложное взаимодействие, при котором биоуголь может влиять на условия окружающей среды или динамику питательных веществ таким образом, что ухудшает покоящиеся структуры патогена. Похожие результаты были показаны Jaiswal et al. (2014) и Lehmann et al. (2011), которые обнаружили, что внесение биоугля в почву может изменить доступность питательных веществ и микробную активность, что косвенно влияет на жизнеспособность патогена. Lehmann и коллеги отметили, что биоуголь может усилить метаболомические процессы, улучшить структуру почвы, удержание питательных веществ и способствовать развитию полезных микробных сообществ, что может создать среду, менее благоприятную для выживания и размножения патогенов. Это поддерживает гипотезу о том, что эффективность биоугля в подавлении патогенов стеблевой гнили обусловлена его способностью изменять почвенную микросреду, усиливая конкурентное преимущество полезных микробов над патогенами.
Тот факт, что наше исследование выявило косвенное ингибирование развития склероциев, подчеркивает, насколько важно понимать сложные взаимосвязи между микробными сообществами, почвенными питательными веществами и биоуглем. Многие почвенные болезни, включая S. rolfsii, зависят от склероциев для своего долгосрочного выживания и распространения. Уменьшая производство склероциев, биоуголь может эффективно снизить способность патогена выживать в почве, тем самым уменьшая частоту заболеваний в последующих посевах. Этот механизм действия указывает на потенциал биоугля как устойчивой почвенной добавки, которая не только улучшает здоровье почвы, но и предоставляет долгосрочную стратегию борьбы с почвенными болезнями.
При переносе этих результатов на полевые условия необходимо учитывать дополнительные переменные, такие как состав почвы, погодные условия и взаимодействия растений с микроорганизмами, которые в частности присутствуют в полевых условиях. Полевые эксперименты предоставляют доказательства того, как косвенное воздействие биоугля на репродуктивные структуры патогена влияет на заболеваемость и здоровье растений в течение вегетационного периода. Наши полевые исследования подтвердили лабораторные результаты, показав, что внесение биоугля (особенно в концентрациях 3% и 5%) эффективно задерживало начало симптомов и снижало заболеваемость. Это поддерживает представление о том, что биоуголь создает менее благоприятные условия для пролиферации патогена, повышая устойчивость растений.
Более того, наше исследование оценило четыре ABL арахиса, среди которых ICGV 171002 показал самый низкий PDI, за ним следовали ICGV 181035, ICGV 211107 и ICGV 171025. Эти результаты подчеркивают генетическую изменчивость устойчивости к болезням среди сортов арахиса. Эффективность обработок биоуглем варьировалась при разных концентрациях (BC3 + Sr, BC2 + Sr, BC1 + Sr, Sr), при этом обработка BC3 + Sr и BC2 + Sr показала наивысшую эффективность в снижении заболеваемости по сравнению с контролем в контролируемых условиях. Это согласуется с исследованиями, указывающими на потенциал биоугля улучшать здоровье почвы и жизнеспособность растений, тем самым снижая восприимчивость к болезням (Jeffery et al., 2011). В полевых условиях обе обработки BC2 + Sr и BC3 + Sr эффективно контролировали стеблевую гниль по сравнению с контролем, хотя значимой разницы между их эффективностью не было. Однако конкретные взаимодействия генотип-биоуголь влияли на исходы заболеваний, при этом ICGV 171002 и ICGV 181035 стабильно демонстрировали самый низкий PDI в разных условиях, что указывает на внутренние генетические признаки, повышающие их устойчивость к патогену. Это может быть связано с дифференциальной экспрессией связанных с защитой генов, при которой определенные генотипы активируют белки, связанные с патогенезом (PR-белки), фенольные соединения или другие защитные механизмы в ответ на патогены. Кроме того, эти генотипы могут иметь лучше развитые корневые системы, а также способность биоугля улучшать удержание питательных веществ в почве, укреплять защиту растений (Kaur et al., 2017). Обработки с большей эффективностью также указывают на то, что концентрация биоугля значительно влияет на подавление болезней, создавая оптимальную среду ризосферы для устойчивых генотипов. Различия в реакциях генотипов на обработки биоуглем также могут быть связаны со способностью модулировать почвенную микробиоту и реагировать на влияние биоугля на гормональные сигнальные пути растений, дальнейше усиливая их защитные реакции. Эти результаты подчеркивают важность выбора подходящих генотипов арахиса и оптимизации стратегий внесения биоугля для максимизации преимуществ борьбы с болезнями в реальных полевых условиях. Наблюдаемые расхождения между лабораторными и полевыми результатами, в частности в отношении эффективности различных концентраций биоугля между BC2+Sr и BC3+Sr, могут быть связаны с несколькими факторами. Полевые условия создают более сложную среду, где колеблющиеся уровни влажности, температурные вариации и различные микробные взаимодействия могут влиять на эффективность биоугля. Кроме того, свойства почвы в поле, включая содержание органического вещества, pH и микробное разнообразие, отличаются от контролируемых условий, потенциально изменяя то, как биоуголь взаимодействует с почвой и патогенами. Более того, лабораторные условия могут быть оптимизированы, в то время как полевые среды часто создают конкурентное давление со стороны других микроорганизмов, что может повлиять на борьбу с патогеном.
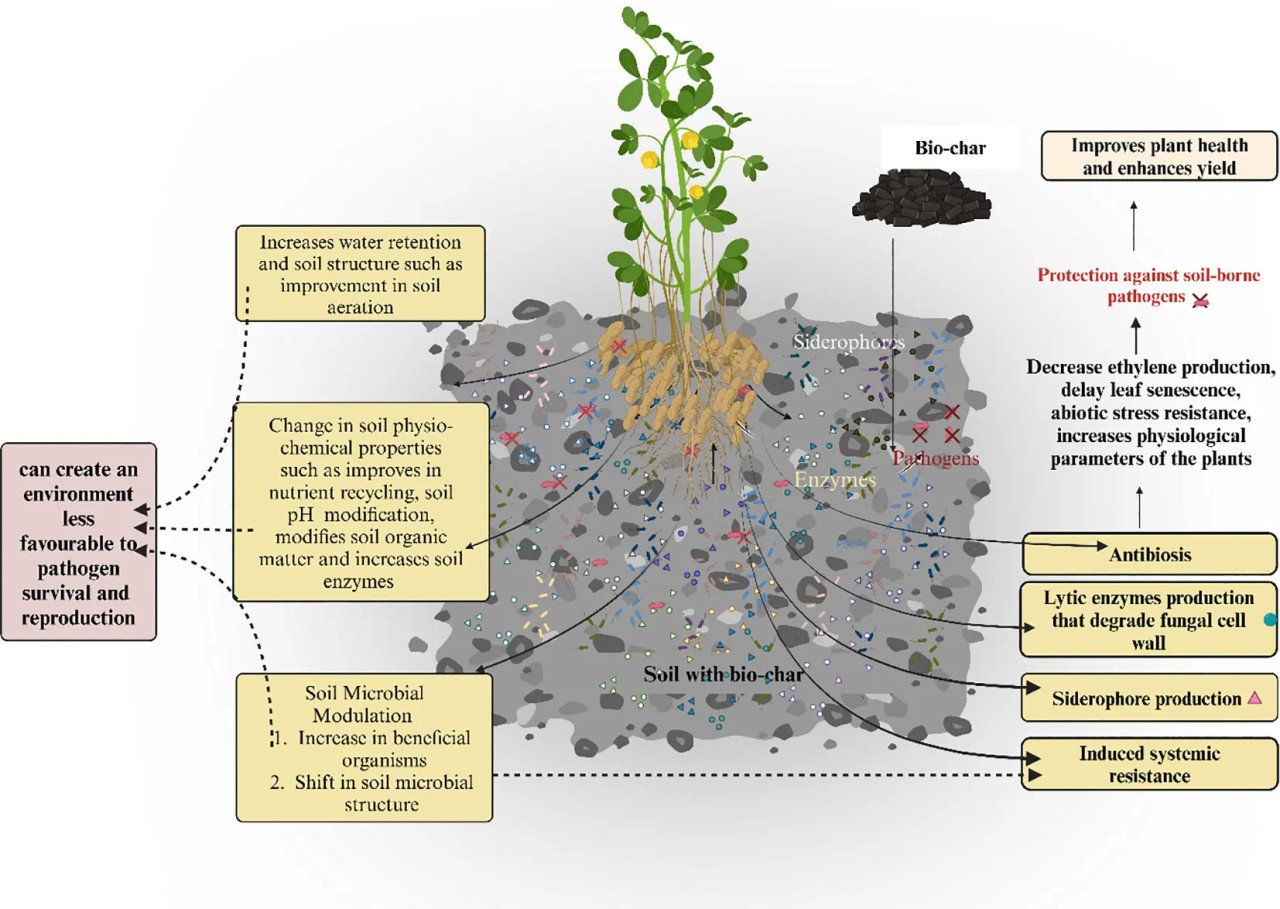
Было показано, что биоуголь изменяет обилие и разнообразие микробных популяций в почве. В нашем исследовании плотность бактерий увеличивалась, а плотность грибов уменьшалась по мере увеличения концентрации биоугля. Предыдущие исследования показали, что почва с нейтральным и слабощелочным pH оказывает стимулирующее влияние на рост бактерий, но оказывает ингибирующее действие на грибы. Кроме того, pH может косвенно влиять на микробиом, изменяя молекулярную структуру родного почвенного органического вещества. Почвенная микробная активность количественно определяет функцию почвы, особенно в циклах углерода и азота и разложении органического вещества (Ameloot et al., 2013). Биологическое разложение органических и минеральных компонентов почвы непосредственно опосредовано почвенными ферментами. Специфические для почвы активности ферментов, такие как активность уреазы, сахаразы, фосфатазы и дегидрогеназы, необходимы для круговорота питательных веществ в почве и могут использоваться для измерения почвенной микробной активности и оценки здоровья почвы. Измерение функции почвы включает измерение почвенной микробной активности, в частности в циклах азота и углерода и разложении органического вещества. Некоторые ферменты, такие как гидралаза и глюкозидаза, способствуют разложению органических веществ. Между тем, ферменты, такие как амидаза, уреаза, фосфатаза и сульфатаза, отвечают за минерализацию питательных веществ. Уреаза, фосфатаза и арилсульфатаза играют ключевую роль в разложении соединений азота, фосфора и серы. Кроме того, может существовать значимая корреляция между почвенными ферментами и подавлением болезней. Некоторые ферменты, такие как хитиназы и глюканазы, могут повышать устойчивость растений к инфекциям, расщепляя полисахариды, хитин и β-глюканы, которые способствуют прочности клеточной стенки грибов. Этот процесс в конечном итоге приводит к разрушению целостности клеточной стенки. В своем исследовании Baek et al. (1999) обнаружили хорошую корреляцию между активностью фермента хитиназы и способностью контролировать болезнь рассады хлопчатника, вызываемую Rhizoctonia solani. Согласно Woo et al. (1999), способность биологического контроля бороться с B. cinerea на листьях фасоли была снижена при нарушении активности хитиназы. Предыдущие исследования показали, что биотические стрессы могут вызывать активацию иммунитета растений (системная устойчивость), который может действовать, чтобы изменить микробиом, обогащая микробы, которые, вероятно, приносят пользу защите растений. Поэтому мы предполагаем, что более высокий положительный эффект 3% и 5% биоугля по сравнению с другими дозами на ABL арахиса и подавление стеблевой гнили был связан с их различным влиянием на разнообразие и состав микробных сообществ ризосферы, особенно более высоким стимулирующим влиянием на некоторые бактерии, которые обладают потенциалом стимуляции роста растений и подавления патогенов. Механизм, лежащий в основе косвенного подавления патогена после внесения биоугля в почву, кратко описан на Рисунке 11.
Рисунок 11 Схематическое представление механизмов, участвующих в косвенном подавлении S. rolfsii.
В заключение, наше исследование предоставляет убедительные доказательства того, что биоуголь из скорлупы арахиса может эффективно подавлять стеблевую гниль, изменяя почвенные условия и усиливая механизмы устойчивости растений. Будущие исследования должны дальше изучать определение оптимальных норм внесения для различных культур и почв, оценку влияния сроков внесения и изучение того, как различные типы биоугля влияют на здоровье почвы. Кроме того, понимание того, как биоуголь взаимодействует с различными почвенными условиями и другими почвенными мелиорантами, оценка его долгосрочных эффектов, требуется ли повторное внесение, если да, то как часто, и оценка его экономических и экологических последствий.
5 Заключение
Общие результаты нашего исследования показывают, что внесение биоугля косвенно ингибирует рост патогена стеблевой гнили, повышает устойчивость растений к болезням, улучшает плодородие почвы и вызывает благоприятные изменения в почвенных микробных сообществах. Сложные взаимодействия биоугля с почвой и патогенами подчеркивают необходимость дальнейших исследований для оптимизации его использования в различных сельскохозяйственных условиях и типах почв. Забегая вперед, исследования должны быть сосредоточены на долгосрочных последствиях внесения биоугля, его влиянии на широкий круг патогенов и механизмах, с помощью которых биоуголь влияет на взаимодействия растение-микроб-патоген. Используя многогранные преимущества биоугля, могут быть разработаны устойчивые методы ведения сельского хозяйства для улучшения здоровья и урожайности сельскохозяйственных культур при одновременном снижении инфекционного давления.
Дополнительный материал
Дополнительный материал к этой статье можно найти онлайн по адресу: https://www.frontiersin.org/articles/10.3389/fagro.2024.1470194/full#supplementary-material
Ссылки
1. Akhter A., Hage-Ahmed K., Soja G., Steinkellner S. (2015). Compost and biochar alter mycorrhization, tomato root exudation, and development of Fusarium oxysporum f. sp. lycopersici. Front. Plant Science. 6. doi: 10.3389/fpls.2015.00529. CrossRef Google Scholar
2. Ameloot N., Graber E. R., Verheijen F. G., De Neve S. (2013). Interactions between biochar stability and soil organisms: review and research needs. Eur. J. Soil Science. 64, 379–390. doi: 10.1111/ejss.12064. CrossRef Google Scholar
3. Antal M. J., Gronli M. (2003). The art, science, and technology of charcoal production. Ind. Eng. Chem. Res. 42, 1619–1640. doi: 10.1021/ie0207919. CrossRef Google Scholar
4. Baek J. M., Howell C. R., Kenerley C. M. (1999). The role of an extracellular chitinase from Trichoderma virens Gv29-8 in the biocontrol of Rhizoctonia solani. Curr. Genet. 35, 41–50. doi: 10.1007/s002940050431. CrossRef Google Scholar
5. Bera S. K., Kamdar J. H., Kasundra S. V., Thirumalaisami P. P. (2016). Identification of groundnut genotypes and wild species resistant to stem rot using an efficient field screening technique. Electronic J. Plant Breeding. 7, 61–70. doi: 10.5958/0975-928X.2016.00009.0. CrossRef Google Scholar
6. Bera S. K., Kasundra S. V., Kamdar J. H., BCA., Lal C., Thirumalasmy P. P., et al. (2014). Variable response of interspecific breeding lines of groundnut to Sclerotium rolfsii infection under field and laboratory conditions. Electronic J. Plant Breeding. 5, 22–29. Google Scholar
7. Chen S., Qi G., Ma G., Zhao X. (2020). Biochar amendment controlled bacterial wilt through changing soil chemical properties and microbial community. Microbiological Res. 231, 126373. doi: 10.1016/j.micres.2019.126373. CrossRef Google Scholar
8. Divya Rani V., Sudini H., Narayan Reddy P., Vijay Krishna Kumar K., Uma Devi G. (2018). Resistance screening of groundnut advanced breeding lines against collar rot and stem rot pathogens. Int. J. Pure Appl. Bioscience. 6, 467–474. doi: 10.18782/2320-7051.5494. CrossRef Google Scholar
9. Elad Y., David D. R., Harel Y. M., Borenshtein M., Kalifa H. B., Silber A., et al. (2010). Induction of systemic resistance in plants by biochar, a soil-applied carbon sequestering agent. Phytopathology. 100, 913–921. doi: 10.1094/PHYTO-100-9-0913. CrossRef Google Scholar
10. Gaskin J. W., Steiner C., Harris K., Das K. C., Bibens B. (2008). Effect of low-temperature pyrolysis conditions on biochar for agricultural use. Trans. ASABE. 51, 2061–2069. doi: 10.13031/2013.25409. CrossRef Google Scholar
11. Graber E. R., Elad Y. (2013). Biochar impact on plant resistance to disease. Biochar Soil biota. 21, 278. doi: 10.1201/b14585-3. CrossRef Google Scholar
12. Graber E. R., Frenkel O., Jaiswal A. K., Elad Y. (2014). How may biochar influence severity of diseases caused by soilborne pathogens? Carbon Manage. 5, 169–183. doi: 10.1080/17583004.2014.913360. CrossRef Google Scholar
13. Graber E. R., Meller Harel Y., Kolton M., Cytryn E., Silber A., Rav David D., et al. (2010). Biochar impact on development and productivity of pepper and tomato grown in fertigated soilless media. Plant soil. 337, 481–496. doi: 10.1007/s11104-010-0544-6. CrossRef Google Scholar
14. Gu Y., Hou Y., Huang D., Hao Z., Wang X., Wei Z., et al. (2017). Application of biochar reduces Ralstonia solanacearum infection via effects on pathogen chemotaxis, swarming motility, and root exudate adsorption. Plant Soil. 415, 269–281. doi: 10.1007/s11104-016-3159-8. CrossRef Google Scholar
15. Helmke P. A., Sparks D. L. (1996). Lithium, sodium, potassium, rubidium, and cesium. In: Methods of soil analysis: Part 3 chemical methods. (Madison: Soil Science Society) 5, 551–574. doi: 10.2136/sssabookser5.3.c19. CrossRef Google Scholar
16. Jacob S., Sajjalaguddam R. R., Sudini H. K. (2018). Streptomyces sp. RP1A-12 mediated control of peanut stem rot caused by Sclerotium rolfsii. J. Integr. agriculture. 17, 892–900. doi: 10.1016/S2095-3119(17)61816-1. CrossRef Google Scholar
17. Jaiswal A. K., Elad Y., Graber E. R., Frenkel O. (2014). Rhizoctonia solani suppression and plant growth promotion in cucumber as affected by biochar pyrolysis temperature, feedstock and concentration. Soil Biol. Biochem. 69, 110–118. doi: 10.1016/j.soilbio.2013.10.051. CrossRef Google Scholar
18. Jaiswal A. K., Elad Y., Paudel I., Graber E. R., Cytryn E., Frenkel O. (2017). Linking the belowground microbial composition, diversity and activity to soilborne disease suppression and growth promotion of tomato amended with biochar. Sci. Rep. 7, 44382. doi: 10.1038/srep44382. CrossRef Google Scholar
19. Jaiswal A. K., Frenkel O., Elad Y., Lew B., Graber E. R. (2015). Non-monotonic influence of biochar dose on bean seedling growth and susceptibility to Rhizoctonia solani: the "Shifted R max-Effect". Plant soil. 395, 125–140. doi: 10.1007/s11104-014-2331-2. CrossRef Google Scholar
20. Jeffery S., Verheijen F. G., van der Velde M., Bastos A. C. (2011). A quantitative review of the effects of biochar application to soils on crop productivity using meta-analysis. Agriculture Ecosyst. environment. 144, 175–187. doi: 10.1016/j.agee.2011.08.015. CrossRef Google Scholar
21. Jin X., Zhou X., Wu F., Xiang W., Pan K. (2023). Biochar amendment suppressed Fusarium wilt and altered the rhizosphere microbial composition of tomatoes. Agronomy. 13, 1811. doi: 10.3390/agronomy13071811. CrossRef Google Scholar
22. Kaur H., Salh P. K., Singh B. (2017). Role of defense enzymes and phenolics in resistance of wheat crop (Triticum aestivum L.) towards aphid complex. J. Plant Interactions. 12, 304–311. doi: 10.21203/rs.3.rs-2779843/v1. CrossRef Google Scholar
23. Klute A. (1986). Water retention: Laboratory methods. In: *Methods of soil analysis: Part 1-Physical and mineralogical methods.* (Madison: American Society of Agronomy, Soil Science Society of America), 635–662. doi: 10.2136/sssabookser5.1.2ed.c26. CrossRef Google Scholar
24. Kumar N. V., Sawargaonkar G., Rani C. S., Pasumarthi R., Kale S., Prakash T. R., et al. (2024). Harnessing the potential of pigeon pea and maize feedstock biochar for carbon sequestration, energy generation, and environmental sustainability. Bioresources Bioprocessing. 11, 5. doi: 10.1186/s40643-023-00719-3. CrossRef Google Scholar
25. Lehmann J., Rillig M. C., Thies J., Masiello C. A., Hockaday W. C., Crowley D. (2011). Biochar effects on soil biota--a review. Soil Biol. Biochem. 43, 1812–1836. doi: 10.1016/j.soilbio.2011.04.022. CrossRef Google Scholar
26. Luigi M., Manglli A., Dragone I., Antonelli M. G., Contarini M., Speranza S., et al. (2022). Effects of biochar on the growth and development of tomato seedlings and on the response of tomato plants to the infection of systemic viral agents. Front. Microbiol. 13. doi: 10.3389/fmicb.2022.862075. CrossRef Google Scholar
27. Mahatma M. K., Thawait L. K., Jadon K. S., Thirumalaisamy P. P., Bishi S. K., Jadav J. K., et al. (2018). Metabolic profiles of groundnut (Arachis hypogaea L.) genotypes differing in Sclerotium rolfsii reaction. Eur. J. Plant Pathology. 151, 463–474. doi: 10.1007/s10658-017-1387-2. CrossRef Google Scholar
28. Martin J. P. (1950). Use of acid, rose bengal, and streptomycin in the plate method for estimating soil fungi. Soil science. 69, 215–232. doi: 10.1097/00010694-195003000-00006. CrossRef Google Scholar
29. Mehan V. K., Mayee C. D., McDonald D. (1994). Management of Sclerotium rolfsii-caused stem and pod rots of groundnut---a critical review. Int. J. Pest Manag. 40, 313–320. doi: 10.1080/09670879409371906. CrossRef Google Scholar
30. Meller Harel Y., Elad Y., Rav-David D., Borenstein M., Shulchani R., Lew B., et al. (2012). Biochar mediates systemic response of strawberry to foliar fungal pathogens. Plant Soil. 357, 245–257. doi: 10.1007/s11104-012-1129-3. CrossRef Google Scholar
31. Nelson D. W., Sommers L. E. (1982). Total carbon, organic carbon, and organic matter. In: Methods of soil analysis: Part 2 chemical and microbiological properties. (Madison: American Society of Agronomy, Soil Science Society of America), 9, 539–579. doi: 10.2134/agronmonogr9.2.2ed.c29. CrossRef Google Scholar
32. Nogiya R., Mahatma M. K., Gowda A., Raval S. S., Rathod V., Gajera H. P., et al. (2021). Changes in expression of polyamines and ethylene biosynthesis genes in groundnut (Arachis hypogaea L.) genotypes during Sclerotium rolfsii infection. Indian J. Exp. Biol. (IJEB). 59, 476–483. doi: 10.56042/ijeb.v59i07.53158. CrossRef Google Scholar
33. Okalebo J. R., Gathua K. W., Woomer P. L. (2002). Laboratory methods of soil and plant analysis: a working manual. 2nd ed. Vol. 21 (Nairobi: Sacred Africa), pp. 25–26. Google Scholar
34. Olsen S. R., Sommers E. L. (1982). Phosphorus soluble in sodium bicarbonate. In: Methods of soil analysis, part, 2. (Madison: American Society of Agronomy, Soil Science Society of America), 404–430. Google Scholar
35. Pasumarthi R., Sawargaonkar G., Kale S., Kumar N. V., Choudhari P. L., Singh R., et al. (2024). Innovative bio-pyrolytic method for efficient biochar production from maize and pigeonpea stalks and their characterization. J. Cleaner Production. 448, 141573. doi: 10.1016/j.jclepro.2024.141573. CrossRef Google Scholar
36. Rani V. D., Sudini H., Reddy P. N., Devi G. U., Kumar K. V. K. (2022). Integrated Management of Stem Rot and Collar Rot Diseases of Groundnut incited by Aspergillus Niger and Sclerotium rolfsii. Biol. Forum 14, 1524–1530. Google Scholar
37. Rhoades J. D. (1996). Salinity: Electrical conductivity and total dissolved solids. In: Methods of soil analysis: Part 3 Chemical methods. (Madison: Soil Science Society of America), 5, 417–435. doi: 10.2136/sssabookser5.3.c14. CrossRef Google Scholar
38. Schmitz H. (1930). Poisoned food technique. Ind. Eng. Chemistry-Analytical Edition. 2, 361–363. Google Scholar
39. Setter C., Borges F. A., Cardoso C. R., Mendes R. F., Oliveira T. J. P. (2020). Energy quality of pellets produced from coffee residue: Characterization of the products obtained via slow pyrolysis. Ind. Crops Products. 154, 112731. doi: 10.1016/j.indcrop.2020.112731. CrossRef Google Scholar
40. Sparks D. L., Page A. L., Helmke P. A., Loeppert R. H., Soltanpour P. N., Tabatabai M. A., et al. (1996). Methods of soil analysis, part 3: Chemical methods (Madison: Soil Science Society of America) 14. doi: 10.2136/sssabookser5.3. CrossRef Google Scholar
41. Sunkad G., Poornima S. H., Naik M. (2016). Diagnosis of stem and pod rot of groundnut and their management. Indian Phytopathology. 69, 38–40. Google Scholar
42. Thalmann A. (1968). Zur Metodik der Bestimmung der De-hydrogenaseaktivität im Boden mittels Triphenyltetrazo-liumchlorid (TTC). Landwirtsch Forsch. 21, 249–258. Google Scholar
43. Thomas G. W. (1996). Soil pH and soil acidity. In: Methods of soil analysis: part 3 chemical methods. (Madison: American Society of Agronomy, Soil Science Society of America), 5, 475–490. doi: 10.2136/sssabookser5.3.c16. CrossRef Google Scholar
44. Tian J. H., Shuang R. A. O., Yang G. A. O., Yang L. U., Cai K. Z. (2021). Wheat straw biochar amendment suppresses tomato bacterial wilt caused by Ralstonia solanacearum: Potential effects of rhizosphere organic acids and amino acids. J. Integr. Agriculture. 20, 2450–2462. doi: 10.1016/S2095-3119(20)63455-4. CrossRef Google Scholar
45. Wang L., Cai K., Chen Y., Wang G. (2013). Silicon-mediated tomato resistance against Ralstonia solanacearum is associated with modification of soil microbial community structure and activity. Biol. Trace element Res. 152, 275–283. doi: 10.1007/s12011-013-9611-1. CrossRef Google Scholar
46. Wang S., Wang L., Li S., Zhang T., Cai K. (2024). The win--win effects of an invasive plant biochar on a soil--crop system: controlling a bacterial soilborne disease and stabilizing the soil microbial community network. Microorganisms. 12, 447. doi: 10.3390/microorganisms12030447. CrossRef Google Scholar
47. Woo S. L., Donzelli B., Scala F., Mach R., Harman G. E., Kubicek C. P., et al. (1999). Disruption of the ech42 (endochitinase-encoding) gene affects biocontrol activity in Trichoderma harzianum P1. Mol. Plant-Microbe Interactions. 12, 419–429. doi: 10.1094/MPMI.1999.12.5.419. CrossRef Google Scholar
48. Wu J., Wang H., Li G., Ma W., Wu J., Gong Y., et al. (2020). Vegetation degradation impacts soil nutrients and enzyme activities in wet meadow on the Qinghai-Tibet Plateau. Sci. Rep. 10, 21271. Google Scholar
49. Yao X.-H., Min H., Lu Z.-H., Yuan H.-P. (2006). Influence of acetamiprid on soil enzymatic activities and respiration. Eur. J. Soil Biol. 42, 120–126. doi: 10.1016/j.ejsobi.2005.12.001. CrossRef Google Scholar
50. Zhang C., Lin Y., Tian X., Xu Q., Chen Z., Lin W. (2017). Tobacco bacterial wilt suppression with biochar soil addition associates to improved soil physiochemical properties and increased rhizosphere bacteria abundance. Appl. Soil Ecology. 112, 90–96. doi: 10.1016/j.apsoil.2016.12.005. CrossRef Google Scholar
51. Zhang D., Yan M., Niu Y., Liu X., van Zwieten L., Chen D., et al. (2016). Is current biochar research addressing global soil constraints for sustainable agriculture? Agriculture Ecosyst. environment. 226, pp. 25–32. doi: 10.1016/j.agee.2016.04.010. CrossRef Google Scholar
52. Zhang X., Wang H., He L., Lu K., Sarmah A., Li J., et al. (2013). Using biochar for remediation of soils contaminated with heavy metals and organic pollutants. Environ. Sci. pollut. Res. 20, 8472–8483. doi: 10.1007/s11356-013-1659-0. CrossRef Google Scholar
Manasa R, Devi RSJ, Vemana K, John K, Rao GR, Anubhava PJ, Vidyashree LK, Sri Ananth K, Santosh K, Sawargaonkar G and Sudini HK (2024) Biochar as a strategy to manage stem rot disease of groundnut incited by Sclerotium rolfsii. Front. Agron. 6:1470194. doi: 10.3389/fagro.2024.1470194
Перевод статьи «Biochar as a strategy to manage stem rot disease of groundnut incited bySclerotium rolfsii» авторов Manasa R, Devi RSJ, Vemana K, John K, Rao GR, Anubhava PJ, Vidyashree LK, Sri Ananth K, Santosh K, Sawargaonkar G and Sudini HK., оригинал доступен по ссылке. Лицензия: CC BY. Изменения: переведено на русский язык


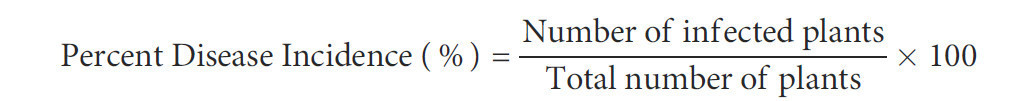

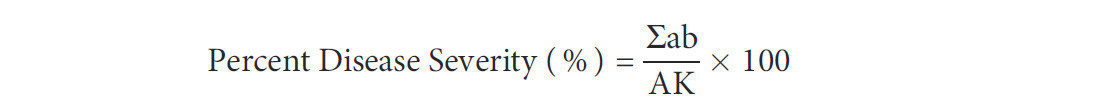











































































































Комментарии (0)