Вешенка против нематод: природная защита баклажанов
Борьба с галловыми нематодами в основном основывалась на использовании химических веществ, которые наносят вред окружающей среде и здоровью человека. Биологический контроль предлагает альтернативный метод управления. В данном исследовании оценивался потенциал использования Pleurotus ostreatus (вешенки обыкновенной), съедобного вида грибов, для борьбы с Meloidogyne spp. на баклажанах.
Методы: In vitro оценивали смертность ювенильных особей (J2) Meloidogyne spp. при воздействии: i) водной суспензии P. ostreatus с активно растущим мицелием и ii) различных разведений фильтрата культуры P. ostreatus, выращенной на картофельно-декстрозном бульоне (PDB). В вегетационном домике нематоцидный потенциал P. ostreatus испытывали на баклажанах, используя искусственно зараженную почву. Для этого ювенильных особей (J2) Meloidogyne spp. вносили в основание растений в горшках, содержащих зерна проса, колонизированные P. ostreatus, смешанные с 3 кг почвы. Оценивали индекс галлообразования (GI) (по шкале от 0 до 5), рост корней и популяции нематод в различных вариантах обработки.
Результаты и обсуждение: Смертность нематод в водной суспензии P. ostreatus со временем значительно возрастала, достигая более 88% через 48 часов и 95% через 72 часа. Смертность в неразбавленном фильтрате была стабильно значительно выше, чем в разбавленных фильтратах и в контроле без P. ostreatus. Смертность в неразбавленном фильтрате увеличилась до 95% через 48 часов. При смешивании 50 г просяной культуры P. ostreatus с 3 кг автоклавированной почвы в горшке наблюдался GI 0,95, который снизился до 0,70 при удвоении инокулюма до 100 г. Для обработки без P. ostreatus был зафиксирован высокий GI — 2,4. Было обнаружено значимое различие в росте корней баклажана и популяции нематод (p = 0,02) между всеми обработками. Результаты этого исследования, полученные как в опытах in vitro, так и в вегетационных опытах, позволяют предположить, что P. ostreatus и его субстрат являются потенциальными биологическими агентами борьбы с фитопаразитическими нематодами на баклажанах.
1 Введение
Баклажан (Solanum melongena L.) является важной овощной культурой семейства Пасленовых (Solanaceae) (Taher и др., 2017). Баклажаны богаты кальцием, магнием, железом, аминокислотами, витаминами и антиоксидантами, которые необходимы для здоровья человека (Sharma и Kaushik, 2021). Баклажан занимает пятое место по экономической значимости среди пасленовых культур после картофеля (Solanum tuberosum), томатов (Solanum lycopersicum), перца (Capsicum annuum) и табака (Nicotiana tabacum) (Taher и др., 2017). В 2021 году мировой объем торговли баклажанами оценивался более чем в 10 миллиардов долларов США при объеме производства около 56 миллионов тонн, что на 32% больше, чем в 2010 году (FAOSTAT, 2022).
Производство баклажанов сильно ограничивается галловыми нематодами (RKN, Meloidogyne spp.). RKN являются печально известными, седентарными эндопаразитами, которые могут вызывать потерю урожая до 60% (Khan и др., 2021). Заражение RKN начинается с проникновения в корни личинок второй стадии (J2) после вылупления в почве из яиц, отложенных самками и хранящихся в яйцевых мешках на зараженных корнях. Во время проникновения в корни личинки второй стадии (J2), которые являются повреждающей стадией Meloidogyne spp., пронзают ткани корня растения с помощью своего выдвижного стилета. Точки проникновения, созданные этими нематодами, также служат входными воротами для других вторичных патогенов, что влияет на качество растения и, следовательно, снижает урожайность. Попав в корневую систему, J2 создает место питания (галлы) и начинает питаться. Образовавшиеся галлы препятствуют поглощению воды и питательных веществ растением, что приводит к снижению урожайности (Coyne и др., 2018).
Как правило, было разработано несколько вариантов борьбы для решения проблемы RKN. Использование устойчивых к Meloidogyne spp. сортов может предоставить эффективную стратегию для снижения повреждающего воздействия RKN. Однако доступно лишь несколько устойчивых сортов, и устойчивость может быть преодолена новыми появляющимися видами RKN (Xiang и др., 2018; Hajihassani и др., 2019). Прививка на устойчивый к RKN подвой, такой как Solanum torvum и S. palinacanthum, является одной из наиболее устойчивых стратегий борьбы с RKN (Goodell, 2010; Gisbert и др., 2011; Murata и др., 2022). Тем не менее, эта практика по-прежнему ограничена некоторыми высокодоходными производственными системами в Европе и Азии из-за ее запретительно высокой стоимости (Goodell, 2010). Другие агротехнические методы борьбы, такие как совместные посадки или севооборот с нехозяевами, парование, борьба с сорняками, солнечная дезинфекция почвы, внесение органических мелиорантов, уничтожение зараженных корней после уборки урожая и использование здоровой рассады, могут снизить популяции нематод (Goodell, 2010; Noling, 2014). В то время как химическая борьба является наиболее распространенной краткосрочной стратегией борьбы с RKN (Coyne и др., 2018), она создает проблемы для окружающей среды и здоровья человека. Таким образом, разработка экологически безопасных и устойчивых альтернативных мер борьбы с RKN остается приоритетом. Использование биологических агентов борьбы (BCA) в борьбе с вредителями и болезнями растений предлагает экологически безопасную альтернативу благодаря их безопасности для человека и нецелевых организмов (Lacey и др., 2001; Lopez-Llorca и др., 2008). Сообщалось о нескольких BCA против фитопаразитических нематод, включая нематофаговые грибы и бактерии, ризобактерии, стимулирующие рост растений, арбускулярные микоризные грибы и хищных нематод (Abd-Elgawad, 2016; Atif и др., 2023). В настоящее время не хватает эффективных и коммерчески доступных BCA для успешной борьбы с нематодами в условиях фермерских хозяйств. В этом исследовании мы изучаем потенциал съедобного вида грибов Pleurotus ostreatus и его отходов в качестве BCA для борьбы с RKN на баклажанах.
Сообщалось, что некоторые съедобные грибы, включая Pleurotus ostreatus (вешенка обыкновенная), который относится к роду Pleurotus, семейству Pleurotacea, порядку Agaricales и классу Basidiomycetes, подавляют фитопаразитических нематод на различных культурах, таких как кукуруза (Zea mays), салат (Lactuca sativa), томаты и соя (Glycine max) (Okorie и др., 2011; Wille и др., 2019). Механизм действия этих грибов включает хищничество, прямое проникновение грибных гиф в нематоду, а также выработку токсинов (Barron и Thorn, 1987; Kwok и др., 1992; Zouhar и др., 2013; Hahn и др., 2019). В исследовании, проведенном Genier и др. (2015), было обнаружено, что P. ostreatus (PO) воздействует на личинок Panagrellus sp., свободноживущего вида нематод, путем прямого захвата и запутывания их с помощью своих грибных гиф и оказывает нематоцидное действие через свои протеазы. Исследования in vitro, проведенные Heydari и др. (2006), показали, что PO и другие виды Pleurotus продуцируют крошечные капли, которые были токсичны и способствовали колонизации личинок Meloidogyne javanica в течение 24–48 часов. Авторы также наблюдали, что фильтраты P. ostreatus обладают нематоцидной активностью против нематоды. В другом исследовании in vitro, проведенном Kanaujiya и др. (2022), было обнаружено, что PO парализует и убивает различные виды фитопаразитических нематод, причем M. incognita пострадала больше всего. Таким образом, PO также может быть нематоциден по отношению к RKN на баклажанах. Помимо нематоцидного действия, благодаря своему влиянию на разложение органических отходов, виды Pleurotus могут также способствовать росту растений (Hahn и др., 2019; Ocimati и др., 2021; Youssef и El-Nagdi, 2021). Таким образом, грибные субстраты потенциально могут быть использованы для борьбы с нематодами на широком спектре культур.
2 Материалы и методы
2.1 Штамм гриба, нематоды и химикаты
Чистая культура P. ostreatus была получена из Центра инкубации грибов Национальных сельскохозяйственных исследовательских лабораторий (NARL)-Каванда. Гриб поддерживали путем повторного субкультивирования каждые 12 дней на половинной концентрации твердой среды картофельно-декстрозного агара (PDA) при 28°C. Личинки Meloidogyne spp. были экстрагированы из сильно зараженного растения краснокочанной капусты (Brassica oleracea) с использованием модифицированного метода воронки Бермана (Coyne и Ross, 2014) и размножены на восприимчивом сорте томата, выращенном в горшках с автоклавированной почвой в вегетационном домике для последующих исследований. Все химикаты, если не указано иное, были приобретены у Sigma-Aldrich (Штайнхайм, Германия).
2.2 Оценка in vitro влияния P. ostreatus на выживаемость личинок Meloidogyne spp.
В лабораторных условиях влияние P. ostreatus на выживаемость личинок Meloidogyne spp. оценивали с помощью: i) суспензии мицелия P. ostreatus в воде и ii) фильтрата культуры P. ostreatus на картофельно-декстрозном бульоне (PDB). Суспензия P. ostreatus в воде была направлена на определение эффекта как активного хищничества мицелия, так и метаболитов P. ostreatus, тогда как фильтрованный PDB – культура P. ostreatus был направлен на удаление всего активно растущего мицелия и спор, чтобы оценить только потенциальный эффект вторичных метаболитов.
2.2.1 Влияние водной суспензии Pleurotus ostreatus на выживаемость личинок Meloidogyne spp.
Для приготовления водной суспензии P. ostreatus активно растущую 7-дневную культуру мицелия P. ostreatus, покрывающую всю поверхность чашки Петри диаметром 90 мм, содержащей PDA, осторожно соскребали стерильным скальпелем и переносили в стерильную ступку. Мицелий осторожно и тщательно растирали пестиком до образования однородной пасты. Затем к пасте добавляли 20 мл дистиллированной воды для получения суспензии мицелия. По 2 мл суспензии мицелия отдельно пипеткой вносили в четыре чашки Петри диаметром 30 мм, и в каждую чашку Петри инокулировали 20 личинок Meloidogyne spp. (J2), инфекционную и повреждающую стадию. Каждая чашка Петри служила повторностью. Контролем служили чашки Петри диаметром 30 мм, в которые вносили 2 мл стерильной воды, инокулированной J2. Эксперимент был повторен четыре раза.
Смертность J2 в суспензии гиф P. ostreatus и дистиллированной воде определяли через 3, 6, 12, 24, 48 и 72 часа после внесения обработки. Подтверждение гибели J2 проводили с использованием метода, описанного Thoden и др. (2009). Нематоды J2, которые казались неподвижными и статичными в каждый временной интервал, были промыты 3 раза дистиллированной водой, перенесены в свежую воду и повторно исследованы через 24 часа при увеличении объектива x40 под микроскопом Primostar (Zeiss microscopy GmbH, Германия). Нематода считалась мертвой, только если она не восстанавливалась после обработки дистиллированной водой. Процент смертности определяли, как описано Youssef и El-Nagdi (2021), ниже:
2.2.2 Влияние фильтрата Pleurotus ostreatus на выживаемость личинок Meloidogyne spp.
Фильтрат Pleurotus ostreatus готовили путем культивирования P. ostreatus в среде PDB в стерильных колбах Эрленмейера объемом 500 мл. Для этого в колбы Эрленмейера объемом 500 мл добавляли 250 мл стерильной бульонной среды и инокулировали блоком мицелия P. ostreatus размером 1 см³, вырезанным из 7-дневной чистой культуры P. ostreatus, активно растущей на чашке Петри с PDA. Инокулированную культуру герметизировали и инкубировали при комнатной температуре на роторном шейкере при 121 об/мин в течение 14 дней.
Затем бульон фильтровали через стерильную марлю, чтобы удалить все фрагменты грибного мицелия, и оставляли среду, содержащую только метаболиты, продуцируемые P. ostreatus во время роста. Фильтрат дополнительно фильтровали через микрофильтры диаметром 0,23 мкм для обеспечения его стерильности и удаления фрагментов грибов и спор. Этот фильтрат был взят в качестве исходной концентрации (т.е. 100% неразбавленного) и впоследствии был серийно разбавлен до четвертого разведения (10⁻⁴). Было приготовлено три обработки фильтратом P. ostreatus: i) исходная концентрация (100%), ii) второе разведение (10⁻²) и iii) четвертое разведение (10⁻⁴). Затем по 2 мл каждого из трех разведений отдельно пипеткой вносили в четыре чашки Петри диаметром 30 мм. В каждую чашку Петри добавляли суспензию из 20 личинок Meloidogyne. Контролем служили чашки Петри, в которые добавляли только 2 мл PDB и 20 личинок. Активность J2 наблюдали, а количество мертвых и живых J2 в фильтрате P. ostreatus и контрольной обработке (дистиллированная вода) регистрировали через 3, 6, 12, 24, 48 и 72 часа после внесения обработки. Смертность J2 определяли после обработки, как описано в разделе выше.
2.3 Оценка в вегетационном домике влияния Pleurotus ostreatus на выживаемость личинок Meloidogyne spp.
2.3.1 Выращивание баклажанов
Семена Solanum melongena (баклажан, сорт 'Purple long') были приобретены в Simlaw Seeds Company Limited, Кампала, Уганда. Семена выращивали в рассадном кассете в течение одного месяца, ежедневно поливая утром и вечером. Затем рассаду подвергали различным обработкам, как описано в разделах ниже.
2.3.2 Приготовление инокулюма Pleurotus ostreatus
Для приготовления инокулюма P. ostreatus зерна проса промывали под чистой проточной водопроводной водой для удаления грязи и пыли. Затем зерна проса ополаскивали дистиллированной водой и замачивали на ночь, чтобы они стали достаточно мягкими для легкой колонизации грибом. Затем зерна проса переносили в прозрачные автоклавируемые мешки в количестве 500 г и автоклавировали в течение 90 минут при температуре 121°C и давлении 15 фунтов на кв. дюйм. Затем зернам проса давали остыть в тщательно продезинфицированном и работающем ламинарном шкафу. Активно растущий 7-дневный мицелий P. ostreatus, выращенный на чашке с PDA, соскребали и инокулировали на зерна проса в прозрачных автоклавируемых мешках. Всего использовали две чашки культуры на 500 г зерен проса. Зерна проса тщательно перемешивали для обеспечения равномерного распределения грибного мицелия, запечатывали и инкубировали при 28°C в течение 14 дней. Культуру перемешивали каждые 3 дня для обеспечения равномерного распределения растущего гриба.
2.3.3 Подготовка почвы
Почвенный субстрат для вегетационного опыта состоял из смеси суглинистой почвы, птичьего помета и песка в соотношении 3:3:1. Стерильную почву тщательно перемешивали для получения однородной смеси и переносили в пластиковые горшки по 3 кг, которые подвергали обработке, как описано в следующем разделе. Горшка объемом 3 кг достаточно для обеспечения адекватного развития и роста корней баклажана в течение периода исследования.
2.3.4 Экспериментальный дизайн
Был проведен горшечный эксперимент с полным рандомизированным дизайном (CRD) с пятью обработками. Они включали баклажаны, высаженные в почву; i) Инокулированную 50 г зерен проса, колонизированных P. ostreatus, и нематодами, ii) Инокулированную 100 г зерен проса, колонизированных P. ostreatus, и нематодами, iii) Инокулированную 50 г зерен проса, колонизированных P. ostreatus, и без нематод, iv) Без P. ostreatus, но с нематодами (положительный контроль), и vi) Без P. ostreatus и без нематод (отрицательный контроль-без обработки). Каждая обработка имела четыре повторности по 12 растений в каждой. Для обработок с P. ostreatus зерна проса, колонизированные P. ostreatus, тщательно перемешивали в 3-килограммовых горшках с почвой во время пересадки (в возрасте одного месяца) и оставляли на две недели для закрепления. Для обработок с личинками Meloidogyne суспензию, содержащую в общей сложности 720 личинок, инокулировали вокруг каждого растения путем пролива через три отверстия, сделанных осторожно, чтобы минимизировать вмешательство в корни. Каждое пролитое отверстие затем засыпали почвой. 720 личинок, использованных в эксперименте, попадают в диапазон, указанный в литературе (Ayeni и др., 2022; Frimpong и др., 2022). Количественное определение нематод для инокуляции проводили, как описано Coyne и Ross (2014). Эксперимент был повторен два раза, и каждый был завершен через два месяца.
2.4 Сбор данных
По окончании эксперимента регистрировали вертикальную длину корней (см) и массу корней (г) с помощью измерительной ленты и прецизионных весов. Параметры роста нематод, собранные по окончании эксперимента, включали количество галлов на растение, популяцию фитопаразитических нематод на 5 г корней, популяцию фитопаразитических и непаразитических нематод на 100 г почвы и индекс галлообразования. Индекс галлообразования оценивали по шкале от 0 до 5, как описано Khun-In и др. (2015), где: 0 = нет галлов; 1 = от 1 до 5 галлов; 2 = от 6 до 20 мелких галлов; 3 = более 20 галлов, равномерно распределенных по корневой системе; 4 = редуцированная и деформированная корневая система с некоторыми крупными галлами; и 5 = полностью деформированная корневая система с несколькими, но крупными галлами. Для определения популяции фитопаразитических нематод на 5 г корней, корни томата нарезали на мелкие кусочки размером от 1 до 3 см и хорошо перемешивали на куске алюминиевой фольги. Отвешивали пять (5) граммов корней с помощью прецизионных лабораторных весов, и нематод экстрагировали с использованием модифицированного метода Бермана. Для экстракции нематод из почвы отбирали 1500 г почвы и хорошо перемешивали в лаборатории перед отвешиванием 100 г для использования при экстракции нематод. Нематод экстрагировали с использованием того же метода, что и для корней выше.
2.5 Анализ данных и визуализация
Данные были проанализированы и визуализированы с использованием статистического пакета R, версия 4.0.2 (R Development Core Team, 2024). Перед статистическим анализом данные были проверены на наличие гомоскедастичности и нормальности (Kozak и Piepho, 2018). Были проведены сравнения между обработками и контролем. Статистическая значимость устанавливалась при p ≤ 0,05. Значимые различия между обработками и контролем проверялись с использованием дисперсионного анализа (ANOVA) и последующего пост-хок анализа с использованием критерия Тьюки для честно значимого различия (Tukey HSD) при значении p 0,05. Когда предположение ANOVA не выполнялось, использовался непараметрический критерий Краскела-Уоллиса, и средние значения сравнивались с использованием непараметрического критерия Вилкоксона при p ≤ 0,05. Все данные представлены как среднее ± стандартная ошибка среднего.
3 Результаты
3.1 Влияние in vitro Pleurotus ostreatus на личинок Meloidogyne видов
3.1.1 Влияние водной суспензии Pleurotus ostreatus
Суспензия гиф P. ostreatus начинала мутнеть после первых 6 часов, причем наибольшая мутность наблюдалась через 72 часа. После внесения нематод в суспензию гиф движение нематод было нормальным в первые 3–6 часов воздействия. Было видно, как нематоды свободно двигались в суспензии, избегая контакта с грибным мицелием. Однако с увеличением времени воздействия подвижность и активность снижались, и через 72 часа не было видимого движения, за исключением нескольких нематод после тщательного наблюдения за хвостовой областью. Нематоды, контактировавшие с грибным мицелием, были обездвижены и колонизированы. В некоторых случаях было видно, как грибные гифы колонизировали и росли через ткани нематоды.
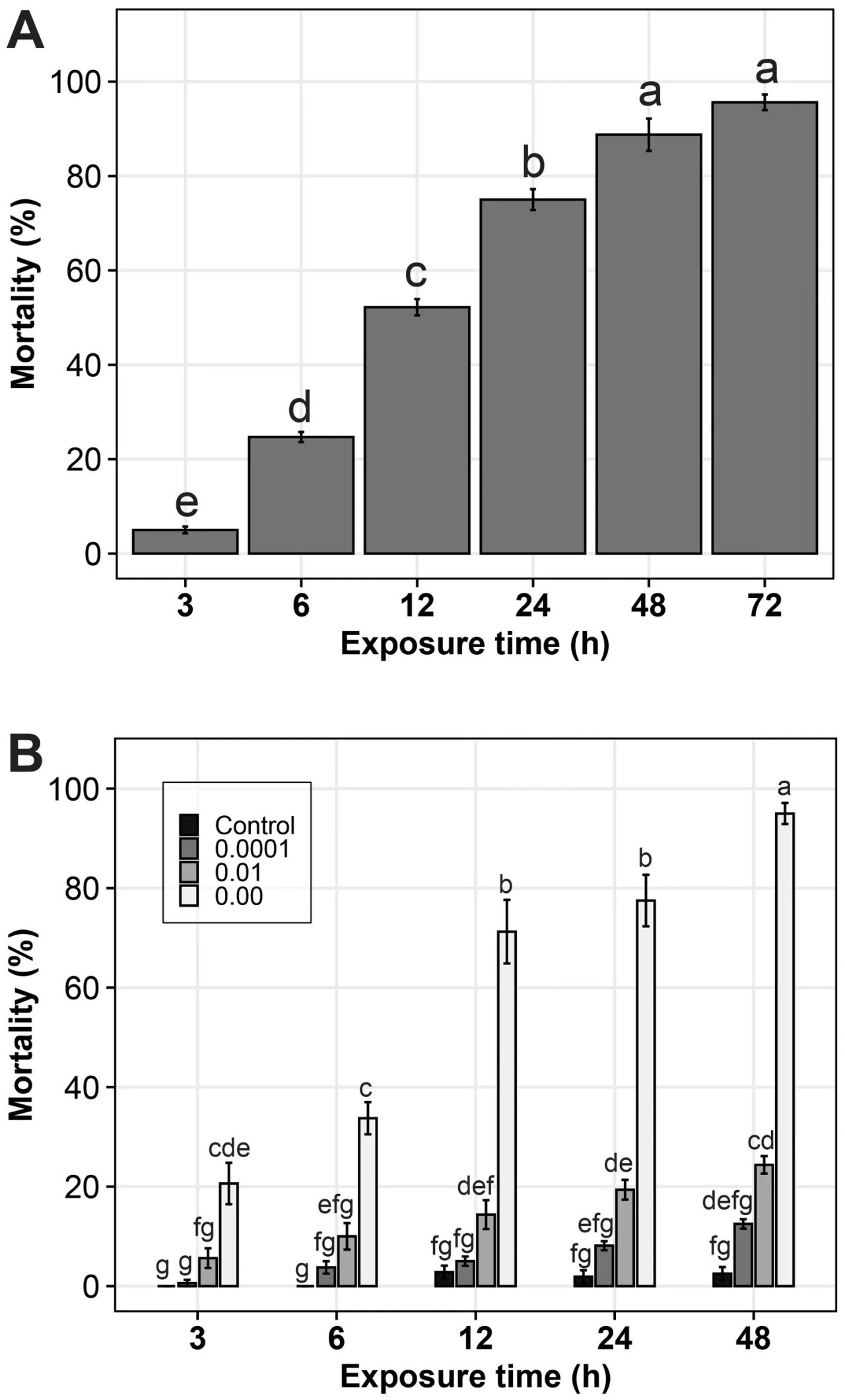
Наблюдалась значительная разница (p значение = 0,02) в уровне смертности нематод по различным временам воздействия. Смертность личинок Meloidogyne наблюдалась в суспензиях P. ostreatus уже через 3 часа, причем смертность увеличивалась с увеличением времени воздействия. Через 3 часа наблюдалась 3% смертность, увеличивающаяся до 95% через 72 часа (Рисунок 1A). В контроле (дистиллированная вода) не было зарегистрировано ни одной смерти нематод за все время воздействия.
Рисунок 1 Смертность (%) личинок Meloidogyne spp. в; (A) водной суспензии Pleurotus ostreatus и (B) различных концентрациях фильтрата культуры P. ostreatus в PDB, в разные периоды воздействия. Планки погрешностей представляют стандартные ошибки. Обработки или комбинации обработок с одинаковыми буквами («a»–«g») над планками погрешностей не являются значимо различными при 5% критерии Тьюки для честно значимого различия.
3.1.2 Влияние фильтрата Pleurotus ostreatus
Было обнаружено, что различные концентрации фильтрата P. ostreatus вызывают смертность личинок Meloidogyne spp. Уровни смертности нематод были значительно различны (p < 0,001) по разным концентрациям фильтрата P. ostreatus. Исходная концентрация фильтрата P. ostreatus показала очень высокую эффективность в вызывании смертности нематод на всех временных интервалах воздействия. Как только нематоды были внесены в исходную концентрацию фильтрата P. ostreatus, было видно, что они быстро двигались. После энергичного движения, особенно к концу 12 часов, большинство из них были неподвижны и выглядели прямыми. Для тех нематод, которые были подвижны, подвижность наблюдалась после осторожного поглаживания хвостовой или головной области нематоды препаровальной иглой. К концу 24 часов более 70% нематод оставались прямыми и неподвижными.
Для концентраций 10⁻² и 10⁻⁴ уровень смертности был ниже, и он медленно увеличивался с увеличением времени воздействия. В конце 48 часов большинство личинок еще двигались, но с меньшей подвижностью по сравнению с контрольной обработкой PDB, что указывает на то, что разведение снизило эффективность активности фильтрата (Рисунок 1B).
3.2 Влияние Pleurotus ostreatus на повреждение нематодами баклажанов в горшках
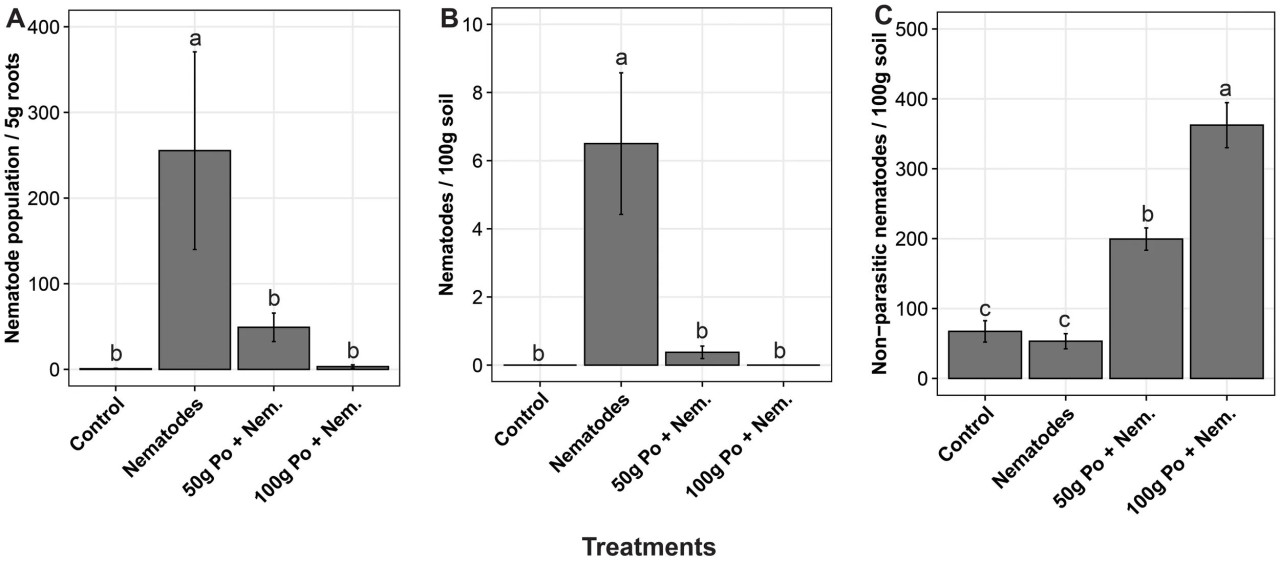
Pleurotus ostreatus снизил популяцию Meloidogyne spp. и стимулировал рост растений баклажана при различных концентрациях. Популяция нематод значительно различалась (p = 0,02) по обработкам. Положительный контроль (почва, инокулированная только нематодами) имел в среднем более 250 нематод на 5 г корневой ткани по сравнению с менее чем 50 нематодами на 5 г корневой ткани и отсутствием нематод на 5 г корневой ткани в почвах, инокулированных 50 г и 100 г просяного субстрата, колонизированного инокулюмом P. ostreatus, соответственно (Рисунок 2A). В почве положительный контроль имел в среднем более шести нематод Meloidogyne spp. на 100 г почвы по сравнению с примерно 0,2 и ни одной в почвах, обработанных 50 г и 100 г просяного субстрата, колонизированного инокулюмом P. ostreatus, соответственно (Рисунок 2B). Было замечено, что применение P. ostreatus увеличивает популяцию непаразитических нематод в почве по сравнению с положительным и отрицательным контролем (Рисунок 2C).
Рисунок 2 Влияние различных концентраций инокулюма P. ostreatus на популяцию; (A) фитопаразитической нематоды Meloidogyne spp. в 5 г корневых тканей баклажана, (B) Meloidogyne spp. в 100 г образца почвы и (C) непаразитических нематод в 100 г образца почвы. Планки погрешностей обозначают стандартные ошибки. Обработки с одинаковыми буквами («a», «b» и «c») над планками погрешностей не являются значимо различными при 5% критерии Тьюки для честно значимого различия.
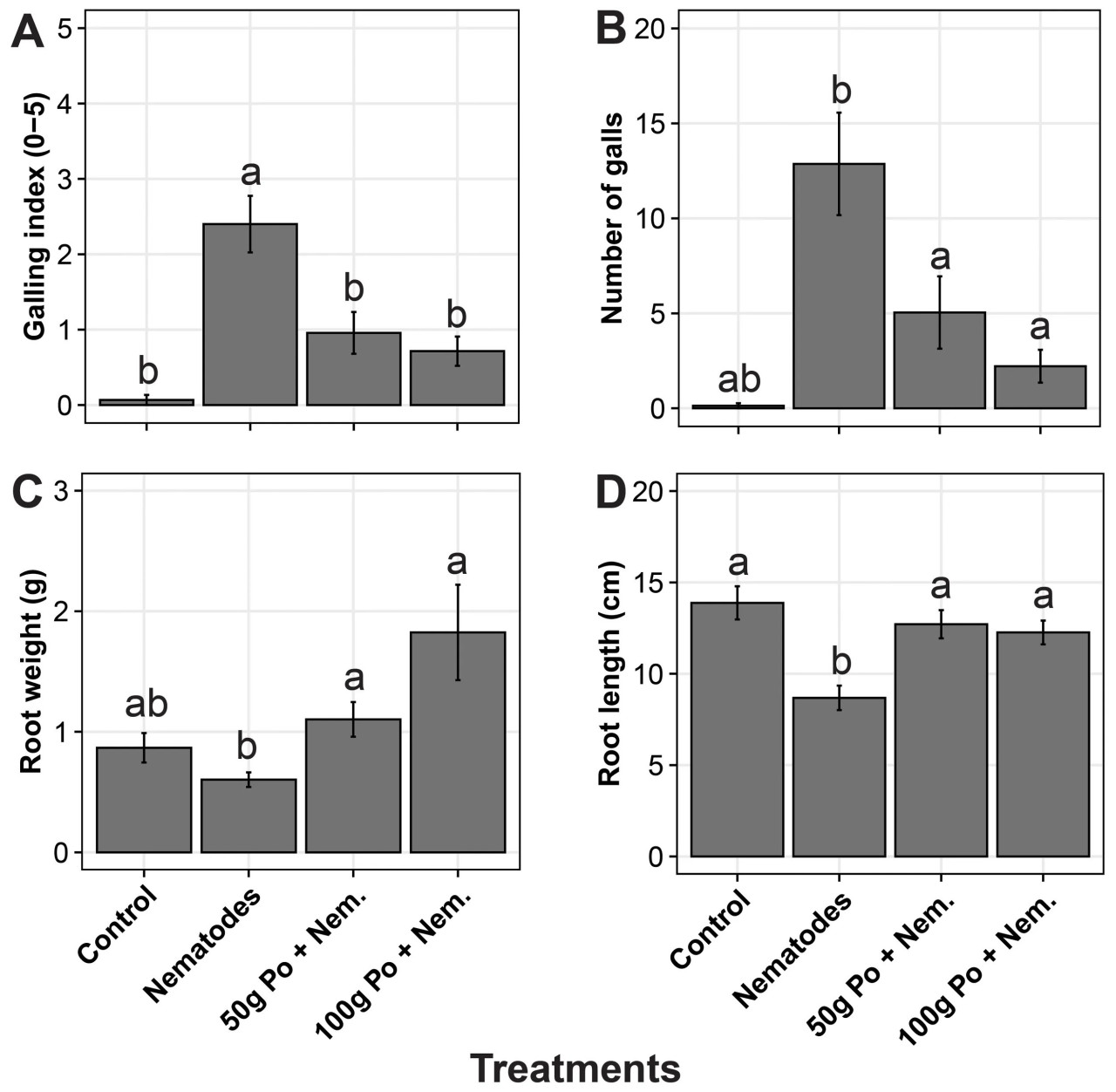
Положительный контроль (т.е., внесение нематод без P. ostreatus) имел большое количество галлов (средний индекс галлообразования (GI) 2,4) по сравнению с минимальным количеством галлов (средний GI < 1) в обработке с 50 г и 100 г просяного субстрата P. ostreatus (Рисунки 3A, B). Галлы (GI = 0) не наблюдались в отрицательном контроле (без P. ostreatus и без нематод). Растения, инокулированные только нематодами, имели значительно (p = 0,02) более низкую биомассу корней и длину корней (Рисунки 3C, D). Длина корней в отрицательном контроле была сравнима с таковой на делянках, обработанных P. ostreatus, в то время как растения, обработанные P. ostreatus, имели более высокую массу корней.
Рисунок 3 (A) Индекс галлообразования, (B) количество галлов, (C) сырая масса корней и (D) длина корней баклажанов, подвергнутых различным обработкам. Обработки включали: i) отрицательный контроль, в который не добавляли субстрат Pleurotus ostreatus и нематод, ii) положительный контроль, в который добавляли нематод без P. ostreatus, iii) обработку, в которой P. ostreatus культивировали на 50 г просяного субстрата, и обработку, в которой добавляли P. ostreatus, культивированный на 100 г. Планки погрешностей обозначают стандартные ошибки. Обработки с одинаковыми буквами («a» и «b») над планками погрешностей не являются значимо различными при 5% критерии Тьюки для честно значимого различия.
4 Обсуждение
Было обнаружено, что P. ostreatus проявляет нематоцидные свойства и подавляет Meloidogyne spp. in vitro и в горшечных баклажанах в условиях вегетационного домика. Подавление in vitro личинок Meloidogyne (J2) чистыми культурами гиф и фильтрата P. ostreatus может быть объяснено как активным хищничеством на нематодах, так и обездвиживанием вторичными метаболитами, продуцируемыми P. ostreatus, базидиомицетом. Сообщалось, что базидиомицеты являются нематофагами с потенциальной способностью продуцировать токсины как уникальную идентификационную характеристику. Satou и др. (2008) идентифицировали такие токсины, как тридекановая, тетрадекановая, линолелаидиновая и транс-2-децендиовая кислоты, перекись линолевой кислоты в этих грибах. Среди всех этих токсинов транс-2-декановая кислота была отмечена как наиболее активный токсин, проявляющий нематоцидные свойства (Kwok и др., 1992). Это соединение продуцируется в виде крошечных капель на кончике грибных гиф, и как только нематода вступает с ним в контакт, нематода становится неподвижной или обездвиженной (Heydari и др., 2006; Castañeda-Ramírez и др., 2020). В текущем исследовании личинки Meloidogyne spp. стали неподвижными и погибли через несколько часов после взаимодействия как с грибной культурой, так и с фильтратом. Таким образом, гибель могла быть вызвана проникновением нематоцидных соединений, таких как 2-декановая кислота, в ткани нематоды, влиянием на осмотическое давление внутренней мембраны, что приводит к некрозу нервной системы (Castañeda-Ramírez и др., 2020). В исследовании на C. elegans было обнаружено, что голова мертвых нематод казалась сморщенной, а пищевод смещенным (Lee и др., 2020). Как только нематода была обездвижена, вокруг нее наблюдались грибные гифы и мицелий, которые впоследствии проникали в ткани нематоды через отверстия тела, что является наблюдением, сходным с работой Palizi и др. (2009). Genier и др. (2015) сообщили, что проникновение и колонизация тел нематод P. ostreatus облегчается протеазами. Протеазы являются вторичными метаболитами, выделяемыми P. ostreatus во время его роста. Протеазы способствуют разрушению протеинового защитного барьера нематоды, позволяя проникать грибным гифам (Inácio и др., 2015).
Pleurotus ostreatus также вызвал снижение популяции нематод, корневых галлов и улучшил рост корней баклажана в горшечных растениях, что является наблюдением, сходным с Youssef и El-Nagdi (2021). Снижение популяции нематод может быть объяснено воздействием токсичных метаболитов и прямым хищничеством на нематодах и яйцах, как описано выше, и как наблюдалось в исследованиях in vitro. Genier и др. (2015) и Hussain и др. (2020) сообщили, что гидролитические ферменты (в основном протеазы), выделяемые P. ostreatus, обладают потенциалом гидролизовать яйца и личинок нематод, таким образом изменяя их размножение и снижая их популяции. Транс-2-деценовая кислота, вторичный метаболит, в основном продуцируемый P. ostreatus, также непосредственно обездвиживает нематод, вызывая их гибель (Castañeda-Ramírez и др., 2020), что также объясняет снижение популяций нематод. Снижение популяций нематод в конечном итоге привело к уменьшению галлообразования и улучшению роста баклажана.
Сообщалось, что гифы P. ostreatus колонизируют корни растений бамии, тем самым препятствуя доступу, прикреплению и проникновению личинок Meloidogyne spp. к корневым кончикам (Bordallo и др., 2002). Этот эффект на корни также может частично объяснить наблюдаемое снижение количества галлов и индекса галлообразования в обработках с P. ostreatus по сравнению с необработанными контролями. Этот механизм действия также сообщался для ряда нематофаговых грибов, в основном Trichoderma harzianum (Kleifeld и Chet, 1992; Yedidia и др., 1999).
В дополнение к защите от нематод, улучшенный рост корней баклажана, выражающийся в более высокой массе корней в обработках с P. ostreatus, может быть связан с сапрофитной природой грибов P. ostreatus, ведущей к лучшему разложению органического вещества, включая просяной субстрат, и повышенной доступности питательных веществ. Улучшенное питание также стимулирует рост растений и устойчивость к инфекциям RKN.
Большая популяция свободноживущих нематод также наблюдалась в почве обработок с P. ostreatus по сравнению с обработками без него. Это могло быть связано с ролью свободноживущих нематод в разложении органического вещества (Yadav и др., 2018). Это также может объяснить улучшенный рост корней у баклажана, обработанного P. ostreatus, по сравнению с контролем без инокулюма P. ostreatus.
Вышеуказанные результаты показывают, что P. ostreatus имеет очень высокий потенциал в борьбе с RKN на баклажанах. Культивирование и потребление P. ostreatus в настоящее время широко распространяется. Таким образом, его продвижение для борьбы с нематодами может быть легко внедрено и будет иметь большую пользу в решении проблем, связанных с нематодами, в сельскохозяйственных производственных системах. Этот гриб был бы отличной альтернативой, поскольку он экологически безопасен и не оказывает вредного воздействия на почву и полезные почвенные микроорганизмы. С развитием технологий активные нематоцидные соединения, продуцируемые грибом, могут быть выделены и массово произведены синтетически в качестве биологических агентов борьбы с нематодами, что сделает их легкодоступными для фермеров.
В текущем исследовании использовались колонизированные просяные субстраты. Потенциал использования отработанных грибных субстратов, которые являются более доступными и дешевыми, для борьбы с нематодами на баклажанах требует изучения. Использование P. ostreatus в качестве подхода биологической борьбы с RKN также должно быть изучено в различных полевых условиях для оценки его эффективности в естественных условиях. При проведении полевых оценок, агротехнические стратегии борьбы с нематодами также должны применяться наряду с P. ostreatus для оценки того, насколько интеграция различных стратегий способствует решению производственных проблем, связанных с RKN.
Ссылки
1. Abd-Elgawad M. M. M. (2016). Biological control agents of plant-parasitic nematodes. Egypt. J. Biol. Pest Control 26, 423–429. doi: 10.1584/... CrossRef Google Scholar
2. Atif A. M., Elzamik F. I., Mohamed G. M., Al-Quwaie D. A., Ashkan M. F., Alqahtani F. S., et al. (2023). Biological control of the root-knot nematode (Meloidogyne incognita) on eggplants with various chitinase-producing Streptomyces strains. Eur. J. Plant Pathol. 167, 371–394. doi: 10.1007/s10658-023-02718-8 CrossRef Google Scholar
3. Ayeni B. P., Claudius-Cole A. O., Abberton M., Coyne D. (2022). Host status of Bambara groundnut accessions to Meloidogyne incognita using conventional screenhouse and novel seedling pouch methods. Nematol 24, 543–558. doi: 10.1163/15685411-bja10150 CrossRef Google Scholar
4. Barron G. L., Thorn R. G. (1987). Destruction of nematodes by species of Pleurotus. Can. J. Bot. 65, 774–778. doi: 10.1139/b87-103 CrossRef Google Scholar
5. Bordallo J. J., Lopez-Llorca L. V., Jansson H. B., Salinas J., Persmark L., Asensio L. (2002). Colonization of plant roots by egg-parasitic and nematode-trapping fungi. New Phyto. 154, 491–499. doi: 10.1046/j.1469-8137.2002.00399.x CrossRef Google Scholar
6. Castañeda-Ramírez G. S., Torres-Acosta J. F. D. J., Sánchez J. E., Mendoza-De-Gives P., González-Cortázar M., Zamilpa A., et al. (2020). The possible biotechnological use of edible mushroom bioproducts for controlling plant and animal parasitic nematodes. Biomed. Res. Int. 1–12. doi: 10.1155/2020/6078917 CrossRef Google Scholar
7. Coyne D., Ross J. L. (2014). Protocol for nematode resistance screening: root knot nematodes. Meloidogyne, 27. CrossRef Google Scholar
8. Coyne D. L., Cortada L., Dalzell J. J., Claudius-Cole A. O., Haukeland S., Luambano N., et al. (2018). Plant-parasitic nematodes and food security in Sub-Saharan Africa. Annu. Rev. Phytopathol. 56, 381–403. doi: 10.1146/annurev-phyto-080417-045833 CrossRef Google Scholar
9. FAOSTAT. (2022). World Food and Agriculture — Statistical Yearbook 2022. Rome: FAO Statistics. doi: 10.4060/cc2211en7544 CrossRef Google Scholar
10. Frimpong M., Osei K., Prempeh R. N. A. (2022). Yield potential and root-knot nematode (Meloidogyne incognita) resistance of six tomato (Solanum lycopersicum L.) genotypes. Int. J. Phyto. Res. 2, 30–33. CrossRef Google Scholar
11. Genier H. L. A., de Freitas Soares F. E., de Queiroz J. H., de Souza Gouveia A., Araújo J. V., Braga F. R., et al. (2015). Activity of the fungus Pleurotus ostreatus and of its proteases on Panagrellus sp. larvae. Afri. J. Biotechnol. 14, 1496–1503. doi: 10.5897/AJB2015.14447 CrossRef Google Scholar
12. Gisbert C., Prohens J., Raigón M. D., Stommel J. R., Nuez F. (2011). Eggplant relatives as sources of variation for developing new rootstocks: Effects of grafting on eggplant yield and fruit apparent quality and composition. Sci. Hortic. 128, 14–22. doi: 10.1016/j.scienta.2010.12.007 CrossRef Google Scholar
13. Goodell P. B. (2010). University of California IPM Pest Management Guidelines: Eggplant. UC ANR Publication. CrossRef Google Scholar
14. Hahn M. H., De Mio L. L. M., Kuhn O. J., Duarte H. D. S. S. (2019). Nematophagous mushrooms can be an alternative to control Meloidogyne javanica. Biol. Control 138, 104024. doi: 10.1016/j.biocontrol.2019.104024 CrossRef Google Scholar
15. Hajihassani A., Davis R. F., Timber P. (2019). Evaluation of selected non fumigant nematicides on increasing inoculation densities of Meloidogyne incognita on Cucumber. Plant Dis. 103, 3161–3165. doi: 10.1094/PDIS-04-19-0836-RE CrossRef Google Scholar
16. Heydari R., Pourjam E., Goltapeh E. M. (2006). Antagonistic effect of some species of Pleurotus on the root-knot nematode, Meloidogyne javanica in vitro. Plant Pathol. J. 5, 173–177. doi: 10.3923/ppj.2006.173.177 CrossRef Google Scholar
17. Hussain M., Manasova M., Zouhar M., Ryšánek P. (2020). Comparative virulence assessment of different nematophagous fungi and chemicals against northern root-knot nematodes, Meloidogyne hapla, on carrots. Pakistan J. Zool. 52, 199. doi: 10.17582/journal.pjz/2020.52.1.199.206 CrossRef Google Scholar
18. Inácio F. D., Ferreira R. O., Araujo C. A. V. D., Brugnari T., Castoldi R., Peralta R. M., et al. (2015). Proteases of wood rot fungi with emphasis on the genus Pleurotus. BioMed. Res. Int. 2015, 290161. doi: 10.1155/2015/290161 CrossRef Google Scholar
19. Kanaujiya D. K., Gupta S. K., Kumar G., Pathak R., Kumar Y. (2022). Ability of Pleurotus ostreatus in vitro to kill different plant parasitic nematodes. Pharma Innov. J. 11, 911–913. CrossRef Google Scholar
20. Khan A., Aiman S. I., Baber Y., Hassan F., Usman H. M., Sohail M. A., et al. (2021). An overview of root-knot nematodes and their management. J. Ento. Zool. Stud. 9, 35–40. CrossRef Google Scholar
21. Khun-In A., Sukhakul S., Chamswarng C., Tangkijchote P., Sasnarukkit A. (2015). Culture filtrate of Pleurotus ostreatus isolate poa3 effect on egg mass hatching and juvenile 2 of Meloidogyne incognita and its potential for biological control. J. Int. Soc Southeast Asian Agric. Sci. 21, 46–54. CrossRef Google Scholar
22. Kleifeld O., Chet I. (1992). Trichoderma harzianum-interaction with plants and effect on growth response. Plant Soil 144, 267–272. doi: 10.1007/BF00012884 CrossRef Google Scholar
23. Kozak M., Piepho H. P. (2018). What's normal anyway? Residual plots are more telling than significance tests when checking ANOVA assumptions. J. Agron. Crop Sci. 204, 86–98. doi: 10.1111/jac.2018.204.issue-1 CrossRef Google Scholar
24. Kwok O. C. H., Plattner R., Weisleder D., Wicklow D. T. (1992). A nematicidal toxin from Pleurotus ostreatus NRRL 3526. J. Chem. Ecol. 18, 127–136. doi: 10.1007/BF00993748 CrossRef Google Scholar
25. Lacey L. A., Frutos R., Kaya H. K., Vail P. (2001). Insect pathogens as biological control agents: Do they have a future? Biol. Control 21, 230–248. doi: 10.1006/bcon.2001.0938 CrossRef Google Scholar
26. Lee C. H., Chang H. W., Yang C. T., Wali N., Shie J. J., Hsueh Y. P. (2020). Sensory cilia as the Achilles heel of nematodes when attacked by carnivorous mushrooms. Proc. Natl. Acad. Sci. 117, 6014–6022. doi: 10.1073/pnas.1918473117 CrossRef Google Scholar
27. Lopez-Llorca L. V., Maciá-Vicente J. G., Jansson H. B. (2008). "Mode of action and interactions of nematophagous fungi," in Integrated management and biocontrol of vegetable and grain crops nematodes (Springer Netherlands, Dordrecht), 51–76. doi: 10.1007/978-1-4020-6063-2_3 CrossRef Google Scholar
28. Murata G., Uehara T., Lee H. J., Mizutani M., Kadota Y., Shinmura Y., et al. (2022). Solanum palinacanthum Dunal as a potential eggplant rootstock resistant to root-knot nematodes. J. Phytopathol. 170, 185–193. doi: 10.1111/jph.v170.3 CrossRef Google Scholar
29. Noling J. W. (2014). Nematode management in tomatoes, peppers, and eggplant. CrossRef Google Scholar
30. Ocimati W., Were E., Tazuba A. F., Dita M., Zheng S.-J., Blomme G. (2021). Spent Pleurotus ostreatus substrate has potential for managing Fusarium wilt of banana. J. Fungi 7, 946. doi: 10.3390/jof7110946 CrossRef Google Scholar
31. Okorie C. C., Ononuuj C. C., Okwujiako I. A. (2011). Management of Meloidogyne incognita with Pleurotus ostreatus and P. tuberregium in soybean. Int. J. Agric. Biol. 13, 401–405. CrossRef Google Scholar
32. Palizi P., Goltapeh E. M., Pourjam E., Safaie N. (2009). Potential of oyster mushrooms for the biocontrol of sugar beet nematode (Heterodera schachtii). J. Plant Prot. Res. 49, 27–33. doi: 10.2478/v10045-009-0004-6 CrossRef Google Scholar
33. R Core Team. (2024). R: A language and environment for statistical computing. Vienna, Austria: R Foundation for Statistical Computing. CrossRef Google Scholar
34. Satou T., Kaneko K., Li W., Koike K. (2008). The toxin produced by Pleurotus ostreatus reduces the head size of nematodes. Biol. Pharm. Bull. 31, 574–576. doi: 10.1248/bpb.31.574 CrossRef Google Scholar
35. Sharma M., Kaushik P. (2021). Biochemical composition of eggplant fruits: A Review. Appl. Sci. 11, 7078. doi: 10.3390/app11157078 CrossRef Google Scholar
36. Taher D., Solberg S. Ø., Prohens J., Chou Y.-Y., Rakha M., Wu T.-H. (2017). World Vegetable Center eggplant collection: origin, composition, seed dissemination and utilization in breeding. Front. Plant Sci. 8. doi: 10.3389/fpls.2017.01484 CrossRef Google Scholar
37. Thoden T. C., Boppré M., Hallmann J. (2009). Effects of pyrrolizidine alkaloids on the performance of plant-parasitic and free-living nematodes. Pest Manage. Sci. 65, 823–830. doi: 10.1002/ps.1764 CrossRef Google Scholar
38. Wille C. N., Gomes C. B., Minotto E., Nascimento J. S. (2019). Potential of aqueous extracts of basidiomycetes to control root-knot nematodes on lettuce. Hortic. Bras. 37, 54–59. doi: 10.1590/s0102-053620190108 CrossRef Google Scholar
39. Xiang N., Lawrence K. S., Donald P. A. (2018). Biological control potential of plant growth-promoting rhizobacteria suppression of Meloidogyne incognita on cotton and Heterodera glycines on soybean: A Review. J. Phytopathol. 166, 449–458. doi: 10.1111/jph.12712 CrossRef Google Scholar
40. Yadav S., Patil J., Kanwar R. S. (2018). The role of free living nematode population in the organic matter recycling. Int. J. Curr. Microb. Appl. Sci. 7, 2726–2734. doi: 10.20546/ijcmas.2018.706.321 CrossRef Google Scholar
41. Yedidia I., Benhamou N., Chet I. (1999). Induction of defense responses in cucumber plants (Cucumis sativus L.) by the biocontrol agent Trichoderma harzianum. Appl. Envir. Microb. 65, 1061–1070. doi: 10.1128/aem.65.3.1061-1070.1999 CrossRef Google Scholar
42. Youssef M. M. A., El-Nagdi W. M. A. (2021). New approach for biocontrolling root-knot nematode, Meloidogyne incognita on Cowpea by commercial fresh Oyster mushroom (Pleurotus ostreatus). Jordan J. Biol. Sci. 14, 173–177. doi: 10.54319/jjbs/140122 CrossRef Google Scholar
43. Zouhar M., Douda O., Nováková J., Doudová E., Mazáková J., Wenzlová J., et al. (2013). First report about the trapping activity of Stropharia rugosoannulata acanthocytes for Northern Root Knot Nematode. Helminthologia 50, 127–131. doi: 10.2478/s11687-013-0120-8 CrossRef Google Scholar
Nyangwire B, Ocimati W, Tazuba AF, Blomme G, Alumai A and Onyilo F (2024) Pleurotus ostreatus is a potential biological control agent of root-knot nematodes in eggplant (Solanum melongena). Front. Agron. 6:1464111. doi: 10.3389/fagro.2024.1464111
Перевод статьи «Pleurotus ostreatusis a potential biological control agent of root-knot nematodes in eggplant (Solanum melongena» авторов Nyangwire B, Ocimati W, Tazuba AF, Blomme G, Alumai A and Onyilo ., оригинал доступен по ссылке. Лицензия: CC BY. Изменения: переведено на русский язык
Фото: freepik











































































































Комментарии (0)