Ключ к выносливости груши: найдены гены, которые экономят фосфорные удобрения и повышают устойчивость к соли
Интенсивное использование фосфорных удобрений вредит экологии, а засоление почв и засухи угрожают садам. Решение этих проблем может лежать в самих растениях. Новое исследование раскрывает генетические основы удивительной выносливости дикой груши 'duli', популярного подвоя. Ученые идентифицировали все 158 генов, ответственных за эффективное усвоение фосфора, и доказали, что их активностью можно управлять с помощью регуляторов роста. Это открывает реальную перспективу для селекции сортов, которые будут требовать меньше удобрений и лучше противостоять стрессам.
Аннотация
Семейство фосфатных транспортеров (PHT) играет важную роль в поглощении и переносе фосфора (P) у растений. В данном исследовании из генома 'duli' было идентифицировано в общей сложности 158 генов PbPHT, включая 70 PbPHT1, 2 PbPHT2, 70 PbPHT3, 12 PbPHT4 и 4 PbPHT5. Из этих 158 генов 150 были картированы на 17 хромосомах 'duli'. Анализ дупликации генов выявил 18 пар тандемно дублированных генов. Анализ промоторов показал наличие большого числа цис-регуляторных элементов, связанных с фитогормонами, ростом, развитием, стрессом и световым ответом, в промоторах генов PbPHT. Анализ методом количественной ПЦР в реальном времени (qRT-PCR) выявил, что большинство генов PHT у 'duli' обладают высокой экспрессией в плодах, цветках, листьях, стеблях и корнях, а 15 генов PbPHT реагировали на обработку 5 мкМ H₂PO₄⁻, 0.5 мМ H₂PO₄⁻, 5 мМ H₂PO₄⁻, NaCl, GR24 (синтетический аналог страголактона), GA₃ (гиббереллин 3), АБК (абсцизовая кислота) и ИУК (индол-3-уксусная кислота). Обработки GR24, GA₃, ИУК и 5 мМ KH₂PO₄ повышали концентрацию, поглощение, перенос и распределение фосфора в корневищах и листьях 'duli', тогда как 5 мкМ KH₂PO₄, NaCl и АБК оказывали противоположный эффект. Таким образом, данное исследование представляет список генов PbPHT, играющих существенную роль в ответе на абиотические стрессы, а также важную информацию для понимания функциональных характеристик PbPHT при устойчивости 'duli' к абиотическим стрессам, и открывает перспективы для изучения функций PbPHT в условиях действия экзогенных гормонов, фосфора и солевого стресса в будущем.
1. Введение
Фосфор (P) является одним из важнейших макроэлементов, необходимых растениям, и представляет собой ключевой компонент нуклеиновых кислот, фосфолипидов, нуклеопротеинов и АТФ [1]. Он также участвует во множестве биологических процессов в растениях, таких как фотосинтез, дыхание, а также перенос сахаров и крахмала. Хотя фосфор в избытке присутствует в почве, он часто образует нерастворимые фосфаты с ионами Ca²⁺, Fe³⁺ и Al³⁺, которые не могут быть легко поглощены и использованы растениями [2]. Однако дефицит P может снизить синтез антоцианов, уменьшить кущение сельскохозяйственных культур, снизить скорость образования почек и цветков у плодовых деревьев и ускорить опадение листьев, тем самым ограничивая рост растений [3]. Растения поглощают фосфор корнями в форме неорганических фосфатов с помощью PHT-белков (фосфатных транспортеров), включая HPO₄²⁻ и H₂PO₄⁻.
У растений семейство PHT делится на пять подсемейств (PHT1, PHT2, PHT3, PHT4 и PHT5) в соответствии с их субклеточной локализацией и последовательностью [4,5]. Семейство PHT1 (phosphate transporter 1) представляет собой плазматические мембранные PHT-белки. Они в основном отвечают за поглощение P корнями растений и его перенос. В настоящее время PHT1 является наиболее изученным семейством фосфатных транспортеров [6]. Семейство PHT1 содержит девять членов, а именно AtPHT1.1-AtPHT1.9 у Arabidopsis thaliana, причем AtPHT1.1 и AtPHT1.4 в основном участвуют в поглощении фосфора из почвы [7,8]. AtPHT1.5 участвует в переносе и распределении P от органа-источника к органу-поглотителю [9]. Семейство PHT2 содержит только один член у Arabidopsis thaliana. AtPHT2 является хлоропластным фосфатным транспортером, который участвует в переносе и распределении фосфора в растениях [10]. Семейство PHT3 представляет собой группу транспортеров, локализованных в митохондриях; у Arabidopsis thaliana идентифицировано три гена, которые отвечают за обмен Pi между матриксом митохондрий и цитоплазмой для поддержания синтеза АТФ [11]. У Arabidopsis thaliana существует шесть членов семейства PHT4. AtPHT4.1 участвует в поддержании баланса Pi и pH в хлоропластах [12], AtPHT4.2 в основном участвует в углеродном метаболизме Arabidopsis thaliana [13], а AtPHT4.6 участвует в реакции Arabidopsis thaliana на солевой стресс [14]. Белки семейства PHT5 (SPX-MFS) расположены в мембране вакуоли. Обнаружено, что семейство PHT5 может регулировать гомеостаз фосфора в растениях. Они играют важную роль в репродукции и росте растений. В условиях достаточного количества Pi члены семейства PHT5 регулируют хранение избытка Pi в вакуолях, предотвращая токсемию цитоплазмы, тогда как в случае дефицита Pi семейство PHT5 регулирует экспорт Pi из вакуолей в цитозоль [15,16,17]. Хотя каждое подсемейство играет важную роль в утилизации фосфора растениями, поглощение, перенос и распределение P зависят от взаимодействия всех семейств PHT. С развитием геномики и биоинформатики семейства PHT были идентифицированы у яблони (Malus domestica) [18], томата (Solanum lycopersicum) [19], сахарного тростника (Saccharum officinarum) [20], перца (Capsicum annuum) [21], тополя (Populus simonii) [22], арабидопсиса (Arabidopsis thaliana) [23] и других видов [24,25,26]. Подобный геномный анализ фосфатных транспортеров ранее не проводился для 'duli' (Pyrus betulifolia Bunge).
Многие почвы северного Китая бедны фосфором. Поэтому в производстве груши ежегодно на поля вносят большое количество фосфорных удобрений. Однако интенсивное использование Pi-удобрений может загрязнять водные ресурсы, что вызывает обеспокоенность с точки зрения охраны окружающей среды [27,28]. 'Duli' обладает высокой засухоустойчивостью и морозостойкостью и обычно используется в качестве подвоя для груши в северном Китае. Повышение способности корней 'duli' поглощать фосфор важно для увеличения урожайности и качества грушевых деревьев и снижения загрязнения Pi [29]. Фосфатные транспортеры играют важную роль в поглощении и использовании фосфора у 'duli'. Поэтому мы идентифицировали ген PbPHT; определили его паттерны экспрессии в корнях, стеблях, листьях, цветках, плодах, а также в ответ на регуляторы роста растений, фосфор и солевой стресс; и проанализировали концентрацию, поглощение, перенос и распределение фосфора в корнях, стеблях и листьях 'duli' при обработке гормонами и Pi. Результаты нашего исследования помогут в дальнейшем изучении функций членов семейства PbPHT. Генно-инженерные подходы могут быть использованы для повышения эффективности поглощения и переноса Pi грушей.
2. Материалы и методы
2.1. Идентификация PbPHT
В данном исследовании последовательности белков и файл GFF/gff3 'duli' были загружены из GDR (https://www.rosaceae.org/organism/26137) (дата обращения: 21 апреля 2024 г.). Последовательности белков AtPHT были загружены из Tair (https://www.arabidopsis.org/) (дата обращения: 21 апреля 2024 г.). Для идентификации членов семейства PHT у 'duli' 22 белковые последовательности AtPHT были использованы в качестве запросов для поиска в базе данных генома 'duli' со значением E-value ≤ 10⁻⁵. Профильная информация о доменах PHT1 (MFS, PF00083), PHT2 (PHO4, PF01384), PHT3 (Mito_carr, PF00153), PHT4 (MFS_1, PF07690) и PHT5 (MFS_1, PF07690 и SPX, PF03105) была получена из базы данных Pfam (http://pfam-legacy.xfam.org/) (дата обращения: 21 апреля 2024 г.). После удаления повторов домены, содержащиеся во всех белковых последовательностях, были проверены с помощью Pfam (http://pfam.janelia.org) (дата обращения: 21 апреля 2024 г.) и SMART (https://smart.embl.de/) (дата обращения: 21 апреля 2024 г.).
Для анализа физико-химических свойств PHT-белков 'duli' молекулярные массы, изоэлектрические точки, гидрофильность и коэффициенты нестабильности каждого члена семейства генов PHT были проанализированы с использованием сайта Expasy (https://web.expasy.org/protparam/) (дата обращения: 21 апреля 2024 г.). Для анализа субклеточной локализации каждого PbPHT использовалось онлайн-программное обеспечение Cell-PLoc 2.0 (http://www.csbio.sjtu.edu.cn/bioinf/Cell-PLoc-2/) (дата обращения: 21 апреля 2024 г.). Онлайн-программное обеспечение Some Secondary Structure Prediction (https://npsa-prabi.ibcp.fr) (дата обращения: 21 апреля 2024 г.) было использовано для анализа вторичной структуры белков PbPHT.
2.2. Филогенетический анализ и хромосомная локализация
Филогенетические деревья были построены с помощью программы MEGA11 методом соседнего присоединения (neighbor-joining) с моделью поправки Пуассона и 1000 повторами бутстрэпа; затем они были аннотированы и визуализированы с помощью Itol (https://itol.embl.de/) (дата обращения: 21 апреля 2024 г.). Распределение по хромосомам и коллинеарность PbPHT были проанализированы с использованием TBtools (версия 2.119, Колледж садоводства, Южно-Китайский сельскохозяйственный университет, Гуанчжоу, Китай).
2.3. Консервативные мотивы, структура гена и цис-регуляторные элементы
Общие консервативные мотивы и структура гена семейства PHT 'duli' были проанализированы онлайн с использованием сайта MEME (https://meme-suite.org/meme/tools/meme) (дата обращения: 24 апреля 2024 г.) и визуализированы с помощью Tbtools. После извлечения 2000 п.н. последовательностей выше по течению от каждого члена семейства PHT 'duli' с помощью Tbtools эти последовательности были загружены на сайт PlantCARE (https://bioinformatics.psb.ugent.be/webtools/plantcare/html/) (дата обращения: 24 апреля 2024 г.) для прогнозирования цис-регуляторных элементов в промоторной области и визуализированы с помощью TBtools.
2.4. Растительный материал и обработки
Образцы тканей (корни, стебли, листья, цветки и плоды) и полугодовалые сеянцы 'duli' с одинаковым ростом и без вредителей и болезней были получены из Инновационного экспериментального парка Хэбэйского сельскохозяйственного университета. В экспериментах использовались полугодовалые сеянцы 'duli'. Сеянцы аналогичного размера были перенесены в серые пластиковые контейнеры (30 × 15 × 10 см), растения были закреплены на губках, каждый контейнер содержал 2,5 л питательного раствора Хогланда половинной концентрации, и в каждый контейнер помещали по 2 воздушных насоса. После 10 дней предварительного культивирования начинали стрессовые обработки. Каждая стрессовая обработка имела три биологические реплики, и каждая реплика содержала 15 растений. Обработки были следующими: (1) контроль KH₂PO₄ (500 мкМ); (2) обработка с низким содержанием P (KH₂PO₄, 5 мкМ); (3) обработка с высоким содержанием P (KH₂PO₄, 5 мМ) [18]; (4) обработка NaCl (200 мМ); (5) обработка GA₃ (0,1 мМ); (6) обработка ИУК (100 мкМ); (7) обработка АБК (300 мкМ); (8) и обработка GR24 [30,31].
2.5. Анализ экспрессии
Образцы собирали в моменты времени 0, 24, 48 и 168 часов после начала эксперимента. Все образцы тканей мгновенно замораживали в жидком азоте, растирали и хранили при -80 °C. РНК экстрагировали с использованием набора для выделения РНК (Omega, Пекин, Китай), а обратную транскрипцию РНК проводили с использованием набора для обратной транскрипции (Yeasen, Шанхай, Китай). Праймеры для 15 генов PbPHT были разработаны с использованием сайта NCBI (https://blast.ncbi.nlm.nih.gov/Blast.cgi) (дата обращения: 28 апреля 2024 г.) (Таблица 1). Праймеры были синтезированы компанией Beijing Biomed (Пекин, Китай). Система и процедуры реакции qRT-PCR проводились в соответствии с методом Yuan Shuai и др. [32]. В качестве внутреннего референсного стандарта использовали PbeActin [30]. Уровни экспрессии PbPHT рассчитывали с использованием метода 2⁻ΔΔCT.
Таблица 1. Члены семейства PHT 'duli' и дизайн праймеров для qRT−PCR.
2.6. Определение содержания фосфора
Листья, стебли и корни собирали и промывали деионизированной водой после 168 часов обработки. Образцы фиксировали при 105 °C в течение 15 минут, а затем высушивали в сушильном шкафу при 70 °C до достижения постоянного веса; затем эти образцы использовали для анализа концентрации питательных веществ. Образцы (0,1 г) помещали в стаканы, в каждый стакан добавляли 1 мл ультрачистой воды, затем 8 мл смеси концентрированной серной и хлорной кислот (10:1). Затем образцы нагревали до 300 °C в устройстве для переваривания тяжелых металлов (Multiwave PRO; Anton–Paar GmbH, Грац, Австрия). После осветления раствора объем в пробирке доводили до 100 мл ультрачистой водой. Содержание P измеряли с помощью проточного анализатора с сегментацией потока (Auto Analyzer 3, SEAL Analytical, Нордерштедт, Германия) [33]. Каждая обработка имела три независимые биологические реплики. Распределение, перенос и поглощение P определяли в соответствии с методами Liang Bowen [34,35].
3. Результаты
3.1. Идентификация и физико-химические свойства генов PHT у 'duli'
Всего в геноме 'duli' с помощью биоинформатических методов было идентифицировано 158 PbPHT. На основе анализа консервативных доменов мы разделили гены PbPHT на пять подсемейств: PHT1 (MFS), PHT2 (PHO4), PHT3 (Mito_Carr), PHT4 (MFS_1) и PHT5 (MFS_1 и SPX). Эти гены были названы соответственно PbPHT1.1–PbPHT1.70, PbPHT2.1–PbPHT2.2, PbPHT3.1–PbPHT3.70, PbPHT4.1–PbPHT4.12 и PbPHT5.1–PbPHT5.4 в соответствии с их положением на хромосомах. Физико-химические свойства белков, кодируемых генами PbPHT, обобщены в Таблице S1 в дополнительных материалах. Длина членов семейства PHT1 варьировала от 294 а.о. до 1094 а.о., молекулярные массы — от 33,07 кДа до 120,77 кДа, а pI — от 5,09 до 9,54. Длина членов семейства PHT3 варьировала от 229 а.о. до 1797 а.о., а pI — от 6,33 до 9,92. Длина членов семейства PHT4 варьировала от 184 а.о. до 610 а.о., молекулярные массы — от 23,34 кДа до 203,17 кДа, а pI — от 6,12 до 10,24. За исключением PbPHT5.2, остальные члены семейства PHT5 имели длину 699 а.о., молекулярные массы варьировали от 77,82 кДа до 82,19 кДа, а pI — от 5,97 до 8,30. Члены семейств PHT2 и PHT5 являются нестабильными и гидрофобными белками. За исключением PbPHT3.26, PbPHT3.27 и PbPHT3.28, остальные члены семейства PHT3 являются гидрофильными белками. За исключением PbPHT4.1, PbPHT4.3 и PbPHT4.12, остальные члены семейства PHT4 являются стабильными белками. Вторичная структура членов семейства PHT была представлена в основном альфа-спиралями, а бета-поворот у всех членов составлял 0.
Субклеточная локализация играет важную роль в изучении функции гена и взаимодействия белков. В данном исследовании прогноз субклеточной локализации показал, что члены семейств PHT1 и PHT4 расположены в клеточных мембранах, члены семейства PHT2 — в хлоропластах, члены семейства PHT3 — в митохондриях, PbPHT5.1 и PbPHT5.4 — в вакуолях, а PbPHT5.2 и PbPHT5.3 — в клеточных мембранах.
3.2. Филогенетический анализ
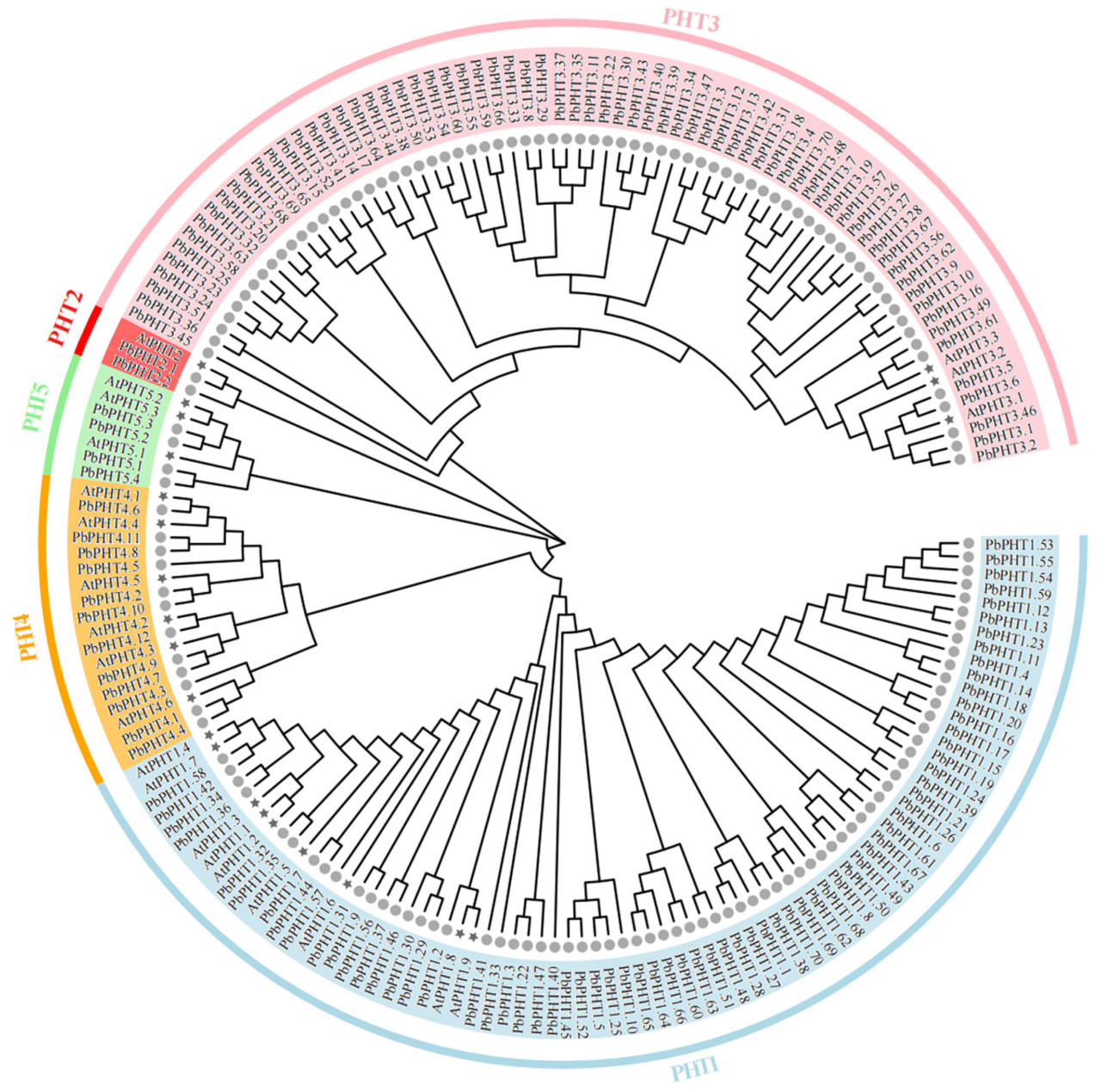
Для анализа эволюционных взаимоотношений между SMXL-белками 'duli' были построены филогенетические отношения между генами PHT 'duli' и арабидопсиса. Мы сгруппировали семейство генов PHT (158 от 'duli' и 22 от арабидопсиса) и разделили его на пять подсемейств: PHT1, PHT2, PHT3, PHT4 и PHT5 (Рисунок 1). Группа PHT1 содержала наибольшее количество членов — 79 PHT-белков. Группа PHT2 содержала наименьшее количество членов — всего три PHT-белка. Как члены PHT 'duli', так и арабидопсиса были сгруппированы под более мелкими ветвями, и гомология членов, сгруппированных в более мелких ветвях, достигала 100%, что предполагает наличие у них сходных биологических функций.
Рисунок 1. Филогенетический анализ PHT-белков. Светло-синий цвет указывает на семейство PHT1. Светло-красный — на семейство PHT2. Розовый — на семейство PHT3. Светло-желтый — на семейство PHT4. Светло-зеленый — на семейство PHT5. Серые кружки обозначают Pyrus betulifolia Bunge (Pb), а черные пентаграммы — Arabidopsis thaliana (At).
3.3. Хромосомная локализация и анализ репликации генов
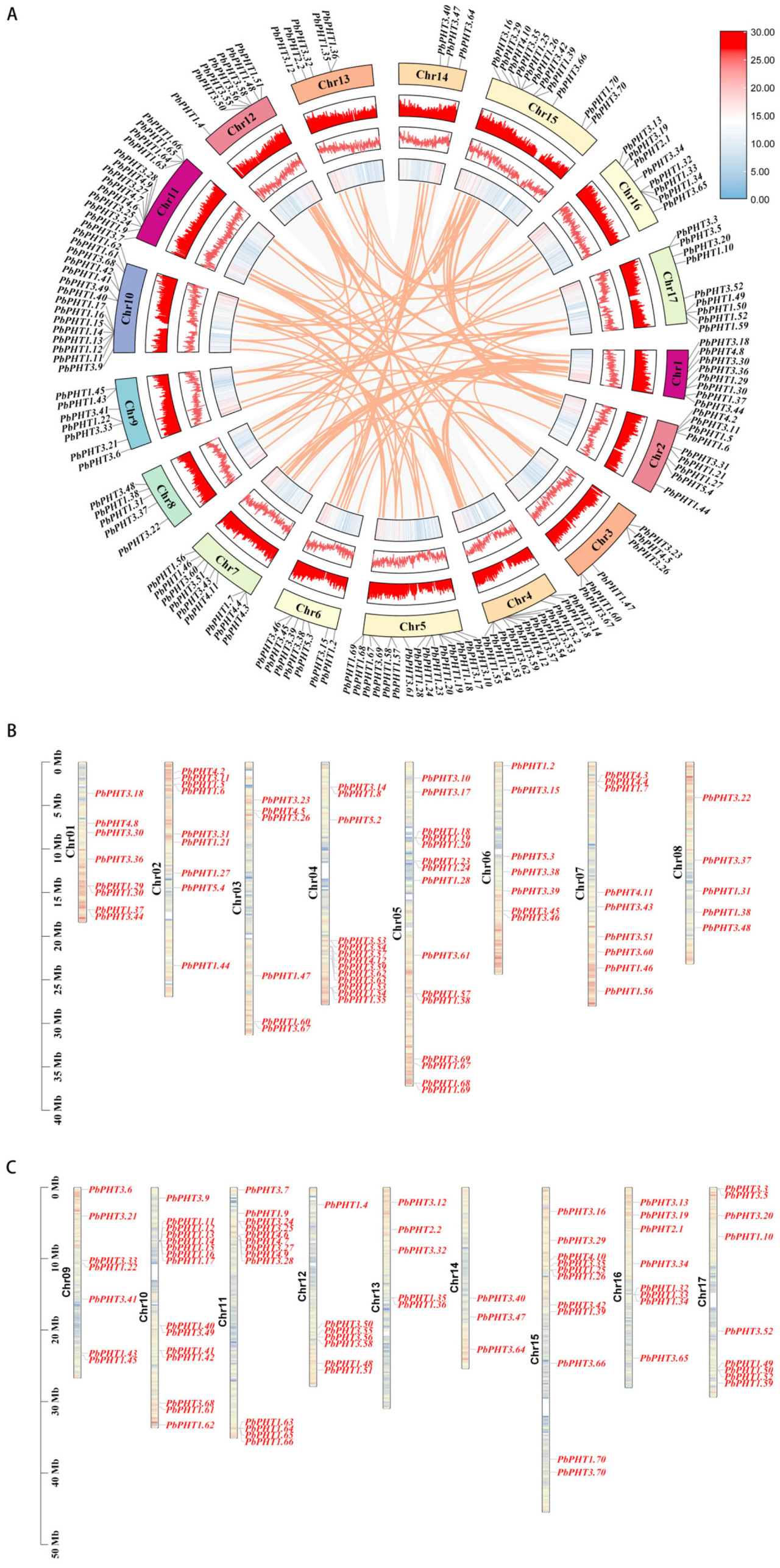
Для изучения геномного распределения генов PHT на хромосомах с помощью программного обеспечения TBtools также был проанализирован хромосомный локус генов семейства PHT. Эти 158 генов расположены на 17 хромосомах (Рисунок 2A). Chr5 и Chr10 содержали наибольшее количество генов PbPHT — по 15 членов PbPHT каждый; за ними следовали Chr04 и Chr11 с 13 членами PbPHT каждый. Chr14 имел наименьшее количество генов PbPHT, включая три члена PbPHT. Также было шесть неименованных хромосом: Scaffold 21, Scaffold 5, Scaffold 2, Contig 15, Scaffold 28 и Contig 11. Генные кластеры в пределах 100 т.п.н. в одних и тех же хромосомных регионах были определены как тандемные дупликации [36]. Мы идентифицировали 18 пар генов PbPHT с тандемными дупликациями (Рисунок 2B,C). Эти пары включали PbPHT1.29 и PbPHT1.30, PbPHT1.37 и PbPHT3.44, PbPHT1.53 и PbPHT1.54, PbPHT1.54 и PbPHT1.55, PbPHT1.18 и PbPHT1.19, PbPHT1.57 и PbPHT1.18, PbPHT1.68 и PbPHT1.69, PbPHT4.3 и PbPHT4.4, PbPHT1.40 и PbPHT3.49, PbPHT1.41 и PbPHT1.42, PbPHT1.35 и PbPHT1.36, PbPHT1.32 и PbPHT1.33, PbPHT1.33 и PbPHT1.34, PbPHT1.63 и PbPHT1.64, PbPHT1.65 и PbPHT1.66, PbPHT1.11 и PbPHT1.12, PbPHT1.13 и PbPHT1.14, а также PbPHT1.15 и PbPHT1.16. Эти события тандемной репликации были наиболее распространены на Chr 01, Chr 04, Chr 05, Chr 06, Chr 07, Chr 10, Chr 11 и Chr 15 и в основном наблюдались у членов семейства PbPHT1.
Рисунок 2. Анализ репликации генов и хромосомной локализации PbPHTs. (A) Анализ коллинеарности PbPHTs. Самый внешний прямоугольный блок представляет собой скелет хромосомы, а три других прямоугольных блока представляют плотность генов на каждой хромосоме. (B) Локализация PbPHTs на хромосомах (Chr 01–Chr 08). (C) Локализация PbPHTs на хромосомах (Chr 09–Chr 17).
3.4. Анализ консервативных мотивов и структуры генов
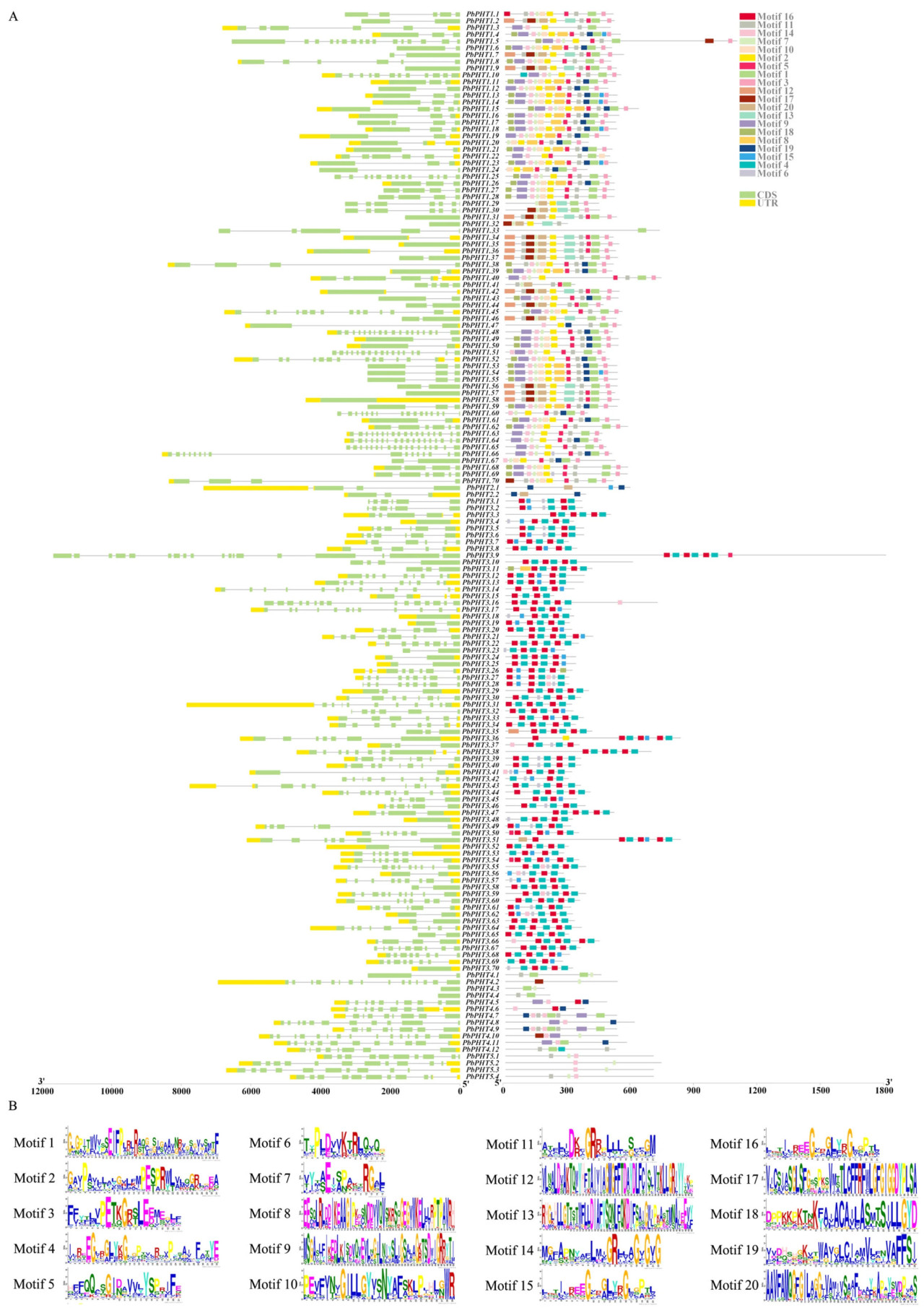
Для дальнейшего уточнения функций PbPHT с использованием полногеномной последовательности 'duli' и файла аннотации генома был проанализирована структура и консервативные мотивы всех PHT-белков. PbPHT имели наиболее разнообразные структуры (Рисунок 3A), количество экзонов варьировало от 0 до 17, что указывает на высокую степень изменчивости между генами. В подсемействе PHT5, за исключением PbPHT5.1, который содержит 9 интронов, остальные члены содержали 10 интронов. Распределение интронов/экзонов относительно равномерно внутри каждого подсемейства, и гены со сходной структурой могут иметь сходные функции. Дополнительно всего было идентифицировано 20 мотивов (Motif 1–Motif 20) у 158 PbPHT (Рисунок 3B). Члены подсемейства PHT1 содержали Motif 1. Члены подсемейства PHT2 содержали только Motif 15, Motif 19 и Motif 20. Все члены подсемейства PHT3 содержали Motif 4 и Motif 5. Семейство PHT5 содержало только три мотива, и все члены семейства PHT5 содержали Motif 7 и Motif 14.
Рисунок 3. Консервативные мотивы и структура генов PbPHTs. (A) Консервативные мотивы и структура генов PbPHTs. Желтые прямоугольники обозначают UTR, а зеленые прямоугольники обозначают CDS. (B) Белковые мотивы (Motif 1–20).
3.5. Анализ цис-регуляторных элементов
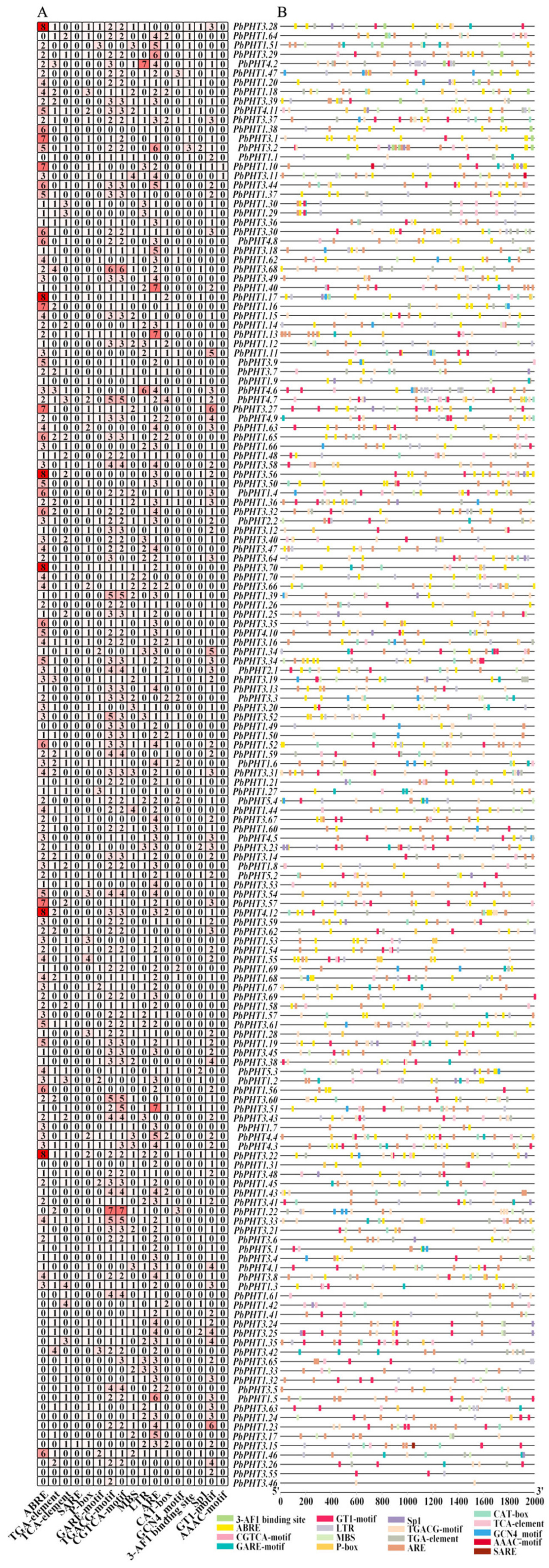
Распределение и количество цис-регуляторных элементов у 158 PbPHT показаны на Рисунке 4. В промоторной области выше по течению были обнаружены светочувствительные элементы, элементы короткого эффектора, элементы, реагирующие на стресс, и элементы, реагирующие на гормоны. Гормональные элементы включали связанные с абсцизовой кислотой ABRE (427), связанные с жасмоновой кислотой TGACG-мотивы (274) и CGTCA-мотивы (272), связанные с гиббереллином P-бокс элементы (86), GARE-мотивы (49), связанные с ауксином TGA-элементы (96) и связанные с салициловой кислотой TCA-элементы (101). PHT2, PHT4 и PHT5 содержали ABRE-элементы; как PHT2, так и PHT5 содержали элементы, связанные с метилжасмонатом. PHT1.17, PHT3.22, PHT3.28, PHT3.56, PHT3.70 и PHT4.12 содержали наибольшее количество ABRE-компонентов (каждый содержал восемь ABRE-компонентов). В PbPHT присутствовали цис-элементы, связанные с абиотическим стрессом, такие как MBS (111), LTR (141) и ARE (365). Дополнительно были идентифицированы цис-регуляторные элементы, связанные с реакцией на свет и ростом, включая 3-AF1 связывающие сайты (17), Sp1 связывающие сайты (39) и GT1-мотив (207), связанные со световыми реакциями, GCN4_мотив (41), связанный с экспрессией эндосперма, и CAT-бокс (81), связанный с меристемой. PbPHT4.7 содержал наибольшее количество цис-регуляторных элементов (28), за ним следовал PbPHT3.22 (24 цис-регуляторных элемента). Большинство членов семейства PbPHT содержали элементы, связанные с гормонами и абиотическим стрессом, но количество этих генов варьировало среди видов.
Рисунок 4. Анализ цис-регуляторных элементов PbPHTs. (A) Количество цис-регуляторных элементов у PbPHTs. Числа внутри ячеек таблицы указывают на количество цис-регуляторных элементов PbPHTs. Оттенок красного цвета указывает на количество цис-регуляторных элементов в генах PbPHT. (B) Распределение цис-регуляторных элементов PbPHTs. Прямоугольники разного цвета представляют различные цис-регуляторные элементы.
3.6. Тканеспецифические паттерны экспрессии PbPHT
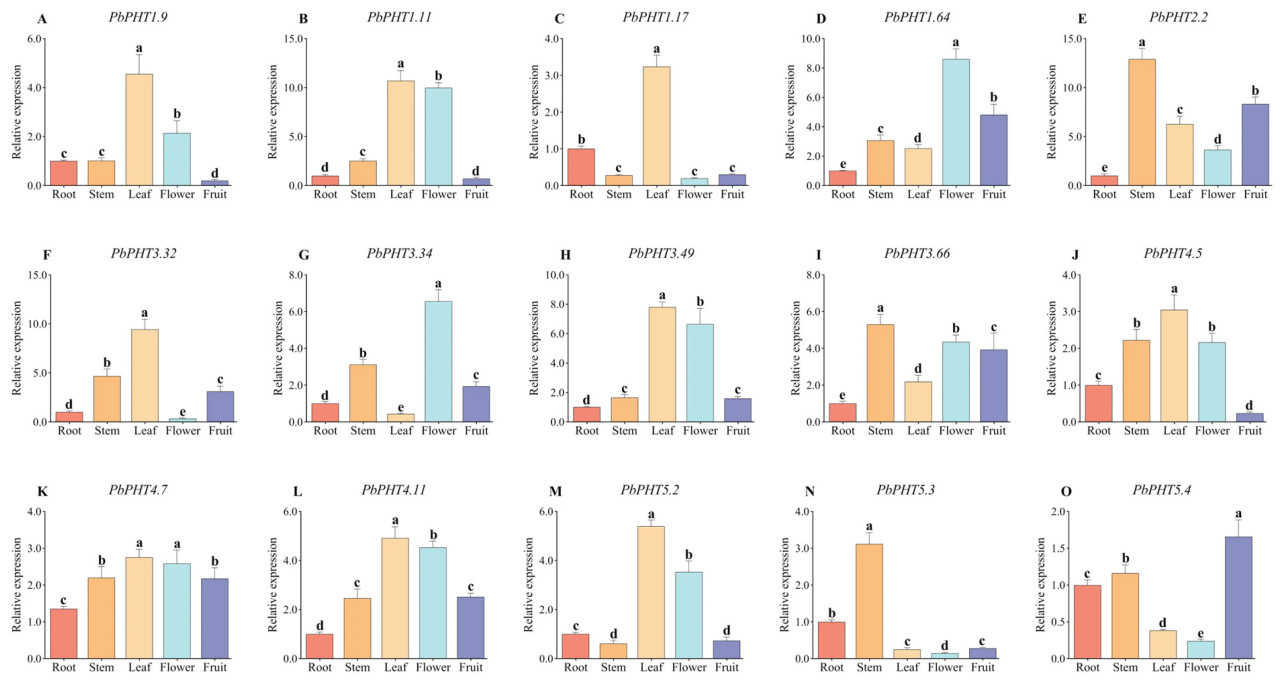
Анализ qRT-PCR показал, что 15 PbPHT повсеместно экспрессировались в плодах, цветках, листьях, стеблях и корнях 'duli' (Рисунок 5). Для членов PHT1, PbPHT1.9 и PbPHT1.17 были повышены в листьях. Уровни экспрессии PbPHT1.11 были выше в листьях, чем в других тканях. Уровни экспрессии PbPHT1.11 были самыми высокими в листьях, и их экспрессия была в 10,71 раза выше в листьях, чем в корнях. PbPHT 2.2 была высоко экспрессирована почти во всех тканях, но ее экспрессия была самой высокой в стеблях, где она была в 1,91 раза выше, чем в корнях. PbPHT4.5 была подавлена в плодах, но повышена в других тканях. Уровни экспрессии PbPHT3.49, PbPHT3.66 и PbPHT4.7 были высокими во всех тканях. Экспрессия PbPHT1.17 была значительно выше в корнях, чем в стеблях, цветках и плодах. Экспрессия PbPHT1.17, PbPHT5.2 и PbPHT5.3 была значительно выше в корнях, чем в стеблях и плодах. Экспрессия PbPHT4.5 и PbPHT4.11 была высокой в стеблях, листьях и цветках, и экспрессия этих генов была самой высокой в листьях. PbPHT5.3 была повышена в листьях, но подавлена в других тканях. Таким образом, уровни экспрессии PbPHT в корнях, стеблях, листьях, цветках и плодах 'duli' были разными.
Рисунок 5. Паттерны экспрессии PbPHTs в различных тканях. Разные строчные буквы указывают на различия между корнями и другими тканями. Разные буквы указывают на значительные различия, а одинаковые буквы указывают на отсутствие значительных различий при p < 0,05.
3.7. Анализ экспрессии PbPHTs в ответ на гормональный, солевой и фосфорный стресс
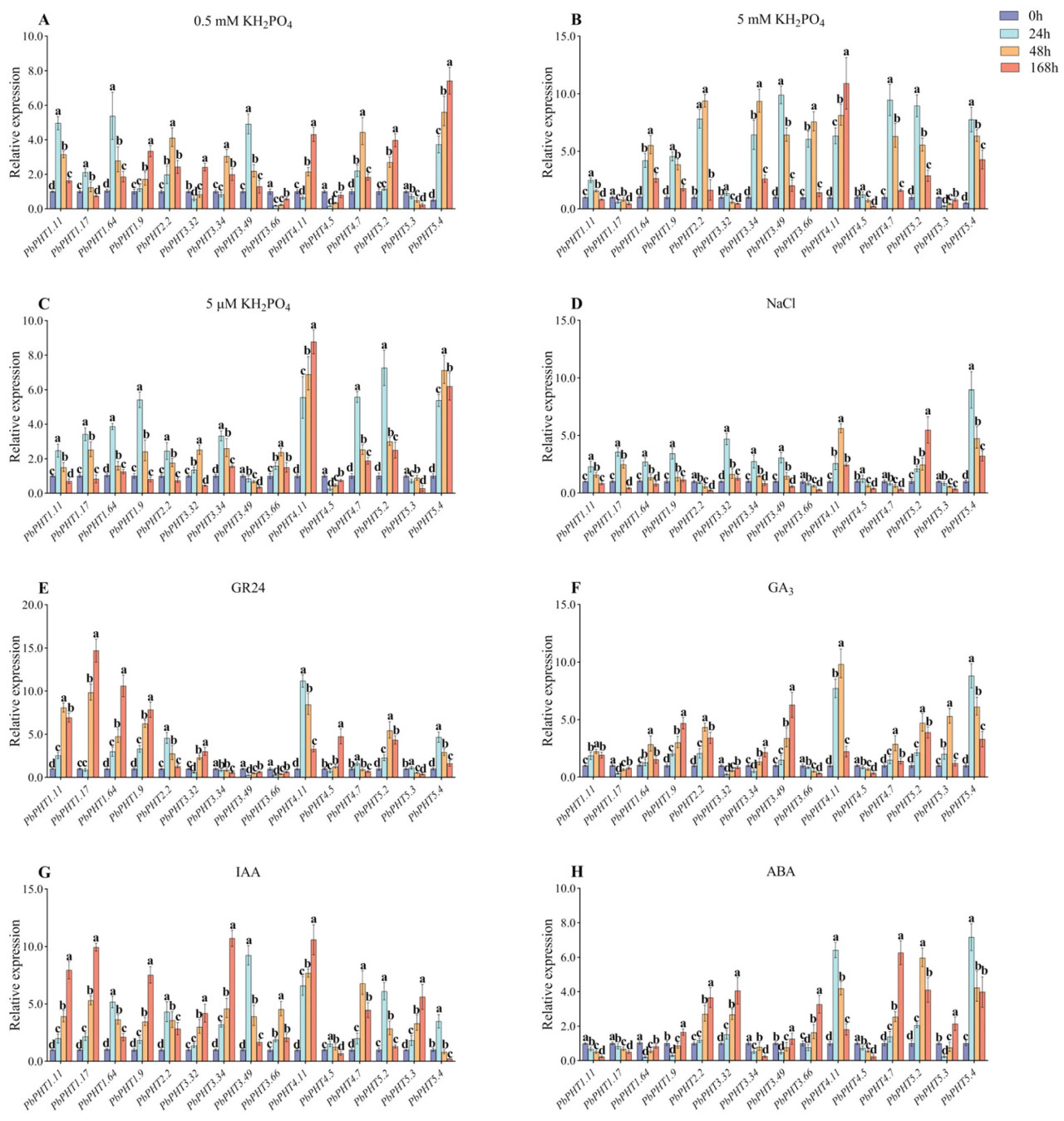
Мы исследовали паттерны экспрессии 15 PbPHT для 'duli' при обработках 5 мкМ KH₂PO₄, 5 мМ KH₂PO₄, 0,5 мМ KH₂PO₄, NaCl, GR24, GA₃, ИУК и АБК (Рисунок 6). После обработки 5 мМ KH₂PO₄ уровни экспрессии PbPHT1.64, PbPHT2.2, PbPHT3.34 и PbPHT3.66 были самыми высокими в 48 ч. После обработки 5 мкМ KH₂PO₄ уровень экспрессии PbPHT4.11 был самым высоким в 168 ч, и уровень экспрессии в 168 ч был в 8,77 раза выше, чем в 0 ч. После обработки NaCl экспрессия восьми PbPHT достигла пика в 24 ч, а затем экспрессия PbPHT1.11, PbPHT1.17, PbPHT1.64, PbPHT1.9, PbPHT3.32, PbPHT3.34, PbPHT3.49 и PbPHT5.4 резко снизилась после 24 ч. Таким образом, большинство PbPHT индуцировались к экспрессии H₂PO₄ и NaCl, но демонстрировали различные паттерны экспрессии.
Рисунок 6. Анализ экспрессии генов PbPHT в ответ на гормональный, солевой и фосфорный стресс: (A) обработка 0,5 мМ KH₂PO₄, (B) обработка 5 мМ KH₂PO₄, (C) обработка 5 мкМ KH₂PO₄, (D) обработка NaCl, (E) обработка GR24, (F) обработка GA₃, (G) обработка ИУК, (H) обработка АБК. Разные строчные буквы указывают на различия между контролем (0 ч) и другими временными точками (24 ч, 48 ч и 168 ч). Разные буквы указывают на значительные различия, а одинаковые буквы указывают на отсутствие значительных различий при p < 0,05.
После обработки GR24 экспрессия PbPHT1.9, PbPHT1.17 и PbPHT1.64 продолжала увеличиваться. Уровень экспрессии PbPHT1.17 был самым высоким в 168 ч, и уровень экспрессии в 168 ч был в 14,69 раза выше, чем в 0 ч. После обработки GA₃ экспрессия PbPHT4.7, PbPHT4.11, PbPHT5.2, PbPHT5.3 и PbPHT5.4 сначала увеличивалась, а затем снижалась. После обработки ИУК экспрессия PbPHT1.11, PbPHT1.17, PbPHT1.9, PbPHT3.32, PbPHT3.34, PbPHT4.7, PbPHT4.11 и PbPHT5.3 продолжала увеличиваться. Уровень экспрессии PbPHT3.34 был самым высоким в 168 ч, и уровень экспрессии в 168 ч был в 10,71 раза выше, чем в 0 ч. Через 24 ч обработки АБК экспрессия PbPHT4.11 и PbPHT5.4 достигла пика. Эти анализы показали, что экспрессия PbPHT индуцировалась обработкой KH₂PO₄, NaCl, GR24, ИУК, GA₃ и АБК, но с различиями в скорости ответа и уровнях экспрессии.
3.8. Содержание, поглощение, перенос и распределение фосфора у 'duli'
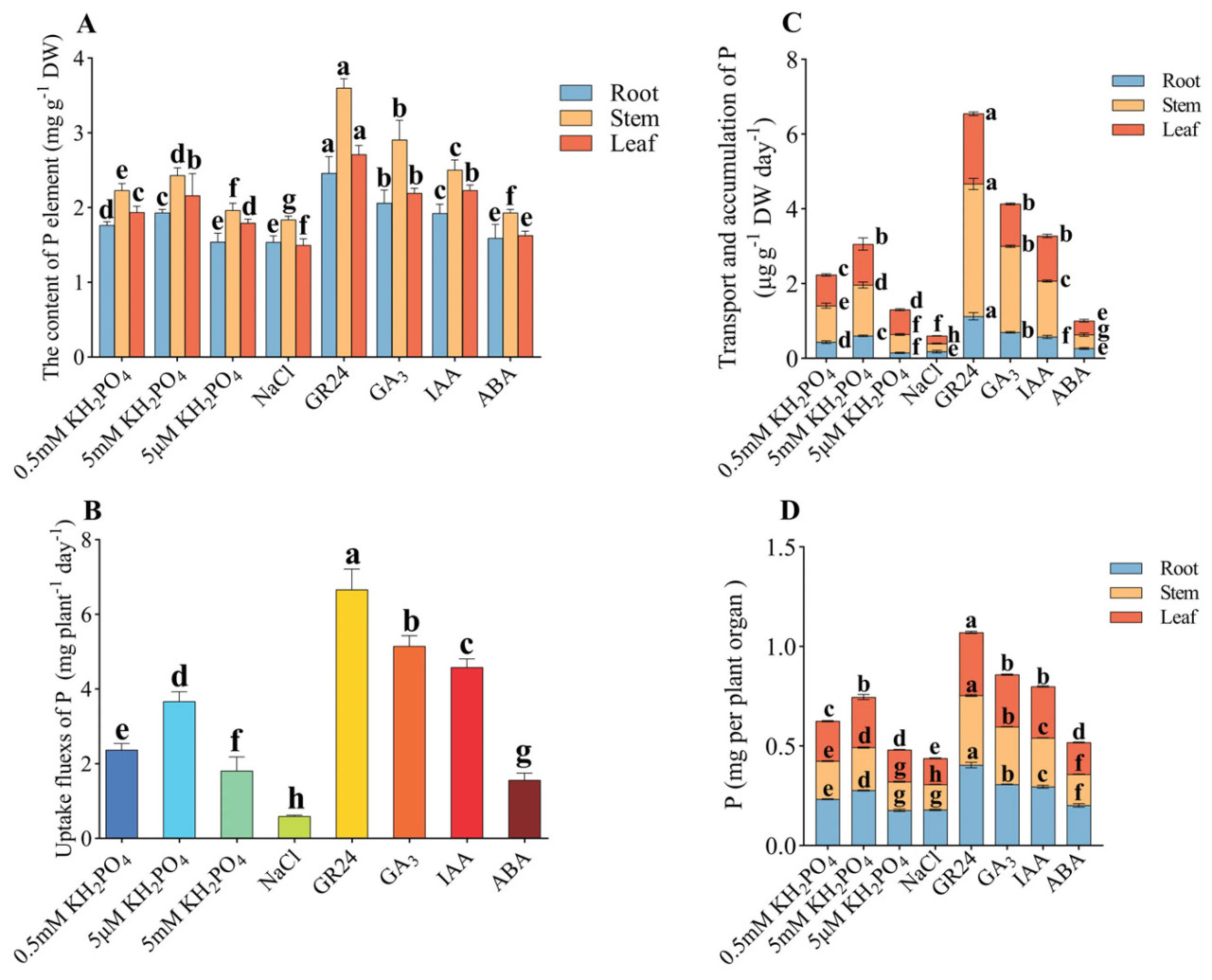
Концентрации P в корнях, стеблях и листьях 'duli' значительно изменились при каждой обработке (Рисунок 7). Концентрация фосфора в листьях, стеблях и корнях значительно увеличивалась при обработках 5 мМ KH₂PO₄, GR24, GA₃ и ИУК. Концентрации P значительно увеличились на 9,42%, 39,65%, 15,06% и 9,11% по сравнению с 0,5 мМ KH₂PO₄ в корнях; концентрации P значительно увеличились на 8,92%, 61,35%, 32,75% и 13,61% по сравнению с 0,5 мМ KH₂PO₄ в стеблях; концентрации P значительно увеличились на 11,63%, 39,93%, 13,26% и 15,11% по сравнению с 0,5 мМ KH₂PO₄ в листьях. Поглощение фосфора 'duli' было значительно снижено обработками 5 мкМ KH₂PO₄, NaCl и АБК, и оно было на 28,73%, 64,92% и 33,44% ниже в этих обработках, чем при обработке 0,5 мМ KH₂PO₄, соответственно. Поглощение P 'duli' было значительно увеличено обработками 5 мМ KH₂PO₄, GR24, GA₃ и ИУК, и поглощение P было самым высоким при обработке GR24; в частности, оно было на 180,13% выше при обработке GR24, чем при обработке 0,5 мМ KH₂PO₄. Известно через перенос (листья и стебли) и накопление (корни) фосфора у 'duli', что скорость переноса P варьировала от 0,22 до 3,54 мкг г⁻¹ день⁻¹ в стеблях, скорость переноса P варьировала от 0,21 до 1,88 мкг г⁻¹ день⁻¹ в листьях, а накопление P варьировало от 0,15 до 1,12 мкг г⁻¹ день⁻¹ в корнях. Известно через распределение фосфора у 'duli' (корни, стебли и листья), что при обработках 5 мМ KH₂PO₄, GR24, GA₃ и ИУК по сравнению с обработкой 0,5 мМ KH₂PO₄ содержание P увеличилось на 18,76%, 73,42%, 31,99% и 26,88% в корнях; содержание P увеличилось на 12,85%, 82,77%, 51,44% и 28,30% в стеблях; и содержание P увеличилось на 26,23%, 57,89%, 30,11% и 28,47% в листьях. При обработках 5 мкМ KH₂PO₄, NaCl и АБК содержание P снизилось на 23,87%, 22,93% и 13,48% в корнях; содержание P снизилось на 25,07%, 33,32% и 18,33% в стеблях; и содержание P снизилось на 20,31%, 34,94% и 20,16% в листьях.
Рисунок 7. Содержание, поглощение, перенос и распределение фосфора у 'duli'. (A) Концентрация фосфора (корни, листья и стебли) у растений 'duli'. Разные строчные буквы указывают на различия между корнями и другими тканями. (B) Поглощение фосфора растениями 'duli'. Столбцы разного цвета указывают на различные стрессовые обработки. (C) Перенос (листья и стебли) и накопление (корни) фосфора у растений 'duli'. (D) Распределение фосфора у растений 'duli'. Разные буквы указывают на значительные различия, а одинаковые буквы указывают на отсутствие значительных различий при p < 0,05.
3.9. Корреляционный анализ
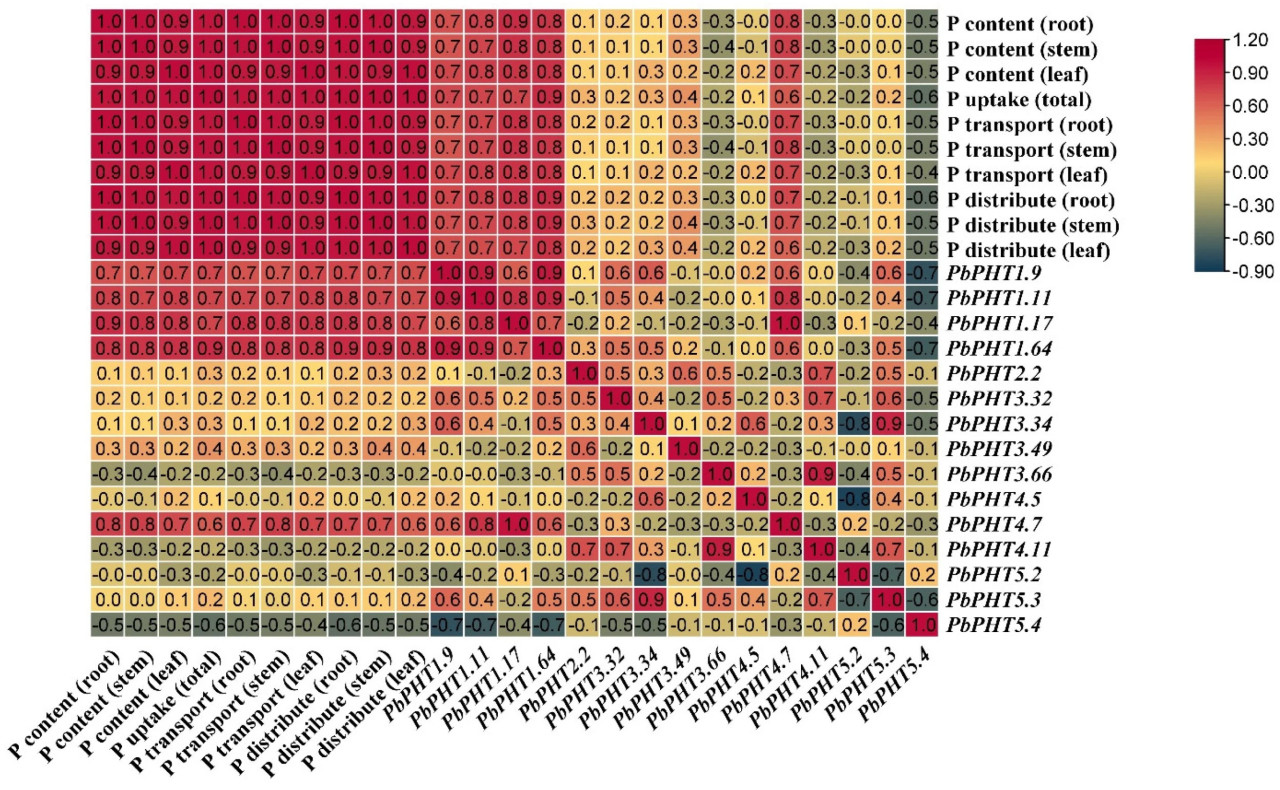
Корреляционный анализ был проведен для 10 физиологических показателей и паттернов экспрессии 15 генов (Рисунок 8). Экспрессия PbPHT1.9, PbPHT1.11, PbPHT1.17, PbPHT1.64 и PbPHT4.7 была значительно положительно коррелирована с поглощением P, а также с концентрацией, переносом и распределением P в корнях, стеблях и листьях. Экспрессия PbPHT5.4 была значительно отрицательно коррелирована с поглощением P, а также с концентрацией, переносом и распределением P в корнях, стеблях и листьях. Экспрессия PbPHT1.9 была значительно положительно коррелирована с экспрессией PbPHT1.11, PbPHT1.17, PbPHT1.64, PbPHT3.32, PbPHT3.34, PbPHT4.7 и PbPHT5.3. Экспрессия PbPHT5.4 была значительно отрицательно коррелирована с экспрессией PbPHT1.9, PbPHT1.1, PbPHT1.64, PbPHT3.32, PbPHT3.34 и PbPHT5.3. Экспрессия PbPHT5.2 была значительно отрицательно коррелирована с экспрессией PbPHT3.34, PbPHT5.3 и PbPHT4.5.
Рисунок 8. Корреляционный анализ между уровнями экспрессии 15 PbPHT и 10 физиологическими показателями. Числа внутри ячеек таблицы представляют коэффициенты корреляции.
4. Обсуждение
4.1. Идентификация, репликация генов и анализ структуры генов PbPHT у 'duli'
P является ключевым компонентом нуклеиновых кислот, фосфолипидов и АТФ, которые участвуют в таких биологических процессах, как перенос энергии и клеточная передача сигналов у растений. У растений гены PHT опосредуют поглощение и транслокацию Pi. Члены семейства генов PHT были описаны для многих растений, включая ячмень [37], пшеницу [38], палец-просо [39], томат [19], зеленые водоросли [40], сахарный тростник [20], Lupinus albus [41], яблоню [18], сорго [24], тополь [22] и Camelina sativa [1]. В данном исследовании было идентифицировано 158 PbPHT, включая 70 PbPHT1, 2 PbPHT2, 70 PbPHT3, 12 PbPHT4 и 4 PbPHT5. Количество PHT в геноме 'duli' было выше, чем в геномах риса, тополя, яблони и сорго, что может быть связано с различиями в размере генома и тандемной дупликацией генов.
Репликация генов является основным драйвером амплификации генных семейств и включает тандемную дупликацию генов и дупликацию фрагментов [20,39]. Анализ дупликации генов выявил 18 пар генов с тандемной дупликацией. В этом исследовании в геноме 'duli' было обнаружено 18 пар тандемно дуплицированных генов; это превышает количество PHT у сорго [24], сахарного тростника [20] и Brassica [25], и увеличение количества тандемных повторов может увеличивать количество членов семейства PbPHT.
На ранних стадиях амплификации генов некоторые гены постепенно теряют свои интроны [42]. В случае селективного давления на интроны гены без интронов могут эволюционировать быстро [43]. Анализ структуры гена и состава мотивов показал, что большинство генов PbPHT одного подсемейства имеют сходную структуру и распределение мотивов. Однако также существуют некоторые гены семейства PbPHT, которые не имеют интронов. Поэтому предполагается, что некоторые PbPHT со временем могут постепенно терять свои интроны и достигать функциональной эволюции.
4.2. Паттерны экспрессии PbPHTs в различных тканях
Паттерны экспрессии PbPHT1s, PbPHT2s, PbPHT3s, PbPHT4s и PbPHT5s различались между тканями. Мы обнаружили, что PbPHT1.9, PbPHT1.11 и PbPHT1.64 были высоко экспрессированы в корнях, листьях и цветках. То же самое наблюдалось у арабидопсиса, где большинство членов семейства AtPHT1 были высоко экспрессированы в корнях, но также и в листьях и цветках [44,45]. У яблони MdPHT1.12 высоко экспрессирован в корнях, листьях и цветках [18]. Эти результаты указывают на то, что гены семейства PHT1 могут играть роль в поглощении Pi у разных видов. PbPHT 2.2, PbPHT3.49, PbPHT3.66 и PbPHT4.7 были высоко экспрессированы почти во всех тканях, PbPHT 5.2 был высоко экспрессирован в листьях и цветках, PbPHT 5.3 был высоко экспрессирован в стеблях, а PbPHT 5.4 был высоко экспрессирован в плодах. Экспрессия генов PbPHT варьировала между тканями, что предполагает, что эти гены могут играть разные роли в поглощении, распределении, переносе и хранении Pi. Аналогичный вывод был сделан в корреляционном анализе. Экспрессия PbPHT1.9, PbPHT1.11, PbPHT1.17, PbPHT1.64 и PbPHT4.7 была положительно коррелирована с поглощением P, а также с концентрацией, переносом и распределением P в корнях, стеблях и листьях. Экспрессия PbPHT5.4 была значительно отрицательно коррелирована с поглощением P, а также с концентрацией, переносом и распределением P в корнях, стеблях и листьях. Эти результаты указывают на то, что экспрессия генов PbPHT1.9, PbPHT1.11, PbPHT1.17, PbPHT1.64, PbPHT4.7 и PbPHT5.4 играет важную роль в поглощении, переносе и хранении Pi. Однако конкретные функции PbPHT1.9, PbPHT1.11, PbPHT1.17, PbPHT1.64, PbPHT4.7 и PbPHT5.4 требуют дальнейшего исследования.
4.3. Анализ экспрессии PbPHTs в ответ на фосфорный стресс
PHT1, кодирующий высокоаффинный транспортер Pi, в основном экспрессировался в корнях, и его экспрессия индуцировалась низким содержанием P. У арабидопсиса [46] и яблони [18] ген PHT1 является высокоаффинным транспортером. Экспрессия большинства генов ATPHT1 была значительно повышена в условиях гипофосфата. MdPHT1.1 и MdPHT1.7 экспрессировались в условиях низкого Pi. Анализ qRT-PCR в данном исследовании показал, что экспрессия PbPHT1.9, PbPHT1.11, PbPHT1.17 и PbPHT1.64 была повышена после обработки с низким содержанием P. Члены семейства PbPHT1 демонстрировали сходные паттерны экспрессии у арабидопсиса и яблони. Эти результаты предполагают, что белок, кодируемый геном PbPHT1, также может быть высокоаффинным транспортером. Когда растения подвергаются избытку Pi, экспрессия PbPHT3.66, PbPHT4.11, PbPHT4.7 и PbPHT5.4 повышается, что предполагает, что они кодируют низкоаффинные транспортеры. Однако детальные характеристики PbPHT требуют дальнейшего исследования.
4.4. Анализ экспрессии PbPHTs в ответ на регуляторы роста растений
Экспрессия генов регулируется цис-регуляторными элементами [39,46,47]. Промоторы PbPHT содержат множество цис-регуляторных элементов, связанных с реакцией на стресс, гормоны и свет. Анализ qRT-PCR PbPHT показал, что разные гены демонстрировали разные паттерны экспрессии при одной и той же обработке, что может быть связано с видом и распределением цис-регуляторных элементов в промоторной области PbPHT. Мы обнаружили избыток ABA-чувствительных элементов, ауксин-чувствительных элементов и GA-чувствительных элементов в промоторных областях разных членов PbPHT. Анализы qRT-PCR выявили, что АБК, ИУК, ГА и GR24 могли индуцировать экспрессию большинства генов PbPHT. Паттерны экспрессии PbPHT1.9, PbPHT2.2, PbPHT4.7, PbPHT4.11, PbPHT5.2 и PbPHT5.4 были чувствительны к обработкам экзогенным GR24, GA, ABA и ИУК, что указывает на то, что они могут играть роль в интеграции путей SL, GA, ABA и ИУК у 'duli'. Однако механизм, с помощью которого PbPHT регулируют взаимодействие между гормонами, требует дальнейшего изучения.
4.5. Анализ экспрессии PbPHTs в ответ на солевой стресс
Солевой стресс может снизить эффективность поглощения и использования P растениями. Экспрессия PbPHT3.32, PbPHT3.34 и PbPHT3.49 была значительно повышена при солевой обработке, а PbPHT3 локализуется в митохондриях. Скорость дыхания 'duli' ускорялась, и производилось больше активных форм кислорода при солевом стрессе. Повышение экспрессии PbPHT3.32, PbPHT3.34 и PbPHT3.49 способствовало переносу Pi и превращению АДФ в АТФ у 'duli', что обеспечивало энергию для повышения его устойчивости к солевому стрессу. Аналогичные выводы были сделаны Takabatake и др. [11]. Семейство PHT3 является митохондриальным транспортером Pi (MPT). Оно поддерживает обмен Pi между цитоплазмой и митохондриальным матриксом через симпорт Pi/H⁺ или антипорт Pi/OH⁻, катализируя реакцию фосфорилирования АДФ и Pi с образованием АТФ [48]. Таким образом, члены семейства PHT3 могут играть важную роль в устойчивости 'duli' к солевому стрессу. Предыдущие исследования гена PHT3 у арабидопсиса показали, что он быстро повышается при солевом стрессе и регулирует уровни АТФ и гиббереллина в ответ на солевой стресс. Поэтому PbPHT3.32, PbPHT3.34 и PbPHT3.49 могут иметь функции, аналогичные гену AtPHT3. Однако конкретные функции PbPHT3.32, PbPHT3.34 и PbPHT3.49 требуют дальнейшего изучения.
4.6. Арбускулярные микоризные (АМ) грибы и фосфор
Некоторые исследования обнаружили, что через обширную гифальную сеть арбускулярных микоризных грибов (АМГ) растения-хозяева могут получать воду и питательные вещества из почвы, особенно фосфор [49]. В данном исследовании было обнаружено, что при обработке GR24 уровни экспрессии генов семейства PbPHT1 были значительно повышены, а экспрессия PbPHT1.9, PbPHT1.11, PbPHT1.17 и PbPHT1.64 была значительно положительно коррелирована с поглощением фосфора. Возможно, что страголактоны способствуют симбиотическим отношениям между Pyrus betulaefolia и арбускулярными микоризными грибами и способствуют ветвлению гиф, и что арбускулярные микоризные грибы индуцируют экспрессию гена PbPHT1, тем самым способствуя поглощению фосфора Pyrus betulaefolia. Исследование Hélène Javot и др. [50] также подтвердило этот момент. Симбиотические отношения с АМ могут влиять на транскрипционный уровень транспортеров PHT1 и влиять на поглощение фосфора растениями.
5. Выводы
Мы идентифицировали 158 генов PbPHT, включая 70 PbPHT1, 2 PbPHT2, 70 PbPHT3, 12 PbPHT4 и 4 PbPHT5 у 'duli', и охарактеризовали их физико-химические свойства, репликацию генов, хромосомное положение, эволюционные отношения, структуры и консервативные мотивы. Анализ экспрессии генов выявил дифференциальные паттерны экспрессии PbPHT в разных тканях и в ответ на 5 мкМ KH₂PO₄, 5 мМ KH₂PO₄, 0,5 мМ KH₂PO₄, NaCl, GA₃, ИУК, GR24 и АБК. Дополнительно мы обнаружили, что обработки 5 мМ KH₂PO₄, GR24, GA₃ и ИУК значительно увеличивали концентрацию, поглощение, перенос, накопление и распределение фосфора; противоположные эффекты наблюдались при обработках 5 мкМ KH₂PO₄, АБК и NaCl. Корреляционный анализ показал, что PbPHT1.9, PbPHT1.11, PbPHT1.17, PbPHT1.64, PbPHT4.7 и PbPHT5.4 были вовлечены в концентрацию, перенос и распределение P. Наши результаты подчеркивают основу для дальнейших исследований функции генов PHT 'duli' и углубленной идентификации генов-кандидатов для селекции 'duli' на устойчивость к абиотическим стрессам.
Дополнительные материалы
Следующая вспомогательная информация может быть загружена по адресу: https://www.mdpi.com/article/10.3390/agriculture15020199/s1, Таблица S1: Физико-химические свойства, вторичная структура белков и прогноз субклеточной локализации PHT-белков 'duli'.
Ссылки
1. Lhamo, D.; Shao, Q.L.; Tang, R.J.; Luan, S. Genome-wide analysis of the five phosphate transporter families in Camelina sativa and their expressions in response to low-P. Int. J. Mol. Sci. 2020, 21, 8365. [Google Scholar] [CrossRef] [PubMed]
2. Ghodszad, L.; Reyhanitabar, A.; Oustan, S.; Alidokht, L. Phosphorus sorption and desorption characteristics of soils as affected by biochar. Soil Till. Res. 2022, 216, 105251. [Google Scholar] [CrossRef]
3. Stewart, A.J.; Chapman, W.; Jenkins, G.I.; Graham, I.; Martin, T.; Crozier, A. The effect of nitrogen and phosphorus deficiency on flavonol accumulation in plant tissues. Plant Cell Environ. 2001, 24, 1189–1197. [Google Scholar] [CrossRef]
4. Gu, M.; Chen, A.Q.; Sun, S.B.; Xu, G.H. Complex regulation of plant phosphate transporters and the gap between molecular mechanisms and practical application: What is missing? Mol.Plant 2016, 9, 396–416. [Google Scholar] [CrossRef] [PubMed]
5. Wang, D.L.Y.; Lv, S.L.; Jiang, P.; Li, Y.X. Roles, regulation, and agricultural application of plant phosphate transporters. Front. Plant Sci. 2017, 8, 817. [Google Scholar] [CrossRef] [PubMed]
6. Zhang, Y.; Hu, L.Z.; Yu, D.S.; Xu, K.D.; Zhang, J.; Li, X.L.; Wang, P.F.; Chen, G.; Liu, Z.H.; Peng, C.F.; et al. Integrative analysis of the wheat PHT1 gene family reveals a novel member involved in arbuscular mycorrhizal phosphate pransport and pmmunity. Cells 2019, 8, 490. [Google Scholar] [CrossRef]
7. Misson, J.; Thibaud, M.C.; Bechtold, N.; Raghothama, K.; Nussaume, L. Transcriptional regulation and functional properties of Arabidopsis Pht1;4, a high affinity transporter contributing greatly to phosphate uptake in phosphate deprived plants. Plant Mol. Biol. 2004, 55, 727–741. [Google Scholar] [CrossRef] [PubMed]
8. Shin, H.; Shin, H.S.; Dewbre, G.R.; Harrison, M.J. Phosphate transport in Arabidopsis Pht1;1 and Pht1;4 play a major role in phosphate acquisition from both low- and high-phosphate environments. Plant J. 2004, 39, 629–642. [Google Scholar] [CrossRef] [PubMed]
9. Nagarajan, V.K.; Jain, A.; Poling, M.D.; Lewis, A.J.; Raghothama, K.G.; Smith, A.P. Arabidopsis Pht1;5 Mobilizes Phosphate between Source and Sink Organs and Influences the Interaction between Phosphate Homeostasis and Ethylene Signaling. Plant Physiol. 2011, 156, 1149–1163. [Google Scholar] [CrossRef] [PubMed]
10. Lin, W.Y.; Huang, T.K.; Chiou, T.J. Nitrogen limitation adaptation, a Target of microRNA827, mediates degradation of plasma membrane-localized phosphate transporters to maintain phosphate homeostasis in Arabidopsis. Plant Cell 2013, 25, 4061–4074. [Google Scholar] [CrossRef] [PubMed]
11. Takabatake, R.; Hata, S.; Taniguchi, M.; Kouchi, H.; Sugiyama, T.; Izui, K. Isolation and characterization of cDNAs encoding mitochondrial phosphate transporters in soybean, maize, rice, and Arabidopsis. Plant Mol. Biol. 1999, 40, 479–486. [Google Scholar] [CrossRef]
12. Wang, G.Y.; Shi, J.L.; Ng, G.; Battle, S.L.; Zhang, C.; Lu, H. Circadian clock-regulated phosphate Transporter PHT4;1 plays an important role in Arabidopsis defense. Mol. Plant 2011, 4, 516–526. [Google Scholar] [CrossRef] [PubMed]
13. Irigoyen, S.; Karlsson, P.M.; Kuruvilla, J.; Spetea, C.; Versaw, W.K. The sink-specific plastidic phosphate transporter PHT4;2 influences starch accumulation and leaf size in arabidopsis. Plant Physiol. 2011, 157, 1765–1777. [Google Scholar] [CrossRef]
14. Cubero, B.; Nakagawa, Y.; Jiang, X.Y.; Miura, K.J.; Li, F.; Raghothama, K.G.; Bressan, R.A.; Hasegawa, P.M.; Pardo, J.M. The phosphate transporter PHT4;6 is a determinant of salt tTolerance that is localized to the golgi apparatus of Arabidopsis. Mol. Plant 2009, 2, 535–552. [Google Scholar] [CrossRef] [PubMed]
15. Liu, T.Y.; Huang, T.K.; Yang, S.Y.; Hong, Y.T.; Huang, S.M.; Wang, F.N.; Chiang, S.F.; Tsai, S.Y.; Lu, W.C.; Chiou, T.J. Identification of plant vacuolar transporters mediating phosphate storage. Nat. Commun. 2016, 7, 11095. [Google Scholar] [CrossRef] [PubMed]
16. Luan, M.D.; Zhao, F.G.; Han, X.B.; Sun, G.F.; Yang, Y.; Liu, J.L.; Shi, J.S.; Fu, A.G.; Lan, W.Z.; Luan, S. Vacuolar phosphate transporters contribute to systemic phosphate homeostasis vital for reproductive development in Arabidopsis. Plant Physiol. 2019, 179, 640–655. [Google Scholar] [CrossRef]
17. Shane, M.W.; McCully, M.E.; Lambers, H. Tissue and cellular phosphorus storage during development of phosphorus toxicity in Hakea prostrata (Proteaceae). J. Exp. Bot. 2004, 55, 1033–1044. [Google Scholar] [CrossRef]
18. Sun, T.T.; Li, M.J.; Shao, Y.; Yu, L.W.; Ma, F.W. Comprehensive genomic identification and expression analysis of the phosphate transporter (PHT) gene family in apple. Front. Plant Sci. 2017, 8, 426. [Google Scholar] [CrossRef] [PubMed]
19. Rui, W.J.; Ma, J.; Wei, N.; Zhu, X.Y.; Li, Z.F. Genome-wide analysis of the PHT gene family and its response to mycorrhizal symbiosis in tomatoes under phosphate starvation conditions. Int. J. Mol. Sci. 2023, 24, 10246. [Google Scholar] [CrossRef] [PubMed]
20. Murugan, N.; Palanisamy, V.; Channappa, M.; Ramanathan, V.; Ramaswamy, M.; Govindakurup, H.; Chinnaswamy, A. Genome-wide in silico identification, structural analysis, promoter analysis, and expression profiling of PHT gene family in sugarcane root under salinity stress. Sustainability 2022, 14, 15893. [Google Scholar] [CrossRef]
21. Ahmad, I.; Rawoof, A.; Islam, K.; Momo, J.; Ramchiary, N. Identification and expression analysis of phosphate transporter genes and metabolites in response to phosphate stress in capsicum annuum. Environ. Exp. Bot. 2021, 190, 104597. [Google Scholar] [CrossRef]
22. Zhang, C.X.; Meng, S.; Li, M.J.; Zhao, Z. Genomic identification and expression analysis of the phosphate transporter gene family in poplar. Front. Plant Sci. 2016, 7, 1398. [Google Scholar] [CrossRef]
23. Okumura, S.; Mitsukawa, N.; Shirano, Y.; Shibata, D. Phosphate transporter gene family of Arabidopsis thaliana. DNA Res. 1998, 5, 261–269. [Google Scholar] [CrossRef]
24. Wang, J.H.; Yang, Y.; Liao, L.; Xu, J.W.; Liang, X.; Liu, W. Genome-wide identification and functional characterization of the phosphate transporter gene family in Sorghum. Biomolecules 2019, 9, 670. [Google Scholar] [CrossRef]
25. Wan, Y.Y.; Wang, Z.; Xia, J.H.; Shen, S.L.; Guan, M.W.; Zhu, M.C.; Qiao, C.L.; Sun, F.J.; Liang, Y.; Li, J.; et al. Genome-wide analysis of phosphorus transporter genes in brassica and their roles in heavy metal stress tolerance. Int. J. Mol. Sci. 2020, 21, 2209. [Google Scholar] [CrossRef]
26. Cao, D.; Liu, Y.L.; Ma, L.L.; Liu, Z.H.; Li, J.; Wen, B.B.; Zhang, X.N.; Yin, P.; Jin, X.F.; Huang, J.N. Genome-wide identification and characterization of phosphate transporter gene family members in tea plants (Camellia sinensis L. O. kuntze) under different selenite levels. Plant Physiol. Biochem. 2021, 166, 668–676. [Google Scholar] [CrossRef]
27. Luo, S.C.; Xu, P.X.; Cheng, A.; Wang, X.; Xu, J.F.; Ma, H.; Zhang, Y.X.; Zhang, H.X. Comprehensive analysis of the bZIP gene family in ‘Duli’ pear (Pyrus betulifolia Bunge): Insights for research on abiotic stress, especially drought, in pear. Sci. Hortic. 2024, 334, 113302. [Google Scholar] [CrossRef]
28. Chen, G.D.; Li, Y.; Jin, C.; Wang, J.Z.; Wang, L.; Wu, J.Y. Physiological and morphological responses of hydroponically grown pear rootstock under phosphorus treatment. Front. Plant Sci. 2021, 12, 696045. [Google Scholar] [CrossRef]
29. Song, K.; Qin, Q.; Yang, Y.F.; Sun, L.J.; Sun, Y.F.; Zheng, X.Q.; Lu, W.G.; Xue, Y. Drip fertigation and plant hedgerows significantly reduce nitrogen and phosphorus losses and maintain high fruit yields in intensive orchards. J. Integr. Agr. 2023, 22, 598–610. [Google Scholar] [CrossRef]
30. Zhang, W.L.; Yuan, S.; Liu, N.; Zhang, H.X.; Zhang, Y.X. Glutamine synthetase and glutamate synthase family perform diverse physiological functions in exogenous hormones and abiotic stress responses in Pyrus betulifolia Bunge (P.be). Plants 2024, 13, 2759. [Google Scholar] [CrossRef]
31. Zhang, W.L.; Cheng, X.H.; Jing, Z.T.; Cao, Y.; Yuan, S.; Zhang, H.X.; Zhang, Y.X. Exogenous GA3 enhances nitrogen uptake and metabolism under low nitrate conditions in ‘Duli’ (Pyrus betulifolia Bunge) seedlings. Int. J. Mol. Sci. 2024, 25, 7967. [Google Scholar] [CrossRef]
32. Yuan, S.; Zhang, W.L.; Zhang, Y.X. Characterization of SUPPRESSOR OF MAX2 1-LIKE (SMXL) Genes in ‘duli’ (Pyrus betulifolia L.) and Expression Analysis of PbSMXLs in Response to Plant Growth Regulators and Salt Stress. Agronomy 2024, 14, 2778. [Google Scholar] [CrossRef]
33. Liang, B.W.; Ma, C.Q.; Zhang, Z.J.; Wei, Z.W.; Gao, T.T.; Zhao, Q.; Ma, F.W.; Li, C. Long-term exogenous application of melatonin improves nutrient uptake fluxes in apple plants under moderate drought stress. Environ. Exp Bot. 2018, 155, 650–661. [Google Scholar] [CrossRef]
34. Liang, B.W.; Gao, T.T.; Zhao, Q.; Ma, C.Q.; Chen, Q.; Wei, Z.W.; Li, C.Y.; Li, C.; Ma, F.W. Effects of exogenous dopamine on the uptake, transport, and resorption of apple ionome under moderate drought. Plant Sci. 2018, 9, 755. [Google Scholar] [CrossRef] [PubMed]
35. Ji, J.H.; He, X.L.; Liu, H.T.; Li, Z.Y.; Zhou, S.S.; Zhang, X.Y.; Xu, J.Z.; Liang, B.W. Influence of dwarfing interstock on the tolerance and nutrient utilization efficiency of apple trees under drought stress. Sci. Hortic. 2023, 315, 111984. [Google Scholar] [CrossRef]
36. Sun, Y.M.; Jia, X.Y.; Yang, Z.R.; Fu, Q.J.; Yang, H.H.; Xu, X.Y. Genome-wide identification of PEBP gene family in Solanum lycopersicum. Int. J. Mol. Sci. 2023, 24, 9185. [Google Scholar] [CrossRef] [PubMed]
37. Rae, A.L.; Cybinski, D.H.; Jarmey, J.M.; Smith, F.W. Characterization of two phosphate transporters from barley; evidence for diverse function and kinetic properties among members of the Pht1 family. Plant Mol. Biol. 2003, 53, 27–36. [Google Scholar] [CrossRef] [PubMed]
38. Teng, W.; Zhao, Y.Y.; Zhao, X.Q.; He, X.; Ma, W.Y.; Deng, Y.; Chen, X.P.; Tong, Y.P. Genome-wide identification, characterization, and expression analysis of PHT1 phosphate transporters in wheat. Front. Plant Sci. 2017, 8, 543. [Google Scholar] [CrossRef]
39. Pudake, R.N.; Mehta, C.M.; Mohanta, T.K.; Sharma, S.; Varma, A.; Sharma, A.K. Expression of four phosphate transporter genes from finger millet (Eleusine coracana L.) in response to mycorrhizal colonization and Pi stress. 3 Biotech 2017, 7, 17. [Google Scholar] [CrossRef] [PubMed]
40. Wang, L.; Xiao, L.; Yang, H.Y.; Chen, G.L.; Zeng, H.Q.; Zhao, H.Y.; Zhu, Y.Y. Genome-wide identification, eexpression profiling, and evolution of phosphate transporter gene family in green algae. Front. Genet. 2020, 11, 590947. [Google Scholar] [CrossRef]
41. Aslam, M.M.; Waseem, M.; Xu, W.; ul Qamar, M.T. Identification and expression analysis of phosphate transporter (PHT) gene family in Lupinus albus cluster root under phosphorus stress. Int. J. Biol. Macromol. 2022, 205, 772–781. [Google Scholar] [CrossRef] [PubMed]
42. Roy, S.W.; Gilbert, W. The evolution of spliceosomal introns: Patterns, puzzles and progress. Nat. Rev. Genet. 2006, 7, 211–221. [Google Scholar] [CrossRef] [PubMed]
43. Roy, S.W.; Penny, D. A very high fraction of unique intron positions in the intron-rich diatom Thalassiosira pseudonana indicates widespread intron gain. Mol. Biol. Evol. 2007, 24, 1447–1457. [Google Scholar] [CrossRef]
44. Mudge, S.R.; Rae, A.L.; Diatloff, E.; Smith, F.W. Expression analysis suggests novel roles for members of the Pht1 family of phosphate transporters in Arabidopsis. Plant J. 2002, 31, 341–353. [Google Scholar] [CrossRef]
45. Schünmann, P.H.D.; Richardson, A.E.; Smith, F.W.; Delhaize, E. Characterization of promoter expression patterns derived from the Pht1 phosphate transporter genes of barley (Hordeum vulgare L.). J. Exp. Bot. 2004, 55, 855–865. [Google Scholar] [CrossRef] [PubMed]
46. Hu, A.Q.; Zhao, Q.Q.; Chen, L.; Zhao, J.P.; Wang, Y.H.; Feng, K.L.; Wu, L.; Xie, M.; Zhou, X.M.; Xiao, L.T.; et al. Identification of Conserved and Divergent Strigolactone Receptors in Sugarcane Reveals a Key Residue Crucial for Plant Branching Control. Front. Plant Sci. 2021, 12, 747160. [Google Scholar] [CrossRef] [PubMed]
47. Chu, M.Y.; Wang, T.Y.; Li, W.T.; Liu, Y.S.; Bian, Z.Y.; Mao, J.; Chen, B.H. Genome-wide identification and analysis of the genes encoding Q-Type C2H2 zinc finger proteins in grapevine. Int. J. Mol. Sci. 2023, 24, 15180. [Google Scholar] [CrossRef] [PubMed]
48. Zhu, W.; Miao, Q.; Sun, D.; Yang, G.; Wu, C.; Huang, J.; Zheng, C. The mitochondrial phosphate transporters modulate plant responses to salt stress via affecting ATP and gibberellin metabolism in Arabidopsis thaliana. PLoS ONE 2012, 7, e43530. [Google Scholar] [CrossRef] [PubMed]
49. Nagy, R.; Karandashov, V.; Chague, V.; Kalinkevich, K.; Tamasloukht, M.; Xu, G.; Jakobsen, I.; Levy, A.A.; Amrhein, N.; Bucher, M. The characterization of novel mycorrhiza-specific phosphate transporters from Lycopersicon esculentum and Solanum tuberosum uncovers functional redundancy in symbiotic phosphate transport in solanaceous species. Plant J. 2005, 42, 236–250. [Google Scholar] [CrossRef]
50. Javot, H.; Pumplin, N.; Harrison, M.J. Phosphate in the arbuscular mycorrhizal symbiosis: Transport properties and regulatory roles. Plant Cell Environ. 2007, 30, 310–322. [Google Scholar] [CrossRef] [PubMed]
Yuan S, Zhang W, Zhang Y. Characterization of PHT Genes in ‘duli’ (Pyrus betulifolia Bunge) and Expression Analysis of PbPHTs in Response to Plant Growth Regulators, P, and Salt Stress. Agriculture. 2025; 15(2):199. https://doi.org/10.3390/agriculture15020199
Перевод статьи «Characterization ofPHTGenes in ‘duli’ (Pyrus betulifolia Bunge) and Expression Analysis ofPbPHTsin Response to Plant Growth Regulators, P, and Salt Stress» авторов Yuan S, Zhang W, Zhang Y., оригинал доступен по ссылке. Лицензия: CC BY. Изменения: переведено на русский язык














































































































Комментарии (0)