Фосфин и яйца вредителей: почему простая фумигация больше не работает и как это исправить
Фосфин является широко используемым фумигантным инсектицидом на складах, где хранятся продукты питания; однако его чрезмерное и неправильное применение способствовало возникновению устойчивости к нему у популяций насекомых. Несмотря на то, что устойчивость к фосфину признана во всем мире, лишь ограниченное число исследований посвящено его воздействию на разные стадии развития насекомых.
Аннотация
Данное исследование изучает эффективность фосфина в отношении яиц основных вредителей запасов, включая Oryzaephilus surinamensis (L.) (жесткокрылые: Silvanidae), Rhyzopertha dominica (F.) (жесткокрылые: Bostrichidae), Tribolium castaneum и T. confusum (жесткокрылые: Tenebrionidae), с акцентом на популяции с разным уровнем восприимчивости к фосфину. Процент вылупления яиц анализировали после воздействия фосфина в концентрациях от 50 до 1000 ppm в течение от 1 до 7 дней. Были построены прогностические модели для корреляции концентрации фосфина и времени воздействия, что способствует определению оптимальных стратегий борьбы с вредителями. Результаты выявили значительные различия в эффективности между видами и популяциями: яйца восприимчивых популяций полностью прекращали вылупление при концентрации 50 ppm, в то время как устойчивые популяции демонстрировали более высокую толерантность. Были определены значения летального времени (LT50 и LT99); LT99 при концентрации 50 ppm варьировало от 6,91 до 12,95 дней, что подчеркивает видоспецифичные различия и различия, связанные с возрастом яиц, в восприимчивости к фосфину. Значения летальной концентрации (LC50 и LC99) удалось оценить только для T. castaneum; LC99 для однодневных яиц после 2,5 дней воздействия составляла от 773,67 ppm до 923,03 ppm. Кроме того, на восприимчивость влиял возраст яиц: двухдневные яйца демонстрировали более высокую смертность по сравнению с однодневными. Это исследование подчеркивает критическую роль концентрации фосфина, продолжительности воздействия и стадии развития в управлении резистентностью, предоставляя ценную информацию для улучшения протоколов фумигации и повышения эффективности борьбы с вредителями на складах продовольствия.
1. Введение
После отказа от использования бромистого метила фосфин стал основным фумигантным инсектицидом, применяемым на складах, где хранятся продукты питания, благодаря своим отличительным преимуществам, включая простоту применения, эффективную проникающую способность, экономическую эффективность и адаптируемость к различным целевым ситуациям [1,2,3]. Широкое использование фосфина в последнее десятилетие в сочетании с неадекватными методами и условиями применения — такими как неоптимальная дозировка, отсутствие мониторинга или короткая продолжительность воздействия — стимулировало активацию генов, ответственных за развитие устойчивости у многих насекомых — вредителей запасов [3,4,5]. В настоящее время многочисленные исследования сообщают об устойчивости к фосфину во многих частях света, включая страны Южной и Северной Америки [6,7,8,9,10], Азии [11,12,13], Африки [14] и Океании [1,15,16,17]. Например, Zettler (1991) провел оценку восприимчивости природных популяций малого мучного хрущака, Tribolium confusum Jacquelin du Val, и рыжего мучного хрущака, Tribolium castaneum (Herbst) (жесткокрылые: Tenebrionidae), из различных мукомольных заводов по всей территории Соединенных Штатов. Насекомые подвергались воздействию различных доз фосфина для определения уровня их устойчивости. Среди 17 протестированных популяций T. confusum 18% проявили устойчивость к фосфину. Что касается T. castaneum, то среди 28 популяций устойчивость к фосфину проявили 46% [18]. В более позднем исследовании, посвященном частоте, распределению и интенсивности устойчивости к фосфину в популяциях малого зернового точильщика, Rhyzopertha dominica (F.) (жесткокрылые: Bostrychidae), в Бразилии, Lorini и Galley (2001) сообщили, что все отобранные популяции проявили устойчивость к фосфину, хотя и в разной степени [19]. Сообщалось также, что суринамский мукоед, Oryzaephilus surinamensis (L.) (жесткокрылые: Silvanidae), проявил измененные уровни восприимчивости в нескольких сериях тестов [20,21,22].
Большинство исследований направлены на оценку толерантности к фосфину в частности на стадии взрослого насекомого, часто упуская из виду изучение уровней восприимчивости на других стадиях развития. Следовательно, это ограничение приводит к неполному пониманию общей толерантности, проявляемой самим видом, с точки зрения различий, которые могут возникать на разных стадиях его жизненного цикла. Многочисленные научные публикации свидетельствуют, что яйцо является наиболее толерантной стадией развития для многих видов насекомых-вредителей запасов [3,21,23,24]. Например, Gourgouta и др. (2021) исследовали восприимчивость к фосфину различных стадий развития в популяции капрового жука, Trogoderma granarium Everts (жесткокрылые: Demestidae). В этом исследовании авторы сообщили, что 3-дневное воздействие 50 ppm привело к смертности имаго, куколок, недиапаузирующих и диапаузирующих личинок этого вида, но для яиц LC99 составила 874.3 ppm, что указывает на их пониженную восприимчивость к фосфину [23]. Athanassiou и др. (2020) представили сходные результаты, выявив различия в восприимчивости к фосфину среди разных стадий развития пестрого кожееда, Trogoderma inclusum LeConte, и ветчинного кожееда, Dermestes maculatus DeGeer (жесткокрылые: Dermestidae); яйца оказались наиболее толерантной стадией для обоих видов [25].
Сообщалось также, что яйца являются наиболее толерантной стадией к нескольким инсектицидам и фумигантам [3,26,27]. Например, при изучении сеноедов запасов (Psocoptera: Liposcelididae), подвергшихся воздействию таких фумигантов, как бромистый метил и фтористый сульфурил, было очевидно, что яйца проявляли самый высокий уровень толерантности среди различных стадий развития [28]. Кроме того, Bell и Savvidou (1999) отметили необходимость использования повышенных концентраций для эффективной борьбы с яйцами мельничной огневки, Ephestia kuehniella Zeller (чешуекрылые: Pyralidae), подчеркнув, что более молодые яйца (1–2 дня) проявляли большую толерантность по сравнению с более старыми (3–4 дня) [29]. В этом контексте Lampiri и Athanassiou (2021) отметили, что возраст яиц был ключевым фактором, влияющим на эффективность фосфина против T. granarium [30]. Hartzer и др. (2010) подчеркнули, что бромистый метил превзошел фтористый сульфурил по своей эффективности против яиц T. castaneum [31].
Наше исследование не только предоставляет важную информацию о толерантности яиц устойчивых и восприимчивых популяций ключевых видов вредителей, но и разрабатывает прогностические модели, которые могут служить бесценными инструментами для управления резистентностью. Эти модели позволяют более точно оценить концентрации фосфина и время воздействия, необходимые для достижения эффективного контроля, способствуя тем самым принятию обоснованных решений в практике фумигации. Кроме того, графическое представление наших результатов повышает их доступность и практическую применимость, позволяя заинтересованным сторонам в индустрии хранения зерна визуализировать и более эффективно внедрять результаты. Учитывая важность фосфина для защиты продукции запасов и принимая во внимание толерантность яиц ко многим используемым в настоящее время инсектицидам и фумигантам, дальнейшие исследования эффективности фосфина на яйцах обычно встречающихся на складах насекомых являются важнейшими. В этом контексте целью настоящего исследования была оценка эффективности фосфина на яйцах различных популяций основных видов насекомых-вредителей запасов.
2. Материалы и методы
2.1. Насекомые
Тестовые насекомые, использованные в настоящем исследовании, выращивались в Лаборатории энтомологии и сельскохозяйственной зоологии (LEAZ) на кафедре сельского хозяйства, защиты растений и сельской среды Университета Фессалии. Они содержались в постоянных условиях при температуре 25 °C и относительной влажности 65% с круглосуточной темнотой. Популяции Tribolium castaneum и T. confusum разводились на пшеничной муке, в то время как популяции R. dominica и O. surinamensis выращивались на целом зерне пшеницы и овсяных хлопьях (Quaker Oats Co., Чикаго, Иллинойс, США) соответственно. Каждый вид был представлен популяцией, восприимчивой и устойчивой к фосфину, на основе тщательных оценок, проведенных в предыдущих исследованиях (см. ниже). Восприимчивые популяции, исходно полученные из Греции, содержались в LEAZ более двух десятилетий [32]. Что касается устойчивых популяций, мы использовали популяции различных видов насекомых, которые были всесторонне протестированы на устойчивость с помощью специализированных протоколов выявления резистентности и однозначно идентифицированы как резистентные. В частности, эти популяции включали T. castaneum TC931 [20,33], а также R. dominica GA6 [33], O. surinamensis Roca Defisan и T. confusum GA12 [32].
Чтобы получить однодневные яйца для каждого вида, мы начинали с приблизительно 100 имаго из лабораторных культур. Каждую группу помещали в отдельные 500-мл банки, содержащие мелко просеянную муку. Затем эти банки инкубировали при 26 °C и 65% относительной влажности в течение 24 ч. После этого периода инкубации мы удаляли имаго из банок и собирали однодневные яйца, используя сито 212 мкм (Woven Wire Sieve, Endecotts Ltd.). Для двухдневных яиц следовали аналогичному процессу. Однако после помещения имаго в банки с мукой и их инкубации в течение 24 ч, мы удаляли имаго, как и раньше. Затем яйца оставляли еще на 24 ч, прежде чем собрать их, используя то же сито 212 мкм.
2.2. Дизайн эксперимента
Яйца подвергали воздействию различных концентраций газообразного фосфина, включая 0 ppm в качестве контроля, а также 50, 200, 500 и 1000 ppm. Мы определили концентрации фосфина для восприимчивости и устойчивости с помощью экспериментального подхода. Первоначально все популяции насекомых подвергались воздействию самой низкой концентрации 50 ppm. Когда при данной концентрации наблюдалась полная смертность (0% вылупления яиц), мы не переходили к воздействию на яйца более высоких концентраций (Таблица 1). Были оценены различные периоды воздействия: 2.5, 5 и 7 дней. По десять яиц каждого вида и популяции аккуратно помещали в стеклянные флаконы диаметром 1.3 см и высотой 4 см вместе с небольшим количеством муки с помощью тонкой кисточки. Впоследствии эти флаконы осторожно переносили в отдельные отсеки внутри герметичных 1-литровых стеклянных банок, причем для каждой комбинации концентрации, интервала воздействия и возраста яиц был свой предназначенный флакон. Получение газа проводили по методу, предложенному Steuerwald и др. (2006), с оценкой концентраций с использованием газовой хроматографии [Shimadzu GC-2010 Plus (Shimadzu, Киото, Япония)] [34]. Для получения газообразного фосфина использовали 5-литровый пластиковый баллон, содержащий 2 таблетки и 50 мл воды в соответствии с протоколом Phosphine Tolerance Test компании Detia Freyberg GmbH (Detia Freyberg GmbH, Лауденбах, Германия). С помощью шприца в 1-литровые стеклянные банки, содержащие флаконы с яйцами, вводили соответствующий объем газа [24]. Эксперимент включал три повторности, каждая с тремя подповторностями, что в сумме дало 9 флаконов для каждой комбинации концентрации, интервала воздействия и возраста яиц. После воздействия показатели выживаемости в виде вылупления яиц регистрировались отдельно через 7 и 14 дней для каждой комбинации вида, концентрации, времени воздействия и возраста яиц.
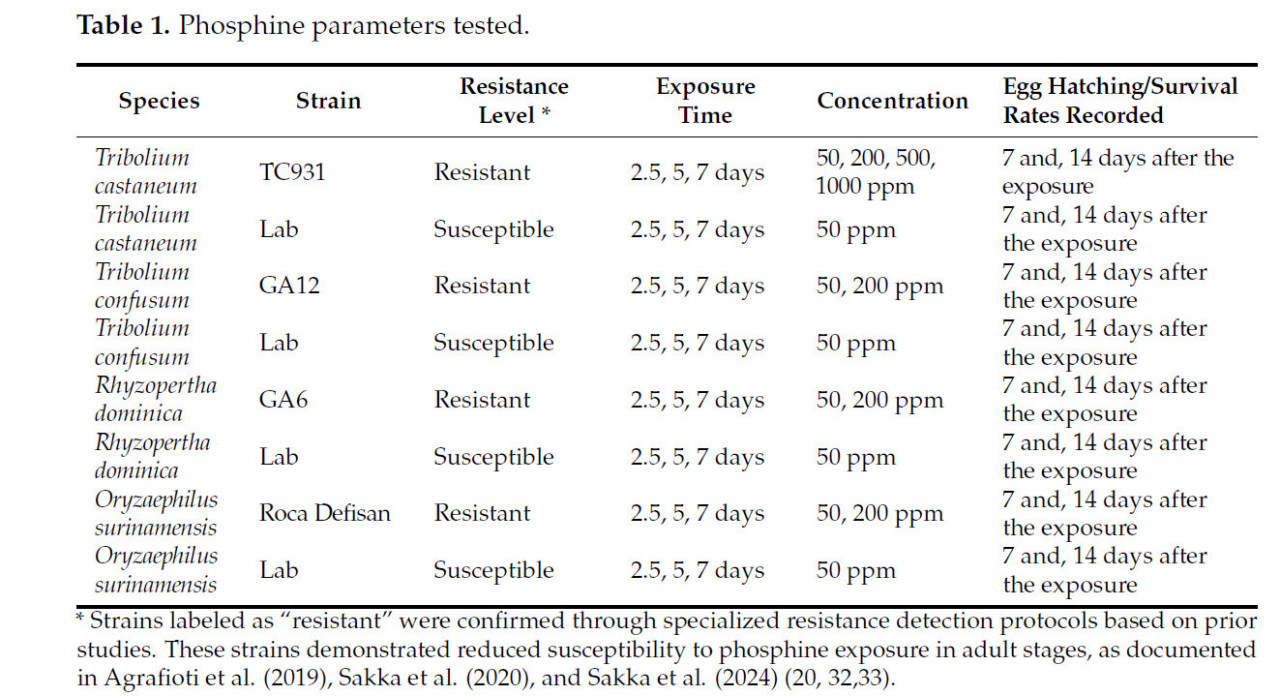
Таблица 1. Протестированные параметры фосфина.
2.3. Статистический анализ
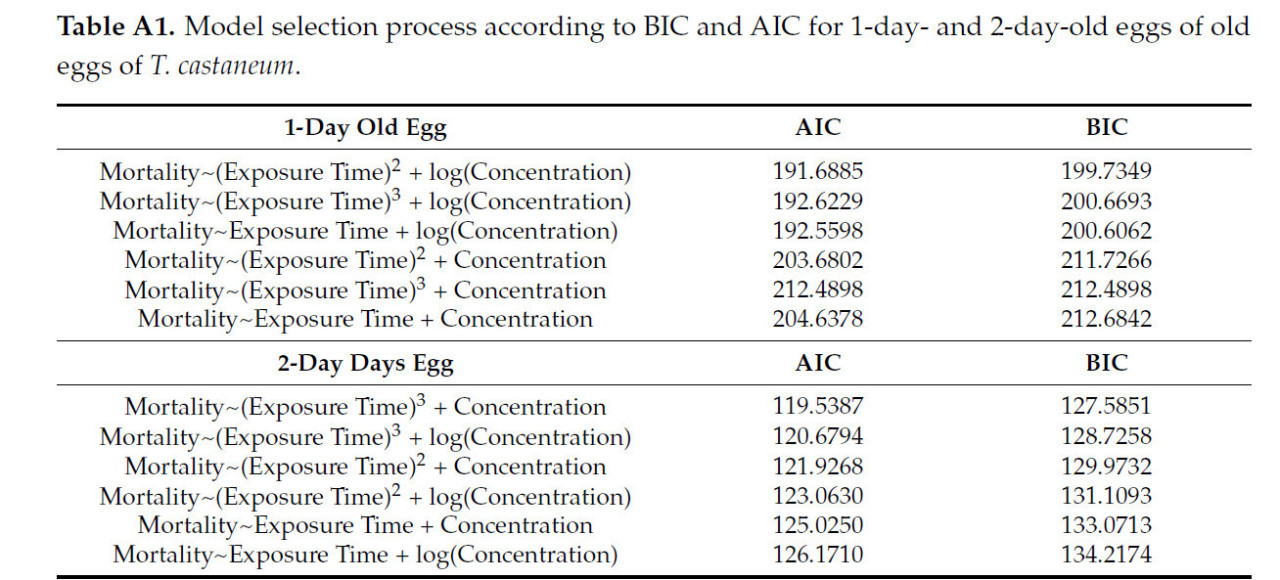
Обобщенные линейные смешанные модели использовались для оценки влияния концентрации и времени на смертность, учитывая эффект группировки по банкам как случайный фактор. Наиболее экономная модель использовалась, в свою очередь, для выводов. Смертность моделировалась как ответная переменная, а концентрация (ppm) и время воздействия (дни) — как предикторы. AIC (информационный критерий Акаике) и BIC (байесовский информационный критерий) использовались для выбора модели. Для T. castaneum соответствующие прогнозируемые вероятности показаны на Рисунках 1, 2, 3 и 4. Логарифмические и квадратичные члены были введены для лучшего учета кривизны функции отклика. AIC и BIC для всех исследованных моделей представлены в Таблице A1. Для остальных видов различия в AIC и BIC для различных формулировок моделей были незначительными, и поэтому к предикторам не применялись никакие преобразования. Концентрация не включалась в модель в качестве предиктора из-за ее незначимого эффекта.
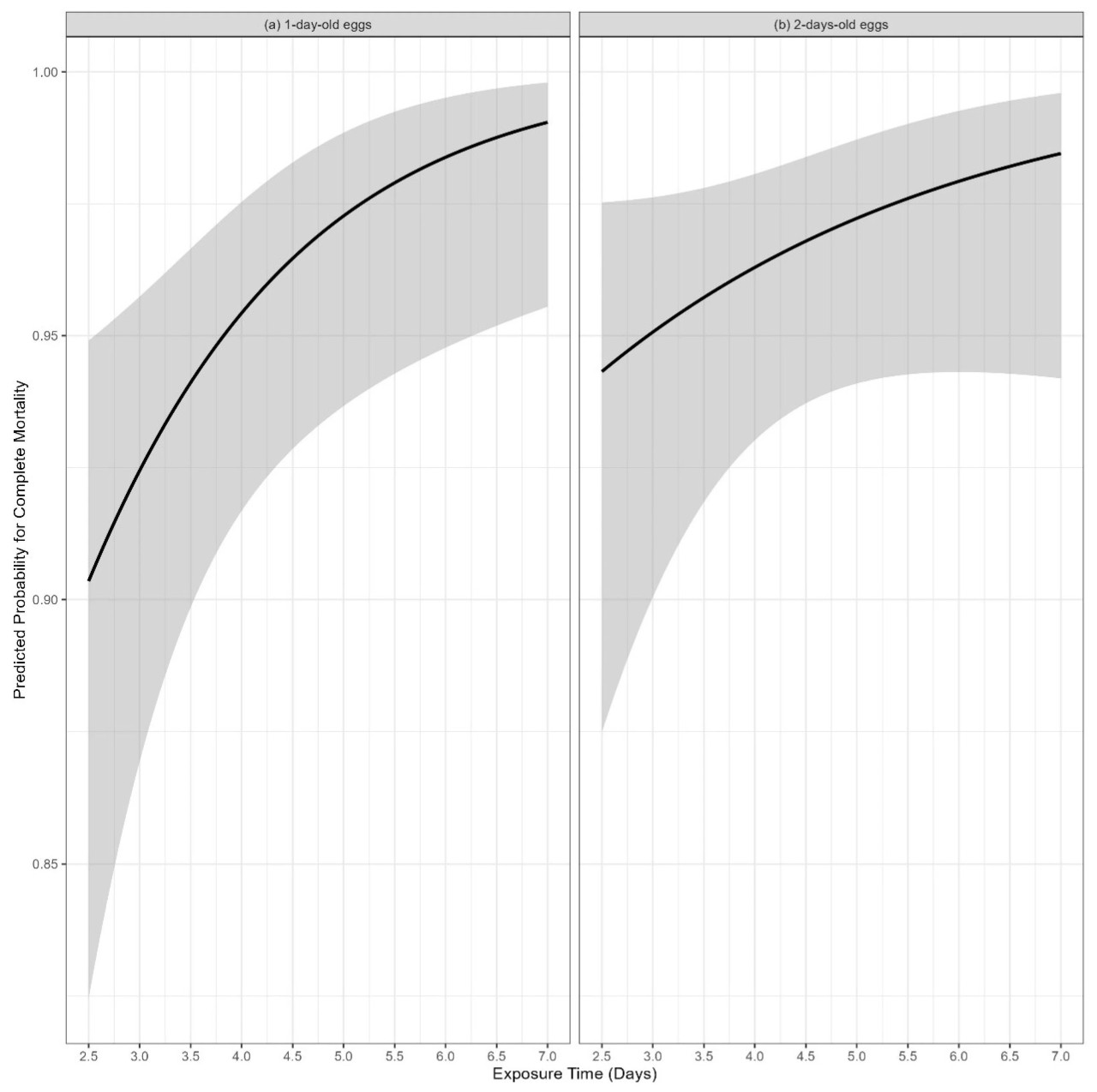
Рисунок 1. Кривые "время–отклик" для (a) однодневных и (b) двухдневных яиц разных видов, подвергнутых воздействию 50 ppm фосфина. Эти кривые отображают прогнозируемые вероятности полной гибели яиц в течение дней воздействия для каждого вида и возрастной группы.
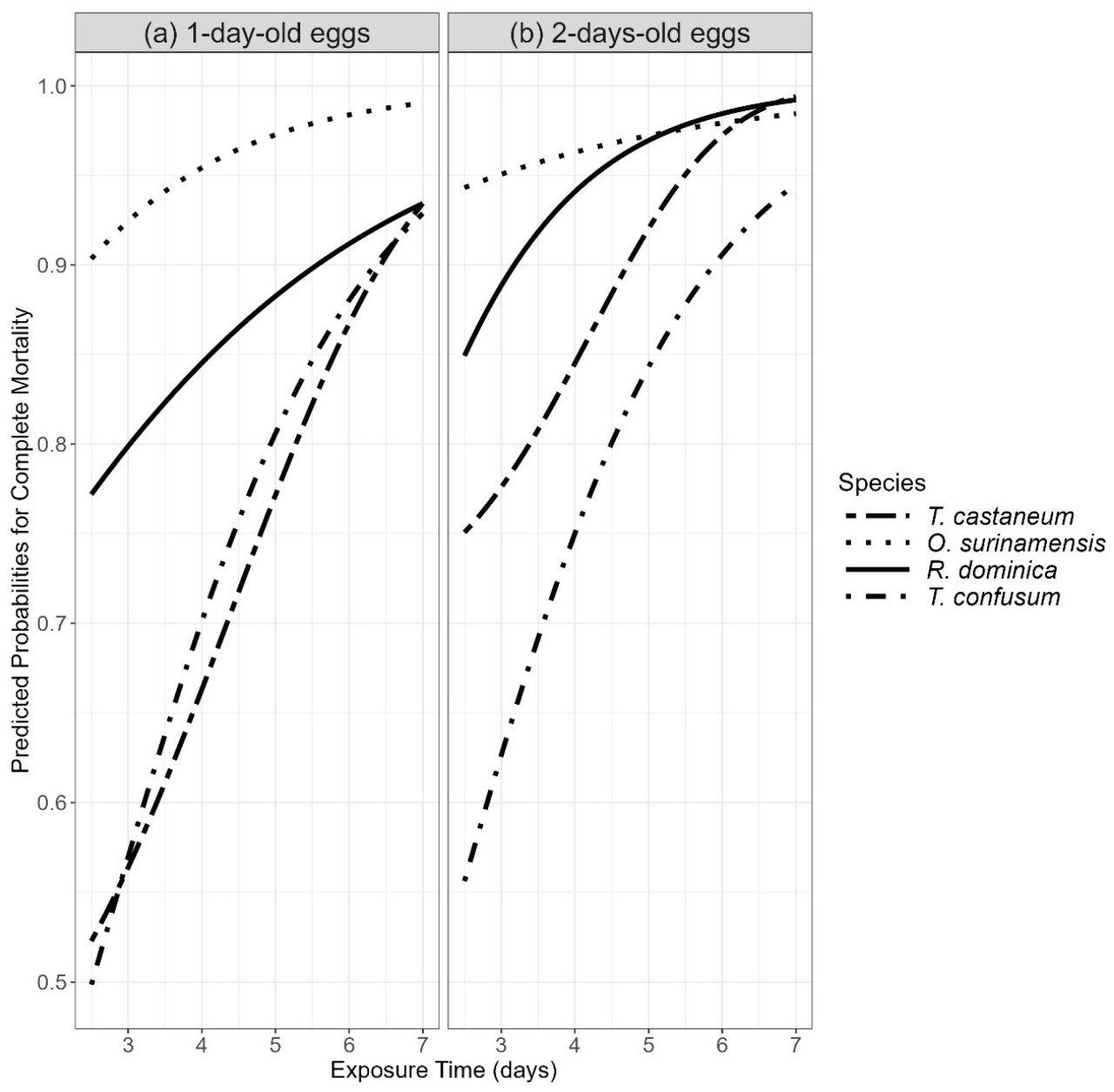
Рисунок 2. Анализ зависимости от концентрации и времени для (a) однодневных и (b) двухдневных яиц устойчивого Tribolium castaneum после 2.5, 4, 5, 6 и 7 дней воздействия. Ось x представляет концентрацию (ppm), в то время как ось y представляет вероятность смертности для разных дней пост-экспозиции.
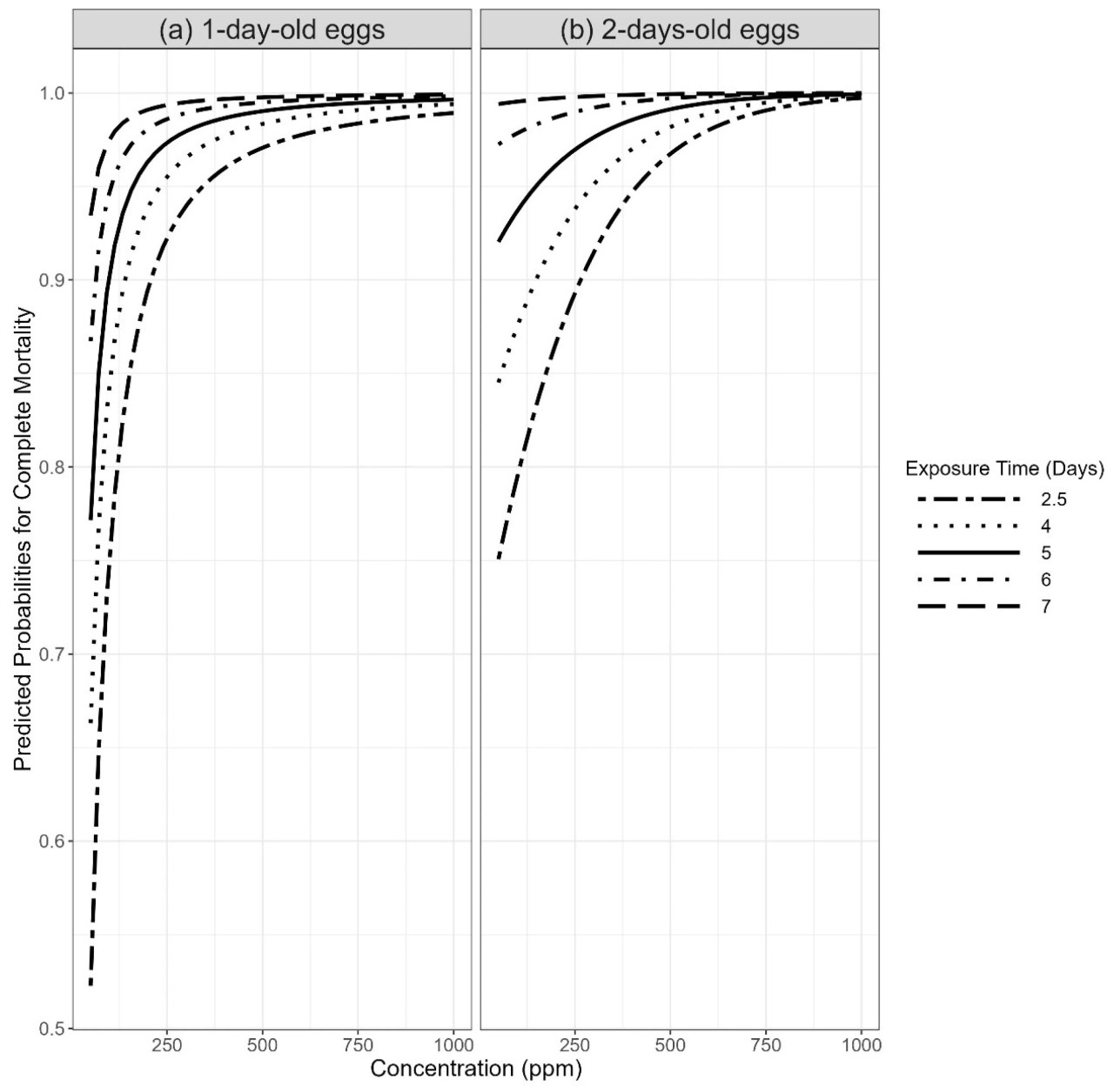
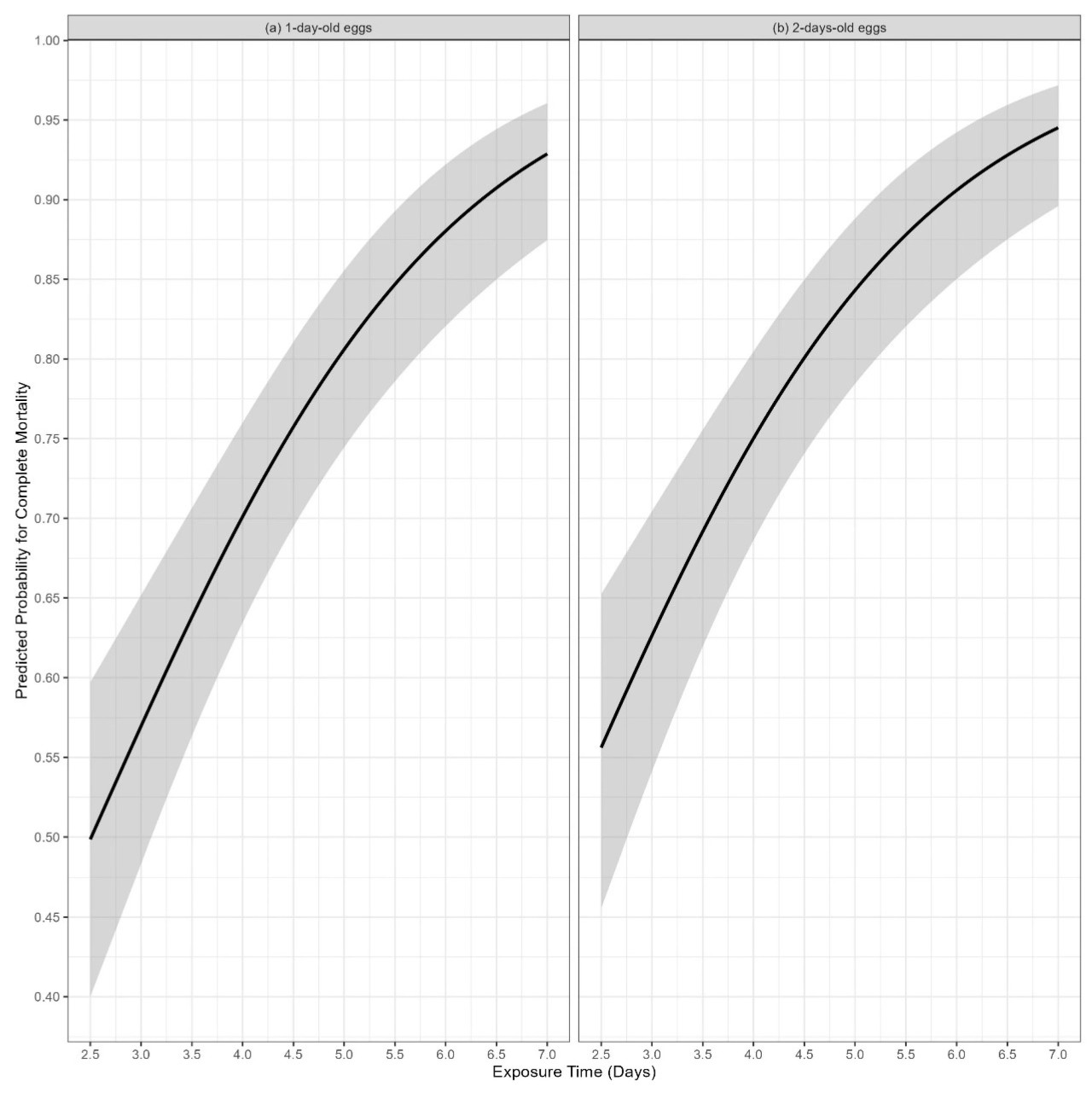
Рисунок 3. Прогнозируемые вероятности полной гибели в зависимости от концентрации и воздействия для (a) однодневных и (b) двухдневных яиц Tribolium castaneum.
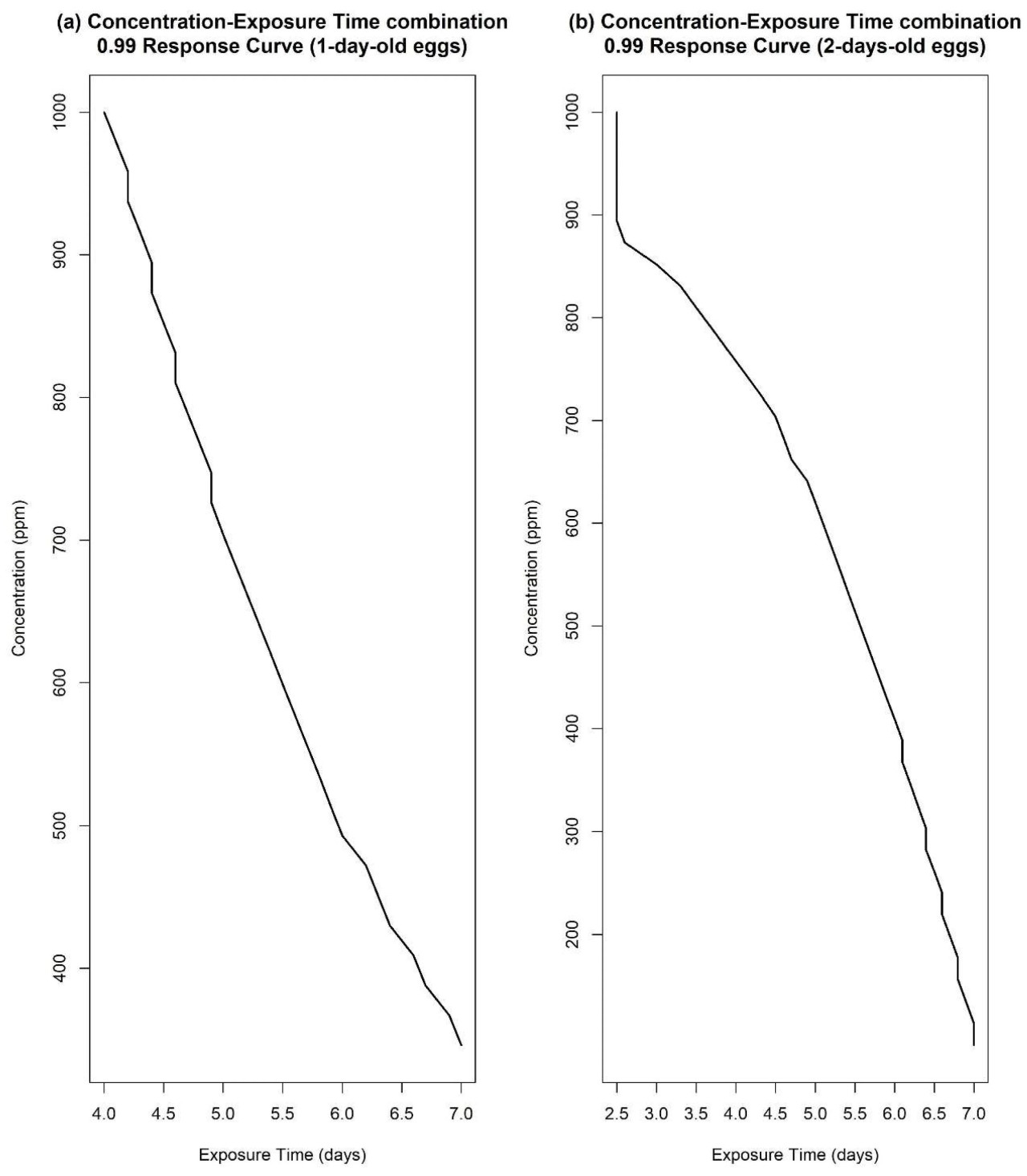
Рисунок 4. Комбинации концентрации и дней воздействия, которые привели к вероятности смертности 0.99 для (a) однодневных яиц и (b) двухдневных яиц Tribolium castaneum.
Для выполнения анализа и создания графиков использовалось программное обеспечение R (R4.3.2) и R Studio (2023.12.0+369).
3. Результаты
3.1. Эффективность фосфина в различных видов и популяций
Наши результаты показывают, что яйца восприимчивых популяций всех видов не вылуплялись при воздействии самой низкой концентрации 50 ppm. Мы наблюдали различающуюся восприимчивость среди яиц разных видов, возрастов и времени воздействия. Примечательно, что все яйца достигали 100% смертности после воздействия 200 ppm, за исключением однодневных и двухдневных яиц T. castaneum, которые проявляли выживаемость даже после воздействия 500 ppm в течение 2.5 дней. Однако полная смертность наблюдалась для всех случаев после воздействия 200 ppm в течение 5 дней.
3.2. Сравнение восприимчивости яиц в зависимости от возраста
Оценка летальной концентрации LC99 для однодневных яиц после воздействия фосфина в концентрациях 50, 200, 500 и 1000 ppm в течение 2.5 дней пост-экспозиционного периода составила 773.67 (95% доверительный интервал (ДИ) = [535, 1012]). Оценка летальной концентрации LC99 для двухдневных яиц после воздействия фосфина в концентрациях 50, 200, 500 и 1000 ppm в течение 2.5 дней пост-экспозиционного периода составила 923.03 (95% ДИ = [548, 1315]) (Таблица 2). Оценка для LC50 недоступна, поскольку экстраполяция подобранных значений не была признана целесообразной, учитывая масштаб доступных измерений. Аналогично, результаты для LC50 и LC99 для 5 и 7 дней пост-экспозиции тривиальны.
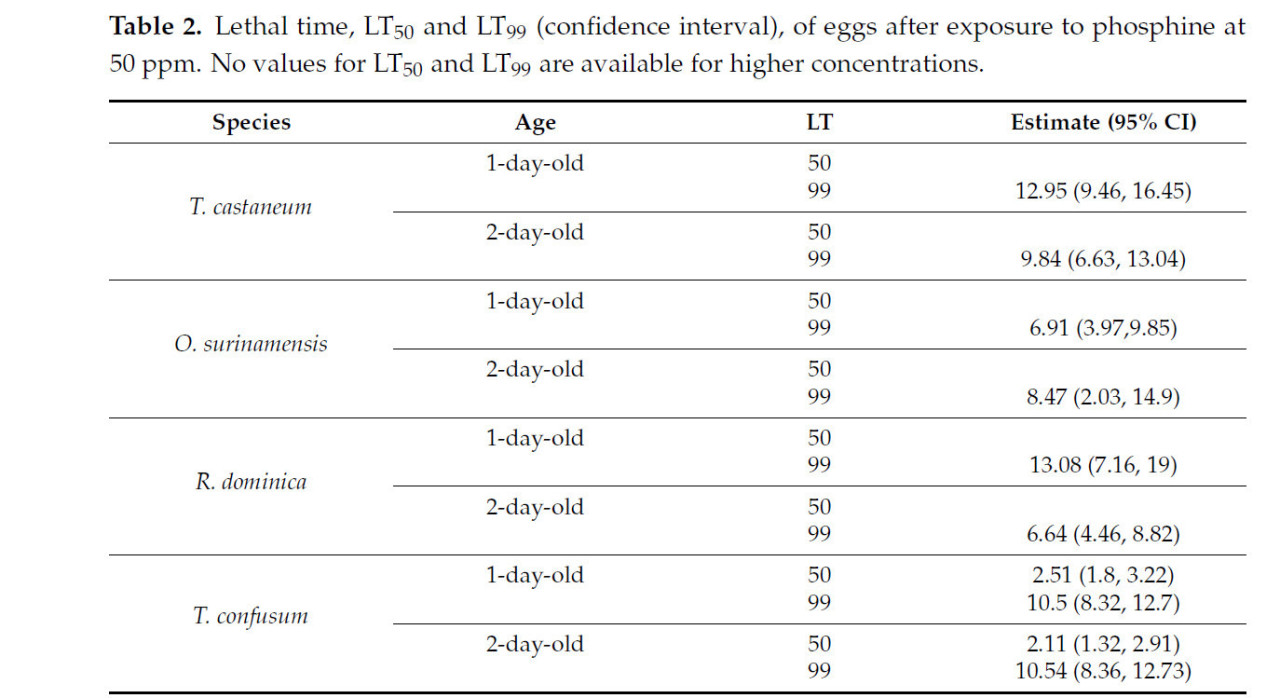
Таблица 2. Летальное время, LT50 и LT99 (доверительный интервал), яиц после воздействия фосфина в концентрации 50 ppm. Значения LT50 и LT99 для более высоких концентраций отсутствуют.
3.3. Значения летальной концентрации (LC) и летального времени (LT)
Значения летального времени (LT50 и LT99) для всех видов представлены в Таблице 2. Эти оценки были получены для яиц, подвергшихся воздействию 50 ppm фосфина. Значения летального времени (LT50 и LT99) были определены исключительно для яиц, подвергшихся воздействию 50 ppm фосфина. При более высоких концентрациях (200, 500 и 1000 ppm) не представлялось возможным рассчитать эти значения, поскольку полная смертность у большинства видов наблюдалась в течение 2.5 дней воздействия. В результате LT50 и LT99 для этих более высоких концентраций не оценивались.
3.4. Прогностическое моделирование тенденций смертности
На Рисунке 1 представлены кривые "время–отклик" для двух разных возрастов яиц различных видов, подвергнутых воздействию 50 ppm фосфина. Эти кривые отображают прогнозируемые вероятности гибели яиц в течение доступных дней воздействия для каждого вида и возрастной группы.
Рисунок 2 иллюстрирует кривые зависимости от концентрации для однодневных (Рисунок 2a) и двухдневных яиц (Рисунок 2b) устойчивого T. castaneum после 2.5, 4, 5, 6 и 7 дней воздействия. Ось x представляет концентрацию (ppm), в то время как ось y представляет вероятность смертности для разных дней пост-экспозиции, и каждая кривая представляет различные дни пост-экспозиции. Наши результаты показывают, что двухдневные яйца проявляли большую восприимчивость по сравнению с их однодневными аналогами, о чем свидетельствуют более высокие вероятности полной смертности при соответствующих временах воздействия.
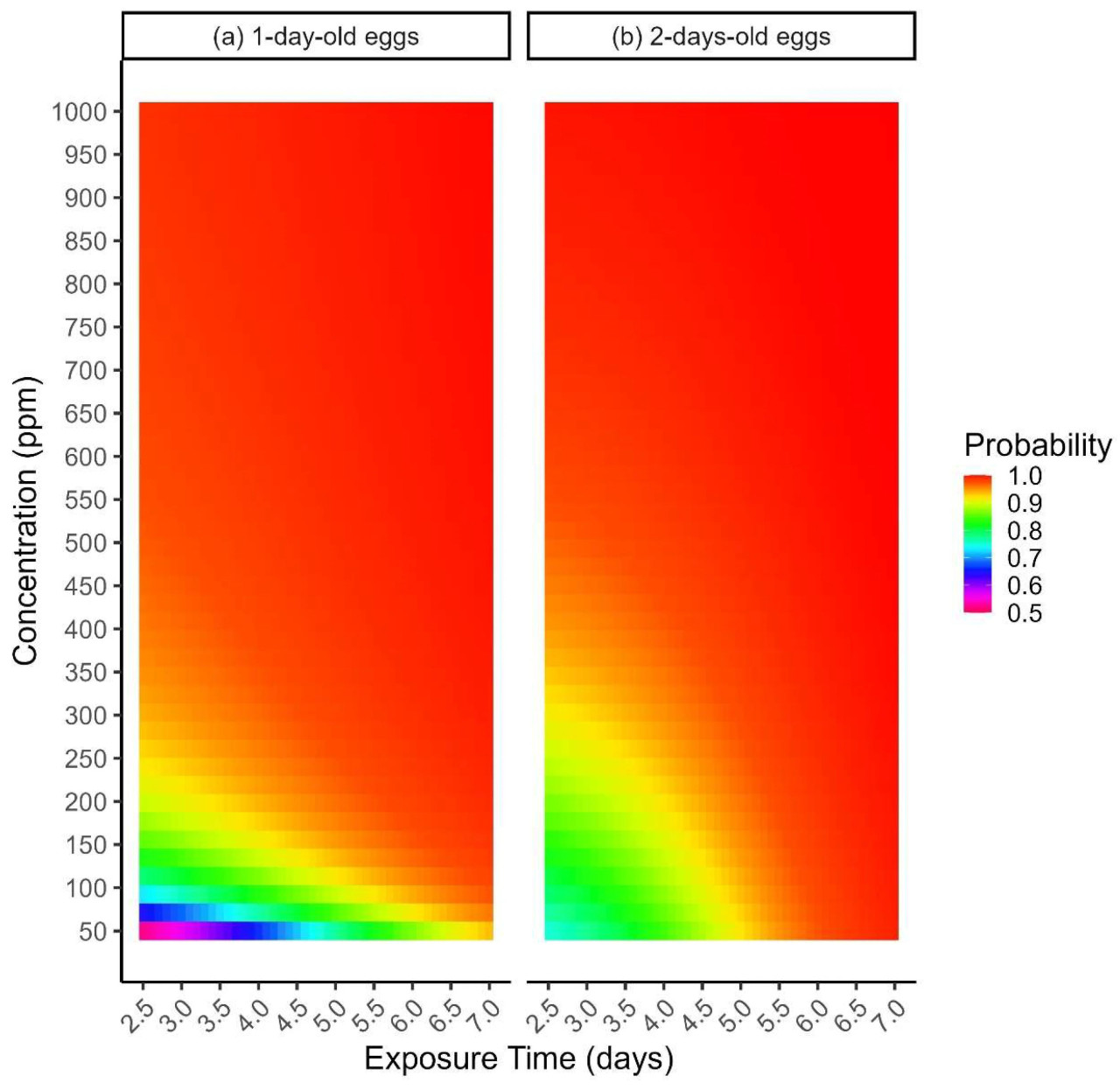
Рисунки 2 и 3 интерпретируются взаимодополняющим образом. В частности, существует взаимосвязь между факторами, определяющими оси x и y, и градиентом времени воздействия в качестве содержания для Рисунка 2 и цветовым контуром прогнозируемых вероятностей для Рисунка 3. На Рисунке 3 мы наблюдаем, что для двухдневных яиц T. castaneum значение вероятности смертности стабильно превышало 0.75 во всех концентрациях воздействия. И наоборот, для однодневных яиц вероятность полной смертности начиналась с 0.5 для самой низкой комбинации концентрации фосфина и времени воздействия. Это расхождение подчеркивает различную восприимчивость между двумя возрастными группами, причем двухдневные яйца проявляют более высокую и быструю смертность по сравнению с однодневными яйцами при воздействии фосфина. Аналогичная тенденция наблюдается и для других видов, где вероятность полной смертности для двухдневных яиц была стабильно выше по сравнению с однодневными яйцами, особенно с шестого дня воздействия и далее (Рисунки 5, 6 и 7). На Рисунке 4 показаны комбинации концентрации и дней, которые привели к вероятности смертности 0.99 для однодневных (Рисунок 4a) и двухдневных яиц (Рисунок 4b).
Рисунок 5. Кривая "доза–отклик" ± 95% доверительные интервалы (серая затененная область) для (a) однодневных и (b) двухдневных яиц устойчивого Oryzaephilus surinamensis после 2.5–7 дней воздействия.
Рисунок 6. Кривая "доза–отклик" ± 95% доверительные интервалы (серая затененная область) для (a) однодневных и (b) двухдневных яиц устойчивого Rhyzopertha dominica после 2.5–7 дней воздействия.
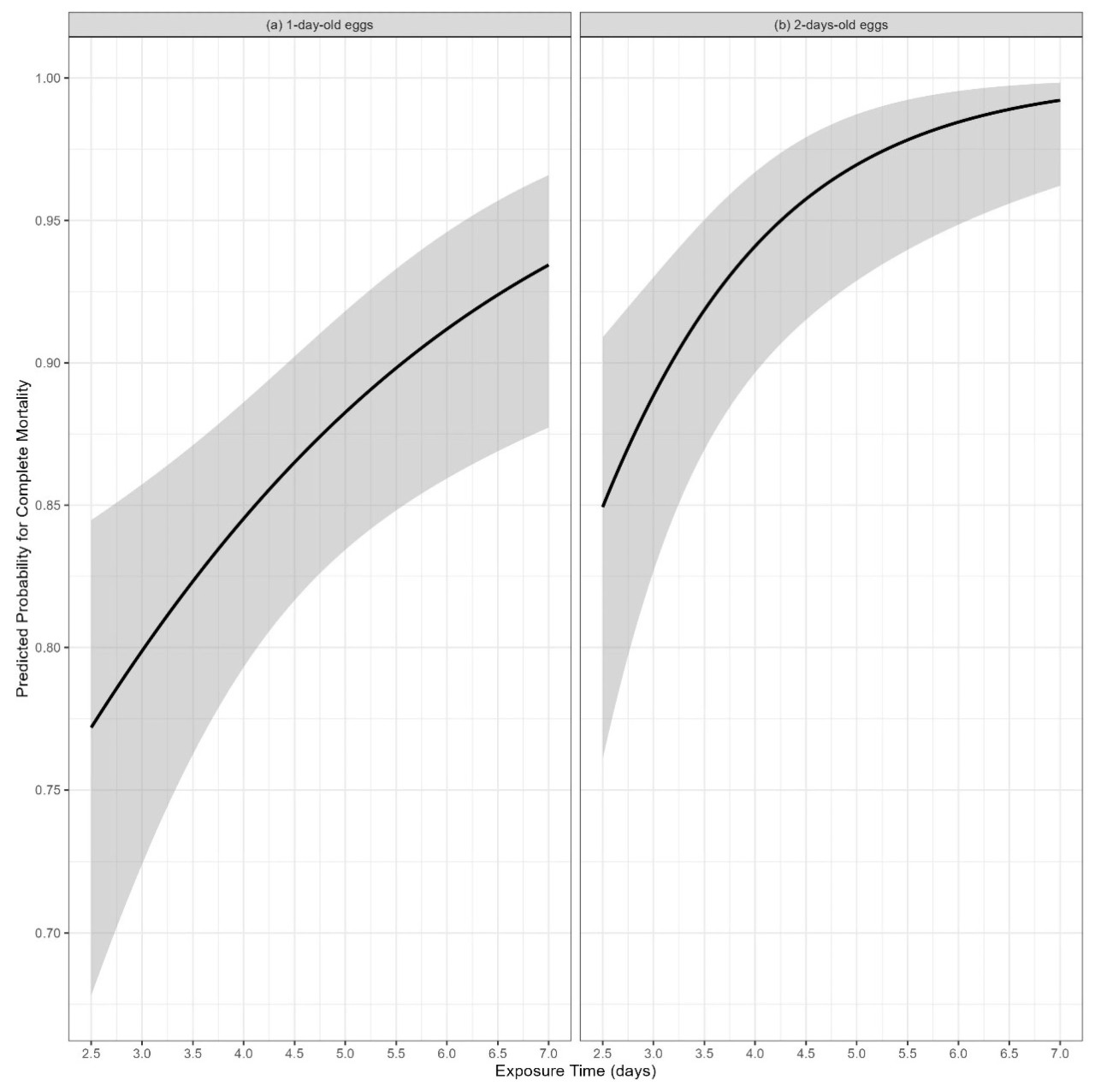
Рисунок 7. Кривая "время–отклик" ± 95% доверительные интервалы (серая затененная область) для (a) однодневных и (b) двухдневных яиц устойчивого Tribolium confusum после 2.5–7 дней воздействия.
4. Обсуждение
Результаты нашего исследования проливают свет на различную восприимчивость яиц разных видов к воздействию фосфина, подчеркивая важность учета вида, возраста и продолжительности воздействия в стратегиях борьбы с вредителями. Как и ожидалось, наше исследование выявило, что яйца устойчивых популяций проявляли более высокую толерантность к фосфину по сравнению с восприимчивыми популяциями. При самой низкой тестируемой концентрации (50 ppm) яйца восприимчивых популяций всех видов не вылуплялись, что указывает на значительную эффективность фосфина при этой концентрации. Однако полная смертность наблюдалась для всех случаев после воздействия 200 ppm в течение 5 дней, что указывает на эффективность более высоких концентраций и более длительных периодов воздействия для достижения контроля. Представленная здесь информация указывает на то, что неадекватная практика фумигации, приводящая к низким концентрациям и коротким воздействиям на виды, хранящиеся в запасах, может повысить выживаемость яиц. Это вызывает особую озабоченность, поскольку выжившие после обработки яйца не только приводят к новым заражениям фумигированного продукта, но и могут способствовать развитию резистентности [4,5]. Это открытие имеет значительные последствия для стратегий борьбы с вредителями, так как свидетельствует, что более высокие концентрации фосфина могут быть необходимы для достижения эффективного контроля в случаях резистентных популяций [3]. Это особенно актуально для объектов и сооружений, где поддержание повышенных концентраций в течение длительного времени может быть затруднено.
Текущее исследование вносит важный вклад в понимание устойчивости насекомых к фосфину, демонстрируя ее проявление на разных стадиях жизненного цикла. В то время как предыдущие исследования изучали различную восприимчивость разных стадий развития одного целевого вида к фосфину [23,25], наше исследование уникально тем, что фокусируется на изучении популяций, которые были предварительно идентифицированы как восприимчивые, так и устойчивые к фосфину [20, 32, 33]. Изучая эти популяции, мы предоставляем новые данные о динамике устойчивости к фосфину в различных стадиях развития вредителей запасов. Наше исследование согласуется с предыдущими выводами Sakka и др. (2024) и Agrafioti и др. (2019), подтверждая вывод о том, что устойчивые популяции насекомых, таких как T. castaneum и R. dominica, проявляют большую толерантность к воздействию фосфина по сравнению с восприимчивыми популяциями [32,33]. Кроме того, мы наблюдали, что яйца устойчивых популяций T. castaneum были наиболее толерантными, что согласуется с тенденциями, наблюдаемыми у имаго. Agrafioti и др. (2019) аналогичным образом сообщили о паттернах устойчивости у O. surinamensis и T. confusum, которые также были протестированы в нашем исследовании [32]. Однако прямое сравнение наших результатов с этими предыдущими исследованиями затруднено из-за различий в экспериментальных протоколах. Хотя наши результаты вносят ценный вклад в понимание статуса устойчивости протестированных популяций, различия в методах подчеркивают необходимость стандартизированных подходов для лучшего понимания динамики резистентности в различных стадиях развития и видов.
Заметным наблюдением была контрастная восприимчивость между однодневными и двухдневными яйцами, где двухдневные яйца стабильно демонстрировали повышенные вероятности полной смертности в различных периодах воздействия. Эта закономерность сохранялась у нескольких видов, подчеркивая ключевую роль возраста яиц во влиянии на восприимчивость к воздействию фосфина. Наши результаты согласуются с предыдущими исследованиями, указывающими на то, что более старые яйца, как правило, более восприимчивы к воздействию фосфина по сравнению с более молодыми яйцами [26,27,30,35]. Например, Lampiri и Athanassiou (2021) обнаружили, что двухдневные яйца T. granarium более восприимчивы, чем однодневные, при воздействии фосфина [30]. Кроме того, Baltaci и др. (2009) сообщили, что яйца E. elutella в возрасте 3 и 4 дней проявляли более низкую восприимчивость по сравнению с яйцами в возрасте 1 и 2 дней при воздействии фтористого сульфурила. Наши данные выявили контраст в восприимчивости между двумя исследованными возрастными группами, особенно заметный при самой низкой концентрации фосфина 50 ppm [35]. Аналогичные результаты были отмечены в исследовании Bell и Wilson (1995), где авторы изучали различные возрастные группы яиц T. granarium. В том исследовании сообщалось, что только яйца в возрасте от 0 до 1 дня выживали после 72-часового воздействия 0.28 ± 0.01 г/м³ фосфина при 25 °C и 70% относительной влажности [27]. Как наблюдается в коммерческих фумигациях, достижение 100% смертности среди «видимых» подвижных стадий — таких как имаго и личинки — может не обязательно остановить производство потомства в обработанном субстрате [36,37].
Несколько исследований, изучавших яйца, подвергшиеся воздействию газообразного фосфина, были сосредоточены на вариациях задержки вылупления яиц [23,30,38]. Наши результаты не показали задержки вылупления яиц после воздействия фосфина, что частично согласуется с предыдущими исследованиями, но также выявляет различия в реакциях развития. Это сходство с некоторыми исследованиями предполагает, что воздействие фосфина не универсально вызывает задержки развития у яиц насекомых. Например, Howe (1973) не сообщил о значительных различиях в смертности яиц Sitophilus granarius (L.) (жесткокрылые: Curculionidae) после фумигации фосфином в течение 1–5 дней, независимо от периода воздействия, а Pike (1994) аналогично не обнаружил заметных различий в смертности яиц Liposcelis entomophila Badonnel (Psocoptera: Liposcelididae) при воздействии фосфина в течение 72 и 120 ч [39,40]. В противоположность этому, Gourgouta и др. (2021) сообщили о задержке развития личинок T. granarium, вылупившихся из яиц, подвергшихся воздействию фосфина, в то время как Nayak и др. (2003) наблюдали задержку вылупления яиц у L. bostrychophila при воздействии фосфина [23,38]. Эти расхождения могут быть следствием видоспецифичных различий в механизмах развития, используемых концентраций фосфина или вариаций в экспериментальных условиях. Например, стрессовые реакции, индуцированные фосфином или его концентрацией, могут различаться у разных видов, потенциально вызывая задержки в развитии в одних случаях, но не в других. Эти вариации подчеркивают важность понимания видоспецифичных реакций на фосфин при разработке протоколов фумигации.
Более ранние исследования подчеркивали значение времени воздействия по сравнению с концентрацией фосфина в определении эффективности против широкого круга вредителей запасов [26,39,41]. В нашем исследовании увеличение времени воздействия фосфина вызывало увеличение смертности яиц T. castaneum, при этом 2.5-дневное воздействие не смогло обеспечить 100% смертность даже при 500 ppm фосфина. Это согласуется с выводами Bell и Wilson (1995), которые использовали аналогичную продолжительность воздействия и подчеркнули, что 2-дневного воздействия фосфина было недостаточно для достижения полного уничтожения яиц при концентрациях ниже 1000 ppm, независимо от возраста яиц [27]. Наши результаты подчеркивают важность учета как времени воздействия, так и концентрации для достижения оптимальных результатов борьбы с вредителями. Другими словами, наши результаты свидетельствуют, что для достижения вероятности 1.0 гибели яиц всех протестированных видов, фосфин следует применять в течение как минимум 2.5 дней в концентрациях, превышающих 400 ppm, в то время как концентрации ниже 100 ppm требуют воздействия более 7 дней. Это также подчеркивает ключевую роль концентрации.
Многие исследования сообщают, что длительное время воздействия повышает эффективность. При наблюдениях за вылуплением яиц как восприимчивых, так и устойчивых к фосфину популяций T. castaneum [42]. Rajendran [43] не обнаружил значительной разницы в смертности восприимчивых популяций, подвергнутых воздействию фосфина в концентрациях 40 ppm и 50 ppm в течение 72–120 ч [43]. Аналогично, Hashem и Reichmuth (1990) продемонстрировали, что длительное воздействие было более эффективным, чем более высокие концентрации газа, для достижения полной смертности яиц R. dominica и большого зернового точильщика, Prostephanus truncatus (Horn) (жесткокрылые: Bostrichidae) [44]. Примечательно, что наше исследование предоставляет новые данные, моделируя взаимосвязь между концентрацией и временем для яиц, выявляя ранее неизвестную информацию. Для сравнения, Bell и др. (1984) предложили комбинацию времени воздействия фосфина и температуры для полного уничтожения T. granarium, указав 7 дней при 20 °C или 4 дня при 30 °C [27]. И наоборот, Lampiri и Athanassiou (2021) подчеркивают, что даже 2-дневное воздействие может не гарантировать 100% смертность яиц, что подчеркивает сложное взаимодействие между концентрацией, временем воздействия и температурой в эффективных стратегиях фумигации фосфином [30]. В свете наших результатов, 2.5-дневное воздействие может привести к некоторому уровню выживания подвергнутых воздействию насекомых, что может привести к сопутствующему восстановлению популяции в обработанном субстрате [30].
В заключение, наше исследование не только освещает различную восприимчивость яиц разных видов к воздействию фосфина, но и подчеркивает важность учета вида, возраста, концентрации и продолжительности воздействия при разработке эффективных стратегий борьбы с вредителями. Демонстрируя проявление устойчивости к фосфину в различных стадиях развития и предоставляя информацию о ключевой роли возраста яиц, наши результаты вносят значительный вклад в понимание динамики устойчивости насекомых. Более того, наше исследование подчеркивает сложное взаимодействие между концентрацией и временем воздействия для достижения оптимального контроля, что может привести к снижению затрат и меньшему воздействию на окружающую среду, предлагая ценные рекомендации для практиков в этой области. Оптимизируя эти факторы, мы направлены на то, чтобы предложить решения, которые минимизируют потребление ресурсов и вред для окружающей среды, одновременно обеспечивая эффективный контроль над вредителями. Мы полагаем, что эти результаты послужат основой и улучшат разработку более целенаправленных и эффективных методов фумигации для действенной борьбы с вредителями запасов.
Приложение А
Ссылки
1. Nayak, M.K.; Collins, P.J. Influence of concentration, temperature and humidity on the toxicity of phosphine to the strongly phosphine-resistant psocid Liposcelis bostrychophila Badonnel (Psocoptera: Liposcelididae). Pest Manag. Sci. 2008, 64, 971–976. [Google Scholar] [CrossRef]
2. Kaur, R.; Subbarayalu, M.; Jagadeesan, R.; Daglish, G.J.; Nayak, M.K.; Naik, H.R.; Ramasamy, S.; Subramanian, C.; Ebert, P.R.; Schlipalius, D.I. Phosphine resistance in India is characterised by a dihydrolipoamide dehydrogenase variant that is otherwise unobserved in eukaryotes. Heredity 2015, 115, 188–194. [Google Scholar] [CrossRef] [PubMed]
3. Nayak, M.K.; Daglish, G.J.; Phillips, T.W.; Ebert, P.R. Resistance to the fumigant phosphine and its management in insect pests of stored products: A global perspective. Annu. Rev. Entomol. 2020, 65, 333–350. [Google Scholar] [CrossRef] [PubMed]
4. Emery, R.N.; Nayak, M.K.; Holloway, J.C. Preventing stored-product insect infestations in packaged-food products. Stewart Postharvest Rev. 2011, 7, 1–5. [Google Scholar] [CrossRef]
5. Gautam, S.G.; Opit, G.P.; Konemann, C.; Shakya, K.; Hosoda, E. Phosphine resistance in saw-toothed grain beetle, Oryzaephilus surinamensis in the United States. J. Stored Prod. Res. 2020, 89, 101690. [Google Scholar] [CrossRef]
6. Pimentel, M.A.G.; Faroni, L.R.D.; Guedes, R.N.C.; Sousa, A.H.; Tótola, M.R. Phosphine resistance in Brazilian populations of Sitophilus zeamais Motschulsky (Coleoptera: Curculionidae). J. Stored Prod. Res. 2009, 45, 71–74. [Google Scholar] [CrossRef]
7. Pimentel, M.A.G.; Faroni, L.R.D.; Tótola, M.R.; Guedes, R.N.C. Phosphine resistance, respiration rate and fitness consequences in stored-product insects. Pest Manag. Sci. 2007, 63, 876–881. [Google Scholar] [CrossRef] [PubMed]
8. Opit, G.P.; Phillips, T.W.; Aikins, M.J.; Hasan, M.M. Phosphine resistance in Tribolium castaneum and Rhyzopertha dominica from stored wheat in Oklahoma. J. Econ. Entomol. 2012, 105, 1107–1114. [Google Scholar] [CrossRef]
9. Sağlam, Ö.; Edde, P.A.; Phillips, T.W. Resistance of Lasioderma serricorne (Coleoptera: Anobiidae) to fumigation with phosphine. J. Econ. Entomol. 2015, 108, 2489–2495. [Google Scholar] [CrossRef]
10. Afful, E.; Elliott, B.; Nayak, M.K.; Phillips, T.W. Phosphine resistance in North American field populations of the lesser grain borer, Rhyzopertha dominica (Coleoptera: Bostrichidae). J. Econ. Entomol. 2018, 111, 463–469. [Google Scholar] [CrossRef]
11. Alam, M.S.; Shahid, S.S.; Mubarik, A.; Shamim, I.; Akhlaq, A. A survey of resistance to phosphine in some Coleopterous pests of stored wheat and rice grain in Pakistan. Pak. J. Biol. Sci. 1999, 2, 623–626. [Google Scholar] [CrossRef][Green Version]
12. Song, X.H.; Wang, P.P.; Zhang, H.Y. Phosphine resistance in Rhyzopertha dominica (Fabricius) (Coleoptera: Bostrichidae) from different geographical populations in China. Afr. J. Biotechnol. 2011, 10, 16367–16373. [Google Scholar] [CrossRef]
13. Ahmad, A.; Ahmed, M.; Noorullah; Ali, Q.M.; Abbas, M.; Arif, S. Monitoring of resistance against phosphine in stored grain insect pests in Sindh. Middle East J. Sci. Res. 2013, 16, 1501–1507. [Google Scholar] [CrossRef]
14. Benhalima, H.; Chaudhry, M.Q.; Mills, K.A.; Price, N.R. Phosphine resistance in stored-product insects collected from various grain storage facilities in Morocco. J. Stored Prod. Res. 2004, 40, 241–249. [Google Scholar] [CrossRef]
15. Collins, P.J.; Daglish, G.J.; Pavic, H.; Kopittke, R.A. Response of mixed-age cultures of phosphine-resistant and susceptible strains of lesser grain borer, Rhyzopertha dominica, to phosphine at a range of concentrations and exposure periods. J. Stored Prod. Res. 2005, 41, 373–385. [Google Scholar] [CrossRef]
16. Nayak, M.K.; Holloway, J.C.; Emery, R.N.; Pavic, H.; Bartlet, J.; Collins, P.J. Strong resistance to phosphine in the rusty grain beetle, Cryptolestes ferrugineus (Stephens) (Coleoptera: Laemophloeidae): Its characterisation, a rapid assay for diagnosis and its distribution in Australia. Pest Manag. Sci. 2013, 69, 48–53. [Google Scholar] [CrossRef]
17. Holloway, J.C.; Falk, M.G.; Emery, R.N.; Collins, P.J.; Nayak, M.K. Resistance to phosphine in Sitophilus oryzae in Australia: A national analysis of trends and frequencies over time and geographical spread. J. Stored Prod. Res. 2016, 69, 129–137. [Google Scholar] [CrossRef]
18. Zettler, L.J. Pesticide resistance in Tribolium castaneum and T. confusum (Coleoptera: Tenebrionidae) from flour mills in the United States. J. Econ. Entomol. 1991, 84, 763–767. [Google Scholar] [CrossRef]
19. Lorini, I.; Galley, D.J. The cross-resistance spectrum in deltamethrin resistance strains of Rhyzopertha dominica (F.) (Coleoptera: Bostrychidae). Neotrop. Entomol. 2001, 30, 321–325. [Google Scholar] [CrossRef]
20. Sakka, M.K.; Romano, D.; Stefanini, C.; Canale, A.; Benelli, G.; Athanassiou, C.G. Mobility parameters of Tribolium castaneum and Rhyzopertha dominica populations with different susceptibility to phosphine. J. Stored Prod. Res. 2020, 87, 101593. [Google Scholar] [CrossRef]
21. Gautam, S.G.; Opit, G.P.; Hosoda, E. Phosphine resistance in adult and immature life stages of Tribolium castaneum (Coleoptera: Tenebrionidae) and Plodia interpunctella (Lepidoptera: Pyralidae) populations in California. J. Econ. Entomol. 2016, 109, 2525–2533. [Google Scholar] [CrossRef]
22. Aulicky, R.; Stejskal, V.; Frydova, B.; Athanassiou, C. Evaluation of phosphine resistance in populations of Sitophilus oryzae, Oryzaephilus surinamensis and Rhyzopertha dominica in the Czech Republic. Insects 2022, 13, 1162. [Google Scholar] [CrossRef]
23. Gourgouta, M.; Agrafioti, P.; Athanassiou, C.G. Insecticidal effect of phosphine for the control of different life stages of the khapra beetle, Trogoderma granarium (Coleoptera: Dermestidae). Crop Prot. 2021, 140, 105409. [Google Scholar] [CrossRef]
24. Gourgouta, M.; Athanassiou, C.G. Efficacy of phosphine on different life stages of Alphitobius diaperinus and Tenebrio molitor (Coleoptera: Tenebrionidae). Sustainability 2023, 15, 2131. [Google Scholar] [CrossRef]
25. Athanassiou, C.G.; Phillips, T.W.; Arthur, F.H.; Aikins, M.J.; Agrafioti, P.; Hartzer, K.L. Efficacy of phosphine fumigation for different life stages of Trogoderma inclusum and Dermestes maculatus (Coleoptera: Dermestidae). J. Stored Prod. Res. 2020, 86, 101556. [Google Scholar] [CrossRef]
26. Bell, C.H.; Wilson, S.M.; Banks, H.J. Studies on the toxicity of phosphine to tolerant stages of Trogoderma granarium Everts (Coleoptera: Dermestidae). J. Stored Prod. Res. 1984, 20, 111–117. [Google Scholar] [CrossRef]
27. Bell, C.H.; Wilson, S.M. Phosphine tolerance and resistance in Trogoderma granarium Everts (Coleoptera: Dermestidae). J. Stored Prod. Res. 1995, 31, 199–205. [Google Scholar] [CrossRef]
28. Athanassiou, C.G.; Hasan, M.M.; Phillips, T.W.; Aikins, M.J.; Throne, J.E. Efficacy of methyl bromide for control of different life stages of stored-product Psocids. J. Econ. Entomol. 2015, 108, 1422–1428. [Google Scholar] [CrossRef] [PubMed]
29. Bell, C.H.; Savvidou, N. The toxicity of Vikane (sulfuryl fluoride) to age groups of eggs of the Mediterranean flour moth (Ephestia kuehniella). J. Stored Prod. Res. 1999, 35, 233–247. [Google Scholar] [CrossRef]
30. Lampiri, E.; Athanassiou, C.G. Insecticidal effect of phosphine on eggs of the Khapra beetle (Coleoptera: Dermestidae). J. Econ. Entomol. 2021, 114, 1389–1400. [Google Scholar] [CrossRef] [PubMed]
31. Hartzer, M.; Subramanyam, B.; Chayaprasert, W.; Maier, D.E.; Savoldelli, S.; Campbell, J.F.; Flinn, P.W. Methyl bromide and sulfuryl fluoride effectiveness against red flour beetle life stages. In Proceedings of the 10th International Working Conference on Stored Product Protection, Estoril, Portugal, 27 June–2 July 2010; Julius Kühn-Institut: Berlin, Germany, 2010; pp. 365–370. [Google Scholar]
32. Agrafioti, P.; Athanassiou, C.G.; Nayak, M.K. Detection of phosphine resistance in major stored-product insects in Greece and evaluation of a field resistance test kit. J. Stored Prod. Res. 2019, 82, 40–47. [Google Scholar] [CrossRef]
33. Sakka, M.K.; Mavridis, K.; Papapostolou, K.M.; Riga, M.; Vontas, J.; Athanassiou, C.G. Development, application and evaluation of three novel TaqMan qPCR assays for phosphine resistance monitoring in major stored product pests Tribolium castaneum and Rhyzopertha dominica. Pest Manag. Sci. 2024, 80, 275–281. [Google Scholar] [CrossRef] [PubMed]
34. Steuerwald, R.; Dierks Lange, H.; Schmitt, S. Rapid bioassay for determining the phosphine tolerance. Campinas. In Proceedings of the 9th International Working Conference on Stored-Product Protection, São Paulo, Brazil, 15–18 October 1994; Lorini, I., Bacaltchuk, B., Beckel, H., Deckers, D., Sundfeld, E., dos Santos, J.P., Biagi, J.D., Celaro, J.C., Faroni, L.R.D.'A., Bortolini, L.d.O.F., et al., Eds.; ABRAPOS: Passo Fundo, Brazil, 15–18 October 2006; pp. 306–311. [Google Scholar]
35. Baltaci, D.; Klementz, D.; Gerowitt, B.; Drinkall, M.J.; Reichmuth, C. Lethal effects of sulfuryl fluoride on eggs of different ages and other life stages of the warehouse moth Ephestia elutella (Hübner). J. Stored Prod. Res. 2009, 45, 19–23. [Google Scholar] [CrossRef]
36. Aulicky, R.; Stejskal, V.; Frydova, B.; Athanassiou, C.G. Susceptibility of two strains of the confused flour beetle (Coleoptera: Tenebrionidae) following phosphine structural mill fumigation: Effects of concentration, temperature, and flour deposits. J. Econ. Entomol. 2015, 108, 2823–2830. [Google Scholar] [CrossRef] [PubMed]
37. Agrafioti, P.; Kaloudis, E.; Bantas, S.; Sotiroudas, V.; Athanassiou, C.G. Modeling the distribution of phosphine and insect mortality in cylindrical grain silos with Computational Fluid Dynamics: Validation with field trials. Comput. Electron. Agric. 2020, 173, 105383. [Google Scholar] [CrossRef]
38. Nayak, M.K.; Collins, P.J.; Pavic, H.; Kopittke, R.A. Inhibition of egg development by phosphine in the cosmopolitan pest of stored products Liposcelis bostrychophila (Psocoptera: Liposcelididae). Pest Manag. Sci. 2003, 59, 1191–1196. [Google Scholar] [CrossRef] [PubMed]
39. Howe, R.W. The susceptibility of the immature and adult stages of Sitophilus granarius to phosphine. J. Stored Prod. Res. 1973, 8, 241–262. [Google Scholar] [CrossRef]
40. Pike, V. Laboratory assessment of the efficacy of phosphine and methyl bromide fumigation against all stages of Liposcelis entomophilus (Enderlein). Crop Prot. 1994, 13, 141–145. [Google Scholar] [CrossRef]
41. Shi, M.; Collins, P.J.; Ridsdill-Smith, J.; Renton, M. Individual-based modelling of the efficacy of fumigation tactics to control lesser grain borer (Rhyzopertha dominica) in stored grain. J. Stored Prod. Res. 2012, 51, 23–32. [Google Scholar] [CrossRef]
42. Rajendran, S. Selection for resistance to phosphine or methyl bromide in Tribolium castaneum (Coleoptera: Tenebrionidae). Bull. Entomol. Res. 1992, 82, 119–124. [Google Scholar] [CrossRef]
43. Rajendran, S. Inhibition of hatching of Tribolium castaneum by phosphine. J. Stored Prod. Res. 2000, 36, 101–106. [Google Scholar] [CrossRef]
44. Hashem, M.Y.; Reichmuth, C. The efficiency of phosphine against eggs of lesser grain borer Rhyzopertha dominica (Fab) and larger grain borer Prostephanus truncatus (Horn) (Coleoptera: Bostrichidae). Nachrichtenbl Deut Pflanzenschutzd 1989, 41, 159–163. [Google Scholar]
Gourgouta M, Sakka MK, Bataka EP, Götze MC, Nakas CT, Athanassiou CG. Modeling the Efficacy of Phosphine on Eggs of Major Stored-Product Insect Species: Investigating Strains with Varying Susceptibility Levels. Agriculture. 2025; 15(3):294. https://doi.org/10.3390/agriculture15030294
Перевод статьи «Modeling the Efficacy of Phosphine on Eggs of Major Stored-Product Insect Species: Investigating Strains with Varying Susceptibility Levels» авторов Gourgouta M, Sakka MK, Bataka EP, Götze MC, Nakas CT, Athanassiou CG., оригинал доступен по ссылке. Лицензия: CC BY. Изменения: переведено на русский язык
Фото: freepik









































































































Комментарии (0)