Ценные отходы: что скрывают кожура лука, томатов и зеленая оболочка фисташек
В данном исследовании представлен всесторонный анализ состава луковой шелухи, томатной кожуры и зеленой оболочки фисташек с акцентом на их структурные и биоактивные компоненты.
Аннотация
Было установлено, что луковая шелуха, независимо от сорта, богата кверцетином и его производными, наряду с другими флавоноидами и пектином. Томатная кожура оказалась заметным источником нарингенина (0.52 мг/г в этанольном экстракте) и рутина (0.24 мг/г в водном экстракте), а также продемонстрировала неожиданно высокое содержание лигнина, составляющее почти 50% ее структурных компонентов. Зеленая оболочка фисташек показала высокое содержание экстрактивных веществ (63.4 г/100 г), 73% из которых были водорастворимыми. Протокатеховая кислота, рутин и производные кверцетина были доминирующими фенольными соединениями в водном экстракте, тогда как лютеолин был наиболее распространен в этанольном экстракте. Что касается структурного состава, томатная кожура и зеленая оболочка фисташек имели сходство, демонстрируя высокое содержание лигнина (53.4% и 33.8% соответственно) и уроновых кислот (10–15%). Напротив, луковая шелуха характеризовалась высоким содержанием глюканов (около 38%) и галактуроновой кислоты (33%). Полученные данные открывают путь для разработки устойчивых и эффективных процессов экстракции, позволяющих осуществлять последовательное извлечение ценных биоактивных соединений и способствующих повышению ценности этих агропромышленных отходов. Дополнительно была оценена луковая и томатная кожура как источники пектина с использованием двух методов экстракции: традиционной экстракции подкисленной водой и экстракции субкритической водой. Результаты выявили значительные различия в составе пектина (53–68% галактуроновой кислоты) и степени этерификации (79–92%) по сравнению с коммерческим пектином (72.8% галактуроновой кислоты и 68% этерификации), что подчеркивает влияние исходного сырья и метода экстракции на конечные свойства пектина.
1. Введение
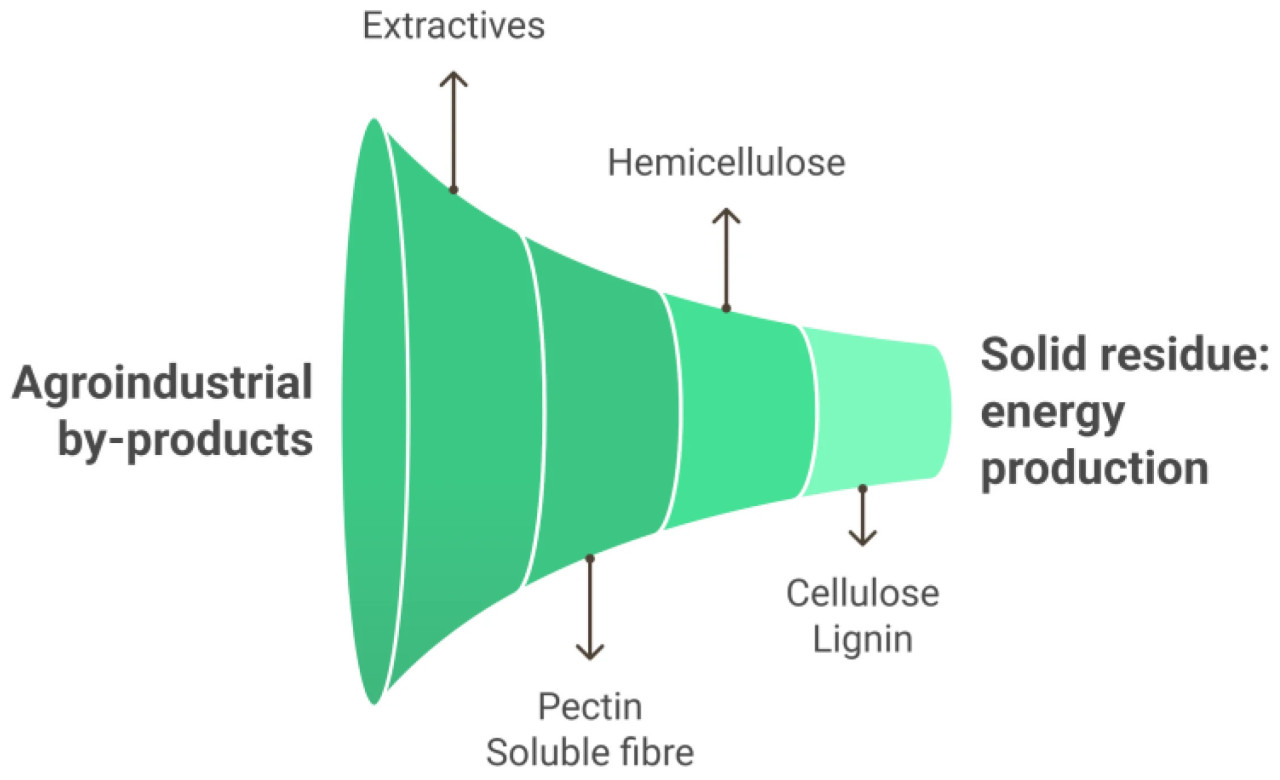
Агропродовольственная промышленность производит огромное количество побочных продуктов и отходов, многие из которых содержат ценные соединения с потенциальным применением в различных секторах, включая пищевую, фармацевтическую и косметическую промышленность. В рамках циркулярной экономики растет интерес к повторному использованию этих побочных продуктов для сокращения отходов и продвижения устойчивого использования ресурсов. Для повышения ценности агропромышленных отходов можно использовать два основных подхода [1]: использование всего потока (после предварительной обработки, если необходимо, сырье непосредственно используется для производства энергии) и использование, ориентированное на компоненты, при котором исходные агроотходы фракционируются иным способом для извлечения специфических соединений, от высокоценных до низкоценных компонентов (Рисунок 1). Комплексная характеристика агропромышленных отходов необходима для разработки этого биокаскадного процесса, так как она позволяет идентифицировать ключевые биоактивные соединения и структурные компоненты, которые могут быть извлечены. Кроме того, при выборе сырья следует отдавать предпочтение местным побочным продуктам, которые могут перерабатываться на централизованных биоперерабатывающих заводах. Эти предприятия могут преобразовывать отходы в ценные продукты и способствовать развитию сельских районов и регионов, где эти отходы образуются. Такой подход снижает зависимость от внешних ресурсов и товаров в глобальной цепочке создания стоимости [2].
Рисунок 1. Биокаскадный подход для полного повышения ценности агропромышленных отходов.
Среди многочисленных побочных продуктов агропродовольственного сектора луковая шелуха и томатные выжимки выделяются благодаря большим объемам производства и высоким концентрациям биоактивных соединений. Лук (Allium cepa) широко культивируется по всему миру, при этом луковая шелуха, состоящая из сухих наружных слоев, представляет собой значительный побочный продукт. Эта шелуха образуется не только на перерабатывающих предприятиях, но также в сельскохозяйственных полях и при потреблении в домохозяйствах. Только в Европейском Союзе ежегодно производится приблизительно 0.6 млн тонн отходов луковой шелухи (ОЛШ) [3] из общего объема производства лука в 6.26 млн тонн [4]. На долю Испании приходится почти 20% производства лука в ЕС, уступая только Нидерландам, которые производят 24%. ОЛШ является богатым источником ценных биоактивных соединений, включая флавоноиды, фенольные кислоты и пектины, которые могут составлять до 30% от сухого веса, как отмечено Бенито-Романом и др. [5]. Эти соединения имеют значительный потенциал для применения в пищевой, фармацевтической и косметической промышленности. Однако большая часть луковой шелухи выбрасывается как отходы, поскольку она непригодна для кормления животных из-за присутствия соединений серы, что приводит к экологическим проблемам и потере ценных ресурсов. В последние годы появился растущий интерес к повышению ценности ОЛШ для улучшения устойчивости и эффективности использования ресурсов. Эта тенденция обусловлена растущим спросом на пектиновые соединения (ПС) в качестве функциональных добавок в фармацевтическом и пищевом секторах. Удовлетворение этого спроса требует изучения новых источников ПС и разработки экологически чистых методов экстракции. Томат (Solanum lycopersicum) является еще одним широко потребляемым овощем, как в свежем виде, так и переработанным в такие продукты, как паста, сок, соус и кетчуп [6]. Переработка этих продуктов генерирует побочный продукт, известный как томатные выжимки, состоящий в основном из кожицы и семян [7,8]. Ежегодное производство томатных выжимок составляет от 5% до 13% от исходного веса томатов, что составляет 0.6–2 млн тонн органических отходов. В 2022 году на Италию приходилось 40% урожая томатов в ЕС, за ней следовали Испания (24%) и Португалия (9%), что в сумме составило 15 млн тонн производства в ЕС, согласно данным FAOSTAT. Томаты богаты ликопином, фенольными соединениями, органическими кислотами и витаминами, что делает томатные выжимки ценным ресурсом [8]. Однако неправильная утилизация этого побочного продукта создает экологические проблемы из-за высокого содержания воды и обилия питательных веществ, что приводит к порче. Эффективное использование томатных выжимок на биоперерабатывающих заводах может преобразовать отходы в ценные продукты, такие как ликопин, пищевые волокна и томатное масло. Этот подход сокращает отходы и повышает эффективность использования ресурсов в томатной промышленности, предлагая более устойчивую альтернативу его нынешнему недоиспользованию в кормлении животных.
В дополнение к луковой шелухе и томатным выжимкам, в это исследование была включена зеленая оболочка фисташек (ЗОФ) в связи с недавним значительным ростом культивирования фисташек и связанными с этим экологическими проблемами. Производство фисташек (Pistacia vera) достигло приблизительно 1.027 млн тонн в мире в 2022 году (FAOSTAT). Побочные продукты переработки фисташек включают зеленую оболочку фисташек (ЗОФ), листья, грозди, остатки ядер и твердые древесные скорлупы [9]. Среди них ЗОФ представляет собой наибольшую часть отходов фисташковой промышленности, составляя 34–45% от общего объема [10]. Несмотря на большой объем, ЗОФ обычно выбрасывается как отходы [11], создавая значительные экологические риски из-за ее накопления в сельскохозяйственных и пищевых производственных условиях. Хотя ЗОФ иногда используется в качестве корма для животных, высокое содержание в ней фенольных соединений и танинов может привести к желудочно-кишечным проблемам, препятствуя усвоению углеводов, белков и минералов [12,13]. Кроме того, ЗОФ содержит более 70% воды, что делает ее очень восприимчивой к микробному загрязнению и ферментации. В результате требуются процессы сушки для снижения содержания влаги и обеспечения безопасного обращения. ЗОФ особенно богата фенольными соединениями, включая галловую кислоту, рутин и лютеолин, которые придают антиоксидантные, антимутагенные, цитопротекторные, противоопухолевые и противораковые свойства [10]. Это подчеркивает ее потенциал как ценного ресурса для извлечения высокоценных биоактивных соединений, открывая возможности для повышения ее экономической ценности и снижения воздействия на окружающую среду.
Все три агропромышленных побочных продукта — луковая шелуха, томатные выжимки и зеленая оболочка фисташек — были идентифицированы как богатые источники биоактивных соединений, включая полифенолы, флавоноиды, каротиноиды, пищевые волокна и эссенциальные минералы. Они также признаны потенциальными источниками пектина, который мог бы помочь удовлетворить растущий спрос на этот биополимер, оцениваемый в 40 000 тонн в год с ежегодным темпом роста приблизительно 5% [8].
Несмотря на свой высокий потенциал, эти побочные продукты сталкиваются с общей проблемой: ограниченным повышением ценности за счет извлечения их ценных биоактивных соединений. Исследования в литературе часто фокусируются на извлечении одного компонента. Напротив, цель этой работы состоит в том, чтобы идентифицировать фенольные и структурные соединения, присутствующие в различных агропромышленных побочных продуктах, предоставляя детальные знания о составе в качестве основы для разработки многостадийного биокаскадного процесса. Этот процесс последовательно извлекает различные семейства соединений, начиная с легко доступных неструктурных компонентов. Максимизируя извлечение и использование этих ценных соединений, данный подход направлен на продвижение устойчивых практик и повышение эффективности использования ресурсов в различных отраслях промышленности, согласуясь с принципами циркулярной экономики.
2. Материалы и методы
2.1. Сырье и химические вещества
Отходы луковой шелухи (ОЛШ) (Allium cepa), использованные в этой работе, соответствовали сортам (cv.) 'Horcal' и 'Red' и были предоставлены местной компанией, занимающейся производством кровяной колбасы. ОЛШ были вручную рассортированы для отделения самых внешних оболочек, которые содержат самые высокие уровни флавоноидов и не имеют кулинарной ценности. Томатные выжимки были любезно предоставлены компанией Vega del Ebro S.L., занимающейся переработкой томатов. Зеленая оболочка фисташек (ЗОФ) была получена из Сантьяго-дель-Арройо (Вальядолид, Испания). Перед химическим анализом, проводимым для определения их состава, все сырьевые материалы были измельчены с использованием мельницы SM100 (Retsch GmbH, Хан, Германия), оснащенной ситом 0.5 мм.
Глюкоза (Glu, 99.5%), галактоза (Gal, 99%), арабиноза (Ara, 99%), рамноза (Rha, 99%), ксилоза (Xyl, 99%) и сахароза (99%) были поставлены Sigma-Aldrich (Берлингтон, Массачусетс, США). Фенольные соединения, использованные в этой работе, были предоставлены Extrasynthese (Лион, Франция), (QC4′ (≥99%), QC3,4′ (≥98%) и изорамнетин (≥99%)); Sigma-Aldrich (США) (QC (≥95%), QC3′ (≥98%), протокатеховая кислота (≥98%), n-кумаровая кислота (≥98%), кемпферол (≥97%), мирицетин (≥98%), хлорогеновая кислота (>95%), лютеолин (>97%), рутин (>95%), нарингенин (≥95%) и нарингин (>90%)) и компанией Honeywell Fluka (Шарлотт, Северная Каролина, США), которая поставила п-гидроксибензойную кислоту (≥98%) и глюкуроновую кислоту (GluA, >98%). D-галактуроновая кислота моногидрат (GalA, чистота >97%) была получена от Alfa Aesar (ThermoFischer GmbH, Кандель, Германия); а серная кислота, использованная для гидролиза образцов, имела чистоту 96% и была предоставлена Labbox Labware (Барселона, Испания), тогда как та, что использовалась для приготовления подвижной фазы для ВЭЖХ, была 96% Suprapur, предоставленная Merck KGaA (Дармштадт, Германия). Все химические вещества использовались без дополнительной очистки.
2.2. Определение и характеристика экстрактивных веществ
Начальный этап характеристики биомассы включал определение экстрактивных веществ. Согласно техническому отчету NREL NREL/TP-510-42619, экстрактивные вещества включают все неструктурные материалы, которые могут мешать последующим анализам, направленным на определение структурных компонентов биомассы. Процедура выполнялась в два этапа. На первом этапе в качестве растворителя использовали воду для извлечения водорастворимых материалов, таких как неорганические соединения, неструктурные сахара и азотистые вещества. Эта экстракция проводилась в течение 24 часов при 60 °C с соотношением растворителя к твердому веществу 20:1. После периода экстракции суспензию фильтровали, и жидкую фазу анализировали согласно протоколу. Твердый остаток затем высушивали и подготавливали для второго этапа экстракции с использованием этанола. На втором этапе этанол служил растворителем для извлечения дополнительных компонентов, включая хлорофилл, воски и второстепенные соединения, такие как полифенолы. Эта экстракция также проводилась в течение 24 часов при 60 °C с сохранением того же соотношения растворителя к твердому веществу 20:1. После этанольной экстракции смесь фильтровали, жидкую фазу анализировали, а твердый остаток высушивали для дальнейшей характеристики структурных компонентов биомассы, как описано в Разделе 2.3.
Экстрактивные вещества были охарактеризованы путем идентификации свободных углеводов как в мономерной, так и в олигомерной формах (после кислотного гидролиза) и фенольных соединений, как подробно описано в Разделах 2.2.1 и 2.2.2 соответственно.
2.2.1. Идентификация углеводов
Для идентификации углеводов использовали систему ВЭЖХ 1260 Infinity II (Agilent Technologies, Санта-Клара, Калифорния, США), оснащенную колонкой Biorad Aminex HPX-87H (300 × 7.8 мм, Bio-Rad Laboratories Inc., Геркулес, Калифорния, США) в сочетании с защитной колонкой Micro-Guards Cation H+ (Bio-Rad Laboratories Inc., Калифорния, США), детектором с переменной длиной волны (VWD, модель G7114A, Agilent Technologies, Калифорния, США) и рефрактометрическим детектором (RID, модель G7162A, Agilent Technologies, Калифорния, США), с использованием 0.005 М серной кислоты в качестве подвижной фазы (0.6 мл/мин). Колонка и детекторы поддерживались при 40 °C, общее время анализа составляло 67 минут на инжекцию. Образцы фильтровали через шприцевой фильтр с размером пор 0.22 мкм (Scharlab, Барселона, Испания).
Для анализа свободных углеводов жидкий образец фильтровали и непосредственно вводили в систему ВЭЖХ, как описано в предыдущем параграфе. Для углеводов в олигомерной форме образец подвергали кислотному гидролизу (121 °C в течение 1 часа после добавления 174 мл 72% серной кислоты). После гидролиза полученную жидкость вводили в систему ВЭЖХ для количественного определения мономеров.
2.2.2. Количественное определение общего органического углерода (TOC) и общего азота (TN)
TOC определяли с использованием анализатора Shimadzu TOC-V CSN (Shimadzu Co., Киото, Япония). TOC рассчитывали как разницу между общим углеродом (TC) и неорганическим углеродом (IC). Стандартом для определения TC служил гидрофталат калия (C8H5KO4) в диапазоне концентраций от 0 ppm до 1000 ppm. Для определения неорганического углерода (IC) в качестве стандарта использовали раствор гидрокарбоната натрия (NaHCO3) до 200 ppm. Результаты выражали в г TOC/100 г сырья.
TN определяли с использованием того же оборудования; стандартом служил раствор нитрата калия (KNO3) в концентрации до 200 ppm. Результаты выражали в г TN/100 г сырья. Из этого значения, используя коэффициент пересчета азота 6.25, рассчитывали содержание белка в водном экстракте (выраженное в г белка/100 г сырья).
2.2.3. Идентификация фенольных соединений
Каждый образец был охарактеризован с помощью высокоэффективной жидкостной хроматографии с диодно-матричным детектором (ВЭЖХ-ДМД, Agilent 1100, Калифорния, США) с колонкой Kinetex® Biphenyl (250 × 4.6 мм, размер частиц 5 мкм, размер пор 100 Å), поставленной Phenomenex (Торранс, Калифорния, США). Подвижная фаза состояла из (A) 5 мМ ацетата аммония с уксусной кислотой (1%, об/об) в воде и (B) 5 мМ ацетата аммония с уксусной кислотой (1%, об/об) в ацетонитриле. Подробное описание метода представлено в работе Бенито-Романа и др. [14].
2.3. Определение и характеристика структурных компонентов
Определение структурных компонентов биомассы проводилось согласно протоколу NREL NREL/TP-510-42618. Как указано NREL, структурные углеводы связаны в матрице биомассы, в то время как неструктурные углеводы могут быть удалены с помощью этапов экстракции или промывки. Эти неструктурные углеводы были предварительно удалены, как описано в Разделе 2.2. Вкратце, протокол NREL использует двухстадийный процесс кислотного гидролиза для расщепления биомассы на мономерные компоненты, которые растворимы в жидкости гидролиза и могут быть количественно определены с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ), как подробно описано в Разделе 2.2.1. Протокол также предоставляет процедуры для определения содержания лигнина — как растворимого лигнина, измеряемого с помощью УФ-видимой спектроскопии, так и нерастворимого лигнина, определяемого гравиметрически — а также содержания золы.
Элементный анализ (C, H, N и S) твердых образцов (сырья и истощенного твердого остатка после экстракции) также был выполнен с использованием элементного анализатора FLASH 2000 (Thermo Fisher Scientific, Сан-Хосе, Калифорния, США). Содержание кислорода в образцах определяли по разнице с учетом содержания золы в образце.
2.4. Выделение и характеристика пектина
В этом исследовании пектин выделяли из выбранного сырья с использованием двух различных методов экстракции: обычной экстракции подкисленной водой и альтернативного метода субкритической водой. В первом методе 10 г сырья смешивали с 100 мл воды (pH 2, доведенный HCl) и нагревали при 90 °C в течение 1.5 ч. Твердый остаток затем отделяли от жидкой фазы фильтрацией. Для осаждения растворенного пектина фильтрат смешивали с равным объемом 80% этанола (об/об). В альтернативной процедуре 15 г сырья обрабатывали в реакторе с субкритической водой, как описано Бенито-Романом и др. [5], с использованием 150 мл воды. Смесь нагревали до 125 °C и перемешивали в течение 180 минут. После экстракции смесь твердого вещества и жидкости разделяли центрифугированием (4500 об/мин, 4 °C, 10 мин), и пектин в супернатанте осаждали добавлением этанола, как в обычном методе. В обеих процедурах осажденный пектин отделяли от смеси этанол-вода фильтрацией через марлю. Твердое вещество затем сушили при 35 °C под вакуумом. После высушивания пектин измельчали в мелкий порошок и хранили при 4 °C до дальнейшего анализа. Выход экстракции пектина рассчитывали по формуле (1):
2.4.1. Состав пектина
Определение нейтральных сахаров и уроновых кислот проводили с использованием системы ВЭЖХ, описанной в Разделе 2.2.1. Для этого анализа готовили водный раствор пектина (1 мг/мл) и подвергали гидролизу. В частности, 5 мл раствора пектина переносили в пробирку объемом 15 мл, затем добавляли 0.174 мл H2SO4 (72%, об/об). Затем образец нагревали при 121 °C в течение 1 ч. После гидролиза для нейтрализации образца использовали CaCO3. На основе результатов состава для GalA и нейтральных сахаров относительные пропорции доменов HG и RG-I оценивали с использованием уравнений (2) и (3), предложенных М'сакни и др. [15]:
2.4.2. Молекулярная масса пектина
Средневесовые молекулярные массы (Mw) и полидисперсность образцов определяли с помощью высокоэффективной эксклюзионной хроматографии, сопряженной с рефрактометрическим детектором (ВЭЭХ-РИД). Система ВЭЖХ 1260 (Agilent Technologies, Калифорния, США) состояла из защитной колонки PL Aquagel, соединенной последовательно с колонками PL Aquagel-OH 30, PL Aquagel-OH 40 от Agilent Technologies (300 мм × 7.5 мм, размер частиц 8 мкм). Характеристику пектина из ОЛШ и гидролизатов субкритической воды проводили при 40 °C. Затем 10 мкл каждого образца элюировали в изократическом режиме 0.01 М NH4Ac при скорости потока 0.7 мл/мин. Кроме того, для калибровки использовали набор стандартов пуллулана (0.342–400 кДа), предоставленный PSS Polymer Standards Service GmbH (Майнц, Германия), а данные анализировали с помощью программного обеспечения Agilent OpenLab Data Analysis 2.5. Стандарты и образцы фильтровали через шприцевые фильтры 0.22 мкм.
2.4.3. Степень этерификации пектина
Степень этерификации выделенных пектинов определяли титриметрическим методом. Вкратце, 0.2 г пектина растворяли в 200 мл воды. Затем этот раствор титровали 0.1 М NaOH с использованием фенолфталеина в качестве индикатора, и объем потребленного раствора регистрировали как V1. После этого омыление пектина инициировали добавлением 10 мл 0.1 М NaOH при интенсивном перемешивании. Когда реакция завершалась, добавляли 10 мл 0.1 М HCl, и избыток HCl нейтрализовали 0.1 М NaOH; объем потребленного раствора регистрировали как V2.
2.5. Статистический анализ
Все статистические расчеты выполнялись с использованием Statgraphics 19-X64. Значимость различий определяли на основе анализа дисперсии с использованием процедуры наименьшей значимой разности (НЗР) Фишера при p-значении ≤ 0.05.
3. Результаты и обсуждение
Предоставленные промышленностью томатные выжимки представляли собой гетерогенную смесь, состоящую из кожуры и семян. Поскольку основным компонентом, представляющим интерес в этой работе, была кожура, семена и стебли были отделены вручную перед определением содержания влаги. Кожура составляла 77% от общего веса, в то время как на семена приходилось 19%, а стебли составляли остальные 4%. Содержание влаги в выделенной томатной кожуре (ТК) было определено как 73.3 ± 1.2%, что является заметно высоким значением, повышающим риск быстрой порчи. Чтобы смягчить это, сырье (после удаления семян и стеблей) было тщательно высушено при умеренной температуре (50 °C в течение 24 ч) перед характеристикой, что привело к конечному содержанию влаги 6.5 ± 0.4%. Для других сырьевых материалов были проанализированы отходы луковой шелухи (ОЛШ), полученные от промышленности. Сорт Horcal показал содержание влаги 11.2 ± 0.4%, в то время как сорт Red имел более высокий уровень влажности — 16.1 ± 0.5%. Зеленая оболочка фисташек (ЗОФ), которая была частично высушена в поле, показала содержание влаги 6.8 ± 0.2% при поступлении в лабораторию. В свете этих измерений содержания влаги все сырьевые материалы впоследствии были охарактеризованы, причем все результаты выражены на основе сухого вещества.
3.1. Количественное определение и идентификация экстрактивных веществ
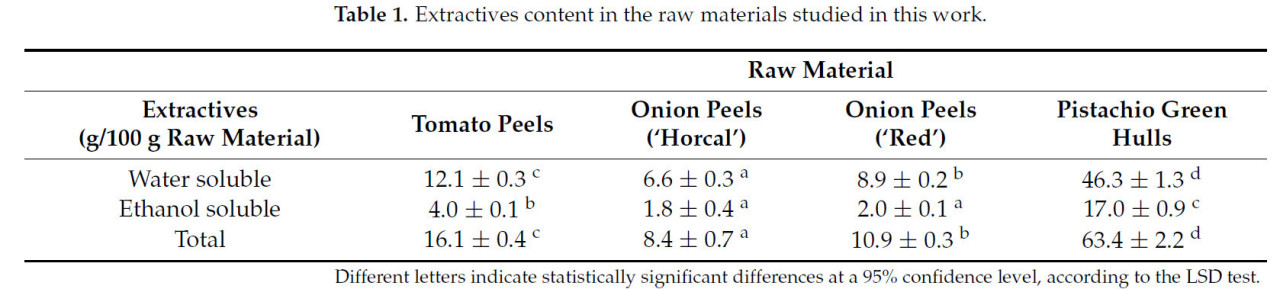
Экстрактивные вещества определяются как любой материал в образце биомассы, который растворим в воде или этаноле в ходе исчерпывающей экстракции. Эти экстрактивные вещества включают неструктурные компоненты, которые могут мешать последующему анализу биомассы. Как показано в Таблице 1, между сырьевыми материалами, проанализированными в этом исследовании, наблюдались значительные различия.
Таблица 1. Содержание экстрактивных веществ в сырьевых материалах, изученных в этой работе.
Наибольшее содержание экстрактивных веществ было обнаружено в ЗОФ — 63.4 ± 1.1 г на 100 г сырья, из которых 73% были водорастворимыми. За ними следовала томатная кожура с содержанием экстрактивных веществ 16.1 ± 0.4 г на 100 г сырья, из которых 75% были водорастворимыми. Луковая шелуха показала сходную тенденцию: приблизительно 80% от общего количества экстрактивных веществ были водорастворимыми. Однако общее содержание экстрактивных веществ в луковой шелухе было ниже и составляло 8.4 ± 0.7 г и 11.1 ± 0.3 г на 100 г сырья для сортов Horcal и Red соответственно. В последующих разделах будет представлен детальный анализ состава как водорастворимых, так и этанолорастворимых экстрактивных веществ.
3.1.1. Неструктурные углеводы в водных экстрактивных веществах
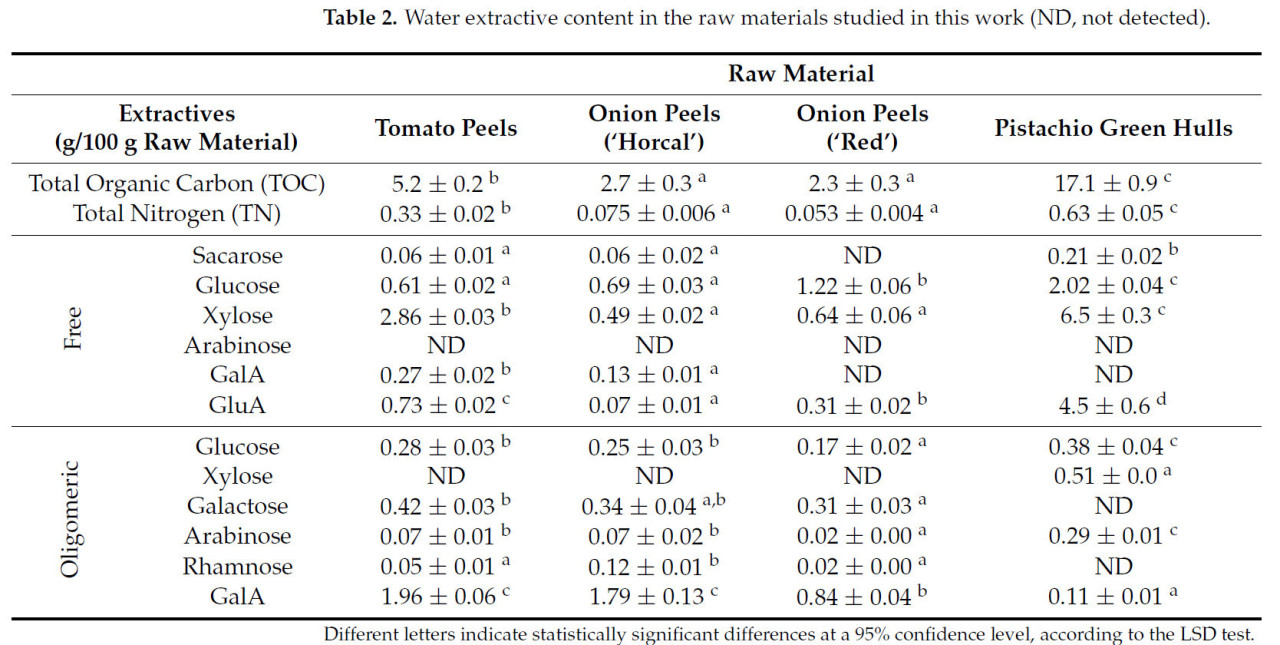
Водные экстрактивные вещества в основном состоят из сахаров, которые могут присутствовать либо в свободной, либо в олигомерной формах, как подробно показано в Таблице 2. В зависимости от анализируемого сырья наблюдаются значительные различия в составе свободных моносахаридов. В томатной кожуре ксилоза является наиболее распространенным моносахаридом, за ней следуют GluA и глюкоза. Высокое содержание ксилозы в томатной кожуре можно объяснить присутствием гемицеллюлоз, основного компонента пищевых волокон в клеточных стенках растений. Томатная кожура особенно богата гемицеллюлозами наряду с пектинами и другими полисахаридами [16]. Манноза, галактоза, ксилоза, арабиноза и глюкоза были идентифицированы как наиболее распространенные сахара в томатной кожуре [17]. Этот состав влияет на их промышленный потенциал, поскольку ксилоза может быть сброжена в биоэтанол или преобразована в ксилит, низкокалорийный подсластитель. Кроме того, функциональные свойства волокна томатной кожуры (например, удержание воды и вязкость) делают его ценным в пищевых применениях в качестве загустителя и стабилизатора. ЗОФ характеризуется высоким содержанием ксилозы, GluA и глюкозы, которые составляют основные водные экстрактивные вещества. Аналогично, луковая шелуха демонстрирует сходный профиль моносахаридов, причем глюкоза и ксилоза являются преобладающими свободными сахарами, независимо от рассматриваемого сорта. Томатная кожура и ЗОФ содержат значительные количества белков (2.1 и 3.9 г/100 г сырья соответственно, рассчитанные из значения TN и коэффициента пересчета азота 6.25), в то время как луковая шелуха показывает значительно более низкие значения.
Таблица 2. Содержание водных экстрактивных веществ в сырьевых материалах, изученных в этой работе (ND — не обнаружено).
Что касается олигомерного состава, галактуроновая кислота (GalA) была наиболее распространенной как в томатной кожуре, так и в сортах лука. Это открытие, наряду с присутствием рамнозы, свидетельствует о наличии пектина в профиле водных экстрактивных веществ этих двух видов сырья. Обнаружение других сахаров, таких как галактоза, дополнительно подтверждает это наблюдение, поскольку галактоза обычно обнаруживается в боковых цепях, присоединенных к остову GalA в пектине. Напротив, наиболее распространенными олигосахаридами в зеленой оболочке фисташек были глюкоза и ксилоза. Профиль олигосахаридов ЗОФ, в котором доминируют ксилоза и глюкоза, согласуется с результатами, опубликованными [18], и отличается от томатной кожуры из-за вариаций в структуре клеточной стенки и содержании полисахаридов. Полисахариды ЗОФ обладают высокой водо- и маслоудерживающей способностью, что делает их пригодными для применения в пищевой промышленности в качестве эмульгаторов и стабилизаторов. Кроме того, их состав поддерживает их использование в производстве биоэтанола и в качестве потенциальных пребиотиков [19], способствующих здоровью кишечника.
3.1.2. Фенольные соединения, присутствующие в экстрактивных веществах
Будучи полярными соединениями, фенольные соединения легко растворяются в полярных растворителях, включая воду и спиртовые органические растворители [9]. Далее описаны индивидуальные фенольные соединения, идентифицированные в водных (Таблица 3) и этанольных (Таблица 4) экстрактивных веществах.
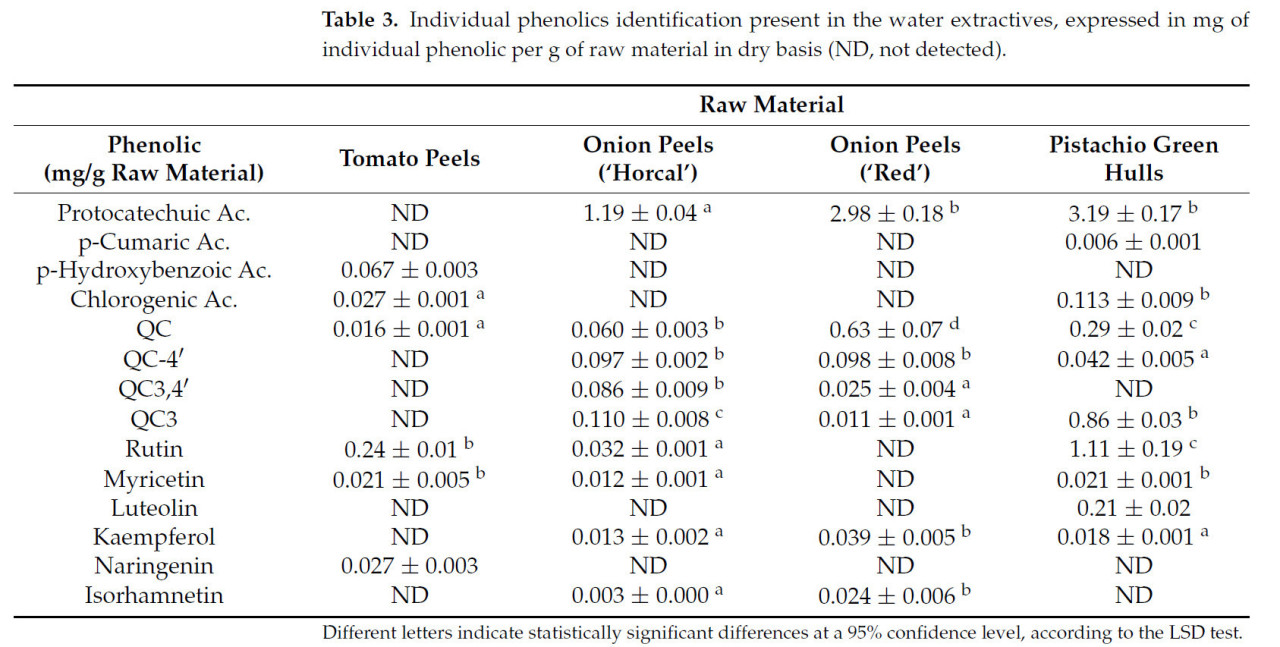
Таблица 3. Идентификация индивидуальных фенольных соединений, присутствующих в водных экстрактивных веществах, выраженная в мг индивидуального фенола на г сырья в пересчете на сухое вещество (ND — не обнаружено).
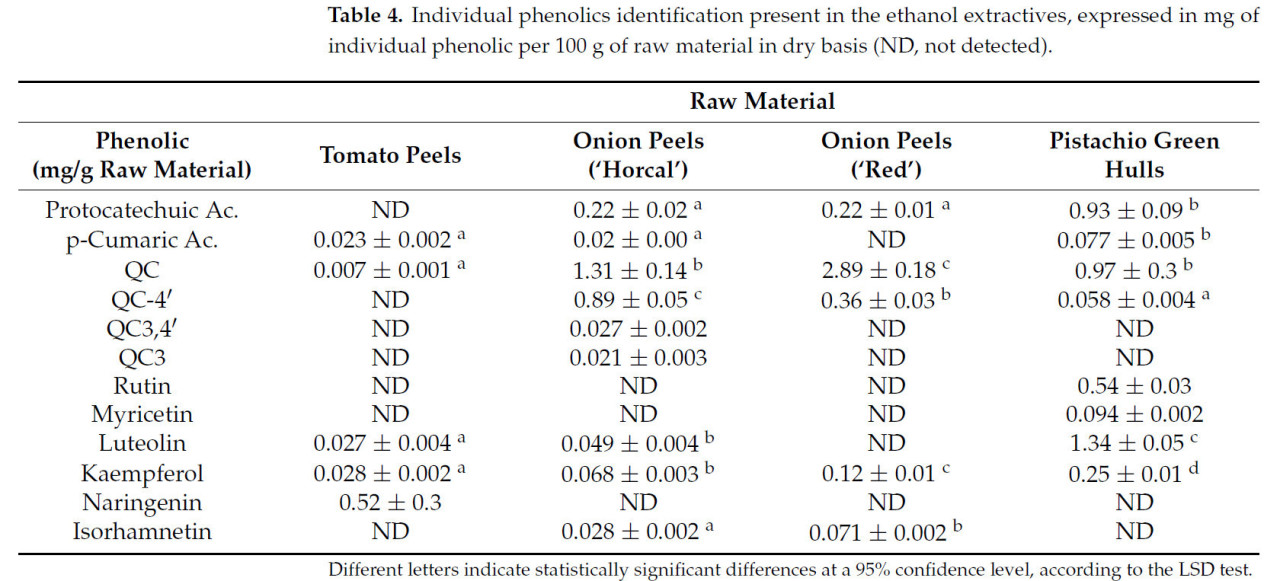
Таблица 4. Идентификация индивидуальных фенольных соединений, присутствующих в этанольных экстрактивных веществах, выраженная в мг индивидуального фенола на 100 г сырья в пересчете на сухое вещество (ND — не обнаружено).
Водорастворимые экстрактивные вещества были дополнительно охарактеризованы путем анализа индивидуальных фенольных соединений, присутствующих в экстрактах. Результаты показаны в Таблице 3. Примечательно, что было обнаружено значительное количество фенольных соединений. В томатной кожуре наиболее распространенным фенолом был флавоноид рутин, за которым следовали п-гидроксибензойная кислота, хлорогеновая кислота и другие второстепенные флавоноиды. Луковая шелуха показала высокие концентрации протокатеховой кислоты, которая обычно хорошо растворима в воде (растворимость при 25 °C составляет 29.4 ± 0.98 г/л), наряду с QC4′ и QC3,4′, флавоноидами, которые обычно проявляют большую водорастворимость по сравнению с QC или QC3′ [14]. В ЗОФ протокатеховая кислота и рутин также присутствовали в значительных количествах, что контрастирует с другими видами сырья. Извлечение этих высокоценных соединений с использованием воды в качестве растворителя при умеренных температурах подчеркивает потенциал этого сырья как источника различных флавоноидов.
Профили этанолорастворимых экстрактивных веществ для каждого из сырьевых материалов представлены в Таблице 4. Как и ожидалось, наиболее распространенным фенольным соединением, обнаруженным в луковой шелухе, независимо от сорта, был кверцетин (QC), за которым следовал QC4′. Это наблюдение согласуется с предыдущими выводами других авторов, которые идентифицировали QC, QC4′ и QC3,4′ как основные флавоноиды в луке [20], в то время как другие соединения, такие как производные кемпферола и изорамнетина, были отмечены как второстепенные флавонолы. В целом, экстракция флавоноидов в литературе осуществляется с использованием смесей этанола и воды. Бенито-Роман и др. [21] продемонстрировали, что смесь этанол/вода (70/30, об/об) дала наилучшие результаты, поскольку дальнейшее увеличение содержания этанола снижало общее количество извлеченного кверцетина и его производных, а чистая вода показала низкую эффективность. Эти результаты согласуются с Халили и др. [22], которые изучали влияние растворителя на общую экстракцию флавоноидов и сообщили о более высоких выходах при использовании органических растворителей (таких как этанол и метанол, которые дали эквивалентные результаты) по сравнению с использованием воды.
Кроме того, нарингенин был идентифицирован как преобладающий флавоноид в томатной кожуре, что подчеркивает потенциал этого материала как ценного источника нарингенина для процессов повышения ценности на ранних стадиях, направленных на извлечение флавоноидов. Присутствие нарингенина и кверцетина также было подтверждено предыдущими исследованиями, такими как Переа-Домингес и др. [23], которые сообщили об этих флавоноидах в связанной форме. В дополнение к нарингенину и кверцетину, эти авторы обнаружили меньшие количества кемпферола и рутина, причем концентрации рутина были почти в 200 раз ниже, чем у нарингенина. Что касается фенольных соединений, наше исследование идентифицировало п-кумаровую и кофейную кислоты как наиболее распространенные. Сравнение наших результатов с результатами, опубликованными в литературе, выявляет значительные расхождения. Например, Сабо и др. [24] проанализировали состав десяти различных сортов томатной кожуры и обнаружили существенные вариации. В их экстракции, выполненной с использованием смеси этанол/вода (80%), нарингенин халкон был идентифицирован как наиболее распространенный флавоноид, за которым следовал рутин (6.4–51 мг/100 г сырья). Нарингенин также был обнаружен в варьирующем диапазоне 4.6–12.1 мг/100 г. Эти два соединения постоянно сообщались как наиболее распространенные флавоноиды в более ранних работах, таких как работа Наварро-Гонсалеса и др. [17], со сходными диапазонами (10.71–41.01 мг/100 г для кверцетин-3-рутинозида и 7.94–28.76 мг/100 г для нарингенина). Наварро-Гонсалес и др. [17] также отметили присутствие производных рутина и хлорогеновой кислоты. Другие исследования, такие как Соуза да Коста и др. [16], использовали растворитель метанол:вода:муравьиная кислота (79:20:1, об/об/об) для экстракции фенольных соединений из фракций томатных выжимок. Их результаты показали общее содержание фенолов в диапазоне от 518.32 до 949.46 мг/кг образца, причем 85.5% из них составляли флавоноиды и 14.5% — фенольные кислоты. В томатной кожуре нарингенин снова был самым распространенным флавоноидом — 557 мг/кг, в то время как концентрации кверцетина и кемпферола составляли 14.6 мг/кг и 1.68 мг/кг соответственно, что согласуется с нашими наблюдениями. Кроме того, они сообщили о присутствии кофейной кислоты (21.26 мг/кг), п-кумаровой кислоты (27.17 мг/кг), гидроксибензойной кислоты (32.1 мг/кг) и протокатеховой кислоты (6.65 мг/кг). При сравнении их результатов с нашими, общая концентрация экстрактивных веществ из водной и этанольной фракций (Таблицы 3 и 4) довольно сходна. Наконец, Мартинес-Инда и др. [25] использовали смесь растворителей этанола (96:4, об/об) при 40 °C, сообщая о хлорогеновой кислоте (0.13 мг/г экстракта), протокатеховой кислоте (0.085 мг/г), галловой кислоте (0.057 мг/г) и кофейной кислоте (0.04 мг/г) с выходом экстракции приблизительно 30% (г экстракта на 100 г сухих измельченных отходов). Широкая вариабельность в опубликованных составах, вероятно, может быть связана с генетическими факторами, условиями культивирования или различиями в методах обработки, таких как используемый растворитель. Фактически, исследование Магед и др. [26] изучало влияние используемого растворителя на выход экстракции фенолов и флавоноидов. Было замечено, что вода позволяет экстрагировать значительные количества этих соединений. В случае томатной кожуры эти авторы сообщили, что наибольшая растворимость наблюдалась при использовании ацетона (5.03 мг фенолов/100 г сухого вещества), за которым следовали вода (3.04 мг фенолов/100 г сухого вещества) и метанол (2.91 мг фенолов/100 г сухого вещества).
В случае ЗОФ было обнаружено, что лютеолин является преобладающим флавоноидом, за которым следуют протокатеховая кислота, кверцетин (QC) и рутин (QC-3-рутинозид). Высокая концентрация этих флавоноидов подчеркивает потенциал ЗОФ для повышения ценности путем извлечения соединений с высокой антиоксидантной активностью. Эти результаты согласуются с предыдущими выводами, опубликованными другими авторами, которые сообщали, что наиболее распространенными являются галловая кислота, кверцетин-3-О-рутинозид, цианидин-3-О-галактозид, кверцетин-О-гексозид, протокатеховая кислота, галлоилшикимовые кислоты, флороглюцин, теогаллин, галлоил-О-гексозид, катехин или пирогаллол [27,28,29,30,31]. Обзор научной литературы выявил, что профиль фенольных соединений ЗОФ варьируется из-за различий в сорте, почвенных условиях, климате, степени зрелости плодов и растворителе, используемом для экстракции. В этом смысле как органические растворители (такие как этанол или метанол), так и вода использовались в литературе, давая отличные результаты. В случае использования воды в качестве растворителя, в исследовании Сейфзаде и др. [30], после характеристики экстракта с помощью УВЭЖХ/МС, эти авторы смогли идентифицировать 34 соединения, включая наиболее распространенные галлоилшикимовые кислоты, галловую кислоту, теогаллин, галлоил-О-гексозид, кверцетин-О-гексозид и пирогаллол. Нурулахи и др. [29] предоставили полную идентификацию фенольных соединений, полученных после водной экстракции: эти авторы сообщили, что преобладающими фенольными кислотными соединениями были кверцетин-О-гексозид (1.363 мкг/г экстракта) и галлоил-О-гексозид-О-кверцетин (0.560 мкг/г экстракта). Напротив, концентрация лютеолина составляла всего 0.024 мкг/г экстракта. Работа Берреки и др. [27] продемонстрировала, что выбор растворителя играет ключевую роль в экстракции фенольных соединений. Метанол, в частности, дал самую высокую эффективность экстракции среди всех фенолов. Выбор соответствующего метода экстракции необходим, чтобы избежать неточного количественного определения компонентов. Метод подготовки и выбор растворителя значительно влияют на экстрагируемость функциональных соединений.
Как было продемонстрировано, в выбранном сырье можно обнаружить различные флавоноиды. Каждый флавоноид обладает специфическими функциональными свойствами, которые делают его пригодным для конкретных применений. Кверцетин более эффективен как антиоксидант, что делает его ценным для консервации пищевых продуктов и в косметике. Лютеолин известен своими мощными антиоксидантными и противовоспалительными свойствами [32], которые делают его ценным для использования в средствах по уходу за кожей и в качестве функционального ингредиента в продуктах питания. Нарингенин, с другой стороны, является флавоноидом с заметными противовоспалительными, противомикробными и потенциальными противораковыми свойствами [33], что делает его особенно полезным для фармацевтической и пищевой промышленности, особенно в разработке функциональных продуктов питания и нутрицевтиков. Метод экстракции также играет роль в селективном извлечении флавоноидов: в зависимости от используемых растворителей и условий, определенные флавоноиды могут экстрагироваться в более высоких концентрациях, влияя на функциональные свойства экстракта и его потенциальное использование в различных приложениях. Вариации в профилях флавоноидов напрямую влияют на свойства экстрактов, такие как растворимость, стабильность, цвет и вкус. Эти характеристики имеют решающее значение для определения пригодности экстрактов для различных промышленных процессов, включая процессы в пищевой, косметической и фармацевтической промышленности.
Учитывая состав как водных, так и этанольных экстрактивных веществ, использование смеси этанол/вода может помочь максимизировать извлечение флавоноидов. Распространенной стратегией для максимизации экстракции флавоноидов является использование смесей этанол/вода, использующих свойства обоих растворителей: вода набухает в растительной матрице и помогает увеличить полярность среды, способствуя экстракции органических соединений, которые растворимы либо в этаноле, либо в воде [34].
3.2. Количественное определение и идентификация структурных компонентов
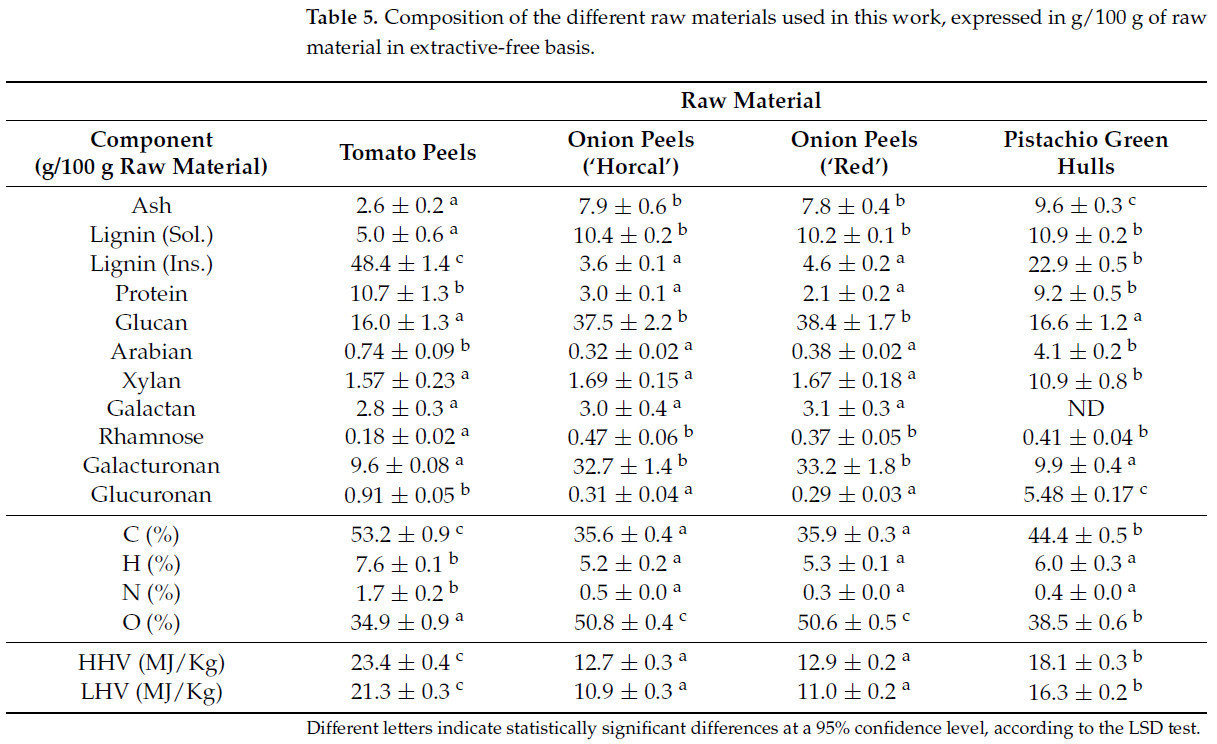
В качестве начального этапа характеристики структурного состава выбранных биомасс был проведен элементный анализ, результаты которого представлены в Таблице 5. Все биомассы показали низкое содержание азота, что свидетельствует о том, что это сырье не подходит в качестве источника белка. Среди них томатная кожура показала самое высокое содержание азота, что может объяснить их текущее использование в кормах для животных. Состав обоих образцов луковой шелухи был довольно сходным, демонстрируя более низкое содержание углерода и более высокие уровни кислорода по сравнению с томатной кожурой. Зеленая оболочка фисташек (ЗОФ) имела промежуточные значения между двумя другими биомассами, что отражается в расчетах высшей теплоты сгорания (HHV) и низшей теплоты сгорания (LHV), основанных на уравнениях, представленных Узоагбой и др. [35]. LHV, по определению, равна HHV минус теплота парообразования содержания воды в образце. Томатная кожура имела самую высокую HHV, что указывает на ее потенциал в качестве источника топлива после извлечения экстрактивных веществ. Напротив, луковая шелуха показала HHV почти на 50% ниже, чем у томатной кожуры, что позволяет предположить, что после извлечения экстрактивных веществ эта биомасса может быть более пригодна для выделения структурных компонентов, таких как пектин. Для ЗОФ необходимо дальнейшее определение структурных компонентов для принятия решений относительно оптимального пути повышения ее ценности.
Таблица 5. Состав различных сырьевых материалов, использованных в этой работе, выраженный в г/100 г сырья на беэкстрактивной основе.
Индивидуальная идентификация структурных компонентов сырьевых материалов, рассмотренных в этой работе, представлена в Таблице 5. Наблюдались значительные различия между сырьевыми материалами (томатная кожура, луковая шелуха и зеленая оболочка фисташек), но не было обнаружено статистически значимых различий между двумя рассматриваемыми сортами лука. В обоих рассматриваемых сортах пектин (32.7 ± 1.4% для сорта Horcal и 33.2 ± 1.8% для сорта Red), наряду с целлюлозой (приблизительно 38% для обоих сортов) и лигнином (составляющим приблизительно 70% от общей растворимой фракции) были основными структурными компонентами, присутствующими в сырье. Также было отмечено незначительное присутствие белков (2–3%), что согласуется с результатами, опубликованными Суутаринен и др. [36], которые обнаружили содержание белка 1.9%. В обоих рассматриваемых в этом исследовании сортах содержание лигнина было значительно выше других результатов, опубликованных в литературе. Например, Чой и др. [37] сообщили, что лигнин Класона составлял 9.4 ± 0.1%. Сложность и вариабельность методов определения лигнина могли бы объяснить различия между результатами, опубликованными в литературе.
Состав томатной кожуры, как показано в Таблице 5, выявляет заметно высокое содержание лигнина, при этом общий лигнин составляет 53.4 ± 2.0% сырья, 91% из которого нерастворим. Томатная кожура также содержит значительные количества глюканов, белков и пектина (галактуронана), каждый на уровне приблизительно 10%, как суммировано в Таблице 5. Это согласуется с предыдущими исследованиями, сообщающими о высоких уровнях пищевых волокон в томатной кожуре. Пищевые волокна представляют собой сложную смесь гидрофильных соединений, таких как растворимые и нерастворимые полисахариды, наряду с ненабухающими соединениями, такими как кутины, суберины и лигнины. Поэтому содержание лигнина, вероятно, включено в общее количество волокон, о котором сообщают другие авторы. Например, Каур и др. [6] сообщили о содержании сырой клетчатки 71.3%, наряду с 14.3% белка, 1.28% золы и 3.5% углеводов. Другие авторы сообщали о диапазонах: влажность 6.69–10%, сырой протеин 10–10.7%, сырой жир 1.7–3.96%, зола 1.13–5.6%, сырая клетчатка 46.1–55.9% и углеводы 26.7%. Другие исследования, такие как исследование Лу и др. [8], сообщили о широких диапазонах состава: белки 5.7–20%, волокна 29.9–65.5%, углеводы 1.1–8.6%, зола 2.6–25.6% и влажность до 10%. Наварро-Гонсалес и др. [17] обнаружили, что томатная кожура содержит 13.3% сырого протеина (13.3%), липидов (6%) и золы (3%). Общее содержание пищевых волокон было высоким — 84.2%, причем 71.8% были нерастворимыми, а остальные 14.4% — растворимыми. Эти авторы провели более полный анализ пищевых волокон, выяснив, что основными сахарами в томатной кожуре были манноза (38.56%), галактоза (16.17%), ксилоза (15.38%), арабиноза (15.16%) и глюкоза (14.64%), что указывает на гемицеллюлозы как на преобладающие полисахариды.
ЗОФ показала отчетливый состав по сравнению с луковой и томатной кожурой, со значительными количествами лигнина, золы и глюканов, а также заметным присутствием уроновых кислот. Тогиани и др. [38] сообщили о 11.4% золы и 13.3% сырого протеина в ЗОФ, в то время как Хассан и др. [11] обнаружили, что это отличный источник углеводов (80.64 ± 0.98%), включая глюкозу, галактозу, рамнозу, арабинозу, ксилозу, маннозу и GalA. Они также сообщили о 6.32 ± 0.26% золы, 1.80 ± 0.28% белка и небольших количествах жиров (0.04 ± 0.005%). Другие исследования, такие как Хамед и др. [39], идентифицировали 39.70% углеводов, 14.74% золы, 11.23% белка и 20.41% жира в ЗОФ. Озбек и др. [40] сообщили о содержании влаги 70.81 ± 0.77% (по сырой массе), наряду с 11.40 ± 0.41% золы, 8.54 ± 0.37% белка и 9.50 ± 0.16% неполярного экстракта в пересчете на сухое вещество.
3.3. Пектин, полученный из луковой и томатной кожуры
После завершения анализа состава различных агропромышленных отходов была проведена экстракция пектина из томатной кожуры и луковой шелухи (сорт 'Horcal') с использованием двух различных методов: обычного метода с подкисленной водой (pH 2, доведенный HCl) и метода экстракции субкритической водой при 125 °C в течение 180 минут. Учитывая высокое содержание экстрактивных веществ в ЗОФ, предлагаемое основное использование этого сырья — в качестве источника фенольных соединений. Выход и результаты состава этих экстракций представлены в Таблице 6, где они сравниваются с коммерческим цитрусовым пектином.
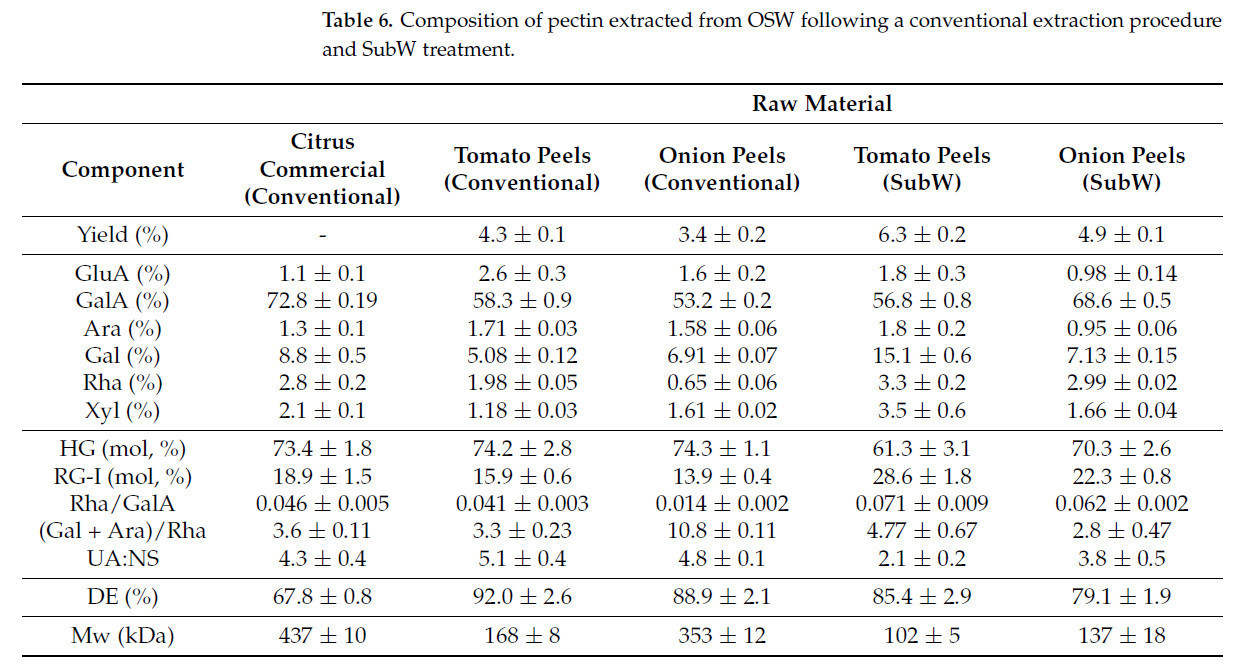
Таблица 6. Состав пектина, экстрагированного из ОЛШ с помощью обычной процедуры экстракции и обработки SubW.
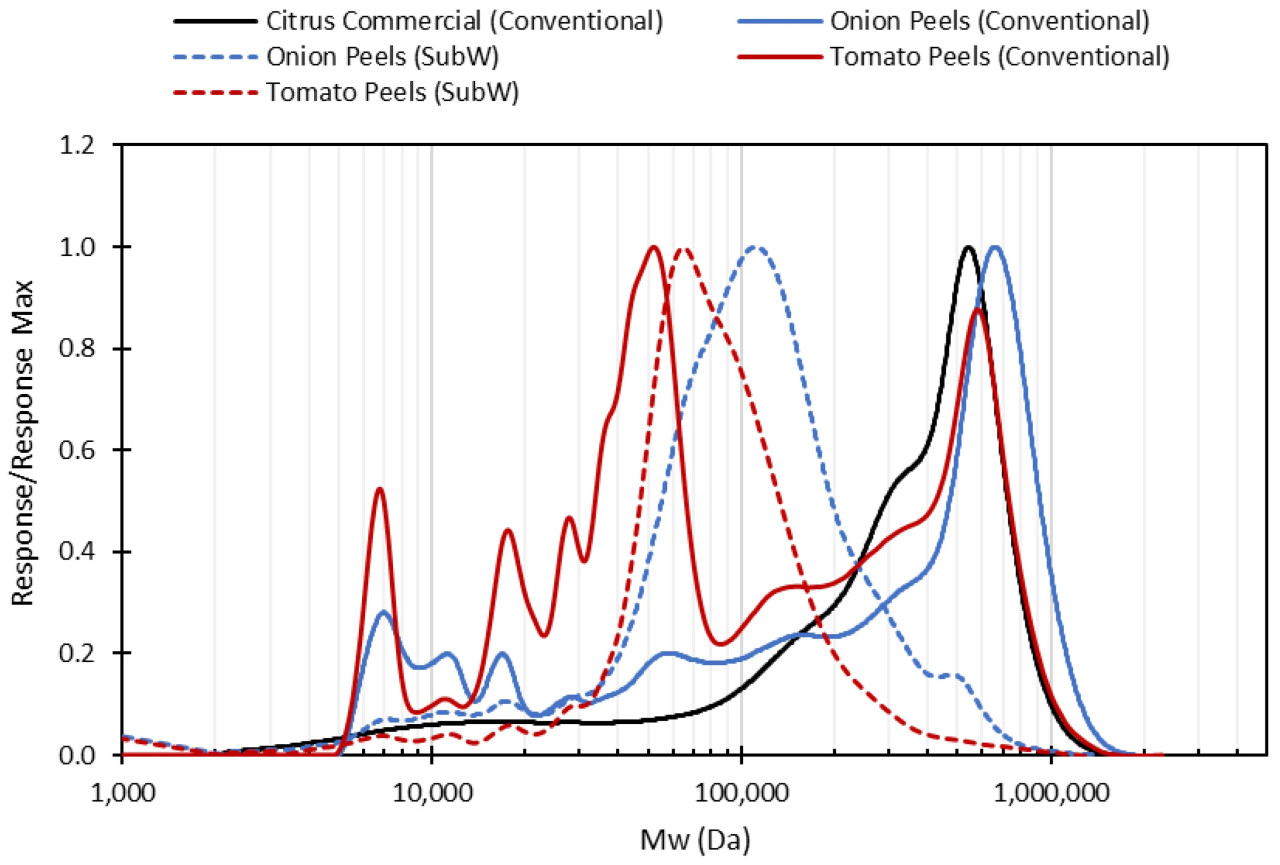
Было обнаружено, что экстракция субкритической водой (SubW) в целом обеспечивала более высокие выходы пектина по сравнению с обычным методом кислотной экстракции. Это подчеркивает способность SubW усиливать реакции гидролиза и облегчать высвобождение структурных компонентов, таких как пектин. Независимо от метода экстракции, томатная кожура давала больше пектина, чем луковая шелуха. По сравнению с коммерческим цитрусовым пектином, пектины, экстрагированные из агропромышленных отходов, во всех случаях демонстрировали более низкое содержание GalA, хотя наблюдались заметные различия в структурных доменах. Пектины, полученные с помощью обычной процедуры, показали относительно низкое присутствие домена RG-I, даже ниже, чем в коммерческом пектине, что позволяет предположить, что разветвленные области гидролизовались в процессе экстракции. Это открытие подтверждается соотношением Rha/GalA, которое отражает вклад домена RG-I. Согласно Янгу и др. [41], когда молярное соотношение Rha/GalA находится между 0.05 и 1, RG-I считается основным компонентом пектина. Как показано в Таблице 6, пектины, полученные с помощью экстракции SubW, имели соотношение Rha/GalA больше 0.05, что указывает на значительное присутствие домена RG-I. Кроме того, соотношение (Gal + Ara)/Rha, также представленное в Таблице 6, помогает оценить, является ли домен RG-I высокоразветвленным. Пектины, экстрагированные SubW, показали более высокие значения для этого соотношения, что позволяет предположить, что домен RG-I более разветвлен по сравнению с пектинами из кислотной экстракции. Значительные различия в распределении молекулярной массы наблюдались в зависимости как от источника пектина, так и от используемого метода экстракции, как показано на Рисунке 2. Коммерческий цитрусовый пектин показал мономодальное распределение, которое аналогично наблюдалось для пектина, экстрагированного обычным способом из ОЛШ. Однако пектин из томатной кожуры отличался, показывая присутствие низкомолекулярных фракций. Для пектинов, полученных с помощью экстракции субкритической водой, основной пик в распределении сместился в сторону низкомолекулярных семейств. Во всех случаях пектины из томатной кожуры демонстрировали более низкие молекулярные массы по сравнению с пектинами из ОЛШ, как указано в Таблице 6.
Рисунок 2. Профили ГПХ пектинов, полученных из различного сырья с использованием разных методов экстракции.
Моралес-Контрерас и др. [42] сообщили, что пектины, экстрагированные обычным методом из томатной шелухи, имели степень этерификации (СЭ) от 63% до 91%, молекулярные массы между 542 и 699 кДа, и галактоза была преобладающим нейтральным сахаром. Аналогично, Грассино и др. [43] сообщили о высоких выходах экстракции (до 32%) и степенях этерификации (до 82.4%) для пектинов, выделенных из томатной кожуры. Сенгар и др. [44] экстрагировали пектин из томатной кожуры с использованием различных методов (на основе ультразвука или микроволн) с кислотной водой в качестве растворителя (pH 1.5 с использованием HCl). Эти авторы сообщили, что процедура экстракции существенно влияла на выход экстракции (в диапазоне 9–25%), степень этерификации (59.8–73.3%), а также на состав пектина. Что касается луковой шелухи, Шен и др. [45] изучали влияние растворителя (вода, различные кислоты и их смеси) и метода экстракции (высокая температура или импульсная ультразвуковая экстракция), заключив о серьезном влиянии каждого из них. Обычная экстракция кислотной водой (HCl) имела выход экстракции 10.6%, а пектин имел степень этерификации 48% с содержанием GalA 55%, значение, довольно близкое к указанному в нашей работе. К сожалению, насколько известно автору, не существует опубликованных исследований по характеристике с точки зрения степени этерификации пектина, экстрагированного из томатной кожуры или луковой шелухи с использованием субкритической воды, с которыми можно было бы сравнить результаты.
4. Выводы
В этом исследовании был изучен состав трех агропромышленных побочных продуктов — луковой шелухи, томатной кожуры и зеленой оболочки фисташек (ЗОФ) — посредством характеристики их водных и этанольных экстрактивных веществ, а также их структурных компонентов. Результаты показали, что все три побочных продукта содержали значительные количества фенольных соединений и флавоноидов. Были отмечены заметные различия в фенольных соединениях, экстрагированных этанолом: кверцетин и его производные были наиболее распространены в луковой шелухе (приблизительно 2.25 мг/г сырья), нарингенин был преобладающим флавоноидом в томатной кожуре, а ЗОФ демонстрировала разнообразный спектр фенольных соединений, включая протокатеховую кислоту, лютеолин и кемпферол. Наиболее распространенным водорастворимым фенолом во всех видах сырья была протокатеховая кислота. Эти различия в профилях фенольных соединений предполагают различный потенциальный промышленный применение для каждого побочного продукта. С точки зрения структурного состава томатная кожура и ЗОФ имели сходство, проявляя высокое содержание лигнина (53.4% и 33.8% соответственно) и уроновых кислот (10–15%). Напротив, луковая шелуха характеризовалась высокими уровнями глюканов (около 38%) и галактуроновой кислоты (33%). Эти детальные знания о составе дают ценную информацию для выявления потенциальных соединений и разработки целенаправленных стратегий повышения ценности для максимизации извлечения ценных компонентов в биокаскадном процессе, который позволяет проводить последовательную экстракцию ценных соединений.
Примером такого подхода является извлечение пектина. После извлечения водорастворимых и этанолорастворимых экстрактивных веществ из трех видов сырья, пектин был экстрагирован на втором этапе биокаскадного процесса с использованием двух различных процедур: обычной кислотной экстракции и экстракции субкритической водой. Результаты показали, что конечные свойства пектина зависели как от сырья, так и от стратегии обработки, используемой для выделения. Эти результаты подчеркивают потенциал пектина из агропромышленных побочных продуктов в качестве альтернативы коммерческому пектину, открывая новые возможности для его использования в различных областях.
Сокращения
ND Не обнаружено
QC Кверцетин
QC4′ Кверцетин-4-глюкозид
QC3 Кверцетин-3-глюкозид
QC3,4′ Кверцетин-3,4′-диглюкозид
DE Степень этерификации
UA:NS Соотношение уроновые кислоты:нейтральные сахара
Ссылки
1. Madeddu, C.; Roda-Serrat, M.C.; Christensen, K.V.; El-Houri, R.B.; Errico, M. A Biocascade Approach Towards the Recovery of High-Value Natural Products from Biowaste: State-of-Art and Future Trends. Waste Biomass Valorization 2021, 12, 1143–1166. [Google Scholar] [CrossRef]
2. Arias, A.; Feijoo, G.; Moreira, M.T. Biorefineries as a Driver for Sustainability: Key Aspects, Actual Development and Future Prospects. J. Clean. Prod. 2023, 418, 137925. [Google Scholar] [CrossRef]
3. Bains, A.; Sridhar, K.; Singh, B.N.; Kuhad, R.C.; Chawla, P.; Sharma, M. Valorization of Onion Peel Waste: From Trash to Treasure. Chemosphere 2023, 343, 140178. [Google Scholar] [CrossRef] [PubMed]
4. EUROSTAT Fruit and Vegetable Production in 2022. Available online: https://ec.europa.eu/eurostat/web/products-eurostat-news/w/ddn-20240301-1#:~:text=Forexample%2CItalyaccountedfor,%25)andPortugal (accessed on 10 December 2024).
5. Benito-Román, Ó.; Melgosa, R.; Illera, A.E.; Sanz, M.T.; Beltr, S. Kinetics of Extraction and Degradation of Pectin Derived Compounds from Onion Skin Wastes in Subcritical Water. Food Hydrocoll. 2024, 153, 109957. [Google Scholar] [CrossRef]
6. Kaur, D.; Wani, A.A.; Oberoi, D.P.S.; Sogi, D.S. Effect of Extraction Conditions on Lycopene Extractions from Tomato Processing Waste Skin Using Response Surface Methodology. Food Chem. 2008, 108, 711–718. [Google Scholar] [CrossRef] [PubMed]
7. Liadakis, G.; Katsouli, M.; Chanioti, S.; Giannou, V.; Tzia, C. Identification, Quantification, and Characterization of Tomato Processing by-Products; Elsevier Inc.: Amsterdam, The Netherlands, 2022; ISBN 9780128228661. [Google Scholar]
8. Lu, Z.; Wang, J.; Gao, R.; Ye, F.; Zhao, G. Sustainable Valorisation of Tomato Pomace: A Comprehensive Review. Trends Food Sci. Technol. 2019, 86, 172–187. [Google Scholar] [CrossRef]
9. Arjeh, E.; Akhavan, H.R.; Barzegar, M.; Carbonell-Barrachina, Á.A. Bio-Active Compounds and Functional Properties of Pistachio Hull: A Review. Trends Food Sci. Technol. 2020, 97, 55–64. [Google Scholar] [CrossRef]
10. Noorolahi, Z.; Sahari, M.A.; Ahmadi Gavlighi, H.; Barzegar, M. Pistachio Green Hull Extract as Natural Antioxidant Incorporated to Omega-3 Rich Kappa-Carrageenan Oleogel in Dry Fermented Sausage. Food Biosci. 2022, 50, 101986. [Google Scholar] [CrossRef]
11. Hassan, S.A.; Abbas, M.; Zia, S.; Maan, A.A.; Khan, M.K.I.; Hassoun, A.; Shehzad, A.; Gattin, R.; Aadil, R.M. An Appealing Review of Industrial and Nutraceutical Applications of Pistachio Waste. Crit. Rev. Food Sci. Nutr. 2024, 64, 3103–3121. [Google Scholar] [CrossRef]
12. Mokhtarpour, A.; Naserian, A.A.; Tahmasbi, A.M.; Valizadeh, R. Effect of Feeding Pistachio By-Products Silage Supplemented with Polyethylene Glycol and Urea on Holstein Dairy Cows Performance in Early Lactation. Livest. Sci. 2012, 148, 208–213. [Google Scholar] [CrossRef]
13. Barış, S.; Elik, A.; Fahrettin, G.; Yanık, D.K. Pistachio Hull as an Alternative Pectin Source: Its Extraction and Use in Oil in Water Emulsion System. Prep. Biochem. Biotechnol. 2023, 53, 433–442. [Google Scholar] [CrossRef] [PubMed]
14. Benito-Román, Ó.; Blanco, B.; Sanz, M.T.; Beltrán, S. Subcritical Water Extraction of Phenolic Compounds from Onion Skin Wastes (Allium cepa Cv. Horcal): Effect of Temperature and Solvent Properties. Antioxidants 2020, 9, 1233. [Google Scholar] [CrossRef]
15. M’sakni, N.H.; Majdoub, H.; Roudesli, S.; Picton, L.; Le Cerf, D.; Rihouey, C.; Morvan, C. Composition, Structure and Solution Properties of Polysaccharides Extracted from Leaves of Mesembryanthenum Crystallinum. Eur. Polym. J. 2006, 42, 786–795. [Google Scholar] [CrossRef]
16. Souza da Costa, B.; García, M.O.; Muro, G.S.; Motilva, M.J. A Comparative Evaluation of the Phenol and Lycopene Content of Tomato By-Products Subjected to Different Drying Methods. LWT 2023, 179, 114644. [Google Scholar] [CrossRef]
17. Navarro-González, I.; García-Valverde, V.; García-Alonso, J.; Periago, M.J. Chemical Profile, Functional and Antioxidant Properties of Tomato Peel Fiber. Food Res. Int. 2011, 44, 1528–1535. [Google Scholar] [CrossRef]
18. Akbari-Alavijeh, S.; Soleimanian-Zad, S.; Sheikh-Zeinoddin, M.; Hashmi, S. Pistachio Hull Water-Soluble Polysaccharides as a Novel Prebiotic Agent. Int. J. Biol. Macromol. 2018, 107, 808–816. [Google Scholar] [CrossRef] [PubMed]
19. Karimi, A.; Ghandehari Yazdi, A.P.; Barzegar, M.; Rahmati, M.; Bazsefidpar, N.; Soltani, A.; Jafari, S.M. Utilizing Pistachio Green Hull Extract to Produce Sugar-Free Muffins with Antioxidant and Antidiabetic Potential. Appl. Food Res. 2024, 4, 100510. [Google Scholar] [CrossRef]
20. Kumar, M.; Barbhai, M.D.; Hasan, M.; Punia, S.; Dhumal, S.; Radha; Rais, N.; Chandran, D.; Pandiselvam, R.; Kothakota, A.; et al. Onion (Allium cepa L.) Peels: A Review on Bioactive Compounds and Biomedical Activities. Biomed. Pharmacother. 2022, 146, 112498. [Google Scholar] [CrossRef]
21. Benito-Román, Ó.; Blanco, B.; Sanz, M.T.; Beltrán, S. Freeze-Dried Extract from Onion (Allium cepa Cv. Horcal) Skin Wastes: Extraction Intensification and Flavonoids Identification. Food Bioprod. Process. 2021, 130, 92–105. [Google Scholar] [CrossRef]
22. Khalili, S.; Saeidi Asl, M.R.; Khavarpour, M.; Vahdat, S.M.; Mohammadi, M. Comparative Study on the Effect of Extraction Solvent on Total Phenol, Flavonoid Content, Antioxidant and Antimicrobial Properties of Red Onion (Allium cepa). J. Food Meas. Charact. 2022, 16, 3578–3588. [Google Scholar] [CrossRef]
23. Perea-Domínguez, X.P.; Hernández-Gastelum, L.Z.; Olivas-Olguin, H.R.; Espinosa-Alonso, L.G.; Valdez-Morales, M.; Medina-Godoy, S. Phenolic Composition of Tomato Varieties and an Industrial Tomato By-Product: Free, Conjugated and Bound Phenolics and Antioxidant Activity. J. Food Sci. Technol. 2018, 55, 3453–3461. [Google Scholar] [CrossRef] [PubMed]
24. Szabo, K.; Diaconeasa, Z.; Cătoi, A.F.; Vodnar, D.C. Screening of Ten Tomato Varieties Processing Waste for Bioactive Components and Their Related Antioxidant and Antimicrobial Activities. Antioxidants 2019, 8, 292. [Google Scholar] [CrossRef] [PubMed]
25. Martínez-Inda, B.; Esparza, I.; Moler, J.A.; Jiménez-Moreno, N.; Ancín-Azpilicueta, C. Valorization of Agri-Food Waste through the Extraction of Bioactive Molecules. Prediction of Their Sunscreen Action. J. Environ. Manag. 2023, 325, 116460. [Google Scholar] [CrossRef] [PubMed]
26. Maged, M.A.; Kishk, Y.F.M.; Khalil, H.I.; Gibriel, A.Y. Determination of Total Phenolics, Flavonoids and Free Radical Scavenging Activities of Pistachio and Tomato By-Products. Ann. Agric. Sci. Ain Shams Univ. 2007, 52, 343–356. [Google Scholar]
27. Barreca, D.; Laganà, G.; Leuzzi, U.; Smeriglio, A.; Trombetta, D.; Bellocco, E. Evaluation of the Nutraceutical, Antioxidant and Cytoprotective Properties of Ripe Pistachio (Pistacia vera L., Variety Bronte) Hulls. Food Chem. 2016, 196, 493–502. [Google Scholar] [CrossRef]
28. Erşan, S.; Güçlü Üstündaǧ, Ö.; Carle, R.; Schweiggert, R.M. Identification of Phenolic Compounds in Red and Green Pistachio (Pistacia vera L.) Hulls (Exo- and Mesocarp) by HPLC-DAD-ESI-(HR)-MSn. J. Agric. Food Chem. 2016, 64, 5334–5344. [Google Scholar] [CrossRef]
29. Noorolahi, Z.; Sahari, M.A.; Barzegar, M.; Ahmadi Gavlighi, H. Tannin Fraction of Pistachio Green Hull Extract with Pancreatic Lipase Inhibitory and Antioxidant Activity. J. Food Biochem. 2020, 44, e13208. [Google Scholar] [CrossRef] [PubMed]
30. Seifzadeh, N.; Ali Sahari, M.; Barzegar, M.; Ahmadi Gavlighi, H.; Calani, L.; Del Rio, D.; Galaverna, G. Evaluation of Polyphenolic Compounds in Membrane Concentrated Pistachio Hull Extract. Food Chem. 2019, 277, 398–406. [Google Scholar] [CrossRef] [PubMed]
31. Tomaino, A.; Martorana, M.; Arcoraci, T.; Monteleone, D.; Giovinazzo, C.; Saija, A. Antioxidant Activity and Phenolic Profile of Pistachio (Pistacia vera L., Variety Bronte) Seeds and Skins. Biochimie 2010, 92, 1115–1122. [Google Scholar] [CrossRef]
32. Ahmadi, R.; Honarvar, M.; Ghavami, M.; Daali, Y. Optimization of Lutein Extraction from Pistachio Waste Using Experimental Design and Ultrasonic Method. Waste Biomass Valorization 2024, 15, 3077–3091. [Google Scholar] [CrossRef]
33. Hou, M.; Li, X.; Chen, F.; Tan, Z.; Han, X.; Liu, J.; Zhou, J.; Shi, Y.; Zhang, J.; Lv, J.; et al. Naringenin Alleviates Intestinal Ischemia/Reperfusion Injury by Inhibiting Ferroptosis via Targeting YAP/STAT3 Signaling Axis. Phytomedicine 2024, 135, 156095. [Google Scholar] [CrossRef] [PubMed]
34. Kashaninejad, M.; Blanco, B.; Benito-Román, Ó.; Beltrán, S.; Niknam, S.M.; Sanz, M.T. Maximizing the Freeze-Dried Extract Yield by Considering the Solvent Retention Index: Extraction Kinetics and Characterization of Moringa Oleifera Leaves Extracts. Food Bioprod. Process. 2021, 130, 132–142. [Google Scholar] [CrossRef]
35. Uzoagba, C.E.J.; Okoroigwe, E.; Kadivar, M.; Anye, V.C.; Bello, A.; Ezealigo, U.; Odette Ngasoh, F.; Pereira, H.; Azikiwe Onwualu, P. Characterization of Wood, Leaves, Barks, and Pod Wastes from Prosopis Africana Biomass for Biofuel Production. Waste Manag. Bull. 2024, 2, 172–182. [Google Scholar] [CrossRef]
36. Suutarinen, M.; Mustranta, A.; Autio, K.; Salmenkallio-Marttila, M.; Ahvenainen, R.; Buchert, J. The Potential of Enzymatic Peeling of Vegetables. J. Sci. Food Agric. 2003, 83, 1556–1564. [Google Scholar] [CrossRef]
37. Choi, I.S.; Cho, E.J.; Moon, J.H.; Bae, H.J. Onion Skin Waste as a Valorization Resource for the By-Products Quercetin and Biosugar. Food Chem. 2015, 188, 537–542. [Google Scholar] [CrossRef] [PubMed]
38. Toghiani, J.; Fallah, N.; Nasernejad, B.; Mahboubi, A.; Taherzadeh, M.J.; Afsham, N. Sustainable Pistachio Dehulling Waste Management and Its Valorization Approaches: A Review. Curr. Pollut. Rep. 2023, 9, 60–72. [Google Scholar] [CrossRef]
39. Hamed, M.; Bougatef, H.; Karoud, W.; Krichen, F.; Haddar, A.; Bougatef, A.; Sila, A. Polysaccharides Extracted from Pistachio External Hull: Characterization, Antioxidant Activity and Potential Application on Meat as Preservative. Ind. Crops Prod. 2020, 148, 112315. [Google Scholar] [CrossRef]
40. Özbek, H.N.; Koçak Yanık, D.; Fadıloğlu, S.; Keskin Çavdar, H.; Göğüş, F. Microwave-Assisted Extraction of Non-Polar Compounds from Pistachio Hull and Characterization of Extracts. Grasas Aceites 2018, 69, e260. [Google Scholar] [CrossRef]
41. Yang, J.S.; Mu, T.H.; Ma, M.M. Extraction, Structure, and Emulsifying Properties of Pectin from Potato Pulp. Food Chem. 2018, 244, 197–205. [Google Scholar] [CrossRef] [PubMed]
42. Morales-Contreras, B.E.; Contreras-Esquivel, J.C.; Wicker, L.; Ochoa-Martínez, L.A.; Morales-Castro, J. Husk Tomato (Physalis ixocarpa Brot.) Waste as a Promising Source of Pectin: Extraction and Physicochemical Characterization. J. Food Sci. 2017, 82, 1594–1601. [Google Scholar] [CrossRef]
43. Grassino, A.N.; Halambek, J.; Djaković, S.; Rimac Brnčić, S.; Dent, M.; Grabarić, Z. Utilization of Tomato Peel Waste from Canning Factory as a Potential Source for Pectin Production and Application as Tin Corrosion Inhibitor. Food Hydrocoll. 2016, 52, 265–274. [Google Scholar] [CrossRef]
44. Sengar, A.S.; Rawson, A.; Muthiah, M.; Kalakandan, S.K. Comparison of Different Ultrasound Assisted Extraction Techniques for Pectin from Tomato Processing Waste. Ultrason. Sonochem. 2020, 61, 104812. [Google Scholar] [CrossRef]
45. Şen, E.; Göktürk, E.; Hajiyev, V.; Uğuzdoğan, E. Comparisons of Pulsed UltrasoundAssi-sted and Hot-Acid Extraction Methods for Pectin Extraction under Dual Acid Mixtures from Onion (Allium cepa L.) Waste. Food Sci. Nutr. 2023, 11, 7320–7329. [Google Scholar] [CrossRef] [PubMed]
Benito-Román Ó, Melgosa R, Benito JM, Sanz MT. Identification of Phenolics and Structural Compounds of Different Agro-Industrial By-Products. Agriculture. 2025; 15(3):299. https://doi.org/10.3390/agriculture15030299
Перевод статьи « Identification of Phenolics and Structural Compounds of Different Agro-Industrial By-Products» авторов Benito-Román Ó, Melgosa R, Benito JM, Sanz MT., оригинал доступен по ссылке. Лицензия: CC BY. Изменения: переведено на русский язык
Фото: freepik
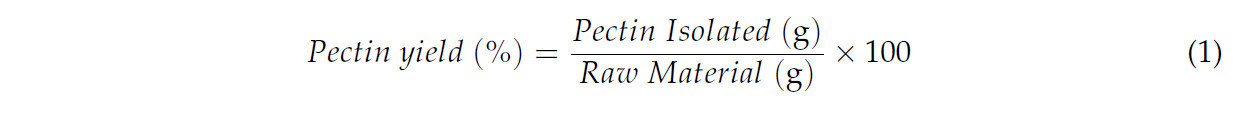
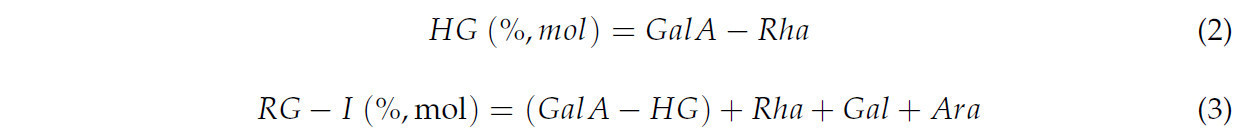













































































































Комментарии (0)