Биоуголь против торфа: неожиданный эффект для салатной зелени
В данном исследовании оценивается возможность использования биоугля в качестве устойчивой альтернативы торфу при беспочвенном выращивании индау посевного (руколы) (Eruca vesicaria (L.) Cav.).
Аннотация
Биоуголь добавляли в торфяной субстрат в концентрациях 0% (контроль), 5%, 10%, 20%, 40% и 70% по объему для изучения его влияния на прорастание семян, рост растений, содержание минеральных веществ и накопление нитратов. Результаты показывают, что концентрации биоугля до 40% по объему поддерживали процент прорастания на уровне выше 80%, аналогичном контролю, в то время как более высокие концентрации (70% по объему) резко снижали прорастание до 29% и полностью нарушали развитие и рост растений. Умеренная концентрация биоугля (20%) оказала положительное влияние на сырую массу и площадь листьев, сохраняя при этом сопоставимые уровни поглощения питательных веществ, содержания хлорофилла и флавонолов. Кроме того, субстраты, обогащенные биоуглем (≥20% по объему), снижали накопление нитратов в листьях на 26–30%, что решает важную проблему качества и безопасности продукции. Высокое содержание биоугля (≥40% по объему) изменяло физико-химические свойства субстрата, включая pH, пористость и электропроводность, негативно влияя на рост растений (снижение роста растений на 38% и площади листьев на 42%) и увеличивая концентрацию тяжелых металлов, например, цинка (~30%). Полученные данные позволяют предположить, что включение до 20% по объему биоугля в беспочвенные субстраты является устойчивой альтернативой торфу, поддерживающей продуктивность индау и улучшающей качество листьев по содержанию нитратов без ущерба для урожайности или безопасности.
1. Введение
Руккола, представительница семейства Капустные (Brassicaceae), является популярной группой листовых овощей, при этом на долю Eruca vesicaria (L.) Cav. и Diplotaxis tenuifolia (L.) D.C. приходится большая часть мирового производства [1]. Эти виды, собираемые в виде целых отдельных листьев для упрощения переработки и увеличения срока хранения после сбора урожая, часто используются в смешанных салатах [2]. Руккола известна своим характерным острым вкусом и ароматом. В настоящее время наблюдается рост популярности и рыночного спроса на продукцию категории "бэби-лист" благодаря ее сенсорным, питательным и антиоксидантным свойствам [3]. Кроме того, ткани рукколы содержат интересный профиль жирных кислот, который смягчает течение некоторых заболеваний человека [4]. С другой стороны, общеизвестно, что руккола накапливает большое количество нитратов, что является негативным фактором качества для листовых овощей [5], потенциально вызывая вредные последствия для здоровья человека, главным образом у новорожденных [6,7]. Регламент ЕС № 1258/2011 устанавливает максимально допустимые уровни нитратов для реализации рукколы на уровне 6000 или 7000 мг NO3 кг−1 сырой массы в зависимости от времени сбора урожая [8].
Беспочвенное культивирование может помочь контролировать накопление нитратов в листовых овощах [9]. Кроме того, такие системы предотвращают заболевания, передающиеся через почву, обеспечивают полный контроль над входными факторами, повышают урожайность и позволяют лучше стандартизировать качество [9]. Можно применять множество различных беспочвенных методов, таких как использование питательных сред для замены почвы или системы, не требующие субстрата (гидропоника или аэропоника) [10].
Субстратное культивирование заключается в использовании питательной среды, заменяющей почву, на протяжении всего жизненного цикла растения, от рассадной до финальной уборки урожая. Питательные среды должны обладать хорошо сбалансированным сочетанием физических и химических свойств. К ним относятся такие факторы, как pH, электропроводность (EC), насыпная плотность, пористость, содержание органического вещества, катионообменная емкость (CEC) и способность удерживать как питательные вещества, так и воду [11]. Известно, что питательные среды значительно влияют на рост растений, регулируя доступность питательных веществ, водоудерживающую способность и аэрацию [12]. Хорошо сбалансированный субстрат обеспечивает адекватное поступление элементов, необходимых для здоровья растений [13,14]. И наоборот, дисбаланс или дефицит в субстрате может привести к нарушениям питания, влияя на общую жизнеспособность растений [15].
Благодаря своим превосходным физическим и химическим характеристикам для выращивания растений, торф является основным компонентом садоводческих питательных сред [16]. Около 40% торфа, потребляемого в Европейском союзе, используется в качестве субстрата для выращивания растений, и из этого объема примерно одна треть предназначена для производства овощей [17], при этом прогнозы указывают на дальнейший рост с 2020 по 2050 год [18]. Однако интенсивное использование торфа в сельском хозяйстве оказывает сильное воздействие на торфяники, которые представляют собой экологически важные, но хрупкие экосистемы [19]. Кроме того, процесс добычи торфа из торфяников высвобождает CO2 в атмосферу [20], что создает дополнительные экологические проблемы. Поэтому в последние годы научное сообщество сосредоточило исследования на субстратах, потенциально способных полностью или частично заменить торф без негативного влияния на урожайность и качество сельскохозяйственных культур [21]. Исследования по использованию биоугля в беспочвенном культивировании вписываются в этот контекст. Биоуголь получают путем пиролиза или газификации растительных отходов/отходов биосолей (например, травянистых/древесных отходов и осадков сточных вод) в почти бескислородной среде [22], что приводит к получению пористого материала, состоящего из органической фракции, богатой углеродными структурами, и неорганической части, состоящей из минералов [23]. В агрономических целях физико-химические свойства биоугля могут оказывать положительное влияние, приводя к увеличению катионообменной емкости (CEC), pH, содержания/доступности питательных веществ и влагоудерживающей способности [24]. Кроме того, сообщается, что его характеристики поддерживают рост разнообразных микробных сообществ, которые необходимы для фиксации азота [25]. Дополнительно, высокое содержание углерода и микропористая структура биоугля способствуют увеличению секвестрации углерода в почвах, что, в свою очередь, помогает сократить выбросы парниковых газов [26].
Применение биоугля в качестве компонента питательной среды показало различные результаты в зависимости от его характеристик и вовлеченных культур [27]. Было проведено много исследований по добавлению биоугля в беспочвенные субстраты для различных овощных культур и продуктов категории "бэби-лист" [27,28,29,30,31]. Умеренная концентрация биоугля (~20% по объему) из лесных отходов улучшила вегетативный рост томатов, не влияя на урожайность или качество [29,30]. Биоуголь из лиственной древесины и жмыха сахарного тростника успешно заменил субстраты на основе коры для томатов и базилика [32]. Кроме того, увеличение урожайности наблюдалось у листовых овощей при использовании смеси перлита и биоугля из рисовой шелухи [33].
Что касается рукколы (Eruca vesicaria), было проведено несколько исследований по выращиванию в горшках, показавших различные результаты [27,28,34,35,36,37]. В этих исследованиях биоуголь добавляли в питательную среду в очень низкой концентрации (менее 2,5% по объему) до максимум 15% по объему, и анализировали различные параметры, такие как прорастание семян, продуктивность растений и физиологические показатели.
В нашей предыдущей работе, лесной биоуголь, смешанный в концентрациях до 40% по объему с торфяной средой, привел к увеличению биомассы растений томата, а урожайность плодов томата при содержании биоугля 10% по объему была сопоставима с контролем [38]. Основываясь на этих предыдущих результатах, мы предположили, что те же смеси биоугля могут подходить для выращивания рукколы. Таким образом, текущее исследование было направлено на оценку влияния биоугля в пяти различных концентрациях (5%, 10%, 20%, 40% и 70% по объему) на прорастание семян рукколы, рост растений, а также содержание питательных веществ и нитратов в листьях. Насколько нам известно, это первая работа, в которой протестированы прорастание и рост рукколы в средах с высоким содержанием биоугля.
2. Материалы и методы
2.1. Экспериментальная установка и характеристика субстрата
Сельскохозяйственный биоуголь был получен из древесной биомассы, источником которой послужили отходы порослевого хозяйства. Процесс производства был осуществлен малым предприятием BioEsperia с использованием запатентованной полномасштабной газификационной установки. Более подробно, древесная биомасса подвергалась процессу газификации при 800–900 °C в течение 10 минут контакта. Репрезентативные образцы из различных производственных партий были собраны для тщательной физико-химической характеристики, а также анализа тяжелых металлов и органических микрозагрязнителей, следуя протоколу, описанному Del Bubba и др. [22]. Характеристика и свойства биоугля уже были представлены Bini и др. [38].
Биоуголь был включен и тщательно перемешан в горшках с коммерческим субстратом, состоящим из торфа и лапиллуса 10/14 мм (1:1 по объему), в результате чего было получено шесть вариантов обработки: BC0 (100% коммерческий субстрат) в качестве контроля, BC5 (содержание биоугля 5% по объему), BC10 (содержание биоугля 10% по объему), BC20 (содержание биоугля 20% по объему), BC40 (содержание биоугля 40% по объему) и BC70 (содержание биоугля 70% по объему). Субстраты BC0, BC5, BC10, BC20 и BC40 использовались в качестве питательных сред для томата в предыдущем исследовании, и их физико-химические свойства, а также аналитические методы их определения уже были представлены Bini и др. [38]. Субстрат BC70, не использовавшийся для томата [38], был проанализирован в этом исследовании теми же методами.
Эксперимент проводился в теплице Департамента DAGRI в Сесто-Фьорентино, Италия (координаты DMS: 43°81′68″ с.ш., 11°19′99″ в.д.), с сентября по декабрь 2022 года. Средняя температура за этот период составила 20 °C, при влажности 65%. Коммерческие семена рукколы (Franchi Sementi Spa, Грассоббио, Бергамо, Италия) были высеяны вскоре после покупки в пластиковые горшки (40 л, 72 × 28 × 40 см, AgriVivai, Пистоя, Италия), заполненные различными субстратами (по 150 семян на горшок), что обеспечило плотность растений 750 растений м−2. Пять горшков на каждый субстрат были расположены по схеме рандомизированных блоков. Орошение было автоматизировано с использованием контроллера полива, по три капельницы на горшок. Удобрение вносилось каждые семь дней после посева с использованием Compo Expert Hakaphos Base NPK 7-12-40 (COMPO EXPERT GmbH, Мюнстер, Германия) в дозировке 1 г на литр воды в каждом горшке.
2.2. Оценка прорастания
Прорастание семян рукколы контролировали ежедневно для каждого горшка и каждой обработки. Семена считались проросшими, когда две семядоли полностью раскрывались. Семена подсчитывали ежедневно до тех пор, пока новые проростки не переставали обнаруживаться в течение двух дней подряд, в результате чего общий подсчет составил 12 дней.
Четырехпараметрическая функция Хилла (4-PHF) использовалась для расчета совокупного прорастания в каждом горшке с рукколой, как ранее описано El-Kassaby и др. [39], с помощью следующего уравнения:
где y представляет процент совокупного прорастания в момент времени x; y0 — это точка пересечения с осью y (≤0); a — асимптота, представляющая максимальный процент совокупного прорастания, который считается максимальной способностью к прорастанию; b — математический параметр, связанный с формой и крутизной кривой прорастания; а c представляет собой количество дней, необходимое для прорастания 50% семян (D50). Путем расчета четырех параметров a, b, c и y0 можно получить время начала прорастания (LAG) и конечный процент прорастания (GP), используя следующие уравнения:
LAG использовался для расчета Dlag50, который представляет собой продолжительность между временем начала прорастания и временем достижения 50% прорастания. Кроме того, среднее время прорастания (MGT) рассчитывали по формуле Эллиса и Робертса [40]:
где n представляет собой количество семян, проросших в момент времени D, который считается количеством дней с момента посева, а ∑n — это итоговое прорастание.
Дополнительно были рассчитаны другие параметры: t50total — время (дни) для достижения 50% прорастания; последнее время прорастания (LastGermTime) — день, когда происходит последнее прорастание; и временной разброс прорастания (TimeSpreadGerm) — разница между последним и первым днем прорастания. Кроме того, скорость прорастания была рассчитана, как сообщалось ранее [41], с использованием следующей формулы:
где Ti представляет время, прошедшее с начала эксперимента до i-го временного интервала, Ni обозначает количество семян, проросших в течение i-го интервала (не совокупное количество, а конкретное число для этого интервала), а k указывает общее количество временных интервалов.
Наконец, индекс прорастания (GI), представленный Melville и др. [42], был получен по последующей формуле:
где Ti представляет время, прошедшее с начала эксперимента до i-го временного интервала, Ni обозначает количество семян, проросших в течение i-го интервала (не совокупное количество, а конкретное число для этого интервала), Nt — общее количество семян, использованных в тесте, а k указывает общее количество временных интервалов. Сообщенные параметры были рассчитаны с использованием пакета germinationmetrics [43] в R-project.
2.3. Анализ роста растений и биомассы
Через пятьдесят дней после посева 15 репрезентативных случайных растений на горшок были отобраны и использованы для проведения биометрических анализов (т.е. количество листьев, длина листовой пластинки и черешка, площадь листьев). Площадь листьев определяли с помощью программного обеспечения Tomato Analyzer 3.0.3 [44]. Кроме того, цвет листьев измеряли с помощью электронного колориметра (Minolta Chromameter CR200, Konica Minolta, Осака, Япония). Впоследствии каждый лист взвешивали, сушили при 65 °C в течение 48 часов, а сырую и сухую массу всей надземной части рассчитывали путем суммирования массы каждого листа. Удельная площадь листьев (SLA) была рассчитана путем деления площади листа на его сухую массу.
2.4. Оценка содержания хлорофилла и флавонолов
Содержание хлорофилла (Chl) и эпидермальных флавонолов (Flavs) определяли с помощью неразрушающего метода на основе сенсора Dualex Scientific (Force-A, Монпелье, Франция). Более подробно, было измерено 10 репрезентативных растений на горшок (по 3 разных листа с растения), всего 150 листьев на обработку. Для каждого листа измерение проводилось как на верхней, так и на нижней стороне листовой пластинки, избегая жилок. Тесты проводились на здоровых листьях (без явно видимых симптомов) утром (9:00–13:00) в солнечный день. Значения для верхней и нижней стороны листовой пластинки были усреднены для содержания Chl и суммированы для содержания Flav.
Оценка Chl (мкг см−2) основана на разнице в пропускании между двумя определенными длинами волн: видимым светом при 650 нм и ближним инфракрасным излучением при 710 нм. Напротив, содержание эпидермальных Flavs (мкг см−2) оценивается путем сравнения поглощения в ультрафиолете А (UVA) при 375 нм с поглощением при 650 нм.
2.5. Нитраты
Концентрацию нитратов определяли с использованием салицилсернокислого метода, описанного Cataldo и др. [45]. Более подробно, листья рукколы (5 независимых повторностей на обработку) лиофилизировали в течение 48 часов, и 100 мг растирали пестиком в ступке. Затем растительный материал суспендировали в 30 мл дистиллированной воды и перемешивали в течение 2 часов при комнатной температуре. Впоследствии 200 мкл образца смешивали с 800 мкл 5% салициловой кислоты в серной кислоте и 30 мл 1,5 N NaOH. Затем образцам давали остыть до комнатной температуры перед измерением оптической плотности при 410 нм с помощью спектрофотометра Hitachi U-2000 (Hitachi High Tech Corporation, Токио, Япония). Уровни нитратов вычисляли с использованием калибровочной кривой стандартов KNO3, и результаты выражали в пересчете на сырую массу (сыр. масса) с учетом соотношения сырой и сухой массы.
2.6. Содержание минеральных веществ
Концентрации минералов и тяжелых металлов (P, Ca, Mg, Na, K, Fe, Cu, Zn, Mn, Ni, Cr, Pb, Cd и V) определяли с использованием масс-спектрометрии с индуктивно-связанной плазмой и оптико-эмиссионной спектрометрии (ИСП-ОЭС) с системой iCAP 7000 Plus (Thermo Fisher Scientific, Уолтем, Массачусетс, США), после микроволнового кислотного разложения (Mars Microwave Digestor, CEM, Мэтьюз, Северная Каролина, США), как сообщалось Bini и др. [38]. В частности, 300 мг предварительно высушенных, измельченных листьев (3 повторности на обработку) взвешивали и помещали в реакционный сосуд микроволновой печи, затем добавляли 2 мл азотной кислоты. Сосуд затем герметично закрывали, и процесс разложения проводили путем нагрева до 190 °C в течение 15 мин, с последующей выдержкой 15 мин при 190 °C. После охлаждения сосуды открывали, и раствор для разложения переносили в мерную пробирку объемом 50 мл, доводили до метки деионизированной водой и анализировали с помощью ИСП-МС, следуя стандартам ISO 11466 [46]. Данные выражены в пересчете на сухую массу (сух. масса).
2.7. Статистический анализ
Статистический анализ проводили с использованием непараметрического теста Краскела-Уоллиса с последующим апостериорным множественным сравнением Данна с поправкой Бенджамини-Хохберга для p-значений для контроля уровня ложных открытий при 95% доверительном уровне (p < 0,05), используя пакет dunn.test [47] в R (версия 4.3.1). Вариации в содержании хлорофилла, флавонолов, цвете листьев и содержании нитратов были дополнительно оценены с использованием теста Геймса-Хауэлла, реализованного через пакет rstatix [48], который позволяет сравнивать средние значения и их стандартные отклонения, учитывая неравные дисперсии между переменными.
Кроме того, был проведен многомерный анализ для оценки всех переменных, связанных с растениями, для каждого субстрата. Первоначально была построена корреляционная матрица с использованием R-пакета corrplot 0.92 [49] на основе коэффициента корреляции Пирсона для оптимизации набора переменных для дальнейшего анализа. В частности, переменные растений были отобраны путем удаления признаков с коэффициентом корреляции >0,95. Впоследствии отобранные признаки растений были использованы для построения биплота метода главных компонент (PCA) с использованием пакетов FactoMineR 2.7 [50] и factoextra 1.0.7 [51] в R.
3. Результаты
3.1. Физико-химические свойства субстратов
В таблице S1 представлены физико-химические свойства субстратов, использованных в этом исследовании. Данные по BC0, BC5, BC10, BC20 и BC40 уже были опубликованы в Bini и др. [38] и приводятся здесь снова в связи с необходимостью сравнения всего набора субстратов. Включение биоугля в среды привело к изменениям в физико-химических свойствах субстратов. В частности, увеличение содержания биоугля привело к снижению насыпной плотности, при этом BC0 и BC70 показали самую высокую и самую низкую плотность (0,804 ± 0,06 г см−3 и 0,401 ± 0,01 г см−3 соответственно). И наоборот, с увеличением концентрации биоугля было выявлено повышение пористости среды и влагоудерживающей способности, при этом самые низкие значения (68,4 ± 0,3% по объему и 39,3 ± 0,1% по объему соответственно) были обнаружены в BC0, а самые высокие — в BC70 (80,6 ± 1,6% по объему и 55,63 ± 1,3% по объему соответственно). Существенных изменений не наблюдалось в легко доступной воде, для которой только BC5 показал значительно более низкое значение. Кроме того, биоуголь повлиял как на уровень pH, так и на EC, вызвав значительное и стабильное увеличение этих параметров с более высокими концентрациями биоугля в субстрате. В частности, все смеси на основе биоугля имели высокий pH, со значениями в диапазоне от 8 до 10,8, тогда как контроль имел слабокислый pH (6,2). Важно отметить, что pH превысил пороговое значение, установленное Законодательным декретом 75/2010 для смешанных сред (pH = 8,5), во всех субстратах с биоуглем, кроме BC5. Что касается EC, содержание биоугля выше 20% по объему привело к заметному повышению уровней EC в средах. Дополнительно, биоуголь повлиял на уровни CEC, которые были выше во всех субстратах с биоуглем по сравнению с контролем (BC0). Однако существенных различий между субстратами, обогащенными биоуглем, не обнаружено, за исключением BC10, который показал более низкие значения CEC, чем BC70 (23,1 ± 0,85 и 28,6 ± 0,71 мэкв 100 г−1 соответственно). Субстраты, обогащенные биоуглем, также показали более высокие концентрации общего органического углерода (TOC) по сравнению с контролем, в то время как существенных изменений в уровнях хлоридов не отмечено. И наоборот, более высокое содержание биоугля (>20% по объему) привело к увеличению содержания аммиака и нитратов, в то время как значительное повышение общего азота наблюдалось только в BC70 (0,22 ± 0,02%). Кроме того, включение биоугля в торфяные субстраты повлияло на уровни макро- и микроэлементов, а также тяжелых металлов. Хотя статистически значимых различий по кальцию (Ca) не наблюдалось, его концентрация увеличивалась с увеличением содержания биоугля в субстратах. Биоуголь также привел к увеличению концентраций магния (Mg) и марганца (Mn). Изменений в уровнях железа (Fe) и цинка (Zn) не наблюдалось, но было отмечено снижение фосфора (P) и натрия (Na) в средах, обогащенных биоуглем. Хотя уровни никеля (Ni) зависели от биоугля и увеличивались с более высокими концентрациями биоугля, они оставались в пределах, установленных Законодательным декретом 75/2010.
3.2. Оценка прорастания
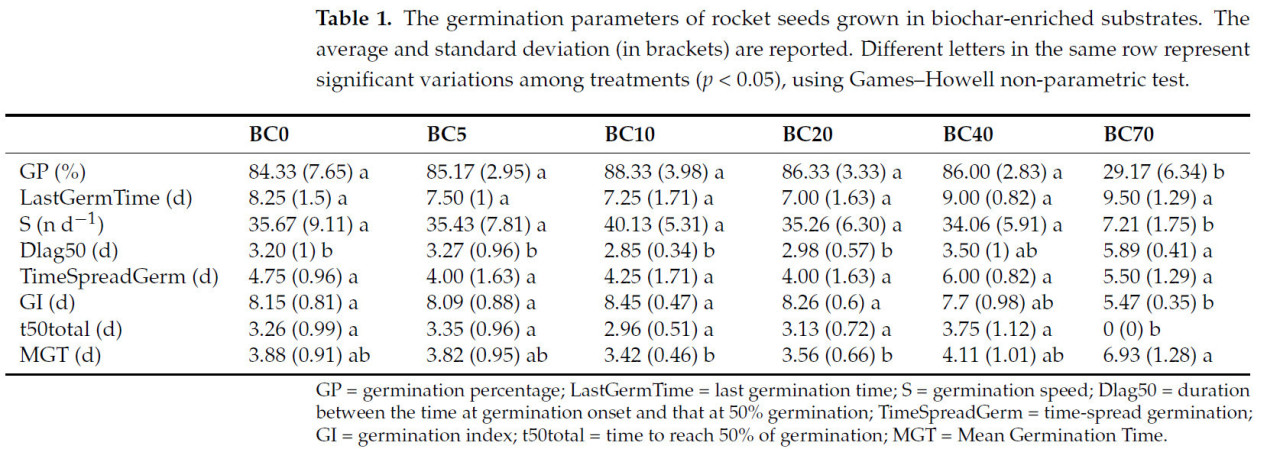
В таблице 1 представлены средние значения и стандартные отклонения параметров прорастания, зарегистрированных в течение 12 дней после посева рукколы. Никаких существенных различий в скорости прорастания не наблюдалось между обработками BC0, BC5, BC10, BC20 и BC40, все они соответствовали минимальному коммерческому стандарту для прорастания семян рукколы (GP > 80%). Напротив, процент прорастания резко снизился на субстрате BC70, где успешно проросло только 29,17 ± 6,34% семян. Аналогичная закономерность наблюдалась для скорости прорастания (S): субстраты от BC0 до BC40 показали сопоставимые значения (диапазон: 34,06–40,13 шт. день−1), в то время как BC70 продемонстрировал резкое снижение приблизительно на 79% (7,21 ± 1,75 шт. день−1).
Таблица 1. Параметры прорастания семян рукколы, выращенной на субстратах, обогащенных биоуглем. Приведены средние значения и стандартные отклонения (в скобках). Разные буквы в одной строке представляют значительные различия между обработками (p < 0,05) с использованием непараметрического теста Геймса-Хауэлла.
Никаких существенных различий не было обнаружено между шестью субстратами по последнему дню прорастания (LastGermTime) и времени между последним и первым днем прорастания (TimeSpreadGerm). Однако сроки прорастания показали противоположную тенденцию по сравнению с предыдущими параметрами. В частности, самое высокое значение Dlag50 было зафиксировано в BC70 (5,89 ± 0,41 дня), а самое низкое наблюдалось в BC10 (2,85 ± 0,34 дня). Существенных различий между BC5, BC10, BC20, BC40 и контролем (BC0) не было, и все они были значительно ниже, чем BC70. Аналогичная тенденция была отмечена для t50total и среднего времени прорастания (MGT), где субстраты с содержанием биоугля до 40% не показали статистической разницы по сравнению с контролем и были значительно ниже, чем BC70.
Более того, концентрация биоугля значительно повлияла на индекс прорастания (GI). Более высокие концентрации биоугля (≥40% по объему) привели к снижению GI по сравнению с контролем и более низкими концентрациями биоугля.
3.3. Урожайность рукколы
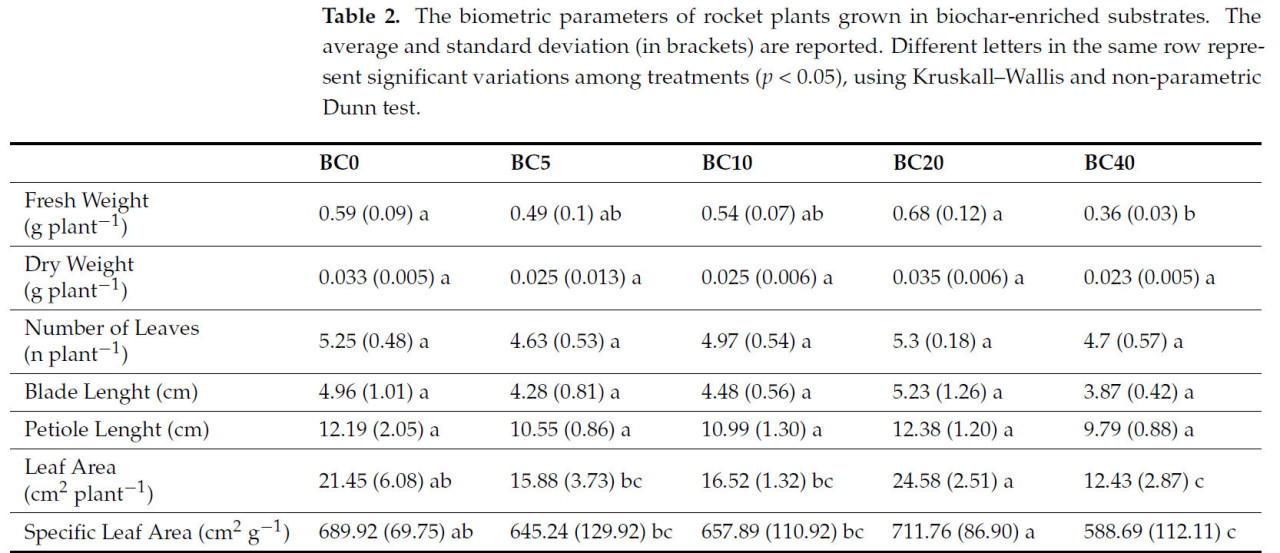
Скорость прорастания в BC70 была чрезвычайно низкой, и стандартизированное коммерческое производство получено не было; поэтому образцы BC70 не рассматривались для дальнейшего анализа. Биометрические параметры рукколы, выращенной на субстратах, обогащенных биоуглем, представлены в таблице 2. Наибольшая сырая масса (FW) надземной части была зафиксирована в BC20 (0,68 ± 0,12 г растение−1), за которым следовали BC0, BC10, BC5 и BC40 (0,59 ± 0,25; 0,49 ± 0,16; 0,45 ± 0,12 и 0,33 ± 0,1 г растение−1 соответственно). Последний (BC40) оказался статистически отличающимся и более низким, чем BC20 (−47%) и контроль BC0 (−38,98%). Хотя наблюдались различия в сырой массе листьев, существенных расхождений не было обнаружено между пятью субстратами в отношении сухой массы (DW) надземной части. Аналогичная тенденция была замечена для количества листьев (NL), длины листовой пластинки (BL) и длины черешка (PL), по которым все субстраты были статистически схожи. Значимые различия наблюдались в площади листьев (LA) и удельной площади листьев (SLA). Более подробно, тенденция была одинаковой для обоих параметров: BC20 > BC0 > BC10 > BC5 > BC40. Субстрат BC20 показал самые высокие значения (24,58 ± 2,51 см2 растение−1 и 711,76 см2 г−1 соответственно), а BC40 — самые низкие (12,43 ± 2,87 см2 растение−1 и 588,69 ± 112,11 см2 г−1 соответственно). Различий для BC20, BC10 и BC5 по сравнению с контролем (BC0) не наблюдалось.
Таблица 2. Биометрические параметры растений рукколы, выращенных на субстратах, обогащенных биоуглем. Приведены средние значения и стандартные отклонения (в скобках). Разные буквы в одной строке представляют значительные различия между обработками (p < 0,05) с использованием теста Краскела-Уоллиса и непараметрического теста Данна.
3.4. Содержание минеральных веществ и тяжелых металлов
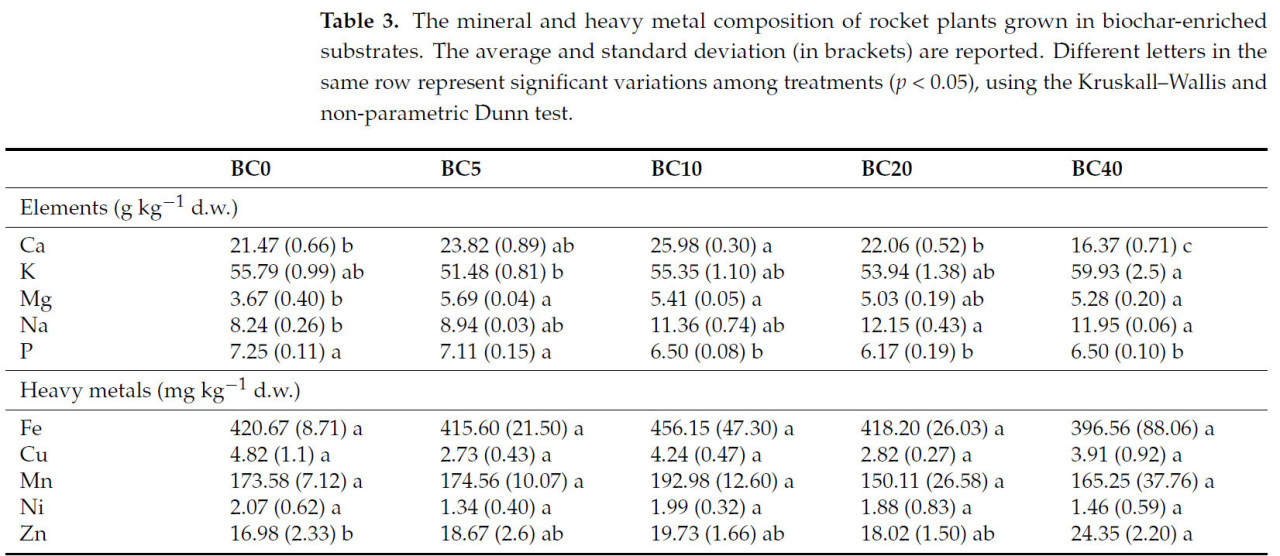
В таблице 3 представлено содержание макро- и микроэлементов, а также тяжелых металлов в побегах рукколы через 50 дней после посева. Субстраты, обогащенные биоуглем, повлияли на макро- и микроэлементы. Низкие концентрации биоугля в субстратах (10% по объему) привели к небольшому увеличению Ca по сравнению с контролем (+17,36%), в то время как при содержании биоугля > 20% по объему наблюдалось снижение (−23,75%). И наоборот, существенных изменений в содержании Fe и K между обработками не отмечено. Существенное увеличение Na было обнаружено в субстратах на основе биоугля, при этом BC20 показал самое высокое накопление (12,15 ± 0,43 г кг−1 сух. масса), а контроль (BC0) — самое низкое (8,24 ± 0,26 мг/кг сух. масса). Низкие концентрации биоугля (BC5) не показали различий по сравнению с контролем, в то время как более высокие концентрации (BC10, BC20 и BC40) дали листья, более богатые Na. Аналогичная тенденция наблюдалась в накоплении Mg в листьях, содержание которого было выше в субстратах, обогащенных биоуглем, по сравнению с контролем (3,67 ± 0,40 г кг−1). И наоборот, небольшое значительное снижение наблюдалось для содержания P в листьях рукколы с увеличением количества биоугля. Никаких различий не наблюдалось между BC0 и BC5, в то время как снижение P было обнаружено при содержании биоугля > 5%. Мышьяк, Cd, V и Cr не были обнаружены в листьях рукколы. Значительных расхождений в содержании Cu не обнаружено. Действительно, BC10, BC20 и BC40 показали схожие значения (4,24 ± 0,47; 2,82 ± 0,27 и 3,91 ± 0,92 мг кг−1 сух. масса соответственно) по сравнению с контролем (4,82 ± 1,1 мг кг−1 сух. масса); BC5 показал самое низкое значение (2,73 ± 0,43 мг кг−1 сух. масса), но оно было статистически схожим с другими. Различий в содержании Ni между различными средами, обогащенными биоуглем, не наблюдалось. И наоборот, содержание Zn увеличивалось с увеличением концентрации биоугля, достигнув самого высокого значения в BC40 (24,35 ± 2,20 мг кг−1 сух. масса). Значительных изменений в содержании Mn в листьях рукколы не обнаружено.
Таблица 3. Минеральный состав и содержание тяжелых металлов в растениях рукколы, выращенных на субстратах, обогащенных биоуглем. Приведены средние значения и стандартные отклонения (в скобках). Разные буквы в одной строке представляют значительные различия между обработками (p < 0,05) с использованием теста Краскела-Уоллиса и непараметрического теста Данна.
3.5. Содержание хлорофилла, флавонолов, нитратов и цвет листьев
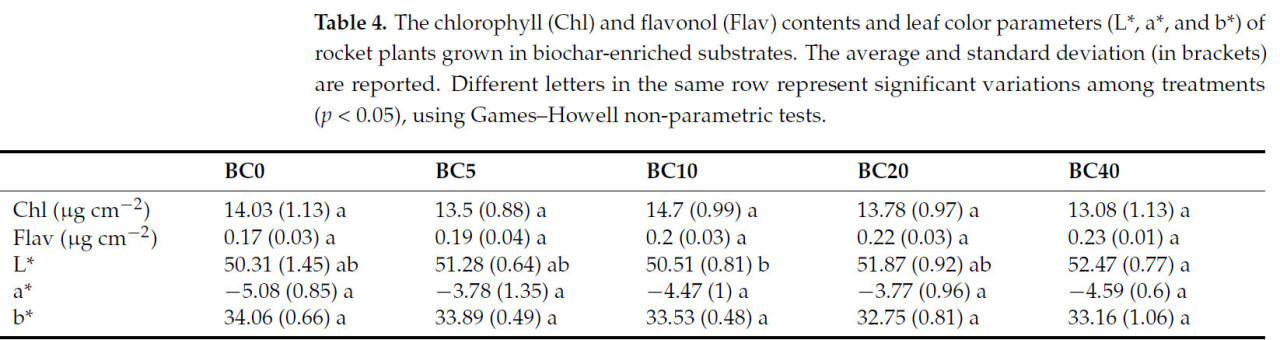
Никаких существенных различий в содержании хлорофилла и флавонолов между субстратами, обогащенными биоуглем, по сравнению с контролем не наблюдалось (Таблица 4). Концентрация хлорофилла варьировала от 13,78 ± 1,13 мкг см−2 (BC40) до 14,7 ± 0,99 мкг см−2 (BC10), а флавонолов — от 0,17 ± 0,03 мкг см−2 (BC0) до 0,23 ± 0,01 мкг см−2 (BC40). И наоборот, были обнаружены небольшие различия в светимости (L), при этом самое высокое значение (52,47 ± 0,77) обнаружено в BC40, а самое низкое (50,51 ± 00,81) — в BC10. Для других параметров цвета (a и b) изменений не обнаружено.
Таблица 4. Содержание хлорофилла (Chl) и флавонолов (Flav), а также параметры цвета листьев (L, a и b) растений рукколы, выращенных на субстратах, обогащенных биоуглем. Приведены средние значения и стандартные отклонения (в скобках). Разные буквы в одной строке представляют значительные различия между обработками (p < 0,05) с использованием непараметрических тестов Геймса-Хауэлла.
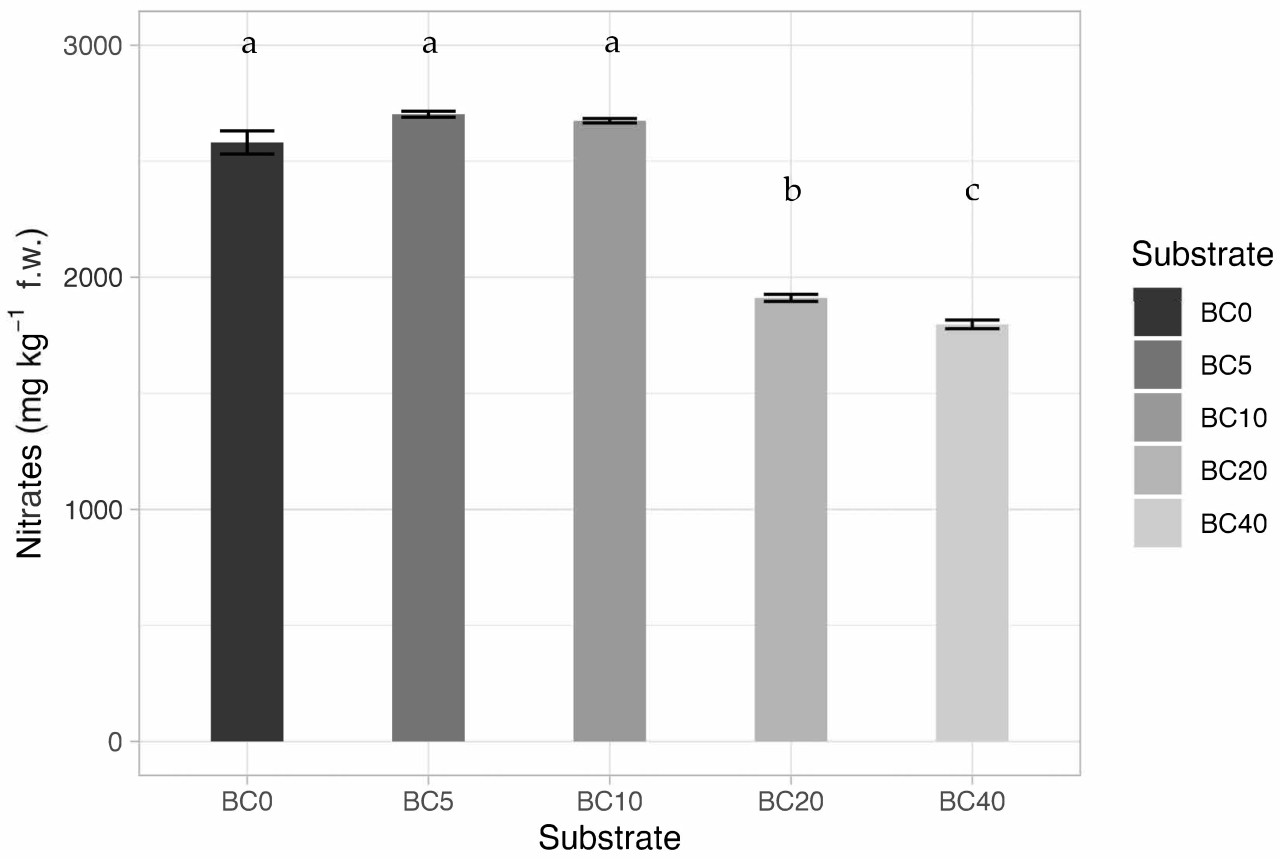
Значительные различия наблюдались для содержания нитратов (Рисунок 1). Более подробно, увеличение содержания биоугля в субстратах (≥20% по объему) привело к снижению концентрации нитратов в листьях рукколы. Самое высокое значение наблюдалось в BC5 (2702,61 ± 12,9 мг кг−1 сыр. масса), а самое низкое — в BC40 (1797,13 ± 18,69 мг кг−1 сыр. масса). Наблюдалась следующая тенденция: BC5 > BC0 > BC10 > BC20 > BC40. В любом случае, все значения соответствовали пороговому значению, установленному Регламентом ЕС № 1258/2011 [8] как максимально допустимые уровни для реализации рукколы.
Рисунок 1. Гистограмма, представляющая концентрации нитратов в растениях рукколы, выращенных на различных субстратах, обогащенных биоуглем. Разные буквы в одной строке представляют значительные различия между обработками (p < 0,05) с использованием непараметрических тестов Геймса-Хауэлла.
3.6. Многомерный анализ
Многомерный подход был сосредоточен на построении биплота метода главных компонент (PCA). Переменные растений были в первую очередь отобраны для определения избыточных признаков, которые показали коэффициент корреляции Пирсона ≥0,95 (Рисунок S1). В частности, десять переменных были удалены из общего числа 31 признака, рассматриваемого в корреляции. В этом контексте высокая корреляция (r > 0,95) наблюдалась между биометрическими параметрами, такими как длина листовой пластинки (BL), длина черешка (PL), площадь листьев (LA) и удельная площадь листьев (SLA), которые были связаны с сырой массой (FW). Кроме того, признаки прорастания сильно зависели друг от друга. Действительно, сильная корреляция (r = 0,95) была обнаружена между последним временем прорастания (LastGermTime) и временным разбросом прорастания (TimeSpreadGerm). Аналогично, t50total и Dlag50 были чрезвычайно связаны с MGT. Наконец, замечательная связь была обнаружена между Fe и хлорофиллом (r = 0,97), а также S (r = 0,98), и между параметрами цвета P и b (r = 0,95).
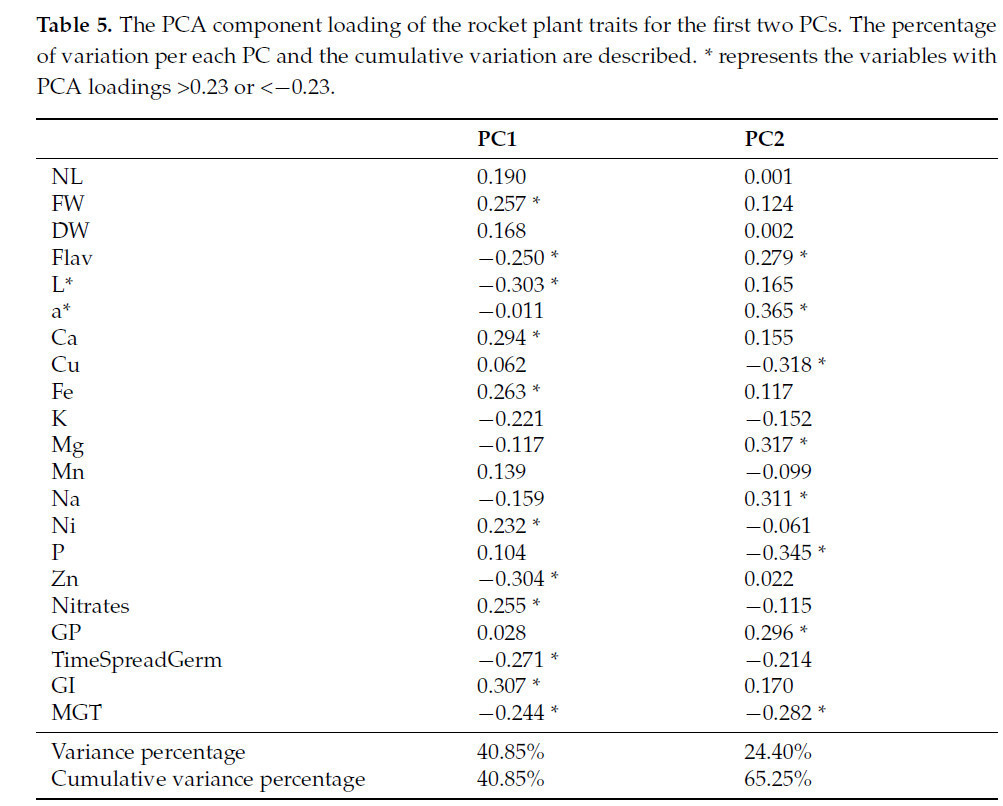
PCA был проведен с использованием средних и стандартизированных значений каждой отобранной переменной. Большая часть общей вариации (т.е. 83,87%) была объяснена первыми тремя компонентами (PC1, PC2 и PC3), которые составили 40,85%, 24,40% и 18,62% изменчивости соответственно. В таблице 5 представлены нагрузки PCA для первых двух компонентов. PC1 оказался положительно коррелирован с FW, содержанием металлов (Fe и Ni), а также нитратами и индексом прорастания (GI). И наоборот, параметры прорастания, связанные со временем (т.е. TimeSpreadGerm и MGT), были отрицательно связаны с PC1, как и K, Zn, флавонолы и светимость цвета (L). PC2 был сильно связан с флавонолами, Gp, Mg и Na, в то время как отрицательно коррелировал с Cu, P и MGT.
Таблица 5. Нагрузки компонентов PCA для признаков растений рукколы по первым двум главным компонентам. Описаны процент вариации для каждой главной компоненты и совокупная вариация. представляет переменные с нагрузками PCA >0,23 или <−0,23.
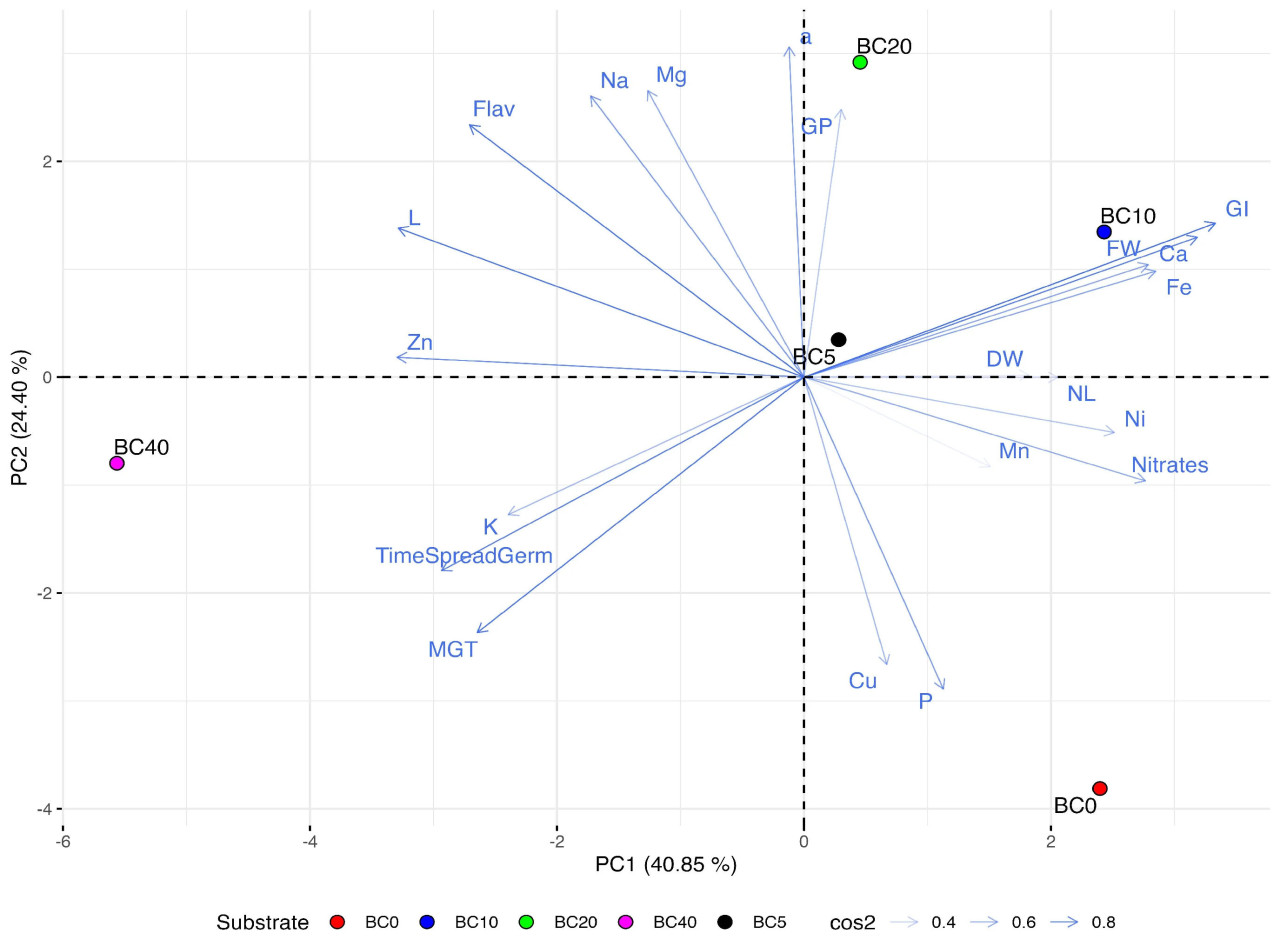
Основываясь на первых двух компонентах, многомерный анализ четко разделил обработку на основе добавления биоугля в субстрат, как показано на биплоте PCA (Рисунок 2). Более подробно, контрольная группа (BC0) располагалась в нижнем правом квадранте биплота, указывая на положительную связь с PC1, определяемую нитратами и FW, и отрицательную корреляцию с PC2, обусловленную в первую очередь содержанием P и Cu. Обработка BC5 была ближе всего к BC0, не показывая влияния ни PC1, ни PC2, находясь около центра начала координат графика. BC10 располагался в верхнем правом квадранте, положительно связанный как с PC1, так и с PC2, отражая его корреляцию с такими переменными, как нитраты, Ca, FW, Fe и GI. И наоборот, BC20 положительно зависел только от PC2 и в основном коррелировал с GP и параметром цвета a, и отрицательно связан с Cu и P. Субстраты BC5, BC10 и BC20 оказались близки друг к другу, располагаясь в одном квадранте. Наконец, BC40 был наиболее удаленной обработкой от других, находясь в нижнем левом квадранте, и был сильно связан с параметрами прорастания, зависящими от времени (например, TimeSpreadGerm, MGT), содержанием Zn и светимостью цвета (L).
Рисунок 2. Биплот PCA пяти субстратов, обогащенных биоуглем, с учетом признаков растений.
4. Обсуждение
Существует много исследований по гидропонному выращиванию Eruca vesicaria [9,52,53], но несколько работ сфокусировали свои тесты на беспочвенном культивировании с использованием биоугля в качестве добавки к субстрату. В частности, насколько нам известно, это первое исследование, в котором оценивается прорастание семян рукколы и показатели растений на субстратах с высоким содержанием биоугля (>15%). Более того, в литературе [54] встречается мало информации о содержании минеральных веществ в рукколе, выращенной на средах, обогащенных биоуглем.
Наше исследование продемонстрировало, что концентрация биоугля до 40% в качестве добавки к субстрату (BC40) не влияет на прорастание семян рукколы. Этот результат не согласуется с выводами Milone и др. [35], в которых концентрации биоугля 2,5% и 5% вызвали снижение прорастания семян. И наоборот, наши результаты согласуются с Sanchez и др. [28], которые получили прорастание семян рукколы ≥80% на субстратах из засоленной почвы и различных концентраций биоугля (т.е. 5%, 10% и 15%). Процент прорастания, наблюдаемый в нашем исследовании, составлял >80% и был аналогичен контролю во всех субстратах, обогащенных биоуглем, вплоть до 40%. И наоборот, более высокие концентрации биоугля (BC = 70% по объему) вызвали резкое снижение GP. Эти выводы согласуются с наблюдениями Carril и др. [55] на томатах и базилике, где было отмечено снижение скорости и индексов прорастания при концентрациях твердой фракции биоугля ≥50% (по объему). Во многих статьях сообщалось, что на прорастание влияет EC, и биоуголь может влиять на этот параметр из-за высокого содержания растворимых солей (например, Na+ и Cl−) [56]. Это может снизить доступность ключевых растворимых питательных веществ (таких как NO3−, K+), что приведет к дисбалансу питательных веществ и снижению осмотического потенциала растений [57,58]. Carrill и др. [55] также утверждали, что профилактические промывки биоугля могут снизить pH и EC, оказывая положительное влияние на прорастание. Наши результаты подтвердили, что биоуголь в количестве до 40% может заменить торф при выращивании в горшках, не влияя на развитие семян.
Что касается биометрических параметров растений, урожайность рукколы (г/растение) согласовывалась с результатами, полученными Fontana и Nicola [9] при культивировании рукколы в беспочвенной плавающей системе. Аналогичные результаты наблюдались также в других исследованиях, представленных Nicola и др. [53]. Наши результаты показали, что умеренные концентрации биоугля (до 20% по объему) не влияют на рост рукколы. В литературе сообщается о многих различных результатах относительно влияния биоугля на растения этого вида. Zabaleta и др. [27] показали увеличение высоты растений с увеличением концентрации биоугля из скорлупы миндаля (до 15%) через 60 дней после посева, в то время как Milone и др. [35] наблюдали, что увеличение содержания биоугля из бамбука в субстрате вызывало снижение этого параметра. Наши результаты больше согласуются с Zabaleta и др. [27]: умеренные концентрации биоугля не влияют на показатели растений или даже увеличивают их. Однако стоит упомянуть, что в исследовании Milone и др. [35] на редисе использование той же концентрации бамбукового биоугля не дало никакого эффекта. Таким образом, действие конкретного биоугля может зависеть от вида. В нашем исследовании было отмечено небольшое снижение урожайности и показателей рукколы в горшках с концентрацией биоугля 40% по объему. Предыдущих исследований с использованием рукколы и содержанием биоугля >15% не проводилось; однако Shen и др. [59] наблюдали аналогичную тенденцию в росте растений сяо бай цай (Brassica rapa cv. Group Pak Choi Green-petioled Form), который принадлежит к тому же семейству, что и E. vesicaria (т.е. Brassicaceae). В частности, авторы зафиксировали наилучшие показатели растений (сырую массу) сяо бай цай при содержании биоугля ~20–30%, в то время как рост снижался с увеличением содержания биоугля (>30%), что согласуется с нашими результатами.
Тип субстрата и его органическое вещество влияют не только на качество субстрата и продуктивность сельскохозяйственных культур, но и на пищевую ценность продуктов, влияя на содержание в них минералов, витаминов, антиоксидантов и фенольных соединений [60]. Минералы необходимы для поддержки широкого спектра биологических активностей на разных этапах роста и развития растений [61]. Общие концентрации минералов (макро- и микроэлементов) в коммерческих съедобных листьях рукколы, обнаруженные в этой работе, сопоставимы с теми, о которых сообщалось в предыдущих работах [52,62]. Увеличение концентрации биоугля в субстратах привело к снижению содержания P в листьях рукколы. Однако в некоторых исследованиях утверждается, что доступность P резко возрастает при внесении биоугля в почву или субстраты [63]. Тем не менее, важно отметить, что на доступность P влияют изменения pH и состава почвы, главным образом содержание кальция, что может оказывать негативное влияние на поглощение P [64,65]. Эти соображения согласуются с нашими результатами, так как в субстратах, обогащенных биоуглем, наблюдалось увеличение Ca, в то время как в листьях рукколы было обнаружено снижение P. Кроме того, мы заметили увеличение концентрации Mg (+30–35%) в субстратах, обогащенных биоуглем. Аналогичный результат наблюдали Farangi-Abriz и Ghassemi-Golezani [66], которые обнаружили повышение содержания Mg в листьях как сафлора, так и мяты (+41% и +63% Mg соответственно). Доступность магния может быть связана с pH субстрата, при этом более низкие уровни pH снижают его доступность [67]. Таким образом, поскольку внесение биоугля обычно повышает pH почвы, магний становится более доступным для растений [68]. Концентрации тяжелых металлов, о которых сообщается в нашем исследовании, сопоставимы с наблюдаемыми в предыдущих исследованиях по рукколе [1,52,62]. Хотя субстраты, обогащенные биоуглем, содержали более высокие уровни Ni, различий в концентрациях Ni в листьях рукколы не наблюдалось. Таким образом, биоуголь не повлиял на поглощение Ni, подтверждая тенденцию, наблюдавшуюся в плодах томата при использовании тех же концентраций биоугля [38]. И наоборот, значительное и небольшое увеличение Zn (+30%) наблюдалось в BC40 по сравнению с контролем BC0. В любом случае, это значение соответствовало количеству Zn, обычно обнаруживаемому в коммерческих листьях рукколы [62]. Однако это увеличение содержания Zn может быть связано с более низкой урожайностью, обнаруженной в BC40. Действительно, корреляционный график (Рисунок S1) показал сильную отрицательную корреляцию между FW и Zn (r = −0,86), что привело к сильному влиянию Zn в BC40, как дополнительно показано PCA (Рисунок 2). Эти результаты свидетельствуют о том, что культивирование и производство рукколы можно осуществлять, добавляя до 20% древесного биоугля в торфяной субстрат, не влияя на рост растений и содержание минеральных веществ. Существенных изменений в содержании хлорофилла и флавонолов или признаках цвета листьев не наблюдалось, за исключением значительного увеличения светимости цвета в BC40.
В листовых овощах категории "бэби-лист", таких как салат латук, руккола, цикорий и шпинат, одним из критических параметров с точки зрения качества и безопасности пищевой продукции является концентрация нитратов в листьях [69]. Эти виды овощей являются основными источниками поступления нитратов с пищей, составляя приблизительно 40–92% от суточного потребления [70]. Чрезмерная концентрация нитратов в овощах обычно считается негативным фактором качества [5] и опасна для здоровья человека [6]. Действительно, сами нитраты не вредны, но их превращение в нитриты в организме представляет риск для здоровья, включая образование канцерогенных нитрозаминов и метгемоглобина. Последний может привести к кислородной недостаточности, особенно у новорожденных, вызывая «синдром голубого ребенка» [6]. Поэтому Всемирная организация здравоохранения (ВОЗ) установила допустимое суточное потребление (ДСП) нитратов на уровне 3,7 мг на кг массы тела [71]. Среди листовых овощей категории "бэби-лист" руккола особенно известна своей способностью накапливать нитраты, причем на уровни влияют такие факторы, как доступность нитратов в почве, методы культивирования, время года и условия окружающей среды [72]. В этом исследовании наблюдалось снижение содержания нитратов с увеличением содержания биоугля в субстратах. В частности, наши результаты выявили снижение уровня нитратов примерно на 26–30% в обработках BC20 и BC40 по сравнению с контролем. Аналогично, снижение содержания нитратов наблюдалось у генотипов капусты с увеличением концентраций биоугля в субстрате [73]. Этот эффект был связан с улучшенными свойствами субстрата, вызванными биоуглем, который обогащает такие элементы, как C, N, O, S и Ca. Повышенные уровни C и N не только улучшают эффективность использования питательных веществ и питательное качество урожая, но и способствуют общему плодородию почвы [73]. Кроме того, характеристики биоугля (т.е. большая площадь поверхности, высокая пористость и катионообменная емкость) делают его эффективным кондиционером почвы, изменяя физико-химические и микробные свойства субстрата для повышения эффективности использования питательных веществ в системах почва/растение [74,75]. В этом конкретном контексте Saffeullah и др. [73] продемонстрировали, что биоуголь из древесины Prosopis может улучшить активность N-метаболизирующих ферментов и, следовательно, повысить эффективность использования азота за счет уменьшения вымывания нитратов и содержания нитратов в листьях капусты. Наше исследование также подтвердило увеличение CEC и пористости субстрата, поддерживая предположение о том, что биоуголь может минимизировать потери N в субстратах, повысить эффективность использования питательных веществ, и особенно в отношении нитратов, снижая их содержание в листьях рукколы. Аналогичные выводы были представлены Haider и др. [76], которые наблюдали снижение уровня нитратов в тканях при внесении биоугля. Основываясь на наших результатах, применение умеренных концентраций биоугля, таких как 20%, в торфяном субстрате не оказывает негативного влияния на прорастание семян и рост растений рукколы, а также улучшает качество листьев за счет снижения концентрации нитратов.
5. Выводы
Беспочвенные системы культивирования широко используются для выращивания листовых овощей категории "бэби-лист", таких как Eruca vesicaria, благодаря эффективному управлению субстратами, водой, питанием растений и условиями окружающей среды, а также их способности смягчать накопление нитратов и болезни. Однако зависимость от торфа как питательной среды вызывает озабоченность в отношении устойчивости, поскольку добыча торфа высвобождает значительное количество CO2 в атмосферу. В этом исследовании изучался потенциал включения биоугля в различных концентрациях в торфяные субстраты для культивирования рукколы.
Наши результаты показали, что концентрации биоугля до 40% по объему не влияют на прорастание семян по сравнению с коммерческим торфяным контролем. Однако более высокие уровни биоугля (70% по объему) значительно снизили как прорастание, так и развитие растений. Умеренные добавки биоугля (до 20% по объему) поддерживали рост растений и содержание минеральных веществ на уровне, сопоставимом с контролем, в то время как более высокие концентрации (40% по объему) отрицательно сказались на росте и увеличили уровни тяжелых металлов, таких как Zn, в субстрате. Примечательно, что высокие уровни биоугля снизили накопление нитратов в листьях рукколы, возможно, благодаря усилению активности N-метаболизирующих ферментов и улучшению эффективности использования азота.
Насколько нам известно, это исследование является первым, в котором оценивается влияние высоких концентраций биоугля (>15% по объему) в торфяных субстратах для рукколы, что дает ценную информацию для более устойчивых методов культивирования, одновременно решая экологические проблемы, связанные с торфом.
Дополнительные материалы
Следующие вспомогательные материалы можно загрузить по адресу: https://www.mdpi.com/article/10.3390/agriculture15030302/s1, Рисунок S1: Корреляционный график на основе коэффициента корреляции Пирсона (r) для признаков растений рукколы; Таблица S1. Физико-химические характеристики субстратов, обогащенных биоуглем, использованных в этом исследовании, с пороговыми пределами, установленными региональным, национальным и европейским законодательством. Средние значения и стандартные отклонения (в скобках) для BC0, BC5, BC10, BC20 и BC40 опубликованы в Bini и др. [38].
Ссылки
1. Tripodi, P.; Francese, G.; Mennella, G. Rocket Salad: Crop Description, Bioactive Compounds and Breeding Perspectives. Adv. Hortic. Sci. 2017, 31, 107–113. [Google Scholar] [CrossRef]
2. Martínez-Sánchez, A.; Luna, M.C.; Selma, M.V.; Tudela, J.A.; Abad, J.; Gil, M.I. Baby-Leaf and Multi-Leaf of Green and Red Lettuces Are Suitable Raw Materials for the Fresh-Cut Industry. Postharvest Biol. Technol. 2012, 63, 1–10. [Google Scholar] [CrossRef]
3. Martínez-Ispizua, E.; Calatayud, Á.; Marsal, J.I.; Cannata, C.; Basile, F.; Abdelkhalik, A.; Soler, S.; Valcárcel, J.V.; Martínez-Cuenca, M.-R. The Nutritional Quality Potential of Microgreens, Baby Leaves, and Adult Lettuce: An Underexploited Nutraceutical Source. Foods 2022, 11, 423. [Google Scholar] [CrossRef] [PubMed]
4. Hetta, M.H.; Owis, A.I.; Haddad, P.S.; Eid, H.M. The Fatty Acid-Rich Fraction of Eruca sativa (Rocket Salad) Leaf Extract Exerts Antidiabetic Effects in Cultured Skeletal Muscle, Adipocytes and Liver Cells. Pharm. Biol. 2017, 55, 810–818. [Google Scholar] [CrossRef] [PubMed]
5. Liang, G.; Zhang, Z. Reducing the Nitrate Content in Vegetables Through Joint Regulation of Short-Distance Distribution and Long-Distance Transport. Front. Plant Sci. 2020, 11, 1079. [Google Scholar] [CrossRef]
6. Santamaria, P. Nitrate in Vegetables: Toxicity, Content, Intake and EC Regulation. J. Sci. Food Agric. 2006, 86, 10–17. [Google Scholar] [CrossRef]
7. EFSA Panel on Contaminants in the Food Chain (CONTAM). Statement on Possible Public Health Risks for Infants and Young Children from the Presence of Nitrates in Leafy Vegetables. EFSA J. 2010, 8, 1935. [Google Scholar]
8. The European Commission. Commission Regulation (EU) No 1258/2011 of 2 December 2011 Amending Regulation (EC) No 1881/2006 as Regards Maximum Levels for Nitrates in Foodstuffs (Text with EEA Relevance). Available online: https://Faolex.Fao.Org/Docs/Pdf/Eur108181.Pdf (accessed on 6 September 2024).
9. Fontana, E.; Nicola, S. Traditional and Soilless Culture Systems to Produce Corn Salad (Valerianella olitoria L.) and Rocket (Eruca sativa Mill.) with Low Nitrate Content. J. Food Agric. Environ. 2009, 7, 405–410. [Google Scholar]
10. Fussy, A.; Papenbrock, J. An Overview of Soil and Soilless Cultivation Techniques—Chances, Challenges and the Neglected Question of Sustainability. Plants 2022, 11, 1153. [Google Scholar] [CrossRef]
11. Méndez, A.; Cárdenas-Aguiar, E.; Paz-Ferreiro, J.; Plaza, C.; Gasco, G. The Effect of Sewage Sludge Biochar on Peat-Based Growing Media. Biol. Agric. Hortic. 2017, 33, 40–51. [Google Scholar] [CrossRef]
12. Barrett, G.E.; Alexander, P.D.; Robinson, J.S.; Bragg, N.C. Achieving Environmentally Sustainable Growing Media for Soilless Plant Cultivation Systems—A Review. Sci. Hortic. 2016, 212, 220–234. [Google Scholar] [CrossRef]
13. Ferrarezi, R.S.; Lin, X.; Gonzalez Neira, A.C.; Tabay Zambon, F.; Hu, H.; Wang, X.; Huang, J.-H.; Fan, G. Substrate pH Influences the Nutrient Absorption and Rhizosphere Microbiome of Huanglongbing-Affected Grapefruit Plants. Front. Plant Sci. 2022, 13, 856937. [Google Scholar] [CrossRef] [PubMed]
14. Ahmed, N.; Zhang, B.; Chachar, Z.; Li, J.; Xiao, G.; Wang, Q.; Hayat, F.; Deng, L.; Bozdar, B.; Tu, P. Micronutrients and Their Effects on Horticultural Crop Quality, Productivity and Sustainability. Sci. Hortic. 2024, 323, 112512. [Google Scholar] [CrossRef]
15. Mall, M.; Kumar, R.; Akhtar, M.Q. Horticultural Crops and Abiotic Stress Challenges. In Stress Tolerance in Horticultural Crops; Elsevier: Amsterdam, The Netherlands, 2021; pp. 1–19. [Google Scholar]
16. Schmilewski, G. The Role of Peat in Assuring the Quality of Growing Media. Mires Peat 2008, 3, 2. [Google Scholar]
17. Tietjen, S.; Graubner, I.; Sradnick, A. Reducing Peat in Substrate Mixture Formulations for Press Pots Using the Taguchi Method. Sci. Hortic. 2022, 295, 110838. [Google Scholar] [CrossRef]
18. Blok, C.; Eveleens, B.; Van Winkel, A. Growing Media for Food and Quality of Life in the Period 2020–2050. Acta Hortic. 2019, 1305, 341–356. [Google Scholar] [CrossRef]
19. Clarke, D.; Rieley, J. Strategy for Responsible Peatland Management; International Peatland Society: Jyväskylä, Finland, 2010; ISBN 9529940122. [Google Scholar]
20. Loisel, J.; Gallego-Sala, A. Ecological Resilience of Restored Peatlands to Climate Change. Commun. Earth Environ. 2022, 3, 208. [Google Scholar] [CrossRef]
21. Chrysargyris, A.; Prasad, M.; Tzortzakis, N. Wood-Based Biochar Ratio Used for Partial Peat Replacement in Growing Media for Antirrhinum Majus Pot Production. Agriculture 2024, 14, 1860. [Google Scholar] [CrossRef]
22. Del Bubba, M.; Anichini, B.; Bakari, Z.; Bruzzoniti, M.C.; Camisa, R.; Caprini, C.; Checchini, L.; Fibbi, D.; El Ghadraoui, A.; Liguori, F. Physicochemical Properties and Sorption Capacities of Sawdust-Based Biochars and Commercial Activated Carbons Towards Ethoxylated Alkylphenols and Their Phenolic Metabolites in Effluent Wastewater from a Textile District. Sci. Total Environ. 2020, 708, 135217. [Google Scholar] [CrossRef]
23. Wood, R.; Mašek, O.; Erastova, V. Developing a Molecular-Level Understanding of Biochar Materials Using Public Characterization Data. Cell Rep. Phys. Sci. 2024, 5, 102036. [Google Scholar] [CrossRef]
24. Das, S.K.; Ghosh, G.K. Development and Evaluation of Biochar-Based Secondary and Micronutrient Enriched Slow Release Nano-Fertilizer for Reduced Nutrient Losses. Biomass Convers. Biorefin 2023, 13, 12193–12204. [Google Scholar] [CrossRef]
25. Allohverdi, T.; Mohanty, A.K.; Roy, P.; Misra, M. A Review on Current Status of Biochar Uses in Agriculture. Molecules 2021, 26, 5584. [Google Scholar] [CrossRef] [PubMed]
26. Linam, F.; Limmer, M.A.; Ebling, A.M.; Seyfferth, A.L. Rice Husk and Husk Biochar Soil Amendments Store Soil Carbon While Water Management Controls Dissolved Organic Matter Chemistry in Well-Weathered Soil. J. Environ. Manag. 2023, 339, 117936. [Google Scholar] [CrossRef] [PubMed]
27. Zabaleta, R.; Sánchez, E.; Fabani, P.; Mazza, G.; Rodriguez, R. Almond Shell Biochar: Characterization and Application in Soilless Cultivation of Eruca sativa. Biomass Convers. Biorefin 2024, 14, 18183–18200. [Google Scholar] [CrossRef]
28. Sánchez, E.; Zabaleta, R.; Fabani, M.P.; Rodriguez, R.; Mazza, G. Effects of the Amendment with Almond Shell, Bio-Waste and Almond Shell-Based Biochar on the Quality of Saline-Alkali Soils. J. Environ. Manag. 2022, 318, 115604. [Google Scholar] [CrossRef]
29. Massa, D.; Bonetti, A.; Cacini, S.; Faraloni, C.; Prisa, D.; Tuccio, L.; Petruccelli, R. Soilless Tomato Grown Under Nutritional Stress Increases Green Biomass but Not Yield or Quality in Presence of Biochar as Growing Medium. Hortic. Environ. Biotechnol. 2019, 60, 871–881. [Google Scholar] [CrossRef]
30. Petruccelli, R.; Bonetti, A.; Traversi, M.L.; Faraloni, C.; Valagussa, M.; Pozzi, A. Influence of Biochar Application on Nutritional Quality of Tomato (Lycopersicon esculentum). Crop Pasture Sci. 2015, 66, 747–755. [Google Scholar] [CrossRef]
31. Simiele, M.; Argentino, O.; Baronti, S.; Scippa, G.S.; Chiatante, D.; Terzaghi, M.; Montagnoli, A. Biochar Enhances Plant Growth, Fruit Yield, and Antioxidant Content of Cherry Tomato (Solanum lycopersicum L.) in a Soilless Substrate. Agriculture 2022, 12, 1135. [Google Scholar] [CrossRef]
32. Yu, P.; Huang, L.; Li, Q.; Lima, I.M.; White, P.M.; Gu, M. Effects of Mixed Hardwood and Sugarcane Biochar as Bark-Based Substrate Substitutes on Container Plants Production and Nutrient Leaching. Agronomy 2020, 10, 156. [Google Scholar] [CrossRef]
33. Awad, Y.M.; Lee, S.-E.; Ahmed, M.B.M.; Vu, N.T.; Farooq, M.; Kim, I.S.; Kim, H.S.; Vithanage, M.; Usman, A.R.A.; Al-Wabel, M. Biochar, a Potential Hydroponic Growth Substrate, Enhances the Nutritional Status and Growth of Leafy Vegetables. J. Clean. Prod. 2017, 156, 581–588. [Google Scholar] [CrossRef]
34. Parlavecchia, M.; Carnimeo, C.; Loffredo, E. Soil Amendment with Biochar, Hydrochar and Compost Mitigates the Accumulation of Emerging Pollutants in Rocket Salad Plants. Water Air Soil. Pollut. 2020, 231, 554. [Google Scholar] [CrossRef]
35. Milone, J.; Casas, C.; Vega, A.S. Guadua chacoensis Bamboo Biochar (Poaceae, Bambuseae) Affected Horticultural Species in a Saline-Alkaline Soil. Cienc. Suelo 2023, 41, 273–284. [Google Scholar]
36. Batta, N.; Heuchan, S.M.; Stokes-Rees, J.; Moreira, C.; Berruti, F. Production of Biochar for Treatment of Retting Effluents and Utilization of Spent Biochar as Potential Germination Medium for Leafy Greens. Biomass Bioenergy 2024, 186, 107266. [Google Scholar] [CrossRef]
37. Sun, R.; Wang, J.; Peng, Y.; Wang, H.; Chen, Q. Mitigation of Arsenic Accumulation in Arugula (Eruca sativa Mill.) Using. Fe/Al/Zn Impregnated Biochar Composites. Environ. Sci. Pollut. Res. 2021, 28, 4136–4146. [Google Scholar]
38. Bini, L.; Renai, L.; Fichera, M.; Petrucci, W.A.; Lenzi, A.; Biricolti, S.; Giordani, E.; Rivoira, L.; Bruzzoniti, M.C.; Piesik, D. Assessing the Impact of Sustainable Biochar-Enriched Substrates on Safety and Quality of Tomato (Solanum lycopersicum L.) as Relevant Model Crop. ACS Agric. Sci. Technol. 2024, 4, 681–689. [Google Scholar]
39. El-Kassaby, Y.A.; Moss, I.; Kolotelo, D.; Stoehr, M. Seed Germination: Mathematical Representation and Parameters Extraction. For. Sci. 2008, 54, 220–227. [Google Scholar] [CrossRef]
40. Ellis, R.H.; Roberts, E.H. Improved Equations for the Prediction of Seed Longevity. Ann. Bot. 1980, 45, 13–30. [Google Scholar]
41. Wardle, D.A.; Ahmed, M.; Nicholson, K.S. Allelopathic Influence of Nodding Thistle (Carduus nutans L.) Seeds on Germination and Radicle Growth of Pasture Plants. N. Z. J. Agric. Res. 1991, 34, 185–191. [Google Scholar]
42. Melville, A.H.; Galletta, G.J.; Draper, A.D.; Ng, T.J. Seed Germination and Early Seedling Vigor in Progenies of Inbred Strawberry Selections. HortScience 1981, 15, 749–750. [Google Scholar]
43. Aravind, J.; Vimala, D.; Radharani, J.; Jacob, S.R.; Srinivasa, K. The Germinationmetrics Package: A Brief Introduction; ICAR-National Bureau of Plant Genetic Resources: New Delhi, India, 2019; pp. 1–62. [Google Scholar]
44. Rodríguez, G.R.; Moyseenko, J.B.; Robbins, M.D.; Morejón, N.H.; Francis, D.M.; van der Knaap, E. Tomato Analyzer: A Useful Software Application to Collect Accurate and Detailed Morphological and Colorimetric Data from Two-Dimensional Objects. J. Vis. Exp. 2010, 37, 1856. [Google Scholar]
45. Cataldo, D.A.; Schrader, L.E.; Youngs, V.L. Analysis by Digestion and Colorimetric Assay of Total Nitrogen in Plant Tissues High in Nitrate 1. Crop Sci. 1974, 14, 854–856. [Google Scholar]
46. DIN ISO 11466:1995-03; Soil Quality—Extraction of Trace Elements Soluble in Aqua Regia. International Organization for Standardization: Geneva, Switzerland, 1995.
47. Dinno, A. Package ‘Dunn. Test’. CRAN 2017. [Google Scholar] [CrossRef]
48. Kassambara, A. Pipe-Friendly Framework for Basic Statistical Tests [R Package Rstatix Version 0.7.0]; Free Software Foundation Inc.: Boston, MA, USA, 2021. [Google Scholar]
49. Wei, T.; Simko, V.R. Package “Corrplot”: Visualization of a Correlation Matrix (Version 0.88). Available online: https://github.com/taiyun/corrplot (accessed on 20 September 2024).
50. Lê, S.; Josse, J.; Husson, F. FactoMineR: An R Package for Multivariate Analysis. J. Stat. Softw. 2008, 25, 1–18. [Google Scholar]
51. Kassambara, A. Factoextra: Extract and Visualize the Results of Multivariate Data Analyses. CRAN 2016. [Google Scholar] [CrossRef]
52. Bulgari, R.; Baldi, A.; Ferrante, A.; Lenzi, A. Yield and Quality of Basil, Swiss Chard, and Rocket Microgreens Grown in a Hydroponic System. N. Z. J. Crop Hortic. Sci. 2017, 45, 119–129. [Google Scholar] [CrossRef]
53. Nicola, S.; Pignata, G.; Casale, M.; Lo Turco, P.E.; Gaino, W. Overview of a Lab-Scale Pilot Plant for Studying Baby Leaf Vegetables Grown in Soilless Culture. Hortic. J. 2016, 85, 97–104. [Google Scholar]
54. Teodoro, M.; Trakal, L.; Gallagher, B.N.; Šimek, P.; Soudek, P.; Pohořelý, M.; Beesley, L.; Jačka, L.; Kovář, M.; Seyedsadr, S.; et al. Application of Co-Composted Biochar Significantly Improved Plant-Growth Relevant Physical/Chemical Properties of a Metal Contaminated Soil. Chemosphere 2020, 242, 125255. [Google Scholar] [CrossRef]
55. Carril, P.; Ghorbani, M.; Loppi, S.; Celletti, S. Effect of Biochar Type, Concentration and Washing Conditions on the Germination Parameters of Three Model Crops. Plants 2023, 12, 2235. [Google Scholar] [CrossRef]
56. Igalavithana, A.D.; Mandal, S.; Niazi, N.K.; Vithanage, M.; Parikh, S.J.; Mukome, F.N.D.; Rizwan, M.; Oleszczuk, P.; Al-Wabel, M.; Bolan, N. Advances and Future Directions of Biochar Characterization Methods and Applications. Crit. Rev. Environ. Sci. Technol. 2017, 47, 2275–2330. [Google Scholar]
57. Mumme, J.; Getz, J.; Prasad, M.; Lüder, U.; Kern, J.; Mašek, O.; Buss, W. Toxicity Screening of Biochar-Mineral Composites Using Germination Tests. Chemosphere 2018, 207, 91–100. [Google Scholar]
58. Prapagdee, S.; Tawinteung, N. Effects of Biochar on Enhanced Nutrient Use Efficiency of Green Bean, Vigna radiata L. Environ. Sci. Pollut. Res. 2017, 24, 9460–9467. [Google Scholar] [CrossRef] [PubMed]
59. Shen, Y.; Song, S.; Thian, B.W.Y.; Fong, S.L.; Ee, A.W.L.; Arora, S.; Ghosh, S.; Li, S.F.Y.; Tan, H.T.W.; Dai, Y.; et al. Impacts of Biochar Concentration on the Growth Performance of a Leafy Vegetable in a Tropical City and Its Global Warming Potential. J. Clean. Prod. 2020, 264, 121678. [Google Scholar] [CrossRef]
60. Wang, S.Y.; Chen, C.-T.; Sciarappa, W.; Wang, C.Y.; Camp, M.J. Fruit Quality, Antioxidant Capacity, and Flavonoid Content of Organically and Conventionally Grown Blueberries. J. Agric. Food Chem. 2008, 56, 5788–5794. [Google Scholar] [CrossRef] [PubMed]
61. Singh, U.M.; Sareen, P.; Sengar, R.S.; Kumar, A. Plant Ionomics: A Newer Approach to Study Mineral Transport and Its Regulation. Acta Physiol. Plant 2013, 35, 2641–2653. [Google Scholar] [CrossRef]
62. Ahmed, I.A.M.; AlJuhaimi, F.; Özcan, M.M.; Uslu, N.; Karrar, E. Effect of Heating Processes on Bioactive Properties, Phenolic Components and Mineral Amounts of Rocket (Eruca sativa Mill.) Leaves. Int. J. Food Sci. Technol. 2024, 59, 4755–4764. [Google Scholar] [CrossRef]
63. Gao, S.; DeLuca, T.H.; Cleveland, C.C. Biochar Additions Alter Phosphorus and Nitrogen Availability in Agricultural Ecosystems: A Meta-Analysis. Sci. Total Environ. 2019, 654, 463–472. [Google Scholar] [CrossRef]
64. Buss, W.; Assavavittayanon, K.; Shepherd, J.G.; Heal, K.V.; Sohi, S. Biochar Phosphorus Release Is Limited by High PH and Excess Calcium. J. Environ. Qual. 2018, 47, 1298–1303. [Google Scholar] [CrossRef]
65. Buss, W.; Bogush, A.; Ignatyev, K.; Masek, O. Unlocking the Fertilizer Potential of Waste-Derived Biochar. ACS Sustain. Chem. Eng. 2020, 8, 12295–12303. [Google Scholar] [CrossRef]
66. Farhangi-Abriz, S.; Ghassemi-Golezani, K. Improving Electrochemical Characteristics of Plant Roots by Biochar Is an Efficient Mechanism in Increasing Cations Uptake by Plants. Chemosphere 2023, 313, 137365. [Google Scholar] [CrossRef]
67. Gunarathne, V.; Mayakaduwa, S.; Vithanage, M. Biochar’s Influence as a Soil Amendment for Essential Plant Nutrient Uptake. In Essential Plant Nutrients: Uptake, Use Efficiency, and Management; Springer: Berlin/Heidelberg, Germany, 2017; pp. 47–67. ISBN 9783319588414. [Google Scholar]
68. Uzoma, K.C.; Inoue, M.; Andry, H.; Fujimaki, H.; Zahoor, A.; Nishihara, E. Effect of Cow Manure Biochar on Maize Productivity under Sandy Soil Condition. Soil. Use Manag. 2011, 27, 205–212. [Google Scholar] [CrossRef]
69. Fontes, P.C.R.; Pereira, P.R.G.; Conde, R.M. Critical Chlorophyll, Total Nitrogen, and Nitrate-Nitrogen in Leaves Associated to Maximum Lettuce Yield. J. Plant Nutr. 1997, 20, 1061–1068. [Google Scholar] [CrossRef]
70. Bahadoran, Z.; Mirmiran, P.; Jeddi, S.; Azizi, F.; Ghasemi, A.; Hadaegh, F. Nitrate and Nitrite Content of Vegetables, Fruits, Grains, Legumes, Dairy Products, Meats and Processed Meats. J. Food Compos. Anal. 2016, 51, 93–105. [Google Scholar] [CrossRef]
71. Signore, A.; Amoruso, F.; Gallegos-Cedillo, V.M.; Gómez, P.A.; Ochoa, J.; Egea-Gilabert, C.; Costa-Pérez, A.; Domínguez-Perles, R.; Moreno, D.A.; Pascual, J.A.; et al. Agro-Industrial Compost in Soilless Cultivation Modulates the Vitamin C Content and Phytochemical Markers of Plant Stress in Rocket Salad (Diplotaxis tenuifolia (L.) DC.). Agronomy 2023, 13, 544. [Google Scholar] [CrossRef]
72. Bonanomi, G.; De Filippis, F.; Zotti, M.; Idbella, M.; Cesarano, G.; Al-Rowaily, S.; Abd-ElGawad, A. Repeated Applications of Organic Amendments Promote Beneficial Microbiota, Improve Soil Fertility and Increase Crop Yield. Appl. Soil. Ecol. 2020, 156, 103714. [Google Scholar] [CrossRef]
73. Saffeullah, P.; Nabi, N.; Zaman, M.B.; Liaqat, S.; Siddiqi, T.O.; Umar, S. Efficacy of Characterized Prosopis Wood Biochar Amendments in Improving Growth, Nitrogen Use Efficiency, Nitrate Accumulation, and Mineral Content in Cabbage Genotypes. J. Soil. Sci. Plant Nutr. 2021, 21, 690–708. [Google Scholar] [CrossRef]
74. Manyà, J.J. Pyrolysis for Biochar Purposes: A Review to Establish Current Knowledge Gaps and Research Needs. Environ. Sci. Technol. 2012, 46, 7939–7954. [Google Scholar] [CrossRef]
75. Shen, Q.; Hedley, M.; Camps Arbestain, M.; Kirschbaum, M.U.F. Can Biochar Increase the Bioavailability of Phosphorus? J. Soil. Sci. Plant Nutr. 2016, 16, 268–286. [Google Scholar] [CrossRef]
76. Haider, G.; Steffens, D.; Moser, G.; Müller, C.; Kammann, C.I. Biochar Reduced Nitrate Leaching and Improved Soil Moisture Content Without Yield Improvements in a Four-Year Field Study. Agric. Ecosyst. Environ. 2017, 237, 80–94. [Google Scholar] [CrossRef]
Bini L, Biricolti S, Lenzi A, Del Bubba M, Petrucci WA, Giordani E. Assessing Seed Germination and Plant Growth of Eruca vesicaria (L.) Cav. Cultivated in Biochar-Enriched Substrates. Agriculture. 2025; 15(3):302. https://doi.org/10.3390/agriculture15030302
Перевод статьи «Assessing Seed Germination and Plant Growth ofEruca vesicaria(L.) Cav. Cultivated in Biochar-Enriched Substrates» авторов Bini L, Biricolti S, Lenzi A, Del Bubba M, Petrucci WA, Giordani E., оригинал доступен по ссылке. Лицензия: CC BY. Изменения: переведено на русский язык
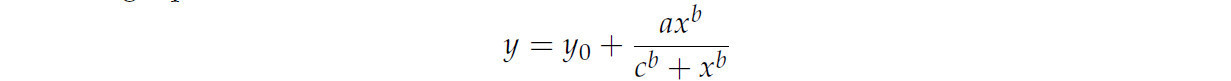
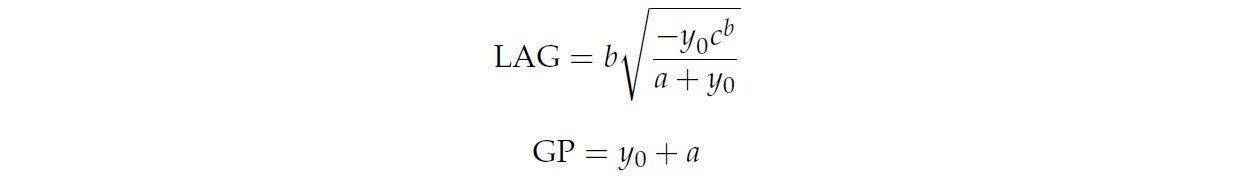
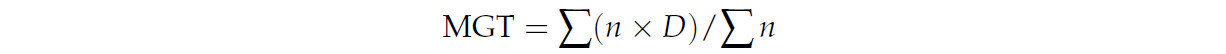
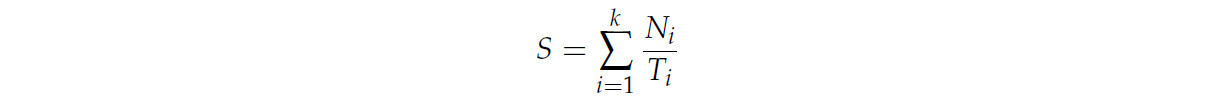
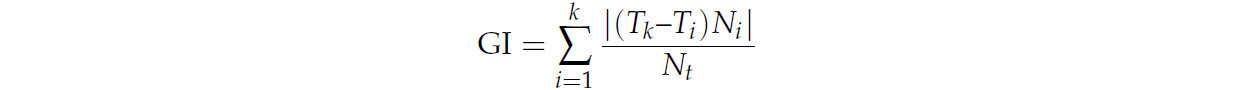













































































































Комментарии (0)