Пробиотики для свиноматок: запуск развития желудка у поросят до и после отъема
Знания о том, как новые антигены или диетические стимулы влияют на развитие и функцию желудка у свиней, остаются ограниченными. Целью данного исследования было изучить характеристики желудка, количество париетальных клеток и экспрессию генов, необходимых для функционирования фундального и пилорического отделов желудка, в момент отъема по сравнению с семью днями после отъема, а также выяснить, влияют ли на эти параметры желудка добавки пробиотиков в рацион свиноматок или уровни триптофана (Trp) в рационе поросят.
Аннотация
Дизайн исследования представлял собой факторный план 2 × 3: 48 свиноматок были распределены на один из двух рационов: базовый или базовый с добавлением *Bacillus subtilis* и *Bacillus amyloliquefaciens*. Их потомство получало предстартерные корма, содержащие 0,22, 0,27 или 0,33% стандартизированного идеально переваримого триптофана (SID Trp). Всего для взятия проб желудка было проведено убоем 96 поросят: 48 в день отъема и 48 на 7-й день после отъема. Через 7 дней после отъема у поросят наблюдалось увеличение количества париетальных клеток и экспрессии генов, связанных с активностью париетальных клеток и пищеварительных ферментов (PGA5 и CHIA) в области фундальных желез (p < 0,05), хотя экспрессия сигнальных молекул, участвующих в регуляции секреции кислоты, не изменилась в области фундальных желез (p > 0,05) и снизилась в области пилорических желез (p < 0,05) по сравнению с днем отъема. В целом, добавление пробиотиков в рацион свиноматок оказало значительное влияние на экспрессию генов в области фундальных желез потомства, повышая уровень нескольких генов, связанных с активностью париетальных клеток (CLIC6, HRH2, KCNE1, KCNQ1, CHRM3, CCKBR и SSTR2) (p < 0,05). Кроме того, наблюдалось взаимодействие факторов времени и рациона свиноматки, когда экспрессия некоторых генов пути секреции кислоты (ATP4A и HDC), гена фермента хитиназы (CHIA) и гена грелина (GHRL) была повышена у потомства свиноматок, получавших пробиотики, по сравнению с потомством контрольных свиноматок в момент отъема (p < 0,05), но не на 7-й день после отъема (p > 0,05). Добавление пробиотиков в рацион свиноматок не повлияло на продуктивность роста в подсосный период или в течение 7-дневного периода после отъема. Влияние уровня триптофана в предстартерном корме или взаимодействия рациона свиноматки и уровня триптофана на продуктивность, экспрессию генов или количество париетальных клеток было ограниченным. Низкое потребление предстартерного корма в подсосный период могло исказить результаты этого анализа. В заключение, добавление пробиотиков в рацион свиноматок ускорило созревание желудка потомства, особенно в отношении экспрессии генов, связанных с секрецией кислоты париетальными клетками.
1. Введение
Чтобы повысить продуктивность свиноматок и соответствовать экономическим требованиям коммерческих свиноводческих ферм, отъем обычно проводят преждевременно, в возрасте трех-четырех недель, когда секреторная способность желудка поросят в отношении кислоты и ферментов все еще развивается [1,2,3]. Кислая среда в желудке играет двойную роль, служа одной из первых линий защиты против проглоченных патогенов, а также способствуя активации ферментов для переваривания белков. У поросят-сосунов ферментация лактозы молока бактериями желудка продуцирует молочную кислоту и ацетат, которые играют ключевую роль в поддержании низкого pH желудка [4]. В момент отъема рацион поросенка резко и преждевременно меняется с молока свиноматки на растительный корм, что приводит к резкому снижению количества лактозы в рационе [5] с прямыми последствиями для кислотности желудка. Это повышает восприимчивость поросенка после отъема к патогенам и снижает активность протеолитических ферментов, которые имеют решающее значение для эффективного переваривания белка [6].
Стратегии по смягчению проблем, связанных с незрелостью желудка в момент отъема, обычно были направлены на снижение pH послеотъемного рациона с использованием слабых органических кислот [7,8,9]. Кроме того, возобновилось внимание к минимизации кислотосвязывающей способности рациона поросят после отъема, чтобы уменьшить нейтрализующий эффект корма на pH желудка [10,11,12]. Хотя обе стратегии кормления, вероятно, будут играть ключевую роль в поддержке поросенка в послеотъемный период, дополнительной стратегией является ускорение развития желудка поросенка до отъема. На сегодняшний день эта стратегия была относительно мало изучена, и только несколько исследований были направлены на характеристику, функционирование и развитие областей желудка [13,14,15,16,17,18] или на влияние диетической модуляции на его функционирование [1,19,20,21,22,23,24,25,26].
Кислая среда, создаваемая ферментацией лактозы до отъема, может задерживать созревание секреторной способности желудка поросенка [4]. Интересно, что предоставление поросятам доступа к предстартерному корму в подсосный период снижает концентрации лактата и ацетата в желудочном химусе [27] и повышает максимальную секрецию кислоты их желудками [19]. Можно выдвинуть гипотезу, что сниженная стимуляция пути секреции кислоты у сосущего поросенка может способствовать задержке созревания, что указывает на стимуляцию этого пути как на потенциальный механизм повышения секреторной способности кислоты до отъема. Предполагается, что кальций-чувствительный рецептор (CaSR) является центральным рецептором, участвующим в регуляции секреции кислоты в ответ на просветный pH [28]. CaSR активируется для стимуляции секреции кислоты двух- и трехвалентными металлами, такими как Ca2+, Mg2+ и Gd3+, а также некоторыми аминокислотами, в частности Trp и фенилаланином [29,30,31,32]. Интересно, что и Trp, и фенилаланин, действуя через CaSR, запускают секрецию гастрина и соматостатина, одновременно повышая активность H+K+-АТФазы в in vitro образцах ткани желудка свиньи [30]. Это свидетельствует о том, что секреция кислоты может стимулироваться специфическими ингредиентами корма, независимо от стимуляции просветным pH. Таким образом, добавление в рацион компонентов, стимулирующих процесс секреции кислоты, таких как Trp, может быть средством стимулирования развития желудка и повышения секреторной способности кислоты у поросят до отъема.
Дополнительной стратегией, которая может улучшить функцию желудка, является модуляция микробного воздействия на поросенка в раннем возрасте. Сложность микробного воздействия на начальном этапе жизни может влиять на функциональное созревание области фундальных желез у молодого поросенка [24]. В последние годы роль пробиотиков как полезных кормовых добавок постоянно подчеркивается [33,34]. Однако потенциальным эффектам добавления пробиотиков на желудок уделялось ограниченное внимание. Добавление Lactobacillus acidophilus или Bifidobacterium breve и Bifidobacterium animalis увеличивает количество эндокринных клеток в желудке на 7, 14, 21, 28 и 35 дни жизни [35]. Добавление бутирата натрия, производного бактериального метаболита бутирата, увеличивает количество париетальных клеток в желудке [21]. Кроме того, при добавлении в послеотъемные рационы, но не в предотъемные, он увеличивает толщину слизистой оболочки желудка и количество соматостатин-положительных клеток [21]. Эти исследования предоставляют предварительные доказательства потенциальной способности пробиотиков или их метаболитов взаимодействовать со слизистой оболочкой желудка. Учитывая, что свиноматка является основным источником микробов в раннем возрасте [36,37], добавление пробиотиков свиноматкам может модулировать микробное воздействие на потомство в раннем возрасте и, таким образом, влиять на функциональное развитие желудка.
В желудке область фундальных желез играет решающую роль в секреции кислоты и пищеварительных ферментов, в то время как область пилорических желез является основным местом секреции гастрина и соматостатина, которые являются ключевыми регуляторами секреции желудочной кислоты [18]. Париетальные клетки, расположенные в фундальной области, специфически участвуют в секреции кислоты в желудке. Выбор генов для анализа, как в области фундальных, так и пилорических желез в текущем исследовании, был основан на их функциональной роли в путях секреции кислоты, пищеварительных ферментов и иммунитета, как ранее было определено в различных областях желудка Kiernan и др. [18]. Таким образом, цели этого исследования были двоякими: изучить характеристики желудка, количество париетальных клеток и экспрессию генов, необходимых для функционирования областей фундальных и пилорических желез в момент отъема по сравнению с семью днями после отъема, а также выяснить, влияют ли на эти желудочные параметры добавки пробиотиков (Bacillus subtilis и Bacillus amyloliquefaciens) в рацион свиноматок или уровни Trp в рационе поросят.
2. Материалы и методы
Все экспериментальные процедуры, описанные в настоящем исследовании, были одобрены Комитетом по этике животных исследований Университетского колледжа Дублина (AREC-2022-ODoherty, AREC-2202-ODoherty) и проводились в соответствии с ирландским законодательством (SI no.543/2012) и директивой ЕС 2010/63/EU по экспериментам на животных.
2.1. Дизайн эксперимента и содержание животных
Эксперимент был проведен по факторной схеме 2 × 3, в которой использовались два рациона для свиноматок и три предстартерных рациона для поросят, что составило шесть экспериментальных диетических групп.
2.1.1. Группы свиноматок по рациону и содержание
В общей сложности 48 помесных свиноматок (генетические линии крупной белой и ландрас) были распределены на блоки на основе порядкового номера опороса (средний номер опороса 4,3 ± 2,5) и ожидаемой даты опороса. Распределение свиноматок по номерам опороса было следующим: 20% свиноматок были с 1-м опоросом, 40% - со 2-го по 4-й опорос и 41% - с 5-м опоросом и более. Затем свиноматки были распределены в одну из двух диетических групп (n = 24 свиноматки/группа): (1) базовый рацион (контроль) и (2) базовый рацион, дополненный пробиотической смесью (Bacillus subtilis–541 и Bacillus amyloliquefaciens–516). Пробиотический продукт (SOLPREME®) был предоставлен компанией Chr. Hansen A/S (Хёрсхольм, Дания). Период кормления длился с 83-го дня (±1,8 дня) супоросности до отъема на 26-й день (±1,8 дня) лактации. Состав ингредиентов и анализ рационов для лактации и супоросности представлены в Таблице 1 и Таблице 2. Рационы были составлены так, чтобы соответствовать или превышать рекомендации Национального исследовательского совета (NRC) (NRC 2012).
Таблица 1. Ингредиентный и химический состав рационов для супоросных, подсосных свиноматок и предстартерного корма.
Таблица 2. Анализ химического состава рационов (г/кг, если не указано иное).
С 83-го по 110-й день супоросности свиноматки содержались в динамических группах по шесть животных в загоне в соответствии с назначенным рационом. Температура в помещении для супоросных свиноматок поддерживалась на уровне 20 °C на протяжении всего эксперимента. В этот период свиноматки получали 3,1 кг/день корма для супоросных. В помещении для супоросных свиноматок кормление осуществлялось в общем корыте (шесть свиноматок на корыто) равными порциями в 8 утра и 2 часа дня.
На 110-й день свиноматок переводили в индивидуальные станки для опороса (2,4 м × 1,8 м), оборудованные клетками, щелевыми полами и грелками для поросят. С 110-го по 113-й день супоросности свиноматки получали 2,9 кг/день корма для подсосных. Со 113-го дня до опороса свиноматки получали 2,3 кг/день корма для подсосных, а затем количество корма увеличивали на 0,7 кг/день до 3-го дня после опороса. После этого свиноматок кормили полу-ad libitum стандартным рационом для лактации, корректируя его для каждой свиноматки на основе ежедневного потребления. В родильном отделении свиноматок кормили в индивидуальных корытах тремя равными порциями в 6 утра, 11 утра и 3 часа дня. Температура в родильном отделении поддерживалась на уровне приблизительно 24 °C во время опороса, постепенно снижаясь до 20 °C к 7 дням после опороса. Свиноматки имели свободный доступ к питьевой воде на протяжении всего экспериментального периода. Пробиотическая добавка содержала 2,75 × 10⁹ колониеобразующих единиц (КОЕ) на грамм, состоящих из жизнеспособных спор Bacillus subtilis (DSM 25841) и Bacillus amyloliquefaciens (DSM 25840). Пробиотик наносили поверх корма для достижения уровня добавки, эквивалентного 400 г пробиотической добавки на тонну потребляемого корма для супоросных/подсосных свиноматок. Корм для супоросных и подсосных свиноматок посыпали пробиотиком во время первого кормления каждое утро для обеспечения потребления.
2.1.2. Опорос, содержание поросят и группы поросят по рациону
За всеми опоросами велось наблюдение. Каждый поросенок в каждом помете был индивидуально взвешен и помечен биркой при рождении. Четыре поросенка (два хрячка и две свинки), близких к средней массе при рождении, были отобраны от каждой свиноматки и исключены из перекрестного выкармливания. Перекрестное выкармливание проводилось через 12–24 часа после опороса в пределах диетических групп свиноматок для выравнивания размера помета (n = 14). Все поросята получали внутримышечную инъекцию железа (Uniferon, Pharmacosmos A/S, Хольбек, Дания) на 1-й день жизни. На 7-й день после опороса каждого поросенка индивидуально взвешивали. На 8-й день после опороса обе материнские группы были разделены на подблоки на три группы на основе номера опороса, возраста помета и размера помета. Затем пометы были распределены в одну из трех групп предстартерного корма: 0,22, 0,27 или 0,33% SID Trp, что соответствует 0,17, 0,21 и 0,25 SID Trp:Lys. Рационы были составлены с SID лизином 1,3%. Текущая рекомендация NRC для поросят 7–11 кг составляет 0,22% SID Trp [39]. Уровни 0,27% и 0,33% SID Trp были выбраны на основе предыдущих исследований [40,41,42,43]. Были небольшие расхождения между рассчитанным и проанализированным содержанием Trp и лизина в рационах. Проанализированные уровни Trp составили 0,24% общего Trp (1,39% общего лизина), 0,28% общего Trp (1,40% общего лизина) и 0,32% общего Trp (1,41 общего лизина), что соответствует 0,17, 0,20 и 0,23 Trp:Lys. Состав ингредиентов и анализ предстартерных рационов представлены в Таблице 1 и Таблице 2.
Два фактора, рацион свиноматки и предстартерный рацион, были организованы по факторной схеме 2 × 3, в результате чего образовалось шесть экспериментальных групп следующим образом: (T1) — BT (контрольные свиноматки и поросята, получавшие 0,22% SID Trp); (T2) — BTT (контрольные свиноматки и поросята, получавшие 0,27% SID Trp); (T3) — BTTT (контрольные свиноматки и поросята, получавшие 0,33% SID Trp); (T4) — PT (свиноматки с пробиотиком и поросята, получавшие 0,22% SID Trp); (T5) — PTT (свиноматки с пробиотиком и поросята, получавшие 0,27% SID Trp); (T6) — PTTT (свиноматки с пробиотиком и поросята, получавшие 0,33% SID Trp) (см. Рисунок 1).
Рисунок 1. Схема дизайна эксперимента.
2.1.3. Послеотъемный период
При отъеме три поросенка из ранее отобранных четырех поросят от каждого помета участвовали в послеотъемном испытании. 144 поросенка со средней массой тела 7,75 ± 1,53 кг (возраст 26 ± 1,8 дней) содержались вместе со своими однопометниками в группах по три (1,68 × 1,22 м) и оставались в тех же диетических группах, что и до отъема. Экспериментальные группы оставались такими, как показано на Рисунке 1. Температура окружающей среды в помещении поддерживалась термостатом на уровне 30 °C в течение первых 7 дней, а затем снижалась на 2 °C/неделю. Влажность контролировалась на уровне 65%. Корм предоставлялся в виде муки в двухместных кормушках, оборудованных ниппельными поилками для воды. Потребление корма измеряли через 7 дней после отъема для расчета среднесуточного потребления корма (ADFI) и прироста/корма (G:F). Среднесуточное потребление Trp рассчитывалось как ADFI (кг/день) × общее содержание Trp в рационе (г/кг).
2.2. Сбор образцов
Всего было проведено убой 96 поросят (2 поросенка/помет из ранее отобранных 4 поросят/помет), 48 в день отъема и 48 через 7 дней после отъема (n = 8/диетическая группа). При отъеме и через 7 дней после отъема одному поросенку/загон (n = 48) была сделана смертельная инъекция пентобарбитала натрия (Euthatal Solution, 200 мг/мл; Merial Animal Health) из расчета 0,71 мл/кг массы тела в краниальную полую вену для гуманного умерщвления животных. Поросята, подвергнутые эвтаназии при отъеме, имели среднюю массу тела 8,44 кг (SD = 1,65), в то время как поросята, подвергнутые эвтаназии через 7 дней после отъема, имели среднюю массу тела 7,95 кг (SD = 1,78). Масса тела поросят, забитых при отъеме, была больше, чем у поросят, забитых через 7 дней после отъема, из-за схемы отбора. При выборе поросенка для убоя при отъеме из 4 поросят/помет, отобранных при рождении, предпочтение отдавалось самым тяжелым поросятам для стандартизации процесса отбора. Аналогичный процесс отбора был выполнен для убоя через 7 дней после отъема.
Эвтаназия выполнялась компетентным лицом в отдельном от других поросят помещении. Поросята не голодали перед убоем. Желудок отделяли от желудочно-кишечного тракта на уровне пищевода и двенадцатиперстной кишки. Желудок взвешивали (вес полного желудка), и измеряли pH желудка, вводя щуп pH-метра (HI-98190, Hanna Instruments, Padovana, Падуя, Италия) в центр просвета. Желудок вскрывали по большой кривизне, содержимое удаляли, и пустой желудок взвешивали (вес пустого желудка). Желудок осторожно промывали стерильным PBS. Для анализа экспрессии генов, ключевых для функционирования желудка, по одному образцу слизистой оболочки (1 см²) было собрано из областей фундальных и пилорических желез, в месте 1 и месте 2 на Рисунке 2, соответственно. Ткани промывали в PBS, отделяли от подлежащей гладкой мускулатуры и помещали в раствор RNAlater® (5 мл) на ночь при 4 °C. Через двадцать четыре часа раствор RNAlater® удаляли, и образцы хранили при -80 °C. Для иммуногистохимического окрашивания париетальных клеток ткань отбирали из области фундальных желез, в месте A на Рисунке 2. Ткань осторожно промывали PBS, прикалывали к планшету для сохранения плоской структуры и ориентации и погружали в 10% нейтральный забуференный формалин до обработки.
Рисунок 2. Изображение желудка свиньи с маркировкой, вскрытого по большой кривизне желудка; изображение адаптировано из [18]. Участки 1 и 2 представляют места отбора проб слизистой оболочки для анализа экспрессии генов. Участок A представляет место отбора проб слизистой оболочки области фундальных желез для иммуногистохимического анализа.
2.3. Анализ экспрессии генов
2.3.1. Экстракция РНК и синтез кДНК
Экстракцию РНК из 100 мг ткани проводили с использованием TriReagent (Sigma-Aldrich, Сент-Луис, Миссури, США) в соответствии с инструкциями производителя. Очистку проводили с помощью набора E.Z.N.A ® Total RNA kit 1, включая стадию с ДНКазой с использованием набора для расщепления on-column DNase 1 Digestion set (Omega Bio-Tek, Норкросс, Джорджия, США). Чистоту и количество определяли по соотношению поглощения при 260 нм и 280 нм на Nanodrop-ND1000 (Thermo Scientific, Уолтем, Массачусетс, США). Обратную транскрипцию 2 мкг общей РНК проводили с использованием набора для обратной транскрипции кДНК высокой емкости High-Capacity cDNA Reverse Transcription Kit (Applied Biosystems, Уолтем, Массачусетс, США) со случайными праймерами в реакции объемом 40 мкл. Полученную кДНК затем разбавляли до конечного объема 400 мкл водой, свободной от нуклеаз.
2.3.2. Количественная ПЦР
Реакционная смесь для QPCR (20 мкл) включала FastStart Universal QPCR Sybr Green Master Mix (Roche Diagnostics, Мангейм, Германия), прямой и обратный праймеры (1,2 мкл смеси 5 мкМ для конечной концентрации 300 нм/RXN), воду, свободную от нуклеаз (3,8 мкл), и кДНК (5 мкл, эквивалентно 25 нг общей РНК). Все реакции выполнялись в дублях на системе обнаружения 7500 ABI Prism Sequence Detection System (Applied Biosystems, Фостер-Сити, Калифорния, США) в условиях циклирования: 95 °C в течение 10 мин, затем 40 циклов по 95 °C в течение 15 с и 60 °C в течение 1 мин. Праймеры были разработаны с помощью программного обеспечения Primer Express™ (v 3.0.1) (Applied Biosystems) и синтезированы компанией Eurofins (Valiant Way, Вулвергемптон, Великобритания). Кривые диссоциации были сгенерированы для подтверждения специфичности продукта ПЦР, а эффективность анализа определяли путем нанесения значений Ct из 4-кратных серийных разведений кДНК против их произвольных количеств. Включали только анализы с эффективностью 90–110% и единичным продуктом. Панель генов была выбрана на основе [18] и дополнительного обзора литературы, с фокусом на ключевых генах, функционирующих в областях фундальных и пилорических желез (секреция кислоты, секреция ферментов, воспаление и защита слизистой оболочки). Учитывая иммуностимулирующие эффекты метаболитов Trp через арил-углеводородный рецептор (AhR) в кишечнике [44] и установленную связь между AhR и IL-22 [45], в панель генов для анализа были включены как AHR, так и IL22. Оптимальные референсные гены были выбраны с использованием алгоритма GeNorm в программном обеспечении qBase PLUS 2.0 (BioGazelle, Гент, Бельгия), при этом среднее геометрическое ACTB и RPL27 использовалось для нормализации экспрессии мишеней. Нормализованные относительные количества были получены с использованием программного обеспечения qBase PLUS, а номера доступа, последовательности праймеров и длины ампликонов представлены в Таблице 3.
Таблица 3. Последовательности праймеров для QPCR анализа.
2.4. Иммуногистохимия
2.4.1. Метод
Для подсчета количества париетальных клеток в области фундальных желез ткань желудочно-кишечного тракта свиньи, фиксированная формалином и залитая в парафин (FFPE) из области фундальных желез, была иммуногистохимически окрашена на водород-калий-АТФазу бета (ATP4B). Последовательные срезы были нарезаны толщиной 4 мкМ. Окрашивание выполняли с использованием автостейнера DAKO Link 48 в соответствии с инструкциями производителя (Agilent Technologies, Пало-Альто, Калифорния, США) и набора EnVision Flex (K8002, DAKO, Agilent Technologies). Демаскировка антигена проводилась с использованием DAKO PTLink (Agilent Technologies) в течение 20 мин при 97 °C в целевом буфере для демаскировки, pH6 (K8005, DAKO, Agilent Technologies). Срезы тканей блокировали для эндогенной пероксидазы и неспецифического связывания путем инкубации с 30% H₂O₂ (H1009, Sigma-Aldrich, Сент-Луис, Миссури, США) в течение 30 мин и белковым блоком (X0909, DAKO, Agilent Technologies) в течение 15 мин. Оптимальное разведение ATP4B (NB300-583, Novus Biologicals Biotechne, Сентьенниал, Колорадо, США) было определено как 1:200 в течение 30 мин, с использованием области фундальных желез свиньи в качестве положительной контрольной ткани. Срезы тканей затем промывали и инкубировали с пероксидазой хрена (HRP) в течение 20 мин. Хромоген 3,39-диаминобензидин (DAB) использовали для проявления (дважды по 5 мин каждый). Отрицательные контроли выполнялись в идентичных условиях с разбавителем вместо первичного антитела и изотипическим контролем (IHC universal negative control reagent ADI-950-231-0025, Enzo Life Sciences, Фармингдейл, Нью-Йорк, США) параллельно с экспериментальными образцами. Срезы докрашивали гематоксилином (K8008, DAKO, Agilent Technologies) и ополаскивали деионизированной водой. Срезы высушивали в печи (58 °C) и заключали под покровное стекло на постоянной основе.
2.4.2. Анализ
После высыхания все предметные стекла были отсканированы и оцифрованы с помощью цифрового сканера слайдов Aperio AT2 (Leica Biosystems, Нуслох, Германия) при увеличении 20×, и изображения были просмотрены с использованием программного обеспечения Aperio ImageScope 12.4 (Leica Biosystems). С помощью инструментов аннотации в ImageScope область анализа была очерчена на всех изображениях слайдов случаев. Для анализа экспрессии ATP4B были обучены различные алгоритмы Aperio распознавать и количественно определять окрашенные клетки в пределах аннотированных областей. Ядерный алгоритм был адаптирован для подсчета общего количества клеток в аннотированных изображениях. ATP4B экспрессируется в цитоплазме клеток, и обученный макрос цветовой деконволюции определял процент ATP4B-положительного окрашивания и площадь анализа. Объединение результатов обоих макросов позволило рассчитать количество ATP4B-положительных клеток на мм² ткани области фундальных желез свиньи. Площадь аннотации использовалась для нормализации результатов по всем обработкам и случаям.
2.5. Анализ кормов
Содержание сухого вещества (AOAC.934.01), сырой клетчатки (CF) (AOAC.962.09) и сырого жира (AOAC.945.16) определяли согласно методам Ассоциации официальных аналитических химиков [46]. Содержание валовой энергии измеряли с помощью адиабатического бомбового калориметра (Parr Instruments, Молин, Иллинойс, США). Содержание азота определяли с использованием прибора LECO FP 528 (Leco Instruments, Мэнсфилд, Великобритания). Содержание нейтрально-детергентной клетчатки определяли, следуя методу, описанному в [47], с использованием анализатора волокна Ankom 220 (Ankom™ Technology, Нью-Йорк, Нью-Йорк, США). Концентрацию незаменимых аминокислот в рационе определяли с помощью ВЭЖХ [48].
2.6. Статистический анализ
Данные были предварительно проверены на нормальность с использованием процедуры UNIVARIATE (PROC UNIVARIATE) в программном обеспечении Statistical Analysis Software (SAS) (v 9.4) (SAS Institute, Кэри, Северная Каролина, США) и при необходимости трансформированы. Загон был экспериментальной единицей для параметров роста (масса тела, среднесуточный прирост, потребление корма и G:F). Данные по продуктивности, pH желудка, массе полного желудка, массе пустого желудка, экспрессии генов (скорректированный по Бонферрони p < 0,05) и количеству париетальных клеток анализировали с использованием процедуры общей линейной модели (PROC GLM) в SAS. Для изучения влияния рациона на продуктивность поросят данные анализировали как факторный эксперимент 2 × 3. Модель включала эффекты рациона свиноматки (контрольный или пробиотик) и рациона поросенка (предстартерный с 0,22, 0,27 или 0,33% SID Trp) и их соответствующие двусторонние взаимодействия. Для изучения влияния времени и рациона на физиологические атрибуты желудка, экспрессию генов и количество париетальных клеток данные анализировали как факторный эксперимент 2 × 2 × 3. Модель включала эффекты времени (отъем или 7 дней после отъема), рациона свиноматки (контрольный или пробиотик) и рациона поросенка (предстартерный с 0,22, 0,27 или 0,33% SID Trp) и их соответствующие двусторонние и трехсторонние взаимодействия. Для анализа генов, сгруппированных по функции, средняя экспрессия выбранных функционально сходных генов рассчитывалась для каждого поросенка, и это среднее значение затем обрабатывалось как отдельная запись в анализе PROC GLM. Результаты представлены в виде наименьших квадратов средних с их стандартными ошибками. Уровень вероятности, обозначающий значимость, составлял p < 0,05. Уровень вероятности, обозначающий тенденцию, составлял p < 0,1. В среде R функция rcorr из пакета Hmisc [49] использовалась для вычисления корреляционной матрицы и p-значений. Пакет ggplot2 [50] в R затем использовался для визуализации корреляционной матрицы выбранных генов с уровнями значимости, в то время как reshape2 использовался для форматирования данных для визуализации.
Схематический обзор режима кормления и анализа, проведенного в исследовании, представлен на Рисунке 3.
Рисунок 3. Схематическое изображение эксперимента. Создано в BioRender. Kiernan, D. (2025) https://BioRender.com/y98r818 (по состоянию на 10 января 2025 г.).
3. Результаты
3.1. Продуктивность
Влияние добавления пробиотиков в рацион свиноматок и уровня диетического триптофана поросят на продуктивность роста всех поросят в предотъемный период и с 0 по 7 день после отъема представлено в Таблице 4. Не было обнаружено влияния рациона свиноматки, предстартерного рациона или взаимодействия рацион свиноматки × предстартерный рацион на массу тела поросят, среднесуточный прирост или потребление корма в любой момент времени (p > 0,05). Не было обнаружено влияния рациона свиноматки, предстартерного рациона или взаимодействия рацион свиноматки × предстартерный рацион на G:F с 0 по 7 день после отъема (p > 0,05). Общее потребление Trp в день численно увеличивалось с увеличением содержания Trp в предстартерном корме (0,22% Trp = 0,63 г/день, 0,27% Trp = 0,72 г/день, 0,33% Trp = 0,82 г/день), но не достигло статистической значимости (p = 0,1287).
Таблица 4. Влияние рациона на массу тела поросят, среднесуточный прирост, потребление корма и прирост:корм в предотъемный и послеотъемный периоды (наименьшие квадраты средних с их стандартными ошибками).
3.2. pH желудка и масса желудка
Влияние времени, добавления пробиотиков свиноматкам и уровня диетического триптофана поросят на массу тела поросят (только забитые поросята), pH желудка, массу полного желудка и массу пустого желудка представлено в Таблице 5. Не было обнаружено двусторонних или трехсторонних взаимодействий; следовательно, результаты представлены только как основные эффекты.
Таблица 5. Влияние рациона и времени на pH желудка и физиологические параметры желудка (наименьшие квадраты средних с их стандартными ошибками).
3.2.1. Влияние времени на pH желудка и массу желудка
Не было различий в массе тела забитых поросят, pH желудка или отношении массы пустого желудка к массе тела между поросятами, забитыми в день отъема или через 7 дней после отъема (p > 0,05). Поросята, забитые при отъеме, имели численно более высокую массу тела, чем группа поросят, забитых через 7 дней после отъема (8,49 против 7,96 кг соответственно) (p > 0,05). Что касается группы, забитой через 7 дней после отъема, эти поросята имели среднюю массу тела 7,68 кг при отъеме и прибавили в среднем 0,27 кг в период между отъемом и 7 днями после отъема (данные не представлены). Масса полного желудка была больше у поросят через 7 дней после отъема по сравнению с отъемом; однако масса пустого желудка была больше при отъеме по сравнению с 7 днями после отъема (p < 0,05).
3.2.2. Влияние рациона свиноматки на pH желудка и массу желудка
Не было обнаружено значимого влияния рациона свиноматки на массу тела забитых поросят, pH желудка, массу пустого желудка, массу полного желудка или отношение массы пустого желудка к массе тела (p > 0,05).
3.2.3. Влияние предстартерного рациона на pH желудка и массу желудка
Не было обнаружено значимого влияния предстартерного рациона на массу тела забитых поросят, pH желудка, массу пустого желудка, массу полного желудка или отношение массы пустого желудка к массе тела (p > 0,05).
3.3. Экспрессия генов
Влияние времени и рациона свиноматки на экспрессию генов в области фундальных и пилорических желез представлено в Таблице 6. Данные о влиянии рациона свиноматки, предстартерного рациона и взаимодействия рацион свиноматки × предстартерный рацион на экспрессию генов в области фундальных и пилорических желез, разделенные по временным точкам (отъем и 7 дней после отъема), представлены в Приложении A (Таблица A1 и Таблица A2 соответственно).
Таблица 6. Влияние рациона свиноматки и времени на экспрессию генов в области фундальных и пилорических желез (наименьшие квадраты средних с их стандартными ошибками).
Среди двадцати трех генов, проанализированных в области фундальных желез, наблюдалось влияние времени на экспрессию шестнадцати генов, влияние рациона свиноматки на экспрессию одиннадцати генов и взаимодействие время × рацион свиноматки на экспрессию шести генов (p < 0,05). Не было обнаружено взаимодействий предстартерный рацион, рацион свиноматки × предстартерный рацион, время × предстартерный рацион или время × рацион свиноматки × предстартерный рацион на экспрессию генов в области фундальных желез (p > 0,05). Среди десяти генов, проанализированных в области пилорических желез, наблюдалось влияние времени на экспрессию семи генов и влияние рациона свиноматки, предстартерного рациона, взаимодействия рацион свиноматки × предстартерный рацион и время × рацион свиноматки на экспрессию одного гена каждое (p < 0,05). Не было обнаружено взаимодействий время × предстартерный рацион или время × рацион свиноматки × предстартерный рацион на экспрессию генов в области пилорических желез (p > 0,05).
3.3.1. Влияние времени на экспрессию генов
В области фундальных желез шесть генов имели более высокую экспрессию при отъеме по сравнению с 7 днями после отъема: AHR, CASR, LCT, CXCL8 и TNF (p < 0,05). Восемь генов имели более высокую экспрессию через 7 дней после отъема по сравнению с отъемом: HRH2, KCNE1, KCNQ1, CHRM3, CHIA, PGA5, CCKBR, MUC6 и SSTR2 (p < 0,05).
В области пилорических желез три гена имели более высокую экспрессию при отъеме по сравнению с 7 днями после отъема: CASR, GAST и SST (p < 0,05). Три гена имели более высокую экспрессию через 7 дней после отъема по сравнению с отъемом: PIGR, MUC5AC и MUC6 (p < 0,05).
3.3.2. Влияние рациона свиноматки и взаимодействий со временем на экспрессию генов
В области фундальных желез наблюдалось влияние рациона свиноматки на экспрессию восьми генов; у поросят от свиноматок, получавших пробиотик, была повышена экспрессия CLIC6, HRH2, KCNE1, KCNQ1, CHRM3, CCKBR, MUC6 и SSTR2 по сравнению с поросятами от контрольных свиноматок (p < 0,05).
В области фундальных желез было обнаружено семь взаимодействий время × рацион свиноматки: у поросят от свиноматок, получавших пробиотик, была повышена экспрессия ATP4A при отъеме по сравнению с поросятами от контрольных свиноматок (p < 0,05), но не через 7 дней после отъема (p > 0,05). Экспрессия ATP4A была выше через 7 дней после отъема по сравнению с отъемом у поросят от контрольных свиноматок (p < 0,05), но не у поросят от свиноматок, получавших пробиотик (p > 0,05); у поросят от свиноматок, получавших пробиотик, была повышена экспрессия CHIA при отъеме по сравнению с поросятами от контрольных свиноматок (p < 0,05), но не через 7 дней после отъема (p > 0,05); у поросят от свиноматок, получавших пробиотик, была повышена экспрессия GHRL по сравнению с поросятами от контрольных свиноматок при отъеме (p < 0,05), но не через 7 дней после отъема (p > 0,05); у поросят от свиноматок, получавших пробиотик, была повышена экспрессия HDC по сравнению с поросятами от контрольных свиноматок при отъеме (p < 0,05), но не через 7 дней после отъема (p > 0,05). Кроме того, экспрессия HDC была выше при отъеме по сравнению с 7 днями после отъема у поросят от свиноматок, получавших пробиотик (p < 0,05), но не у поросят от контрольных свиноматок (p > 0,05); у поросят от свиноматок, получавших пробиотик, была повышена экспрессия MUC5AC по сравнению с поросятами от контрольных свиноматок через 7 дней после отъема (p < 0,05), но не при отъеме (p > 0,05); экспрессия TLR4 была выше при отъеме по сравнению с 7 днями после отъема у поросят от контрольных свиноматок (p < 0,05), но не у поросят от свиноматок, получавших пробиотик (p > 0,05).
В области пилорических желез было обнаружено одно взаимодействие время × рацион свиноматки: экспрессия AHR была выше при отъеме по сравнению с 7 днями после отъема у поросят от свиноматок, получавших пробиотик (p < 0,05), но не у поросят от контрольных свиноматок (p > 0,05).
3.3.3. Влияние предстартерного рациона и взаимодействий со временем на экспрессию генов
В области пилорических желез наблюдалось влияние предстартерного рациона на экспрессию PIGR (p < 0,05); у поросят, получавших предстартерный корм с 0,27 или 0,33% Trp, была повышена экспрессия PIGR по сравнению с поросятами, получавшими 0,22% Trp (1,38 и 1,36 против 0,91 соответственно, SEM = 0,13) (p < 0,05). Не было обнаружено влияния предстартерного рациона на экспрессию генов в области фундальных желез, а также взаимодействий время × предстартерный рацион на экспрессию генов в областях фундальных или пилорических желез (p > 0,05).
3.3.4. Взаимодействия рациона свиноматки и предстартерного рациона на экспрессию генов
В области пилорических желез наблюдалось взаимодействие рацион свиноматки × предстартерный рацион на экспрессию GAST (p < 0,05); экспрессия GAST была повышена у поросят от свиноматок, получавших пробиотик и кормившихся 0,33% Trp, и от контрольных свиноматок, кормившихся 0,22% Trp, по сравнению с поросятами от контрольных свиноматок, получавших 0,27% или 0,33% Trp (1,80 и 1,79 против 0,89 и 1,12 соответственно, SEM = 0,19) (p < 0,05).
Не было обнаружено взаимодействий время × рацион свиноматки × предстартерный рацион на экспрессию генов в областях фундальных или пилорических желез (p > 0,05).
3.4. Гены, сгруппированные по функции
Влияние времени и рациона свиноматки на экспрессию генов, сгруппированных по функции, в областях фундальных и пилорических желез представлено в Таблице 7. Не было обнаружено взаимодействий предстартерный рацион, рацион свиноматки × предстартерный рацион, время × предстартерный рацион или время × рацион свиноматки × предстартерный рацион на экспрессию генов, сгруппированных по функции, в областях фундальных или пилорических желез (p > 0,05).
Таблица 7. Влияние рациона и времени на экспрессию генов, сгруппированных по функции, в областях фундальных и пилорических желез (наименьшие квадраты средних с их стандартными ошибками).
3.4.1. Влияние времени на гены, сгруппированные по функции
В области фундальных желез у поросят через 7 дней после отъема была выше экспрессия генов стимуляции кислоты и ингибирования кислоты по сравнению с поросятами при отъеме (p < 0,05). В области пилорических желез у поросят через 7 дней после отъема была выше экспрессия генов продукции слизи по сравнению с поросятами при отъеме (p < 0,05).
3.4.2. Влияние рациона свиноматки и взаимодействие со временем на гены, сгруппированные по функции
У поросят от свиноматок, получавших пробиотик, была повышена экспрессия генов стимуляции кислоты, ингибирования кислоты и продукции слизи в области фундальных желез по сравнению с поросятами от контрольных свиноматок (p < 0,05). Наблюдалось взаимодействие время × рацион свиноматки на экспрессию генов секреции кислоты; у поросят от свиноматок, получавших пробиотик, была повышена экспрессия генов секреции кислоты по сравнению с поросятами от контрольных свиноматок при отъеме (p < 0,05), но не через 7 дней после отъема (p > 0,05). Кроме того, экспрессия генов секреции кислоты была выше через 7 дней после отъема по сравнению с отъемом у поросят от контрольных свиноматок (p < 0,05), но не у поросят от свиноматок, получавших пробиотик (p > 0,05).
3.5. Количество париетальных клеток
Влияние времени на количество париетальных клеток на мм² в области фундальных желез представлено на Рисунке 4. Количество париетальных клеток на мм² ткани фундальных желез было больше через 7 дней после отъема по сравнению с отъемом (1250 против 913, SEM = 104) (p < 0,05). Не было обнаружено влияния рациона свиноматки, предстартерного рациона, взаимодействия рацион свиноматки × предстартерный рацион, время × рацион свиноматки или рацион свиноматки × предстартерный рацион × время на количество париетальных клеток при отъеме или через 7 дней после отъема (p > 0,05; данные не представлены).
Рисунок 4. Количество париетальных клеток на мм² ткани области фундальных желез у поросят при отъеме по сравнению с 7 днями после отъема.
3.6. Корреляционный анализ
Учитывая важность развития секреции кислоты и ферментов в области фундальных желез молодого поросенка, были выполнены корреляции Пирсона для оценки паттернов совместной экспрессии и корреляций между физиологическими параметрами поросенка и экспрессией генов в области фундальных желез как при отъеме, так и через 7 дней после отъема. Для корреляций использовались данные по генам, сгруппированным по функции, для стимуляции кислоты, секреции кислоты, ингибирования кислоты и продукции слизи, а не индивидуальные значения экспрессии генов. Корреляции Пирсона для области пилорических желез при отъеме и через 7 дней после отъема не обсуждаются, но представлены в Приложении A (Рисунок A1 и Рисунок A2).
3.6.1. Отъем
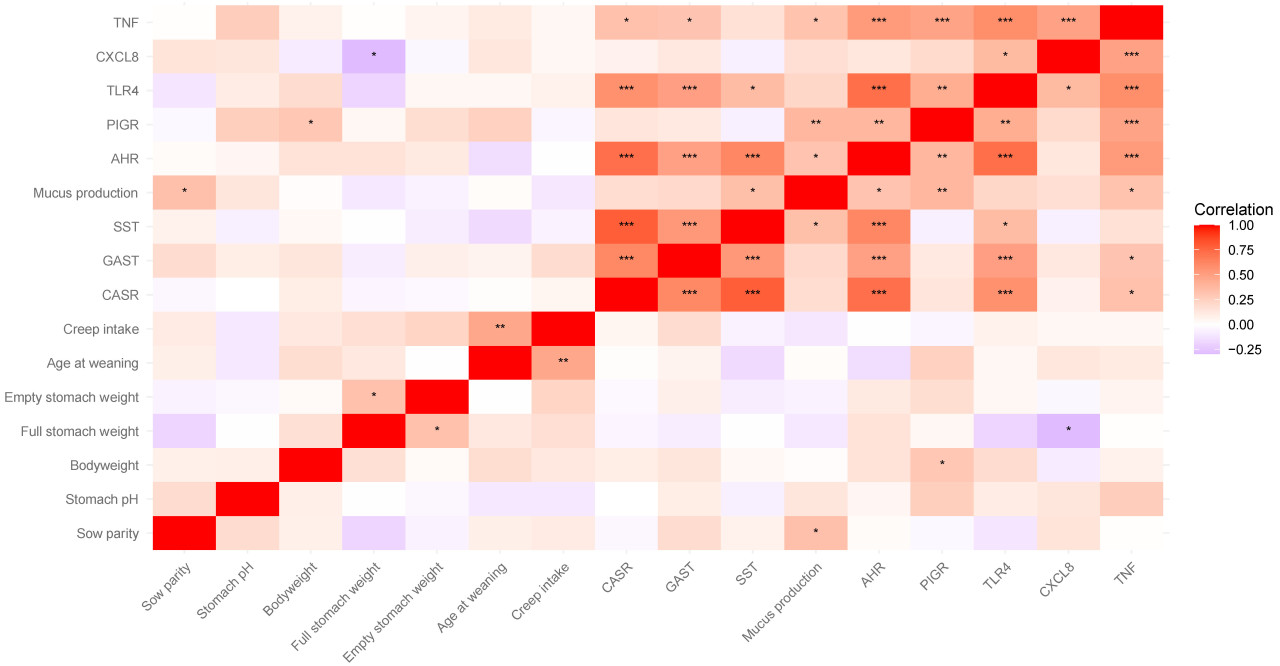
Корреляции Пирсона между экспрессией генов в области фундальных желез, потреблением предстартерного корма до отъема, номером опороса свиноматки, возрастом поросенка при отъеме, массой полного желудка, массой пустого желудка, pH желудка, массой тела и количеством париетальных клеток в момент отъема представлены на Рисунке 5.
Рисунок 5. Корреляционная матрица, иллюстрирующая корреляции Пирсона экспрессии генов в области фундальных желез и физиологических параметров до отъема. Положительные (красный) и отрицательные (синий) корреляции представлены интенсивностью цвета по шкале от -1 до 1. p < 0,05, p < 0,01, p < 0,001.
Наиболее заметно, что экспрессия генов секреции кислоты (ATP4A, CLIC6, KCNE1 и KCNQ1), стимуляции кислоты (HRH2, CCKBR, CHRM3 и HDC), ингибирования кислоты (SST и SSTR2), пищеварительных ферментов (PGA5 и CHIA) и грелина (GHRL) была положительно коррелирована. В целом, pH желудка, номер опороса свиноматки и масса тела имели минимальные корреляции с экспрессией генов, количеством париетальных клеток или выбранными производственными параметрами: pH желудка был положительно коррелирован с экспрессией CASR; масса тела была положительно коррелирована с уровнем экспрессии генов, связанных с секрецией кислоты, а номер опороса свиноматки не имел корреляций. Интересно, что потребление предстартерного корма было положительно коррелировано с секрецией кислоты, пищеварительными ферментами PGA5 и CHIA и экспрессией GHRL. Как и ожидалось, масса полного желудка и масса пустого желудка были положительно коррелированы, в то время как масса пустого желудка также была положительно коррелирована с секрецией кислоты, PGA5 и CHIA и отрицательно коррелирована с экспрессией TLR4. Гены иммунного ответа CXCL8, IL22, TNF и TLR4 были положительно коррелированы друг с другом, в то время как AHR был положительно коррелирован с TLR4, TNF и экспрессией продукции слизи. Уровни экспрессии нескольких генов иммунного ответа, CXCL8, IL22 и TLR4, были отрицательно коррелированы с экспрессией генов стимуляции кислоты и ингибирования кислоты, в то время как TLR4 также был отрицательно коррелирован с секрецией кислоты. Экспрессия CASR была положительно коррелирована с pH желудка, ингибированием кислоты и экспрессией GHRL; однако, удивительно, она была отрицательно коррелирована как с экспрессией стимуляции, так и секреции кислоты. Более того, количество париетальных клеток (ATP4B+) не коррелировало ни с какой экспрессией генов в области фундальных желез или с какими-либо параметрами продуктивности.
3.6.2. Семь дней после отъема
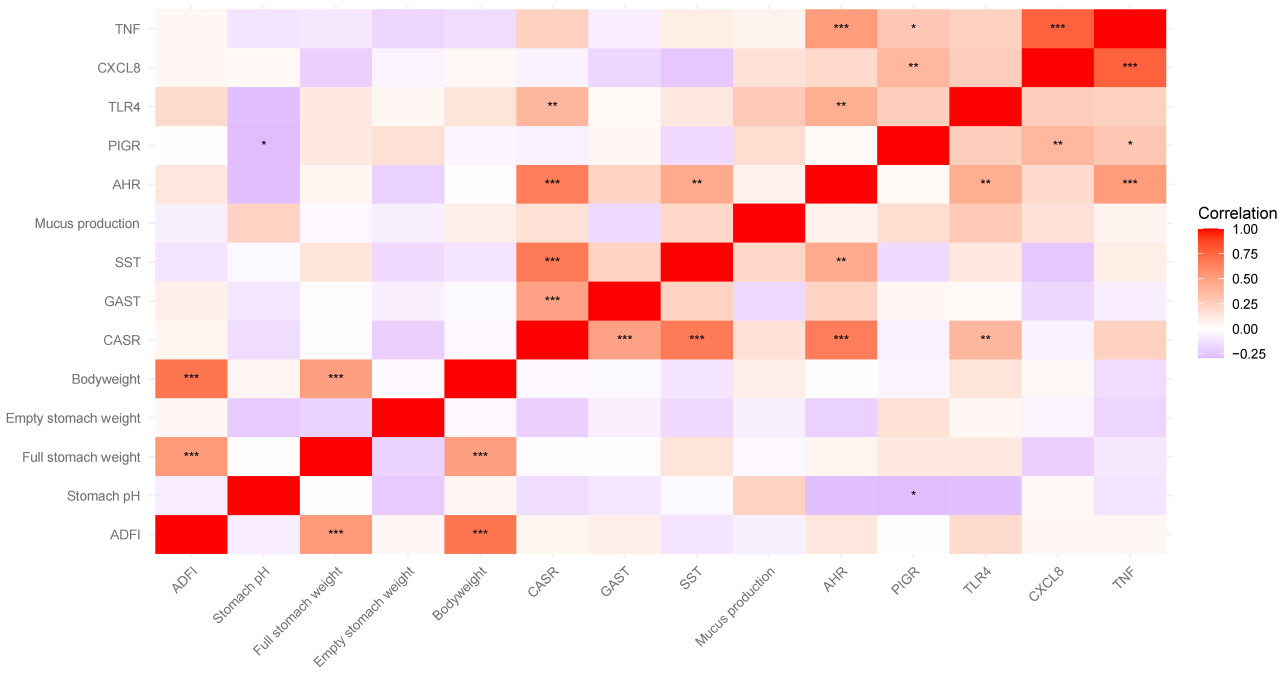
Корреляции Пирсона между экспрессией генов в области фундальных желез и ADFI поросенка после отъема, pH желудка, массой полного желудка, массой пустого желудка, массой тела и количеством париетальных клеток через 7 дней после отъема представлены на Рисунке 6.
Рисунок 6. Корреляционная матрица, иллюстрирующая корреляции Пирсона экспрессии генов в области фундальных желез и физиологических параметров после отъема. Положительные (красный) и отрицательные (синий) корреляции представлены интенсивностью цвета по шкале от -1 до 1. p < 0,05, p < 0,01, p < 0,001. ADFI — среднесуточное потребление корма.
Примечательно, что масса тела, масса полного желудка, масса пустого желудка и ADFI были положительно коррелированы друг с другом. ADFI и масса тела также были положительно коррелированы с экспрессией генов секреции кислоты. Интересно, что среднесуточный прирост и масса полного желудка были отрицательно коррелированы с экспрессией LCT, CASR, TLR4 и TNF, в то время как масса полного желудка также была отрицательно коррелирована с GHRL. Как и при отъеме, секреция кислоты, стимуляция кислоты, ингибирование кислоты и пищеварительные ферменты PGA5 и CHIA были положительно коррелированы друг с другом. Кроме того, экспрессия GHRL была положительно коррелирована со стимуляцией кислоты, ингибированием кислоты и экспрессией пищеварительных ферментов PGA5 и CHIA. Иммунные гены CXCL8, IL22, TNF и TLR4 были положительно коррелированы друг с другом, в то время как AHR был положительно коррелирован с CXCL8, TLR4, TNF и экспрессией продукции слизи. Однако, в отличие от предотъемного периода, где эти гены иммунного ответа были отрицательно коррелированы с генами секреции кислоты и ферментов, единственной отрицательной корреляцией экспрессии генов с геном иммунного ответа была корреляция между CXCL8 и GHRL. Экспрессия CASR не коррелировала ни с какими генами, связанными с секрецией кислоты, но, как и до отъема, она имела положительную корреляцию с GHRL. Более того, CASR был отрицательно коррелирован с ADFI и массой полного желудка. Количество париетальных клеток (ATP4B+) не коррелировало с экспрессией генов секреции кислоты в области фундальных желез. Количество париетальных клеток было положительно коррелировано с массой полного желудка и экспрессией CXCL8.
4. Обсуждение
Пространственно-временное развитие желудочной функции в желудке по отношению к диете представляет собой относительно малоизученный аспект физиологии свиней [51]. В текущем исследовании у поросят через 7 дней после отъема был более функционально зрелый желудок по сравнению с отъемом, что выражалось в большем количестве париетальных клеток, большей экспрессии генов, участвующих в активности париетальных клеток, и изменении экспрессии генов пищеварительных ферментов. Уровень диетического Trp, скармливаемого поросятам, оказал ограниченное влияние на продуктивность роста, pH желудка, экспрессию генов или количество париетальных клеток в желудке поросенка. В целом, добавление пробиотиков в рацион свиноматок оказало значимое влияние на экспрессию генов в области фундальных желез потомства, в частности, повышая экспрессию нескольких генов, связанных с секрецией кислоты париетальными клетками. Однако добавление пробиотиков свиноматкам не повлияло на продуктивность роста в предотъемный период или в течение 7-дневного послеотъемного периода.
4.1. Влияние времени: день отъема по сравнению с 7 днями после отъема
Анализ изменений в желудке поросенка при отъеме по сравнению с 7 днями после отъема дает ценную информацию о непосредственных эффектах отъема на желудок. Как правило, количество кислотопродуцирующих париетальных клеток неуклонно увеличивается с возрастом в подсосный период и выше у поросят через 14 дней после отъема по сравнению с предотъемным периодом [1]. В соответствии с этим, количество париетальных клеток в области фундальных желез было больше у поросят через 7 дней после отъема по сравнению с поросятами при отъеме в текущем исследовании. Согласуясь с этим, уровни экспрессии нескольких генов, связанных с активностью париетальных клеток, таких как секреция кислоты (KCNE1, KCNQ1) и клеточные рецепторы, связанные как со стимуляцией секреции кислоты (CCKBR, CHRM3, HRH2), так и с ингибированием (SSTR2), были выше в области фундальных желез у поросят через 7 дней после отъема по сравнению с поросятами при отъеме. Регуляция желудочной кислоты включает сложную систему рецепторов, лигандов и сигнальных каскадов. Секреция кислоты париетальными клетками регулируется паракринными (гистамин), эндокринными (гастрин/соматостатин) и нейральными (ацетилхолин) путями. Экспрессия соответствующих рецепторов для каждого из этих путей была выше в области фундальных желез у поросят через 7 дней после отъема по сравнению с отъемом. Однако удивительно, что экспрессия генов, связанных с продукцией соответствующих сигнальных молекул, гистамина и соматостатина, не различалась в области фундальных желез между пред- и послеотъемным периодами. Кроме того, уровни экспрессии гастрина и соматостатина в области пилорических желез, основном месте их продукции [18], были в 2 раза и в 1,5 раза выше соответственно у поросят при отъеме по сравнению с поросятами через 7 дней после отъема. В исследовании Trevisi и др. [1] на экспрессию гастрина возраст не повлиял; однако наблюдалось численное снижение через 14 дней после отъема по сравнению с отъемом. Когда гены были сгруппированы по функции, стимуляция кислоты и ингибирование кислоты были выше в области фундальных желез через 7 дней после отъема по сравнению с отъемом. Кроме того, продукция слизи была выше в области пилорических желез через 7 дней после отъема по сравнению с отъемом. Если рассматривать конкретно временную точку отъема, добавление пробиотиков свиноматкам увеличило экспрессию дополнительных генов, связанных с секрецией кислоты в области фундальных желез потомства, что будет подробно обсуждаться позже. Это увеличение привело к взаимодействию время × рацион свиноматки для определенных генов, таких как ATP4A, а также для генов секреции кислоты при группировке по функции. Примечательно, что эти гены имели более высокую экспрессию через 7 дней после отъема по сравнению с отъемом у потомства от контрольных свиноматок, тогда как эта закономерность не наблюдалась у потомства от свиноматок, получавших пробиотик, из-за их уже повышенных предотъемных уровней экспрессии.
Экспрессия CASR, стимуляция которого может приводить к увеличению активности кислотной помпы H+/K+-АТФазы, а также экспрессии гастрина и соматостатина [30,31,52], была выше как в области фундальных, так и пилорических желез у предотъемных поросят по сравнению с послеотъемными. Учитывая его предполагаемую роль в секреции кислоты, удивительно, что экспрессия CASR не совпадала с экспрессией генов секреции кислоты. Экспрессия пищеварительных ферментов, CHIA и PGA5, была выше через 7 дней после отъема по сравнению с отъемом, в то время как экспрессия пищеварительного фермента лактазы, LCT, была ниже через 7 дней после отъема по сравнению с отъемом. Снижение LCT неудивительно, учитывая снижение количества диетической лактозы в послеотъемном рационе по сравнению с молоком свиноматки до отъема. Насколько известно авторам, это первое исследование, документирующее экспрессию гена LCT в желудке, так как литература свидетельствует о том, что его экспрессия ограничена кишечником, а предыдущие исследования были сосредоточены на активности кишечной лактазы [53] и экспрессии генов [54]. Хотя кишечник действительно может быть преобладающим местом его экспрессии, этот результат свидетельствует о том, что LCT, по крайней мере, транскрибируется в желудке.
Послеотъемный период обычно ассоциируется с повышенной экспрессией маркеров воспаления и иммунитета в кишечнике [55,56]. Однако в текущем исследовании экспрессия провоспалительных маркеров, CXCL8 и TNF, была выше в области фундальных желез при отъеме по сравнению с 7 днями после отъема. Кроме того, у поросят от контрольных свиноматок TLR4 был выше при отъеме по сравнению с 7 днями после отъема. Однако, согласно Trevisi и др. [15], экспрессия полимерного иммуноглобулинового рецептора, PIGR, ключевого компонента врожденной иммунной системы, была выше в области пилорических желез через 7 дней после отъема по сравнению с отъемом.
Примечательно, что масса тела группы, забитой при отъеме, была в среднем на 0,53 кг больше, чем у послеотъемной группы, хотя это различие не было статистически значимым. Через 7 дней после отъема масса полного желудка была в два раза выше по сравнению с отъемом, вероятно, из-за увеличенного количества твердого желудочного содержимого. Несмотря на это увеличение массы полного желудка, масса пустого желудка была ниже через 7 дней после отъема по сравнению с отъемом, что, возможно, связано с разницей в массе тела между двумя забитыми группами. Не было различий в отношении массы пустого желудка к массе тела или pH желудка между отъемом и 7 днями после отъема.
4.2. Влияние добавления пробиотиков в рацион свиноматок
Это исследование является первым, в котором изучается влияние добавления пробиотиков в рацион свиноматок на желудок потомства у свиней. Интересно, что у потомства от свиноматок, получавших пробиотики, наблюдалась дифференциальная экспрессия нескольких генов по сравнению с потомством от контрольных свиноматок. В целом, в области фундальных желез у потомства от свиноматок, получавших пробиотик, была повышена экспрессия генов, связанных с активностью париетальных клеток, KCNE1, KCNQ1, CLIC6, HRH2, CHRM3, CCKBR и SSTR2. Аналогично, когда гены были сгруппированы по функции, у потомства от свиноматок, получавших пробиотик, была повышена экспрессия генов, связанных со стимуляцией и ингибированием кислоты и продукцией слизи в области фундальных желез, по сравнению с потомством от контрольных свиноматок. Кроме того, когда временные точки отъема и 7 дней после отъема анализировались отдельно, у потомства от свиноматок, получавших пробиотик, при отъеме было несколько дополнительных генов с повышенной экспрессией по сравнению с потомством от контрольных свиноматок. Они включали гены пищеварительных ферментов, такие как CHIA и PGA5; GHRL, который участвует в пищевом поведении и энергетическом балансе при отъеме [57,58]; HDC, который участвует в стимуляции секреции кислоты париетальными клетками; и, при группировке по функции, гены секреции кислоты (см. Приложение A: Таблица A1). Кроме того, добавление пробиотиков свиноматкам снизило экспрессию TLR4 в области фундальных желез при отъеме, что, учитывая его роль в распознавании микроб-ассоциированных молекулярных паттернов [59], может указывать на потенциальное изменение бактериальных популяций в желудке при отъеме. Несколько генов, которые были дифференциально повышены у поросят от свиноматок, получавших пробиотик, при отъеме, были численно повышены снова через 7 дней после отъема. Однако этот эффект не достиг статистической значимости, возможно, из-за увеличенной вариабельности через 7 дней после отъема. Это очевидно из того факта, что при анализе общих данных (комбинация отъема и 7 дней после отъема) статистически значимое увеличение при отъеме и численное увеличение после отъема привели к значимым общим эффектам для нескольких генов, без значимых взаимодействий время × рацион свиноматки.
В дополнение к увеличению экспрессии генов активности париетальных клеток у поросят от свиноматок, получавших пробиотик, наблюдалась тенденция к снижению pH желудка у этих поросят по сравнению с поросятами от контрольных свиноматок (3,4 против 3,7, SEM = 0,13). Кроме того, у поросят от свиноматок, получавших пробиотик, наблюдалась тенденция к увеличению отношения массы пустого желудка к массе тела по сравнению с поросятами от контрольных свиноматок. Хотя эти эффекты были лишь статистическими тенденциями, они предоставляют дополнительные доказательства влияния добавления пробиотиков в рацион свиноматок на развитие желудка потомства. Не было обнаружено влияния пробиотиков в рационе свиноматок на количество париетальных клеток или на массу пустого или полного желудка. Примечательно, что экспрессия генов, связанных с активностью париетальных клеток, была повышена у поросят от свиноматок, получавших пробиотик, в то время как количество париетальных клеток осталось неизменным. Это свидетельствует о том, что добавление пробиотиков свиноматкам усиливает функциональную активность париетальных клеток, а не увеличивает их количество.
Интересно, что у поросят от свиноматок, получавших пробиотик, наблюдалась повышенная экспрессия генов продукции слизи в области фундальных желез по сравнению с поросятами от контрольных свиноматок, когда MUC1, MUC5AC и MUC6 были сгруппированы вместе. Муцины являются ключевым компонентом желудочной слизи, защищающим эпителиальный слой от кислого желудочного содержимого и вредных патогенов. Добавление пробиотиков свиньям может увеличить количество бокаловидных клеток и экспрессию слизи в кишечнике [60,61,62]; однако, насколько известно авторам, это первое исследование, демонстрирующее влияние пробиотиков на продукцию слизи в желудке свиней.
Если рассматривать конкретно временную точку отъема, у поросят от свиноматок, получавших пробиотик, была повышена экспрессия генов, связанных со стимуляцией кислоты (HRH2, CHRM3, CCKBR, HDC), ингибированием кислоты (SST, SSTR2), секрецией кислоты (ATP4A, CLIC6, KCNE1, KCNQ1), пищеварительными ферментами (CHIA, PGA5), GHRL и MUC6 в области фундальных желез. Напротив, экспрессия TLR4 была ниже у поросят от свиноматок, получавших пробиотик, по сравнению с поросятами от контрольных свиноматок в области фундальных желез при отъеме. Интересное сравнение с анализом отъема против 7 дней после отъема выявило сильное сходство в паттернах экспрессии генов; через 7 дней после отъема у поросят наблюдалась повышенная экспрессия тех же генов, связанных с регуляцией кислоты, пищеварительными ферментами, GHRL и MUC6, со снижением экспрессии TLR4. Эти параллельные паттерны позволяют предположить, что добавление пробиотиков свиноматкам ускорило созревание функции желудка потомства до отъема.
Несмотря на улучшение функции желудка у поросят от свиноматок, получавших пробиотик, это не трансформировалось в улучшение продуктивности в предотъемный или непосредственный послеотъемный период. Продуктивность роста зависит от сложного взаимодействия множества систем в организме, включая пищеварительную и иммунную системы. Хотя при добавлении пробиотиков свиноматкам наблюдались улучшения функции желудка, они не привели к измеримым эффектам на продуктивность в течение короткой продолжительности испытания. Однако отсутствие улучшения продуктивности роста в предотъемный период противоречит недавним исследованиям с использованием этой конкретной смеси Bacillus subtilis и Bacillus amyloliquefaciens, где добавление увеличило прирост массы потомства и массу при отъеме, как при добавлении только свиноматке [63], так и в сочетании с прямым добавлением поросятам [64,65]. Насколько известно авторам, влияние добавления этого пробиотика свиноматкам на послеотъемную продуктивность еще не задокументировано в литературе. Продление периода оценки за пределы первой недели после отъема может дать дополнительное понимание потенциальных долгосрочных преимуществ добавления этой смеси пробиотиков Bacillus свиноматкам на продуктивность потомства и здоровье желудочно-кишечного тракта. Добавление пробиотиков свиноматкам может оказывать ограниченные краткосрочные эффекты, но существенно влиять на долгосрочную продуктивность потомства. Это подтверждается работой Crespo-Piazuelo и др. [66], в которой добавление Bacillus altitudinis свиноматкам не повлияло на массу тела потомства на 14, 28 или 56 день после отъема, но увеличило массу тела на 105 и 127 день после отъема.
Установление здоровой микробиоты, которая является разнообразной, с высоким обилием полезных бактерий и низким обилием потенциально патогенных бактерий, является целью с точки зрения модуляции микробиоты для улучшения здоровья и продуктивности. Состав микробиоты ЖКТ у постнатальных поросят может зависеть от различных микробных источников, причем свиноматка является одним из основных источников [36,37,67,68,69,70]. Пробиотики определяются как «живые микроорганизмы, которые при введении в адекватных количествах оказывают благоприятное воздействие на здоровье хозяина» [71]. Общий механизм действия пробиотика заключается во введении полезных микробных штаммов в среду ЖКТ, которые затем заполняют экологические ниши. Это, в свою очередь, приводит к повышению разнообразия микробиоты, увеличению устойчивости хозяина к патогенам и увеличению продукции метаболитов, способствующих здоровью хозяина, тем самым улучшая общее состояние здоровья хозяина, как рассмотрено в [33]. Потенциал добавления пробиотиков свиноматкам подробно рассмотрен в [33]. Положительные изменения в составе микробиоты свиноматки могут принести пользу здоровью свиноматки и облегчить передачу полезных микробов (через фекалии свиноматки или потребление молока), включая добавленный штамм пробиотика, потомству [66,72]. Однако, насколько известно авторам, это первое исследование, в котором анализируется влияние добавления пробиотиков в рацион свиноматок на характеристики желудка, экспрессию генов, ключевых для функционирования желудка, или количество париетальных клеток в желудке потомства. Значительные эффекты добавления Bacillus subtilis и Bacillus amyloliquefaciens свиноматкам на желудок потомства являются интригующим результатом в текущем исследовании, хотя точные механизмы неясны. Ограниченная информация в литературе о взаимодействии между микробным воздействием в раннем возрасте и развитием желудка была предоставлена в двух предыдущих исследованиях Trevisi и др. [1,24]. В первом исследовании у поросят, рожденных путем кесарева сечения, изолированных от свиноматки и получивших пероральную дозу простых стартерных бактерий (Lactobacillus amylovorus, Clostridium glycolicum и Parabacteroides spp.) при рождении, с последующей пероральной дозой разбавленных фекалий свиноматки на 3-й день жизни, наблюдалось усиленное функциональное созревание области фундальных желез в двухнедельном возрасте по сравнению с поросятами, которые получили только пероральную дозу стартерных бактерий при рождении [24]. Это исследование подчеркивает потенциальное влияние состава микробного воздействия на функционирование желудка у молодых поросят. Во втором исследовании Trevisi и др. [1] изучили влияние лечения свиноматок антибиотиками на развитие секреции кислоты, регуляцию грелина и вкус умами у потомства и пришли к выводу, что, хотя на вкус умами и регуляцию грелина может влиять материнская среда, развитие секреции кислоты в основном контролируется процессами развития. Результаты текущего исследования несколько противоречат этому и позволяют предположить, что материнская среда действительно влияет на путь секреции кислоты в желудке потомства. Чтобы лучше понять механизмы, лежащие в основе наблюдаемых эффектов добавления пробиотиков свиноматкам в этом исследовании, анализ изменений в составе микробиоты свиноматок и, более конкретно, в составе микробиоты желудка потомства и содержании метаболитов в желудке был бы ценным и должен быть рассмотрен в будущих исследованиях.
4.3. Влияние повышенного уровня диетического триптофана поросят
Рекомендуемый NRC уровень включения Trp для поросят массой 5–7 кг и 7–11 кг составляет 0,25% SID Trp (SID Trp:Lys 0,17) и 0,22% SID Trp (SID Trp:Lys 0,16) соответственно [39]. Из-за недостатка данных о биологических взаимосвязях у поросят массой менее 20 кг модель NRC не генерировала точные оценки для этих поросят, полагаясь вместо этого на простой математический подход и эмпирические оценки [39]. Интерес к уровням включения Trp в последнее время возрос из-за влияния Trp на иммунный ответ, как рассмотрено в [73,74], и его влияния на состав микробиоты ЖКТ, как рассмотрено в [75]. Однако в отношении его влияния на желудок существуют лишь ограниченные исследования: одно исследование ex vivo изучало влияние Trp на секрецию кислоты в желудках свиней на откорме [30], и одно исследование in vivo изучало его влияние на экспрессию грелина в желудке поросят после отъема [76].
Недавние исследования показывают, что текущие рекомендованные NRC уровни Trp могут быть неоптимальными для послеотъемной продуктивности [41,43,77]. В мета-регрессионном анализе Chae и др. [43] определили, что 0,21 SID Trp:Lys является оптимальным для эффективности корма у поросят массой 7–11 кг. В мета-анализе Simongiovanni и др. [78] определили, что 0,22 SID Trp:Lys является оптимальным для среднесуточного прироста и ADFI и 0,20 для эффективности корма, хотя выбор модели может иметь значение. Однако трудно определить оптимальные уровни включения, так как потребности в Trp могут различаться в зависимости от патогенной нагрузки окружающей среды и степени воспаления в ЖКТ [79,80]. Рекомендованные NRC уровни включения для поросят массой 5–7 кг и 7–11 кг основаны на предполагаемом суточном потреблении 280 г/день и 493 г/день и соответствуют потреблению Trp 0,7 г/день и 1,2 г/день соответственно [39]. Среднее потребление может сильно варьироваться от исследования к исследованию, особенно в непосредственный послеотъемный период. Это часто упускается из виду в литературе, и поэтому полезно рассчитывать и представлять общее потребление Trp в день. В настоящем исследовании анализировалось влияние трех различных уровней включения Trp (0,22 против 0,27 против 0,33% SID Trp, 1,3% SID лизина, что соответствует SID Trp:Lys 0,17, 0,21 и 0,25) в пред- и послеотъемных рационах на продуктивность и параметры желудка при отъеме и через 7 дней после отъема.
В текущем исследовании повышение уровня включения Trp до и после отъема не оказало влияния на продуктивность роста до отъема или в первые 7 дней после отъема. Средняя начальная масса тела для послеотъемного периода составляла 7,8 кг, а ADFI с 0 по 7 день после отъема составляло 0,27 кг во всех диетических группах. Эти показатели потребления сопоставимы с другими исследованиями для первой недели после отъема [40,81]. Не было статистической разницы в потреблении Trp в день в послеотъемный период между диетическими группами; однако потребление Trp в день численно увеличивалось с увеличением уровня включения Trp в рацион (0,22% Trp = 0,63 г/день, 0,27% Trp = 0,72 г/день, 0,33% Trp = 0,77 г/день). В исследовании Capozzalo и др. [40] не было влияния повышенного Trp на продуктивность с 1 по 8 день после отъема; однако с 8 по 15 день повышенный Trp улучшил среднесуточный прирост, ADFI и FCR, причем уровень 0,23 SID Trp:Lys, что соответствует примерно 0,31% включения SID Trp, оптимизировал как среднесуточный прирост, так и FCR в течение первых двух недель после отъема. Таким образом, необходимо дальнейшее изучение эффектов повышенного уровня Trp после отъема за пределами первой недели после отъема.
Не было заметных эффектов уровня включения Trp на экспрессию генов в области фундальных или пилорических желез или на количество париетальных клеток в области фундальных желез, а также не было заметных взаимодействий рацион свиноматки × предстартерный рацион. Потребление предстартерного корма до отъема было крайне ограниченным, что могло помешать потенциальным эффектам на желудок при отъеме, хотя потребление после отъема было достаточным, и все же не было эффекта на экспрессию генов в области фундальных или пилорических желез или на количество париетальных клеток. Это удивительно, поскольку в предыдущих исследованиях Trp стимулировал CaSR [30,82] и запускал секрецию гастрина и соматостатина и повышал активность H+/K+-АТФазы в образцах ткани желудка свиньи ex vivo [30]. Отсутствие эффектов после отъема может быть связано с несколькими потенциальными причинами, такими как слишком близкие уровни включения для наблюдения дифференциальной экспрессии между группами, или сложность среды желудка in vivo, включая большие колебания типов и уровней поступающих питательных веществ, может быть сбивающим фактором.
Примечательным в корреляционном анализе текущего исследования была положительная корреляция между потреблением предстартерного корма до отъема и экспрессией генов секреции кислоты, генов пищеварительных ферментов и грелина в области фундальных желез при отъеме. Это согласуется с ранним исследованием Cranwell и др. [19], в котором предотъемное кормление предстартерным кормом увеличило секреторную способность кислоты и пепсина. Кроме того, в момент отъема наблюдалась отрицательная корреляция между генами, связанными с иммунитетом, в частности CXCL8, IL22 и TLR4, и экспрессией генов, связанных с областью фундальных желез, таких как гены, связанные с секрецией кислоты и ферментов. Аналогичные результаты сообщались ранее у поросят после отъема [18]; однако в текущем исследовании корреляции были очевидны только при отъеме, а не через 7 дней после отъема. Удивительно, но экспрессия генов, связанная с активностью париетальных клеток, не коррелировала с количеством париетальных клеток (ATP4B+ клетки) ни при отъеме, ни через 7 дней после отъема. Это может быть связано с тем, что париетальные клетки могут присутствовать в желудке в раннем возрасте, но быть функционально незрелыми. Trevisi и др. [1] отметили, что у молодых поросят часто наблюдаются морфологические признаки, указывающие на незрелость области фундальных желез, причем одним из признаков является атипичная форма H+/K+-АТФаза-иммунореактивных клеток.
Сосредоточившись на корреляциях экспрессии CASR, экспрессия CASR при отъеме была положительно коррелирована с pH желудка и ингибированием секреции кислоты в области фундальных желез (SST и SSTR2) и экспрессией GHRL. Кроме того, при отъеме и через 7 дней после отъема (см. Приложение A: Рисунок A1 и Рисунок A2) CASR был положительно коррелирован с экспрессией как GAST, так и SST в области пилорических желез. Это несколько подтверждает роль CaSR в регуляции секреции кислоты в ответ на просветный pH [28] и что секреция соматостатина связана с CaSR [30]. Однако, удивительно, экспрессия CASR была отрицательно коррелирована с экспрессией генов стимуляции кислоты (HRH2, CCKBR, CHRM3, HDC) и секреции кислоты (ATP4A, CLIC6, KCNE1, KCNQ1) при отъеме. Через 7 дней после отъема экспрессия CASR в области фундальных желез, как и при отъеме, коррелировала с экспрессией GHRL, но не с какими-либо генами, связанными с секрецией кислоты. Наблюдалась положительная корреляция между номером опороса свиноматки и CASR в области фундальных желез после отъема. Номер опороса свиноматки, особенно свинки по сравнению со свиноматками, часто упоминается как фактор, влияющий на развитие и продуктивность их потомства [83,84], поэтому текущее исследование включило номер опороса в корреляционный анализ. Однако номер опороса свиноматки не коррелировал ни с какими пред- или послеотъемными параметрами продуктивности, в то время как до отъема номер опороса свиноматки коррелировал только с экспрессией генов продукции слизи в области пилорических желез.
5. Выводы
Улучшение развития желудка поросенка в раннем возрасте является важной областью исследований, так как это может снизить восприимчивость поросенка к инфекциям и улучшить пищеварительную функцию, что особенно важно в непосредственный послеотъемный период. Настоящая работа дает представление об изменениях в области фундальных и пилорических желез поросят при отъеме по сравнению с 7 днями после отъема. Эти изменения характеризовались в основном увеличением количества париетальных клеток, повышением экспрессии генов, участвующих в активности париетальных клеток, и изменением экспрессии генов пищеварительных ферментов в области фундальных желез. Однако экспрессия сигнальных молекул, участвующих в регуляции секреции кислоты, не изменилась в области фундальных желез и снизилась в области пилорических желез по сравнению с днем отъема. При анализе влияния рациона уровень Trp в рационе поросенка оказал минимальное влияние на продуктивность или желудок, хотя низкое потребление предстартерного корма до отъема могло ограничить любое потенциальное влияние в предотъемный период. В целом, добавление Bacillus subtilis и Bacillus amyloliquefaciens свиноматкам с 83-го дня супоросности оказало значительное влияние на экспрессию генов в области фундальных желез потомства, повышая экспрессию нескольких генов, связанных с активностью париетальных клеток и путем секреции кислоты. Когда гены были сгруппированы по функции, у поросят от свиноматок, получавших пробиотик, наблюдалась повышенная экспрессия генов секреции кислоты и продукции слизи. Эти изменения экспрессии генов свидетельствуют о том, что добавление пробиотиков свиноматкам ускорило созревание желудка потомства. Однако добавление пробиотиков свиноматкам не повлияло на продуктивность роста в предотъемный период или в течение 7-дневного послеотъемного периода. Необходимы дальнейшие исследования, чтобы лучше понять механизмы, с помощью которых добавление пробиотиков свиноматкам влияет на развитие и функцию желудка потомства, а также долгосрочные последствия для продуктивности животных.
Приложение А
Ссылки
1. Trevisi, P.; Luise, D.; Correa, F.; Messori, S.; Mazzoni, M.; Lallès, J.P.; Bosi, P. Maternal antibiotic treatment affects offspring gastric sensing for umami taste and ghrelin regulation in the pig. J. Anim. Sci. Biotechnol. 2021, 12, 31. [Google Scholar] [CrossRef]
2. Du, G.M.; Shi, Z.M.; Wei, X.H.; Liu, M.J.; Zhang, L.; Zhao, R.Q. Expression of gastric ghrelin and H+–K+-ATPase MRNA in weanling piglets and effect of ghrelin on H+–K+-ATPase expression and activity in gastric mucosal cells in vitro. Res. Vet. Sci. 2007, 82, 99–104. [Google Scholar] [CrossRef]
3. Cranwell, P.; Moughan, P. Biological limitations imposed by the digestive system to the growth performance of weaned pigs. In Manipulating Pig Produduction II, Proceedings of the Biennial Conference of the Australasian Pig Science Association, Albury, Australia, 27–29 November 1989; Australasian Pig Science Association: Werribee, Australia, 1989; pp. 140–160. [Google Scholar]
4. Cranwell, P.; Noakes, D.; Hill, K. Gastric secretion and fermentation in the suckling pig. Br. J. Nutr. 1976, 36, 71–86. [Google Scholar] [CrossRef] [PubMed]
5. Suiryanrayna, M.V.A.N.; Ramana, J.V. A review of the effects of dietary organic acids fed to swine. J. Anim. Sci. Biotechnol. 2015, 6, 45. [Google Scholar] [CrossRef] [PubMed]
6. Hedemann, M.S.; Jensen, B.B. Variations in enzyme activity in stomach and pancreatic tissue and digesta in piglets around weaning. Arch. Anim. Nutr. 2004, 58, 47–59. [Google Scholar] [CrossRef] [PubMed]
7. Henry, R.; Pickard, D.; Hughes, P. Citric acid and fumaric acid as food additives for early-weaned piglets. Anim. Sci. 1985, 40, 505–509. [Google Scholar] [CrossRef]
8. Canibe, N.; Højberg, O.; Højsgaard, S.; Jensen, B.B. Feed physical form and formic acid addition to the feed affect the gastrointestinal ecology and growth performance of growing pigs. J. Anim. Sci. 2005, 83, 1287–1302. [Google Scholar] [CrossRef] [PubMed]
9. Nowak, P.; Zaworska-Zakrzewska, A.; Frankiewicz, A.; Kasprowicz-Potocka, M. Accepted Author Version of the Manuscript: The effects and mechanisms of acids on the health of piglets and weaners—A review. Ann. Anim. Sci. 2020, 21, 433–455. [Google Scholar]
10. Lawlor, P.G.; Lynch, P.B.; Caffrey, P.J. Effect of Fumaric Acid, Calcium Formate and Mineral Levels in Diets on the Intake and Growth Performance of Newly Weaned Pigs. Ir. J. Agric. Food Res. 2006, 45, 61–71. [Google Scholar]
11. Stas, E.B.; Tokach, M.D.; DeRouchey, J.M.; Goodband, R.D.; Woodworth, J.C.; Gebhardt, J.T. Evaluation of the acid-binding capacity of ingredients and complete diets commonly used for weanling pigs. Transl. Anim. Sci. 2022, 6, txac104. [Google Scholar] [CrossRef] [PubMed]
12. Wang, L.; Bergstrom, J.; Hahn, J.; Young, M.; Zijlstra, R. Acid-binding capacity of feed in swine nutrition. Anim. Feed. Sci. Technol. 2023, 295, 115519. [Google Scholar] [CrossRef]
13. Sangild, P.T.; Fowden, A.L.; Trahair, J.F. How does the foetal gastrointestinal tract develop in preparation for enteral nutrition after birth? Livest. Prod. Sci. 2000, 66, 141–150. [Google Scholar] [CrossRef]
14. Sangild, P.T.; Schmidt, M.; Elnif, J.; Björnvad, R.; Weström, B.R.; Buddington, B.K. Prenatal development of gastrointestinal function in the pig and the effects of fetal esophageal obstruction. Pediatr. Res. 2002, 52, 416–424. [Google Scholar] [CrossRef]
15. Trevisi, P.; Gandolfi, G.; Priori, D.; Messori, S.; Colombo, M.; Mazzoni, M.; Lallès, J.-P.; Bosi, P. Age-Related Expression of the Polymeric Immunoglobulin Receptor (pIgR) in the Gastric Mucosa of Young Pigs. PLoS ONE 2013, 8, e81473. [Google Scholar] [CrossRef]
16. Colombo, M.; Priori, D.; Trevisi, P.; Bosi, P. Differential Gene Expression in the Oxyntic and Pyloric Mucosa of the Young Pig. PLoS ONE 2014, 9, e111447. [Google Scholar] [CrossRef] [PubMed]
17. Fothergill, L.J.; Galiazzo, G.; Hunne, B.; Stebbing, M.J.; Fakhry, J.; Weissenborn, F.; Coles, T.E.F.; Furness, J.B. Distribution and co-expression patterns of specific cell markers of enteroendocrine cells in pig gastric epithelium. Cell Tissue Res. 2019, 378, 457–469. [Google Scholar] [CrossRef]
18. Kiernan, D.P.; O’doherty, J.V.; Connolly, K.R.; Ryan, M.; Sweeney, T. Exploring the Differential Expression of a Set of Key Genes Involved in the Regulation and Functioning of the Stomach in the Post-Weaned Pig. Vet. Sci. 2023, 10, 473. [Google Scholar] [CrossRef] [PubMed]
19. Cranwell, P.D. The development of acid and pepsin (EC 3. 4. 23. 1) secretory capacity in the pig; the effects of age and weaning: 1. Studies in anaesthetized pigs. Br. J. Nutr. 1985, 54, 305–320. [Google Scholar] [CrossRef] [PubMed]
20. Bosi, P.; Maurizio, M.; Sara, D.F.; Paolo, T.; Luisa, C.; Gregorio, P.; Giovanna, L.-C. A continuous dietary supply of free calcium formate negatively affects the parietal cell population and gastric RNA expression for H+/K+-ATPase in weaning pigs. J. Nutr. 2006, 136, 1229–1235. [Google Scholar] [CrossRef] [PubMed][Green Version]
21. Mazzoni, M.; Le Gall, M.; De Filippi, S.; Minieri, L.; Trevisi, P.; Wolinski, J.; Lalatta-Costerbosa, G.; Lallès, J.-P.; Guilloteau, P.; Bosi, P. Supplemental Sodium Butyrate Stimulates Different Gastric Cells in Weaned Pigs. J. Nutr. 2008, 138, 1426–1431. [Google Scholar] [CrossRef]
22. Colombo, M.; Priori, D.; Gandolfi, G.; Boatto, G.; Nieddu, M.; Bosi, P.; Trevisi, P. Effect of free thymol on differential gene expression in gastric mucosa of the young pig. Animal 2014, 8, 786–791. [Google Scholar] [CrossRef] [PubMed]
23. Luise, D.; Motta, V.; Salvarani, C.; Chiappelli, M.; Fusco, L.; Bertocchi, M.; Mazzoni, M.; Maiorano, G.; Costa, L.N.; Van Milgen, J.; et al. Long-term administration of formic acid to weaners: Influence on intestinal microbiota, immunity parameters and growth performance. Anim. Feed. Sci. Technol. 2017, 232, 160–168. [Google Scholar] [CrossRef]
24. Trevisi, P.; Priori, D.; Motta, V.; Luise, D.; Jansman, A.J.M.; Koopmans, S.-J.; Bosi, P. Effects of starter microbiota and the early life feeding of medium chain triglycerides on the gastric transcriptome profile of 2-or 3-week-old cesarean delivered piglets. J. Anim. Sci. Biotechnol. 2017, 8, 82. [Google Scholar] [CrossRef] [PubMed]
25. Maher, S.; Sweeney, T.; Kiernan, D.P.; Ryan, M.T.; Gath, V.; Vigors, S.; Connolly, K.R.; O’doherty, J.V. Organic acid preservation of cereal grains improves grain quality, growth performance, and intestinal health of post-weaned pigs. Anim. Feed. Sci. Technol. 2024, 316, 116078. [Google Scholar] [CrossRef]
26. Connolly, K.R.; Sweeney, T.; Kiernan, D.; Round, A. The Role of Propionic Acid as a Feed Additive and Grain Preservative on Weanling Pig Performance and Digestive Health. 2024. Available online: https://ssrn.com/abstract=4919186 (accessed on 18 October 2024).
27. Lerch, F.; Yosi, F.; Vötterl, J.C.; Koger, S.; Ehmig, J. An insight into the temporal dynamics in the gut microbiome, metabolite signaling, immune response, and barrier function in suckling and weaned piglets under production conditions. Front. Vet. Sci. 2023, 10. [Google Scholar] [CrossRef]
28. Quinn, S.J.; Bai, M.; Brown, E.M. pH Sensing by the calcium-sensing receptor. J. Biol. Chem. 2004, 279, 37241–37249. [Google Scholar] [CrossRef] [PubMed]
29. Busque, S.M.; Kerstetter, J.E.; Geibel, J.P.; Insogna, K. l-Type amino acids stimulate gastric acid secretion by activation of the calcium-sensing receptor in parietal cells. Am. J. Physiol.-Gastrointest. Liver Physiol. 2005, 289, G664–G669. [Google Scholar] [CrossRef]
30. Xian, Y.; Zhao, X.; Wang, C.; Kang, C.; Ding, L.; Zhu, W.; Hang, S. Phenylalanine and tryptophan stimulate gastrin and somatostatin secretion and H+-K+-ATPase activity in pigs through calcium-sensing receptor. Gen. Comp. Endocrinol. 2018, 267, 1–8. [Google Scholar] [CrossRef]
31. Casare, F.; Milan, D.; Fernandez, R. Stimulation of calcium-sensing receptor increases biochemical H+-ATPase activity in mouse cortex and outer medullary regions. Can. J. Physiol. Pharmacol. 2013, 92, 181–188. [Google Scholar] [CrossRef]
32. Dufner, M.M.; Kirchhoff, P.; Remy, C.; Hafner, P. The calcium-sensing receptor acts as a modulator of gastric acid secretion in freshly isolated human gastric glands. Am. J. Physiol.-Gastrointest. Liver Physiol. 2005, 289, G1084–G1090. [Google Scholar] [CrossRef] [PubMed][Green Version]
33. Kiernan, D.P.; O’Doherty, J.V.; Sweeney, T. The effect of maternal probiotic or synbiotic supplementation on sow and offspring microbiome, health, and performance. Animals 2023, 13, 2996. [Google Scholar] [CrossRef] [PubMed]
34. Ali, M.S.; Lee, E.-B.; Hsu, W.H.; Suk, K.; Sayem, S.A.J.; Ullah, H.M.A.; Lee, S.-J.; Park, S.-C. Probiotics and Postbiotics as an Alternative to Antibiotics: An Emphasis on Pigs. Pathogens 2023, 12, 874. [Google Scholar] [CrossRef] [PubMed]
35. Babińska, I.; Rotkiewicz, T.; Otrocka-Domagała, I. The effect of Lactobacillus acidophilus and Bifidobacterium spp. administration on the morphology of the gastrointestinal tract, liver and pancreas in piglets. Pol. J. Vet. Sci. 2005, 8, 29–35. [Google Scholar] [PubMed]
36. Chen, X.; Xu, J.; Ren, E.; Su, Y.; Zhu, W. Co-occurrence of early gut colonization in neonatal piglets with microbiota in the maternal and surrounding delivery environments. Anaerobe 2018, 49, 30–40. [Google Scholar] [CrossRef]
37. Adams, S.; Knapp, J.P.; Neujahr, A.; Burkey, T.; Miller, P.S. 276 Investigating the Colonization History of Early-Life Microbiome of Piglets. J. Anim. Sci. 2023, 101 (Suppl. S2), 165–166. [Google Scholar]
38. Sauvant, D.; Perez, J.-M.; Tran, G. Tables of Composition and Nutritional Value of Feed Materials: Pigs, Poultry, Cattle, Sheep, Goats, Rabbits, Horses and Fish; Brill: Leiden, The Netherlands, 2023. [Google Scholar]
39. NRC. Nutrient Requirements of Swine, 11th ed.; National Academies Press: Washington, DC, USA, 2012. [Google Scholar]
40. Capozzalo, M.; Kim, J.; Htoo, J.; de Lange, C.; Mullan, B.; Resink, J.; Hansen, C.; Stumbles, P.; Hampson, D.; Ferguson, N.; et al. Estimating the standardised ileal digestible tryptophan requirement of pigs kept under commercial conditions in the immediate post-weaning period. Anim. Feed. Sci. Technol. 2020, 259, 114342. [Google Scholar] [CrossRef]
41. Capozzalo, M.M.; Kim, J.C.; Htoo, J.K.; de Lange, J.F. Effect of increasing the dietary tryptophan to lysine ratio on plasma levels of tryptophan, kynurenine and urea and on production traits in weaner pigs experimentally infected with an enterotoxigenic strain of Escherichia coli. Arch. Anim. Nutr. 2015, 69, 17–29. [Google Scholar] [CrossRef] [PubMed]
42. Capozzalo, M.M.; Kim, J.C.; Htoo, J.K.; de Lange, C.F.M.; Mullan, B.P.; Hansen, C.F.; Resink, J.W.; Stumbles, P.A.; Hampson, D.J.; Pluske, J.R. An increased ratio of dietary tryptophan to lysine improves feed efficiency and elevates plasma tryptophan and kynurenine in the absence of antimicrobials and regardless of infection with enterotoxigenic Escherichia coli in weaned pigs. J. Anim. Sci. 2012, 90 (Suppl. S4), 191–193. [Google Scholar] [CrossRef] [PubMed]
43. Chae, B.; Poaty Ditengou, J.I.C.; Lee, A.-L.; Tak, J.; Cheon, I.; Choi, N.-J. An Estimation of the Requirements of the Standardized Ileal Digestible Tryptophan, Valine, Isoleucine and Methionine on Young Pigs’ (Up to 50 kg) Feed Efficiency: A Meta-Regression Analysis. Animals 2024, 14, 2884. [Google Scholar] [CrossRef]
44. Lamas, B.; Natividad, J.M.; Sokol, H. Aryl hydrocarbon receptor and intestinal immunity. Mucosal Immunol. 2018, 11, 1024–1038. [Google Scholar] [CrossRef] [PubMed]
45. Sun, M.; Ma, N.; He, T.; Johnston, L.J.; Ma, X. Tryptophan (Trp) modulates gut homeostasis via aryl hydrocarbon receptor (AhR). Crit. Rev. Food Sci. Nutr. 2020, 60, 1760–1768. [Google Scholar] [CrossRef]
46. AOAC. Official Methods of Analysis of AOAC International; AOAC International Gaithersburg: Gaithersburg, MD, USA, 2005; Volume 1. [Google Scholar]
47. Van Soest, P.V.; Robertson, J.B.; Lewis, B.A. Methods for dietary fiber, neutral detergent fiber, and nonstarch polysaccharides in relation to animal nutrition. J. Dairy Sci. 1991, 74, 3583–3597. [Google Scholar] [CrossRef] [PubMed]
48. Iwaki, K.; Nimura, N.; Hiraga, Y.; Kinoshita, T.; Takeda, K.; Ogura, H. Amino acid analysis by reversed-phase high-performance liquid chromatography. Automatic pre-column derivatization with activated carbamate reagent. J. Chromatogr. 1987, 407, 273–279. [Google Scholar] [CrossRef] [PubMed]
49. Harrell, F.E. Package ‘hmisc’. CRAN2018 2019, 2019, 235–236. [Google Scholar]
50. Barret Schloerke, D.C.; Larmarange, J.; Briatte, F.; Marback, M.; Theon, E.; Elberg, A.; Toomet, O.; Crowley, J. GGally: Extension to ‘ggplot2’, R package version 2.2.1. 2024.
51. O’Doherty, J.V.; Kiernan, D.P.; Sweeney, T. Advances in understanding pig digestive physiology. In Advances in Pig Nutrition; Wiseman, J., Ed.; Burleigh Dodds Science Publishing: Cambridge, UK, 2024. [Google Scholar]
52. Dos Santos, P.M.C.; Amaral, D.; Tararthuch, A.L.; Fernandez, R. Calcium-sensing receptor (CaSR) modulates vacuolar H+-ATPase activity in a cell model of proximal tubule. Clin. Exp. Nephrol. 2018, 22, 1258–1265. [Google Scholar] [CrossRef]
53. Cheng, Y.; Ding, S.; Azad, A.K.; Song, B.; Kong, X. Small Intestinal Digestive Functions and Feed Efficiency Differ in Different Pig Breeds. Animals 2023, 13, 1172. [Google Scholar] [CrossRef]
54. Liu, G.; Mo, W.; Cao, W.; Jia, G.; Zhao, H.; Chen, X.; Wu, C.; Zhang, R.; Wang, J. Digestive abilities, amino acid transporter expression, and metabolism in the intestines of piglets fed with spermine. J. Food Biochem. 2020, 44, e13167. [Google Scholar] [CrossRef] [PubMed]
55. Lallès, J.P.; Sève, B.; Pié, S.; Blazy, F.; Laffitte, J.; Oswald, I.P.; Sève, B. Weaning Is Associated with an Upregulation of Expression of Inflammatory Cytokines in the Intestine of Piglets. J. Nutr. 2004, 134, 641–647. [Google Scholar] [CrossRef]
56. Bomba, L.; Minuti, A.; Moisá, S.J.; Trevisi, E.; Eufemi, E.; Lizier, M.; Chegdani, F.; Lucchini, F.; Rzepus, M.; Prandini, A.; et al. Gut response induced by weaning in piglet features marked changes in immune and inflammatory response. Funct. Integr. Genom. 2014, 14, 657–671. [Google Scholar] [CrossRef]
57. Dong, X.-Y.; Xu, J.; Tang, S.-Q.; Li, H.-Y.; Jiang, Q.-Y.; Zou, X.-T. Ghrelin and its biological effects on pigs. Peptides 2009, 30, 1203–1211. [Google Scholar] [CrossRef] [PubMed]
58. Scrimgeour, K.; Gresham, M.J.; Giles, L.R.; Thomson, P.C.; Wynn, P.C.; E Newman, R. Ghrelin secretion is more closely aligned to energy balance than with feeding behaviour in the grower pig. J. Endocrinol. 2008, 198, 135. [Google Scholar] [CrossRef] [PubMed][Green Version]
59. Akira, S.; Takeda, K. Toll-like receptor signalling. Nat. Rev. Immunol. 2004, 4, 499–511. [Google Scholar] [CrossRef]
60. Pang, J.; Liu, Y.; Kang, L.; Ye, H.; Zang, J.; Wang, J.; Han, D. Bifidobacterium animalis promotes the growth of weaning piglets by improving intestinal development, enhancing antioxidant capacity, and modulating gut microbiota. Appl. Environ. Microbiol. 2022, 88, e01296-22. [Google Scholar] [CrossRef] [PubMed]
61. Zhang, W.; Zhu, Y.-H.; Zhou, D.; Wu, Q.; Song, D.; Dicksved, J.; Wang, J.-F. Oral Administration of a Select Mixture of Bacillus Probiotics Affects the Gut Microbiota and Goblet Cell Function following Escherichia coli Challenge in Newly Weaned Pigs of Genotype MUC4 That Are Supposed To Be Enterotoxigenic E. coli F4ab/ac Receptor Negative. Appl. Environ. Microbiol. 2017, 83, e02747-16. [Google Scholar]
62. Desantis, S.; Mastrodonato, M.; Accogli, G.; Rossi, G.; Crovace, A.M. Effects of a probiotic on the morphology and mucin composition of pig intestine. Histol. Histopathol. 2019, 34, 1037–1050. [Google Scholar] [PubMed]
63. Barbosa, A.M.S.; Carvalho, M.P.S.; Naves, L.d.P.; da Motta, S.A.B.; Chaves, R.F.; Resende, M.; de Lima, D.; Hansen, L.H.B.; Cantarelli, V.D.S. Performance and Health Parameters of Sows and Their Litters Using a Probiotic Supplement Composed of Bacillus subtilis 541 and Bacillus amyloliquefaciens 516. Animals 2024, 14, 3511. [Google Scholar] [CrossRef] [PubMed]
64. Konieczka, P.; Ferenc, K.; Jørgensen, J.N.; Hansen, L.H.; Zabielski, R.; Olszewski, J.; Gajewski, Z.; Mazur-Kuśnirek, M.; Szkopek, D.; Szyryńska, N.; et al. Feeding Bacillus-based probiotics to gestating and lactating sows is an efficient method for improving immunity, gut functional status and biofilm formation by probiotic bacteria in piglets at weaning. Anim. Nutr. 2023, 13, 361–372. [Google Scholar] [CrossRef] [PubMed]
65. Mazur-Kuśnirek, M.; Lipiński, K.; Jørgensen, J.N.; Hansen, L.H.B.; Antoszkiewicz, Z.; Zabielski, R.; Konieczka, P. The Effect of a Bacillus-Based Probiotic on Sow and Piglet Performance in Two Production Cycles. Animals 2023, 13, 3163. [Google Scholar] [CrossRef] [PubMed]
66. Crespo-Piazuelo, D.; Gardiner, G.E.; Ranjitkar, S.; Bouwhuis, M.A.; Ham, R.; Phelan, J.P.; Marsh, A.; Lawlor, P.G. Maternal supplementation with Bacillus altitudinis spores improves porcine offspring growth performance and carcass weight. Br. J. Nutr. 2022, 127, 403–420. [Google Scholar] [CrossRef] [PubMed]
67. Liu, H.; Zeng, X.; Zhang, G.; Hou, C.; Li, N.; Yu, H.; Shang, L.; Zhang, X.; Trevisi, P.; Yang, F.; et al. Maternal Breast Milk and Fecal Microbes Guide the Spatiotemporal Development of Mucosa-Associated Microbiota and Barrier Function in the Neonatal Gut. 2019. Available online: https://ssrn.com/abstract=3403346 (accessed on 18 July 2024).
68. Lim, J.-A.; Cha, J.; Choi, S.; Kim, J.-H.; Kim, D. Early Colonization of the Intestinal Microbiome of Neonatal Piglets Is Influenced by the Maternal Microbiome. Animals 2023, 13, 3378. [Google Scholar] [CrossRef]
69. Liu, S.; Zhang, Z.; Ma, L. A Review Focusing on Microbial Vertical Transmission during Sow Pregnancy. Vet. Sci. 2023, 10, 123. [Google Scholar] [CrossRef] [PubMed]
70. Quan, J.; Xu, C.; Ruan, D.; Ye, Y.; Qiu, Y.; Wu, J.; Zhou, S.; Luan, M.; Zhao, X.; Chen, Y.; et al. Composition, function, and timing: Exploring the early-life gut microbiota in piglets for probiotic interventions. J. Anim. Sci. Biotechnol. 2023, 14, 143. [Google Scholar] [CrossRef] [PubMed]
71. FAO; WHO. Health and nutritional properties of probiotics in food including powder milk with live lactic acid bacteria. Prevention 2001, 5, 1–10. [Google Scholar]
72. Baker, A.A.; Davis, E.; Spencer, J.D.; Moser, R.; Rehberger, T. The effect of a Bacillus-based direct-fed microbial supplemented to sows on the gastrointestinal microbiota of their neonatal piglets. J. Anim. Sci. 2013, 91, 3390–3399. [Google Scholar] [CrossRef] [PubMed]
73. Zhao, X.; Pang, J.; Zhang, W.; Peng, X.; Yang, Z.; Bai, G.; Xia, Y. Tryptophan metabolism and piglet diarrhea: Where we stand and the challenges ahead. Anim. Nutr. 2024, 17, 123–133. [Google Scholar] [CrossRef]
74. Hu, Z.; Feng, L.; Jiang, Q.; Wang, W.; Tan, B.; Tang, X.; Yin, Y. Intestinal tryptophan metabolism in disease prevention and swine production. Anim. Nutr. 2023, 15, 364–374. [Google Scholar] [CrossRef]
75. Kiernan, D.P.; O’Doherty, J.V.; Sweeney, T. The effect of prebiotic supplements on the gastrointestinal microbiota and associated health parameters in the pig. Animals 2023, 13, 3012. [Google Scholar] [CrossRef]
76. Zhang, H.; Yin, J.; Li, D.; Zhou, X.; Li, X. Tryptophan enhances ghrelin expression and secretion associated with increased food intake and weight gain in weanling pigs. Domest. Anim. Endocrinol. 2007, 33, 47–61. [Google Scholar] [CrossRef]
77. Chen, C.; Hu, H.; Li, Z.; Qi, M.; Qiu, Y.; Hu, Z.; Feng, F.; Tang, W.; Diao, H.; Sun, W.; et al. Dietary tryptophan improves growth and intestinal health by promoting the secretion of intestinal β-defensins against enterotoxigenic Escherichia coli F4 in weaned piglets. J. Nutr. Biochem. 2024, 129, 109637. [Google Scholar] [CrossRef]
78. Simongiovanni, A.; Corrent, E.; Le Floc’H, N.; van Milgen, J. Estimation of the tryptophan requirement in piglets by meta-analysis. Animal 2012, 6, 594–602. [Google Scholar] [CrossRef]
79. Le Floc’h, N.; Seve, B. Biological roles of tryptophan and its metabolism: Potential implications for pig feeding. Livest. Sci. 2007, 112, 23–32. [Google Scholar] [CrossRef]
80. Le Floc’H, N.; LeBellego, L.; Matte, J.J.; Melchior, D.; Sève, B. The effect of sanitary status degradation and dietary tryptophan content on growth rate and tryptophan metabolism in weaning pigs. J. Anim. Sci. 2009, 87, 1686–1694. [Google Scholar] [CrossRef] [PubMed]
81. Jayaraman, B.; Htoo, J.K.; Nyachoti, C.M. Effects of different dietary tryptophan: Lysine ratios and sanitary conditions on growth performance, plasma urea nitrogen, serum haptoglobin and ileal histomorphology of weaned pigs. Anim. Sci. J. 2017, 88, 763–771. [Google Scholar] [CrossRef]
82. Zhao, X.; Xian, Y.; Wang, C.; Ding, L.; Meng, X.; Zhu, W.; Hang, S. Calcium-sensing receptor-mediated L-tryptophan-induced secretion of cholecystokinin and glucose-dependent insulinotropic peptide in swine duodenum. J. Vet. Sci. 2018, 19, 179–187. [Google Scholar] [CrossRef] [PubMed]
83. Piñeiro, C.; Manso, A.; Manzanilla, E.G.; Morales, J. Influence of sows’ parity on performance and humoral immune response of the offspring. Porc. Health Manag. 2019, 5, 1. [Google Scholar] [CrossRef] [PubMed]
84. Craig, J.R.; Dunshea, F.R.; Cottrell, J.J.; Furness, J.B.; A Wijesiriwardana, U.; Pluske, J.R. A comparison of the anatomical and gastrointestinal functional development between gilt and sow progeny around birth and weaning. J. Anim. Sci. 2019, 97, 3809–3822. [Google Scholar] [CrossRef]
Kiernan DP, O’Doherty JV, Ryan MT, Sweeney T. Effects of Maternal Probiotics and Piglet Dietary Tryptophan Level on Gastric Function Pre- and Post-Weaning. Agriculture. 2025; 15(3):310. https://doi.org/10.3390/agriculture15030310
Перевод статьи «Effects of Maternal Probiotics and Piglet Dietary Tryptophan Level on Gastric Function Pre- and Post-Weaning» авторов Kiernan DP, O’Doherty JV, Ryan MT, Sweeney T., оригинал доступен по ссылке. Лицензия: CC BY. Изменения: переведено на русский язык
Фото: freepik
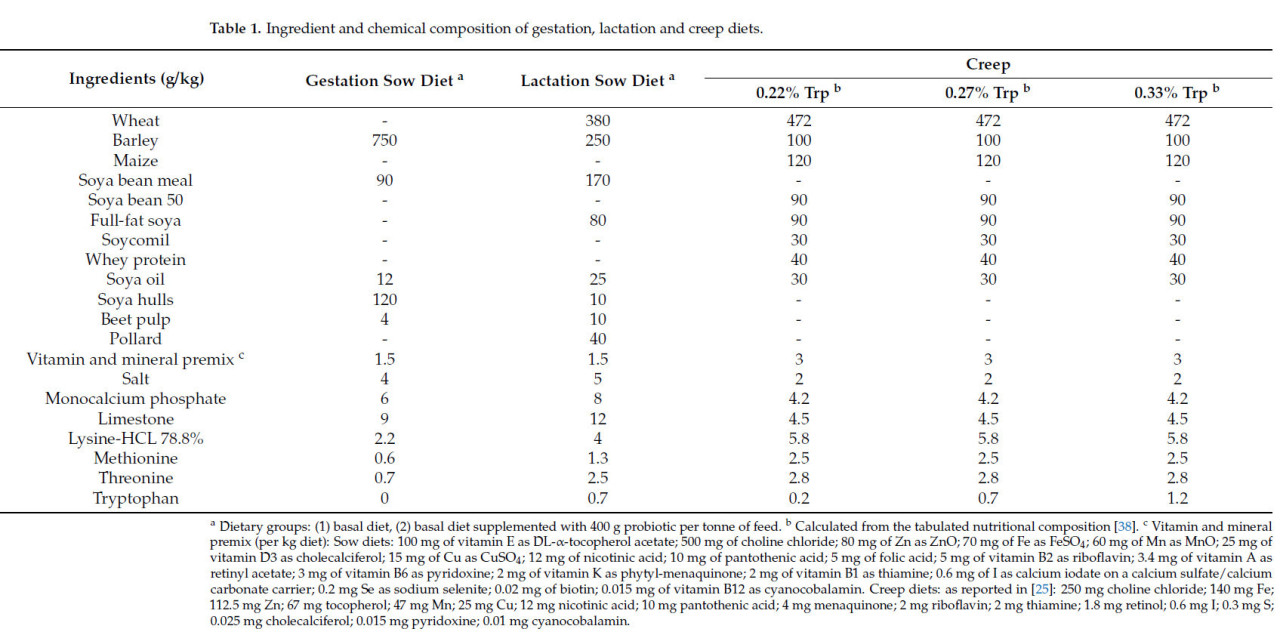
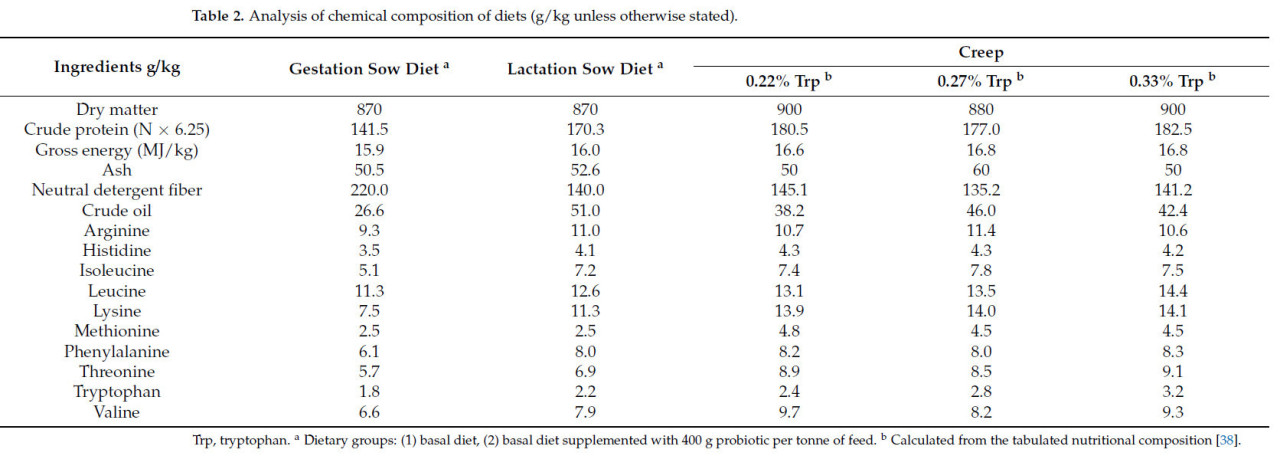

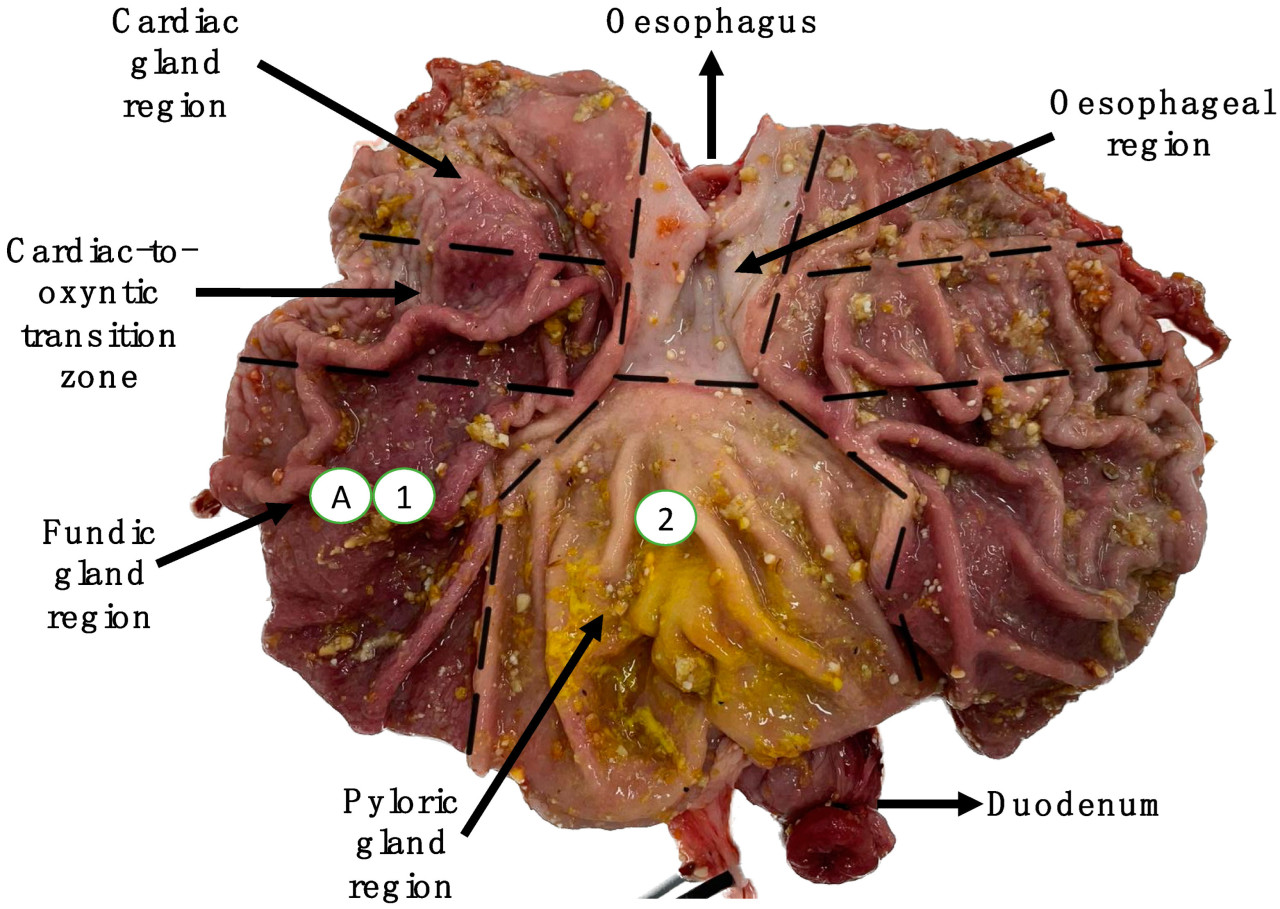
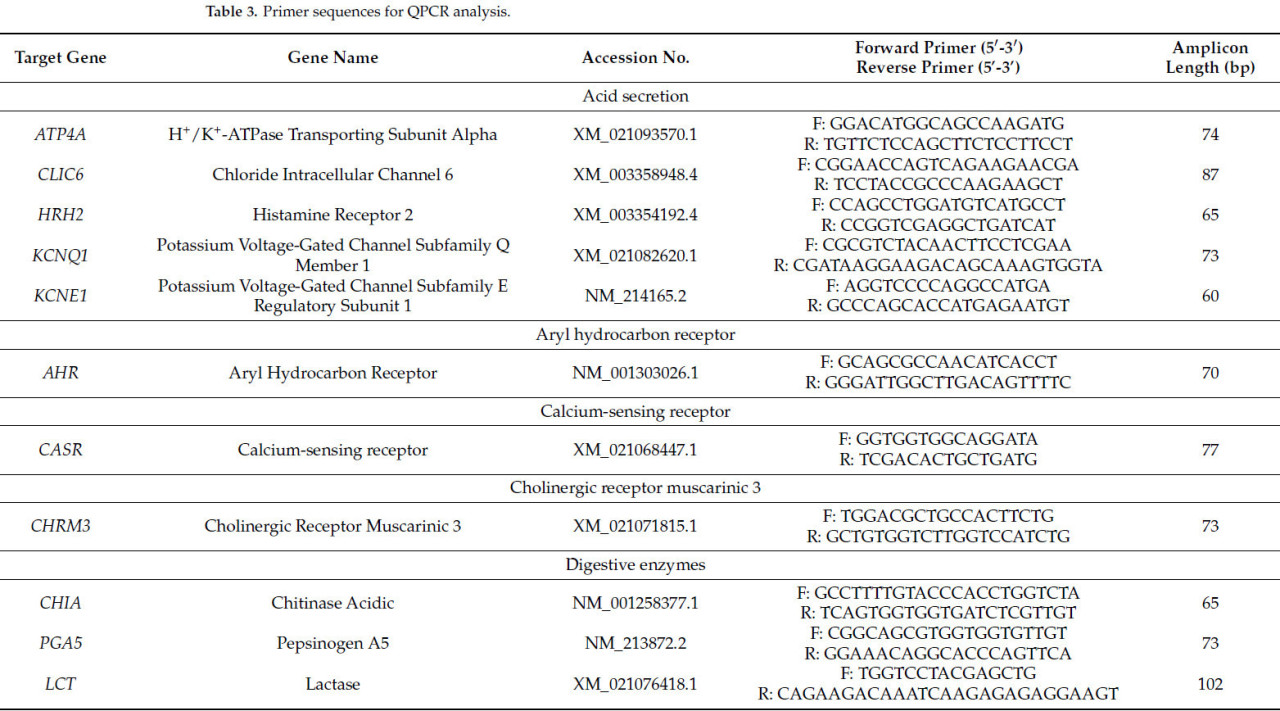
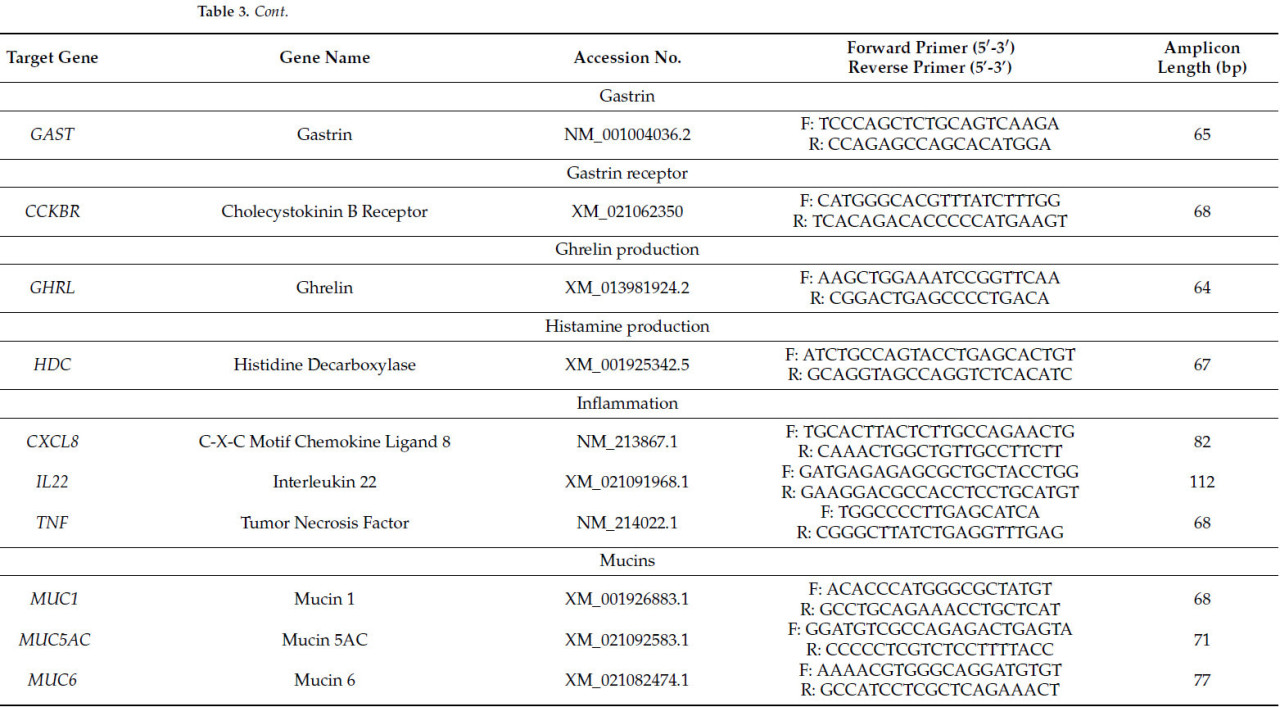
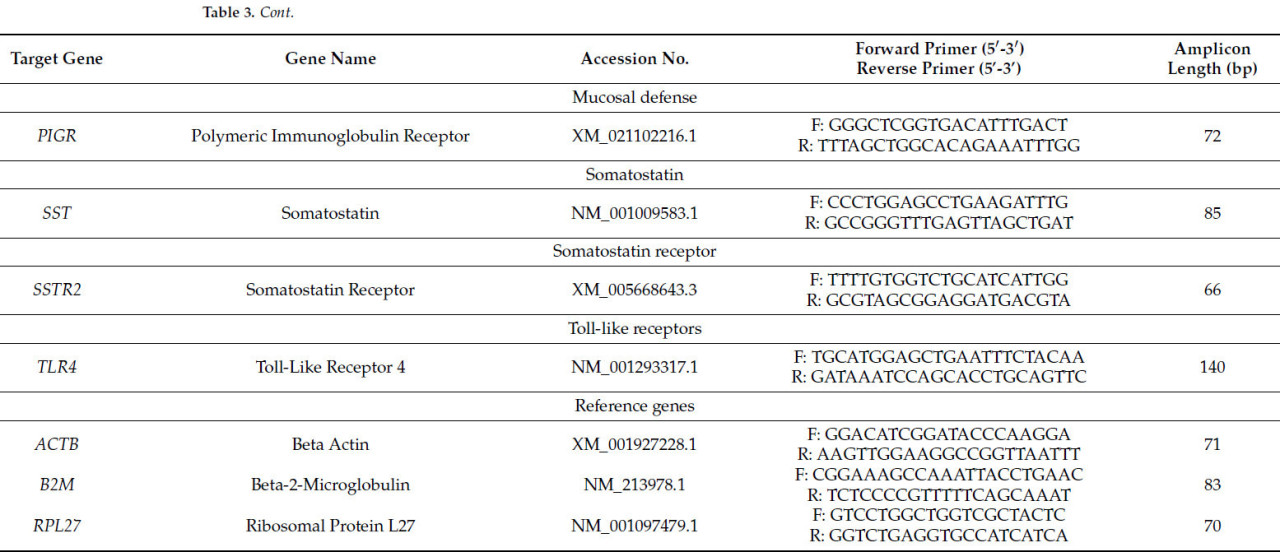
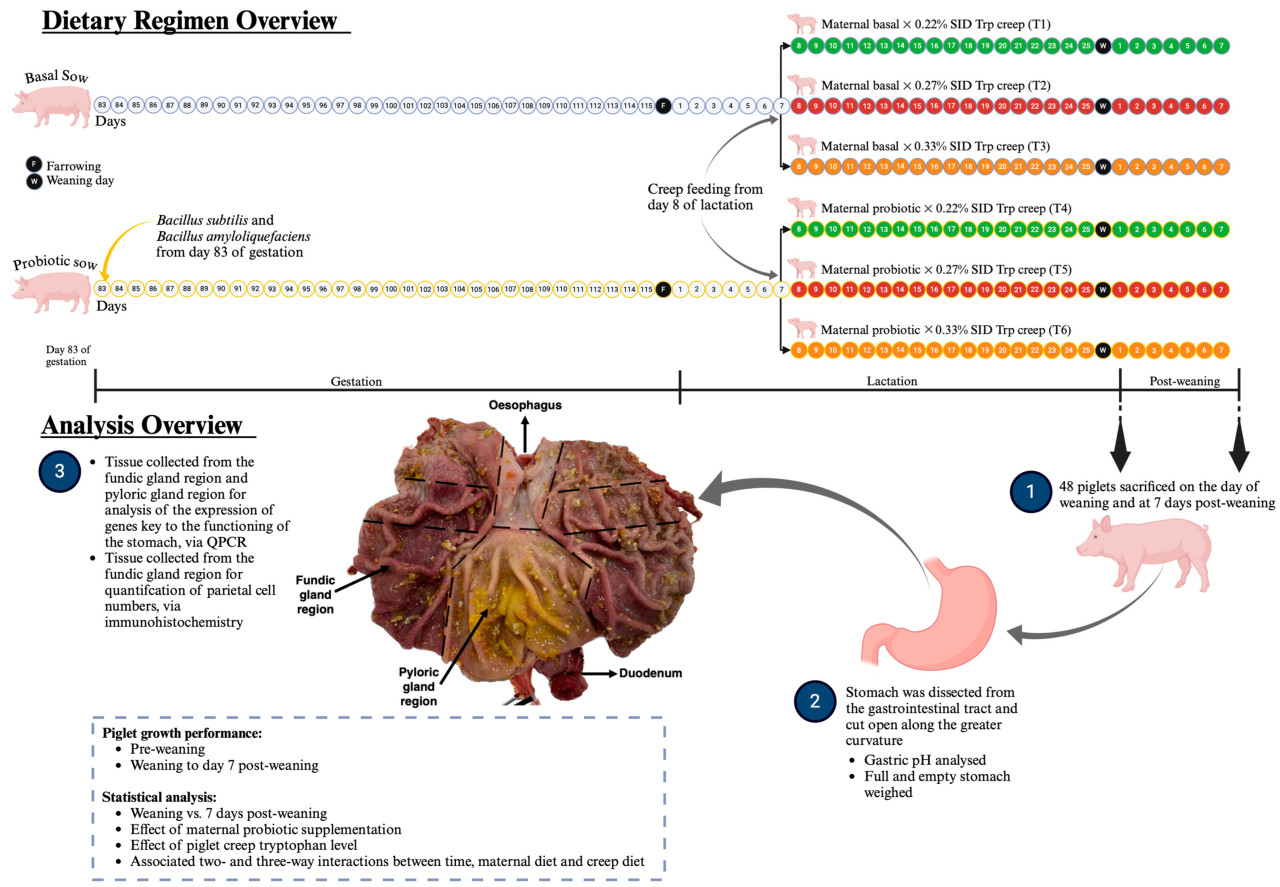
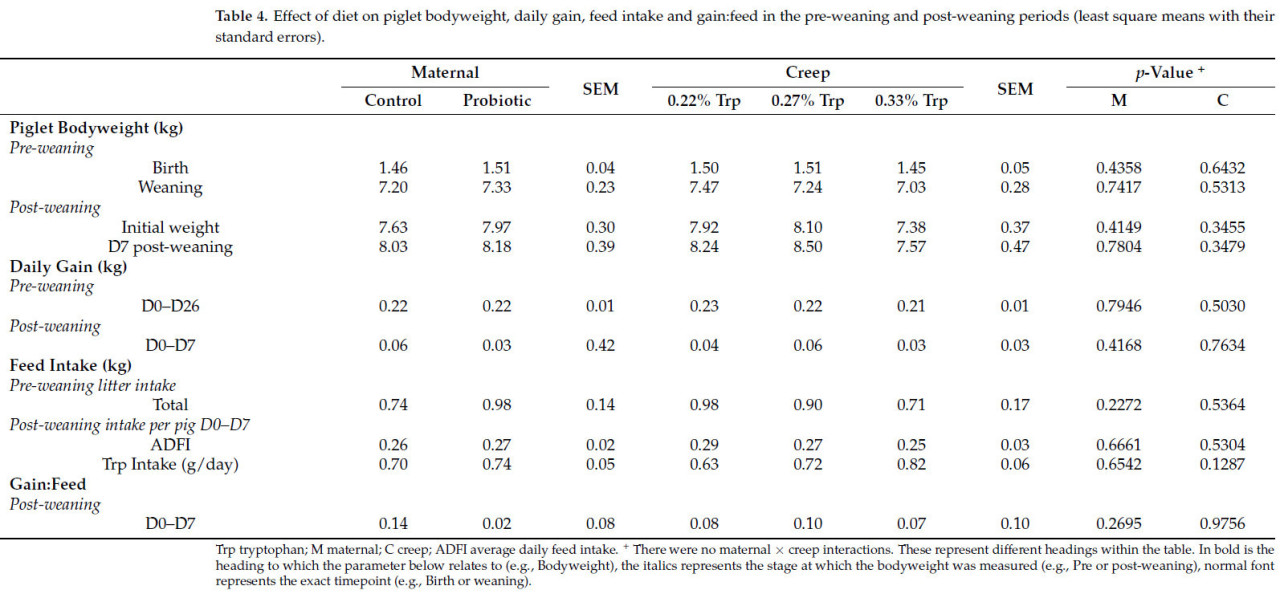
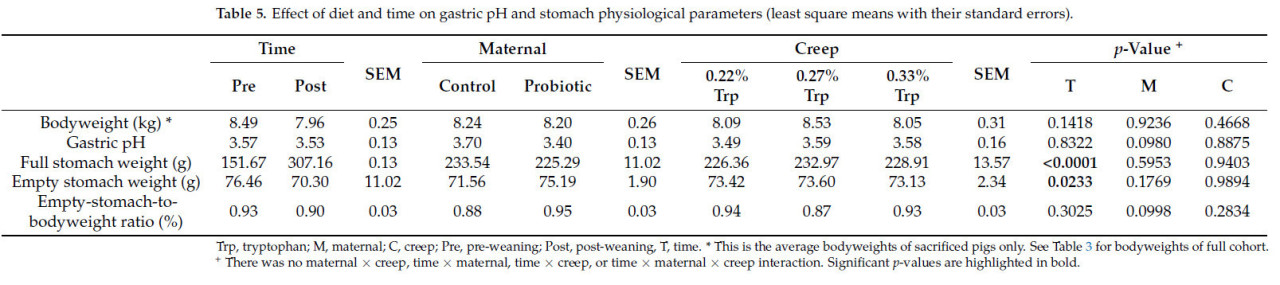
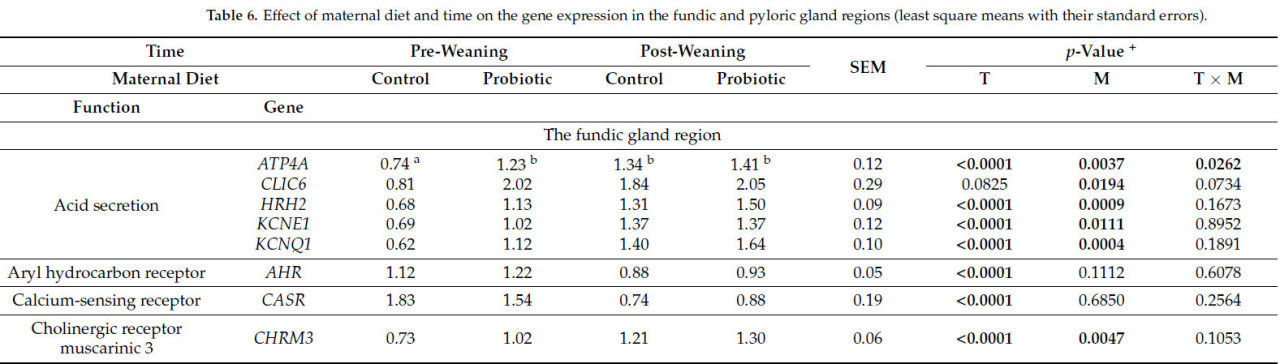
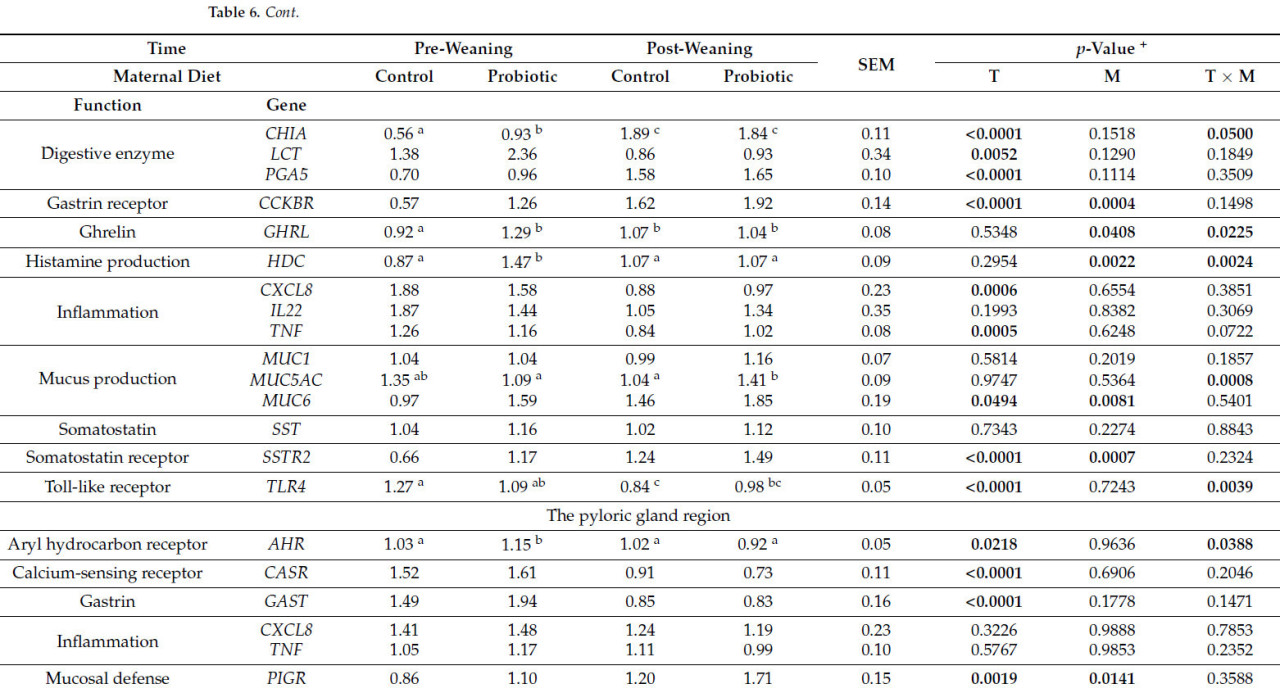
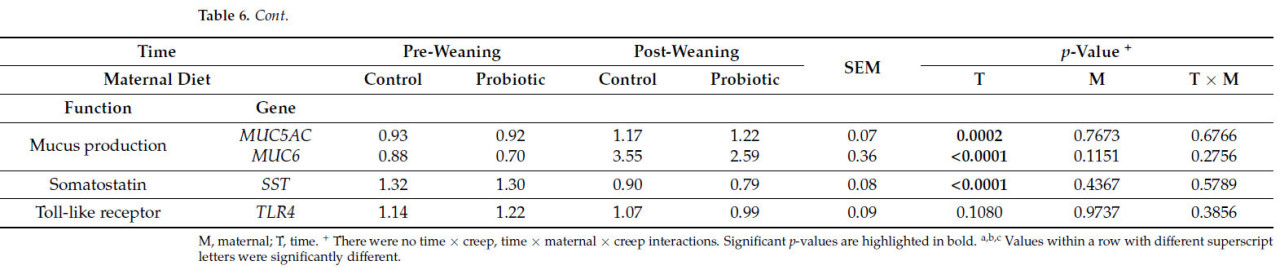
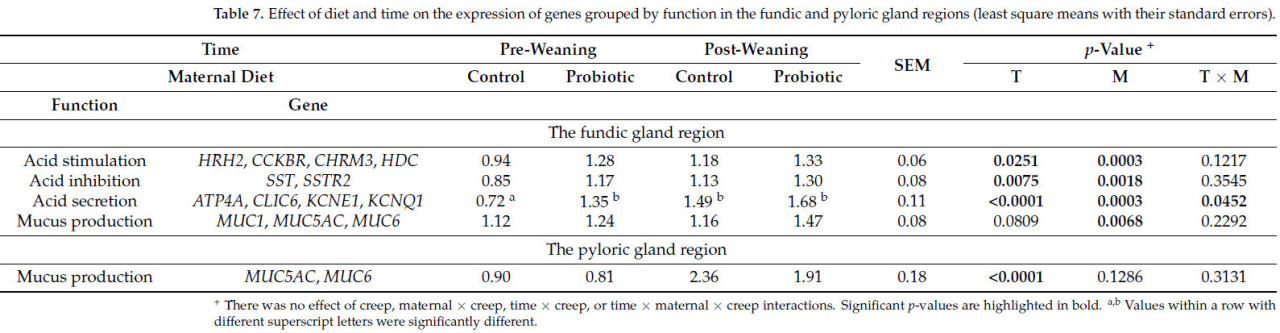
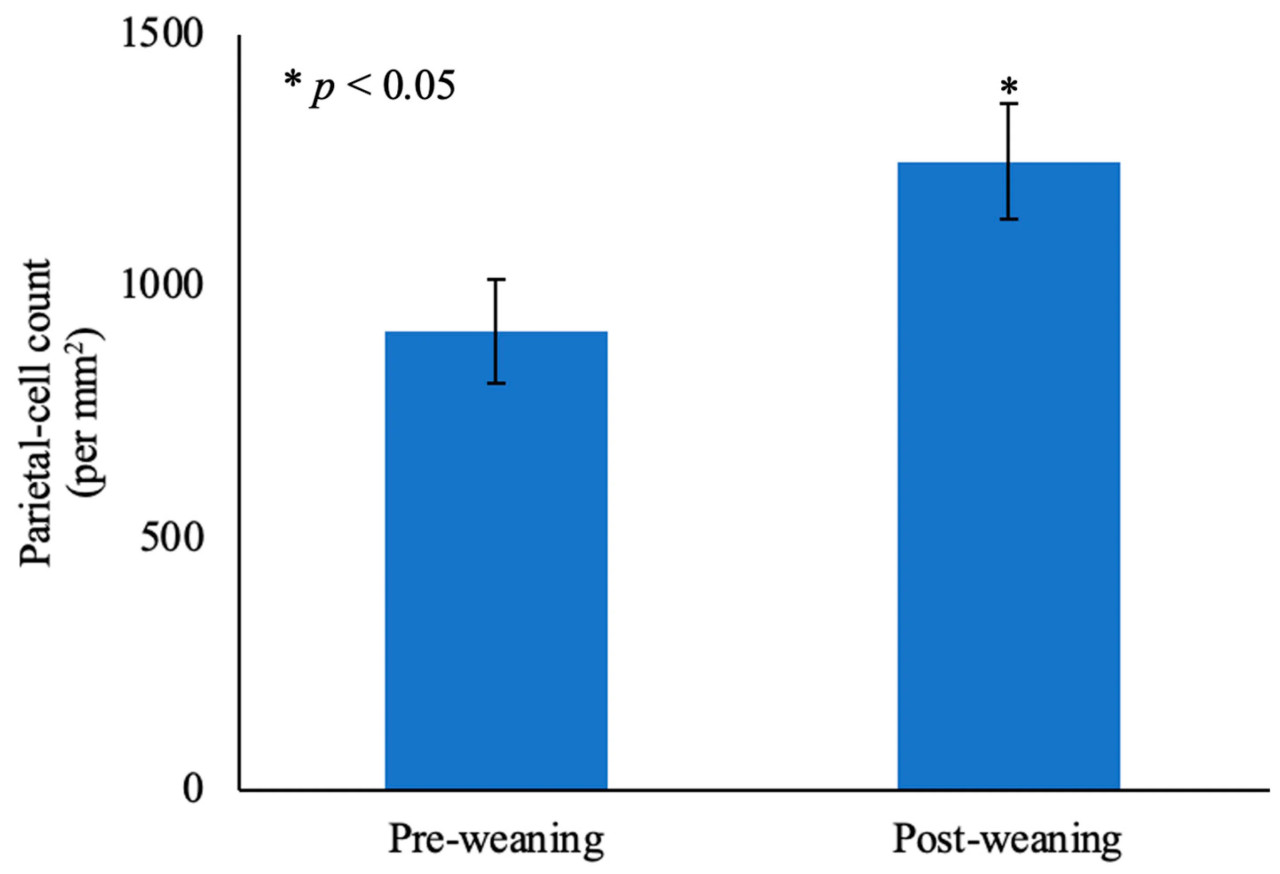
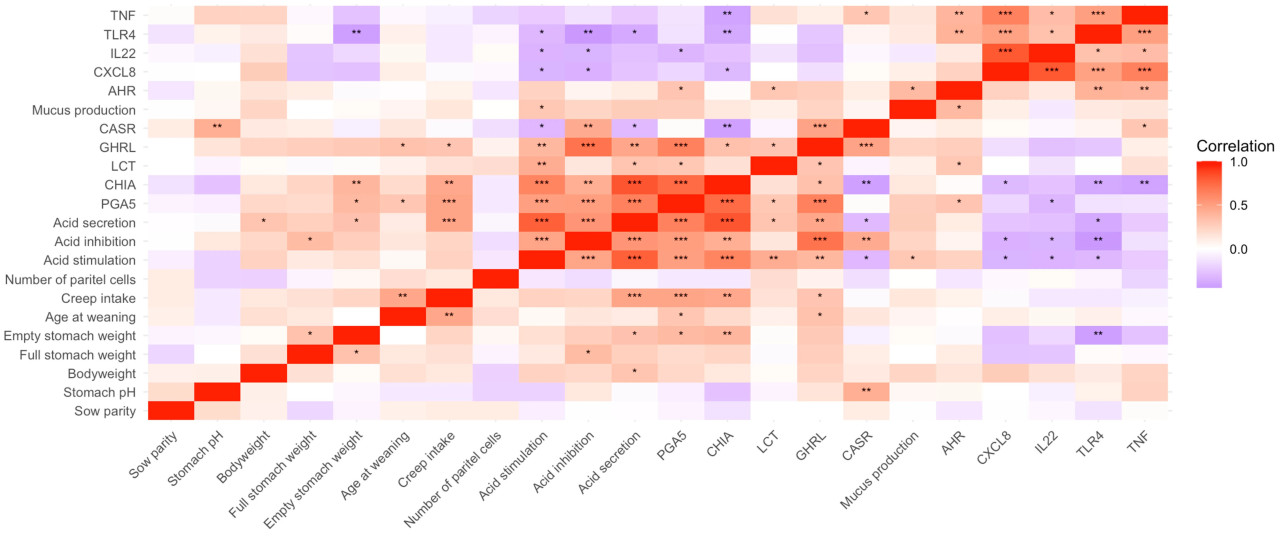
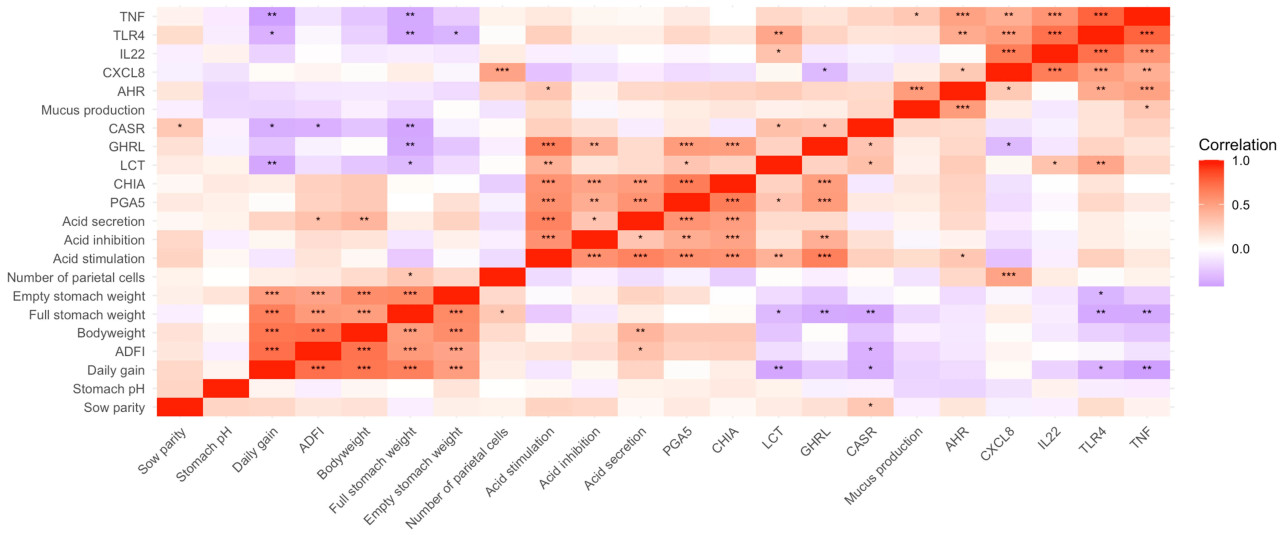
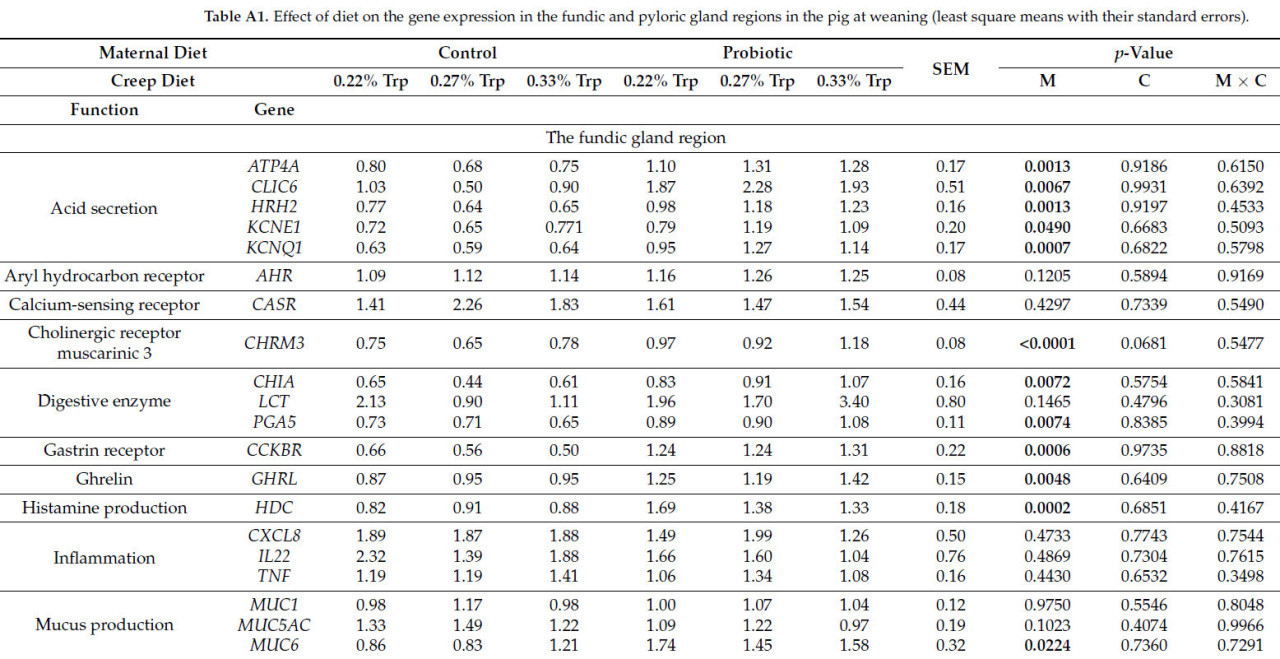
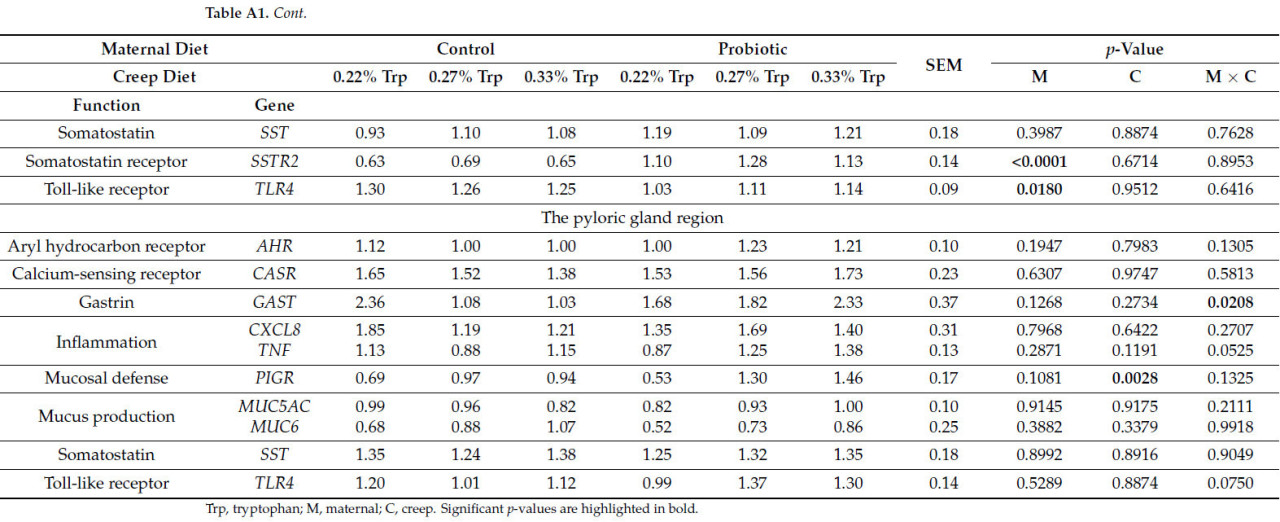
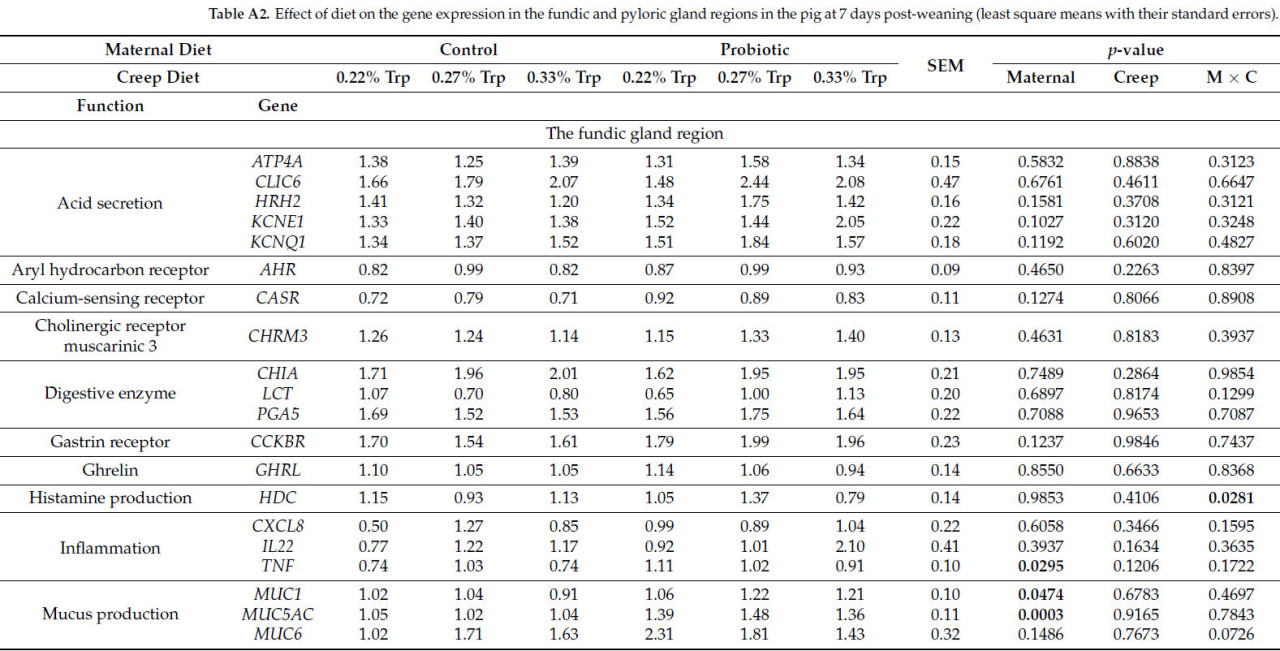
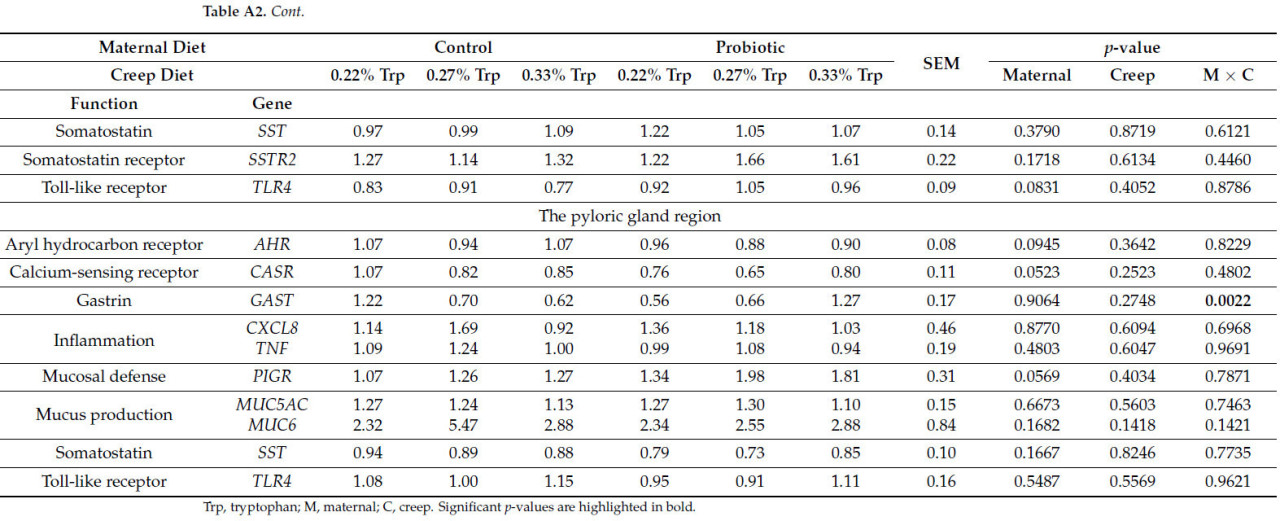















































































































Комментарии (0)