Улучшение устойчивости риса к тепловому стрессу: молекулярные механизмы и сорта риса
Глобальное потепление влияет на рост и развитие сельскохозяйственных культур, создавая угрозу продовольственной безопасности. Рис, являясь одной из важнейших продовольственных культур, серьезно страдает от воздействия высокотемпературного стресса, что снижает как его урожайность, так и качество. Таким образом, глубокое понимание молекулярных механизмов ответной реакции риса на тепловой стресс и выведение толерантных к такому стрессу сортов риса имеет решающее значение для поддержания продовольственной безопасности.
Аннотация
В этом обзоре обобщены данные о влиянии теплового стресса на признаки, связанные с урожайностью и качеством, на разных стадиях роста и развития риса, о молекулярных механизмах восприятия и ответной реакции риса на тепловой стресс, а также об улучшении и селекции жаростойких сортов риса с использованием существующих супераллелей и количественных локусов признаков (QTL). Мы также обсуждаем возможности и проблемы создания высокоустойчивого к теплу зародышевой плазмы риса, предлагая новые идеи и перспективы для будущей селекции жаростойких сортов риса.
1. Введение
Рис является одной из основных продовольственных культур в мире и занимает важное место в сельскохозяйственном производстве. Увеличение производства продуктов питания — это ключевая стратегия обеспечения продовольственной безопасности. Межправительственная группа экспертов по изменению климата (МГЭИК) в своем Шестом оценочном докладе указала, что за последнее столетие сжигание ископаемого топлива, неустойчивое использование энергии и нерациональное землепользование привели к непрерывному повышению глобальной температуры, которая сейчас на 1,1 °C выше, чем в доиндустриальный период [1]. Высокие температуры, вызванные изменением климата, существенно повлияли на рост и развитие основных продовольственных культур, серьезно ограничив сельскохозяйственное производство. Исследования показывают, что на каждый 1 °C повышения глобальной средней температуры урожайность нескольких основных продовольственных культур, в частности пшеницы, риса, кукурузы и сои, снижается на 6,0%, 3,2%, 7,4% и 3,1% соответственно [2]. В южных регионах Китая средняя температура с 2009 по 2018 год была на 0,7 °C выше по сравнению с периодом с 1961 по 1970 год. Раннеспелый рис очень чувствителен к высоким температурам в фазе налива зерна; в течение вегетационного периода повышение температуры на 1 °C приводит к снижению урожайности раннеспелого риса на 8% [3]. За последние 35 лет в Китае, с 1985 по 2020 год, средний показатель качества риса снизился с 65% до 60%. В Японии за статистический период с 1979 по 2018 год доля высококачественного риса также демонстрировала общую тенденцию к снижению, и ожидается, что эта тенденция сохранится в обозримом будущем [4]. Вызванный температурой тепловой стресс обычно определяется как быстрое повышение температуры, превышающее пороговый уровень в течение определенного периода, что вызывает необратимые повреждения роста и развития растений [5]. Тепловой стресс оказывает значительное негативное воздействие на весь цикл роста риса, серьезно ограничивая повышение как урожайности, так и качества риса [6]. Рис обеспечивает 21% мирового потребления калорий и является основой пропитания для более чем половины населения мира. Учитывая это, существует острая необходимость в разработке сортов риса с повышенной теплоустойчивостью.
Рис очень чувствителен к тепловому стрессу на всех этапах роста и развития. На стадии проростков оптимальная температура для роста риса составляет 28 °C днем и 22 °C ночью; когда температура превышает 32 °C, рост и развитие риса нарушаются на всех этапах. Например, фаза колошения наступает раньше, чтобы избежать повреждения жарой; удлинение гипокотиля и черешка способствует поддержанию оптимальной архитектоники растения; закрытие устьиц и увеличение плотности трихом способствуют сохранению содержания воды в растении. Эти термоморфогенные реакции смягчают неблагоприятные последствия повышенных температур для роста риса [7]. Температура выше 35 °C может серьезно ограничить налив зерна и урожайность [2,8,9,10]. Являясь прикрепленным организмом, рис в ходе длительной эволюции выработал сложный набор механизмов реагирования на тепловой стресс. Поэтому углубленное исследование молекулярных механизмов, лежащих в основе реакции на тепловой стресс, способствует созданию сортов риса с повышенной теплоустойчивостью. Во-первых, в данном обзоре представлен всесторонний обзор воздействия высокотемпературного стресса на урожайность и качество на различных этапах роста риса, затем рассматривается влияние высокотемпературного стресса на физиологические механизмы риса, описываются механизмы реагирования и молекулярные регуляторные сети риса на высокотемпературный стресс и, наконец, обсуждается повышение теплоустойчивости сортов риса с использованием идентифицированных супергаплотипов/количественных локусов признаков (QTL) и технологий редактирования генома. Также предлагается идея использования редактирования генома в сочетании с искусственным интеллектом для поиска новых генов теплоустойчивости и создания термоустойчивого гермоплазмы риса, что позволит выводить теплоустойчивые сорта риса.
2. Влияние теплового стресса на вегетативный и репродуктивный рост: урожайность и качество риса
Фазы вегетативного и репродуктивного роста являются критическими этапами, определяющими весь жизненный цикл риса (Рисунок 1). Длительное воздействие высокотемпературной среды индуцирует тепловой стресс, который негативно влияет на обе эти фазы, в конечном итоге сказываясь на урожайности и качестве риса [11]. В частности, во время вегетативного роста тепловой стресс повреждает рост растений и подавляет эффективное кущение. На репродуктивной стадии тепловой стресс влияет на ключевые процессы развития колосков, включая такие этапы, как формирование колоса, колошение и цветение, которые определяют критические показатели урожайности, такие как количество зерен в колосе и озерненность. Кроме того, процессы, имеющие решающее значение для конечного качества зерна, такие как опыление, налив зерна и накопление веществ, также негативно страдают от высоких температур [12].
Рисунок 1. Длительное воздействие высокой температуры угнетает выживаемость, урожайность и качество риса, создавая угрозу на всех этапах его жизненного цикла.
2.1. Влияние теплового стресса на количество побегов, число зерен и процент завязываемости: урожайность риса
Накопление биомассы в вегетативный период имеет решающее значение для риса, и количество базовой биомассы напрямую определяет уровень конечной урожайности. Начальный этап вегетативного роста начинается с прорастания семян. Постоянная высокотемпературная среда существенно ограничивает процесс прорастания семян и подавляет рост и развитие проростков. Это означает, что тепловой стресс охватывает практически весь жизненный цикл риса [13]. На стадии проростков высокотемпературный стресс ускоряет потерю воды и подавляет фотосинтез в растениях, что приводит к пожелтению листьев (хлорозу) и повреждению корней. Эти эффекты значительно снижают жизнеспособность риса на ранней фазе вегетативного роста, тем самым ставя под угрозу накопление базовой биомассы [14]. Фаза кущения — ключевой этап, определяющий урожайность риса, поскольку стабильность количества продуктивных побегов напрямую влияет на общую архитектонику растения и общее количество зерен, формирующихся на последующих этапах. Непрерывное воздействие высоких температур подавляет инициацию и рост пазушных почек, что приводит к сокращению как общего количества побегов, так и числа продуктивных побегов, тем самым влияя на потенциальную урожайность риса [15].
Морфологическая целостность и нормальное развитие колосков не только напрямую связаны с формированием зерна, но и оказывают глубокое влияние на конечное качество риса. Что касается общего количества зерен в метелке, то продолжительный высокотемпературный стресс нарушает процесс дифференциации колосков, приводя к уменьшению размера и плотности метелки, что значительно снижает общее количество зерен в метелке. В дополнение к негативному эффекту от снижения общего числа зерен, тепловой стресс сильно подавляет фертильность колосков, препятствуя нормальному мейозу, что приводит к существенному снижению процента завязываемости семян. В фазы колошения и цветения воздействие теплового стресса на цветочные органы особенно значительно и тяжело. В условиях высоких температур пыльники риса склонны к инактивации, что приводит к заметному снижению жизнеспособности пыльцы и, в свою очередь, вызывает стерильность колосков [2,17]. Эти эффекты конкретно проявляются как нарушение вскрытия пыльников, подавление набухания пыльцевых зерен и ограничение роста пыльцевых трубок. В совокупности эти факторы препятствуют нормальным процессам опыления и оплодотворения [18,19,20]. В конечном итоге тепловой стресс воздействует на фазу репродуктивного роста риса, приводя к уменьшению числа зерен в метелке и процента завязываемости, что значительно снижает урожайность риса.
2.2. Влияние теплового стресса на содержание сахарозы, стекловидность и содержание крахмала: качество риса
Во время фазы налива зерна высокие температуры окружающей среды оказывают значительное влияние на качество риса. Это связано с тем, что фаза налива зерна определяет конечную урожайность и процесс накопления запасных веществ в зерновке; в конечном итоге это влияет на внешний вид, выход крупы при помоле, пищевую ценность, а также кулинарные и вкусовые качества риса [21]. Недостаточный налив и щуплость зерновок являются следствием повышенной скорости налива и сокращения периода налива соответственно. Полнота зерновок в первую очередь определяется накоплением продуктов фотосинтеза и транспортом между источниками и потребителями ассимилятов [22]. Сахароза является преобладающей формой углеводов, синтезируемых в фотосинтезирующих тканях-источниках, таких как листья. Первоначально она загружается во флоэму и впоследствии транспортируется по сосудистым путям на большие расстояния к тканям-потребителям [23]. В период налива зерна высокие температуры приводят к повышению стекловидности и уменьшению размера зерен риса, тем самым ухудшая его внешние качества. Повышенные температуры способствуют накоплению активных форм кислорода (АФК) в зерновках риса, и увеличение количества АФК в этот период значительно повышает как стекловидность, так и долю стекловидных зерен [24]. После воздействия кратковременного экстремального высокотемпературного стресса во время цветения налив зерна подавляется. Стебли активируются как основной поглощающий орган, что приводит к увеличенному накоплению в них питательных веществ и, как следствие, к снижению качества зерна [25]. Поскольку содержание крахмала и его структурная композиция определяют внешний вид, а также кулинарно-вкусовые качества, недостаточный налив зерна в условиях высоких температур, приводящий к аномальному содержанию и структуре крахмала, является одним из основных факторов, способствующих изменению качества риса [26]. Содержание и молекулярная масса амилозы и амилопектина, а также распределение длины их цепей в совокупности определяют качество крахмала. Это связано с подавлением экспрессии генов, связанных с синтезом крахмала, и снижением активности соответствующих ферментов-синтаз в условиях теплового стресса. Например, сканирующая электронная микроскопия показывает, что клетки эндосперма мутанта flo24 продуцируют рыхло расположенные крахмальные гранулы, а скорость налива зерна у flo24 стабильно ниже, чем у линии дикого типа, и эта ситуация становится более выраженной при тепловом стрессе. Кроме того, исследования показали, что белок FLO24 активно взаимодействует с ключевыми ферментами, участвующими в синтезе крахмала, включая AGPL1, AGPL3 и PHO1 [27]. Экспрессия генов и активность ферментов, участвующих в путях распада крахмала, значительно индуцируются высокими температурами, что в конечном итоге приводит к снижению синтеза крахмала и ускорению его деградации. Кроме того, содержание белка в зерне также страдает от высоких температур, что, в свою очередь, влияет на внешний вид, пищевую ценность и текстуру зерен.
3. Молекулярные механизмы восприятия и ответной реакции риса на тепловой стресс
3.1. Восприятие сигнала теплового стресса запускает механизм проведения ионов кальция у риса
Клеточная мембрана очень чувствительна к высоким температурам. Тепловой стресс способствует поступлению ионов кальция (Ca²⁺), и увеличение внутриклеточной концентрации Ca²⁺ формирует Ca²⁺-сигнал, который играет ключевую роль в пути восприятия и ответной реакции на тепловой стресс у риса [28]. Генерация внутриклеточных Ca²⁺-сигналов тесно связана с восприятием температуры клеточной мембраной. Тепловой стресс индуцирует изменения текучести, структуры и стабильности мембраны, что, в свою очередь, запускает клеточный стресс и возникновение внутриклеточных сигналов ответа на тепловой стресс. Поступление Ca²⁺ при высоких температурах опосредовано каналами, локализованными в мембране, которые могут воспринимать тепловые сигналы и реагировать на них. Циклические нуклеотид-управляемые ионные каналы (CNGC) представляют собой класс относительно консервативных Ca²⁺-каналов у растений (Рисунок 2). У риса идентифицированы следующие локализованные в мембране представители семейства CNGC: OsCNGC1, OsCNGC2, OsCNGC4, OsCNGC5, OsCNGC6, OsCNGC9, OsCNGC10, OsCNGC12, OsCNGC13, OsCNGC14, OsCNGC15 и OsCNGC16, и они, вероятно, тесно связаны с температурными реакциями [29,30,31]. В условиях теплового стресса OsCNGC14, OsCNGC15 и OsCNGC16 способствуют поступлению Ca²⁺ (Таблица 1). Однако линии мутантов cngc14, cngc15 и cngc16 демонстрируют ослабленную способность реагировать на тепловой стресс и индуцировать цитозольные Ca²⁺-сигналы, что делает их более восприимчивыми к повреждению тепловым стрессом [30,31]. Недавнее исследование показало, что OsCNGC14, OsCNGC15 и OsCNGC16 образуют гетеромеры для совместного опосредования стрессовых реакций [31]. Сверхэкспрессия OsCNGC16 усиливает поступление Ca²⁺ и придает повышенную устойчивость к высоким температурам и другим стрессам, что в первую очередь связано с его способностью быстро контролировать закрытие устьиц в ответ на стресс [31]. Кроме того, проницаемые для Ca²⁺ аннексины также регулируют поступление Ca²⁺. OsANN1, аннексин риса с Ca²⁺-связывающей и АТФазной активностью, модулирует удаление активных форм кислорода (АФК) и управляет поступлением Ca²⁺ и транспортом через Ca²⁺-каналы в условиях теплового стресса [32,33]. Растения со сверхэкспрессией OsANN1 демонстрируют усиленный рост в условиях теплового стресса и других абиотических стрессов, тогда как линии РНК-интерференции (RNAi) OsANN1 более чувствительны к тепловому и засушливому стрессам [32]. Однако специфические эффекты Ca²⁺-сигнализации на термотолерантность риса весьма сложны и не могут быть просто классифицированы как положительная или отрицательная регуляция в рамках различных сигнальных путей. Исследования показали, что γ-субъединица G-белка TT2 способствует связыванию кальмодулина (CaM) с модулируемыми Ca²⁺ белками-факторами транскрипции SCT1 и SCT2 через Ca²⁺-сигнализацию, тем самым подавляя экспрессию регуляторного гена биосинтеза воска OsWR2 и, следовательно, негативно регулирует термотолерантность риса за счет снижения содержания воска [34]. Таким образом, тепловой стресс индуцирует чувствительность к высоким температурам у риса через путь G-белок — Ca²⁺-сигнализация — биосинтез воска. В итоге, Ca²⁺ играют ключевую роль в пути ответа на тепловой стресс у риса. Поддержание постстрессового содержания и скорости поступления Ca²⁺ в цитоплазму имеет решающее значение для функции ключевых нижестоящих белков, противодействующих тепловому стрессу.
Рисунок 2. Регуляторная сеть ответа на тепловой стресс и устойчивости к нему у риса. Когда растения подвергаются тепловому стрессу, текучесть клеточной мембраны изменяется, способствуя поступлению внеклеточного Ca²⁺ в цитоплазму. Тепловой стресс стимулирует накопление АФК в хлоропластах, митохондриях и других органеллах. TT3.1 убиквитинирует и деградирует TT3.2 в условиях теплового стресса, что подавляет повреждение ФСII белком TT3.2. Серия ферментов, связанных с активными формами кислорода, включая субъединицы 26S протеасомы, может ингибировать продукцию внутриклеточных АФК. Ряд хлоропластных белков защищает хлоропласты от теплового стресса. Тепловой стресс может стимулировать стресс эндоплазматического ретикулума (ER stress) и образование большого количества развернутых или неправильно свернутых белков. Стресс ЭПР активирует ответ на развернутые белки (UPR), который снимает ингибирующее действие IRE1. IRE1 регулирует альтернативный сплайсинг мРНК bZIP60, активируя его, и активная форма bZIP60 участвует в регуляции пути деградации неправильно свернутых белков. TT1 убиквитинирует SCE1 и инактивирует SUMO-модификацию нижестоящих малых белков теплового шока (sHSP). Кроме того, высокотемпературный стресс модулирует реакцию на тепловой стресс, регулируя активность ряда транскрипционных факторов.
3.2. Регуляция гомеостаза АФК у риса в условиях теплового стресса
Воздействие на растений высокотемпературного стресса приводит к существенному накоплению активных форм кислорода (АФК), включая синглетный кислород (¹O₂), супероксид-анион (O₂⁻), пероксид водорода (H₂O₂) и гидроксильные радикалы (OH⁻). Поддержание АФК на умеренном уровне необходимо для здорового роста растений [35]. В целом, механизмы удаления АФК играют ключевую роль в защите растений от повреждений, вызванных высокотемпературным стрессом, что, в свою очередь, приводит к значительной положительной корреляции между антиоксидантной способностью и термотолерантностью риса. HTH5 кодирует белок гомеостаза пиридоксальфосфата, который способствует удалению АФК. Линии риса со сверхэкспрессией HTH5 усиливают толерантность к высокотемпературному стрессу за счет снижения окислительного повреждения, вызванного накоплением АФК в условиях теплового стресса [36]. Супероксиддисмутаза (СОД) функционирует как первая линия защиты от активных форм кислорода (АФК), катализируя превращение супероксидных радикалов (O₂⁻) в молекулярный кислород (O₂) и пероксид водорода (H₂O₂), который затем восстанавливается до воды аскорбатпероксидазой (АПО) [37]. Shiraya и др. идентифицировали термотолерантную марганец-супероксиддисмутазу 1 (MSD1) у риса [38]. Трансгенные растения с конститутивной экспрессией MSD1 демонстрируют значительно лучшее качество зерна в условиях высоких температур (33 °C) по сравнению с растениями дикого типа. Это сопровождается более высокими уровнями экспрессии генов, связанных с удалением АФК, включая медь/цинк-супероксиддисмутазу, антиоксидантные белки, тиоредоксины и аскорбатпероксидазу, по сравнению с растениями дикого типа [38]. SNAC3 кодирует стресс-чувствительный NAC-транскрипционный фактор, который регулирует экспрессию генов, связанных с АФК, для модулирования динамического баланса H₂O₂, тем самым повышая термотолерантность [39]. У риса мутанты с потерей функции гена OsEDS1, регулирующего H₂O₂, проявляют повышенную чувствительность к тепловому стрессу. Дальнейший анализ показал, что OsEDS1 образует комплексы с каталазами OsCATB и OsCATC для удаления H₂O₂ в условиях теплового стресса [40]. Успешная колонизация эндофитов внутри растений риса служит экологически безопасным подходом к повышению термотолерантности риса. Pseudomonas linzhiensis RS16, продуцирующая 1-аминоциклопропан-1-карбоксилат (АЦК) деаминазу, при инокуляции в рис эффективно снижает повышенные уровни этилена, вызванные высокими температурами. Поскольку этилен-чувствительные гены часто коррелируют с продукцией активных форм кислорода (АФК), это приводит к значительному снижению содержания АФК [41]. OsRbohB — это ген дыхательной оксидазы у риса. В условиях высоких температур мутантные линии с нарушенной функцией OsRbohB демонстрируют разную степень снижения накопления АФК в различных частях растения по сравнению с растениями дикого типа. В то же время экспрессия генов, связанных с тепловым шоком, включая OsHSP23.7, OsHSP17.7, OsHSF7 и OsHsfA2a, значительно индуцируется [12]. У риса существует модель регуляции ответа на тепловой стресс, включающая в основном модификации метилирования. Деметилаза JMJ713 взаимодействует с JMJ708, усиливая уровень деметилирования H3K36me2, тем самым способствуя удалению АФК и повышая термотолерантность риса [42]. Уровни экспрессии нескольких генов, связанных с удалением АФК, включая OsCATC, OsCSD3 и OsAPX, значительно индуцируются в трансгенных растениях со сверхэкспрессией JMJ713 в условиях теплового стресса [42]. Недавнее исследование показало, что вспомогательная субъединица N-концевой ацетилтрансферазы A (NatA) OsNAA15 подвергается температурно-зависимому альтернативному сплайсингу, давая начало двум вариантам белка: OsNAA15.1 и OsNAA15.2. Изоформа OsNAA15.1 полезна для нормального роста риса в условиях высокотемпературного стресса, тогда как OsNAA15.2 оказывает противоположный эффект [43]. Это дифференциальное влияние объясняется способностью OsNAA15.1 образовывать стабильный комплекс NatA с каталитической субъединицей OsNAA10, который способствует ацетилированию гликолатоксидазы (GLO1/5) и направляет ее на деградацию в 26S протеасоме. Этот процесс эффективно снижает накопление H₂O₂, продуцируемого GLO1/5, особенно в условиях высокотемпературного стресса [43]. В итоге, гомеостаз уровней пероксидов у риса в условиях высоких температур достигается за счет регуляции серии ферментов, удаляющих АФК, и генов, связанных с продукцией АФК.
3.3. Поддержание функции хлоропластов для стабильного производства риса в условиях теплового стресса
Хлоропласты являются важнейшими органеллами для поддержания фотосинтеза и обеспечения роста растений в условиях теплового стресса. Многочисленные белки внутри хлоропластов играют критическую роль в защите от повреждений, вызванных тепловым стрессом. Что касается транскрипционных процессов внутри хлоропластов, OsFLN1 и OsFLN2 у риса функционируют как часть пластидного РНК-полимеразного комплекса (PEP), защищая нормальное возникновение и развитие хлоропластов при тепловом стрессе [44,45]. OsTRXz регулирует редактирование РНК в хлоропластах при тепловом стрессе через взаимодействие с множественными органеллярными факторами редактирования РНК 2 (OsMORF2), OsMORF8 и OsMORF9 [46]. Как OsFLN1, так и OsFLN2 взаимодействуют с тиоредоксином OsTRXz, образуя модуль TRX-FLN, который поддерживает окислительно-восстановительный баланс в хлоропластах при тепловом стрессе [44,47]. Нарушение модуля OsTRXz-OsFLN1/2 разрушает стабильность транскрипционно-активных хроматиновых комплексов и активность PEP (пластидной РНК-полимеразы), что приводит к подавлению PEP-зависимой экспрессии генов внутри хлоропластов [44,47]. Фотосистема II (ФСII), расположенная на тилакоидной мембране хлоропластов, очень чувствительна к высокотемпературному стрессу, который легче нарушает электрон-транспортную цепь фотосинтеза, повреждая ФСII [48]. При воздействии теплового стресса белок-предшественник хлоропластов TT3.2 у риса рекрутируется в вакуолярный путь для убиквитинирования и деградации; его перемещение из хлоропластов в эндосомы снижает повреждение тилакоидов тепловым стрессом, тем самым поддерживая функциональность хлоропластов в условиях теплового стресса [49]. Хлорофилл, ключевой пигмент для фотосинтеза в хлоропластах, синтезируется через тетрапиррольный биосинтетический путь, в котором НАДФН-протохлорофиллидоксидоредуктаза B катализирует восстановление протохлорофиллида до хлорофиллида [50]. Исследования показали, что PGL10 поддерживает фотосинтетическую активность в условиях высокотемпературного стресса, сохраняя нормальную функцию хлоропластов [50]. Кроме того, в пути биосинтеза хлорофилла, известном как метилэритритол-4-фосфатный (MEP) путь, фермент 4-гидрокси-3-метилбут-2-енилдифосфатредуктаза (GRY3) участвует в синтезе геранилгеранилдифосфата в хлоропластах. Этот процесс необходим для поддержания нормальной продукции хлорофилла и развития хлоропластов, а также для обеспечения реакции на высокотемпературный стресс и стресс от интенсивного света [51]. Аномальная функция PGL10 или GRY3 приводит к снижению содержания хлорофилла и нарушению развития хлоропластов, делая растения более восприимчивыми к избыточному накоплению АФК, индуцированному тепловым стрессом, что в конечном итоге ухудшает рост риса [50,51]. Тепловой стресс также влияет на стабильность хлоропластов, стимулируя накопление АФК внутри них. При умеренном высокотемпературном стрессе HES1 (UDP-N-ацетилглюкозаминпирофосфорилаза), обладающая определенными способностями к удалению АФК, при потере своей функции вызывает всплеск АФК в хлоропластах и тепловое повреждение ядерной ДНК, что приводит к преждевременному старению листьев, значительному снижению продуктов фотосинтеза и серьезным потерям урожая [52]. В дополнение к вышеупомянутым механизмам, высокие температуры также подавляют активность рибулозо-1,5-бисфосфаткарбоксилазы/оксигеназы (Рубиско), ключевого фермента фотосинтеза, определяющего скорости ассимиляции углерода и фотодыхания [53,54]. Недавнее исследование демонстрирует, что трансгенные растения со сверхэкспрессией как Рубиско, так и рубиско-активазы (линия oxRCA-RBCS) сохраняли более высокие скорости фотосинтеза и демонстрировали лучший рост в условиях высоких температур (40 °C) по сравнению с растениями дикого типа. Это свидетельствует о том, что повышение содержания рубиско-активазы без снижения содержания Рубиско могло бы улучшить урожайность и устойчивость риса в условиях высокотемпературного стресса, потенциально внося вклад в будущие стратегии повышения продуктивности риса и обеспечения устойчивого производства в условиях потепления климата [54]. Следовательно, поддержание целостности функции хлоропластов имеет положительное значение для борьбы с тепловым стрессом, удаления активных форм кислорода (АФК) и стабилизации урожайности.
3.4. Убиквитинирование и деградация неправильно свернутых белков у риса в условиях теплового стресса
Тепловой стресс индуцирует в растительных клетках стрессовую реакцию эндоплазматического ретикулума (ЭПР), которая приводит к продукции и накоплению в клетке развернутых или неправильно свернутых белков. Накопление этих аномальных белков нарушает функцию других нормальных белков, особенно во время фазы налива зерна, когда стресс ЭПР серьезно повреждает конечную урожайность и качество риса [55,56]. В растительных клетках в условиях теплового стресса активируется путь ответа на развернутые белки (UPR) для усиления фолдинга белков и ускорения их деградации, тем самым уменьшая трансляцию и устраняя накопление неправильно свернутых белков в ЭПР [57,58]. Белки теплового шока (HSP), действуя как молекулярные шапероны, предотвращают необратимую агрегацию частично развернутых белков [59]. Мембраносвязанный транскрипционный фактор OsNTL3 из семейства NAC у риса передает сигналы от плазматической мембраны к ядру в условиях теплового стресса и регулирует фолдинг белков ЭПР при тепловом стрессе, связываясь с промотором OsbZIP74 (также известного как OsbZIP50; в этой статье мы обобщенно называем его OsbZIP74) [60]. Интересно, что повышение регуляции экспрессии OsNTL3 при тепловом стрессе контролируется OsbZIP74, что позволяет транскрипционному регуляторному модулю OsNTL3-OsbZIP74 опосредовать сигнализацию между эндоплазматическим ретикулумом (ЭПР), плазматической мембраной и ядром через взаимную транскрипционную регуляцию, тем самым в совокупности способствуя ослаблению повреждения от теплового стресса [60]. В условиях стресса ЭПР сенсор ЭПР риса — фермент, требующий инозитола 1 (OsIRE1), — подвергает сплайсингу мРНК OsbZIP74, превращая ее в форму, лишенную мембраносвязывающего домена, что позволяет активированному OsbZIP74 более эффективно проникать в ядро для выполнения своей транскрипционной регуляторной функции в ответ на высокую температуру и другие стрессы [58,61]. Во время развития эндосперма после налива зерна OsbZIP60 (также известный как OPAQUE3) напрямую связывается и активирует гены шаперонов ЭПР OsBiP1 и PDIL1-1, тем самым поддерживая гомеостаз ЭПР в условиях высоких температур [56]. Исследования показали, что мутанты OsbZIP60 демонстрируют стресс ЭПР, который усугубляется высокой температурой, что приводит к нарушению синтеза запасных белков и крахмала в зерне [56]. Чтобы противодействовать тепловому стрессу при нарушенной функции OsbZIP60, в ядре частично активируются OsbZIP74 и другие факторы транскрипции ЭПР посредством обратной связи, чтобы индуцировать экспрессию генов ответа на развернутые белки (UPR), тем самым снижая стресс ЭПР [56].
Чтобы противодействовать накоплению неправильно свернутых или утративших функцию белков, вызванному тепловым стрессом, путь убиквитин-протеасома деградирует эти белки, защищая тем самым клетки от токсических эффектов накопления белка [62]. В условиях теплового стресса α2-субъединица 26S протеасомы TT1, ключевой компонент пути убиквитин-протеасома, повышает скорость деградации убиквитинированных субстратов, уменьшая разнообразие и количество токсичных денатурированных белков, накапливающихся в клетке, и таким образом защищая клетки растений от теплового повреждения [62]. Недавнее исследование демонстрирует, что TT1 негативно регулирует SUMO-E2-лигазу SCE1, вовлеченную в термотолерантность риса, путем убиквитинирования и направления ее на деградацию в 26S протеасоме [63]. В клетках риса в условиях теплового стресса увеличивается количество SUMOилированных белков, включая малый белок теплового шока (sHSP) Hsp24.1, который является ключевым положительным регулятором термотолерантности [63]. У мутанта sce1 количество SUMOилированных белков снижено, в то время как накопление Hsp24.1 повышено, что приводит к усилению термотолерантности и повышению урожайности в условиях теплового стресса [63]. TT3.1 кодирует локализованную в плазматической мембране E3-убиквитинлигазу, которая реагирует на сигналы теплового стресса. В условиях теплового стресса TT3.1 перемещается от плазматической мембраны к эндосомам и убиквитинирует белок-предшественник хлоропластов TT3.2, который негативно регулирует термотолерантность риса, направляя его на деградацию и тем самым поддерживая стабильность хлоропластов и усиливая термотолерантность [49]. Кроме того, E3-убиквитинлигаза OsHIRP1 и локализованная в аппарате Гольджи RING-типа E3-лигаза OsHCI1 также вносят вклад в термотолерантность риса [64,65]. Следовательно, независимо от того, являются ли они развернутыми, неправильно свернутыми или белками, оказывающими негативное влияние на термотолерантность риса, эти белки обычно поддерживаются с помощью серии положительных регуляторных механизмов, таких как путь убиквитинирования-деградации и ответ на развернутые белки, для обеспечения стабильности клеточных белков в ответ на непрерывный тепловой стресс.
3.5. Механизм гормональной регуляции у риса в условиях теплового стресса
Жасмоновая кислота (ЖК) представляет собой класс гормонов, регулирующих устойчивость растений к стрессам. Недавние исследования показали, что ЖК участвует в регуляции термотолерантности риса. Ген пути передачи сигнала ЖК OsJAZ9 положительно регулирует термотолерантность риса, и его экспрессия положительно регулируется геном ответа на тепловой стресс HTG3a [66]. В условиях теплового стресса линии со сверхэкспрессией OsJAZ9 значительно увеличивают площадь зеленых листьев и стабилизируют процент завязываемости семян по сравнению с растениями дикого типа [66]. В присутствии ЖК ингибитор пути передачи сигнала ЖК OsJAZ1 метилируется аргинин-метилтрансферазой OsPRMT6a. Метилированная форма OsJAZ1 может быть убиквитинирована и деградирована E3-убиквитинлигазами OsCOI1a/OsCOI1b, тем самым снимая ингибирование сигнального пути жасмоновой кислоты и способствуя нормальному росту колосков риса в условиях высоких температур [67]; при этом высвобождается фактор транскрипции OsMYC2, который подавляется OsJAZ1, и OsMYC2, в свою очередь, подавляет OsPRMT6a, действуя как механизм отрицательной обратной связи для сигнализации жасмоновой кислоты [67]. Таким образом, существование модуля OsPRMT6a-OsJAZ1-OsMYC2 связывает ЖК-сигнализацию с нормальным развитием колосков в условиях теплового стресса и функционирует как переключатель для реагирования на тепловой стресс, одновременно координируя гомеостаз пути ЖК-сигнализации внутри растения риса. Время цветения в дневное время (DFOT) является важным показателем для изучения роста и развития риса. Сверхэкспрессия связанного с биосинтезом ЖК гена OsAOS1 у риса значительно способствует накоплению ЖК и смещает DFOT, чтобы избежать цветения в условиях высоких температур [68]. Кроме того, гены, связанные с DFOT, такие как OsAOS1, OsSWEET4, OsPIP2;2 и OsXTH9, являются прямыми мишенями и регулируются OsMYC2 [68]. OsFBN1 кодирует пластид-ассоциированный липидный белок — фибриллин. OsFBN1 подавляет экспрессию гена биосинтеза жасмоновой кислоты OsAOS2. В условиях теплового стресса по сравнению с растениями дикого типа трансгенные линии риса со сверхэкспрессией OsFBN1 демонстрируют значительно сниженное содержание ЖК, а также значительно сниженную термотолерантность на стадиях проростков и репродуктивного роста [69]. Эти результаты указывают на то, что ЖК в основном регулирует адаптацию риса к высокотемпературному стрессу, участвуя в таких процессах, как рост колосков и цветение.
Фитогормон индол-3-уксусная кислота (ИУК) и ее сигнальный путь были широко изучены в процессах роста риса, включая развитие корней, рост надземной части и фотосинтез. Однако сообщения об их участии в регуляции термотолерантности относительно ограничены. В условиях теплового стресса экспрессия OsIAA7, кодирующего белок семейства факторов ответа на ауксин, значительно индуцируется. Сверхэкспрессия OsIAA7 значительно повышает выживаемость проростков в условиях высоких температур. Несколько генов, связанных с тепловым стрессом, таких как OsFKBP20, OsTOGR1, OsTT1 и OsTT3.1, значительно повышают свою регуляцию под действием OsIAA7 в условиях высоких температур, в то время как OsARF6 (фактор, отвечающий на ИУК) снижает регуляцию этих генов. Кроме того, OsIAA7 подавляет OsARF6, чтобы интегрировать сигнальный путь ИУК и повысить термотолерантность риса [70]. Аналогично, OsIAA29 конкурирует с OsIAA21 за связывание и активацию транскрипционной активности OsARF17, тем самым способствуя наливу зерна в условиях высоких температур [71]. Как термотолерантные, так и тепловосприимчивые сорта риса страдают от снижения фертильности колосков и жизнеспособности пыльцы при тепловом стрессе, в то время как экзогенное применение ИУК эффективно ослабляет повреждения, вызванные тепловым стрессом [72]. В условиях теплового стресса уровни эндогенной ИУК значительно снижаются и положительно коррелируют с жизнеспособностью пыльцы, количеством зерен в метелке, массой метелки и урожайностью с одного растения [72].
В условиях высокотемпературного стресса содержание АБК и АФК в пыльниках значительно увеличивается, жизнеспособность пыльцы подавляется, а запрограммированная клеточная гибель (PCD) в клетках тапетума ускоряется [73]. Кроме того, гены, лимитирующие скорость биосинтеза АБК, OsNCED3 и OsNCED5, значительно индуцируются высокими температурами. Экзогенное применение высоких концентраций АБК приводит к значительному увеличению содержания АФК в пыльниках, снижению жизнеспособности микроспор, жизнеспособности пыльцы и ухудшению фертильности [73,74]. Потеря функции киназы сигналинга АБК SAPK2 нарушает передачу сигнала АБК и приводит к блокированию PCD в тапетуме, но не влияет на продукцию опосредованных АБК АФК в условиях теплового стресса [74]. В условиях теплового стресса экзогенное применение АБК помогает подавлять чрезмерное накопление АФК в зерновках и улучшает урожайность зерна, качество помола и внешний вид [75]. OsRbohH — это ген дыхательной оксидазы у риса. В трансгенных линиях со сверхэкспрессией OsRbohH в условиях теплового стресса гены, связанные с биосинтезом АБК, OsNCED3 и OsNCED4, значительно повышают свою регуляцию, в то время как ген пути метаболизма АБК OsABA8ox3 значительно ее снижает. Эти линии высокочувствительны к экзогенной АБК, демонстрируя улучшенную выживаемость проростков и уровень хлорофилла при тепловом стрессе [76]. Кроме того, в трансгенных линиях со сверхэкспрессией OsRbohH гены, связанные с передачей сигнала АБК, OsDREB2A, OsLEA3, OsbZIP66 и OsbZIP72, значительно снижают свою регуляцию, но уровни их экспрессии демонстрируют противоположную тенденцию в условиях засухи, что указывает на сложные регуляторные механизмы АБК у риса в ответ на различные абиотические стрессы [76].
Салициловая кислота (СК), небольшая фенольная молекула, как было показано, участвует не только в защитных реакциях растений, но и в ответах на абиотические стрессы. Например, у Arabidopsis thaliana после 10 дней низкотемпературной обработки эндогенный уровень СК значительно повышается, но скорость роста растений снижается из-за компромисса между ростом и устойчивостью к стрессу [77]. В период налива зерна у кукурузы воздействие высоких температур значительно снижает продолжительность и максимальную скорость налива зерна, но это тепловое повреждение ослабляется экзогенным применением СК [78]. Аналогично, у риса экзогенное применение 1 мМ и 10 мМ СК значительно увеличивает количество колосков на метелку и процент завязываемости семян в условиях высокотемпературного стресса по сравнению с необработанными растениями [79,80]. Более того, после применения СК содержание осмопротекторов в колосках, таких как растворимые сахара, пролин, другие растительные гормоны и антиоксидантные ферменты, значительно индуцируется [79,80].
Брассиностероиды (БР) являются высокоэффективными и экологически чистыми растительными гормонами, которые могут регулировать транспорт ионных каналов и повышать урожайность сельскохозяйственных культур, модулируя экспрессию стрессоустойчивых генов. В условиях высокотемпературного стресса степень дегенерации колосков тепловосприимчивого сорта риса IR36 увеличилась на 62%, в то время как у жаростойкого сорта HHZ наблюдалась относительно более низкая степень дегенерации колосков. Однако применение 2,4-эпибрассинолида значительно снизило степень дегенерации колосков у обоих сортов, причем более выраженное снижение наблюдалось у IR63, тем самым ослабляя повреждение колосков, вызванное высокотемпературным стрессом [81]. Тепловой стресс и экзогенный EBR (синтетический брассиностероид) совместно индуцируют экспрессию генов, связанных с синтезом БР, D11, BRD2 и D2, а один только тепловой стресс также индуцирует экспрессию генов метаболизма БР OsCYP734A2, OsCYP734A4 и OsCYP734A6. Напротив, уровни экспрессии этих генов, связанных с метаболизмом БР, значительно снижаются при применении EBR [81]. Другое исследование показало, что в условиях высокотемпературного стресса умеренное орошение способствует увеличению содержания БР в колосках и корнях риса. Кроме того, устьичная проводимость, скорость транспирации и скорость фотосинтеза листьев риса при таком методе орошения значительно выше, чем у риса, орошаемого обычной водой в условиях высокотемпературного стресса [82]. БР индуцируют продукцию белков теплового шока в условиях высокотемпературного стресса для поддержания правильного фолдинга белков. Более того, БР усиливают активность ферментов, связанных с аскорбат-глутатионовым (AsA-GSH) циклом, тем самым повышая клеточный антиоксидантный уровень, что полезно для поддержания гомеостаза роста растений в условиях высокотемпературного стресса [83,84].
3.6. Механизм транскрипционной регуляции у риса в условиях теплового стресса
Транскрипционные факторы играют ключевую роль в термотолерантности растений. После того как рис воспринимает тепловой стресс и передает сигнал внутрь клетки, транскрипционные факторы из семейств NAC, MYB, WRKY и bZIP в ядре активируют соответствующую транскрипционную регуляцию и инициируют экспрессию генов устойчивости к тепловому стрессу. В целом, факторы теплового шока (HSF) могут связываться со специфическими областями, известными как элементы теплового шока, в промоторах генов белков теплового шока (HSP), чтобы регулировать их экспрессию и противодействовать тепловому стрессу [85]. В условиях высокотемпературного стресса OsHSFA2d подвергается альтернативному сплайсингу, в результате чего образуется транскрипционно активная форма, которая локализуется только в ядре и может реагировать на тепловой стресс через путь ответа на развернутые белки [85]. Фактор транскрипции WRKY риса OsWRKY10 негативно регулирует термотолерантность. Сверхэкспрессия OsWRKY10 способствует накоплению АФК в хлоропластах, делая растения более чувствительными к тепловому стрессу и склонными к гибели в условиях высоких температур [86]. Было обнаружено, что белок VQ8, содержащий валин-глутаминовый (VQ) мотив, ингибирует ДНК-связывающую активность OsWRKY10, предотвращая его транскрипционную активацию генов-мишеней, таких как NAC4, тем самым подавляя тепловую чувствительность, вызванную опосредованным OsWRKY10 балансом АФК и реакцией гиперчувствительности [86]. Конструкция для слитой экспрессии промотора OsHSP101 и кДНК OsWRKY11 при сверхэкспрессии значительно усиливает термотолерантность и устойчивость к засухе у трансгенных растений [66].
В условиях теплового стресса транспорт питательных веществ между источником и потребителем у риса также контролируется транскрипционной регуляцией. Транскрипционные факторы риса OsMADS7 и OsbZIP58 участвуют в регуляции термостабильности синтеза крахмала в зерне [21,87]. Подавление OsMADS7 приводит к более стабильному синтезу крахмала в эндосперме в условиях теплового стресса [87]. Напротив, высокая температура индуцирует альтернативный сплайсинг OsbZIP58, в результате чего образуется укороченная форма с более низкой активностью, что приводит к подавлению транскрипции основного гена синтеза амилозы Wx [21]. Недавнее исследование показало, что OsbZIP14 и OsbZIP58 могут поддерживать стабильный налив зерна риса в условиях теплового стресса посредством синергетической регуляции, а трансгенные растения со сверхэкспрессией OsbZIP14 демонстрируют повышенную термотолерантность [88]. MYB-транскрипционный фактор OsMYB55 может связываться и активировать экспрессию таких генов, как OsGS1;2 (глутаминсинтетаза), GAT1 (глутаминамидотрансфераза) и GAD3 (глутаматдекарбоксилаза). Сверхэкспрессия OsMYB55 способствует накоплению L-глутамата, ГАМК, аргинина и общих аминокислот, тем самым повышая термотолерантность риса [89]. NAC-транскрипционные факторы ONAC127 и ONAC129 образуют гетеродимер для поддержания нормального налива зерна и накопления крахмала у риса в условиях теплового стресса [90]. Было обнаружено, что в условиях теплового стресса ONAC127 и ONAC129 регулируют гены, связанные с транспортом питательных веществ, такие как OsMST6 (транспортер моносахаридов) и OsSWEET4 (транспортер сахаров), которые влияют на транспорт сахаров [90]. Последние исследования показывают, что у таких растений, как рис, в условиях высоких температур может существовать консервативный механизм, связывающий термоморфогенез и уровень питательных веществ, причем основную роль играет транскрипционная регуляция. В условиях теплового стресса, когда в окружающей среде достаточно азота и фосфора, фактор транскрипции HY5 подавляет экспрессию гена NRT1.1, интегратора пути поглощения азота и фосфора, у Arabidopsis thaliana, способствуя быстрому росту корней и тем самым контролируя поступление из источника [91]. При дефиците азота и фосфора в среде и воздействии на растения теплового стресса ингибирующий эффект HY5 на NRT1.1 значительно снижается, что полезно для усиления поглощения питательных веществ растением. В то же время рост корней замедляется, что дает преимущество для выживания растений в неблагоприятных условиях [91].
В условиях непрерывного теплового стресса часто одновременно возникает засушливый стресс. NAC-транскрипционный фактор SNAC3 положительно регулирует толерантность риса к высоким температурам и засухе, активируя экспрессию генов удаления АФК [39]. Кроме того, недавнее исследование показало, что ONAC023 является ключевым NAC-фактором транскрипции, участвующим в регуляции ответов на засуху и тепловой стресс у риса на протяжении большей части его фаз роста [92]. Тепловой стресс и засуха могут активировать экспрессию и ядерную транслокацию ONAC023, тем самым способствуя экспрессии стресс-чувствительных генов, таких как OsPIP2;7, PGL3, OsFKBP20-1b и OsSF3B [92].
Эти транскрипционные факторы играют ключевую роль в термотолерантности риса, повышая адаптацию растений к высокотемпературному стрессу путем регуляции экспрессии специфических генов. Дальнейшее исследование и применение этих транскрипционных факторов может обеспечить важные генетические ресурсы для улучшения термотолерантности риса и других сельскохозяйственных культур.
4. Селекция и улучшение жаростойких сортов риса
Изучение отличных генетических ресурсов имеет большое значение для селекции высококачественных сортов риса и устойчивого развития сельскохозяйственного производства. На сегодняшний день мы использовали ряд супераллелей и QTL для улучшения сортов риса, позволяя рису сохранять хороший рост и стабильную урожайность в условиях теплового стресса (Рисунок 3).
Рисунок 3. Путем углубленного анализа механизмов регуляции жаростойкости, изучения генов/QTL жаростойкости и рационального использования технологий редактирования генома были созданы сорта риса, характеризующиеся жаростойкостью, стабильной урожайностью и стабильным качеством.
В процессе эволюции SLG1 подвергся селективному распространению у азиатского культурного риса. Анализ выравнивания последовательностей показывает, что промоторные и кодирующие области SLG1 демонстрируют четкие различия между сортами indica и japonica [93]. Супераллель SLG1 у сортов indica повышает уровень тиолированной тРНК — высококонсервативной модификации тРНК у живых организмов, что полезно для повышения толерантности к таким абиотическим стрессам, как тепловой стресс [94]. Интрогрессия аллеля SLG1 от сорта indica ZF802 в сорт japonica KY131 привела к созданию почти изогенной линии (НИЛ) NIL-SLG1^Ind, которая значительно улучшила показатели выживаемости в условиях высокотемпературного стресса [94]. Аналогично, введение TT1 от сорта O. glaberrima CG14 в сорт japonica WYJ дало НИЛ NIL-TT1^SG42, которая проявила значительную толерантность к высокотемпературному стрессу как на стадии проростков, так и на стадии зрелости. Линии, несущие TT1^SG42, показали более высокую массу 1000 зерен, процент завязываемости и количество зерен в метелке в условиях высокотемпературного стресса в фазы цветения и налива зерна [62]. Интрогрессия гена TT2 от африканского сорта культурного риса HP21 (донор) в родительскую линию-реципиент HJX привела к созданию высокотермотолерантной НИЛ NIL-TT2^HPS32. Это объяснялось поддержанием стабильных слоев кутикулярного воска и снижением поступления Ca²⁺ в условиях высокотемпературного стресса по сравнению с NIL-TT2^HJX [34]. С использованием африканского сорта риса CG14 и сорта japonica WYJ была создана линия с замещением одного сегмента, и интрогрессия TT3^CG14 в WYJ дала НИЛ NIL-TT3^CG14, которая проявила термотолерантность на стадии репродуктивного роста в условиях высокотемпературного стресса [49]. Анализ геномного секвенирования показал, что ген TT3 содержит два локуса, реагирующих на температуру, TT3.1 и TT3.2, с противоположными регуляторными функциями в адаптации к тепловому стрессу. Сверхэкспрессия TT3.1^CG14 обеспечивала более высокую устойчивость риса к высоким температурам, в то время как мутант tt3.2 проявил высокую устойчивость к тепловому стрессу [49]. Кроме того, сверхэкспрессия основного транскрипта HTG3a гена HTG3 значительно усиливала толерантность к высокотемпературному стрессу. Делеция MITE (миниатюрного инвертированного повтора транспозабельного элемента, относящегося к B-подобному суперсемейству) в промоторе гена HTG3 у сорта japonica NIP значительно повышала экспрессию HTG3. И наоборот, вставка MITE в промотор гена HTG3 у сорта indica ZH97 с помощью технологии редактирования генома значительно снижала экспрессию HTG3 [93]. Интрогрессия гена HTH5 от сорта indica HHT3 в Shuhui527 и сорт japonica Sasanishiki привела к созданию почти изогенных линий, которые значительно улучшили процент завязываемости и конечную урожайность в условиях высокотемпературного стресса в фазе колошения, причем более выраженное увеличение наблюдалось у сорта Sasanishiki [36]. Большинство сортов japonica, несущих PWL1 Hap1, избегают преждевременного старения в условиях теплового стресса [95].
AtPLC9 является геном, связанным с сигналом теплового шока, у Arabidopsis thaliana. Гетерологичная экспрессия AtPLC9 в азиатском сорте риса Changyou No. 1 значительно увеличила содержание хлорофилла и выживаемость проростков в условиях высокотемпературного стресса, демонстрируя большой потенциальный вклад гетерологичной экспрессии в селекционное улучшение [96]. Учитывая высококонсервативный ген инвертазы клеточной стенки LIN5 у томата, была достигнута оптимизация распределения углерода в условиях теплового стресса у различных сортов томата M82 и современной инбредной линии томата Yuanwei-1 (YW1). Используя технологию редактирования генома, элемент ответа на тепловой стресс 'ATTCTAGAAT' был вставлен в промотор гена инвертазы клеточной стенки GIF1 у Wuyoudao-4 (WYD-4). Полученная линия wyd-gif1-de продемонстрировала более высокую урожайность с одного растения и индекс урожая в условиях теплового стресса, достигнув более рационального распределения ресурсов между источником и потребителем [97].
Используя сорт indica Huajingxian74 в качестве рекуррентного родителя и американский сорт japonica Lemont в качестве донора, была получена почти изогенная линия (НИЛ) NIL-gs10 путем создания линии замещения. Эта линия характеризовалась более мелкими зернами и сниженной массой 1000 зерен. Соответственно, мы определили аллель Huajingxian74 как GS10, также известный как MADS56 [98,99]. Геномная инверсия — это сложный тип структурной вариации генома. Локус инверсии eQTL OsINV10, расположенный в промоторной области MADS56, значительно усиливал экспрессию MADS56 и сильно повышал его толерантность к тепловому стрессу [98,99]. В процессе эволюции ген гаплотипа SRL10^HaP3 подвергся сильному отбору у риса типа aus. Этот гаплотип демонстрировал значительно более высокие уровни экспрессии, чем другие гаплотипы, и достигал значительно улучшенных показателей завязываемости семян при тепловом стрессе 42 °C [100]. МикроРНК (miRNA) также обладают большим потенциалом в повышении термотолерантности риса. Перенос miR169r-5p от жаростойкого сорта риса Gan-Xiang-Nuo (GXN) в тепловосприимчивый сорт Hua-Jing-Xian-74 (HJX) значительно оптимизировал адаптацию к тепловому стрессу на стадии цветения [101].
Линия с замещением одного сегмента IL01-15, сформированная путем введения единственного фрагмента, содержащего qHTB1-1^HHT4, от Hehuatang No. 4 в сорт R53, проявила чрезвычайно высокую фертильность колосков в условиях высокотемпературного стресса, со значительным увеличением процента завязываемости и количества колосков [102]. Путем создания рекомбинантных инбредных линий сегменты QTL DTH8, qHD3, qHD5 и qHD7 от сорта риса Dan 71 были введены в сорт Zhonghui 161, что задержало фазу колошения и эффективно позволило избежать колошения в периоды высоких температур, тем самым снизив ущерб урожаю от высоких температур. QTL qSF1, qSF2, qSF3.2 и qSF8 у Zhonghui 161, а также qSF3.1 у Dan 71 эффективно улучшили фертильность колосков в условиях высоких температур [103]. Тепловосприимчивый сорт IR64 содержит сегмент QTL термотолерантности qHTSF1.1; его введение в жаростойкий сорт риса N22 незначительно улучшило его фертильность при высокой температуре. qHTSF4.1 — это сегмент QTL термотолерантности, расположенный у сорта N22; введение qHTSF4.1^N22 в IR64 значительно усилило его фертильность на стадии инициации метелки в условиях теплового стресса. Более того, анализ фертильности при инициации метелки у потомства скрещивания между N22 и IR64 указал на взаимодействие между двумя QTL qHTSF1.1 и qHTSF4.1 [104]. Сорт indica IR64 содержит QTL раннего цветения qEMF3. Путем создания почти изогенных линий и введения его в рекуррентный родитель Nanjing 11 время цветения Nanjing 11 было значительно сдвинуто на более ранний срок, что помогло избежать цветения в периоды самых высоких температур и предотвратило повреждение высокой температурой [105]. Пирамидирование генов способствует более эффективной селекции превосходных сортов. Аналогично, путем скрещивания почти изогенных линий NIL-qHTSF4.1^N22 и NIL-qEMF3^IR64 была получена линия с пирамидой генов NIL-qHTSF4.1^N22 qEMF3^IR64 на фоне IR64, которая значительно повысила фертильность колосков и процент завязываемости в условиях высокотемпературного стресса, а также сдвинула время цветения на более ранний срок, чтобы избежать вреда от высоких температур, что полностью демонстрирует превосходство пирамидирования генов при их объединении [106]. Жаростойкий сорт риса Liaoyan241 содержит сегменты QTL qHTS3, qHTS1b и qHTS4. Аналогично, путем создания рекомбинантных инбредных линий и введения этих трех сегментов QTL в тепловосприимчивый суходольный сорт риса IAPAR-9 была улучшена толерантность к высокой температуре в фазы колошения и цветения. Супергаплотип qHTS1a^IAPAR−9 проявил сильную устойчивость к тепловому стрессу, в то время как qHTS3^IAPAR−9 лишь незначительно улучшил устойчивость к тепловому стрессу [107,108].
Несмотря на то, что использование превосходных генетических ресурсов жаростойкости уже дало некоторые положительные результаты, наше понимание этой области остается ограниченным. Будущие исследования должны быть сосредоточены на активном изучении отличных генетических ресурсов жаростойкости с целью пирамидирования генов жаростойкости для создания высококачественных, жаростойких сортов риса.
5. Заключение и перспективы
В связи с глобальным изменением климата и увеличением частоты экстремальных высокотемпературных явлений тепловой стресс уже оказал широкомасштабное воздействие на производство сельскохозяйственных культур. Чтобы удовлетворить постоянно растущий спрос на продовольствие, селекция высокотермотолерантных сортов является первоочередной задачей в борьбе с тепловым стрессом в настоящее время. На сегодняшний день, хотя идентифицировано множество генов, связанных с толерантностью риса к тепловому стрессу, их применение все еще очень ограничено, и существует много пробелов в понимании реакций риса на тепловой стресс [109,110]. До сих пор наше понимание основных генов устойчивости, включая тепловой стресс и наложение множественных абиотических стрессов, все еще очень ограничено, что указывает на то, что это может быть проблемой, заслуживающей глубокого изучения. Кроме того, в настоящее время понимание сенсоров в клетках риса, которые непосредственно воспринимают сигналы теплового стресса, все еще очень ограничено. Из-за возможной избыточности некоторых генов, кодирующих сенсоры, и летальности мутаций в этих генах, отсутствие подходящих методов исследования делает идентификацию этих сенсоров, связанных с температурным стрессом, очень сложной задачей [111]. Экспериментальные результаты, полученные в лабораторных условиях, часто сильно отличаются от результатов, полученных в реальных полевых условиях. Например, в условиях одного лишь теплового стресса устьица листьев растений будут открываться для охлаждения путем транспирации. Однако реальность такова, что засушливый стресс часто возникает одновременно с тепловым, и засушливый стресс будет подавлять открытие устьиц, чтобы уменьшить потерю воды растениями [112]. Совместное возникновение множественных стрессов будет серьезно повреждать рост и развитие растений, и это также является центром внимания будущих исследователей. Долгое время исследования тепловых сенсоров в условиях высокотемпературного стресса были в основном сосредоточены на клеточной мембране. Однако клеточное ядро, как центральная органелла для транскрипционной регуляции при тепловом стрессе, также может содержать первичные сенсоры сигналов. Ученые разрабатывают нанотермометры. Эти крошечные термометры могут выявлять различия температур между разными клетками и внутри одной клетки для изучения прямой реакции клеточного ядра на изменения температуры [113]. В будущем ожидается применение этой технологии на растениях для идентификации большего количества ядерных сенсоров сигналов теплового стресса. Кроме того, по мере постепенного созревания вспомогательных технологий, рациональное использование GWAS и других технических средств для изучения отличных природных аллелей, использование CRISPR/Cas9 и других технологий редактирования генома для точного создания превосходных аллелей, а также использование ИИ и анализа больших данных для прогнозирования комбинаций аллелей с отличными признаками и новых генов с функциями жаростойкости — эти методы имеют положительное значение для повышения жаростойкости риса. Сочетание традиционных методов селекции с современными молекулярными биотехнологиями позволяет быстрее и точнее достичь селекции и улучшения жаростойких сортов риса, что требует углубленного анализа функций генов жаростойкости для содействия определению конкретных путей термотолерантности риса и, таким образом, получения наиболее подходящих стратегий улучшения жаростойких сортов риса. В итоге, применение новых технологий привнесло большие изменения в методы селекции, повысило эффективность и точность селекции и предоставило возможность для быстрого и эффективного выведения высокоурожайных и жаростойких сортов риса, что помогает удовлетворить растущий спрос на продовольствие и противостоять экологическим вызовам.
Ссылки
1. IPCC. 2023: Sections. In Climate Change 2023: Synthesis Report. Contribution of Working Groups I, II and III to the Sixth Assessment Report of the Intergovernmental Panel on Climate Change; Core Writing Team, Lee, H., Romero, J., Eds.; IPCC: Geneva, Switzerland, 2023; pp. 35–115. [Google Scholar] [CrossRef]
2. Zhao, C.; Liu, B.; Piao, S.; Wang, X.; Lobell, D.B.; Huang, Y.; Huang, M.; Yao, Y.; Bassu, S.; Ciais, P.; et al. Temperature increase reduces global yields of major crops in four independent estimates. Proc. Natl. Acad. Sci. USA 2017, 114, 9326–9331. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
3. Song, Y.; Wang, C.; Linderholm, H.W.; Fu, Y.; Cai, W.; Xu, J.; Zhuang, L.; Wu, M.; Shi, Y.; Wang, G.; et al. The negative impact of increasing temperatures on rice yields in southern China. Sci. Total Environ. 2022, 820, 153262. [Google Scholar] [CrossRef] [PubMed]
4. Liu, X.; Ciais, P.; Makowski, D.; Liang, J. Warming Leads to Lower Rice Quality in East Asia. Geophys. Res. Lett. 2024, 51, e2024GL110557. [Google Scholar] [CrossRef]
5. Khan, S.; Anwar, S.; Ashraf, M.Y.; Khaliq, B.; Sun, M.; Hussain, S.; Gao, Z.Q.; Noor, H.; Alam, S. Mechanisms and Adaptation Strategies to Improve Heat Tolerance in Rice. A Review. Plants 2019, 8, 508. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
6. Shi, P.; Tang, L.; Wang, L.; Sun, T.; Liu, L.; Cao, W.; Zhu, Y. Post-Heading Heat Stress in Rice of South China during 1981–2010. PLoS ONE 2015, 10, e0130642. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
7. Li, Y.; Tang, Y.; Wu, Y.F.; Jiang, M.; Chen, J.D. Response Mechanism and Defense Measures Against High Temperature Adversity in Rice: A Review. Chin. Agric. Sci. Bull. 2024, 40, 1–10. [Google Scholar] [CrossRef]
8. Das, S.; Krishnan, P.; Nayak, M.; Ramakrishnan, B. High temperature stress effects on pollens of rice (Oryza sativa L.) genotypes. Environ. Exp. Bot. 2014, 101, 36–46. [Google Scholar] [CrossRef]
9. Aghamolki, M.T.K.; Yusop, M.K.; Oad, F.C.; Zakikhani, H.; Jaafar, H.Z.; Kharidah, S.; Hanafi, M.M. Heat stress effects on yield parameters of selected rice cultivars at reproductive growth stages. J. Food Agric. Environ. 2014, 12, 741–746. [Google Scholar]
10. Ding, C.; Shao, Z.; Yan, Y.; Zhang, G.; Zeng, D.; Zhu, L.; Hu, J.; Gao, Z.; Dong, G.; Qian, Q.; et al. Carotenoid isomerase regulates rice tillering and grain productivity by its biosynthesis pathway. J. Integr. Plant Biol. 2024, 66, 172–175. [Google Scholar] [CrossRef] [PubMed]
11. Ji, D.L.; Xiao, W.H.; Sun, Z.W.; Liu, L.J.; Gu, J.F.; Zhang, H.; Matthew, T.H.; Liu, K.; Wang, Z.Q.; Wang, W.L.; et al. Translocation and Distribution of Carbon-Nitrogen in Relation to Rice Yield and Grain Quality as Affected by High Temperature at Early Panicle Initiation Stage. Rice Sci. 2023, 30, 598–612. [Google Scholar] [CrossRef]
12. Liu, X.; Ji, P.; Liao, J.; Duan, X.; Luo, Z.; Yu, X.; Jiang, C.J.; Xu, C.; Yang, H.; Peng, B.; et al. CRISPR/Cas knockout of the NADPH oxidase gene OsRbohB reduces ROS overaccumulation and enhances heat stress tolerance in rice. Plant Biotechnol. J. 2025, 23, 336–351. [Google Scholar] [CrossRef] [PubMed]
13. Lin, G.; Yang, Y.; Chen, X.; Yu, X.; Wu, Y.; Xiong, F. Effects of high temperature during two growth stages on caryopsis development and physicochemical properties of starch in rice. Int. J. Biol. Macromol. 2020, 145, 301–310. [Google Scholar] [CrossRef] [PubMed]
14. Bahuguna, R.N.; Jha, J.; Pal, M.; Shah, D.; Lawas, L.M.; Khetarpal, S.; Jagadish, K.S. Physiological and biochemical characterization of NERICA-L-44: A novel source of heat tolerance at the vegetative and reproductive stages in rice. Physiol. Plant. 2015, 154, 543–559. [Google Scholar] [CrossRef] [PubMed]
15. Hayano-Saito, Y.; Hayashi, K. Stvb-i, a Rice Gene Conferring Durable Resistance to Rice stripe virus, Protects Plant Growth from Heat Stress. Front. Plant Sci. 2020, 11, 519. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
16. Gu, X.; Si, F.; Feng, Z.; Li, S.; Liang, D.; Yang, P.; Yang, C.; Yan, B.; Tang, J.; Yang, Y.; et al. The OsSGS3-tasiRNA-OsARF3 module orchestrates abiotic-biotic stress response trade-off in rice. Nat. Commun. 2023, 14, 4441. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
17. Mamrutha, H.M.; Rinki Singh, S.K.; Gopalareddy, K.; Tiwari, R.; Venkatesh, K.; Kumar, Y.; Singh, G.; Singh, G.P. Abiotic stress tolerance in wheat: Physiological interventions. In New Horizons in Wheat and Barley Research; Kashyap, P.L., Gupta, V., Gupta, O.P., Sendhil, R., Gopalareddy, K., Jasrotia, P., Singh, G.P., Eds.; Springer: Singapore, 2022; pp. 507–530. [Google Scholar] [CrossRef]
18. Xing, Y.H.; Lu, H.; Zhu, X.; Deng, Y.; Xie, Y.; Luo, Q.; Yu, J. How Rice Responds to Temperature Changes and Defeats Heat Stress. Rice 2024, 17, 73. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
19. Arshad, M.S.; Farooq, M.; Asch, F.; Krishna, J.S.V.; Prasad, P.V.V.; Siddique, K.H.M. Thermal stress impacts reproductive development and grain yield in rice. Plant Physiol. Biochem. 2017, 115, 57–72. [Google Scholar] [CrossRef] [PubMed]
20. Jagadish, S.V.; Craufurd, P.Q.; Wheeler, T.R. High temperature stress and spikelet fertility in rice (Oryza sativa L.). J. Exp. Bot. 2007, 58, 1627–1635. [Google Scholar] [CrossRef] [PubMed]
21. Xu, H.; Li, X.; Zhang, H.; Wang, L.; Zhu, Z.; Gao, J.; Li, C.; Zhu, Y. High temperature inhibits the accumulation of storage materials by inducing alternative splicing of OsbZIP58 during filling stage in rice. Plant Cell Environ. 2020, 43, 1879–1896. [Google Scholar] [CrossRef] [PubMed]
22. Ma, B.; Zhang, L.; He, Z. Understanding the regulation of cereal grain filling: The way forward. J. Integr. Plant Biol. 2023, 65, 526–547. [Google Scholar] [CrossRef] [PubMed]
23. Julius, B.T.; Leach, K.A.; Tran, T.M.; Mertz, R.A.; Braun, D.M. Sugar Transporters in Plants: New Insights and Discoveries. Plant Cell Physiol. 2017, 58, 1442–1460. [Google Scholar] [CrossRef] [PubMed]
24. Chen, L.; Li, X.; Zheng, M.; Hu, R.; Dong, J.; Zhou, L.; Liu, W.; Liu, D.; Yang, W. Genes controlling grain chalkiness in rice. Crop J. 2024, 12, 979–991. [Google Scholar] [CrossRef]
25. Sun, T.; Liu, B.; Hasegawa, T.; Liao, Z.; Tang, L.; Liu, L.; Cao, W.; Zhu, Y. Sink-source unbalance leads to abnormal partitioning of biomass and nitrogen in rice under extreme heat stress: An experimental and modeling study. Eur. J. Agron. 2022, 142, 126678. [Google Scholar] [CrossRef]
26. Lu, Y.; Wang, Q.; Duan, X.; Zhang, D.; Sun, H. Effect of harvest period on the eating quality and starch characteristics of Nanjing 3908. J. Zhejiang Univ. (Agric. Life Sci.) 2024, 50, 406–417. [Google Scholar] [CrossRef]
27. Wu, H.; Ren, Y.; Dong, H.; Xie, C.; Zhao, L.; Wang, X.; Zhang, F.; Zhang, B.; Jiang, X.; Huang, Y.; et al. FLOURY ENDOSPERM24, a heat shock protein 101 (HSP101), is required for starch biosynthesis and endosperm development in rice. New Phytol. 2024, 242, 2635–2651. [Google Scholar] [CrossRef] [PubMed]
28. Sita, K.; Sehgal, A.; HanumanthaRao, B.; Nair, R.M.; Vara Prasad, P.V.; Kumar, S.; Gaur, P.M.; Farooq, M.; Siddique, K.H.M.; Varshney, R.K.; et al. Food Legumes and Rising Temperatures: Effects, Adaptive Functional Mechanisms Specific to Reproductive Growth Stage and Strategies to Improve Heat Tolerance. Front. Plant Sci. 2017, 8, 1658. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
29. Nawaz, Z.; Kakar, K.U.; Saand, M.A.; Shu, Q.Y. Cyclic nucleotide-gated ion channel gene family in rice, identification, characterization and experimental analysis of expression response to plant hormones, biotic and abiotic stresses. BMC Genom. 2014, 15, 853. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
30. Cui, Y.; Lu, S.; Li, Z.; Cheng, J.; Hu, P.; Zhu, T.; Wang, X.; Jin, M.; Wang, X.; Li, L.; et al. CYCLIC NUCLEOTIDE-GATED ION CHANNELs 14 and 16 Promote Tolerance to Heat and Chilling in Rice. Plant Physiol. 2020, 183, 1794–1808. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
31. Luo, L.; Cui, Y.; Ouyang, N.; Huang, S.; Gong, X.; Wei, L.; Zou, B.; Hua, J.; Lu, S. Tolerance to multiple abiotic stresses is mediated by interacting CNGC proteins that regulate Ca2+ influx and stomatal movement in rice. J. Integr. Plant Biol. 2025. Epub ahead of print. [Google Scholar] [CrossRef] [PubMed]
32. Qiao, B.; Zhang, Q.; Liu, D.; Wang, H.; Yin, J.; Wang, R.; He, M.; Cui, M.; Shang, Z.; Wang, D.; et al. A calcium-binding protein, rice annexin OsANN1, enhances heat stress tolerance by modulating the production of H2O2. J. Exp. Bot. 2015, 66, 5853–5866. [Google Scholar] [CrossRef]
33. Wang, X.; Ma, X.; Wang, H.; Li, B.; Clark, G.; Guo, Y.; Roux, S.; Sun, D.; Tang, W. Proteomic study of microsomal proteins reveals a key role for Arabidopsis annexin 1 in mediating heat stress-induced increase in intracellular calcium levels. Mol. Cell. Proteom. 2015, 14, 686–694. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
34. Kan, Y.; Mu, X.; Zhang, H.; Gao, J.; Shan, J.-X.; Ye, W.-W.; Lin, H.-X. TT2 controls rice thermotolerance through SCT1-dependent alteration of wax biosynthesis. Nat. Plants 2022, 8, 53–67. [Google Scholar] [CrossRef] [PubMed]
35. Mei, W.; Chen, W.; Wang, Y.; Liu, Z.; Dong, Y.; Zhang, G.; Deng, H.; Liu, X.; Lu, X.; Wang, F.; et al. Exogenous Kinetin Modulates ROS Homeostasis to Affect Heat Tolerance in Rice Seedlings. Int. J. Mol. Sci. 2023, 24, 6252. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
36. Cao, Z.; Tang, H.; Cai, Y.; Zeng, B.; Zhao, J.; Tang, X.; Lu, M.; Wang, H.; Zhu, X.; Wu, X.; et al. Natural variation of HTH5 from wild rice, Oryza rufipogon Griff., is involved in conferring high-temperature tolerance at the heading stage. Plant Biotechnol. J. 2022, 20, 1591–1605. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
37. Allakhverdiev, S.I.; Kreslavski, V.D.; Klimov, V.V.; Los, D.A.; Carpentier, R.; Mohanty, P. Heat stress: An overview of molecular responses in photosynthesis. Photosynth. Res. 2008, 98, 541–550. [Google Scholar] [CrossRef] [PubMed]
38. Shiraya, T.; Mori, T.; Maruyama, T.; Sasaki, M.; Takamatsu, T.; Oikawa, K.; Itoh, K.; Kaneko, K.; Ichikawa, H.; Mitsui, T. Golgi/plastid-type manganese superoxide dismutase involved in heat-stress tolerance during grain filling of rice. Plant Biotechnol. J. 2015, 13, 1251–1263. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
39. Fang, Y.; Liao, K.; Du, H.; Xu, Y.; Song, H.; Li, X.; Xiong, L. A stress-responsive NAC transcription factor SNAC3 confers heat and drought tolerance through modulation of reactive oxygen species in rice. J. Exp. Bot. 2015, 66, 6803–6817. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
40. Liao, M.; Ma, Z.; Kang, Y.; Zhang, B.; Gao, X.; Yu, F.; Yang, P.; Ke, Y. ENHANCED DISEASE SUSCEPTIBILITY 1 promotes hydrogen peroxide scavenging to enhance rice thermotolerance. Plant Physiol. 2023, 192, 3106–3119. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
41. Choi, J.; Roy Choudhury, A.; Walitang, D.I.; Lee, Y.; Sa, T. ACC deaminase-producing Brevibacterium linens RS16 enhances heat-stress tolerance of rice (Oryza sativa L.). Physiol. Plant. 2022, 174, e13584. [Google Scholar] [CrossRef] [PubMed]
42. Chai, J.; Gu, X.; Song, P.; Zhao, X.; Gao, Y.; Wang, H.; Zhang, Q.; Cai, T.; Liu, Y.; Li, X.; et al. Histone demethylase JMJ713 interaction with JMJ708 modulating H3K36me2, enhances rice heat tolerance through promoting hydrogen peroxide scavenging. Plant Physiol. Biochem. 2024, 217, 109284. [Google Scholar] [CrossRef] [PubMed]
43. Li, X.; Tang, H.; Xu, T.; Wang, P.; Ma, F.; Wei, H.; Fang, Z.; Wu, X.; Wang, Y.; Xue, Y.; et al. N-terminal acetylation orchestrates glycolate-mediated ROS homeostasis to promote rice thermoresponsive growth. New Phytol. 2024, 243, 1742–1757. [Google Scholar] [CrossRef] [PubMed]
44. Lv, Y.; Shao, G.; Qiu, J.; Jiao, G.; Sheng, Z.; Xie, L.; Wu, Y.; Tang, S.; Wei, X.; Hu, P. White Leaf and Panicle 2, encoding a PEP-associated protein, is required for chloroplast biogenesis under heat stress in rice. J. Exp. Bot. 2017, 68, 5147–5160. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
45. Qiu, Z.; Kang, S.; He, L.; Zhao, J.; Zhang, S.; Hu, J.; Zeng, D.; Zhang, G.; Dong, G.; Gao, Z.; et al. The newly identified heat-stress sensitive albino 1 gene affects chloroplast development in rice. Plant Sci. 2018, 267, 168–179. [Google Scholar] [CrossRef] [PubMed]
46. Wang, Y.; Wang, Y.; Ren, Y.; Duan, E.; Zhu, X.; Hao, Y.; Zhu, J.; Chen, R.; Lei, J.; Teng, X.; et al. White panicle2 encoding thioredoxin z, regulates plastid RNA editing by interacting with multiple organellar RNA editing factors in rice. New Phytol. 2021, 229, 2693–2706. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
47. He, L.; Zhang, S.; Qiu, Z.; Zhao, J.; Nie, W.; Lin, H.; Zhu, Z.; Zeng, D.; Qian, Q.; Zhu, L. FRUCTOKINASE-LIKE PROTEIN 1 interacts with TRXz to regulate chloroplast development in rice. J. Integr. Plant Biol. 2018, 60, 94–111. [Google Scholar] [CrossRef] [PubMed]
48. Mathur, S.; Agrawal, D.; Jajoo, A. Photosynthesis: Response to high temperature stress. J. Photochem. Photobiol. B 2014, 137, 116–126. [Google Scholar] [CrossRef] [PubMed]
49. Zhang, H.; Zhou, J.F.; Kan, Y.; Shan, J.X.; Ye, W.W.; Dong, N.Q.; Guo, T.; Xiang, Y.H.; Yang, Y.B.; Li, Y.C.; et al. A genetic module at one locus in rice protects chloroplasts to enhance thermotolerance. Science 2022, 376, 1293–1300. [Google Scholar] [CrossRef] [PubMed]
50. Ahmad, S.; Tabassum, J.; Sheng, Z.; Lv, Y.; Chen, W.; Zeb, A.; Dong, N.; Ali, U.; Shao, G.; Wei, X.; et al. Loss-of-function of PGL10 impairs photosynthesis and tolerance to high-temperature stress in rice. Physiol. Plant. 2024, 176, e14369. [Google Scholar] [CrossRef] [PubMed]
51. Jiang, H.; Zhang, A.; Ruan, B.; Hu, H.; Guo, R.; Chen, J.; Qian, Q.; Gao, Z. Identification of Green-Revertible Yellow 3 (GRY3), encoding a 4-hydroxy-3-methylbut-2-enyl diphosphate reductase involved in chlorophyll synthesis under high temperature and high light in rice. Crop J. 2023, 11, 1171–1180. [Google Scholar] [CrossRef]
52. Xia, S.; Liu, H.; Cui, Y.; Yu, H.; Rao, Y.; Yan, Y.; Zeng, D.; Hu, J.; Zhang, G.; Gao, Z.; et al. UDP-N-acetylglucosamine pyrophosphorylase enhances rice survival at high temperature. New Phytol. 2022, 233, 344–359. [Google Scholar] [CrossRef] [PubMed]
53. Perdomo, J.A.; Capó-Bauçà, S.; Carmo-Silva, E.; Galmés, J. Rubisco and Rubisco Activase Play an Important Role in the Biochem-ical Limitations of Photosynthesis in Rice, Wheat, and Maize under High Temperature and Water Deficit. Front. Plant Sci. 2017, 8, 490. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
54. Qu, Y.; Sakoda, K.; Fukayama, H.; Kondo, E.; Suzuki, Y.; Makino, A.; Terashima, I.; Yamori, W. Overexpression of both Rubisco and Rubisco activase rescues rice photosynthesis and biomass under heat stress. Plant Cell Environ. 2021, 44, 2308–2320. [Google Scholar] [CrossRef] [PubMed]
55. He, W.; Wang, L.; Lin, Q.; Yu, F. Rice seed storage proteins: Biosynthetic pathways and the effects of environmental factors. J. Integr. Plant Biol. 2021, 63, 1999–2019. [Google Scholar] [CrossRef] [PubMed]
56. Cao, R.; Zhao, S.; Jiao, G.; Duan, Y.; Ma, L.; Dong, N.; Lu, F.; Zhu, M.; Shao, G.; Hu, S.; et al. OPAQUE3, encoding a transmembrane bZIP transcription factor, regulates endosperm storage protein and starch biosynthesis in rice. Plant Commun. 2022, 3, 100463. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
57. Howell, S.H. Evolution of the unfolded protein response in plants. Plant Cell Environ. 2021, 44, 2625–2635. [Google Scholar] [CrossRef] [PubMed]
58. Lu, S.J.; Yang, Z.T.; Sun, L.; Sun, L.; Song, Z.T.; Liu, J.X. Conservation of IRE1-regulated bZIP74 mRNA unconventional splicing in rice (Oryza sativa L.) involved in ER stress responses. Mol. Plant 2012, 5, 504–514. [Google Scholar] [CrossRef] [PubMed]
59. Kotak, S.; Larkindale, J.; Lee, U.; von Koskull-Döring, P.; Vierling, E.; Scharf, K.D. Complexity of the heat stress response in plants. Curr. Opin. Plant Biol. 2007, 10, 310–316. [Google Scholar] [CrossRef] [PubMed]
60. Liu, X.H.; Lyu, Y.S.; Yang, W.; Yang, Z.T.; Lu, S.J.; Liu, J.X. A membrane-associated NAC transcription factor OsNTL3 is involved in thermotolerance in rice. Plant Biotechnol. J. 2020, 18, 1317–1329. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
61. Hayashi, S.; Wakasa, Y.; Takahashi, H.; Kawakatsu, T.; Takaiwa, F. Signal transduction by IRE1-mediated splicing of bZIP50 and other stress sensors in the endoplasmic reticulum stress response of rice. Plant J. 2012, 69, 946–956. [Google Scholar] [CrossRef]
62. Li, X.M.; Chao, D.Y.; Wu, Y.; Huang, X.; Chen, K.; Cui, L.G.; Su, L.; Ye, W.W.; Chen, H.; Chen, H.C.; et al. Natural alleles of a proteasome α2 subunit gene contribute to thermotolerance and adaptation of African rice. Nat. Genet. 2015, 47, 827–833. [Google Scholar] [CrossRef] [PubMed]
63. Yu, H.X.; Cao, Y.J.; Yang, Y.B.; Shan, J.X.; Ye, W.W.; Dong, N.Q.; Kan, Y.; Zhao, H.Y.; Lu, Z.Q.; Guo, S.Q.; et al. A TT1-SCE1 module integrates ubiquitination and SUMOylation to regulate heat tolerance in rice. Mol. Plant 2024, 17, 1899–1918. [Google Scholar] [CrossRef] [PubMed]
64. Kim, J.H.; Lim, S.D.; Jang, C.S. Oryza sativa heat-induced RING finger protein 1 (OsHIRP1) positively regulates plant response to heat stress. Plant Mol. Biol. 2019, 99, 545–559. [Google Scholar] [CrossRef] [PubMed]
65. Lim, S.D.; Cho, H.Y.; Park, Y.C.; Ham, D.J.; Lee, J.K.; Jang, C.S. The rice RING finger E3 ligase, OsHCI1, drives nuclear export of multiple substrate proteins and its heterogeneous overexpression enhances acquired thermotolerance. J. Exp. Bot. 2013, 64, 2899–2914. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
66. Wu, X.; Shiroto, Y.; Kishitani, S.; Ito, Y.; Toriyama, K. Enhanced heat and drought tolerance in transgenic rice seedlings overexpressing OsWRKY11 under the control of HSP101 promoter. Plant Cell Rep. 2009, 28, 21–30. [Google Scholar] [CrossRef] [PubMed]
67. Dong, K.; Wu, F.; Cheng, S.; Li, S.; Zhang, F.; Xing, X.; Jin, X.; Luo, S.; Feng, M.; Miao, R.; et al. OsPRMT6a-mediated arginine methylation of OsJAZ1 regulates jasmonate signaling and spikelet development in rice. Mol. Plant 2024, 17, 900–919. [Google Scholar] [CrossRef] [PubMed]
68. Ding, W.; Gou, Y.; Li, Y.; Li, J.; Fang, Y.; Liu, X.; Zhu, X.; Ye, R.; Heng, Y.; Wang, H.; et al. A jasmonate-mediated regulatory network modulates diurnal floret opening time in rice. New Phytol. 2024, 244, 176–191. [Google Scholar] [CrossRef] [PubMed]
69. Li, J.; Yang, J.; Zhu, B.; Xie, G. Overexpressing OsFBN1 enhances plastoglobule formation, reduces grain-filling percent and jasmonate levels under heat stress in rice. Plant Sci. 2019, 285, 230–238. [Google Scholar] [CrossRef] [PubMed]
70. Qiu, R.; Yao, P.; Yang, J.; Hou, J.; Xiao, H.; Wu, Y.; Tu, D.; Ma, X.; Zhao, Y.; Li, L. OsIAA7 enhances heat stress tolerance by inhibiting the activity of OsARF6 in rice. Int. J. Biol. Macromol. 2024, 288, 138746. [Google Scholar] [CrossRef] [PubMed]
71. Chen, Z.; Zhou, W.; Guo, X.; Ling, S.; Li, W.; Wang, X.; Yao, J. Heat Stress Responsive Aux/IAA Protein, OsIAA29 Regulates Grain Filling Through OsARF17 Mediated Auxin Signaling Pathway. Rice 2024, 17, 16. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
72. Sharma, L.; Dalal, M.; Verma, R.; Kumar, S.; Yadav, S.; Pushkar, S.; Kushwaha, S.; Bhowmik, A.; Chinnusamy, V. Auxin protects spikelet fertility and grain yield under drought and heat stresses in rice. Environ. Exp. Bot. 2018, 150, 9–24. [Google Scholar] [CrossRef]
73. Chen, Y.; Xiang, Z.; Liu, M.; Wang, S.; Zhang, L.; Cai, D.; Huang, Y.; Mao, D.; Fu, J.; Chen, L. ABA biosynthesis gene OsNCED3 contributes to preharvest sprouting resistance and grain development in rice. Plant Cell Environ. 2023, 46, 1384–1401. [Google Scholar] [CrossRef] [PubMed]
74. Zhao, Q.; Guan, X.; Zhou, L.; Asad, M.A.; Xu, Y.; Pan, G.; Cheng, F. ABA-triggered ROS burst in rice developing anthers is critical for tapetal programmed cell death induction and heat stress-induced pollen abortion. Plant Cell Environ. 2023, 46, 1453–1471. [Google Scholar] [CrossRef] [PubMed]
75. Liu, X.; Zhong, X.; Liao, J.; Ji, P.; Yang, J.; Cao, Z.; Duan, X.; Xiong, J.; Wang, Y.; Xu, C.; et al. Exogenous abscisic acid improves grain filling capacity under heat stress by enhancing antioxidative defense capability in rice. BMC Plant Biol. 2023, 23, 619. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
76. Chen, Y.; Zhang, R.; Wang, R.; Li, J.; Wu, B.; Zhang, H.; Xiao, G. Overexpression of OsRbohH Enhances Heat and Drought Tolerance through ROS Homeostasis and ABA Mediated Pathways in Rice (Oryza sativa L.). Plants 2024, 13, 2494. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
77. Wang, W.; Zhao, C.; Li, G.; Xu, K.; Jiang, D.; Huo, Z. Role of salicylic acid in plant response to cold stress. Plant Physiol. J. 2020, 56, 2585–2594. [Google Scholar] [CrossRef]
78. Guo, J.; Wang, Z.; Li, J.; Qu, L.; Chen, Y.; Li, G.; Lu, D. Salicylic acid promotes endosperm development and heat-tolerance of waxy maize (Zea mays L. var. ceratina Kulesh) under heat stress. Plant Stress 2024, 14, 100684. [Google Scholar] [CrossRef]
79. Zhang, C.; Feng, B.; Chen, T.; Zhang, X.; Tao, L.; Fu, G. Sugars, antioxidant enzymes and IAA mediate salicylic acid to prevent rice spikelet degeneration caused by heat stress. Plant Growth Regul. 2017, 83, 313–323. [Google Scholar] [CrossRef]
80. Feng, B.; Zhang, C.; Chen, T.; Zhang, X.; Tao, L.; Fu, G. Salicylic acid reverses pollen abortion of rice caused by heat stress. BMC Plant Biol. 2018, 18, 245. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
81. Chen, Y.; Wang, Y.; Chen, H.; Xiang, J.; Zhang, Y.; Wang, Z.; Zhu, D.; Zhang, Y. Brassinosteroids Mediate Endogenous Phytohormone Metabolism to Alleviate High Temperature Injury at Panicle Initiation Stage in Rice. Rice Sci. 2023, 30, 70–86. [Google Scholar] [CrossRef]
82. Zhang, W.; Huang, H.; Zhou, Y.; Zhu, K.; Wu, Y.; Xu, Y.; Wang, W.; Zhang, H.; Gu, J.; Xiong, F.; et al. Brassinosteroids mediate moderate soil-drying to alleviate spikelet degeneration under high temperature during meiosis of rice. Plant Cell Environ. 2023, 46, 1340–1362. [Google Scholar] [CrossRef] [PubMed]
83. Singh, I.; Shono, M. Physiological and Molecular Effects of 24-Epibrassinolide, a Brassinosteroid on Thermotolerance of Tomato. Plant Growth Regul. 2005, 47, 111–119. [Google Scholar] [CrossRef]
84. Kaur, H.; Sirhindi, G.; Bhardwaj, R.; Alyemeni, M.N.; Siddique, K.H.M.; Ahmad, P. 28-homobrassinolide regulates antioxidant enzyme activities and gene expression in response to salt- and temperature-induced oxidative stress in Brassica juncea. Sci. Rep. 2018, 8, 8735. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
85. Cheng, Q.; Zhou, Y.; Liu, Z.; Zhang, L.; Song, G.; Guo, Z.; Wang, W.; Qu, X.; Zhu, Y.; Yang, D. An alternatively spliced heat shock tran-scription factor, OsHSFA2dI, functions in the heat stress-induced unfolded protein response in rice. Plant Biol. 2015, 17, 419–429. [Google Scholar] [CrossRef] [PubMed]
86. Chen, S.; Cao, H.; Huang, B.; Zheng, X.; Liang, K.; Wang, G.L.; Sun, X. The WRKY10-VQ8 module safely and effectively regulates rice thermotolerance. Plant Cell Environ. 2022, 45, 2126–2144. [Google Scholar] [CrossRef] [PubMed]
87. Zhang, H.; Xu, H.; Feng, M.; Zhu, Y. Suppression of OsMADS7 in rice endosperm stabilizes amylose content under high temperature stress. Plant Biotechnol. J. 2018, 16, 18–26. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
88. Qiu, F.; Zheng, Y.; Lin, Y.; Woldegiorgis, S.T.; Xu, S.; Feng, C.; Huang, G.; Shen, H.; Xu, Y.; Kabore, M.A.F.; et al. Integrated ATAC-Seq and RNA-Seq Data Analysis to Reveal OsbZIP14 Function in Rice in Response to Heat Stress. Int. J. Mol. Sci. 2023, 24, 5619. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
89. El-Kereamy, A.; Bi, Y.M.; Ranathunge, K.; Beatty, P.H.; Good, A.G.; Rothstein, S.J. The rice R2R3-MYB transcription factor OsMYB55 is involved in the tolerance to high temperature and modulates amino acid metabolism. PLoS ONE 2012, 7, e52030. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
90. Ren, Y.; Huang, Z.; Jiang, H.; Wang, Z.; Wu, F.; Xiong, Y.; Yao, J. A heat stress responsive NAC transcription factor heterodimer plays key roles in rice grain filling. J. Exp. Bot. 2021, 72, 2947–2964. [Google Scholar] [CrossRef] [PubMed]
91. Lee, S.; Showalter, J.; Zhang, L.; Cassin-Ross, G.; Rouached, H.; Busch, W. Nutrient levels control root growth responses to high ambient temperature in plants. Nat. Commun. 2024, 15, 4689. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
92. Chang, Y.; Fang, Y.; Liu, J.; Ye, T.; Li, X.; Tu, H.; Ye, Y.; Wang, Y.; Xiong, L. Stress-induced nuclear translocation of ONAC023 improves drought and heat tolerance through multiple processes in rice. Nat. Commun. 2024, 15, 5877. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
93. Wu, N.; Yao, Y.; Xiang, D.; Du, H.; Geng, Z.; Yang, W.; Li, X.; Xie, T.; Dong, F.; Xiong, L. A MITE variation-associated heat-inducible isoform of a heat-shock factor confers heat tolerance through regulation of JASMONATE ZIM-DOMAIN genes in rice. New Phytol. 2022, 234, 1315–1331. [Google Scholar] [CrossRef] [PubMed]
94. Xu, Y.; Zhang, L.; Ou, S.; Wang, R.; Wang, Y.; Chu, C.; Yao, S. Natural variations of SLG1 confer high-temperature tolerance in indica rice. Nat. Commun. 2020, 11, 5441. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
95. Xu, J.; Wang, C.; Wang, F.; Liu, Y.; Li, M.; Wang, H.; Zheng, Y.; Zhao, K.; Ji, Z. PWL1, a G-type lectin receptor-like kinase, positively regulates leaf senescence and heat tolerance but negatively regulates resistance to Xanthomonas oryzae in rice. Plant Biotechnol. J. 2023, 21, 2525–2545. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
96. Liu, Y.; Liu, X.; Wang, X.; Gao, K.; Qi, W.; Ren, H.; Hu, H.; Sun, D.; Bai, J.; Zheng, S. Heterologous expression of heat stress-responsive AtPLC9 confers heat tolerance in transgenic rice. BMC Plant Biol. 2020, 20, 514. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
97. Lou, H.; Li, S.; Shi, Z.; Zou, Y.; Zhang, Y.; Huang, X.; Yang, D.; Yang, Y.; Li, Z.; Xu, C. Engineering source-sink relations by prime editing confers heat-stress resilience in tomato and rice. Cell 2025, 188, 530–549.e20. [Google Scholar] [CrossRef] [PubMed]
98. Zhan, P.; Ma, S.; Xiao, Z.; Li, F.; Wei, X.; Lin, S.; Wang, X.; Ji, Z.; Fu, Y.; Pan, J.; et al. Natural variations in grain length 10 (GL10) regulate rice grain size. J. Genet. Genom. 2022, 49, 405–413. [Google Scholar] [CrossRef] [PubMed]
99. He, W.; He, H.; Yuan, Q.; Zhang, H.; Li, X.; Wang, T.; Yang, Y.; Yang, L.; Yang, Y.; Liu, X.; et al. Widespread inversions shape the genetic and phenotypic diversity in rice. Sci. Bull. 2024, 69, 593–596. [Google Scholar] [CrossRef] [PubMed]
100. Wang, J.; Xu, J.; Wang, L.; Zhou, M.; Nian, J.; Chen, M.; Lu, X.; Liu, X.; Wang, Z.; Cen, J.; et al. SEMI-ROLLED LEAF 10 stabilizes catalase isozyme B to regulate leaf morphology and thermotolerance in rice (Oryza sativa L.). Plant Biotechnol. J. 2023, 21, 819–838. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
101. Liu, Q.; Yang, T.; Yu, T.; Zhang, S.; Mao, X.; Zhao, J.; Wang, X.; Dong, J.; Liu, B. Integrating Small RNA Sequencing with QTL Mapping for Identification of miRNAs and Their Target Genes Associated with Heat Tolerance at the Flowering Stage in Rice. Front. Plant Sci. 2017, 8, 43. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
102. Cao, Z.; Li, Y.; Tang, H.; Zeng, B.; Tang, X.; Long, Q.; Wu, X.; Cai, Y.; Yuan, L.; Wan, J. Fine mapping of the qHTB1-1QTL, which confers heat tolerance at the booting stage, using an Oryza rufipogon Griff. introgression line. Theor. Appl. Genet. 2020, 133, 1161–1175. [Google Scholar] [CrossRef] [PubMed]
103. Huang, D.; Zhang, Z.; Fan, Y.; Tang, S.; Zhuang, J.; Zhu, Y. Detection of QTL for High-Temperature Tolerance in Rice Using a High-Density Bin Map. Agronomy 2023, 13, 1582. [Google Scholar] [CrossRef]
104. Ye, C.; Argayoso, M.; Redoña, E.; Sierra, S.; Laza, M.; Dilla, C.; Mo, Y.; Thomson, M.; Chin, J.; Delaviña, C.; et al. Mapping QTL for heat tolerance at flowering stage in rice using SNP markers. Plant Breed. 2012, 131, 33–41. [Google Scholar] [CrossRef]
105. Hirabayashi, H.; Sasaki, K.; Kambe, T.; Gannaban, R.B.; Miras, M.A.; Mendioro, M.S.; Simon, E.V.; Lumanglas, P.D.; Fujita, D.; Takemoto-Kuno, Y.; et al. qEMF3, a novel QTL for the early-morning flowering trait from wild rice, Oryza officinalis, to mitigate heat stress damage at flowering in rice, O. sativa. J. Exp. Bot. 2015, 66, 1227–1236. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
106. Ye, C.; Ishimaru, T.; Lambio, L.; Li, L.; Long, Y.; He, Z.; Htun, T.M.; Tang, S.; Su, Z. Marker-assisted pyramiding of QTLs for heat tolerance and escape upgrades heat resilience in rice (Oryza sativa L.). Theor. Appl. Genet. 2022, 135, 1345–1354. [Google Scholar] [CrossRef] [PubMed]
107. Li, M.; Li, X.; Li-qin Yu Wu, J.; Li, H.; Liu, J.; Ma, X.; Jo, S.; Park, D.; Song, Y.; Shin, D.; et al. Identification of QTLs associated with heat tolerance at the heading and flowering stage in rice (Oryza sativa L.). Euphytica 2018, 214, 70. [Google Scholar] [CrossRef]
108. Nguyen, T.; Shen, S.; Cheng, M.; Chen, Q. Identification of QTLs for Heat Tolerance at the Flowering Stage Using Chromosome Segment Substitution Lines in Rice. Genes 2022, 13, 2248. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
109. Zhang, H.; Zhu, J.; Gong, Z.; Zhu, J.K. Abiotic stress responses in plants. Nat. Rev. Genet. 2022, 23, 104–119. [Google Scholar] [CrossRef] [PubMed]
110. Ren, D.; Ding, C.; Qian, Q. Molecular bases of rice grain size and quality for optimized productivity. Sci. Bull. 2023, 68, 314–350. [Google Scholar] [CrossRef] [PubMed]
111. Zhu, J.K. Abiotic Stress Signaling and Responses in Plants. Cell 2016, 167, 313–324. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
112. Mondal, K.; Kar, R.K.; Chakraborty, A.; Dey, N. Concurrent effect of drought and heat stress in rice (Oryza sativa L.): Physio-biochemical and molecular approach. 3 Biotech 2024, 14, 132. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
113. Zhu, H.; Xu, H.; Zhang, Y.; Brodský, J.; Gablech, I.; Korabečná, M.; Neuzil, P. Exploring the Frontiers of Cell Temperature Measurement and Thermogenesis. Adv. Sci. 2025, 12, e2402135. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
Liu H, Wei Y, Xia S, Xie W, Ren D, Rao Y. Improvements in Tolerance to Heat Stress in Rice via Molecular Mechanisms and Rice Varieties. Agriculture. 2025; 15(3):318. https://doi.org/10.3390/agriculture15030318
Перевод статьи «Improvements in Tolerance to Heat Stress in Rice via Molecular Mechanisms and Rice Varieties» авторов Liu H, Wei Y, Xia S, Xie W, Ren D, Rao Y., оригинал доступен по ссылке. Лицензия: CC BY. Изменения: переведено на русский язык
Фото: freepik
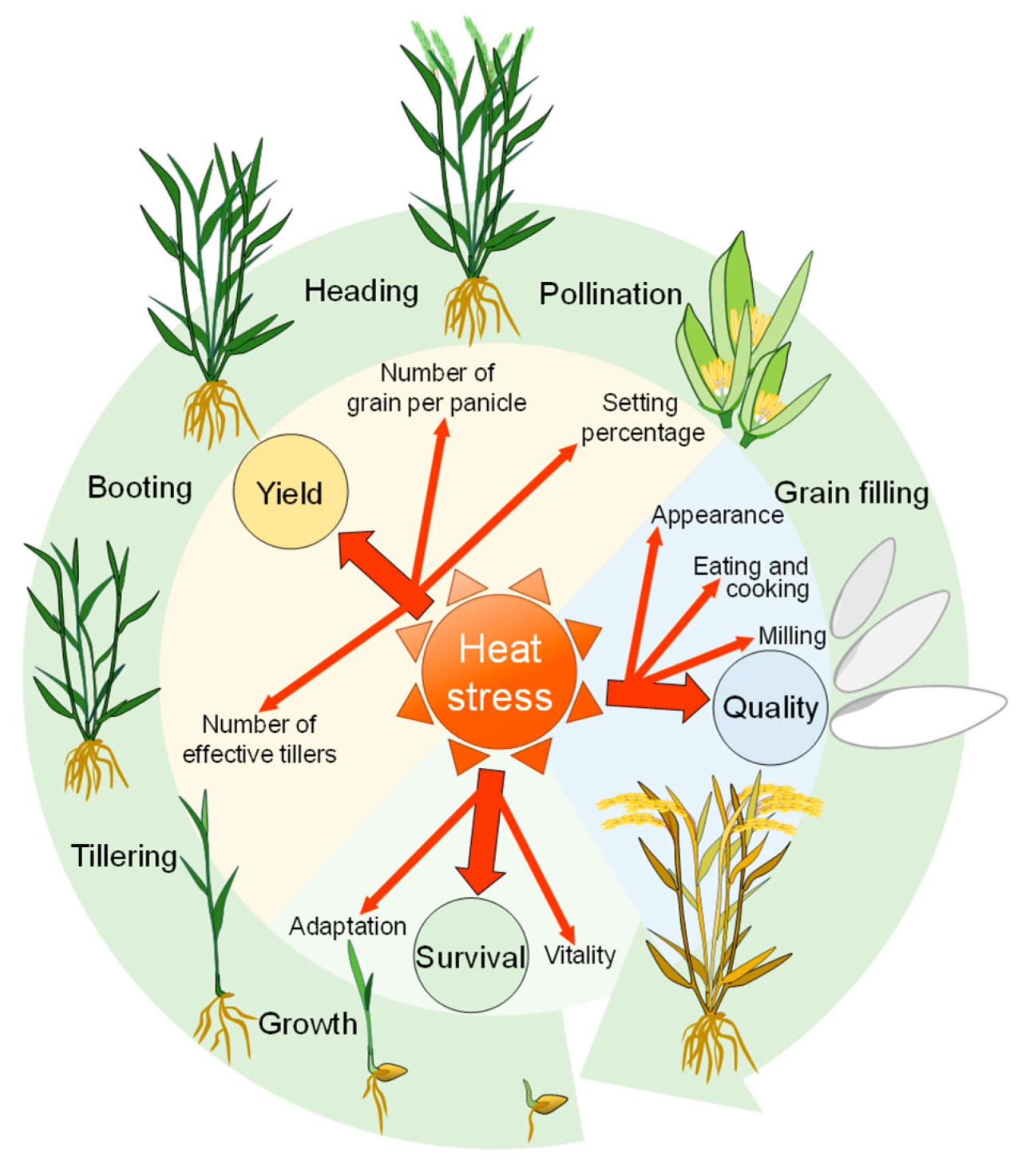
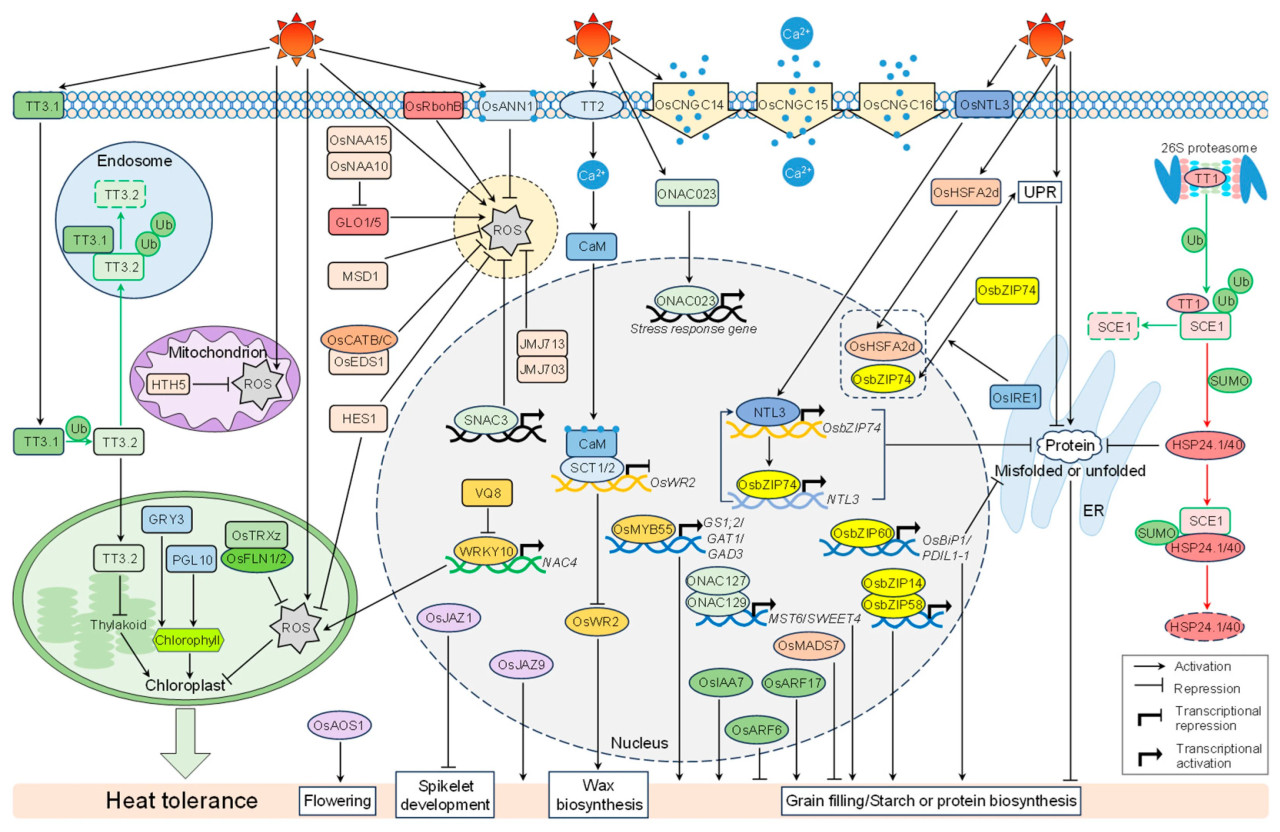
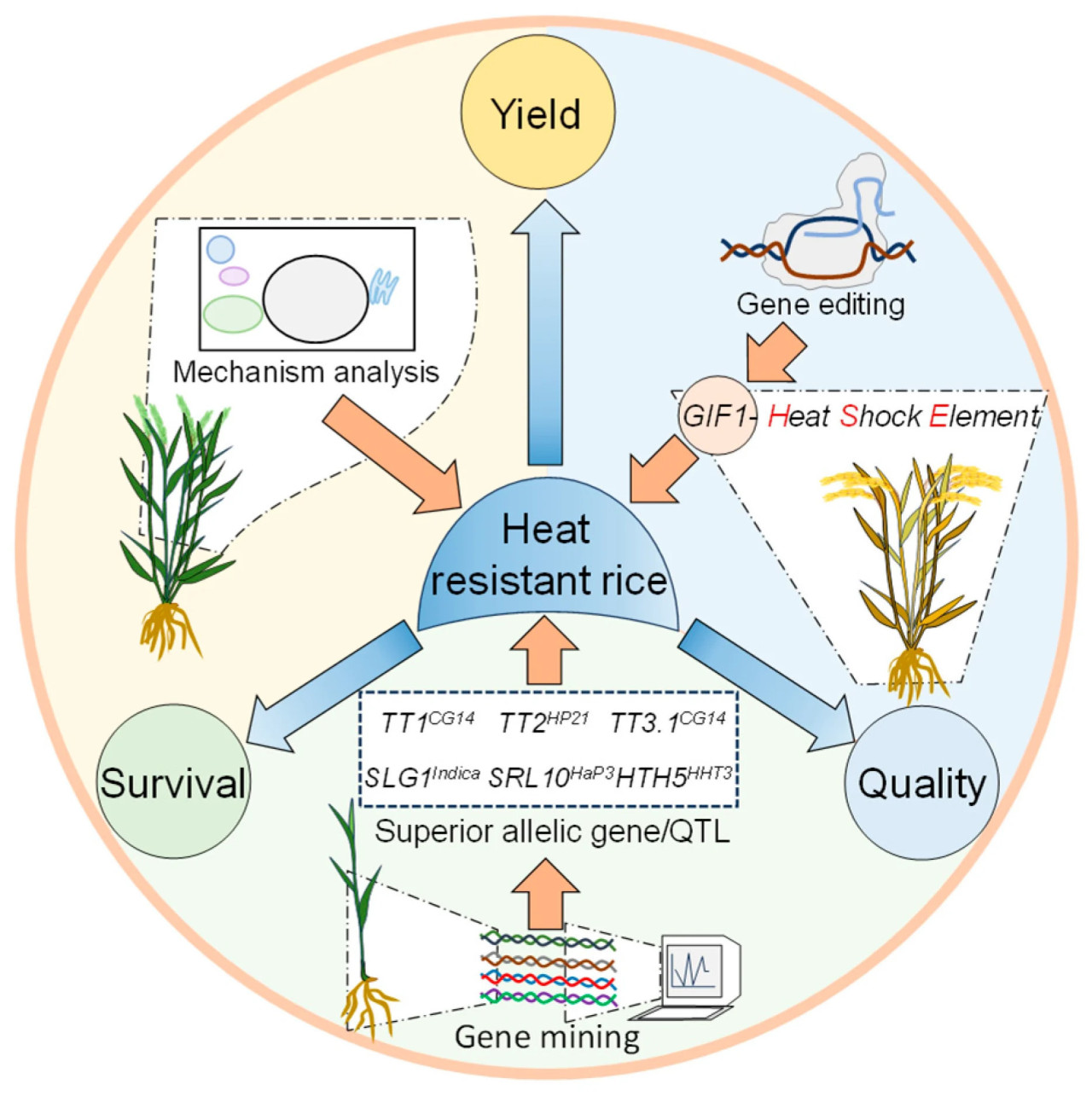
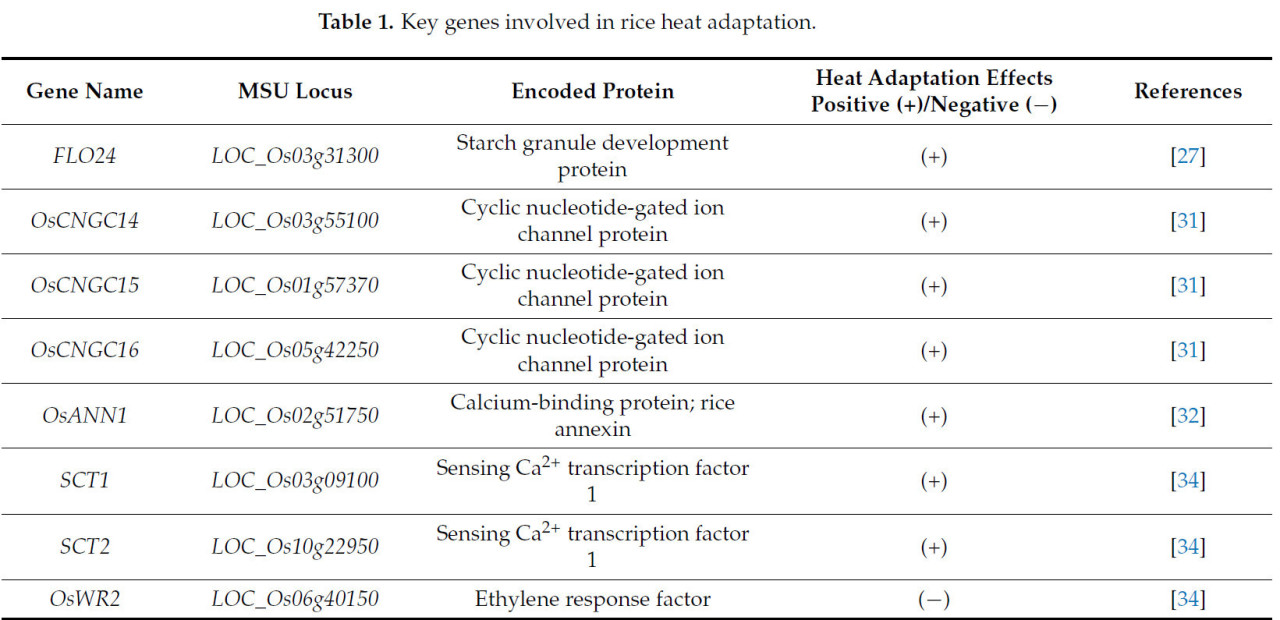
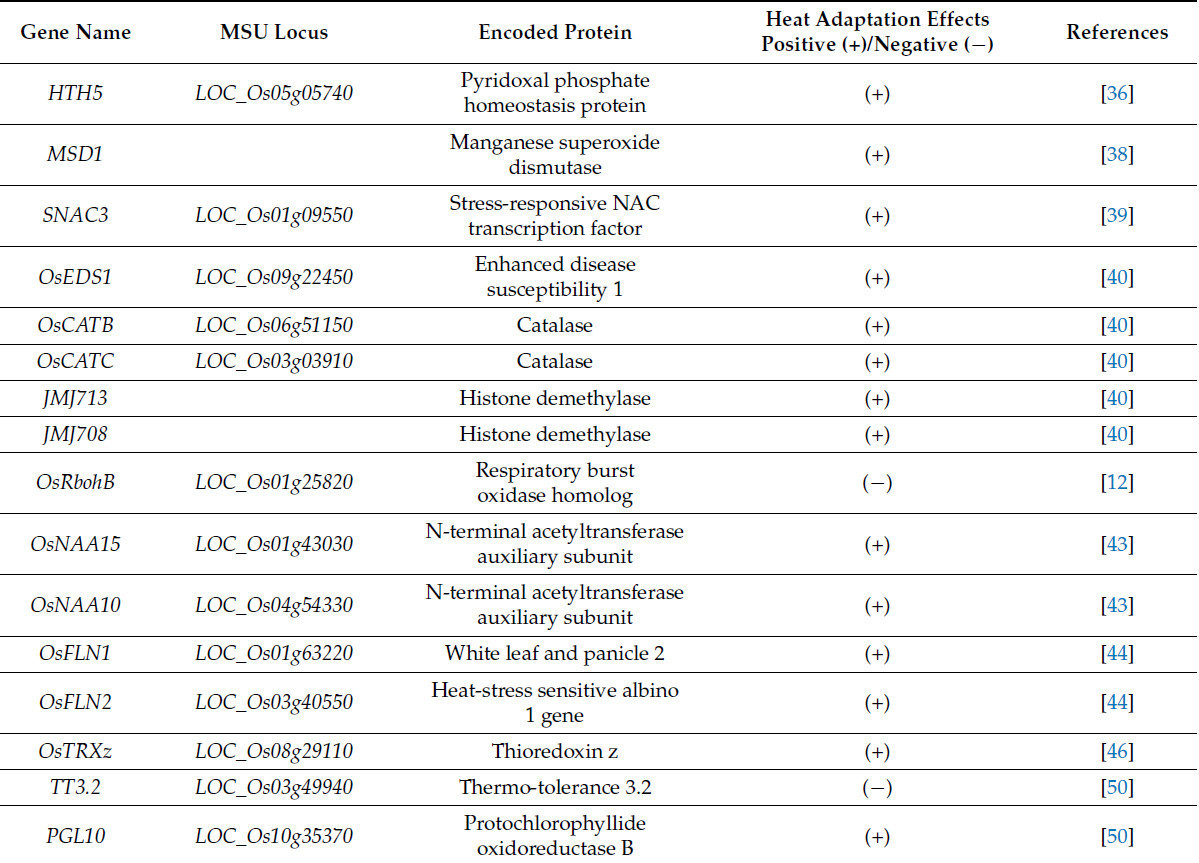

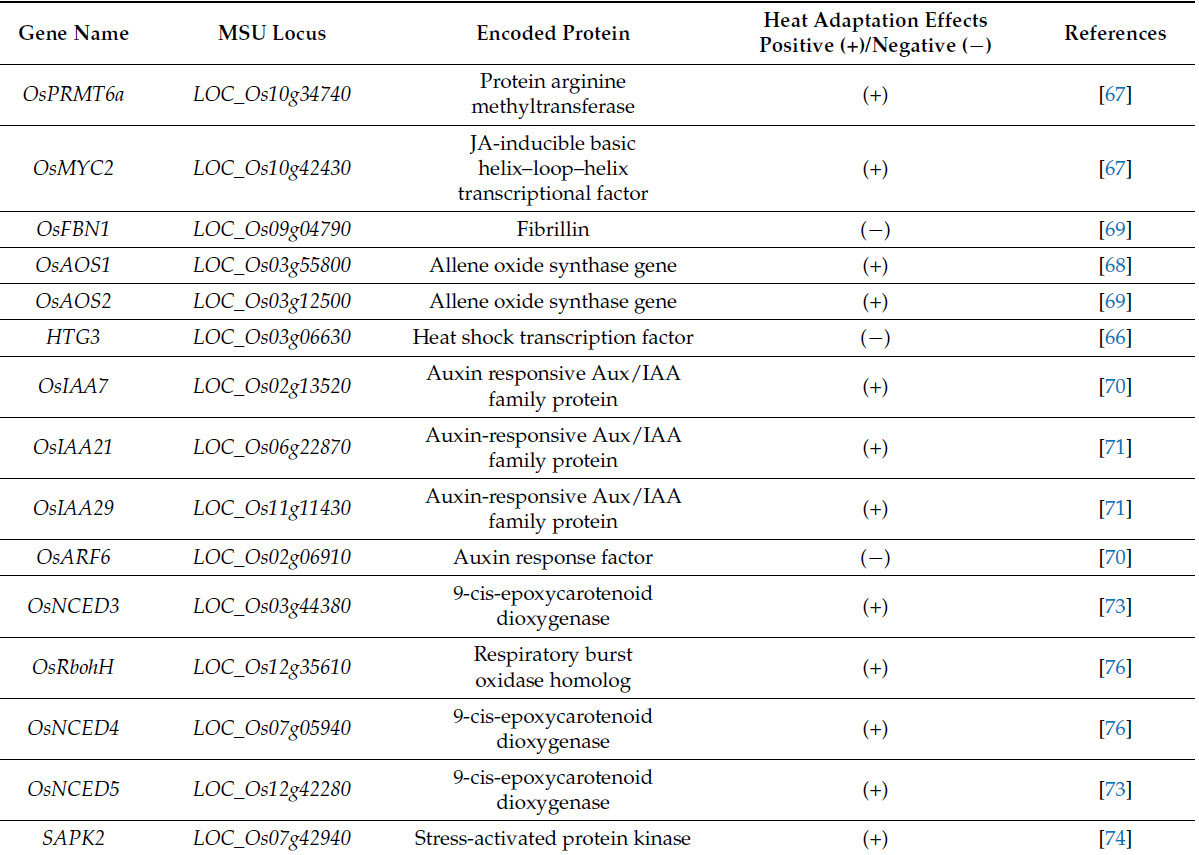
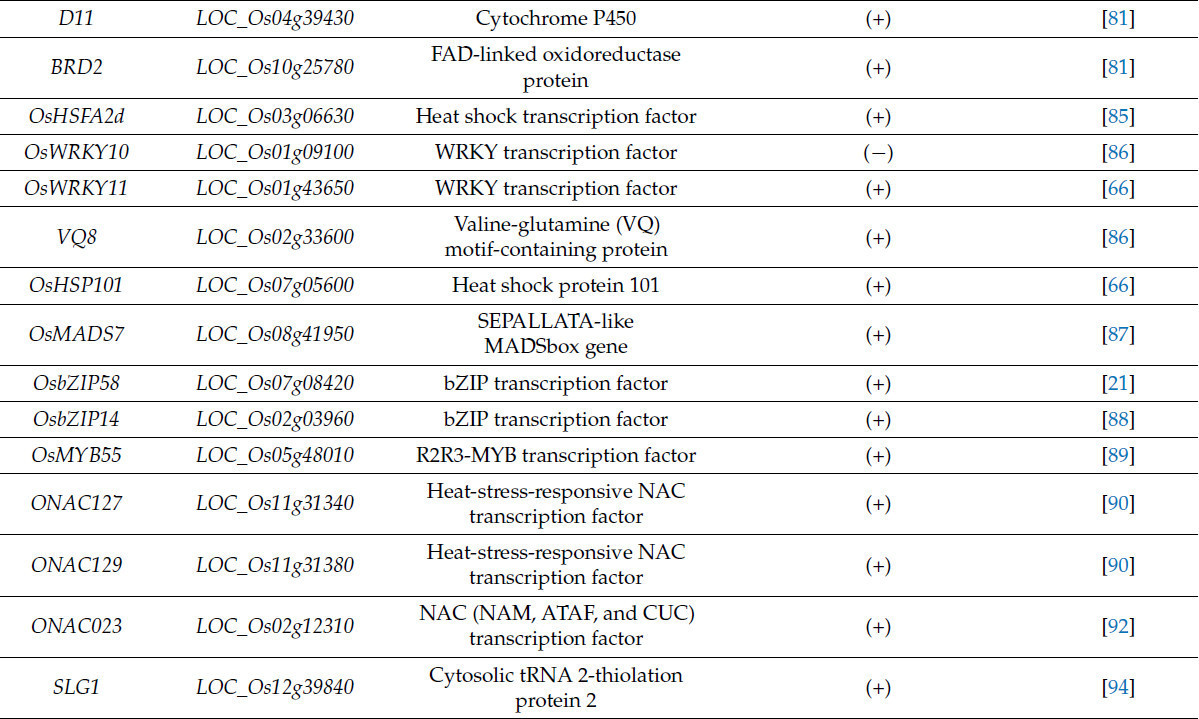
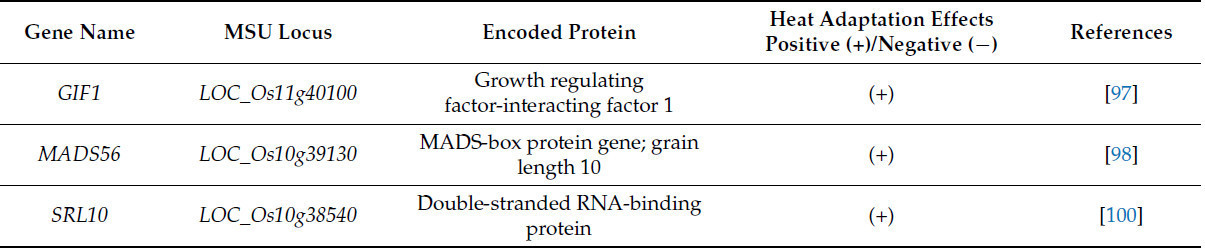















































































































Комментарии (0)