Почему в почве чайных плантаций накапливается углерод: роль азота и бактерий
Углеродно-азотная (C-N) связь является фундаментальной концепцией в экологии экосистем. Долгосрочное чрезмерное внесение удобрений в чайных плантациях привело к нарушению баланса углерода и азота в почве, что вызвало экологические проблемы. Понимание углеродно-азотной связи в условиях азотной нагрузки необходимо для устойчивого управления, однако механизмы остаются неясными. В этом исследовании изучалась углеродно-азотная связь в почвах чайных плантаций при пяти режимах внесения удобрений: без удобрений, химические удобрения, химические + органические жмыховые удобрения, химические + микробные удобрения и химические + биоуголь.
Аннотация
Внесение удобрений в основном увеличивало содержание частичного органического углерода (POC) и неорганического азота, что обусловлено изменениями в составе и функциях бактериальных сообществ. Смешанные режимы внесения удобрений усиливали связь между бактериальными сообществами и свойствами почвы, повышая экологическую сложность без изменения общих тенденций. Грибные сообщества оказывали незначительное влияние на углеродно-азотную динамику почвы. Микробный некромассовый углерод (MNC) и эффективность микробного углеродного насоса (MCP), отражающие долгосрочный потенциал накопления углерода, показали минимальную реакцию на краткосрочное внесение удобрений. Однако коэффициент накопления микробного некромассового углерода (NAC) оказался чувствительным к азоту, указывая на краткосрочные реакции. Анализ PLS-PM выявил согласованную углеродно-азотную связь во всех режимах обработки, при которой почвенный азот влиял на углерод через ферментативную активность и MCP, в то время как бактериальные сообщества напрямую влияли на накопление углерода. Эти результаты дают представление для точного управления углеродом и азотом в почве и устойчивой практики ведения чайных плантаций в условиях изменения климата.
1. Введение
Чай (Camellia sinensis L.) является одним из трех самых популярных безалкогольных напитков в мире и важной экономической культурой в развивающихся странах, таких как Китай, Индия, Шри-Ланка и Кения. Площадь его возделывания неуклонно расширяется [1]. В 2022 году мировая площадь чайных плантаций достигла приблизительно 5,32 миллиона гектаров, из которых на Китай приходилось 3,33 миллиона гектаров, что составляет 62,6% от общемирового показателя [2]. Однако долгосрочная практика внесения удобрений в чайных плантациях привела к дисбалансу углерода и азота в почве, вызывая ряд экологических проблем, таких как деградация почвы, увеличение выбросов парниковых газов и обострение проблемы диффузного загрязнения [3]. Чайные плантации также стали очагами выбросов N2O [4]. Следовательно, понимание механизмов углеродно-азотной связи в почве и оптимизация управления углеродом и азотом имеют основополагающее значение для устойчивого развития экосистем чайных плантаций.
Углеродно-азотная связь изначально понималась как азотное лимитирование, поскольку рост растений в целом увеличивается с дополнительным поступлением азота [5]. Однако долгосрочные азотные добавки (например, удобрения) повысили доступность азота, существенно повлияв на динамику и накопление углерода в почве [6]. В удобряемых экосистемах потери азота в атмосферу в течение дней или недель, главным образом за счет летучести и денитрификации, зависят от формы вносимого азота и последующих практик управления почвой. Лишь небольшая часть азота ассимилируется растениями или удерживается в почве [7]. Предыдущие исследования предполагали, что добавление азота влияет на накопление углерода в почве, воздействуя на микробный метаболизм и подземную биомассу. Поступление азота снижает продукцию ферментов, разлагающих углерод, микроорганизмами, одновременно повышая подземную продуктивность растений, тем самым способствуя накоплению углерода в почве [8]. Добавление азота изменяет структуру микробного сообщества и метаболическую активность, способствуя пролиферации азот-ассоциированных функциональных микроорганизмов (например, нитрификаторов и денитрификаторов) и увеличивая активность азот-ассоциированных ферментов (например, NAG, LAP) [9]. Эти изменения ускоряют разложение органического вещества почвы. Одновременно увеличивается доступность аммония и нитрата для корней растений, что усиливает опосредованное растениями поступление углерода в почву [10]. В последние годы роли микробного некромассового углерода в накоплении и трансформации углерода в почве уделяется все больше внимания. Добавление азота не только влияет на транзиторные реакции микробных сообществ, но и прямо или косвенно влияет на вклад микроорганизмов в накопление и трансформацию углерода в почве [11]. Микробный рост и метаболизм играют ключевую роль в регуляции формирования и накопления пулов почвенного углерода. После отмирания микроорганизмов их некромасса и метаболические побочные продукты остаются относительно стабильными в почве, внося вклад в пул почвенного углерода в виде микробных остатков. Непрерывное образование микробных остатков, обусловленное итеративным ростом и отмиранием микробных сообществ, определяется как микробный углеродный насос (MCP) [12]. Отношение микробного некромассового углерода к почвенному органическому углероду представляет собой эффективность MCP. Добавление азота усиливает микробную активность и скорость обмена веществ, ускоряя образование микробного некромассового углерода и изменяя эффективность MCP [13]. Микробный некромассовый углерод, как компонент устойчивого органического углерода, необходим для регуляции стабильности пула почвенного углерода через скорость его накопления и эффективность MCP [14].
Почвенные ферменты играют критическую роль в разложении органического вещества, причем их высокая активность высвобождает значительные количества биодоступного органического азота и углерода, тем самым влияя на метаболические паттерны бактериальных сообществ [15]. В условиях высокого содержания азота растения снижают прямой поступление углерода в почву, что приводит к уменьшению соотношения углерода к азоту (C/N) в почве. Изменения активности почвенных ферментов впоследствии регулируют растворимый C/N, что способствует пролиферации специфических бактериальных сообществ, одновременно подавляя микроорганизмы, зависящие от высоко-углеродных источников [16]. Хотя растения снижают поступление углерода в ризосферу в условиях высокого содержания азота, это не отрицает их влияния на углеродно-азотную связь в почве. Вместо этого растения могут косвенно формировать функции микробных сообществ, регулируя активность почвенных ферментов [17]. Регуляторные соединения, секретируемые корнями растений, такие как органические кислоты, аминокислоты и фенольные соединения, могут значительно изменять активность почвенных ферментов, тем самым влияя на микробные стратегии использования углерода и азота [18]. Это отражает адаптивную стратегию растений в средах с высоким содержанием азота, при которой растения снижают поступление углерода в корни, чтобы минимизировать конкуренцию с микроорганизмами и избежать ненужных потерь углерода, поддерживая при этом стабильное C/N [19]. Следовательно, зависимость микроорганизмов от источников углерода смещается от прямого поступления от растений к продуктам разложения, высвобождаемым активностью почвенных ферментов [20,21]. Таким образом, понимание того, как почвенные ферменты регулируют микробные сообщества и эффективность MCP после внесения удобрений, является ключом к выяснению углеродно-азотной связи.
Из-за высокой экономической ценности чая нормы внесения азота в чайных плантациях значительно выше, чем в других управляемых экосистемах [22]. Чайные растения, как листовая товарная культура, требуют значительных поступлений азота, причем нормы внесения варьируются от 100 до 1200 кг N га⁻¹ год⁻¹ [23,24]. В общем, нормы внесения азота от 100 до 300 кг N га⁻¹ год⁻¹ показывают положительную корреляцию как с урожайностью, так и с качеством чая [25]. Чрезмерное внесение химических удобрений не обеспечивает эффективно урожайность и качество чая, а вместо этого усугубляет подкисление почвы и дисбаланс питательных веществ [26]. Чтобы повысить эффективность использования азота и снизить экологические риски, многочисленные исследования изучили смешанные практики внесения удобрений, сочетающие химические удобрения с органическими удобрениями, микробными инокулянтами или биоуглем [27]. Было также показано, что такие практики увеличивают запасы углерода в почве чайных плантаций [28]. Хотя более высокий уровень SOC может повысить урожайность чая при низких или умеренных нормах внесения азота, чрезмерное поступление азота в сочетании с высоким уровнем SOC может снизить эффективность удобрений в повышении урожайности [29]. Добавление азота нарушает стехиометрический баланс почвы, изменяя распределение микробных ресурсов и структуру сообщества, что влияет на эффективность MCP через взаимодействия между доступностью азота и динамикой углерода в почве [30]. Следовательно, выяснение процессов углеродно-азотной связи в почве при внесении удобрений необходимо для оптимизации взаимосвязи между азотом и урожайностью в чайных плантациях и содействия долгосрочной секвестрации углерода.
В этом исследовании мы исследовали процессы углеродно-азотной связи в почвах чайных плантаций в условиях высокого содержания азота на начальном этапе внесения удобрений. Были исследованы пять распространенных режимов внесения удобрений: без удобрений (CK), химическое удобрение (FF), комбинированное применение химического и органического жмыхового удобрения (FO), комбинированное применение химического и микробного удобрения (FM) и комбинированное применение химического удобрения и биоугля (FB). Мы выдвинули следующие гипотезы: (i) внесение удобрений увеличивает микробный некромассовый углерод, тем самым способствуя накоплению углерода в почве; (ii) внесение удобрений изменяет стратегии микробов по приобретению ресурсов; (iii) различные режимы внесения удобрений оказывают минимальное краткосрочное воздействие на эффективность MCP, при этом почвенные ферменты играют доминирующую роль в регуляции углеродно-азотной связи в почве в этот период.
2. Материалы и методы
2.1. Описание места проведения и дизайн эксперимента
Исследование было проведено на экспериментальной чайной плантации Чанчун в Хэфэй, провинция Аньхой, Китай (117°8′52″ в.д., 31°18′53″ с.ш.). Территория характеризуется субтропическим муссонным климатом с четко выраженными сезонами. Среднегодовая температура составляет 15,8 °C, а среднегодовое количество осадков — 1188 мм, причем большая часть осадков выпадает с мая по июль. В течение экспериментального периода среднесуточная температура составила 22,27 ± 2,42 °C, средняя влажность — 78,01 ± 5,18%, а общее количество осадков достигло 97 мм. Тип почвы классифицируется как желто-бурая почва.
Это исследование было проведено на единообразно управляемой чайной плантации с возрастом чайных растений шесть лет. Были применены пять режимов внесения удобрений: без удобрений (CK), химическое удобрение (FF), комбинированное применение химического и органического жмыхового удобрения (FO), комбинированное применение химического и микробного удобрения (FM) и комбинированное применение химического удобрения и биоугля (FB). Был принят рендомизированный блочный дизайн с 20 участками (5 × 5 м) и четырьмя повторностями на обработку. Химическое удобрение содержало азот (N), фосфор (P) и калий (K) в соотношении 22:8:15. Органическое жмыховое удобрение состояло из 60,40% органического вещества, 7,02% N, 3,01% P и 1,60% K. Микробное удобрение (Пекин Runze Xinye Bioengineering Technology Co., Ltd., Пекин, Китай) содержало 40% органического вещества, 5% общих питательных веществ и 2 миллиарда жизнеспособных микробов на грамм почвы. Биоуголь состоял из 42,21% органического углерода, 8,34% N, 2,31% P и 16,12% K. Органическое жмыховое удобрение было получено в основном из рапсового жмыха, микробное удобрение содержало штаммы Bacillus, а биоуголь был произведен с использованием стеблей кукурузы в качестве основного сырья. Нормы внесения удобрений следовали местной практике: химическое удобрение — 300 кг N га⁻¹ год⁻¹, органическое удобрение — 12 т га⁻¹ год⁻¹, микробное удобрение — 1,8 т га⁻¹ год⁻¹ и биоуголь — 10 т га⁻¹ год⁻¹. Обработки удобрениями были применены в мае 2023 года. Траншеи глубиной приблизительно 15 см были выкопаны на расстоянии около 10 см от корней чайных растений, и удобрения были равномерно распределены в траншеях перед засыпкой их землей.
2.2. Отбор почвенных образцов и анализ
Образцы верхнего слоя почвы (0–20 см) были отобраны как до внесения удобрений, так и через 30 дней после обработки. Пять почвенных кернов были случайным образом взяты с каждого участка и объединены в один составной образец. Составные образцы были просеяны через сито с ячейкой 2 мм и разделены на три части для последующего анализа. Одна часть хранилась при 4 °C и была проанализирована на активность почвенных ферментов в течение одной недели. Другая часть хранилась при комнатной температуре для измерений физико-химических свойств почвы. Оставшаяся часть хранилась при температуре -80 °C для экстракции ДНК с целью анализа микробного разнообразия. Используя полный набор данных, мы проанализировали процессы углеродно-азотной связи в почвах чайных плантаций в условиях высокого содержания азота на ранних стадиях внесения удобрений.
Содержание общего углерода (TC) и общего органического углерода (TOC) измеряли с помощью анализатора общего органического углерода (Shimadzu, TOC-LCPH, Киото, Япония). Содержание общего азота (TN) определяли с помощью элементного анализатора (Elementar, vario MACRO cube, Лангензельбольд, Германия). Растворенный органический углерод (DOC) был количественно определен с использованием автоматического анализатора органического углерода (Elementar, vario TOC cube, Лангензельбольд, Германия). Содержание частичного органического углерода (POC) и минерал-ассоциированного органического углерода (MAOC) измеряли с помощью метода нагревания с бихроматом калия [31]. Аммонийный азот (NH₄⁺-N) анализировали с использованием индофенольного колориметрического метода, нитратный азот (NO₃⁻-N) — с помощью УФ-спектрофотометрии, а нитритный азот (NO₂⁻-N) — с помощью диазотирования–азосочетания колориметрического метода. Эти формы азота были количественно определены с помощью УФ-видимого спектрофотометра (UV-1800PC, Shanghai Meipuda Instruments Co., Ltd., Шанхай, Китай). Микробный биомассовый углерод (MBC) и азот (MBN) в почве определяли методом хлороформной фумигации–экстракции [32]. pH почвы измеряли с помощью pH-метра после смешивания почвы и деионизированной воды в соотношении 1:2,5 (масса/объем). Кроме того, содержание неорганического углерода (IC) и органического азота (ON) в почве рассчитывали с помощью следующих формул:
2.3. Активность почвенных ферментов
Активность β-1,4-глюкозидазы (BG), β-1,4-N-ацетилглюкозаминидазы (NAG) и лейцинаминопептидазы (LAP) измеряли с использованием флуоресцентного метода [33]. Приблизительно 1 г свежей почвы смешивали с 50 мл 50 мМ ацетатного буфера (pH 5,0) и обрабатывали на вортексе в течение 30 с для приготовления почвенной суспензии. Затем 200 мкл почвенной суспензии и 50 мкл раствора субстрата распределяли в черные микропланшеты. NAG инкубировали в течение 2 часов, тогда как BG и LAP инкубировали в течение 4 часов. Интенсивность флуоресценции измеряли при длине волны возбуждения 360 нм и длине волны эмиссии 460 нм.
2.4. Анализ микробного разнообразия
ДНК экстрагировали из 0,5 г почвы на образец с использованием набора E.Z.N.A.® Soil DNA Kit (Omega Bio-tek, Norcross, Джорджия, США) в соответствии с инструкциями производителя для получения тотальной геномной ДНК из микробных сообществ. Качество экстрагированной ДНК оценивали с помощью электрофореза в 1% агарозном геле, а концентрацию и чистоту ДНК определяли с использованием спектрофотометра NanoDrop2000 (Thermo Scientific, Уолтем, Массачусетс, США). Экстрагированная ДНК была использована в качестве матрицы для ПЦР-амплификации вариабельной области V3-V4 гена 16S рРНК с использованием прямого праймера 338F (5′-ACTCCTACGGGAGGCAGCAG-3′) и обратного праймера 806R (5′-GGACTACHVGGGTWTCTAAT-3′). Для анализа грибного сообщества область ITS2 амплифицировали с использованием прямого праймера ITS3F (5′-GCATCGATGAAGAACGCAGC-3′) и обратного праймера ITS4R (5′-TCCTCCGCTTATTGATATGC-3′). Условия ПЦР для гена 16S рРНК были следующими: начальная денатурация при 95 °C в течение 3 мин, затем 27 циклов денатурации при 95 °C в течение 30 с, отжига при 55 °C в течение 30 с и элонгации при 72 °C в течение 30 с, с финальной элонгацией при 72 °C в течение 10 мин. Для амплификации области ITS применялись те же температурные условия, за исключением 35 циклов вместо 27. Продукты ПЦР затем хранили при 4 °C (ПЦР-амплификатор: ABI GeneAmp® 9700, Фостер-Сити, Калифорния, США). Секвенирование было выполнено на платформе Illumina Nextseq2000 компанией Shanghai Majorbio Bio-Pharm Technology Co., Ltd. (Шанхай, Китай).
Проконтролированные по качеству и объединенные последовательности были деноизированы с использованием плагина DADA2 в конвейере Qiime2, генерируя варианты ампликонной последовательности (ASV). Последовательности, аннотированные как хлоропласты и митохондрии, были удалены из всех образцов. Затем глубина секвенирования была разрежена до 20 000 последовательностей на образец для обеспечения единообразия. Таксономическая классификация ASV была выполнена с использованием классификатора Наивного Байеса, реализованного в Qiime2. База данных генов 16S рРНК Silva (v138) была использована для классификации бактериальных сообществ, а база данных UNITE 9.0 — для классификации грибных сообществ.
2.5. Расчеты эффективности MCP
Почвенные аминосахара измеряли с использованием газовой хроматографии–масс-спектрометрии (ГХ-МС). Приблизительно 0,5–1,0 г почвы помещали в гидролизные пробирки, затем добавляли 5 мл 6 моль л⁻¹ HCl вдоль стенки пробирки. Воздух в гидролизной пробирке вытесняли азотом в течение 2 мин перед герметизацией пробирки. Образцы гидролизовали при 105 °C в течение 8 ч в печи. После охлаждения до комнатной температуры к гидролизату добавляли 250 мкг инозита, затем следовали центрифугирование и выпаривание досуха. Остаток растворяли в 20 мл чистой воды и доводили pH до 6,6–6,8. После центрифугирования остаток растворяли в 10 мл безводного метанола. После дальнейшего центрифугирования и продувки азотом супернатант выпаривали досуха, добавляли 100 мкг арабита и 1 мл воды и лиофилизировали. Дериватизированные образцы анализировали на содержание аминосахаров с использованием газового хроматографа (GC TRACE 1300, Thermo Fisher, Уолтем, Массачусетс, США). Бактериальный некромассовый углерод (BNC) и грибной некромассовый углерод (FNC) рассчитывали на основе содержания аминосахаров с использованием следующих формул [34]:
Общий микробный некромассовый углерод (MNC) рассчитывали как сумму BNC и FNC. Эффективность MCP рассчитывали как отношение MNC к TOC [35]. Аналогично, эффективность бактериального углеродного насоса (BCP) рассчитывали как отношение BNC к TOC, а эффективность грибного углеродного насоса (FCP) — как отношение FNC к TOC. Общий коэффициент накопления микробного некромассового углерода (T-NAC) рассчитывали как отношение MNC к MBC [36]. Коэффициент накопления бактериального некромассового углерода (B-NAC) определяли как отношение BNC к MBC, а коэффициент накопления грибного некромассового углерода (F-NAC) — как отношение FNC к MBC.
2.6. Статистический анализ
Эффекты обработок удобрениями были количественно оценены с использованием индекса ответа (R), который рассчитывается как R = ln (T/C), где T представляет значение в условиях обработки, а C представляет значение в контрольных условиях. Вычисления данных были выполнены с использованием Excel 2021, а визуализации были созданы с использованием R 4.3.3. Положительное значение R указывает на положительный эффект обработки, тогда как отрицательное значение R указывает на отрицательный эффект обработки [37].
Следующие анализы и визуализации были проведены с использованием R 4.3.3 и Gephi 0.10.1. Сходство структуры микробного сообщества между образцами оценивали с использованием анализа главных координат (PCoA) на основе алгоритма расстояния Брея–Кертиса. Чтобы оценить, значительно ли различались структуры микробных сообществ между группами образцов, был проведен анализ сходства (ANOSIM). Сеть корреляций была построена с использованием 100 наиболее обильных микробных таксонов на основе коэффициентов корреляции Спирмена между видами и средой (|r| > 0,6, p < 0,05). Тепловая карта, иллюстрирующая корреляции между микробными таксонами и факторами окружающей среды, была создана с использованием коэффициентов корреляции Спирмена, с иерархической кластеризацией, выполненной с использованием алгоритма евклидова расстояния и полной связи. Групповые различия в MNC, T-NAC и эффективности MCP были проанализированы с использованием множественного теста сравнения Фишера LSD. Тепловая карта корреляций факторов окружающей среды была построена с использованием коэффициентов корреляции Пирсона для визуализации взаимосвязей между этими факторами. Взаимосвязи между MNC, T-NAC, эффективностью MCP и каждым фактором окружающей среды были проанализированы с использованием теста Мантеля. Взаимосвязи между обработками удобрениями, физико-химическими свойствами почвы и микробными сообществами были дополнительно исследованы с использованием модели частичного наименьших квадратов на пути (PLS-PM).
3. Результаты
3.1. Реакция физико-химических свойств почвы на внесение удобрений
Все обработки удобрениями значительно повлияли на накопление компонентов углерода и азота в почве, хотя механизмы и масштабы их воздействия различались в зависимости от обработки. Все обработки положительно повлияли на POC, неорганические формы азота (NH₄⁺-N, NO₃⁻-N и NO₂⁻-N) и активность NAG. Среди обработок FM оказал наиболее комплексное положительное влияние на компоненты углерода и азота, хотя он не показал самого высокого воздействия для каждого отдельного показателя. FO продемонстрировал самый сильный эффект на POC с размером эффекта 0,86. Однако FO оказал самое слабое воздействие на NO₃⁻-N (размер эффекта 1,48), в то время как другие обработки превысили 2,50. Для NO₂⁻-N FB оказал самое слабое воздействие с размером эффекта 1,09, тогда как FF имел более высокий размер эффекта 2,41, а другие обработки превысили 3,40. Для NH₄⁺-N все обработки продемонстрировали сходную силу с размерами эффекта более 3,50. Обработки FM и FO оказали более сильное воздействие на активность NAG по сравнению с FF и FB. MBC показал тенденцию к снижению, тогда как MBN увеличился во всех обработках. pH почвы продемонстрировал минимальные вариации в зависимости от обработки (Рисунок 1).
Рисунок 1. Размер эффекта различных обработок удобрениями на физико-химические свойства почвы. Размеры эффекта представлены как среднее ± стандартная ошибка. Статистическая значимость была определена с использованием критерия Вальда типа II, причем значительные различия обозначены звездочками: 0,01 < p < 0,05, 0,001 < p < 0,01, p < 0,001. CK: без удобрений, FF: химическое удобрение, FO: комбинированное применение химического и органического жмыхового удобрения, FM: комбинированное применение химического и микробного удобрения, FB: комбинированное применение химического удобрения и биоугля. TC: общий углерод, TOC: общий органический углерод, IC: неорганический углерод, POC: частичный органический углерод, MAOC: минерал-ассоциированный органический углерод, DOC: растворенный органический углерод, TN: общий азот, ON: органический азот, NH₄⁺-N: аммонийный азот, NO₃⁻-N: нитратный азот, NO₂⁻-N: нитритный азот, BG: β-1,4-глюкозидаза, NAG: β-1,4-N-ацетилглюкозаминидаза, LAP: лейцинаминопептидаза, MBC: микробный биомассовый углерод, MBN: микробный биомассовый азот.
3.2. Реакция микробных сообществ на внесение удобрений
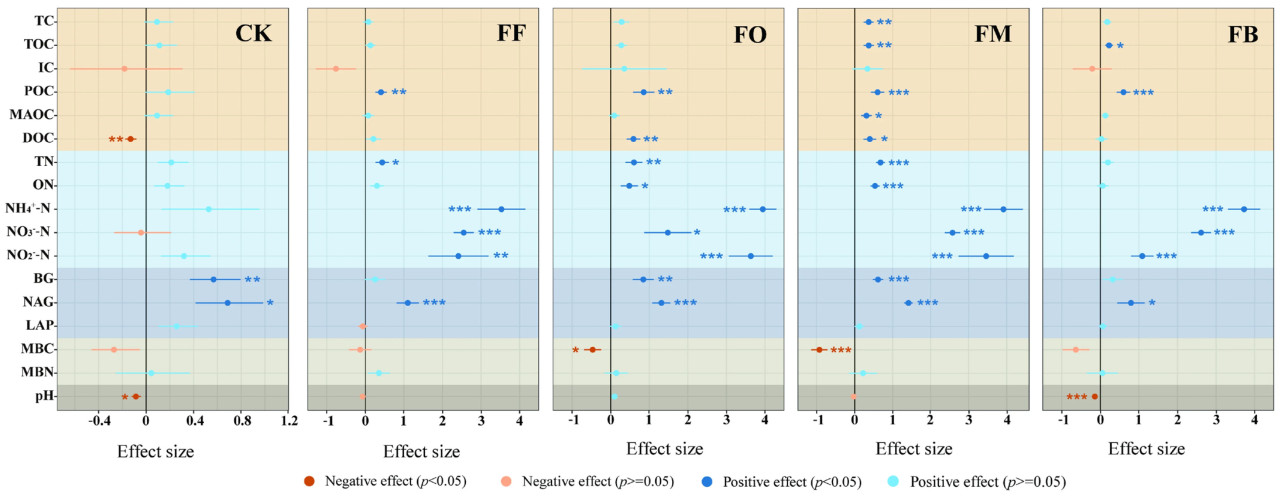
После внесения удобрений не наблюдалось значительных различий в составе бактериальных сообществ на уровне типа в зависимости от обработки (Рисунок 2a). Однако структура сообщества значительно различалась между обработками (Рисунок 2c). Доминирующими бактериальными типами, идентифицированными в этом исследовании, были Acidobacteriota, Proteobacteria, Chloroflexi, Actinobacteriota и Firmicutes. После внесения удобрений самый обильный бактериальный тип сместился с Proteobacteria на Acidobacteriota. В частности, FO увеличил относительное обилие Acidobacteriota, Firmicutes и Methylomirabilota, одновременно снижая относительное обилие Chloroflexi и Actinobacteriota. Бактериальный состав при других обработках удобрениями показал меньшие различия.
Рисунок 2. Состав бактериального сообщества до и после различных обработок удобрениями (a). Состав грибного сообщества до и после различных обработок удобрениями (d). Состав сообщества основан на классификации на уровне типа, включая типы с относительным обилием > 0,01; типы с относительным обилием < 0,01 сгруппированы как "другие". PCoA анализ состава бактериального сообщества до и после различных обработок удобрениями (b, c). PCoA анализ состава грибного сообщества до и после различных обработок удобрениями (e, f). R был рассчитан с использованием ANOSIM, а P был определен с использованием перестановочных тестов с 999 перестановками. CK: без удобрений, FF: химическое удобрение, FO: комбинированное применение химического и органического жмыхового удобрения, FM: комбинированное применение химического и микробного удобрения, FB: комбинированное применение химического удобрения и биоугля.
Обработки удобрениями не привели к значительным различиям в составе грибного сообщества на уровне типа (Рисунок 2d), а также не было значительных изменений в структуре сообщества (Рисунок 2f). Доминирующими грибными таксонами, идентифицированными в этом исследовании, были Ascomycota, неклассифицированные и Basidiomycota. При обработке FF относительное обилие Ascomycota увеличилось, в то время как относительное обилие неклассифицированных грибов уменьшилось. Аналогично, FB увеличил относительное обилие Ascomycota, но снизил относительное обилие Basidiomycota. Другие обработки показали минимальные различия в грибном составе.
В целом, бактериальные сообщества продемонстрировали более выраженные реакции на обработки удобрениями, со значительными изменениями в составе и структуре. Напротив, грибные сообщества не показали значительных изменений в ответ на обработки удобрениями.
3.3. Взаимосвязь между микробным сообществом и физико-химическими свойствами почвы
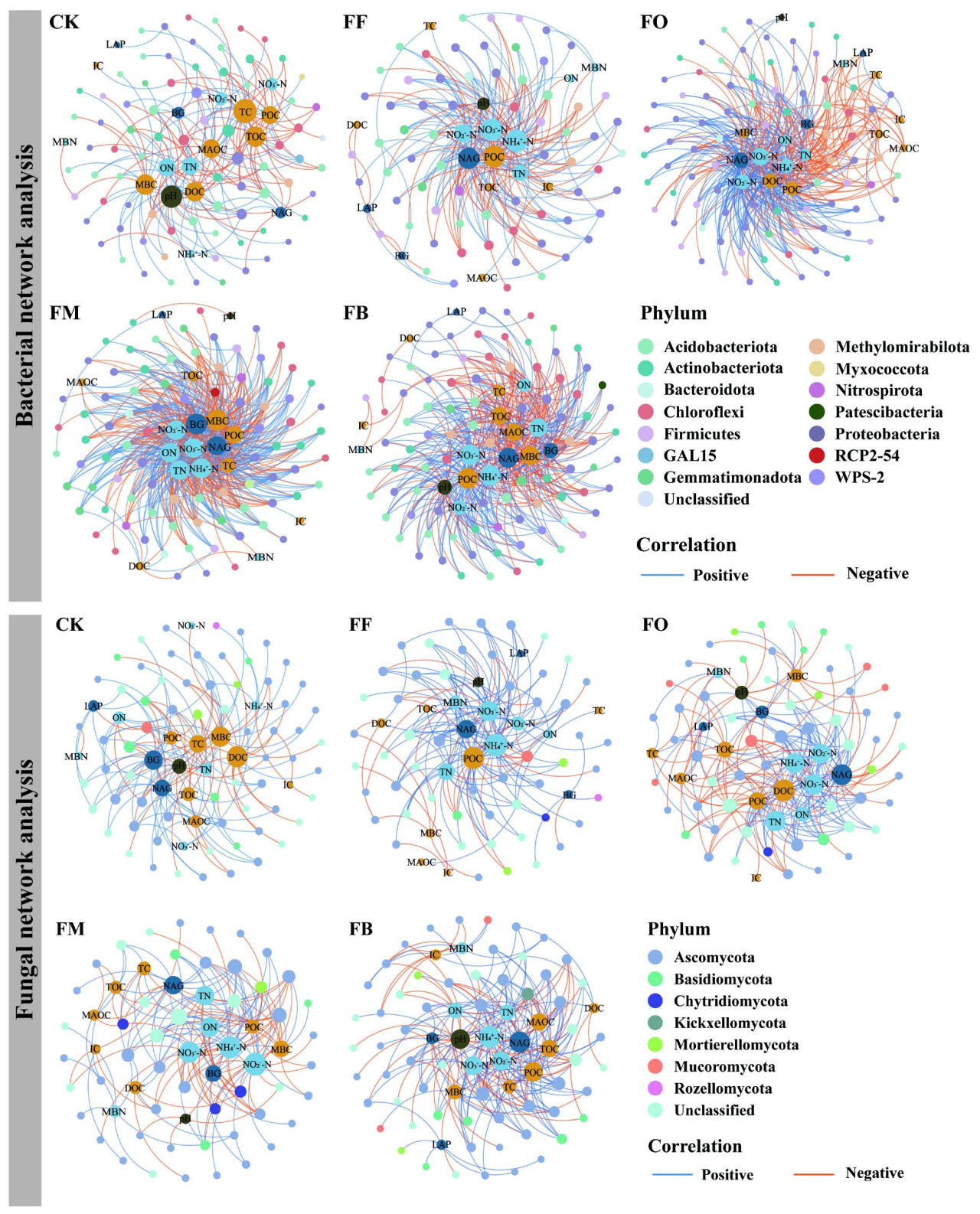
В бактериальной сети, связывающей сообщества с физико-химическими свойствами почвы, средние значения степени для CK, FF, FO, FM и FB составили 3,92, 5,59, 8,29, 10,99 и 8,97 соответственно. По сравнению с CK и FF, обработки смешанными удобрениями (FO, FM, FB) усилили связность между бактериальными сообществами и физико-химическими свойствами почвы, указывая на более сложные экологические взаимодействия (Рисунок 3). FM продемонстрировал самую высокую среднюю степень, отражая самую сильную общую реакцию бактериального сообщества на физико-химические свойства почвы. За ним следовали FB и FO, причем FB и FO показали ассоциации с более широким кругом свойств почвы, что предполагает более разнообразные бактериальные функции. Напротив, обработки FF и FM продемонстрировали меньшее, но более сфокусированное количество ассоциаций со свойствами почвы (Рисунок 3). Во всех обработках бактериальные сообщества были в основном ассоциированы с TN, NH₄⁺-N, NO₃⁻-N, NO₂⁻-N, POC и NAG. В грибной сети средние значения степени для CK, FF, FO, FM и FB составили 3,34, 4,17, 5,49, 5,09 и 5,45 соответственно. По сравнению с бактериальными сообществами, грибные сообщества продемонстрировали более слабые общие реакции на физико-химические свойства почвы (Рисунок 3). Смешанное внесение удобрений увеличило связность грибов со свойствами почвы по сравнению с CK и FF, но различия между обработками были меньше, чем те, которые наблюдались для бактериальных сообществ. Основываясь на размере и кластеризации узлов свойств почвы, FB усилил функциональное разнообразие грибов и увеличил количество ассоциаций со свойствами почвы, за ним следовал FO. Напротив, FF и FM вызвали меньшие изменения во взаимосвязях грибов со свойствами почвы. В целом, грибные сообщества реагировали на обработки удобрениями слабее по сравнению с бактериальными сообществами, при этом смешанное внесение удобрений способствовало несколько более высокой связности и функциональному разнообразию.
Рисунок 3. Сетевой анализ микробных сообществ и физико-химических свойств почвы при различных обработках удобрениями. Размер узла соответствует количеству ребер, связанных с этим узлом, представляя степень связности. В сети отображены только микроорганизмы со значительными корреляциями Спирмена (|r| > 0,6, p < 0,05) со свойствами почвы. CK: без удобрений, FF: химическое удобрение, FO: комбинированное применение химического и органического жмыхового удобрения, FM: комбинированное применение химического и микробного удобрения, FB: комбинированное применение химического удобрения и биоугля. TC: общий углерод, TOC: общий органический углерод, IC: неорганический углерод, POC: частичный органический углерод, MAOC: минерал-ассоциированный органический углерод, DOC: растворенный органический углерод, TN: общий азот, ON: органический азот, NH₄⁺-N: аммонийный азот, NO₃⁻-N: нитратный азот, NO₂⁻-N: нитритный азот, BG: β-1,4-глюкозидаза, NAG: β-1,4-N-ацетилглюкозаминидаза, LAP: лейцинаминопептидаза, MBC: микробный биомассовый углерод, MBN: микробный биомассовый азот.
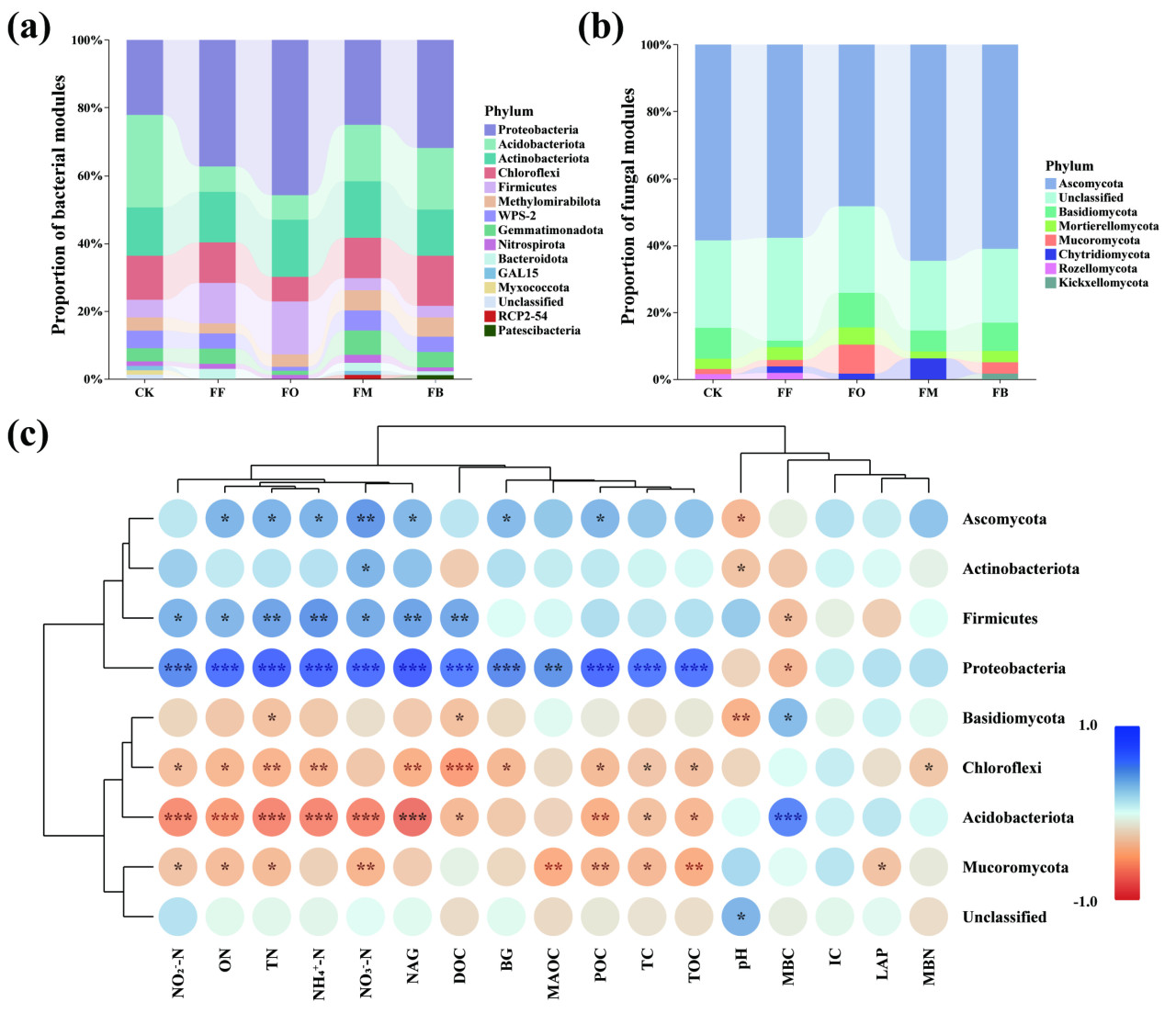
Чтобы дополнительно выяснить взаимосвязи между микробными сообществами и физико-химическими свойствами почвы, мы сосредоточились на доминирующих сообществах, определяемых как те, которые составляют более 5% модулей в сети. Доминирующие бактериальные сообщества включали Acidobacteriota, Proteobacteria, Actinobacteriota, Chloroflexi и Firmicutes (Рисунок 4a), тогда как доминирующими грибными сообществами были Ascomycota, Basidiomycota, Mucoromycota и неклассифицированные (Рисунок 4b). Actinobacteriota, Proteobacteria, Firmicutes и Ascomycota положительно коррелировали с компонентами углерода и азота почвы, а также с активностью почвенных ферментов (BG и NAG), но отрицательно коррелировали с MBC. Напротив, Acidobacteriota, Chloroflexi, Basidiomycota и Mucoromycota показали отрицательные корреляции с компонентами углерода и азота почвы и активностью ферментов, но положительные корреляции с MBC (Рисунок 4c). Неклассифицированная группа не оказала значительного влияния на компоненты углерода и азота почвы. Эти результаты подчеркивают различные функциональные роли микробных таксонов в круговороте углерода и азота в почве, при этом некоторые группы способствуют обороту углерода и азота, а другие потенциально ингибируют эти процессы.
Рисунок 4. Доли модулей бактериальных типов в сети корреляций (a). Доли модулей грибных типов в сети корреляций (b). Корреляционный анализ микробных таксонов с физико-химическими свойствами почвы для модулей с долями более 5% (c). Кластеризация была выполнена с использованием алгоритма евклидова расстояния и иерархической кластеризации полной связью. Были рассчитаны коэффициенты корреляции Спирмена, и значимость обозначена звездочками: 0,01 < p < 0,05, 0,001 < p < 0,01, p < 0,001. CK: без удобрений, FF: химическое удобрение, FO: комбинированное применение химического и органического жмыхового удобрения, FM: комбинированное применение химического и микробного удобрения, FB: комбинированное применение химического удобрения и биоугля. TC: общий углерод, TOC: общий органический углерод, IC: неорганический углерод, POC: частичный органический углерод, MAOC: минерал-ассоциированный органический углерод, DOC: растворенный органический углерод, TN: общий азот, ON: органический азот, NH₄⁺-N: аммонийный азот, NO₃⁻-N: нитратный азот, NO₂⁻-N: нитритный азот, BG: β-1,4-глюкозидаза, NAG: β-1,4-N-ацетилглюкозаминидаза, LAP: лейцинаминопептидаза, MBC: микробный биомассовый углерод, MBN: микробный биомассовый азот.
3.4. Реакция микробного некромассового углерода на внесение удобрений
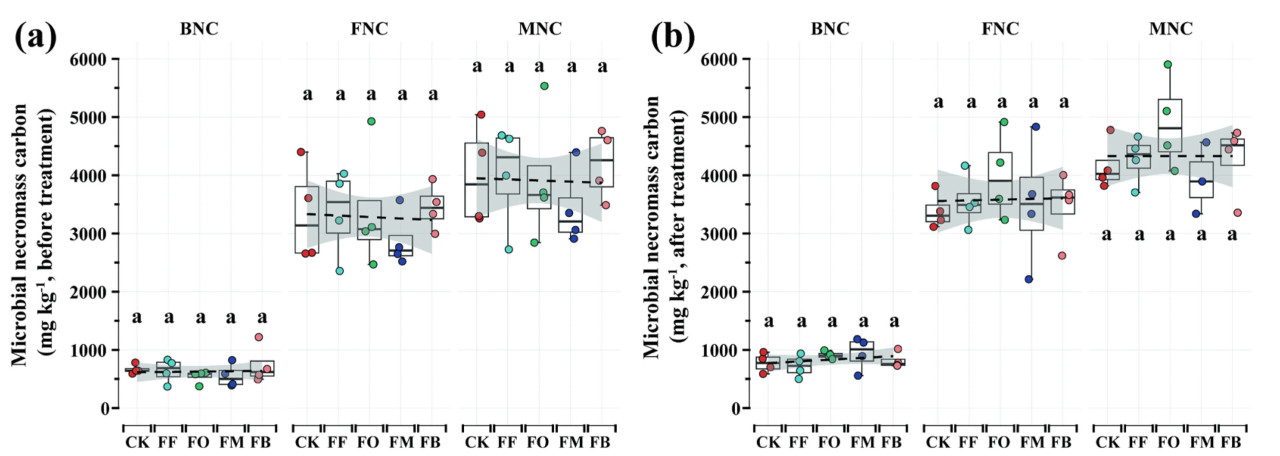
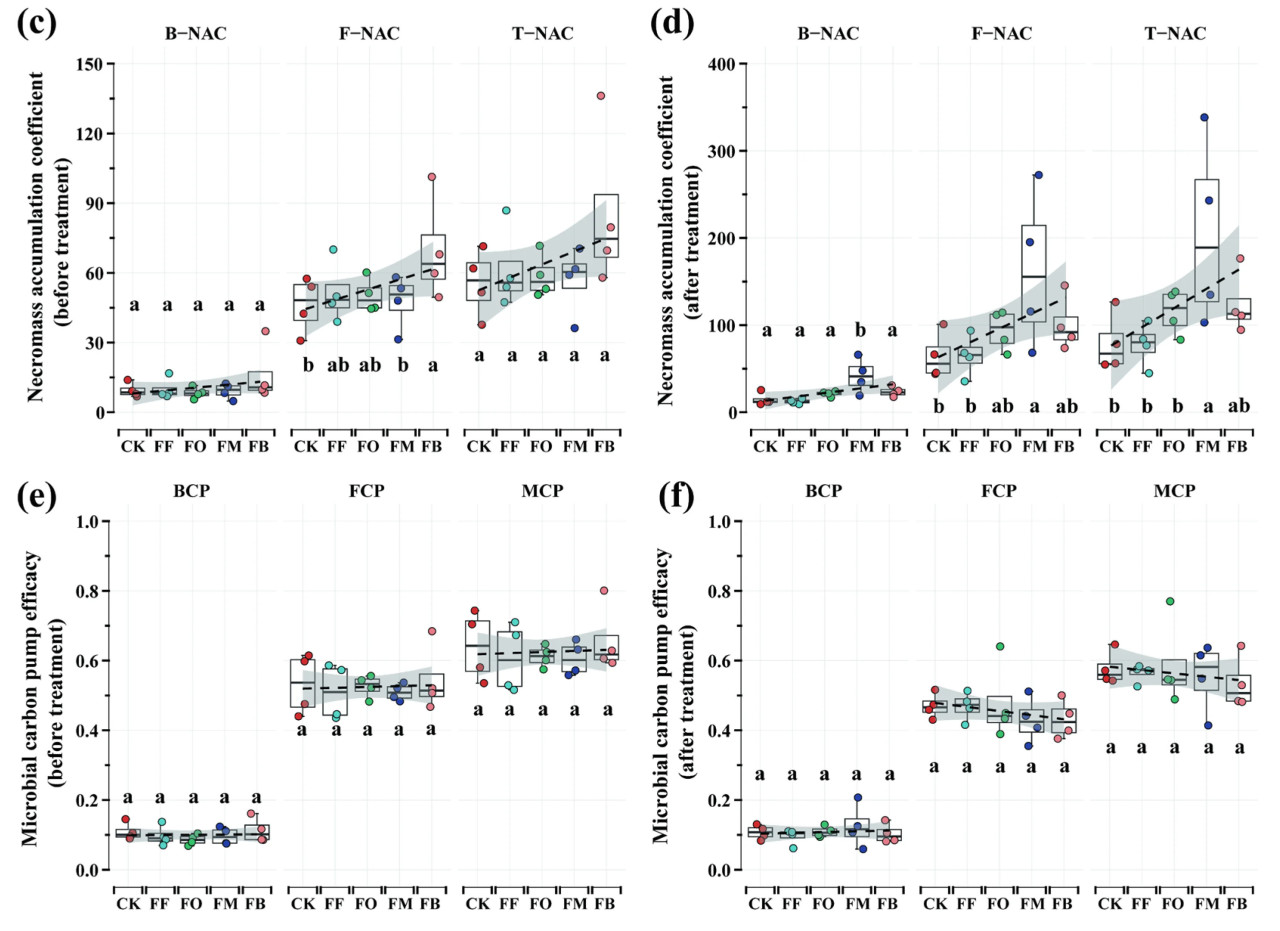
Наблюдались минимальные изменения BNC, FNC и MNC до и после обработок удобрениями, причем не было обнаружено значительных различий между группами обработок (Рисунок 5a, b). Это указывает на то, что внесение удобрений оказало ограниченное влияние на накопление MNC. В то время как B-NAC показал небольшие изменения в зависимости от обработок, F-NAC и T-NAC были значительно выше при обработке FM по сравнению с другими обработками. Различные обработки удобрениями оказали прогрессирующее влияние на F-NAC и T-NAC (Рисунок 5c, d). Эффективность MCP не показала значительных различий в различных обработках удобрениями, что предполагает слабое влияние удобрений на эффективность MCP (Рисунок 5e, f). В целом, хотя обработки удобрениями оказали ограниченное влияние на MNC, они повлияли на процесс накопления некромассы, причем FM был более благоприятен для накопления микробной некромассы. Однако влияние удобрений на эффективность MCP было незначительным.
Рисунок 5. Различия в MNC до и после различных обработок удобрениями (a, b). Различия в NAC до и после различных обработок удобрениями (c, d). Различия в эффективности MCP до и после различных обработок удобрениями (e, f). Групповые различия были проанализированы с использованием множественных сравнений Фишера LSD, причем обработки, обозначенные различными буквами (например, "a" и "b"), указывают на значительные различия (p < 0,05). CK: без удобрений, FF: химическое удобрение, FO: комбинированное применение химического и органического жмыхового удобрения, FM: комбинированное применение химического и микробного удобрения, FB: комбинированное применение химического удобрения и биоугля, MNC: общий микробный некромассовый углерод, BNC: бактериальный некромассовый углерод, FNC: грибной некромассовый углерод, NAC: коэффициент накопления микробного некромассового углерода, T-NAC: общий коэффициент накопления микробного некромассового углерода, B-NAC: коэффициент накопления бактериального некромассового углерода, F-NAC: коэффициент накопления грибного некромассового углерода, MCP: микробный углеродный насос, BCP: бактериальный углеродный насос, FCP: грибной углеродный насос.
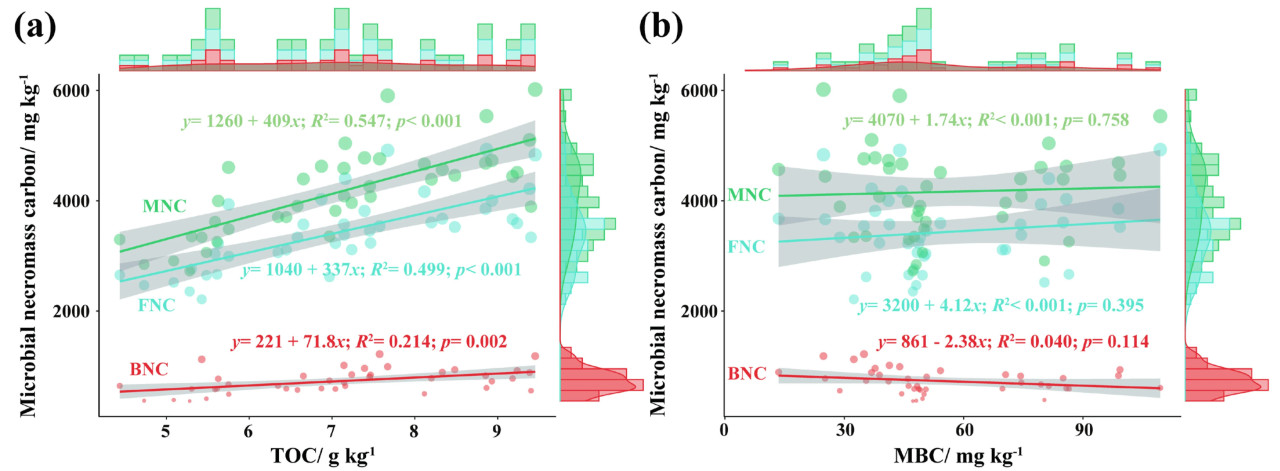
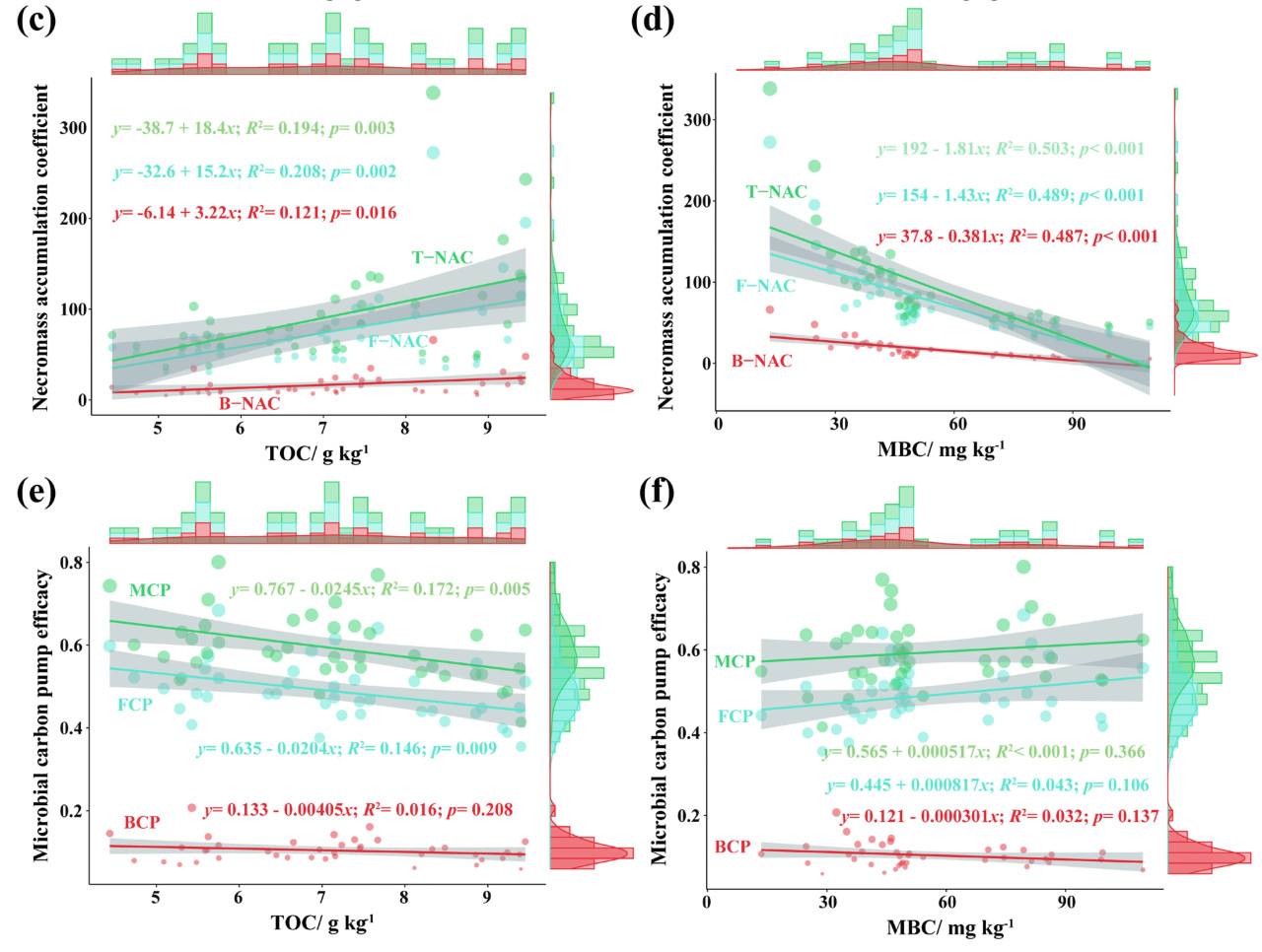
Чтобы прояснить характеристики MNC, T-NAC и эффективности MCP на ранней стадии внесения удобрений, были проанализированы их взаимосвязи с TOC и MBC. MNC и FNC значительно увеличивались с ростом TOC, показывая высокие значения R², что указывает на сильное положительное влияние TOC на накопление MNC и FNC. BNC также увеличивался с ростом TOC, но с более низким R², что предполагает, что BNC был меньше подвержен влиянию TOC (Рисунок 6a). Напротив, взаимосвязи между MNC, FNC, BNC и MBC не были значительными, с низкими значениями R², что указывает на слабое влияние MBC на MNC (Рисунок 6b). T-NAC, F-NAC и B-NAC показали значительные положительные корреляции с TOC, но значения R² были низкими, что предполагает, что коэффициент накопления микробного некромассового углерода (NAC) лишь незначительно подвержен влиянию TOC (Рисунок 6c). Однако T-NAC, F-NAC и B-NAC отрицательно коррелировали с MBC, с высокими и значительными значениями R², что указывает на сильное ингибирующее влияние MBC на NAC (Рисунок 6d). Эффективность MCP и эффективность FCP снижались с ростом TOC, но значения R² были низкими, что указывает на минимальное влияние TOC на эффективность MCP и FCP. Влияние TOC на эффективность BCP не было значительным (Рисунок 6e). Эффективность MCP и эффективность FCP были значительно положительно связаны с MBC, но с низкими значениями R², в то время как эффективность BCP не была значительно затронута MBC (Рисунок 6f). В целом, TOC и MBC являются ключевыми факторами, влияющими на накопление микробного некромассового углерода. TOC оказывает сильное положительное влияние, тогда как MBC оказывает сильное отрицательное влияние. Напротив, эффективность MCP меньше подвержена влиянию как TOC, так и MBC.
Рисунок 6. Графики линейной регрессии и гистограммы маргинального распределения MNC, NAC и эффективности MCP с TOC (a, c, e). Графики линейной регрессии и гистограммы маргинального распределения MNC, NAC и эффективности MCP с MBC (b, d, f). В регрессионном анализе R² представляет коэффициент детерминации, а p было рассчитано с использованием t-тестов. TOC: общий органический углерод, MBC: микробный биомассовый углерод, MNC: общий микробный некромассовый углерод, BNC: бактериальный некромассовый углерод, FNC: грибной некромассовый углерод, NAC: коэффициент накопления микробного некромассового углерода, T-NAC: общий коэффициент накопления микробного некромассового углерода, B-NAC: коэффициент накопления бактериального некромассового углерода, F-NAC: коэффициент накопления грибного некромассового углерода, MCP: микробный углеродный насос, BCP: бактериальный углеродный насос, FCP: грибной углеродный насос.
3.5. Процессы углеродно-азотной связи в условиях высокого содержания азота
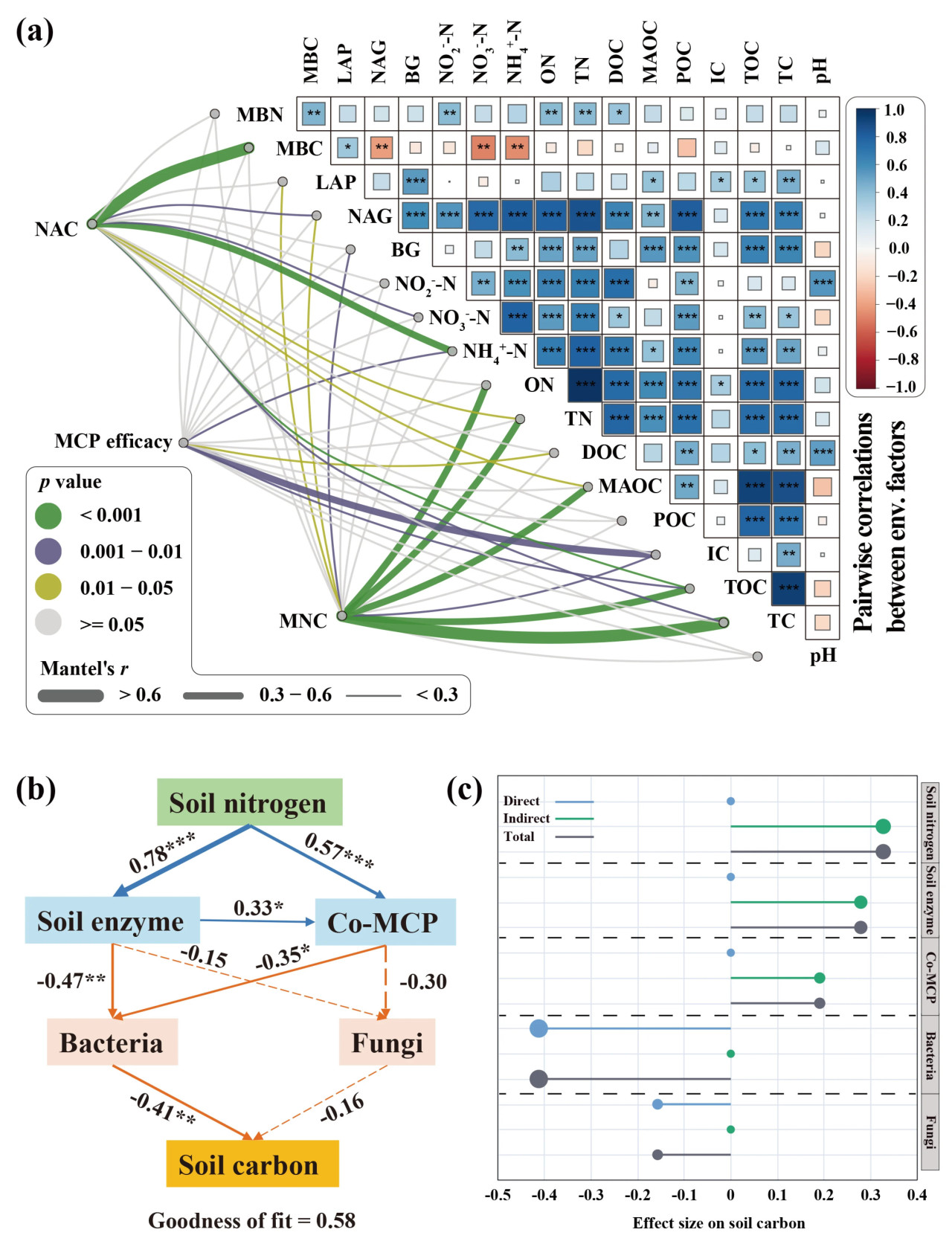
Используя полный набор данных, мы проанализировали процессы углеродно-азотной связи в почвах чайных плантаций в условиях высокого содержания азота на ранних стадиях внесения удобрений. В целом, физико-химические свойства почвы продемонстрировали значительные положительные корреляции, за исключением MBC, который показал значительные отрицательные корреляции с NAG, NH₄⁺-N и NO₃⁻-N. MNC имел сильную и значительную положительную корреляцию с TC (r > 0,6) и умеренную положительную корреляцию с TOC, MAOC, TN и ON (0,3 < r < 0,6); NAC показал сильную положительную корреляцию с MBC (r > 0,6) и значительную положительную корреляцию с NH₄⁺-N, демонстрируя при этом более слабые корреляции с NO₃⁻-N и NAG. Эффективность MCP была значительно положительно связана только с IC и показала более слабые положительные корреляции с NH₄⁺-N и DOC (Рисунок 7a).
Рисунок 7. Корреляции между физико-химическими свойствами почвы и их взаимосвязи с MNC, NAC и эффективностью MCP (a). Корреляции основаны на коэффициентах Пирсона, причем цветовой градиент представляет силу корреляции. Статистическая значимость обозначена звездочками: 0,01 < p < 0,05, 0,001 < p < 0,01, p < 0,001. Взаимосвязи углеродно-азотной связи на основе PLS-PM (b). Синие и оранжевые стрелки представляют положительные и отрицательные взаимосвязи соответственно. Ширина стрелок соответствует коэффициентам пути, которые были рассчитаны с использованием схемы взвешивания пути. Сплошные линии указывают на значительные взаимосвязи (p < 0,05), в то время как пунктирные линии указывают на незначительные взаимосвязи. Значимость коэффициентов пути была определена с использованием t-тестов и обозначена звездочками: 0,01 < p < 0,05, 0,001 < p < 0,01, p < 0,001. В PLS-PM скрытая переменная "почвенный азот" включает TN, ON, NH₄⁺-N, NO₃⁻-N и NO₂⁻-N. Скрытая переменная "почвенный фермент" включает BG и NAG. Скрытая переменная "Co-MCP" состоит из MNC, NAC и эффективности MCP. Скрытая переменная "бактерии" включает Acidobacteriota, Proteobacteria, Actinobacteriota, Chloroflexi и Firmicutes, в то время как скрытая переменная "грибы" включает Ascomycota, Basidiomycota и Mucoromycota. Скрытая переменная "почвенный углерод" включает TC, TOC, IC, DOC, MAOC, POC и MBC. Размер эффекта скрытых переменных на почвенный углерод в PLS-PM (c). TC: общий углерод, TOC: общий органический углерод, IC: неорганический углерод, POC: частичный органический углерод, MAOC: минерал-ассоциированный органический углерод, DOC: растворенный органический углерод, TN: общий азот, ON: органический азот, NH₄⁺-N: аммонийный азот, NO₃⁻-N: нитратный азот, NO₂⁻-N: нитритный азот, BG: β-1,4-глюкозидаза, NAG: β-1,4-N-ацетилглюкозаминидаза, LAP: лейцинаминопептидаза, MBC: микробный биомассовый углерод, MBN: микробный биомассовый азот.
Основываясь на результатах, PLS-PM была использована для выяснения процессов углеродно-азотной связи в условиях высокого содержания азота на ранних стадиях внесения удобрений. Модель объяснила приблизительно 58% вариаций почвенного углерода. Учитывая отсутствие значительных изменений в эффективности MCP, наблюдаемые переменные MNC, NAC и эффективность MCP были объединены в скрытую переменную, названную Co-MCP. Анализ показал, что бактериальные сообщества оказывали прямое ингибирующее влияние на накопление углерода в почве. И наоборот, почвенный азот косвенно способствовал накоплению углерода в почве, усиливая активность почвенных ферментов и Co-MCP, что, в свою очередь, подавляло бактериальные сообщества. Активность почвенных ферментов также косвенно способствовала накоплению углерода в почве через свое влияние на Co-MCP. Грибные сообщества, однако, не оказали значительного влияния на этот процесс (Рисунок 7b, c). Резюмируя, в условиях высокого содержания азота почвенный азот регулирует бактериальные сообщества, воздействуя на активность почвенных ферментов и Co-MCP, тем самым способствуя секвестрации углерода в почве.
4. Обсуждение
4.1. Влияние почвенных ферментов на углеродно-азотную связь
Обычно считается, что в условиях высокого содержания азота бактерии и грибы способны использовать дополнительный азот для пролиферации, что приводит к усилению секреции и активности почвенных ферментов [38]. Однако результаты этого исследования указывают на то, что активность почвенных ферментов регулирует бактериальные сообщества (Рисунок 7b). Активность почвенных ферментов и микробные сообщества могут участвовать в более сложных механизмах обратной связи. Почвенные ферменты разлагают и трансформируют органические и неорганические субстраты, тем самым прямо или косвенно влияя на энергетические и питательные ресурсы, доступные микроорганизмам, и перестраивая структуру и функцию сообщества [39]. Различные функциональные микробные группы отдают приоритет различным наборам внеклеточных ферментов, дополнительно изменяя эффективность круговорота питательных веществ и, в свою очередь, оказывая взаимную регуляцию на ферментативную систему [40]. Со временем эта двусторонняя обратная связь устанавливает динамическое равновесие, в котором почвенная система претерпевает непрерывную микросредовую перестройку и функциональную сукцессию, в конечном итоге обеспечивая тесную связь между процессами азота и углерода.
Мы обнаружили, что Actinobacteriota, Proteobacteria, Firmicutes и Ascomycota демонстрировали положительные корреляции с компонентами углерода и азота почвы, а также с активностью почвенных ферментов, тогда как Acidobacteriota, Chloroflexi, Basidiomycota и Mucoromycota показали отрицательные корреляции (Рисунок 4c). Эта закономерность может отражать различные стратегии наследования ресурсов. В условиях высокой доступности питательных веществ и повышенной активности ферментов микроорганизмы, способные быстро использовать растворимый углерод и азот, одновременно синтезируя и секретируя множество внеклеточных ферментов (например, некоторые Proteobacteria, Actinobacteriota, Firmicutes и Ascomycota), часто получают конкурентное преимущество [41]. Постоянно усиливая продукцию и разнообразие этих ферментов, они ускоряют расщепление и трансформацию питательных веществ, тем самым закрепляя за собой эвтрофную почвенную нишу, характеризующуюся высокой активностью ферментов и биомассой. Как только эта ниша и связанное с ней микробное сообщество установлены, они, как правило, придают генетический или мемориальный эффект последующей микробной сукцессии и сохранению функциональных генов [42]. Напротив, олиготрофные таксоны, такие как Acidobacteriota, Chloroflexi, Basidiomycota и Mucoromycota, лучше адаптированы к средам, где органическое вещество почвы относительно устойчиво к разложению или эффективность использования азота низка [43]. В этих бедных питательными веществами условиях они используют специализированные метаболические пути, модификации структурных белков или экологические стратегии (например, формирование грибных сетей или секрецию меньшего количества, но более целевых ферментов) для использования устойчивых субстратов [44]. Как только такие бедные питательными веществами микросреды достигают стабильного состояния, характерные черты этих сообществ могут сохраняться, отражая их способность поддерживать стабильные популяции даже в условиях ограниченной доступности ресурсов [39].
В условиях высокого содержания азота сдвиги в стратегиях использования ресурсов как растениями, так и микроорганизмами могут создавать более сложные кооперативные или конкурентные взаимодействия, а не просто оказывать стимулирующее или ингибирующее воздействие на микробные сообщества. Различные факторы, включая физическую структуру почвы, корневые экссудаты и параметры окружающей среды, могут также вмешиваться, либо усиливая, либо ослабляя наблюдаемые положительные или отрицательные корреляции. Архитектура почвенного порового пространства влияет на диффузию ферментов и доступность субстрата, благоприятствуя микробным популяциям, способным использовать ресурсы на микроуровне. Аналогично, корневые экссудаты могут изменять локальный pH или предоставлять специфические органические кислоты, формируя как конкурентные, так и мутуалистические взаимосвязи среди сосуществующих таксонов [45]. Более того, климатические импульсы (например, сезонные дожди или засуха) периодически изменяют активность почвенных ферментов и доступность субстрата, приводя к циклическому расширению или сокращению микробных групп, демонстрирующих положительные или отрицательные корреляции со свойствами почвы [46]. Под влиянием таких многофакторных воздействий механизмы, с помощью которых почвенные ферменты и микробные сообщества совместно регулируют углеродно-азотную связь, часто проявляют выраженную пространственно-временную гетерогенность.
4.2. Реакция эффективности MCP на добавление азота
Эффективность MCP измеряет способность микробных сообществ трансформировать и накапливать органический углерод в почве, представляя их роль в долгосрочной секвестрации углерода [47]. Эффективность MCP фокусируется на стабильности углерода и его долгосрочном удержании, а не на краткосрочных реакциях [48]. Таким образом, в этом исследовании эффективность MCP не показала значительной реакции на обработки удобрениями (Рисунок 5c, d), но была значительно положительно связана с IC (Рисунок 7a). Это подчеркивает потенциал неорганического углерода как индикатора эффективности MCP. Накопление и стабильность IC в почве отражают регуляторную функцию микробной активности в круговороте углерода в почве, в частности в трансформации углерода и его долгосрочном хранении [49]. Образование IC тесно связано с микробными процессами, особенно в образовании карбонатов, что представляет собой конверсию органического углерода в более стабильные формы и может рассматриваться как часть процесса MCP [50]. Более того, изменения содержания IC могут указывать на баланс между стабилизацией и потерей углерода, косвенно отражая долгосрочную эффективность MCP [51]. Однако накопление IC значительно ограничено в кислых почвах [52], что предполагает необходимость дальнейших исследований для проверки его универсальности и точности как индикатора эффективности MCP.
Эффективность MCP имеет определенные ограничения при изучении процессов углеродно-азотной связи в почве после внесения удобрений. Чтобы решить эту проблему, мы расширили концепцию MCP, включив наблюдаемые переменные MNC, NAC и эффективность MCP в новую скрытую переменную Co-MCP. Было обнаружено, что на эту новую переменную влияют почвенный азот и активность ферментов в условиях высокого содержания азота, что, в свою очередь, изменяет бактериальные сообщества и способствует накоплению углерода (Рисунок 7b). Однако экологическое значение Co-MCP требует дальнейшего изучения. Как и в случае с эффективностью MCP, краткосрочное добавление азота значительно не влияет на уровни MNC в почве. Напротив, в условиях высокого содержания азота микробные сообщества склонны направлять больше ресурсов на рост клеток и метаболизм, что приводит к значительному увеличению NAC, тем самым повышая потенциал хранения SOC [53]. Изменения NAC отражают динамическую регуляцию почвенных питательных веществ и микробной активности в краткосрочной перспективе, тогда как изменения эффективности MCP и MNC в большей степени указывают на долгосрочные балансы между процессами накопления и разложения в системе [54]. Включение MNC и NAC в структуру MCP повышает точность описания и прогнозирования процессов углеродно-азотной связи. Однако необходимы дальнейшие исследования для проверки этой расширенной системы показателей.
Кроме того, мы обнаружили, что MNC, NAC и эффективность MCP были значительно связаны с TOC, тогда как только F-NAC и T-NAC показали значительные корреляции с MBC (Рисунок 6). Этот результат, вероятно, отражает различные микробные стратегии в углеродно-азотной связи и распределении питательных веществ. Грибы обычно обладают более обширными грибными сетями и секретируют более широкий спектр внеклеточных ферментов, что позволяет им расщеплять более сложные или устойчивые источники углерода в почве. После образования грибные остатки демонстрируют высокую стабильность и сильную удерживающую способность, легко связываясь с почвенными минералами или органическими коллоидами, таким образом демонстрируя более выраженную положительную взаимосвязь с MBC. Грибные остатки часто накапливаются в почвенных агрегатах или глинисто-органических комплексах, играя ключевую роль в стабилизации структуры почвы и удержании как углерода, так и азота [55]. Хотя бактерии встречаются в большем количестве и растут быстрее, их остатки более подвержены последующей микробной деградации или трансформации. Следовательно, B-NAC менее сильно связан с MBC, вероятно, потому, что бактериальные остатки быстрее оборачиваются в почве и оказывают сравнительно более слабый кумулятивный эффект [56]. Когда TOC увеличивается, микробные сообщества, особенно грибы, склонны направлять больше энергии на биосинтез и секрецию ферментов, тем самым способствуя поглощению азота, ассимиляции и образованию остатков [57]. Следовательно, формирование и накопление грибных остатков служат критическим мостом между пулами почвенной биомассы и остатков. При управлении накоплением микробных остатков в почве следует уделять больше внимания усилению или поддержанию грибных сообществ. Это может быть достигнуто путем включения органических материалов, богатых лигнином или полисахаридами, для предоставления потенциальных субстратов, или путем поддержания относительно стабильной влажности почвы и структуры агрегатов, которые способствуют росту грибов и стабилизации остатков. Такие практики предлагают перспективные пути для увеличения органического вещества почвы и улучшения удержания питательных веществ за счет усиленного вклада грибов.
4.3. Влияние прайминг-эффекта на почвенный углерод при совместном внесении удобрений
Совместное внесение удобрений значительно усилило взаимосвязи между микробными сообществами и физико-химическими свойствами почвы, что привело к более сложным экологическим процессам (Рисунок 3 и Рисунок 4). Кроме того, корреляции между различными микробными таксонами и углеродом и азотом почвы продемонстрировали согласованную тенденцию, способствуя общему накоплению углерода в почве (Рисунок 1 и Рисунок 4c). Этот результат, по-видимому, противоречит типичному прайминг-эффекту. Прайминг-эффект относится к стимуляции микробной активности после поступления внешних источников углерода (например, органических удобрений), что ускоряет разложение ранее существовавшего SOC [58]. Этот эффект возникает потому, что микроорганизмы получают дополнительные энергетические ресурсы, изменяя свои метаболические пути и увеличивая скорость разложения органического вещества почвы [59]. Это несоответствие предполагает, что, хотя совместное внесение удобрений усиливает углеродно-азотную связь и микробные взаимодействия со свойствами почвы, оно также может снижать величину прайминг-эффекта, способствуя секвестрации углерода в почве, а не ускорению разложения. Дальнейшие исследования необходимы для выяснения этих противоположных механизмов.
Совместное внесение удобрений индуцирует прайминг-эффект, но все же приводит к накоплению углерода в почве, вероятно, из-за взаимодействия множества факторов. Хотя прайминг-эффект усиливает микробную активность и ускоряет разложение органического вещества почвы, поступление внешнего органического углерода может превышать скорость микробного разложения [60]. Кроме того, микроорганизмы используют внешний углерод для улучшения метаболической эффективности, частично превращая его в микробный некромассовый углерод или метаболические побочные продукты. Эти компоненты микробного некромассового углерода, такие как фрагменты клеток и внеклеточные полимеры, являются более устойчивыми и постепенно накапливаются в почве [61]. Более того, совместное внесение удобрений увеличивает содержание минеральных питательных веществ в почве (например, оксидов железа, алюминия или глинистых минералов), которые могут связываться с продуктами микробного происхождения, образуя стабильные минерально-органические комплексы, тем самым снижая дальнейшее разложение органического углерода [62]. Совместное внесение также способствует росту растений, причем поступление углерода из корней дополнительно пополняет запасы SOC. Позитивные механизмы обратной связи между корнями растений и ризосферными микроорганизмами могут дополнительно ускорять накопление углерода в почве, а не его потерю [63,64]. Таким образом, прайминг-эффект, вызванный совместным внесением удобрений, можно рассматривать как краткосрочное нарушение углеродного баланса почвы. По мере того как эффект удобрения постепенно ослабевает, почва переходит к новому равновесию накопления углерода. В этом процессе поступление внешних питательных веществ изменяет использование микроорганизмами почвенных источников углерода, стабилизируя углеродный баланс почвы после первоначальных колебаний. Однако если прайминг-эффект сохраняется сильно, это может привести к устойчивому истощению пулов почвенного углерода, потенциально подрывая способность почвы к накоплению углерода. В контексте долгосрочного внесения удобрений в сельскохозяйственных почвах это может увеличить риск истощения пула почвенного углерода, что подчеркивает необходимость тщательного управления практиками внесения удобрений для балансировки динамики почвенного углерода.
Несмотря на различные краткосрочные воздействия пяти обработок удобрениями (CK, FF, FO, FM и FB) на прайминг-эффект в почве, в целом они соответствовали общей структуре углеродно-азотной связи на ранней стадии внесения удобрений (Рисунок 7b). Другими словами, вскоре после внесения удобрений почвенная система следовала пути, инициированному поступлением почвенного азота, модулируемому через активность почвенных ферментов и микробную трансформацию углерода (Co-MCP), и подверженному обратной связи со стороны почвенного углерода и микробного сообщества. В краткосрочной перспективе экзогенный азот стал наиболее непосредственным драйвером, стимулируя ферментативные системы почвы и микробное использование углерода в разной степени. В условиях высокого содержания азота микробные пути разложения и поглощения углерода относительно сходны. Интересно, что почвенный углерод показал отрицательную корреляцию с микробным сообществом (в особенности с бактериями), что может быть связано с динамикой "поставка углерода – потребление микроорганизмами" [65]. Когда почвенный углерод относительно обилен и легко разлагается, микробные популяции изначально выигрывают; однако быстрая оборачиваемость и последующее перераспределение питательных веществ могут способствовать замене определенных бактериальных таксонов более конкурентными группами [66]. Это открытие согласуется с нашим наблюдением, что доминирующий бактериальный тип сместился с Proteobacteria на Acidobacteriota (Рисунок 2a). В течение раннего периода внесения удобрений эти различные стратегии удобрения, таким образом, следуют объединяющей модели, в которой поступление азота стимулирует активность ферментов и микробную обработку углерода, в конечном итоге влияя на пулы почвенного углерода и структуру микробного сообщества. По мере продолжения внесения удобрений и эволюции почвенной среды каждая обработка, вероятно, будет по-разному влиять на стабильность почвенного углерода, судьбу азота и состав микробного сообщества. Тем не менее, на начальных стадиях во всех обработках наблюдается согласованный механизм углеродно-азотной связи. Эта согласованность предоставляет более простой и точный подход для оценки и количественного определения углеродного пула в чайных плантациях после внесения удобрений.
5. Выводы
На ранних стадиях внесения удобрений почвенный углерод накапливался в основном в форме POC, что было обусловлено повышенной бактериальной активностью и опосредованными ферментами трансформациями питательных веществ. В то время как MNC и эффективность MCP продемонстрировали ограниченные краткосрочные реакции, NAC стал азот-чувствительным индикатором, отражающим микробные адаптации к обогащению азотом. Режимы смешанного внесения удобрений способствовали активности почвенных ферментов (BG и NAG) и усиливали микробные взаимодействия со свойствами почвы, в особенности среди бактериальных сообществ (Actinobacteriota, Proteobacteria и Ascomycota), которые существенно способствовали процессам углеродно-азотной связи в почве. Чтобы интегрировать целенаправленную регуляцию ферментов и управление микробными сообществами в практику внесения удобрений, фермеры могут рассмотреть возможность применения микробных инокулянтов для стимулирования опосредованного ферментами круговорота питательных веществ и выбора смешанных удобрений (например, комбинирование органических и микробных удобрений) для содействия синергичным микробным взаимодействиям. Эти стратегии направлены на повышение секвестрации углерода в почве при одновременном смягчении экологических рисков, связанных с азотом. Будущие исследования должны усовершенствовать структуру MCP для количественной связи эффективности накопления углерода в почве с урожайностью чая и экологической устойчивостью, прокладывая путь для точного управления питательными веществами в многолетних сельскохозяйственных системах.
Список сокращений
BCP бактериальный углеродный насос
BG β-1,4-глюкозидаза
B-NAC коэффициент накопления бактериального некромассового углерода
BNC бактериальный некромассовый углерод
CK без удобрений
C-N углерод–азот
DOC растворенный органический углерод
FB комбинированное применение химического удобрения и биоугля
FCP грибной углеродный насос
FF химическое удобрение
FM комбинированное применение химического и микробного удобрения
F-NAC коэффициент накопления грибного некромассового углерода
FNC грибной некромассовый углерод
FO комбинированное применение химического и органического удобрения
IC неорганический углерод
LAP лейцинаминопептидаза
MAOC минерал-ассоциированный органический углерод
MBC микробный биомассовый углерод
MBN микробный биомассовый азот
MCP микробный углеродный насос
MNC общий микробный некромассовый углерод
NAG β-1,4-N-ацетилглюкозаминидаза
NAC коэффициент накопления микробного некромассового углерода
NH₄⁺-N аммонийный азот
NO₂⁻-N нитритный азот
NO₃⁻-N нитратный азот
ON органический азот
POC частичный органический углерод
SOC почвенный органический углерод
TC общий углерод
TN общий азот
T-NAC общий коэффициент накопления микробного некромассового углерода
TOC общий органический углерод
Ссылки
1. Yan, P.; Shen, C.; Fan, L.; Li, X.; Zhang, L.; Zhang, L.; Han, W. Tea planting affects soil acidification and nitrogen and phosphorus distribution in soil. Agric. Ecosyst. Environ. 2018, 254, 20–25. [Google Scholar] [CrossRef]
2. FAO. International Tea Market: Market Situation, Prospects and Emerging Issues. 2022. Available online: https://openknowledge.fao.org (accessed on 13 January 2025).
3. Yang, X.; Ni, K.; Shi, Y.; Yi, X.; Ji, L.; Wei, S.; Jiang, Y.; Zhang, Y.; Cai, Y.; Ma, Q.; et al. Metagenomics reveals N-induced changes in carbon-degrading genes and microbial communities of tea (Camellia sinensis L.) plantation soil under long-term fertilization. Sci. Total Environ. 2023, 856, 159231. [Google Scholar] [CrossRef] [PubMed]
4. Wang, Y.; Yao, Z.; Pan, Z.; Wang, R.; Yan, G.; Liu, C.; Su, Y.; Zheng, X.; Butterbach-Bahl, K. Tea-planted soils as global hotspots for N2O emissions from croplands. Environ. Res. Lett. 2020, 15, 104018. [Google Scholar] [CrossRef]
5. Vitousek, P.; Howarth, R. Nitrogen limitation on land and in the sea: How can it occur? Biogeochemistry 1991, 13, 87–115. [Google Scholar] [CrossRef]
6. Jiang, N.; Huang, W.; Chen, Z.; Zhang, Y.; Jiang, D.; Wu, C.; Yao, Z.; Chen, L. More labile carbon inputs lessen the positive effects of nitrogen enrichment on soil carbon storage in a temperate grassland. Plant Soil 2023, 505, 225–237. [Google Scholar] [CrossRef]
7. Niu, S.; Song, L.; Wang, J.; Luo, Y.; Yu, G. Dynamic carbon-nitrogen coupling under global change. Sci. China Life Sci. 2023, 66, 771–782. [Google Scholar] [CrossRef]
8. Ni, H.; Liu, C.; Sun, B.; Liang, Y. Response of global farmland soil organic carbon to nitrogen application over time depends on soil type. Geoderma 2022, 406, 115542. [Google Scholar] [CrossRef]
9. Wang, X.; Feng, J.; Ao, G.; Qin, W.; Han, M.; Shen, Y.; Liu, M.; Chen, Y.; Zhu, B. Globally nitrogen addition alters soil microbial community structure, but has minor effects on soil microbial diversity and richness. Soil. Biol. Biochem. 2023, 179, 108982. [Google Scholar] [CrossRef]
10. Feng, X.; Qin, S.; Zhang, D.; Chen, P.; Hu, J.; Wang, G.; Liu, Y.; Wei, B.; Li, Q.; Yang, Y.; et al. Nitrogen input enhances microbial carbon use efficiency by altering plant-microbe-mineral interactions. Glob. Chang. Biol. 2022, 28, 4845–4860. [Google Scholar] [CrossRef]
11. Tian, J.; Dungait, J.A.J.; Hou, R.; Deng, Y.; Hartley, I.P.; Yang, Y.; Kuzyakov, Y.; Zhang, F.; Cotrufo, M.F.; Zhou, J. Microbially mediated mechanisms underlie soil carbon accrual by conservation agriculture under decade-long warming. Nat. Commun. 2024, 15, 377. [Google Scholar] [CrossRef]
12. Liang, C.; Schimel, J.P.; Jastrow, J.D. The importance of anabolism in microbial control over soil carbon storage. Nat. Microbiol. 2017, 2, 17105. [Google Scholar] [CrossRef] [PubMed]
13. Zhu, X.; Jackson, R.D.; DeLucia, E.H.; Tiedje, J.M.; Liang, C. The soil microbial carbon pump: From conceptual insights to empirical assessments. Glob. Chang. Biol. 2020, 26, 6032–6039. [Google Scholar] [CrossRef] [PubMed]
14. Yang, L.; Canarini, A.; Zhang, W.; Lang, M.; Chen, Y.; Cui, Z.; Kuzyakov, Y.; Richter, A.; Chen, X.; Zhang, F.; et al. Microbial life-history strategies mediate microbial carbon pump efficacy in response to N management depending on stoichiometry of microbial demand. Glob. Chang. Biol. 2024, 30, e17311. [Google Scholar] [CrossRef] [PubMed]
15. Allison, S.D.; Martiny, J.B. Resistance, resilience, and redundancy in microbial communities. Proc. Natl. Acad. Sci. USA 2008, 105, 11512–11519. [Google Scholar] [CrossRef]
16. Wang, F.; Liu, Q.; Hu, X.; Fang, X.-M.; Wang, S.; Chen, F.-S. Divergent responses of soil microbial community to long-term nitrogen and phosphorus additions in a subtropical Chinese fir plantation. CATENA 2024, 242, 108132. [Google Scholar] [CrossRef]
17. Mori, T. Does ecoenzymatic stoichiometry really determine microbial nutrient limitations? Soil. Biol. Biochem. 2020, 146, 107816. [Google Scholar] [CrossRef]
18. Zhang, X.; Dippold, M.A.; Kuzyakov, Y.; Razavi, B.S. Spatial pattern of enzyme activities depends on root exudate composition. Soil. Biol. Biochem. 2019, 133, 83–93. [Google Scholar] [CrossRef]
19. Craine, J.M.; Jackson, R.D. Plant nitrogen and phosphorus limitation in 98 North American grassland soils. Plant Soil 2009, 334, 73–84. [Google Scholar] [CrossRef]
20. Henneron, L.; Kardol, P.; Wardle, D.A.; Cros, C.; Fontaine, S. Rhizosphere control of soil nitrogen cycling: A key component of plant economic strategies. New Phytol. 2020, 228, 1269–1282. [Google Scholar] [CrossRef]
21. Moreau, D.; Bardgett, R.D.; Finlay, R.D.; Jones, D.L.; Philippot, L.; Power, S. A plant perspective on nitrogen cycling in the rhizosphere. Funct. Ecol. 2019, 33, 540–552. [Google Scholar] [CrossRef]
22. Qiao, C.; Xu, B.; Han, Y.; Wang, J.; Wang, X.; Liu, L.; Liu, W.; Wan, S.; Tan, H.; Liu, Y.; et al. Synthetic nitrogen fertilizers alter the soil chemistry, production and quality of tea. A meta-analysis. Agron. Sustain. Dev. 2018, 38, 10. [Google Scholar] [CrossRef]
23. Bonheure, D.; Willson, K. Mineral Nutrition and Fertilizers; Willson, K.C., Clifford, M.N., Eds.; Springer: Dordrecht, The Netherlands, 1992; pp. 269–329. [Google Scholar] [CrossRef]
24. Wanyoko, J.; Owuor, P. Effects of plant densities and nitrogen fertilizer rates on the yield of mature seedling Kenyan tea. Tea 1995, 16, 14–20. Available online: https://www.cabidigitallibrary.org/doi/full/10.5555/19960304943 (accessed on 13 January 2025).
25. Ma, L.; Yang, X.; Shi, Y.; Yi, X.; Ji, L.; Cheng, Y.; Ni, K.; Ruan, J. Response of tea yield, quality and soil bacterial characteristics to long-term nitrogen fertilization in an eleven-year field experiment. Appl. Soil Ecol. 2021, 166, 103976. [Google Scholar] [CrossRef]
26. Ye, J.; Wang, Y.; Wang, Y.; Hong, L.; Jia, X.; Kang, J.; Lin, S.; Wu, Z.; Wang, H. Improvement of soil acidification in tea plantations by long-term use of organic fertilizers and its effect on tea yield and quality. Front. Plant Sci. 2022, 13, 1055900. [Google Scholar] [CrossRef]
27. Han, Z.; Lin, H.; Xu, P.; Li, Z.; Wang, J.; Zou, J. Impact of organic fertilizer substitution and biochar amendment on net greenhouse gas budget in a tea plantation. Agric. Ecosyst. Environ. 2022, 326, 107779. [Google Scholar] [CrossRef]
28. Xie, S.; Yang, F.; Feng, H.; Yu, Z.; Liu, C.; Wei, C.; Liang, T. Organic fertilizer reduced carbon and nitrogen in runoff and buffered soil acidification in tea plantations: Evidence in nutrient contents and isotope fractionations. Sci. Total Environ. 2021, 762, 143059. [Google Scholar] [CrossRef]
29. Giannitsopoulos, M.L.; Burgess, P.J.; Sakrabani, R.; Holden, A.; Saini, H.; Kirui, C. Modelling the effects of soil organic content and pH on the yield responses of tea to nitrogen fertilizer. Agric. Syst. 2023, 212, 103754. [Google Scholar] [CrossRef]
30. Hu, J.; Huang, C.; Zhou, S.; Liu, X.; Dijkstra, F.A. Nitrogen addition increases microbial necromass in croplands and bacterial necromass in forests: A global meta-analysis. Soil Biol. Biochem. 2022, 165, 108500. [Google Scholar] [CrossRef]
31. Fang, X.; Zhou, G.; Qu, C.; Huang, W.; Zhang, D.; Li, Y.; Yi, Z.; Liu, J. Translocating subtropical forest soils to a warmer region alters microbial communities and increases the decomposition of mineral-associated organic carbon. Soil. Biol. Biochem. 2020, 142, 107707. [Google Scholar] [CrossRef]
32. Vance, E.D.; Brookes, P.C.; Jenkinson, D.S. An extraction method for measuring soil microbial biomass C. Soil Biol. Biochem. 1987, 19, 703–707. [Google Scholar] [CrossRef]
33. Bell, C.W.; Fricks, B.E.; Rocca, J.D.; Steinweg, J.M.; McMahon, S.K.; Wallenstein, M.D. High-throughput fluorometric measurement of potential soil extracellular enzyme activities. J. Vis. Exp. 2013, e50961. [Google Scholar] [CrossRef]
34. Liang, C.; Amelung, W.; Lehmann, J.; Kastner, M. Quantitative assessment of microbial necromass contribution to soil organic matter. Glob. Chang. Biol. 2019, 25, 3578–3590. [Google Scholar] [CrossRef] [PubMed]
35. Jiao, N.; Luo, T.; Chen, Q.; Zhao, Z.; Xiao, X.; Liu, J.; Jian, Z.; Xie, S.; Thomas, H.; Herndl, G.J.; et al. The microbial carbon pump and climate change. Nat. Rev. Microbiol. 2024, 22, 408–419. [Google Scholar] [CrossRef] [PubMed]
36. Han, B.; Yao, Y.; Wang, Y.; Su, X.; Ma, L.; Chen, X.; Li, Z. Microbial traits dictate soil necromass accumulation coefficient: A global synthesis. Glob. Ecol. Biogeogr. 2023, 33, 151–161. [Google Scholar] [CrossRef]
37. Shi, Y.; Wang, J.; Ao, Y.; Han, J.; Guo, Z.; Liu, X.; Zhang, J.; Mu, C.; Le Roux, X. Responses of soil N2O emissions and their abiotic and biotic drivers to altered rainfall regimes and co-occurring wet N deposition in a semi-arid grassland. Glob. Chang. Biol. 2021, 27, 4894–4908. [Google Scholar] [CrossRef]
38. Li, J.; Sang, C.; Yang, J.; Qu, L.; Xia, Z.; Sun, H.; Jiang, P.; Wang, X.; He, H.; Wang, C. Stoichiometric imbalance and microbial community regulate microbial elements use efficiencies under nitrogen addition. Soil Biol. Biochem. 2021, 156, 108207. [Google Scholar] [CrossRef]
39. Philippot, L.; Griffiths, B.S.; Langenheder, S. Microbial Community Resilience across Ecosystems and Multiple Disturbances. Microbiol. Mol. Biol. Rev. 2021, 85, e00026-20. [Google Scholar] [CrossRef]
40. Xiao, W.; Chen, X.; Jing, X.; Zhu, B. A meta-analysis of soil extracellular enzyme activities in response to global change. Soil Biol. Biochem. 2018, 123, 21–32. [Google Scholar] [CrossRef]
41. Stock, S.C.; Köster, M.; Dippold, M.A.; Nájera, F.; Matus, F.; Merino, C.; Boy, J.; Spielvogel, S.; Gorbushina, A.; Kuzyakov, Y. Environmental drivers and stoichiometric constraints on enzyme activities in soils from rhizosphere to continental scale. Geoderma 2019, 337, 973–982. [Google Scholar] [CrossRef]
42. Louca, S.; Polz, M.F.; Mazel, F.; Albright, M.B.N.; Huber, J.A.; O’Connor, M.I.; Ackermann, M.; Hahn, A.S.; Srivastava, D.S.; Crowe, S.A.; et al. Function and functional redundancy in microbial systems. Nat. Ecol. Evol. 2018, 2, 936–943. [Google Scholar] [CrossRef]
43. Fierer, N.; Bradford, M.A.; Jackson, R.B. Toward an ecological classification of soil bacteria. Ecology 2007, 88, 1354–1364. [Google Scholar] [CrossRef] [PubMed]
44. Manici, L.M.; Caputo, F.; De Sabata, D.; Fornasier, F. The enzyme patterns of Ascomycota and Basidiomycota fungi reveal their different functions in soil. Appl. Soil. Ecol. 2024, 196, 105323. [Google Scholar] [CrossRef]
45. Burns, R.G.; DeForest, J.L.; Marxsen, J.; Sinsabaugh, R.L.; Stromberger, M.E.; Wallenstein, M.D.; Weintraub, M.N.; Zoppini, A. Soil enzymes in a changing environment: Current knowledge and future directions. Soil Biol. Biochem. 2013, 58, 216–234. [Google Scholar] [CrossRef]
46. Li, H.; Yang, S.; Semenov, M.V.; Yao, F.; Ye, J.; Bu, R.; Ma, R.; Lin, J.; Kurganova, I.; Wang, X.; et al. Temperature sensitivity of SOM decomposition is linked with a K-selected microbial community. Glob. Chang. Biol. 2021, 27, 2763–2779. [Google Scholar] [CrossRef]
47. Feng, X.; Wang, S. Plant influences on soil microbial carbon pump efficiency. Glob. Chang. Biol. 2023, 29, 3854–3856. [Google Scholar] [CrossRef]
48. Liang, C.; Zhu, X. The soil microbial carbon pump as a new concept for terrestrial carbon sequestration. Sci. China Earth Sci. 2021, 64, 545–558. [Google Scholar] [CrossRef]
49. Qu, Y.; Tang, J.; Liu, B.; Lyu, H.; Duan, Y.; Yang, Y.; Wang, S.; Li, Z. Rhizosphere enzyme activities and microorganisms drive the transformation of organic and inorganic carbon in saline-alkali soil region. Sci. Rep. 2022, 12, 1314. [Google Scholar] [CrossRef]
50. Lux, S.; Baldauf-Sommerbauer, G.; Siebenhofer, M. Hydrogenation of Inorganic Metal Carbonates: A Review on Its Potential for Carbon Dioxide Utilization and Emission Reduction. ChemSusChem 2018, 11, 3357–3375. [Google Scholar] [CrossRef]
51. Bailey, V.L.; Pries, C.H.; Lajtha, K. What do we know about soil carbon destabilization? Environ. Res. Lett. 2019, 14, 083004. [Google Scholar] [CrossRef]
52. Raza, S.; Miao, N.; Wang, P.; Ju, X.; Chen, Z.; Zhou, J.; Kuzyakov, Y. Dramatic loss of inorganic carbon by nitrogen-induced soil acidification in Chinese croplands. Glob. Chang. Biol. 2020, 26, 3738–3751. [Google Scholar] [CrossRef]
53. Bai, Y.; Cotrufo, M.F. Grassland soil carbon sequestration: Current understanding, challenges, and solutions. Science 2022, 377, 603–608. [Google Scholar] [CrossRef] [PubMed]
54. Liang, G.; Stark, J.; Waring, B.G. Mineral reactivity determines root effects on soil organic carbon. Nat. Commun. 2023, 14, 4962. [Google Scholar] [CrossRef] [PubMed]
55. Xu, X.; Schimel, J.P.; Janssens, I.A.; Song, X.; Song, C.; Yu, G.; Sinsabaugh, R.L.; Tang, D.; Zhang, X.; Thornton, P.E. Global pattern and controls of soil microbial metabolic quotient. Ecol. Monogr. 2017, 87, 429–441. [Google Scholar] [CrossRef]
56. Kallenbach, C.M.; Frey, S.D.; Grandy, A.S. Direct evidence for microbial-derived soil organic matter formation and its ecophysiological controls. Nat. Commun. 2016, 7, 13630. [Google Scholar] [CrossRef] [PubMed]
57. Cui, Y.; Moorhead, D.L.; Guo, X.; Peng, S.; Wang, Y.; Zhang, X.; Fang, L. Stoichiometric models of microbial metabolic limitation in soil systems. Glob. Ecol. Biogeogr. 2021, 30, 2297–2311. [Google Scholar] [CrossRef]
58. Fontaine, S.; Barot, S.; Barre, P.; Bdioui, N.; Mary, B.; Rumpel, C. Stability of organic carbon in deep soil layers controlled by fresh carbon supply. Nature 2007, 450, 277–280. [Google Scholar] [CrossRef]
59. Yan, S.; Yin, L.; Dijkstra, F.A.; Wang, P.; Cheng, W. Priming effect on soil carbon decomposition by root exudate surrogates: A meta-analysis. Soil. Biol. Biochem. 2023, 178, 108955. [Google Scholar] [CrossRef]
60. Kuzyakov, Y. Priming effects: Interactions between living and dead organic matter. Soil. Biol. Biochem. 2010, 42, 1363–1371. [Google Scholar] [CrossRef]
61. Buckeridge, K.M.; Creamer, C.; Whitaker, J. Deconstructing the microbial necromass continuum to inform soil carbon sequestration. Funct. Ecol. 2022, 36, 1396–1410. [Google Scholar] [CrossRef]
62. Lehmann, J.; Kleber, M. The contentious nature of soil organic matter. Nature 2015, 528, 60–68. [Google Scholar] [CrossRef]
63. Chen, L.; Fang, K.; Wei, B.; Qin, S.; Feng, X.; Hu, T.; Ji, C.; Yang, Y. Soil carbon persistence governed by plant input and mineral protection at regional and global scales. Ecol. Lett. 2021, 24, 1018–1028. [Google Scholar] [CrossRef] [PubMed]
64. Dijkstra, F.A.; Zhu, B.; Cheng, W. Root effects on soil organic carbon: A double-edged sword. New Phytol. 2021, 230, 60–65. [Google Scholar] [CrossRef] [PubMed]
65. Ren, C.; Wang, T.; Xu, Y.; Deng, J.; Zhao, F.; Yang, G.; Han, X.; Feng, Y.; Ren, G. Differential soil microbial community responses to the linkage of soil organic carbon fractions with respiration across land-use changes. For. Ecol. Manag. 2018, 409, 170–178. [Google Scholar] [CrossRef]
66. Wang, C.; Kuzyakov, Y. Mechanisms and implications of bacterial–fungal competition for soil resources. ISME J. 2024, 18, wrae073. [Google Scholar] [CrossRef] [PubMed]
Shu Q, Gao S, Liu X, Yao Z, Wu H, Qi L, Zhang X. Soil Enzyme Activities and Microbial Carbon Pump Promote Carbon Storage by Influencing Bacterial Communities Under Nitrogen-Rich Conditions in Tea Plantation. Agriculture. 2025; 15(3):238. https://doi.org/10.3390/agriculture15030238
Перевод статьи «Soil Enzyme Activities and Microbial Carbon Pump Promote Carbon Storage by Influencing Bacterial Communities Under Nitrogen-Rich Conditions in Tea Plantation» авторов Shu Q, Gao S, Liu X, Yao Z, Wu H, Qi L, Zhang X., оригинал доступен по ссылке. Лицензия: CC BY. Изменения: переведено на русский язык
Фото: freepik
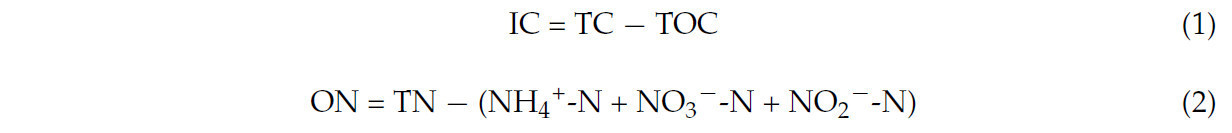
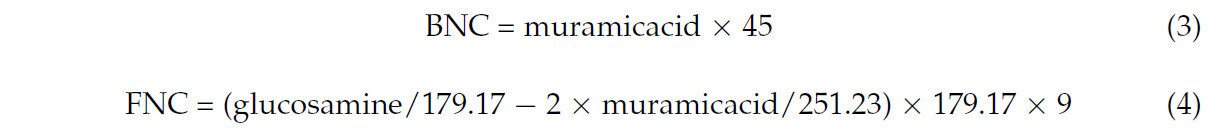













































































































Комментарии (0)