Больше различий внутри, чем между сортами: генетика итальянского и пастбищного райграса в Корее
Итальянский райграс (Lolium multiflorum, IRG) и райграс пастбищный (Lolium perenne L., PRG) широко культивируются в Корее в качестве кормовых злаков с использованием методов гетерогенного и поликросс-размножения, которые способствуют поддержанию генетического разнообразия внутри сортов. Однако закономерности их генетического разнообразия в Корее остаются малоизученными. В данном исследовании оценивалось генетическое разнообразие IRG (восемь сортов, включая один экзотический) и PRG (два экзотических сорта) с использованием 66 маркеров простых последовательностных повторов (SSR).
Аннотация
В 87 образцах (девять сортов IRG и два сорта PRG) было идентифицировано 655 аллелей, в среднем 9,9 на локус. Ключевые генетические параметры включали: гетерозиготность (0,399), наблюдаемую гетерозиготность (0,675), индекс фиксации (0,4344) и полиморфный информационный контент (0,6428). Наименьшее внутрисортовое генетическое расстояние наблюдалось у сорта «Hwasan 104ho» (0,469), тогда как наибольшее — у сорта «IR901» (0,571). Среди сортов наименьшее генетическое расстояние было между «Greencall» и «Greencall 2ho» (0,542), а наибольшее — между «Kowinmaster» и «Aspire» (0,692). Анализ молекулярной дисперсии показал 90% изменчивости внутри сортов и 10% — между сортами. Было выделено пять кластеров (I–V), причем кластер I включал в основном диплоидные сорта IRG и тетраплоидный сорт «Hwasan 104ho». Структурный анализ позволил дифференцировать диплоидные и тетраплоидные сорта (K = 2) и далее разделить тетраплоидные IRG и PRG (K = 3). Анализ главных компонент подтвердил эти группировки: наименьшее генетическое расстояние наблюдалось между «Greencall» и «Greencall 2ho» (0,227), а наибольшее — между «Greencall» и «Aspire» (0,384). Полученные результаты служат основой для маркер-ориентированной селекции, направленной на улучшение хозяйственно ценных признаков и повышение эффективности программ селекции райграса.
1. Введение
Итальянский райграс (Lolium multiflorum; IRG), принадлежащий к семейству злаковых (Poaceae), является одним из многих однолетних кормовых злаков, культивируемых в Корее в зимний период [1]. Родом из прибрежного региона Средиземноморья, в частности Италии, IRG представляет собой верховой злак с отчетливыми жилками листьев и поверхностным блеском с обратной стороны. Преимущественно произрастая в теплом климате, IRG демонстрирует высокую волокнистую поедаемость, устойчивость к переувлажнению и способность к регенерации. Тем не менее, он восприимчив к летней депрессии [2,3]. В Корее было выведено 20 сортов IRG, причем к рекомендуемым местным сортам относятся Kowinearly, Greenfarm и Kowinmaster, а к рекомендуемым иностранным сортам — такие сорта, как Florida80 и Tetraflorum [4,5]. Кроме того, райграс пастбищный (Lolium perenne; PRG), также представитель семейства злаковых (Poaceae), является одним из нескольких многолетних кормовых видов, культивируемых в Европе [6]. PRG имеет сходные морфологические признаки с IRG, такие как высота и плоские блестящие листья. Однако усилия по улучшению сортов PRG ограничены невысоким разнообразием внутри его сортов, которое может быть использовано для селекции в корейских условиях возделывания. В настоящее время исследования по селекции и культивированию сортов IRG в основном сконцентрированы в Корее, где IRG часто используется в двойных системах севооборота с рисом. Напротив, PRG не получил широкого распространения в селекции в Корее и в основном используется для создания смешанных пастбищ. Среди рекомендуемых иностранных сортов PRG — Reville и Bastion [5].
Молекулярные маркеры на основе ДНК предлагают несколько преимуществ, включая независимость от влияния окружающей среды и способность обеспечивать объективную оценку генетического разнообразия и родства. В случае IRG в молекулярных исследованиях использовались AFLP, RFLP, SSR и STS для оценки генетического разнообразия как внутри сортов, так и среди диких видов [7,8,9,10]. Аналогично, исследования PRG применяли AFLP [11], анализ SNP [12] и методологии RFLP, STS и SSR [13,14,15,16,17,18]. Более того, SSR-маркеры, характеризующиеся кодоминантной природой, множественностью аллелей и высокими значениями PIC, в первую очередь использовались для различения сортов и оценки генетического разнообразия и пластичности генетических ресурсов [19,20,21,22,23,24]. Кроме того, недавно было идентифицировано значительное количество EST, и исследования с использованием EST-SSR маркеров были проведены для различных видов или родов в пределах нескольких зерновых культур [25,26,27,28,29]. В частности, поскольку EST-SSR маркеры эволюционно консервативны, они обладают потенциалом для генетического переноса между вовлеченными видами [30].
Понимание обилия и распределения генетического разнообразия имеет ключевое значение, поскольку они влияют на эволюционный потенциал видов [31]. SSR-маркеры предлагают доступный и практичный метод, не требующий дорогостоящего оборудования. Ранее было проведено несколько исследований на пастбищных и поликросс-сортах [2,32,33,34]. Тем не менее, исследований, подтверждающих генетическое разнообразие внутри сортов, недостаточно. В этом исследовании 87 образцов, включающих девять сортов IRG и два сорта PRG, были проанализированы с использованием 66 полиморфных SSR-маркеров. Исследование было направлено на определение распределения генетического разнообразия как внутри отдельных сортов, так и между сортами. В конечном итоге, результаты этого исследования облегчают создание сортов, демонстрирующих превосходное развитие по сравнению с их родителями, посредством поликросса и гетерозисной селекции. Полученные результаты предоставляют базу данных, которая ускорит процесс селекции и улучшит экономические результаты, одновременно способствуя развитию сортов в будущем.
2. Материалы и методы
2.1. Растительный материал
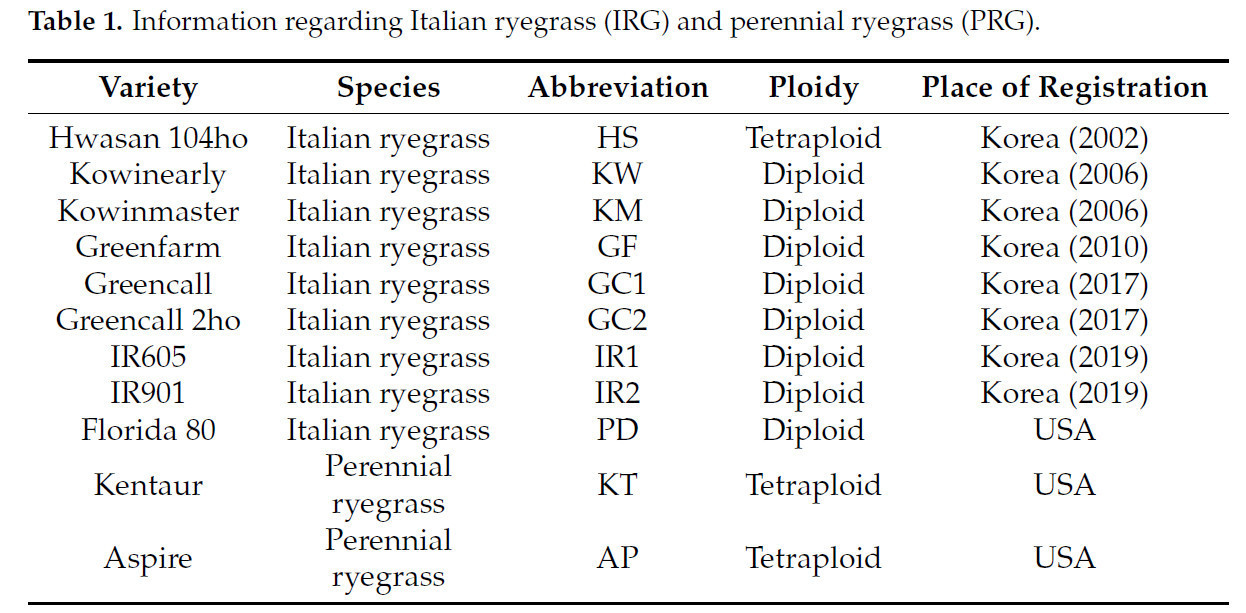
Это исследование оценивает генетическое разнообразие восьми сортов IRG (Hwasan 104ho, Kowinearly, Kowinmaster, Greenfarm, Greencall, Greencall 2ho, IR605 и IR901), одного экзотического сорта IRG (Florida 80) и двух сортов райграса пастбищного (Kentaur и Aspire). Все семена были предоставлены Национальным институтом животноводства (Чонджу, Республика Корея), за исключением Aspire, который был получен от Samoeco (Соннам, Республика Корея). Два сорта PRG были включены в этот анализ, поскольку они привлекают внимание корейской животноводческой промышленности. Это было сделано для лучшего понимания генетического родства между IRG и PRG. Тридцать два семени каждого сорта были выращены в высокотехнологичной теплице Университета Чхунбук для сравнения фенотипов. Из каждого сорта было отобрано восемь особей для анализа (за исключением Aspire, который включал семь особей) на основе наблюдаемых различий (Таблица 1).
Таблица 1. Информация об итальянском райграсе (IRG) и райграсе пастбищном (PRG).
2.2. Выделение ДНК
Растения культивировали в течение 60 дней, отбирали и пробовали молодые ярко-зеленые листья. Впоследствии эти образцы измельчали в жидком азоте и обрабатывали в соответствии с протоколами, описанными в наборе DNeasy® Plant Mini Kit (Qiagen, Хильден, Германия). ДНК, выделенная из образцов, была количественно оценена в 10 нг/мкл с использованием спектрофотометра NanoDrop One C (Thermo Fisher Scientific, Уолтем, MA, США).
2.3. Выбор SSR-маркеров и анализ разнообразия
ПЦР-амплификацию проводили с использованием системы AllInOneCycle™ PCR (Bioneer Corp., Тэджон, Республика Корея). Общий объем реакционной смеси составлял 10 мкл, включая 1 мкл ДНК концентрацией 10 нг/мкл, 5 мкл GoTaq Green Master Mix (Promega, Мэдисон, WI, США) и 2 мкл прямого и обратного праймеров концентрацией 10 пмоль/мкл каждый. Используемые маркеры были произведены компанией Bioneer Company (Тэджон, Республика Корея). ПЦР начинали с денатурации при 95 °C в течение 9 мин, с последующими 34 циклами в следующих условиях: денатурация при 95 °C в течение 30 с, отжиг при 50–60 °C в течение 30 с и элонгация при 72 °C в течение 1 мин. Заключительная элонгация при 72 °C в течение 7 мин завершала процесс. Электрофорез проводили при 150 В в течение 50 мин с использованием 2,5% агарозного геля, приготовленного с Tris-ацетат-EDTA (TAE) буфером на основе выбранных маркеров. Впоследствии EtBr (бромистый этидий) добавляли в емкость с TAE буфером, и агарозный гель окрашивали в течение 10 мин. Затем гель подвергали УФ-облучению с помощью системы цифровой визуализации GDS-200D (Korea Lab Tech, Соннам, Республика Корея) для подтверждения картины полос. Для более точного определения размеров в парах оснований (bp) выбранные маркеры были проанализированы с использованием 96-капиллярного автоматического анализатора фрагментов ДНК (Fragment Analyzer™ 96, Advanced Analytical Technologies, Inc., Эймс, IA, США). Необходимые материалы для этого анализа включали FA dsDNA гель, 5 × 930 dsDNA входной буфер, буфер для разведения 1× TE, вставляющийся краситель, маркеры, ДНК-лестницу (с фрагментами 35, 75, 100, 150, 200, 250, 300, 400 и 500 bp), 5 × раствор для кондиционирования капилляров, раствор для хранения капилляров и минеральное масло. База данных была создана на основе только полос в диапазоне 35–500 bp, а анализ был выполнен с использованием программного обеспечения PROSize™ 3.0 (Advanced Analytical Technologies, Inc., Анкени, IA, США).
2.4. Анализ данных
Генетическое расстояние было проанализировано с использованием метода [35], реализованного в программном обеспечении power marker, и полученные данные были использованы для построения дендрограммы UPGMA с применением генетического расстояния Nei в MEGA 4.0 [35,36]. Генетическое сходство было определено на основе коэффициента простого соответствия (SM) Rohlf с использованием программного обеспечения NTSYSpc вер. 2.1, где аллели обозначались как «1» или «0» в зависимости от их наличия или отсутствия [37]. Отобранные SSR использовались для расчета среднего числа аллелей (Na), среднего эффективного числа аллелей (Ne), наблюдаемой гетерозиготности (Ho), ожидаемой гетерозиготности (He), индекса фиксации (FST) и частных аллелей (PA), а также AMOVA для оценки значимости генетической вариации внутри и между особями с использованием пакета анализа GenAlEx вер. 6.5 [35]. Программа STRUCTURE вер. 2.3.4 была использована для обнаружения потенциальных субпопуляций (K = 1 до K = 15) с использованием модели, допускающей примесь и коррелированные частоты аллелей. Этот анализ включал прогрев в 100 000 итераций и длину прогона в 100 000, после чего было выполнено 20 итераций [36]. Оптимальное количество популяций соответствовало наибольшему значению на k-графике [38]. Стратегия объединения (bulk strategy) была реализована с восемью особями на группу (за исключением Aspire, у которого было семь особей), чтобы определить генетическое расстояние между группами. Стратегия объединения включала выделение ДНК из индивидуальных образцов и ее разведение до 10 нг/мкл с использованием спектрофотометра NanoDrop (Thermo Fisher Scientific, Уолтем, MA, США). Условия ПЦР (Bioneer Corporation, Тэджон, Республика Корея) были идентичны ранее описанным, при этом мы использовали 60 маркеров для каждого образца ДНК. Соответственно, каждый образец ДНК был разделен на 60 аликвот, и в каждую аликвоту для ПЦР-амплификации добавляли один маркер. Точные длины в парах оснований (bp) были определены с использованием 96-капиллярного автоматического анализатора фрагментов ДНК (Fragment Analyzer™ 96, Advanced Analytical Technologies, Inc., Эймс, IA, США). Наличие или отсутствие фрагментов ДНК в индивидуальных ПЦР-образцах регистрировали как «1» для четкой полосы и «0» для отсутствия полосы. Эти бинарные значения от восьми образцов на сорт были сгруппированы по сортам для дальнейшего анализа. Кроме того, стратегия объединения использовалась совместно с программным обеспечением NTSYSpc вер. 2.1 [39] и GenAlEx вер. 6.51 [40] для построения дендрограмм UPGMA и анализа главных координат (PCoA) в 2D и 3D моделях (т.е. с «1», представляющей идентичную полосу, и «0», представляющей отсутствующую или отличающуюся полосу) [39].
3. Результаты
3.1. Полиморфизм SSR-локусов
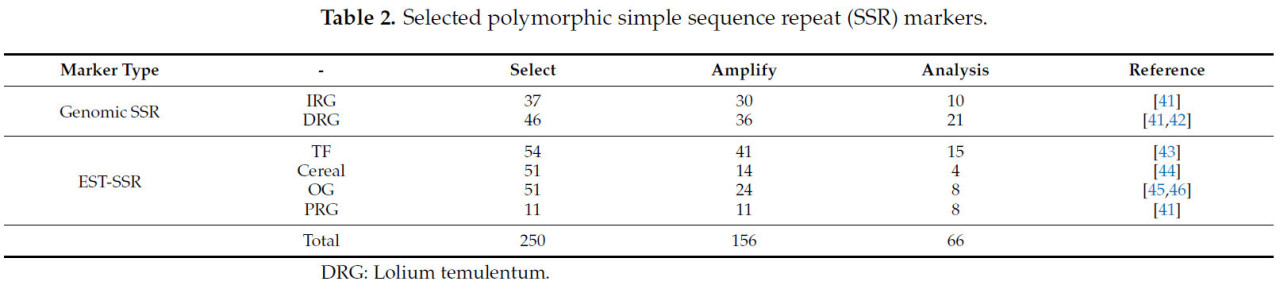
Полиморфизм 250 маркеров был подтвержден на 2,5% агарозном геле, на что указывали высокие значения PIC в анализе генетического разнообразия. Источники маркеров и их детали суммированы в Таблице 2. В частности, 66 маркеров (включая 31 геномный SSR и 35 EST-SSR) были выбраны на основе их четких полос и полиморфизма, наблюдаемых в агарозном геле (Таблица 3). В общей сложности 11 сортов Lolium (87 особей) были проанализированы с использованием 66 маркеров (35 EST-SSR маркеров и 31 геномного SSR маркера), что привело к обнаружению 655 аллелей, в среднем 9,9 аллелей на маркер (Таблица S1). Средние значения наблюдаемой гетерозиготности, ожидаемой гетерозиготности и индекса фиксации (FST) были зафиксированы на уровнях 0,399, 0,675 и 0,4344 соответственно. Значения PIC варьировались от 0,0742 (NFFA142) до 0,8721 (LMgSSR10-10C), со средним значением 0,6428 (Рисунок S1a, Таблица 4). Число аллелей варьировалось от 2 (для маркеров NFFA100 и NFFA142) до 22 (для LMgSSR10-10C), причем большинство значений PIC попадало в диапазон между 0,7 и 0,8 (Рисунок S1b).
Таблица 2. Отобранные полиморфные маркеры простых последовательностных повторов (SSR).
Таблица 3. Маркеры, использованные для SSR-анализа IRG и PRG.
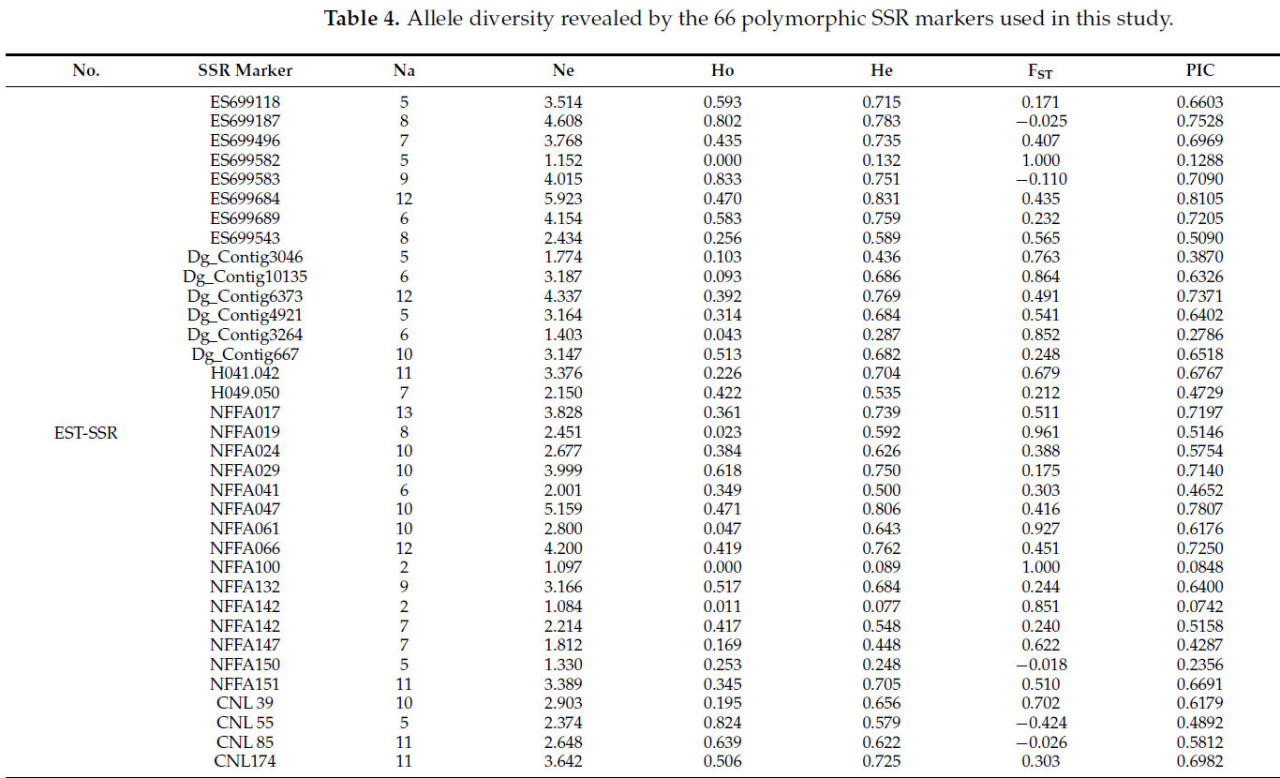
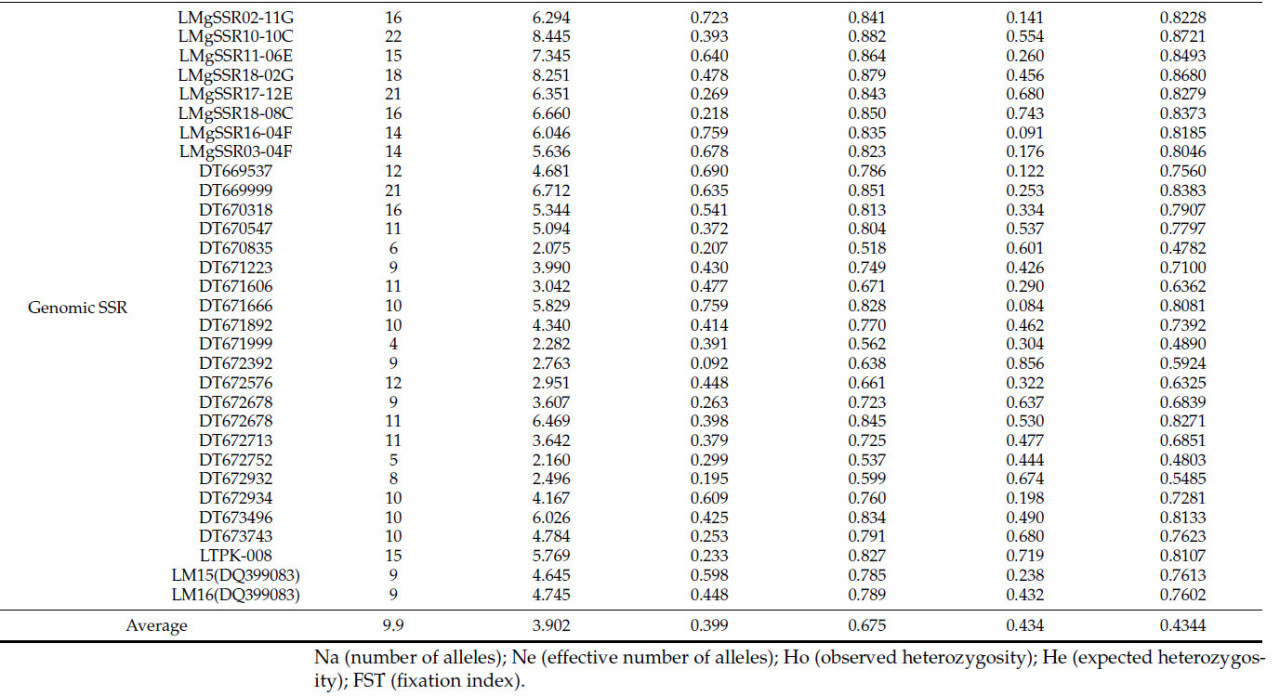
Таблица 4. Аллельное разнообразие, выявленное с помощью 66 полиморфных SSR-маркеров, использованных в этом исследовании.
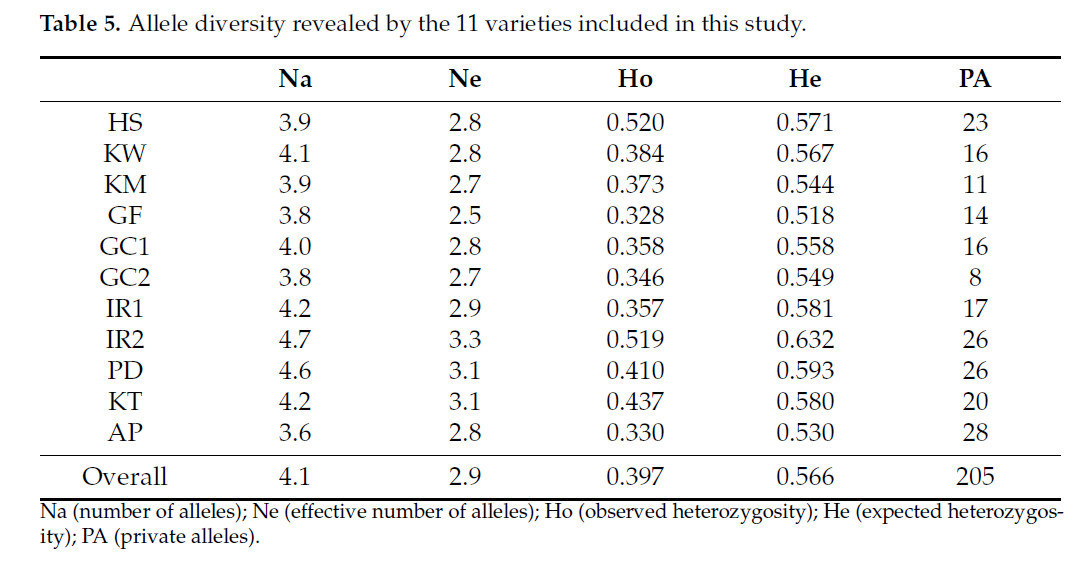
В случае EST-SSR маркеров было идентифицировано 281 аллель, в среднем 8,0 аллелей на маркер. Наблюдаемая гетерозиготность, ожидаемая гетерозиготность и индекс фиксации (FST) были зафиксированы как 0,361, 0,597 и 0,442 соответственно. Значения PIC варьировались от 0,0742 (NFFA142) до 0,8105 (для ES699684), со средним значением PIC 0,5603 (Рисунок S2a, Таблица 4). Число аллелей варьировалось от двух (NFFA100, NFFA142) до тринадцати (NFFA017), причем большинство значений PIC попадало в диапазон между 0,6 и 0,7 (Рисунок S2b, Таблица S1). Для геномных SSR было идентифицировано 374 аллеля, в среднем 12,1 аллелей на маркер. Наблюдаемая гетерозиготность, ожидаемая гетерозиготность и индекс фиксации (FST) были зафиксированы как 0,442, 0,764 и 0,426 соответственно. Значения PIC варьировались от 0,4782 (для DT670835) до 0,8721 (для LMgSSR10-10C), со средним значением PIC 0,7359 (Рисунок S3a, Таблица 4). Число аллелей варьировалось от 4 для маркеров (NFFA100 и NFFA142) до 22 (для NFFA017), причем большинство значений PIC попадало в диапазон между 0,8 и 0,9 (Рисунок S3b, Таблица S1). При анализе сортов среднее число аллелей (Na) составило 4,1, среднее эффективное число аллелей (Ne) — 2,9, средняя наблюдаемая гетерозиготность — 0,566, а среднее число частных аллелей — 205 (Таблица 5).
Таблица 5. Аллельное разнообразие, выявленное для 11 сортов, включенных в это исследование.
3.2. Генетическое разнообразие и кластерный анализ
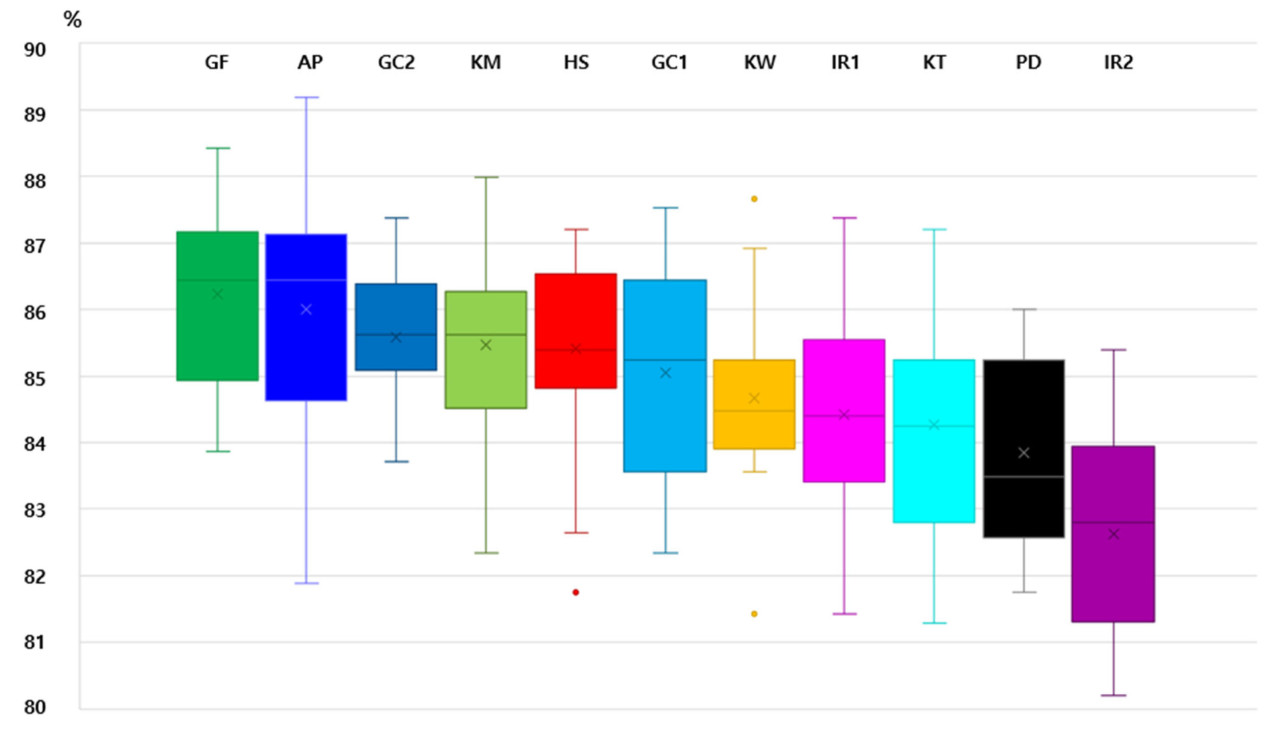
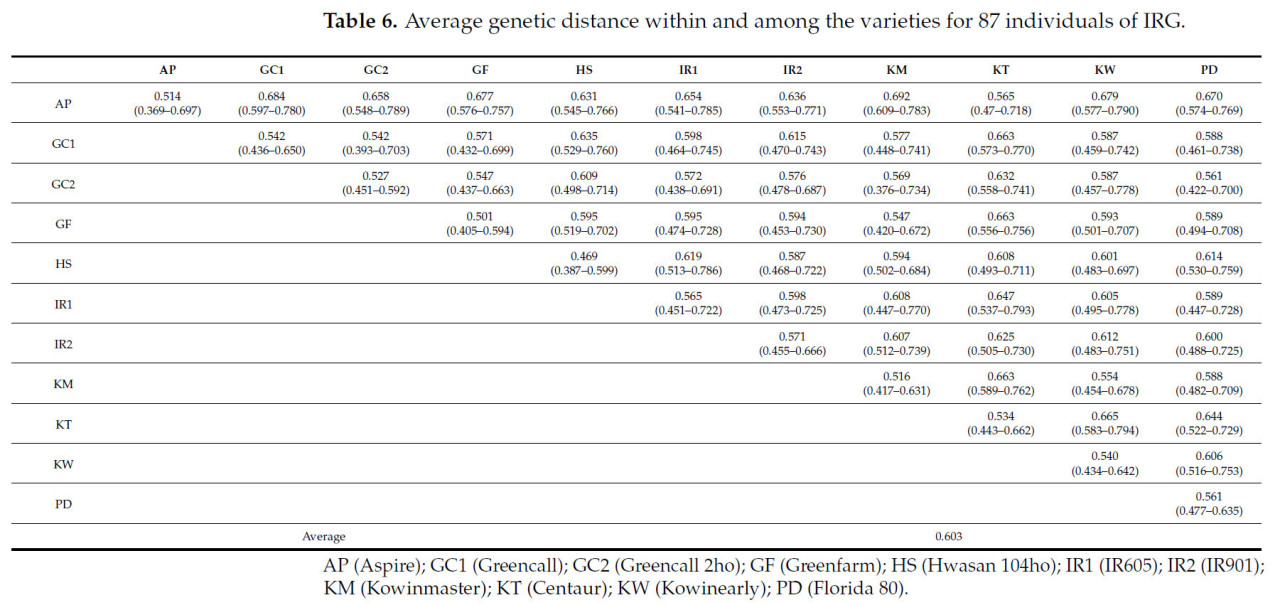
Аллели, полученные от 87 особей и 66 SSR-маркеров, были использованы для изучения генетического разнообразия и сходства внутри и между сортами (Таблица S2). Внутри сортов наименьшее генетическое расстояние наблюдалось у Hwasan 104ho (Таблица 6), со средним значением 0,469 и максимальным различием 0,212 (Таблица 6 и Таблица S3). И наоборот, наибольшее генетическое разнообразие было обнаружено у IR901 (Таблица 6), со средним значением 0,571 и максимальным различием 0,211 (Таблица 6 и Таблица S3). Что касается генетического разнообразия между сортами, Greencall и Greencall 2ho продемонстрировали наибольшее сходство (Таблица 6), со средним значением 0,542 и максимальным различием 0,310. Напротив, Kowinmaster (диплоидный корейский сорт) и Aspire (тетраплоидный импортный сорт из США) показали, как и ожидалось, наибольшее генетическое разнообразие между сортами, со средним значением 0,692 и максимальным различием 0,174 (Таблица 6). Генетическое расстояние между особями было наименьшим у AP-1 и AP-7 — 0,361, и наибольшим у KW-3 и KT-4 — 0,7945, со средним расстоянием 0,603 по всем 87 особям (Таблица S2). Генетическое сходство варьировалось от 80% до 90%, причем Greenfarm демонстрировал наибольшее сходство (86,45 ± 2,28%), а IR901 — наименьшее (82,80 ± 2,59%) в пределах своих сортов (Рисунок 1).
Рисунок 1. Блочная диаграмма генетического сходства (ось y) внутри сортов (87 особей). Прямая линия (-) внутри блока указывает на медиану, а отметка «X» внутри квадрата обозначает среднее значение (%). Точки представляют собой выбросы. GF (Greenfarm); AP (Aspire); GC2 (Greencall 2ho); KM (Kowinmaster); HS (Hwasan 104ho); GC1 (Greencall); KW (Kowinearly); IR1 (IR605); KT (Kentaur); PD (Florida 80); IR2 (IR901).
Таблица 6. Среднее генетическое расстояние внутри и между сортами для 87 особей IRG.
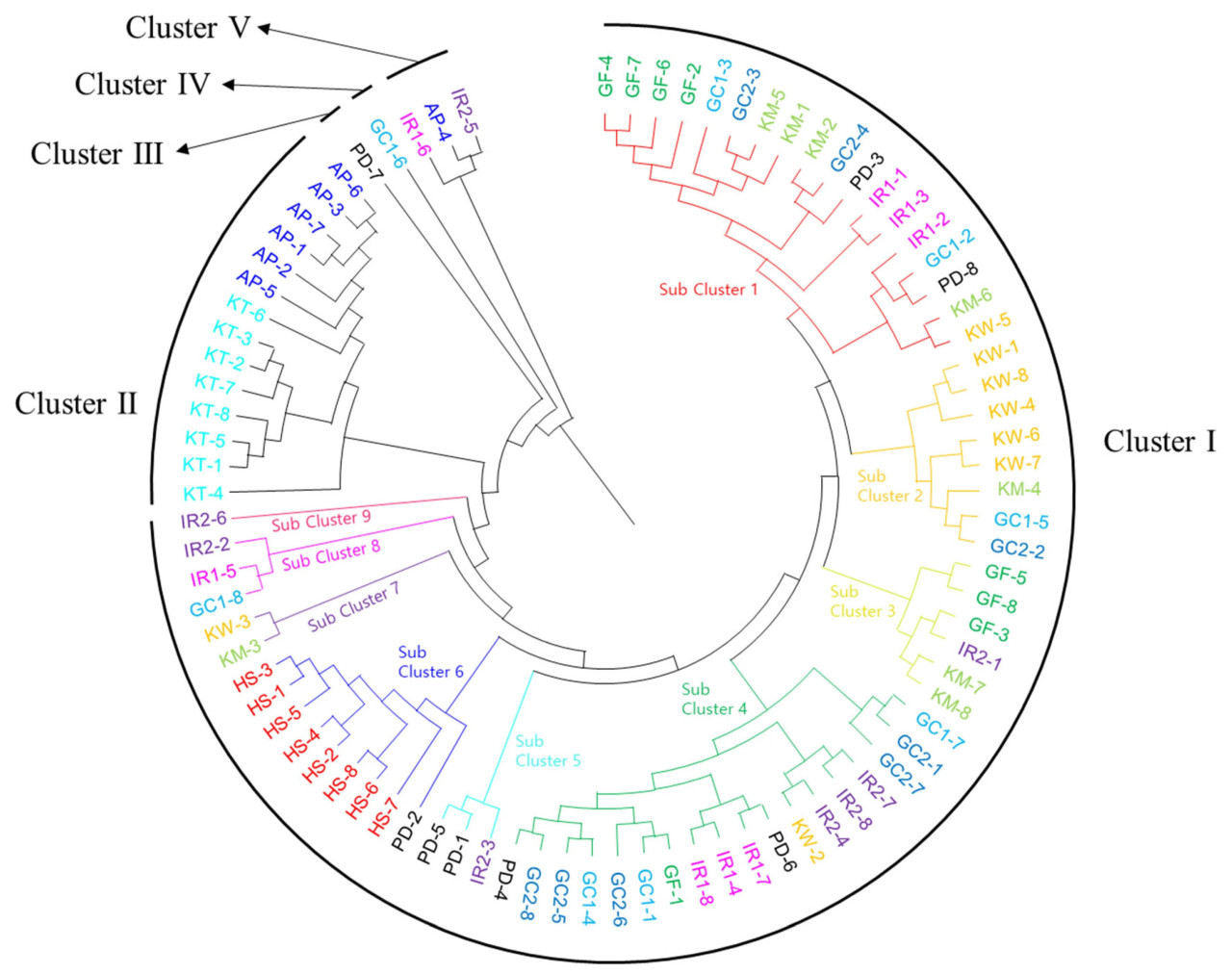
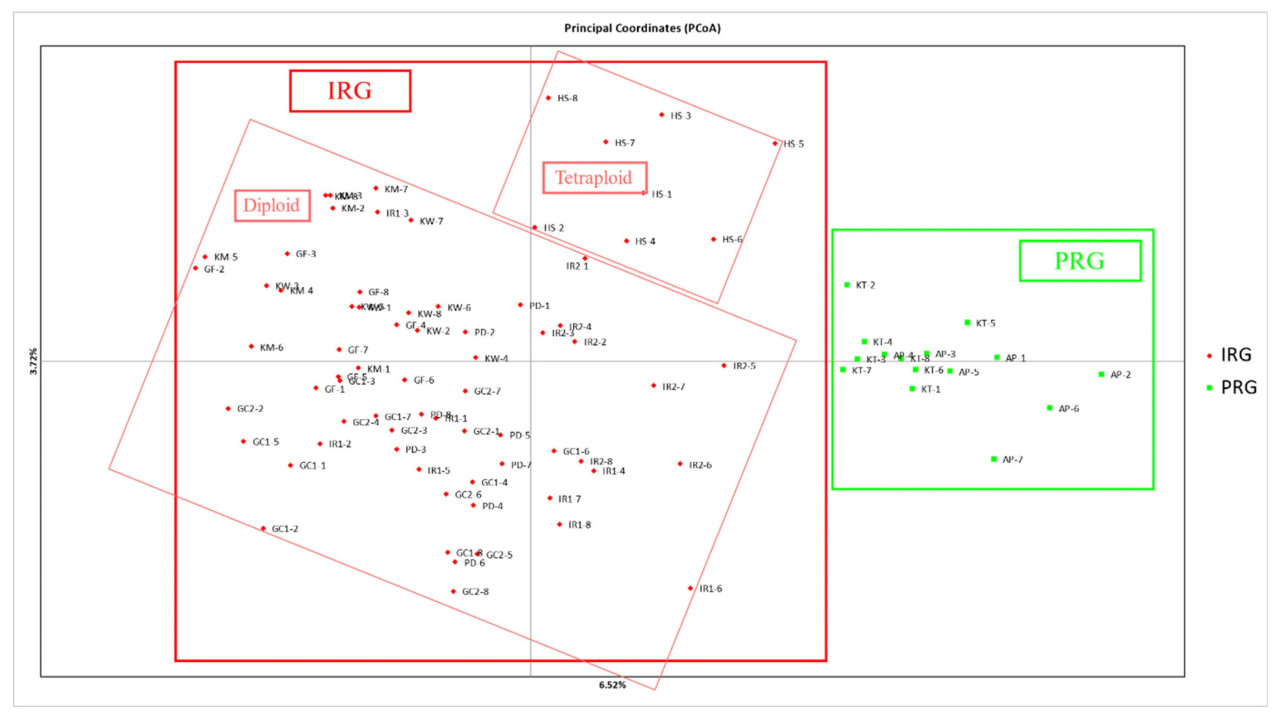
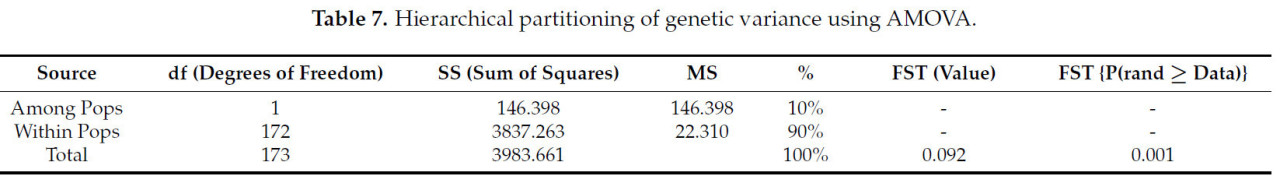
Был проведен AMOVA для изучения распределения генетической дифференциации внутри и между сортами IRG. Результаты AMOVA показали, что 90% вариации приходится на группы, тогда как 10% — между группами (Таблица 7). Значение FST и p-value показали, что небольшая генетическая разница между двумя популяциями была статистически значимой. Идентичные результаты были получены при индивидуальном анализе каждого типа маркеров (EST-SSR, геномный SSR) (Таблицы S4 и S5). Был проведен кластерный анализ для выявления генетической вариации внутри сортов и построения дендрограмм (Рисунок 2). Эти кластеры, созданные с использованием генетического расстояния Nei для 87 особей, позволили нам выделить пять различных групп. Кластеры I, III, IV и V включали сорта IRG, тогда как кластер II включал исключительно сорта PRG (Таблица S6). В основном диплоидные сорта были включены в кластер I. Однако тетраплоидный сорт IRG «Hwasan 104ho» также можно было отличить наряду с диплоидными сортами (Рисунок 2, Таблица S7). Кластеры III, IV и V состояли из четырех сортов IRG, которые считаются неизвестными выбросами. Сорта IRG и PRG являются разными видами, и эта дифференциация сохранялась даже при раздельном анализе EST-SSR и геномных SSR-маркеров (Рисунки S4 и S5). В 2D PCoA генетических расстояний, определенных с использованием базы данных, вариация, объясняемая первыми двумя осями, составила 6,52% и 3,72%, что в совокупности составляет 10,24% от общей вариации (Рисунок 3). Сорта IRG были преимущественно представлены красным цветом, тогда как сорта PRG — зеленым, что облегчает классификацию видов. Наш 2D PCoA 87 образцов разделил их на группы IRG и PRG, тем самым позволив дальнейшее подразделение на диплоидные и тетраплоидные сорта. Было обнаружено отчетливое разделение между Kowinmaster, Florida 80 и IR901 при исследовании отдельных областей. Кроме того, Kowinearly и IR605 были включены во все области, занятые другими диплоидными сортами IRG (Рисунок S6).
Рисунок 2. Филогенетическое дерево, построенное с использованием метода невзвешенного попарного группового среднего (UPGMA), с применением данных 66 SSR-маркеров по 87 отдельным особям сортов IRG. AP (Aspire); GC1 (Greencall); GC2 (Greencall 2ho); GF (Greenfarm); HS (Hwasan 104ho); IR1 (IR605); IR2 (IR901); KM (Kowinmaster); KT (Kentaur); KW (Kowinearly); PD (Florida 80).
Рисунок 3. График 2D модели анализа главных координат (PCoA), использующий исключительно геномные SSR-маркеры для отдельных растений следующих сортов Lolium: AP (Aspire), GC1 (Greencall), GC2 (Greencall 2ho), GF (Greenfarm), HS (Hwasan 104ho), IR1 (IR605), IR2 (IR901), KM (Kowinmaster), KT (Kentaur), KW (Kowinearly) и PD (Florida 80). Анализ был проведен на основе измерений среднего генетического расстояния. Первые три главные координаты объясняют 6,52%, 3,72% и 2,87% вариации соответственно.
Таблица 7. Иерархическое разделение генетической дисперсии с использованием AMOVA.
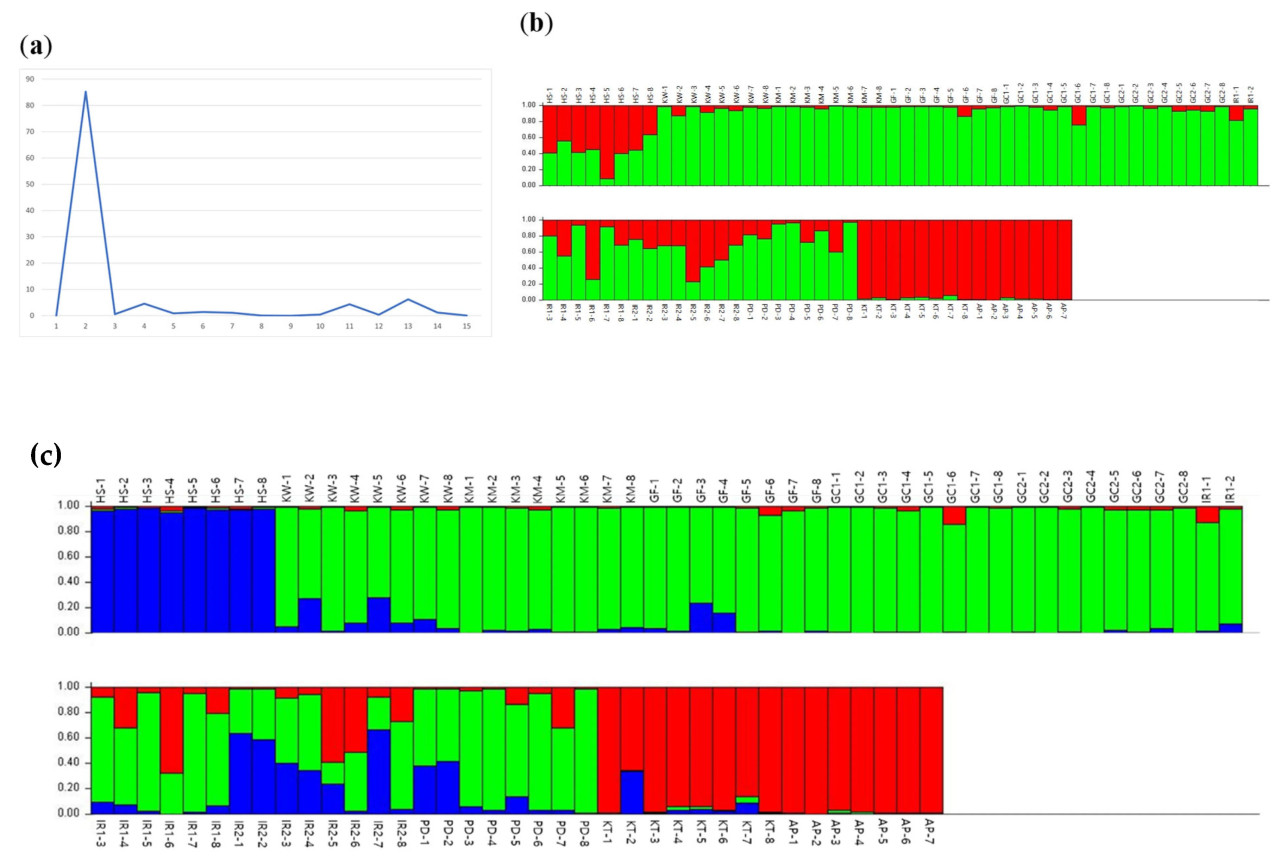
Популяционная структура 87 особей, представляющих девять сортов IRG и два сорта PRG, была определена с использованием STRUCTURE v2.3.3 на основе всех 66 SSR-маркеров. Мы вычислили ΔK для определения оптимального значения K в диапазоне от K = 1 до K = 15. Поскольку в этом исследовании использовались сорта Lolium, наибольшее значение ΔK было идентифицировано при «K = 2» (Рисунок 4a). Следовательно, были выделены две основные субпопуляции, Pop 1 и Pop 2, имеющие наибольшее значение ΔK. Эти субпопуляции в основном классифицировали особи IRG и PRG в соответствии с их диплоидными или тетраплоидными характеристиками. Pop 1 (изображен красным на Рисунке 4b) состоял из 24 особей, тогда как Pop 2 (изображен зеленым на Рисунке 4b) включал 63 особи, все из которых были корейского происхождения. Отчетливая дифференциация между тетраплоидным IRG и PRG появилась при «K = 3» (Рисунок 4c). Особи, отнесенные к голубой категории, были представлены сортом Hwasan 104ho, тогда как особи, отнесенные к красной категории, в основном включали сорта Kentaur и Aspire.
Рисунок 4. (a) Значения ΔK, где модальное значение указывает на истинное K (K = 2). (b) Принадлежность на основе модели девяти сортов IRG и двух сортов PRG, определенная с использованием STRUCTURE. Цвета обозначают субпопуляции на основе модели: красный — Pop 1; зеленый — Pop 2. (c) Принадлежность на основе модели девяти сортов IRG и двух сортов PRG, определенная с использованием STRUCTURE. Цвета представляют субпопуляции на основе модели: голубой — Pop 1; зеленый — Pop 2; красный — Pop 3.
3.3. Стратегия объединения (bulk strategy), примененная для кластерной оценки генетического разнообразия по сортам
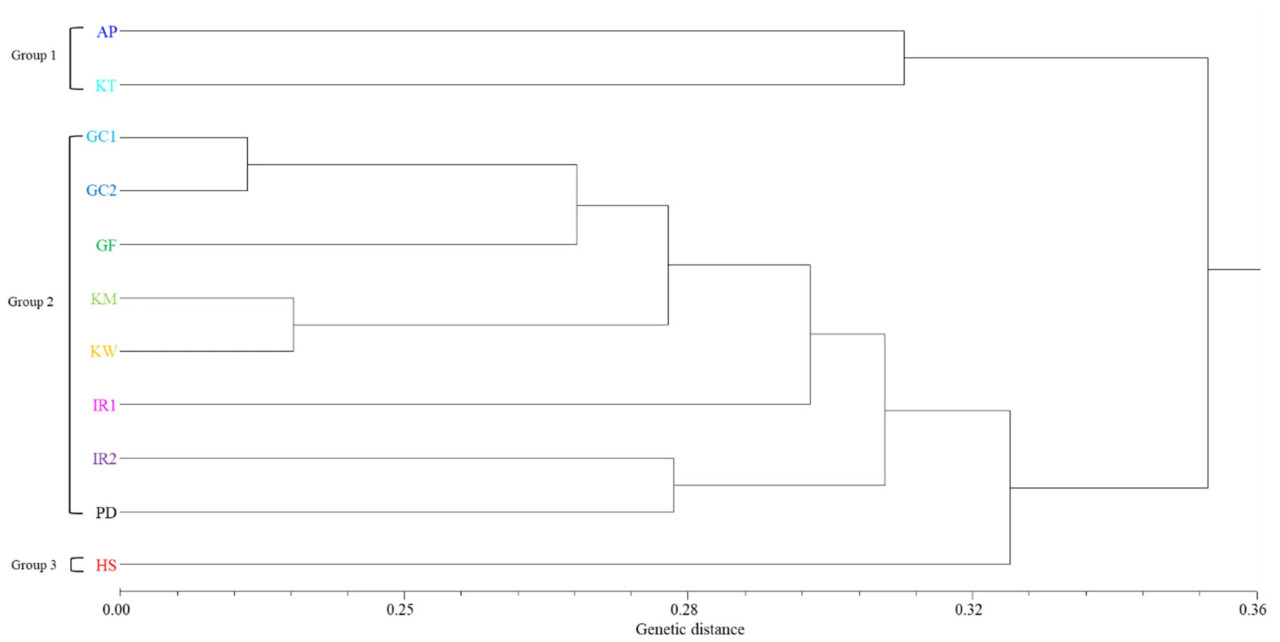
Стратегия объединения требует группы особей одного сорта. Филогенетическое дерево UPGMA было сгенерировано с использованием генетических расстояний, определенных с помощью стратегии объединения. «Greencall» и «Greencall 2ho» были наиболее близкими сортами со средним генетическим расстоянием 0,227, в то время как «Greencall» и «Aspire» демонстрировали наибольшее расстояние со средним значением 0,384 (Рисунок 5 и Рисунок 6, Таблица S8). Дендрограмма, полученная с помощью стратегии объединения, дала результаты, согласующиеся с результатами структурного анализа при K = 3. В частности, Группа 1 включала сорта PRG (Aspire, Kentaur), Группа 2 состояла из диплоидных сортов IRG, а Группа 3 включала тетраплоидные сорта IRG. Кроме того, согласованные результаты были получены при раздельном анализе каждого типа маркеров, при этом сорта разделились на три отдельные группы (EST-SSR, геномный SSR) (Рисунки S7 и S8). В 3D PCoA первые три главные координаты объясняли 16,6%, 11,9% и 11,4% общей вариации соответственно, что в сумме составило 39,9%. Эти результаты соответствовали результатам структурного анализа (Рисунок 6). Аналогичные результаты были получены при выполнении 3D PCoA для каждого типа маркеров (EST-SSR, геномный SSR; Рисунки S9 и S10). Кроме того, при использовании только EST-SSR маркера наименьшее генетическое расстояние наблюдалось между Kowinmaster и Kowinearly — 0,221, тогда как наибольшее расстояние было отмечено между Hwasan 104ho и Greencall — 0,388 (Таблица S8). При использовании только геномного SSR маркера наименьшее генетическое расстояние наблюдалось между Greencall и Greencall 2ho — 0,223, тогда как наибольшее расстояние было отмечено между Greenfarm и Aspire — 0,436 (Таблица S9).
Рисунок 5. Филогенетическое дерево UPGMA для объединенных образцов сортов IRG и PRG: AP (Aspire), GC1 (Greencall), GC2 (Greencall 2ho), GF (Greenfarm), HS (Hwasan 104ho), IR1 (IR605), IR2 (IR901), KM (Kowinmaster), KT (Kentaur), KW (Kowinearly) и PD (Florida 80). Это дерево было построено на основе измерений среднего генетического расстояния.
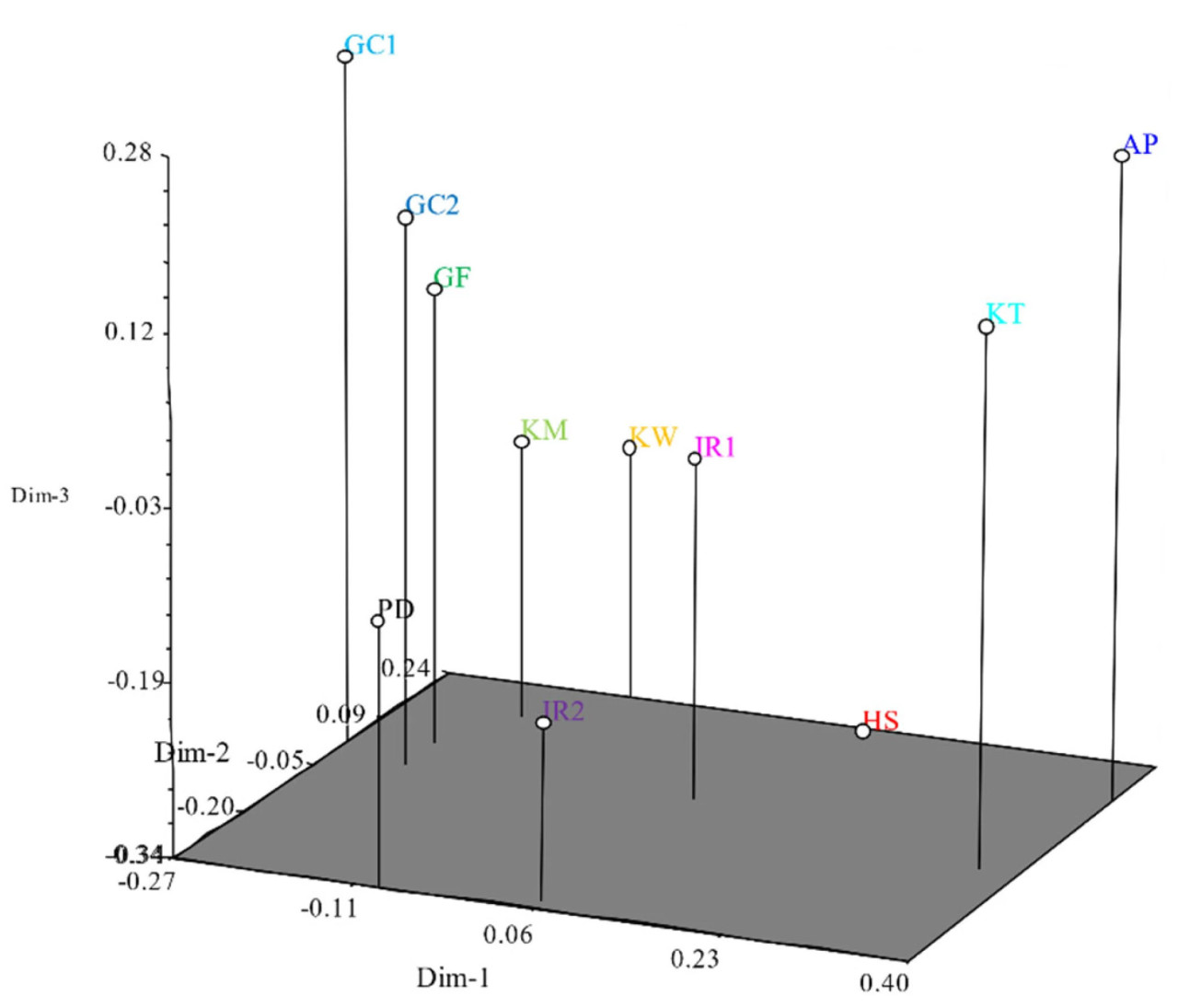
Рисунок 6. График 3D модели, использованной в анализе главных компонент (PCoA) для отдельных растений сортов IRG и PRG: AP (Aspire), GC1 (Greencall), GC2 (Greencall 2ho), GF (Greenfarm), HS (Hwasan 104ho), IR1 (IR605), IR2 (IR901), KM (Kowinmaster), KT (Kentaur), KW (Kowinearly) и PD (Florida 80). Этот анализ был проведен с использованием измерений среднего генетического расстояния. Примечательно, что первые три главные координаты объясняют 16,6%, 11,9% и 11,4% вариации соответственно.
4. Обсуждение
Морфологические признаки традиционно использовались для характеристики и различения сортов растений. Однако этот метод может оказаться неточным из-за различий в условиях произрастания в разных регионах, что делает его неэффективным, трудоемким и дорогостоящим [47]. За последние два десятилетия молекулярные маркеры и агрономические признаки активно использовались в исследованиях кормовых злаков [48,49,50,51]. Среди этих маркеров SSR-маркеры привлекли внимание благодаря их высокому полиморфизму и надежной воспроизводимости [52]. EST-SSR маркеры, которые нацелены на ДНК кодирующих областей, предлагают преимущества по сравнению с геномными SSR-маркерами, особенно в приложениях, включающих транскрипционные последовательности и гетерологичные виды [22,53]. Следовательно, SSR-маркеры стали инструментальными в оценке генетического разнообразия и идентификации разнообразия внутри различных культур [54,55,56], садовых растений [57,58,59] и кормовых видов [60,61,62].
Это исследование оценивало генетическую вариацию внутри и между популяциями, охватывающую 87 образцов. Они включали восемь сортов IRG, выведенных в Корее, один экзотический сорт и два экзотических сорта PRG, каждый из которых состоял из восьми особей, за исключением Aspire, у которого было семь.
В этом исследовании использовались 66 SSR-маркеров. Предыдущие исследования генетического разнообразия показали диапазоны 0,25–0,76 [63] и 0,019–0,236 [34]. Однако наше исследование продемонстрировало более высокий диапазон генетического разнообразия (0,469–0,571). В настоящее время в Корее регистрация новых сортов в соответствии с Законом о защите новых сортов растений учитывает новизну (Статья 17), отличимость (Статья 18), однородность (Статья 19), стабильность (Статья 20), родословную, фенотип и другие агрономические характеристики, такие как морфологические, физиологические и биохимические признаки. Этот подход имеет решающее значение для повышения надежной идентификации сортов и защиты прав селекционеров. Пастбищная селекция обычно включает гетерозис и поликросс, что приводит к большому генетическому расстоянию внутри сортов и низкой дифференциации между вариантами [64]. Соответственно, метод отбора образцов и методы селекции с использованием молекулярных маркеров служат инструментами для повышения эффективности селекции.
Предыдущие исследования изучали кластеры на дендрограммах, фокусируясь на сходных характеристиках, таких как морфология и дата колошения, с учетом сорта, места селекции и страны [65]. Наше исследование дало сходные результаты в кластерном анализе, PCoA и анализе с использованием стратегии объединения в отношении генетического расстояния между сортами. В частности, сорта одного вида были в основном сгруппированы в соответствии с плоидностью. Кроме того, Greencall и Greencall 2ho стабильно показывали сходные результаты на нашей дендрограмме. Всякий раз, когда Greencall 2ho присутствовал в кластере, он располагался под Greencall. Это наблюдение согласуется с нашими данными по селекционным линиям, которые были получены от родительских линий со сходным генетическим фоном (Таблица S10). Кроме того, мы обнаружили, что Greencall и Greencall 2ho имеют морфологическое сходство, сходные привычки роста и периоды цветения. Однако Greencall 2ho имеет более толстый стебель по сравнению с Greencall. Аналогично, Kowinearly и Kowinmaster показали сходные паттерны в дендрограмме, PCoA и анализе с использованием стратегии объединения. Всякий раз, когда Kowinmaster был сгруппирован, он включался в Kowinearly, и эти наблюдения были подтверждены структурным анализом. Кроме того, Kowinearly и Kowinmaster были выведены с использованием пяти различных родительских линий, три из которых являются общими (Таблица S10). Это объясняет их сходные морфологические характеристики, привычки роста и периоды цветения. Однако они различались по периодам цветения: Kowinearly является скороспелым сортом, а Kowinmaster — среднеспелым сортом [66,67]. Интересно, что в PCoA было обнаружено, что Kowinearly, Greenfarm и Greencall 2ho имеют общую селекционную историю с Florida 80, что указывает на общее генетическое наследие. Кроме того, Greencall и Greencall 2ho использовали Kowinearly для скрещивания, что привело к общему генетическому наследию с Kowinearly. Аналогично, Greencall и Greenfarm использовали Kospeed для скрещивания, что привело к общему генетическому наследию с Kospeed (Таблица S10). Структурный анализ при значении K = 2 изначально создавал трудности в различении полиплоидных видов, таких как диплоиды или тетраплоиды. Однако эта проблема была решена путем увеличения значения K до 3. Структурный анализ показал результаты, сходные с результатами 2D PCoA для 87 образцов. Это свидетельствует о том, что как структурный анализ, так и PCoA могут эффективно различать пастбищные виды. Эти анализы могут быть использованы для подтверждения полиплоидии между сортами или для получения информации о новых сортах. Крайне важно использовать установленные базы данных, поскольку эти методы полагаются на стандартизированные контрольные точки, полученные из существующих знаний о сортах.
Информация о системе размножения, репродуктивной биологии и жизненном цикле вида определяет решения относительно количества особей для отбора в популяциях. Это может подразумевать отбор многих особей из нескольких популяций или отбор меньшего количества особей из большего числа популяций [68]. Генетическое разнообразие злаков, как правило, превосходит таковое у обычных растений, таких как рис [55] и соя [56], из-за уникальных характеристик злаков, таких как используемые методы поликросс-селекции, их перекрестноопыляемая природа, гетерозис и самонесовместимость. Исследования генетического разнообразия пастбищных злаков, таких как IRG, PRG и ежа сборная, различались по подходам к отбору проб: некоторые исследования анализировали всего 1–3 особи на сорт, в то время как другие анализировали до 100 или более особей на сорт [2,33,34,46,48,69,70]. В нашем исследовании использовались анализ генетического разнообразия и AMOVA, среди прочих методов, с семью-восемью особями на сорт, и оно дало результаты, согласующиеся с результатами предыдущих исследований. Результаты нашего исследования свидетельствуют о том, что использование молекулярных маркеров для селекции сортов является как экономичным по времени, так и по затратам.
AMOVA выявил более высокую вариацию внутри сортов — 90%, чем между ними. Сходные результаты наблюдались в предыдущих исследованиях пастбищных злаков, что согласуется с нашими выводами [71,72]. Генетическая вариация внутри сортов выше, чем между одной материнской и одной отцовской линией, потому что пастбищные злаки характеризуются самонесовместимостью, перекрестноопыляемыми растениями и методом поликросс-селекции. Следовательно, генетическое расстояние между сортами было подтверждено с использованием стратегии объединения, которая позволила нам анализировать сорта, демонстрирующие высокую генетическую вариацию [73]. Кроме того, стратегии объединения служат ценными инструментами для обработки «редких» полос, которые возникают из-за разнообразия, создающего внутрисортовую вариацию [8,74]. В анализе с использованием стратегии объединения восемь особей на сорт (за исключением Aspire, который состоял из семи особей) были сгруппированы, что дало результаты, сходные с теми, которые были получены при использовании структурного анализа и 2D PCoA.
5. Выводы
В этом исследовании было изучено генетическое разнообразие и родство между восемью сортами IRG и двумя сортами PRG с использованием 66 SSR-маркеров, выявив значительную внутрисортовую вариацию (90%), как показано с помощью AMOVA. Молекулярные маркеры, включая геномные SSR и EST-SSR, эффективно дифференцировали диплоидные и тетраплоидные сорта, а также различали виды IRG и PRG. Такие анализы, как кластеризация, PCoA и структурная оценка, стабильно группировали сорта по видам и плоидности, одновременно выделяя тесные генетические взаимосвязи, такие как взаимосвязь между Greencall и Greencall 2ho. Стратегия объединения дополнительно подтвердила эти результаты, подтвердив генетическое разнообразие и отчетливую кластеризацию таких сортов, как Kowinearly и Kowinmaster, которые имеют общие родительские линии и признаки.
Несмотря на растущий импорт кормовых злаков в Корее, доступность высококачественных отечественных сортов остается ограниченной. В то время как традиционная селекция была ключевой в разработке сортов, исследования молекулярных маркеров, широко принятые на международном уровне, остаются недостаточно используемыми на местном уровне. Это исследование подчеркивает потенциал молекулярных маркеров и карт связывания как мощных инструментов для выяснения генетического разнообразия и сортовых характеристик корейских кормовых злаков. Чтобы максимизировать применимость этих результатов, крайне важно включать ключевые агрономические признаки, такие как биомасса и содержание целлюлозы. Исследовательская группа активно готовится к оценке агрономической продуктивности этих сортов, обеспечивая комплексный подход к улучшению кормовых злаков. Интегрируя надежную базу данных для маркер-ориентированной селекции с анализом агрономической продуктивности, это исследование предлагает путь к улучшению агрономических признаков, повышению эффективности селекции и стимулированию инноваций в корейской индустрии кормовых злаков, прокладывая путь к более устойчивому и самодостаточному будущему.
Вспомогательные материалы
Следующую вспомогательную информацию можно загрузить по адресу: https://www.mdpi.com/article/10.3390/agriculture15030244/s1. Рисунок S1: Число аллелей (a) и PIC (b) на локус для 66 SSR-маркеров; Рисунок S2: Число аллелей (a) и PIC (b) на локус для EST-SSR маркеров; Рисунок S3: Число аллелей (a) и PIC (b) на локус для геномных SSR маркеров; Рисунок S4: Филогенетическое дерево UPGMA с использованием 35 EST-SSR маркеров для 87 отдельных сортов IRG и PRG; Рисунок S5: Филогенетическое дерево UPGMA с использованием 31 геномного SSR маркера для 87 отдельных сортов IRG и PRG; Рисунок S6: График 2D модели PCoA с использованием 66 маркеров для отдельных растений сортов IRG и PRG: AP (Aspire), GC1 (Greencall), GC2 (Greencall 2ho), GF (Greenfarm), HS (Hwasan 104ho), IR1 (IR605), IR2 (IR901), KM (Kowinmaster), KT (Kentaur), KW (Kowinearly) и PD (Florida 80), рассчитанный с использованием измерений расстояния Nei; Рисунок S7: Филогенетическое дерево UPGMA, построенное с использованием только EST-SSR маркеров для объединенных образцов сортов IRG и PRG: AP (Aspire), GC1 (Greencall), GC2 (Greencall 2ho), GF (Greenfarm), HS (Hwasan 104ho), IR1 (IR605), IR2 (IR901), KM (Kowinmaster), KT (Kentaur), KW (Kowinearly) и PD (Florida 80), рассчитанное с использованием измерений среднего генетического расстояния; Рисунок S8: Филогенетическое дерево UPGMA, построенное с использованием только геномных SSR маркеров для объединенных образцов сортов IRG и PRG: AP (Aspire), GC1 (Greencall), GC2 (Greencall 2ho), GF (Greenfarm), HS (Hwasan 104ho), IR1 (IR605), IR2 (IR901), KM (Kowinmaster), KT (Kentaur), KW (Kowinearly) и PD (Florida 80), рассчитанное с использованием измерений среднего генетического расстояния; Рисунок S9: График 3D модели PCoA с использованием только EST-SSR маркеров для отдельных растений сортов IRG и PRG: AP (Aspire), GC1 (Greencall), GC2 (Greencall 2ho), GF (Greenfarm), HS (Hwasan 104ho), IR1 (IR605), IR2 (IR901), KM (Kowinmaster), KT (Kentaur), KW (Kowinearly) и PD (Florida 80), рассчитанный с использованием измерений среднего генетического расстояния, где первые три главные координаты объясняли 16,1%, 13,3% и 11,5% вариации соответственно; Рисунок S10: График 3D модели PCoA с использованием только геномных SSR маркеров для отдельных растений сортов IRG и PRG: AP (Aspire), GC1 (Greencall), GC2 (Greencall 2ho), GF (Greenfarm), HS (Hwasan 104ho), IR1 (IR605), IR2 (IR901), KM (Kowinmaster), KT (Kentaur), KW (Kowinearly) и PD (Florida 80), рассчитанный с использованием измерений среднего генетического расстояния, где первые три главные координаты объясняли 17,5%, 11,9% и 11,2% вариации соответственно; Таблица S1: Сравнение полезности между геномными SSR и EST-SSR маркерами для 66 образцов IRG и PRG; Таблица S2: Общие данные по генетическим расстояниям IRG и PRG; Таблица S3: Отклонения генетического расстояния; Таблица S4: Иерархическое разделение генетической вариации, созданное с помощью AMOVA только EST-SSR маркеров; Таблица S5: Иерархическое разделение генетической вариации, созданное с помощью AMOVA только геномных SSR маркеров; Таблица S6: Распределение сортов по кластерам; Таблица S7: Распределение сортов по субкластерам; Таблица S8: Генетическое расстояние между сортами, полученное с помощью стратегии объединения с использованием только EST-SSR маркеров; Таблица S9: Генетическое расстояние между сортами, полученное с помощью стратегии объединения с использованием только геномных SSR маркеров; Таблица S10: Селекционные линии сортов, выведенных в Корее.
Ссылки
1. NIAS (National Institute of Animal Science). Characteristics of Italian Ryegrass Breeds and Descriptions for Use of Cultivation. 2022. Available online: https://lib.rda.go.kr/search/mediaView.do?sysdiv=CAT&ctrl=000000640132 (accessed on 1 December 2024).
2. Kubik, C.; Sawkins, M.; Meyer, W.A.; Gaut, B.S. Genetic diversity in seven perennial ryegrass (Lolium perenne L.) cultivars based on SSR markers. Crop Sci. 2001, 41, 1565–1572. [Google Scholar] [CrossRef]
3. Kim, K.Y.; Lee, S.H.; Choi, G.J.; Park, H.S.; Hwang, T.Y.; Lee, K.-W. A Medium Maturing Variety of Italian Ryegrass (Lolium multiflorum Lam.), ‘IR605’, with High Forage Productivity in Southern Region of Korea. Korean Soc. Grassl. Forage Sci. 2020, 40, 156–160. [Google Scholar] [CrossRef]
4. Choi, G.J.; Lim, Y.C.; Rim, Y.W.; Sung, B.R.; Kim, M.J.; Kim, K.Y.; Seo, S. A Cold-Tolerant and High-yielding Italian Ryegrass New Variety, ‘Kowinner’. Korean Soc. Grassl. Forage Sci. 2006, 26, 171–176. [Google Scholar]
5. Nongsaro. Italian Ryegrass. 2024. Available online: https://www.nongsaro.go.kr/portal/search/nongsaroSearch.ps?menuId=PS00007&categoryName=SCH01&sortOrdr=01&pageIndex=1&pageSize=10&pageUnit=10&includeWord=&exEqWord=&ikEqWork=&excludeWord=&Hflag=&qura=&reCountingYn=Y&field=SCH01&searchWord=%EC%82%AC%EB%A3%8C (accessed on 1 December 2024).
6. Cai, H.; Stewart, A.; Inoue, M.; Yuyama, N.; Hirata, M. Lolium. In Wild Crop Relatives: Genomic and Breeding Resources: Millets and Grasses; Springer: Berlin/Heidelberg, Germany, 2010; pp. 165–173. [Google Scholar]
7. Hirata, M. Development of simple sequence repeat (SSR) markers in Italian ryegrass. In Proceedings of the Molecular Breeding of Forage Crops 2000, Lorne and Hamilton, Australia, 19–24 November 2000; Volume 51. [Google Scholar]
8. Forster, J.W.; Jones, E.S.; Kölliker, R.; Drayton, M.C.; Smith, K.F. Development and Implementation of Molecular Markers for Forage Crop Improvement; Springer: Dordrecht, The Netherlands, 2001. [Google Scholar]
9. Inoue, M.; Cai, H. Sequence analysis and conversion of genomic RFLP markers to STS and SSR markers in Italian ryegrass (Lolium multiflorum Lam.). Breed. Sci. 2004, 54, 245–251. [Google Scholar] [CrossRef]
10. Inoue, M.; Yuyama, N.; Cai, H. Development of SSR markers for variety identification in Italian ryegrass (Lolium multiflorum Lam.). In Molecular Breeding for the Genetic Improvement of Forage Crops and Turf; Wageningen Academy: Wageningen, The Netherlands, 2005; p. 130. [Google Scholar]
11. Guthridge, K.M.; Dupal, M.P.; Kölliker, R.; Jones, E.S.; Smith, K.F.; Forster, J.W. AFLP analysis of genetic diversity within and between populations of perennial ryegrass (Lolium perenne L.). Euphytica 2001, 122, 191–201. [Google Scholar] [CrossRef]
12. Fois, M.; Bellucci, A.; Malinowska, M.; Greve, M.; Ruud, A.K.; Asp, T. Genome-Wide Association Mapping of Crown and Brown Rust Resistance in Perennial Ryegrass. Genes 2021, 13, 20. [Google Scholar] [CrossRef]
13. Miura, Y.; Hirata, M.; Fujimori, M. Mapping of EST-derived CAPS markers in Italian ryegrass (Lolium multiflorum Lam.). Plant Breed. 2007, 126, 353–360. [Google Scholar] [CrossRef]
14. Kubik, C.; Meyer, W.A.; Gaut, B.S. Assesing the Abundance and Polymorphism of Simple Sequence Repeats in Perennial Ryegrass. Crop Sci. 1999, 39, 1136–1141. [Google Scholar] [CrossRef]
15. Jones, E.S.; Dupal, M.P.; Kolliker, R.; Drayton, M.C.; Forster, J.W. Development and characterisation of simple sequence repeat (SSR) markers for perennial ryegrass (Lolium perenne L.). Theor. Appl. Genet. 2001, 102, 405–415. [Google Scholar] [CrossRef]
16. Jones, S.; Dupal, P.; Dumsday, L.; Hughes, J.; Forster, W. An SSR-based genetic linkage map for perennial ryegrass (Lolium perenne L.). Theor. Appl. Genet. 2002, 105, 577–584. [Google Scholar] [CrossRef]
17. Jones, E.S.; Mahoney, N.L.; Hayward, M.D.; Armstead, I.P.; Jones, J.G.; Humphreys, M.O.; King, I.P.; Kishida, T.; Yamada, T.; Balfourier, F.; et al. An enhanced molecular marker based genetic map of perennial ryegrass (Lolium perenne) reveals comparative relationships with other Poaceae genomes. Genome 2002, 45, 282–295. [Google Scholar] [CrossRef] [PubMed]
18. Studer, B.; Kolliker, R.; Muylle, H.; Asp, T.; Frei, U.; Roldan-Ruiz, I.; Barre, P.; Tomaszewski, C.; Meally, H.; Barth, S.; et al. Est-derived ssr markers used as anchor loci for the construction of a consensus linkage map in ryegrass (Lolium spp.). BMC Plant Biol. 2010, 10, 177–187. [Google Scholar] [CrossRef]
19. Song, Q.J.; Shi, J.R.; Singh, S.; Fickus, E.W.; Costa, J.M.; Lewis, J.; Gill, B.S.; Ward, R.; Cregan, P.B. Development and mapping of microsatellite (STMS) markers in wheat. Theor. Appl. Genet. 2005, 110, 550–560. [Google Scholar] [CrossRef] [PubMed]
20. Hwang, T.Y.; Sayama, T.; Takahashi, M.; Takada, Y.; Nakamoto, Y.U.M.I.; Funatsuki, H.; Hisano, H.; Sasamoto, S.; Sato, S.; Tabata, S.; et al. High-density integrated linkage map based on SSR markers in soybean. DNA Res. 2009, 16, 213–225. [Google Scholar] [CrossRef] [PubMed]
21. Van de Wouw, M.; van Hintum, T.; Kik, C.; van Treuren, R.; Visser, B. Genetic diversity trends in twentieth century crop cultivars: A meta analysis. Theor. Appl. Genet. 2010, 120, 1241–1252. [Google Scholar] [CrossRef]
22. Parthiban, S.; Govindaraj, P.; Senthilkumar, S. Comparison of relative efficiency of genomic SSR and EST-SSR markers in estimating genetic diversity in sugarcane. 3 Biotech 2018, 8, 144. [Google Scholar] [CrossRef]
23. Ioannidis, K.; Tomprou, I.; Mitsis, V.; Koropouli, P. Genetic evaluation of in vitro micropropagated and regenerated plants of Cannabis sativa L. using SSR molecular markers. Plants 2022, 11, 2569. [Google Scholar] [CrossRef]
24. Fernandez, E.C.J.; Nuñez, J.P.P.; Gardoce, R.R.; Manohar, A.N.C.; Bajaro, R.M.; Lantican, D.V. Genetic purity and diversity assessment of parental corn inbred lines using SSR markers for Philippine hybrid breeding. SABRAO J. Breed. Genet. 2023, 55, 598–608. [Google Scholar] [CrossRef]
25. Thiel, T.; Michalek, W.; Varshney, R.; Graner, A. Exploiting EST databases for the development and characterization of gene-derived SSR-markers in barley (Hordeum vulgare L.). Theor. Appl. Genet. 2003, 106, 411–422. [Google Scholar] [CrossRef]
26. Teshome, A.; Bryngelsson, T.; Dagne, K.; Geleta, M. Assessment of Genetic Diversity in Ethiopian Field Pea (Pisum sativum L.) Accessions with Newly Developed EST-SSR Markers. BMC Genet. 2015, 16, 102. [Google Scholar] [CrossRef]
27. Chombe, D.; Bekele, E.; Bryngelsson, T.; Teshome, A.; Geleta, M. Genetic structure and relationships within and between cultivated and wild korarima [Aframomum corrorima (Braun) P.C.M. Jansen] in Ethiopia as revealed by simple sequence repeat (SSR) markers. BMC Genet. 2017, 18, 72. [Google Scholar] [CrossRef] [PubMed]
28. Gadissa, F.; Tesfaye, K.; Dagne, K.; Geleta, M. Genetic diversity and population structure analyses of Plectranthus edulis (Vatke) Agnew collections from diverse agro-ecologies in Ethiopia using newly developed EST-SSRs marker system. BMC Genet. 2018, 19, 92–107. [Google Scholar] [CrossRef]
29. Serbessa, T.B.; Dagne, W.K.; Teshome, G.A.; Geleta, D.M.; Tesfaye, G.K. Analyses of genetic diversity and population structure of anchote (Coccinia abyssinica (Lam.) Cogn.) using newly developed EST-SSR markers. Genet. Resour. Crop. Evol. 2021, 68, 2337–2350. [Google Scholar] [CrossRef]
30. Karan, M.; Evans, D.S.; Reilly, D.; Schulte, K.; Wright, C.; Innes, D.; Holton, T.A.; Nikles, D.G.; Dickinson, G.R. Rapid microsatellite marker development for African mahogany (Khaya senegalensis, Meliaceae) using next-generation sequencing and assessment of its intra-specific genetic diversity. Mol. Ecol. Resour. 2012, 12, 344–353. [Google Scholar] [CrossRef]
31. Futuyma, D.J. Evolutionary Biology Today and the Call for an Extended Synthesis. Interface Focus 2017, 7, 20160145. [Google Scholar] [CrossRef]
32. Bolaric, S.; Barth, S.; Melchinger, A.E.; Posselt, U.K. Genetic Diversity in European Perennial Ryegrass Cultivars Investigated with RAPD Markers. Plant Breed. 2005, 124, 161–166. [Google Scholar] [CrossRef]
33. Tamura, K.I.; Arakawa, A.; Kiyoshi, T.; Yonemaru, J.I. Genetic diversity and structure of diploid Italian ryegrass (Lolium multiflorum Lam.) cultivars and breeding materials in Japan based on genome-wide allele frequency. Grassl. Sci. 2022, 68, 263–276. [Google Scholar] [CrossRef]
34. Pasquali, E.; Palumbo, F.; Barcaccia, G. Assessment of the Genetic Distinctiveness and Uniformity of Pre-Basic Seed Stocks of Italian Ryegrass Varieties. Genes 2022, 13, 2097. [Google Scholar] [CrossRef]
35. Nei, M. Estimation of genetic distances and phylogenetic trees from DNA analysis. In Proceedings of the 5th World Congress on Genetics Applied to Livestock Production, Guelph, ON, Canada, 7–12 August 1994; Volume 21, p. 405. [Google Scholar]
36. Pritchard, J.K.; Stephens, M.; Donnelly, P. Inference of Population Structure Using Multilocus Genotype Data. Genetics 2000, 155, 945–959. [Google Scholar] [CrossRef]
37. Falush, D.; Stephens, M.; Pritchard, J.K. Inference of population structure using multilocus genotype data: Linked loci and correlated allele frequencies. Genetics 2003, 164, 1567–1587. [Google Scholar] [CrossRef]
38. Evanno, G.; Regnaut, S.; Goudet, J. Detecting the number of clusters of individuals using the software STRUCTURE: A simulation study. Mol. Ecol. 2005, 14, 2611–2620. [Google Scholar] [CrossRef] [PubMed]
39. Rohlf, F. NTSYS-PC, Numerical Taxonomy System for the PC Exeter Software, Version 2.1; Applied Biostatistics Inc.: Setauket E. Setauket, NY, USA, 2000. [Google Scholar]
40. Peakall, R.O.D.; Smouse, P.E. GENALEX 6: Genetic analysis in Excel. Population genetic software for teaching and research. Mol. Ecol. Notes 2006, 6, 288–295. [Google Scholar] [CrossRef]
41. Hirata, M.; Yuyama, N.; Cai, H. Isolation and characterization of simple sequence repeat markers for the tetraploid forage grass Dactylis glomerata. Plant Breed. 2011, 130, 503–506. [Google Scholar] [CrossRef]
42. Studer, B.; Widmer, F.; Enkerli, J.; Koelliker, R. Development of novel microsatellite markers for the grassland species Lolium multiflorum, Lolium perenne and Festuca pratensis. Mol. Ecol. Notes 2006, 6, 1108–1110. [Google Scholar] [CrossRef]
43. Saha, M.C.; Mian, R.; Eujayl, I.; Zwonitzer, J.C.; Wang, L.; May, G.D. Tall fescue EST-SSR markers with transferability across several grass species. Theor. Appl. Genet. 2004, 109, 783–791. [Google Scholar] [CrossRef]
44. Kantety, R.V.; Rota, M.L.; Matthews, D.E.; Sorrells, M.E. Data mining for simple sequence repeats in expressed sequence tags from barley, maize, rice, sorghum and wheat. Plant Mol. Biol. 2002, 48, 501–510. [Google Scholar] [CrossRef]
45. Bushman, B.S.; Larson, S.R.; Tuna, M.; West, M.S.; Hernandez, A.G.; Vullaganti, D.; Gong, G.; Robins, J.G.; Jensen, K.B.; Thimmapuram, J. Orchardgrass (Dactylis glomerata L.) EST and SSR marker development, annotation, and transferability. Theor. Appl. Genet. 2011, 123, 119–129. [Google Scholar] [CrossRef]
46. Yan, H.D.; Zhang, Y.; Zeng, B.; Yin, G.H.; Zhang, X.Q.; Ji, Y.; Huang, L.K.; Jiang, X.M.; Liu, X.C.; Peng, Y.; et al. Genetic diversity and association of EST-SSR and SCoT markers with rust traits in orchardgrass (Dactylis glomerata L.). Molecules 2016, 11, 66. [Google Scholar] [CrossRef]
47. Singh, A.; Prasad, S.; Singh, V.; Chaturvedi, G.; Singh, B. Morphological traits for vegetative stage drought tolerance in rice (Oryza sativa). In Resilient Crops for Water Limited Environments; International Maize and Wheat Improvement Center (CIMMYT): Veracruz, Mexico, 2004; p. 188. [Google Scholar]
48. Guo, Z.H.; Fu, K.X.; Zhang, X.Q.; Zhang, C.L.; Sun, M.; Huang, T.; Peng, Y.; Huang, L.K.; Yan, Y.H.; Ma, X. SSRs transferability and genetic diversity of three allogamous ryegrass species. Comptes Rendus Biol. 2016, 339, 60–67. [Google Scholar] [CrossRef]
49. Sartie, A.M.; Easton, H.S.; Matthew, C.; Rolston, M.P.; Faville, M.J. Seed yield in perennial ryegrass (Lolium perenne L.): Comparative importance of component traits and detection of seed-yield-related QTL. Euphytica 2018, 214, 226. [Google Scholar] [CrossRef]
50. Nie, G.; Huang, T.; Ma, X.; Huang, L.; Peng, Y.; Yan, Y.; Li, Z.; Wang, X.; Zhang, X. Genetic variability evaluation and cultivar identification of tetraploid annual ryegrass using SSR markers. PeerJ 2019, 7, e7742. [Google Scholar] [CrossRef] [PubMed]
51. Cropano, C.; Manzanares, C.; Yates, S.; Copetti, D.; Canto, J.D.; Lübberstedt, T.; Koch, M.; Studer, B. Identification of candidate genes for self-compatibility in perennial ryegrass (Lolium perenne L.). Front. Plant Sci. 2021, 12, 707901. [Google Scholar] [CrossRef]
52. Formisano, G.; Roig, C.; Esteras, C.; Ercolano, M.R.; Nuez, F.; Monforte, A.J.; Picó, M.B. Genetic diversity of Spanish Cucurbita pepo landraces: An unexploited resource for summer squash breeding. Genet. Resour. Crop Evol. 2012, 59, 1169–1184. [Google Scholar] [CrossRef]
53. Mian, M.A.R.; Saha, M.C.; Hopkins, A.A.; Wang, Z. Use of tall fescue EST-SSR markers in phylogenetic analysis of cool-season forage grasses. Genome 2005, 48, 637–647. [Google Scholar] [CrossRef]
54. Wang, L.-X.; Jun, Q.; Chang, L.F.; Liu, L.-H.; Li, H.-B.; Pang, B.S.; Zhao, C.-P. Assessment of wheat variety distinctness using SSR markers. J. Integr. Agric. 2015, 14, 1923–1935. [Google Scholar] [CrossRef]
55. Singh, N.; Roy Choudhury, D.; Tiwari, G.; Singh, A.; Kumar, S.; Srinivasan, K.; Tyagi, R.; Sharma, A.D.; Singh, N.; Singh, R. Genetic Diversity Trend in Indian Rice Varieties: An Analysis Using SSR Markers. BMC Genet. 2016, 17, 127. [Google Scholar] [CrossRef]
56. Hwang, T.Y.; Gwak, B.S.; Sung, J.; Kim, H.S. Genetic diversity patterns and discrimination of 172 korean soybean (Glycine max (L.) merrill) varieties based on SSR analysis. Agriculture 2020, 10, 77. [Google Scholar] [CrossRef]
57. Tsai, C.C.; Chen, Y.U.K.H.; Chen, C.H.; Weng, I.S.; Tsai, C.M.; Lee, S.R.; Lin, Y.S.; Chiang, Y.C. Cultivar identification and genetic relationship of mango (Mangifera indica) in Taiwan using 37 SSR markers. Sci. Hortic. 2013, 164, 196–201. [Google Scholar] [CrossRef]
58. Xie, W.; Zhang, X.; Cai, H.; Huang, L.; Peng, Y.; Ma, X. Genetic maps of ssr and srap markers in diploid orchardgrass (Dactylis glomerata L.) using the pseudo-testcross strategy. Genome 2011, 54, 212–221. [Google Scholar] [CrossRef]
59. Saidi, A.; Eghbalnegad, Y.; Hajibarat, Z. Study of genetic diversity in local rose varieties (Rosa spp.) using molecular markers. Banat. J. Biotechnol. 2017, 8, 148–157. [Google Scholar]
60. Tehrani, M.S.; Mardi, M.; Sahebi, J.; Catalán, P.; Díaz-Pérez, A. Genetic Diversity and Structure among Iranian Tall Fescue Populations Based on Genomic-SSR and EST-SSR Marker Analysis. Plant Syst. Evol. 2009, 282, 57–70. [Google Scholar] [CrossRef]
61. Herrmann, D.; Flajoulot, S.; Julier, B. Sample size for diversity studies in tetraploid alfalfa (Medicago sativa) based on codominantly coded SSR markers. Euphytica 2010, 171, 441–446. [Google Scholar] [CrossRef]
62. Jiang, L.F.; Zhang, X.Q.; Ma, X.; Huang, L.K.; Xie, W.G.; Ma, Y.M.; Zhao, Y.F. Identification of orchardgrass (Dactylis glomerata L.) cultivars by using simple sequence repeat markers. Genet. Mol. Res. 2013, 12, 5111–5123. [Google Scholar] [CrossRef]
63. Guan, X.; Yuyama, N.; Stewart, A.; Ding, C.; Xu, N.; Kiyoshi, T.; Cai, H. Genetic Diversity and Structure of Lolium Species Surveyed on Nuclear Simple Sequence Repeat and Cytoplasmic Markers. Front. Plant Sci. 2017, 8, 584. [Google Scholar] [CrossRef]
64. Roldán-Ruiz, I.; Dendauw, J.; Van Bockstaele, E.; Depicker, A.; De Loose, M. AFLP markers reveal high polymorphic rates in ryegrasses (Lolium spp.). Mol. Breed. 2000, 6, 125–134. [Google Scholar] [CrossRef]
65. Tamura, K.I.; Kiyoshi, T.; Kubota, A.; Arakawa, A.; Fujimori, M.; Yonemaru, J.I. Genetic relationship and diversity of cultivars and breeding lines of tetraploid Italian ryegrass (Lolium multiflorum Lam.) and its hybrids with Lolium-Festuca complex based on genome-wide allele frequency. Grassl. Sci. 2023, 69, 65–78. [Google Scholar] [CrossRef]
66. Choi, G.J.; Lim, Y.C.; Kim, K.Y.; Kim, M.J.; Ji, H.C.; Lee, S.H.; Park, H.S.; Moon, C.S.; Lee, E.S.; Seo, S. A cold-tolerant and medium -maturing Italian ryegrass (Lolium multiflorum Lam.) new variety, ‘Kowinmaster’. Korea Soc. Grassl. Forage Sci. 2008, 28, 177–184. [Google Scholar]
67. Choi, G.J.; Ji, H.C.; Kim, K.Y.; Park, H.S.; Seo, S.; Lee, K.W.; Lee, S.H. Growth characteristics and productivity of cold-tolerant “Kowinearly” Italian ryegrass in the northern part of South Korea. Afr. J. Biotechnol. 2011, 10, 2676–2682. [Google Scholar]
68. Ward, S.M.; Jasieniuk, M. Review: Sampling weedy and invasive plant populations for genetic diversity analysis. Weed Sci. 2009, 57, 593–602. [Google Scholar] [CrossRef]
69. Mao, J.X.; Luo, D.; Wang, G.W.; Zhang, J.; Yang, Y.M.; Zhang, X.Q.; Zeng, B. Genetic diversity of orchardgrass (Dactylis glomerata L.) cultivars revealed by simple sequence repeats (SSR) markers. Biochem. Syst. Ecol. 2016, 66, 337–343. [Google Scholar] [CrossRef]
70. Nabhan, A.; Arvas, Ö.; Furan, M.A. The applicability of wheat SSR markers to analyzing the molecular diversity and distribution of orchardgrass (Dactylis glomerata L.) genotypes from eastern Anatolian habitats. Yüzüncü Yıl Üniversitesi Fen Bilim. Enstitüsü Derg. 2023, 28, 732–744. [Google Scholar]
71. Last, L.; Widmer, F.; Fjellstad, W.; Stoyanova, S.; Kölliker, R. Genetic Diversity of Natural Orchardgrass (Dactylis glomerata L.) Populations in Three Regions in Europe. BMC Genet. 2013, 14, 102. [Google Scholar] [CrossRef] [PubMed]
72. Benfriha, H.; Mefti, M.; Robbins, M.; Thorsted, K.; Bushman, S. Molecular characterization of Algerian populations of cocksfoot and tall fescue: Ploidy level determination and genetic diversity analysis. Grassl. Sci. 2021, 67, 167–176. [Google Scholar] [CrossRef]
73. Liu, S.; Feuerstein, U.; Luesink, W.; Schulze, S.; Asp, T.; Studer, B.; Becker, H.C.; Dehmer, K.J. DArT, SNP, and SSR Analyses of Genetic Diversity in Lolium perenne L. Using Bulk Sampling. BMC Genet. 2018, 19, 10. [Google Scholar] [CrossRef]
74. ReyesValdes, H.M.; SantacruzVarela, A.; Martinez, O.; Simpson, J.; HayanoKanashiro, C.; CortesRomero, C. Analysis and optimization of bulked DNA sampling with binary scoring for germplasm characterization. PLoS ONE 2013, 8, 79936. [Google Scholar]
Nam D-G, Baek E-S, Hwang E-B, Gwak S-C, Lee Y-H, Cho S-W, Yu J-K, Hwang T-Y. Genetic Diversity Patterns Within and Among Varieties of Korean Italian Ryegrass (Lolium multiflorum) and Perennial Ryegrass (Lolium perenne) Based on Simple Sequence Repetition. Agriculture. 2025; 15(3):244. https://doi.org/10.3390/agriculture15030244
Перевод статьи «Genetic Diversity Patterns Within and Among Varieties of Korean Italian Ryegrass (Lolium multiflorum) and Perennial Ryegrass (Lolium perenne) Based on Simple Sequence Repetition» авторов Nam D-G, Baek E-S, Hwang E-B, Gwak S-C, Lee Y-H, Cho S-W, Yu J-K, Hwang T-Y., оригинал доступен по ссылке. Лицензия: CC BY. Изменения: переведено на русский язык















































































































Комментарии (0)