Тайна окраски космеи: как метаболизм и гены создают белые, розовые и красные цветы
В природе растения обладают богатой и яркой окраской. Цвет цветка может придавать декоративным растениям экономическую и эстетическую ценность и является одним из целевых признаков для современной направленной селекции. Поэтому крайне важно понимать молекулярные механизмы регуляции формирования окраски цветков у декоративных растений. Однако у космеи дваждыперистой (Cosmos bipinnata Cav.), одного из важнейших декоративных растений, метаболические пути и молекулярные механизмы регуляции, лежащие в основе формирования разной окраски цветков, до сих пор не ясны, что значительно ограничивает молекулярную селекцию сортов с различной окраской цветков.
Аннотация
Мы выбрали три сорта космеи дваждыперистой с белыми, розовыми и красными цветками в качестве объектов исследования и выявили значительно различающиеся метаболиты между ними с помощью сверхвысокоэффективной жидкостной хроматографии-масс-спектрометрии (UPLC-MS/MS) и метода главных компонент (PCA). Затем, используя анализ обогащения в базе данных KEGG (Kyoto Encyclopedia of Genes and Genomes) и транскриптомное секвенирование цветков разной окраски, мы показали, что дифференциальные метаболиты обогащены в метаболических путях флавоноидов, а связанные со структурой гены экспрессируются дифференциально. Кроме того, мы идентифицировали дифференциально экспрессирующиеся представители семейств транскрипционных факторов MYB и bHLH, которые играют ключевую роль в регуляции биосинтеза антоцианов. С помощью построения филогенетического древа и совместного анализа данных транскриптома и метаболома мы дополнительно охарактеризовали молекулярную регуляторную сеть, лежащую в основе формирования окраски цветков у космеи дваждыперистой. Это исследование не только предоставляет теоретическую основу и генетические ресурсы для селекции, направленной на изменение окраски, и создания новых сортов с другой окраской, но и открывает новые перспективы в понимании молекулярных механизмов формирования окраски цветков у растений.
1. Введение
Cosmos bipinnata Cav. родом из Мексики и является однолетним или многолетним травянистым цветком рода Космея семейства Астровые. Космея дваждыперистая — одно из часто используемых растений для озеленения городов в Китае. Ее цветки легкие и яркие, с пышным и естественным цветением и сильной способностью к самосеву. При посадке большими массивами она создает впечатление дикой и естественной природы. Широко используется в садах, может размещаться вдоль дорог, на газонах и опушках леса, а также использоваться в качестве цветочных бордюров, живых изгородей, цветочных групп. Ее также можно использовать как почвопокровное растение или для срезки. Кроме того, космея дваждыперистая обладает чрезвычайно высокой лекарственной ценностью, а ее соцветия, семена и все растение оказывают жаропонижающее, детоксицирующее действие, улучшают зрение и выводят влагу. Для создания нового цветочного гермоплазм генетический перенос как представитель методов биологической селекции является революционной технологией в области селекции и новым направлением, которое необходимо освоить. Это также требует углубленного анализа пути биосинтеза целевого метаболита и его молекулярного механизма регуляции. В настоящее время исследования космеи дваждыперистой в основном сосредоточены на показателях завязывания семян и характеристиках прорастания, сроках посева семян, а также на агротехнике выращивания и ухода. Недостаток исследований пути биосинтеза и молекулярного механизма регуляции антоцианов у космеи дваждыперистой значительно ограничивает процесс развития молекулярной селекции, что не способствует максимизации ее коммерческой и практической ценности.
В природе растительные пигменты наделяют растения богатой и яркой окраской. В производстве и выращивании садовых культур яркий внешний вид, обеспечиваемый растительными пигментами, не только помогает растениям привлекать опылителей, но и приносит огромную коммерческую ценность садовым культурам как важный декоративный признак. Поэтому такие агрономические признаки, как окраска цветков, окраска листьев и окраска плодов, всегда были важными целями селекции садовых культур [1]. Современные исследования показывают, что флавоноиды могут придавать растениям широкий диапазон окрасок [2,3,4,5]. А антоцианы, как тип флавоноидных соединений, обуславливают красную, пурпурную и синюю окраску многих цветов и плодов. Они служат биохимической основой окраски декоративных растений и играют важнейшую роль в определении их декоративной ценности [6]. Поэтому крайне важно выяснить молекулярные механизмы, лежащие в основе формирования различной окраски цветков у космеи дваждыперистой.
По предварительным данным, антоцианы обнаружены у растений 73 родов и 27 семейств. К антоцианам относят шесть основных соединений: пеларгонидин, цианидин, пеонидин, дельфинидин, петунидин и мальвидин [7]. Дельфинидин часто придает цветкам синий/пурпурный цвет, цианидин придает цветкам красный/пурпурно-красный цвет, оранжевые/кирпично-красные цветки содержат в основном пеларгонидин, пеонидин, образующийся в результате метилирования цианидина, часто имеет пурпурно-красный цвет, а мальвидин, образующийся в результате метилирования дельфинидина, имеет пурпурный цвет [8,9,10,11].
У растений антоцианы образуются в результате метаболизма флавоноидов. Исследования метаболизма флавоноидов имеют давнюю историю и проводятся на углубленном уровне. Исследования на хризантемах показали, что накопление антоцианов в цветках хризантемы является результатом совместной экспрессии ключевых структурных генов, таких как CHS, CHI, F3H, F3′H, DFR и ANS [12,13]. Этот путь относительно консервативен у многих видов, например, у арабидопсиса [14] и петунии [15].
Биосинтез антоцианов у растений регулируется как внутренними, так и внешними факторами, причем внешние факторы в основном включают ряд экологических факторов, таких как интенсивность света, фотопериод, качество света и температура [16]. Внутренние факторы в основном относятся к генам, связанным с метаболизмом флавоноидов у растений. С одной стороны, это структурные гены биосинтеза флавоноидов, кодирующие соответствующие ферменты, а с другой стороны — транскрипционные факторы, участвующие в регуляции метаболизма флавоноидов, такие как MYB, bHLH, WRKY, YABBY, белок WD40, белок bZIP и цинк-пальцевый белок. За последние несколько десятилетий исследования молекулярной регуляции биосинтеза флавоноидов стали дальнейший более углубленными [17,18], причем исследования участия белков MYB, bHLH, WD40 и WRKY в регуляции являются наиболее углубленными и обширными. В исследовании хризантем Xiang и др. впервые идентифицировали вышестоящий регуляторный комплекс CmMYB6-CMBHLH2 в пути метаболизма антоцианов, который способствует накоплению антоцианов, стимулируя экспрессию генов CmDFR [19,20]. Кроме того, постепенно показываются молекулярные механизмы регуляции биосинтеза антоцианов хризантемы такими транскрипционными факторами, как CmMYB01, CmMYB21, CmMYB9a и CmMYB#7 [21,22,23,24]. Дополнительно, PtrRML1 ингибирует биосинтез антоцианов через аналогичный механизм у тополя [25], биосинтез антоцианов регулируется AtHY5 через транскрипционную активацию AtPAP1 у арабидопсиса [26], а MdMYB1 сумоилируется и стабилизируется на уровне белка для стимулирования биосинтеза антоцианов при низких температурах у яблони [27].
С революционным развитием технологий высокопроизводительного секвенирования методы омиксного анализа предоставляют богатую информационную базу для процессов роста и развития животных и растений. Однако живые системы — это организмы со множеством взаимосвязанных компонентов, представляющие собой высокосложные и масштабные системы. Одноомиксные исследования могут идентифицировать только отдельные изменения, не могут обнаружить причины изменений и не могут изучать взаимосвязи сложных биологических процессов. Путем объединения нескольких омиксных анализов для установления взаимосвязей данных между молекулами на различных уровнях и сочетания функционального анализа, обогащения метаболических путей и т.д. проводится систематический и всесторонний анализ функций и механизмов регуляции биомолекул. Мультиомикса как метод исследования, объединяющий две или более омиксных технологий, стал одним из наиболее эффективных инструментов в исследованиях системной биологии [28,29]. Сочетание транскриптома и метаболома в настоящее время является наиболее зрелой и углубленной технологией в мультиомиксных исследованиях. Результаты сплайсинга данных транскриптома могут использоваться для предсказания новых генов и анализа новых транскриптов, поиска ключевых регуляторных генов важных признаков или фенотипов растений. Метаболом — это совокупность всех метаболитов, продуцируемых клетками, тканями и органами организма, которые являются конечными продуктами экспрессии генов в организме [30]. В этом исследовании мы выбрали три различных по окраске сорта космеи дваждыперистой, а именно белого, розового и красного цветов, в качестве объектов исследования. Мы предполагаем, что различная окраска может быть обусловлена различиями в метаболических путях и механизмах регуляции растительных пигментов. Для того чтобы выяснить молекулярные механизмы формирования различной окраски цветков у космеи дваждыперистой, мы использовали транскриптомно-метаболомный анализ, сосредоточив внимание на путях и регуляции, связанных с метаболизмом растительных пигментов. Это предоставит теоретическую основу и генетический резерв для селекции, направленной на изменение окраски, и создания новых сортов космеи дваждыперистой с различной окраской.
2. Материалы и методы
2.1. Растительные материалы и условия выращивания
Растения космеи дваждыперистой выращивали в теплице с температурой 24 °C при 16-часовом световом дне и 16 °C при 8-часовой темноте и влажностью 70%. Затем было собрано не менее 5 биологических повторностей лепестков для каждой окраски, часть для последующего измерения цвета, а другая часть заморожена при −80 °C для будущих экспериментов.
2.2. Измерение окраски цветков
Международная комиссия по освещению (CIE) ввела цветовое пространство Lab в 1976 году, которое представляет собой комплексную модель, охватывающую все оттенки, воспринимаемые человеческим зрением. Эта модель основана на трех компонентах: светимость (обозначается "L"), и каналах "a" и "b", причем первый указывает на спектр от красного до зеленого, а второй — от синего до желтого [31]. Для определения цветовых характеристик трех различных сортов космеи дваждыперистой использовали портативный колориметр Minolta CR-400 (Konica Minolta, Japan). С помощью этого устройства были получены измерения светимости (L) и хроматических элементов a и b. Насыщенность, или хрома (C), была рассчитана по формуле: C = (a² + b²)¹/² [32]. Эксперимент был проведен шесть раз для обеспечения надежности.
2.3. Метаболомный анализ
Для каждого образца было проведено шесть биологических повторностей. Экспериментальная процедура начинается с экстракции метаболитов из образцов с использованием 80% метанола, с последующим хранением при −80 °C для последующего LC-MS анализа. Жидкостная хроматография выполнялась на системе UPLC UltiMate 3000 (Thermo Fisher Scientific, Bremen, Germany) с использованием градиентного элюирования. Детектирование масс-спектрометрии выполнялось на системе TripleTOF 6600 (SCIEX, Framingham, MA, USA), работающей как в режиме положительных, так и отрицательных ионов, с динамическим сбором данных и регулярной калибровкой для точности. Анализ данных включал предварительную обработку с помощью программного обеспечения XCMS 3.4.1, преобразование исходных файлов в формат mzXML и использование инструментов на основе R (версия 4.0.0), таких как CAMERA и metaX, для идентификации пиков и их группировки. Аннотация метаболитов проводилась с использованием баз данных KEGG и HMDB, с дальнейшей валидацией из внутренней библиотеки спектров. Статистический анализ в R включал нормализацию, иерархическую кластеризацию, PCA и PLSDA, выявляя значимые метаболиты на основе комбинации p-значений, fold change и VIP-оценок. Анализ обогащения с помощью GSEA и MSigDB оценивал различия в наборах генов в различных путях KEGG, при этом значимость определялась по NES, p-значениям и q-значениям, что в итоге позволило сопоставить метаболиты с их соответствующими путями. Используемый пакет R (версия 4.0.0) показан в Таблице S2.
2.4. Подготовка образцов, транскриптомное секвенирование и анализ дифференциально экспрессирующихся генов (DEG)
Общую РНК экстрагировали из лепестков различной окраски с использованием реагента RNAiso Reagent (Takara, Tokyo, Japan) в соответствии с инструкциями производителя. Было сконструировано девять библиотек кДНК для белых, розовых и красных лепестков, по три биологических повторности для каждого образца. Библиотеки РНК были секвенированы на платформе Illumina NovaseqTM 6000 (LC Bio Technology Co., Ltd. Hangzhou, China). Последующий биоинформатический анализ был выполнен с использованием инструментов OmicStudio по адресу https://www.omicstudio.cn/tool (доступ 1 июля 2024 г.) [33].
2.5. Построение филогенетических деревьев
Для этого исследования мы использовали метод присоединения соседей (NJ) для построения филогенетического дерева с использованием программного обеспечения MEGA 7.0. Последовательности белков MYB и bHLH у арабидопсиса были получены из базы данных информации об арабидопсисе (TAIR) по адресу https://www.arabidopsis.org (доступ 1 сентября 2024 г.). Мы выровняли целевые последовательности генов с помощью ClustalW, удалили плохо выровненные концевые последовательности, а затем провели NJ-анализ с 500 начальными загрузками (bootstrap) для оценки поддержки узлов. Полученное дерево было визуализировано и аннотировано в программном обеспечении MEGA7.0 для дальнейшей биологической интерпретации.
2.6. Совместный анализ метаболомики и транскриптомики
Во-первых, значимо дифференциально экспрессирующиеся гены и метаболиты были отобраны в данных транскриптома и метаболома соответственно. Затем, на основе пересечения этих путей, были найдены дифференциально экспрессирующиеся гены и дифференциальные метаболиты в пересекающихся путях. Впоследствии структура была представлена в виде сетевой диаграммы, отображающей связанные данные, с особым акцентом на интересующие пути и различные паттерны экспрессии РНК. Используемый пакет R показан в Таблице S2.
2.7. Статистический анализ
Данные представлены как средние значения. Многогрупповые сравнения выполнялись с использованием однофакторного дисперсионного анализа (ANOVA), а для сравнений между двумя группами использовался t-критерий Стьюдента. Дифференциально экспрессирующиеся гены классифицируются на основе fold change (FC) ≥ 2 или FC ≤ 0,5 (т.е. абсолютное значение log2FC ≥ 1) и уровня ложных открытий (FDR) < 0,05 (|log2FC| ≥ 1 & FDR < 0,05) в качестве стандарта. Дифференциальные метаболиты должны одновременно удовлетворять следующим условиям: FC ≥ 1,2 или FC ≥ 1/1,2, p-значение < 0,05, VIP ≥ 1).
3. Результаты
3.1. Метаболомное профилирование лепестков космеи дваждыперистой трех разных окрасок
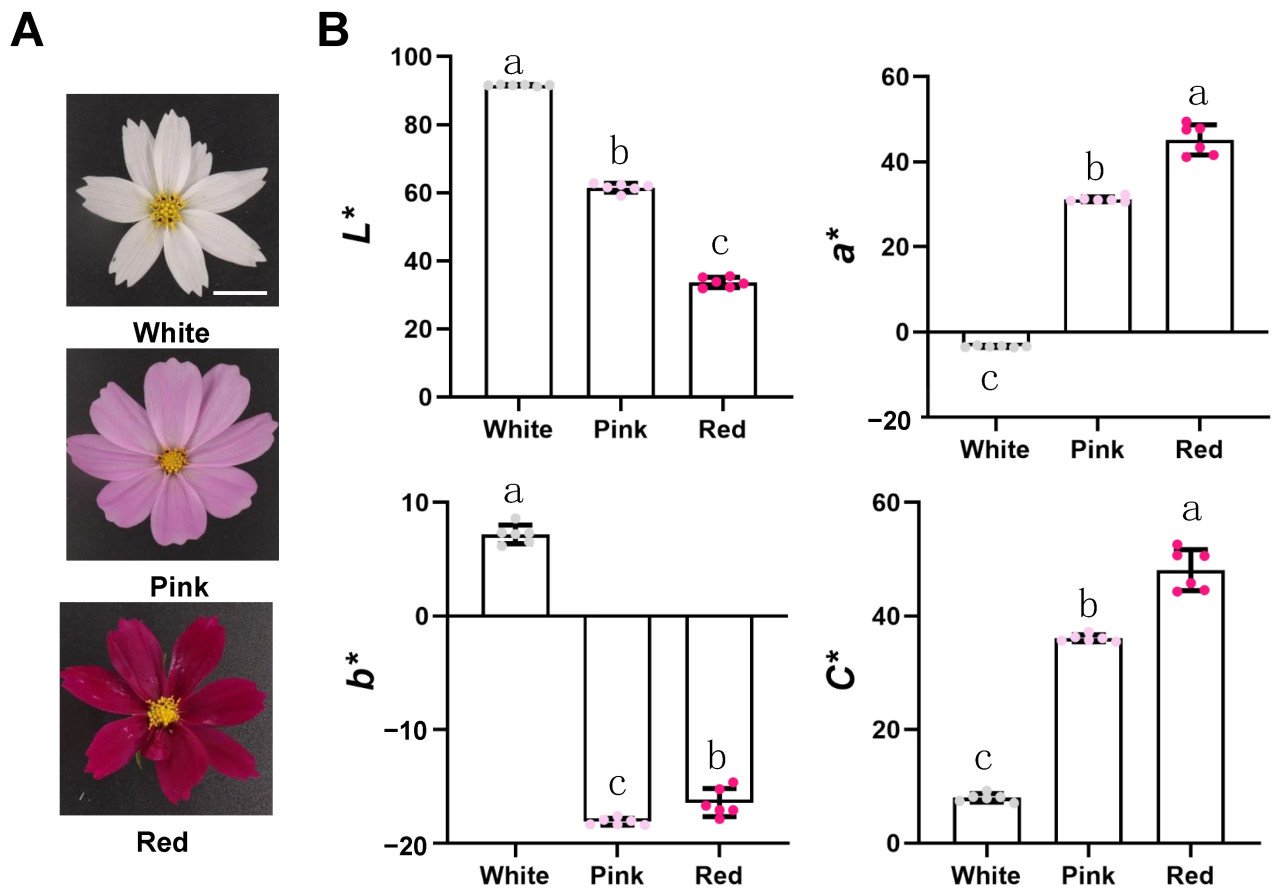
Цветущие белые, розовые и красные цветы являются объектами исследования (Рисунок 1A). Мы выполнили CIElab анализ фенотипов с использованием портативного колориметра Minolta CR-400 (Konica Minolta, Japan), различая белые, розовые и красные цветы (Рисунок 1B). Мы обнаружили, что их значения светлоты (L) постепенно уменьшались, в то время как значения хромы C постепенно увеличивались. В то же время мы обнаружили, что значение a белых цветов является отрицательным, значение a красных цветов значительно выше, чем у розовых цветов, и все они положительны; однако значение b белых, розовых и красных цветов, которое находится в диапазоне от синего до желтого, противоположно a.
Рисунок 1. Фенотип лепестков космеи дваждыперистой (Cosmos bipinnatus Cav.) с разной окраской цветков. Масштабные отрезки = 1 см. (A) Космея дваждыперистая с разной окраской цветков, а именно белой, розовой и красной. (B) Параметры цвета CIELab лепестков цветков трех разных окрасок. Планки погрешностей указывают стандартное отклонение шести биологических повторностей. Образцы, обозначенные разными буквами, значимо различаются (p < 0,05, ANOVA).
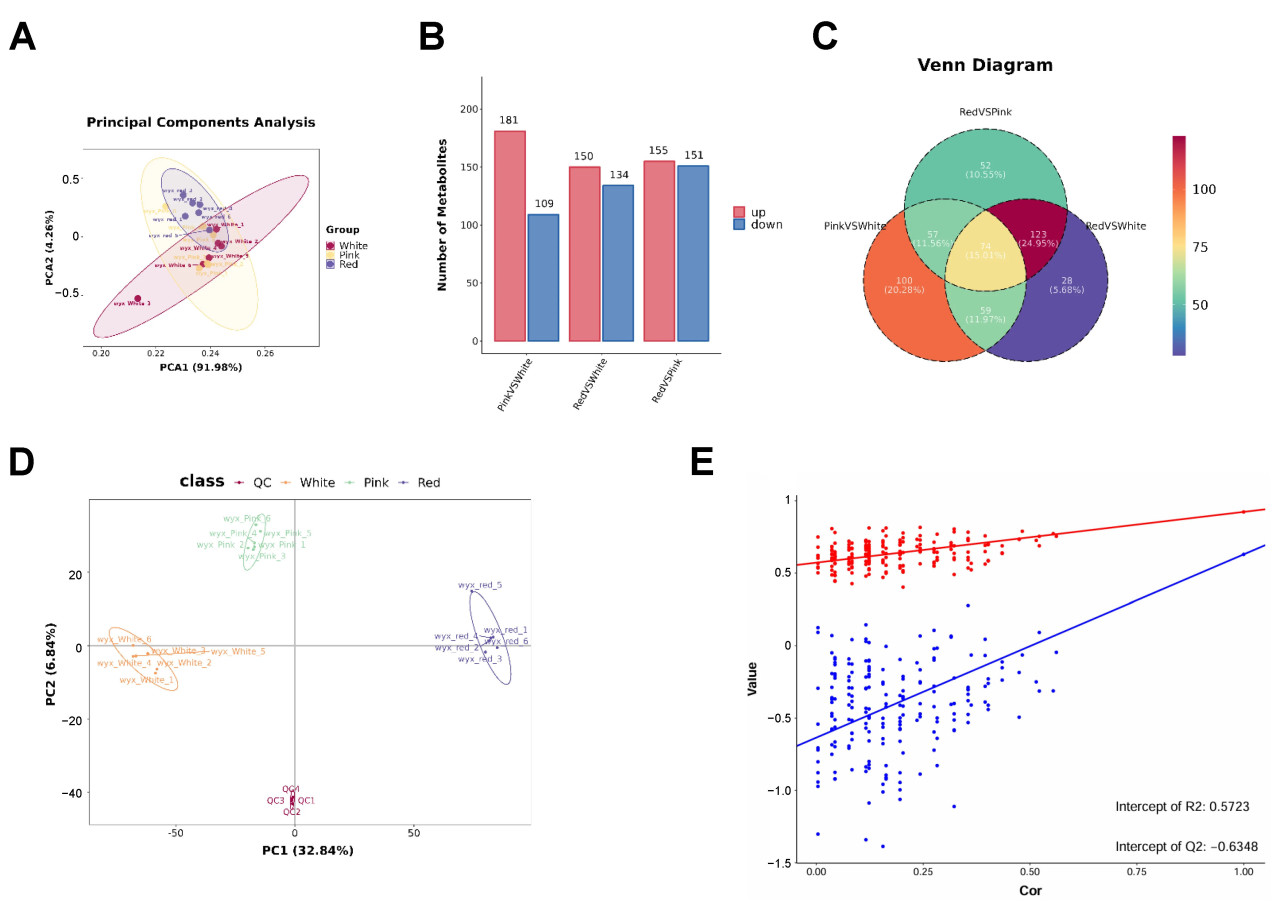
Для дальнейшего количественного определения общего профиля метаболитов был проведен анализ UPLC–MS/MS, чтобы дополнительно определить основные метаболические изменения между красными, розовыми и белыми цветками. Анализ главных компонент (PCA) показал значения PC1 91,98% и PC2 4,26% (Рисунок 2A). Всего мы идентифицировали 13 604 первичных метаболита и 1180 вторичных метаболитов. Было 181 вторичных метаболита, которые были значительно выше у розовых цветов, чем у белых, 150 вторичных метаболитов выше у красных, чем у белых, и 155 вторичных метаболитов выше у красных, чем у розовых. Однако было 109 вторичных метаболитов, которые были значительно ниже у розовых, чем у белых, 134 вторичных метаболита ниже у красных, чем у белых, и 151 вторичный метаболит ниже у красных, чем у розовых (Рисунок 2B). Было 74 вторичных метаболита, общих для всех трех попарных сравнений: красные против розовых, розовые против белых и красные против белых (Рисунок 2C).
Рисунок 2. Комплексный анализ профилей метаболитов в лепестках космеи дваждыперистой (Cosmos bipinnatus Cav.) с разной окраской цветков. (A) График анализа главных компонент (PCA), иллюстрирующий разделение профилей метаболитов на основе классов окраски цветков. (B) Столбчатая диаграмма, показывающая количество метаболитов, идентифицированных в каждом классе окраски цветков. (C) Диаграмма Венна, показывающая уникальные и общие метаболиты среди трех классов окраски цветков. (D,E) Комбинированный анализ графика PCA и точечной диаграммы указывает на хорошее разделение данных между разными группами и демонстрирует прогностическую точность модели.
Кроме того, мы провели многомерный статистический анализ метаболома с использованием PLS-DA (дискриминантный анализ методом наименьших квадратов), результаты которого показаны на Рисунке 2D,E. График оценок PLS-DA показал PC1 32,84% и PC2 6,84%. Каждая точка на графике представляет образец, причем разные группы отображены разными цветами. Относительное положение каждой точки представляет степень дисперсии между образцами. Этот рисунок указывает на то, что паттерны экспрессии внутри трех групп схожи, но различаются между группами (Рисунок 2D). Наконец, график теста перестановок указывает на то, что метаболомная модель не переобучена (Рисунок 2E).
3.2. Определение ключевых метаболических путей
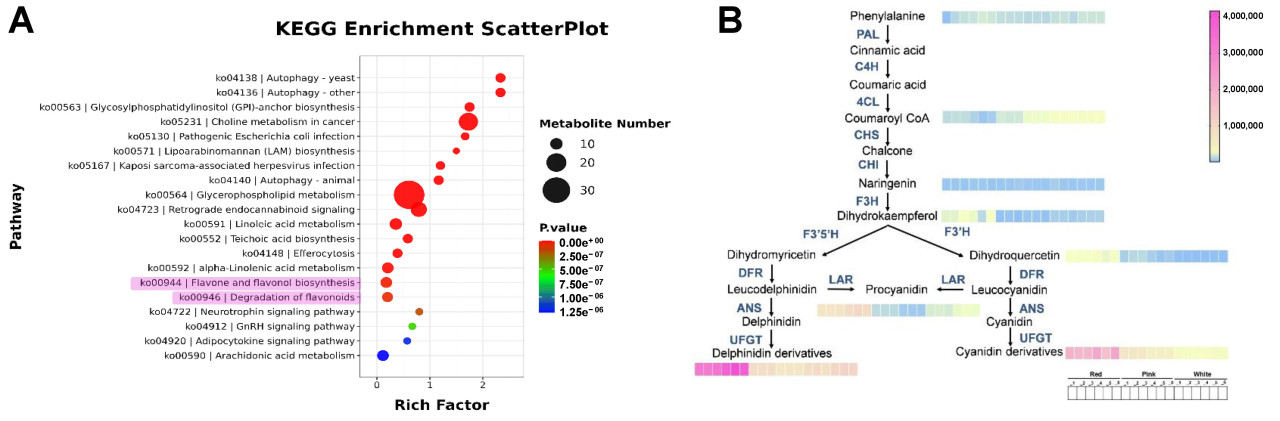
Для дальнейшего анализа дифференциальных метаболитов и их функций мы провели анализ обогащения KEGG (Kyoto Encyclopedia of Genes and Genomes) дифференциальных метаболитов. Как показано на Рисунке 3A, пути, по которым обогащаются дифференциальные метаболиты, включают пути, связанные с метаболизмом флавоноидов.
Рисунок 3. Анализ метаболических путей. (A) Точечный график обогащения KEGG. Размер точек представляет количество метаболитов, участвующих в каждом пути, причем большие точки указывают на большее количество. Цветовая градиентная шкала от синего к красному обозначает p-значение, причем красный указывает на более значимое обогащение. (B) Схема метаболического пути. Стрелки указывают направление метаболического потока, а цветовая градиентная шкала от синего к розовому представляет количество метаболитов, причем розовый указывает на большее количество.
С целью понимания тенденции изменений метаболитов мы построили карту метаболических путей KEGG (Рисунок 3B). Результаты показывают, что на ранних стадиях метаболизма нет значимой разницы в содержании фенилаланина между тремя группами. В метаболическом пути флавоноидов содержание первого предшественника, Coumaroyl CoA, значительно выше в белой группе, чем в розовой, которая, в свою очередь, выше, чем в красной группе. Это может быть связано с тем, что биосинтез большего количества антоцианов требует катализа большего количества веществ-предшественников. Однако нет значимой разницы в содержании промежуточного продукта нарингенина между вышеуказанными группами, но его нижестоящие промежуточные продукты, дигидрокемпферол и дигидрокверцетин, показывают тенденцию к значительно более высокому содержанию в красной группе. Аналогично, красная группа также имеет значительно более высокое содержание, чем другие две группы, в отношении пигментных веществ, включая проантоцианидины, производные дельфинидина и производные цианидина. Вышеуказанные результаты предварительно свидетельствуют о том, что на различную окраску цветков космеи дваждыперистой влияет метаболизм антоцианов.
3.3. Идентификация дифференциально экспрессирующихся генов (DEG) с помощью транскриптома
Общая РНК, экстрагированная из цветков различной окраски, отобранных на стадии цветения, послужила матрицей для RNA-seq анализа. Всего было получено девять образцов (по три биологических повторности для каждого из трех окрашенных цветков). Результатом процедуры сборки стал набор из 180 912 транскриптных последовательностей с N50 1976 п.н., содержанием GC 39,31% и набор из 57 971 генных последовательностей с N50 1633 п.н. и содержанием GC 39,37% (Таблица S1).
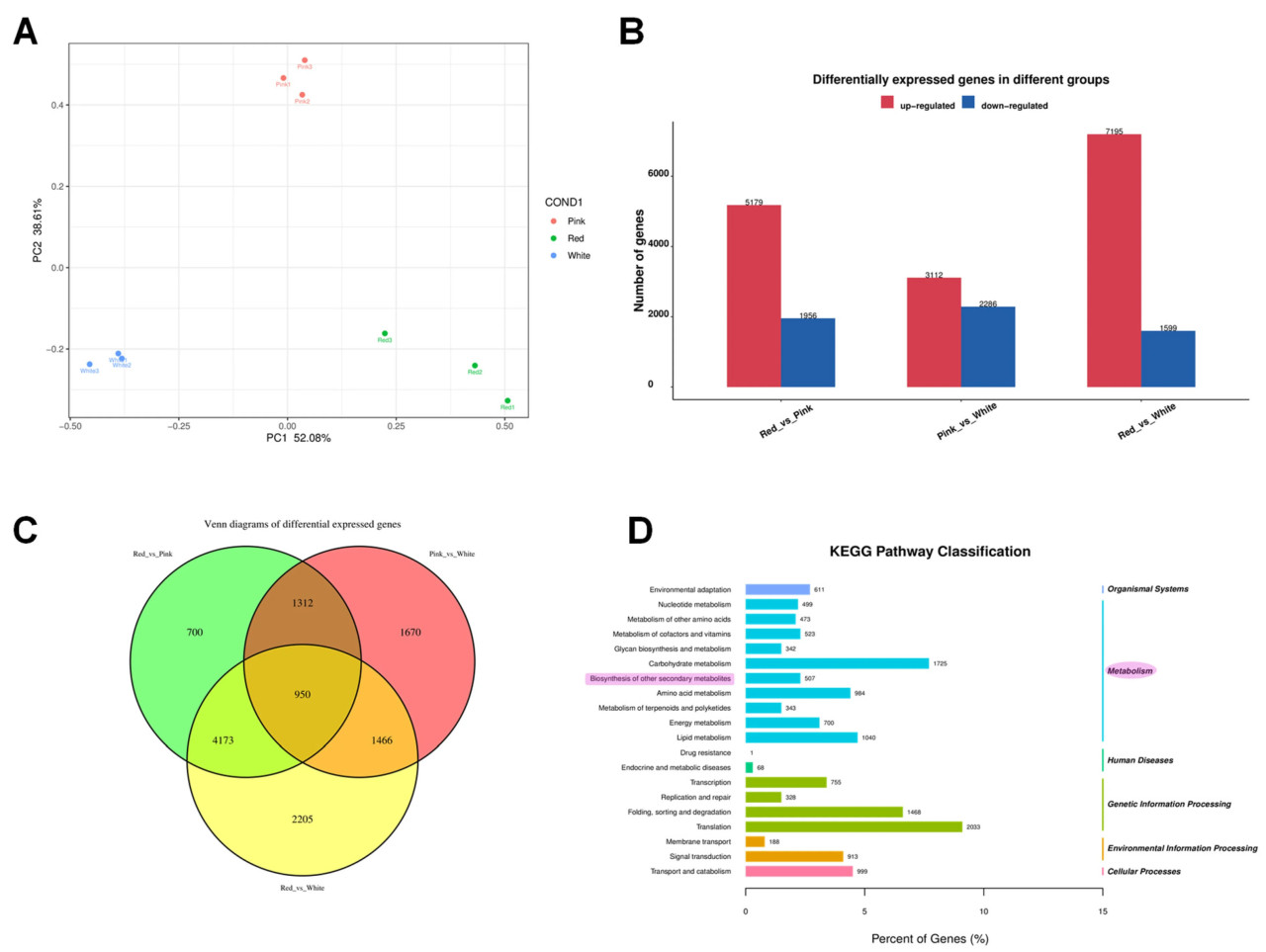
Анализ главных компонент (PCA) показал, что PC1 составил 52,08%, а PC2 — 38,61%, и график PCA иллюстрирует четкое различие в генетической экспрессии между белыми, розовыми и красными группами (Рисунок 4A). Дифференциально экспрессирующиеся гены (DEG) были проанализированы путем попарных сравнений транскриптомов между цветками различной окраски (белыми, розовыми и красными) (FDR ≤ 0,05 и |log2FC| ≥ 1) (Рисунок 4B). Было 5179 генов со значительно более высокой экспрессией у красных, чем у розовых цветков, 3112 генов с более высокой экспрессией у розовых, чем у белых, и 7195 генов с более высокой экспрессией у красных, чем у белых. Однако было 1956 генов со значительно более низкой экспрессией у красных, чем у розовых цветков, 2286 генов с более низкой экспрессией у розовых, чем у белых, и 1599 генов с более низкой экспрессией у красных, чем у белых (Рисунок 4B). Было 950 DEG, общих для всех трех попарных сравнений: красные против розовых, розовые против белых и красные против белых (Рисунок 4C).
Рисунок 4. Комплексный анализ дифференциальной экспрессии генов и классификации путей у космеи дваждыперистой (Cosmos bipinnatus Cav.). (A) График анализа главных компонент (PCA), показывающий распределение образцов в различных группах окраски цветков. (B) Столбчатая диаграмма, представляющая количество дифференциально экспрессирующихся генов (DEG) в разных группах. Красные столбцы указывают на гены с повышенной регуляцией, а синие столбцы — на гены с пониженной регуляцией. Группы сравнения обозначены как "Red_vs._Pink", "Pink_vs._White" и "Red_vs._White". (C) Диаграмма Венна, иллюстрирующая пересечение дифференциально экспрессирующихся генов среди трех групп. Числа в каждом разделе представляют количество уникальных и общих генов в различных группах. (D) Классификация путей KEGG для дифференциально экспрессирующихся генов. Столбчатая диаграмма показывает количество генов, связанных с каждой категорией пути.
3.4. Функциональный анализ DEG
Чтобы глубже понять транскрипционную регуляцию генов, лежащих в основе изменений метаболитов между группами с различной окраской цветков (белой, розовой и красной), мы выполнили анализ обогащения KEGG для дифференциально экспрессирующихся генов, который указал на их обогащение вторичными метаболитами (Рисунок 4D).
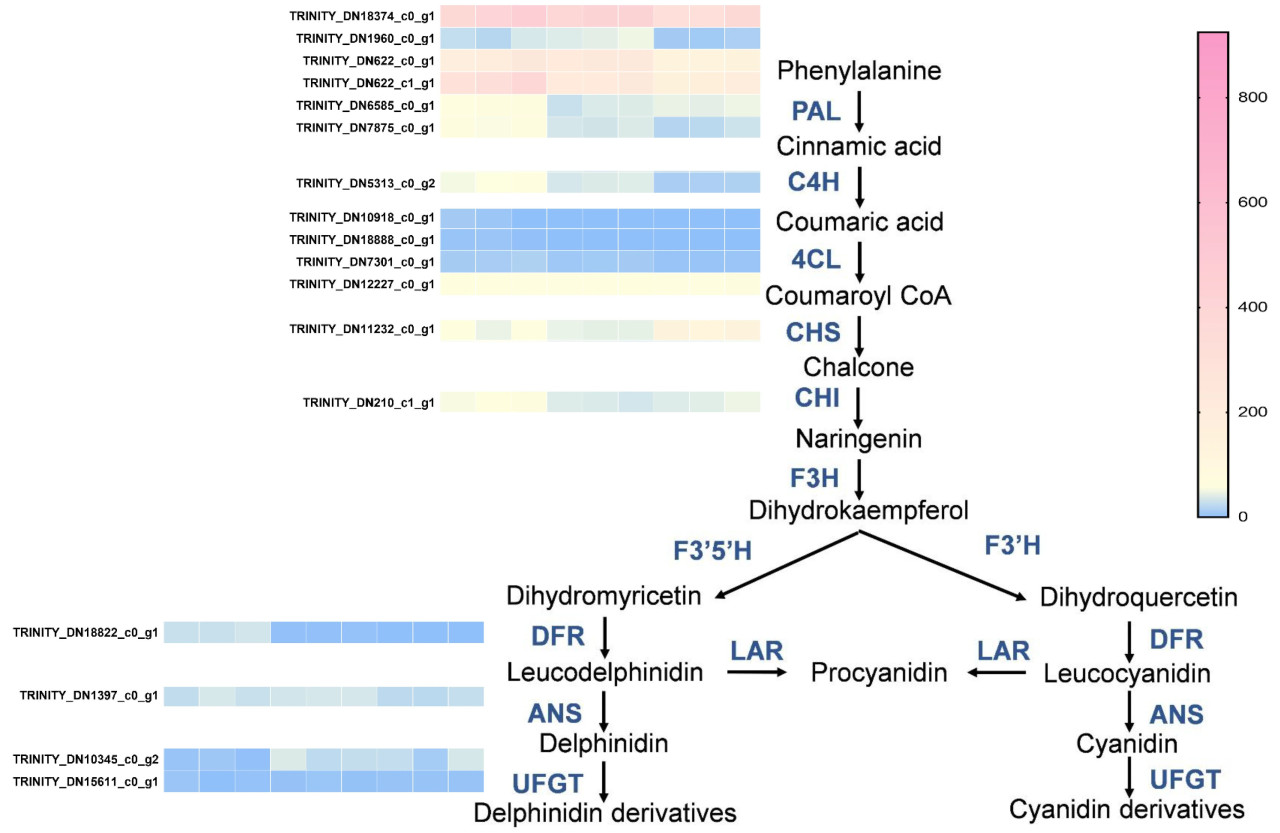
После этого мы проанализировали экспрессию структурных генов в метаболическом пути фенилаланина и пути синтеза антоцианов. Этот анализ поможет выяснить, как экспрессия этих генов способствует наблюдаемым изменениям метаболитов и, возможно, различиям в окраске цветков. Мы обнаружили, что экспрессия генов PAL (TRINITY_DN18304_c0_g1, TRINITY_DN1960_c0_g1, TRINITY_DN622_c0_g1, TRINITY_DN622_c1_g1, TRINITY_DN6585_c0_g1, TRINITY_DN7875_c0_g1) и C4H (TRINITY_DN5313_c0_g2) была повышена в красной и розовой группах по сравнению с белой группой, в то время как экспрессия 4CL (TRINITY_DN10918_c0_g1, TRINITY_DN18888_c0_g1, TRINITY_DN7301_c0_g1, TRINITY_DN12227_c0_g1) не показала значимых различий между тремя группами. В метаболическом пути флавоноидов CHI (TRINITY_DN210_c1_g1) и DFR (TRINITY_DN18822_c0_g1) проявляли тенденцию к повышению регуляции в красных группах. Однако экспрессия CHS (TRINITY_DN11232_c0_g1), ANS (TRINITY_DN1397_c0_g1) и UFGT (TRINITY_DN10345_c0_g2, TRINITY_DN15611_c0_g1) в метаболическом пути флавоноидов значимо не изменилась (Рисунок 5).
Рисунок 5. Анализ дифференциально экспрессирующихся генов (DEG) в разных группах путей биосинтеза флавоноидов. Тепловая карта, иллюстрирующая уровни экспрессии генов, участвующих в пути биосинтеза флавоноидов в различных группах. Цветовая градиентная шкала от синего к розовому представляет низкие и высокие уровни экспрессии соответственно. Гены обозначены их соответствующими идентификаторами Trinity.
3.5. Идентификация кандидатных членов комплекса MBW в дифференциально экспрессирующихся генах
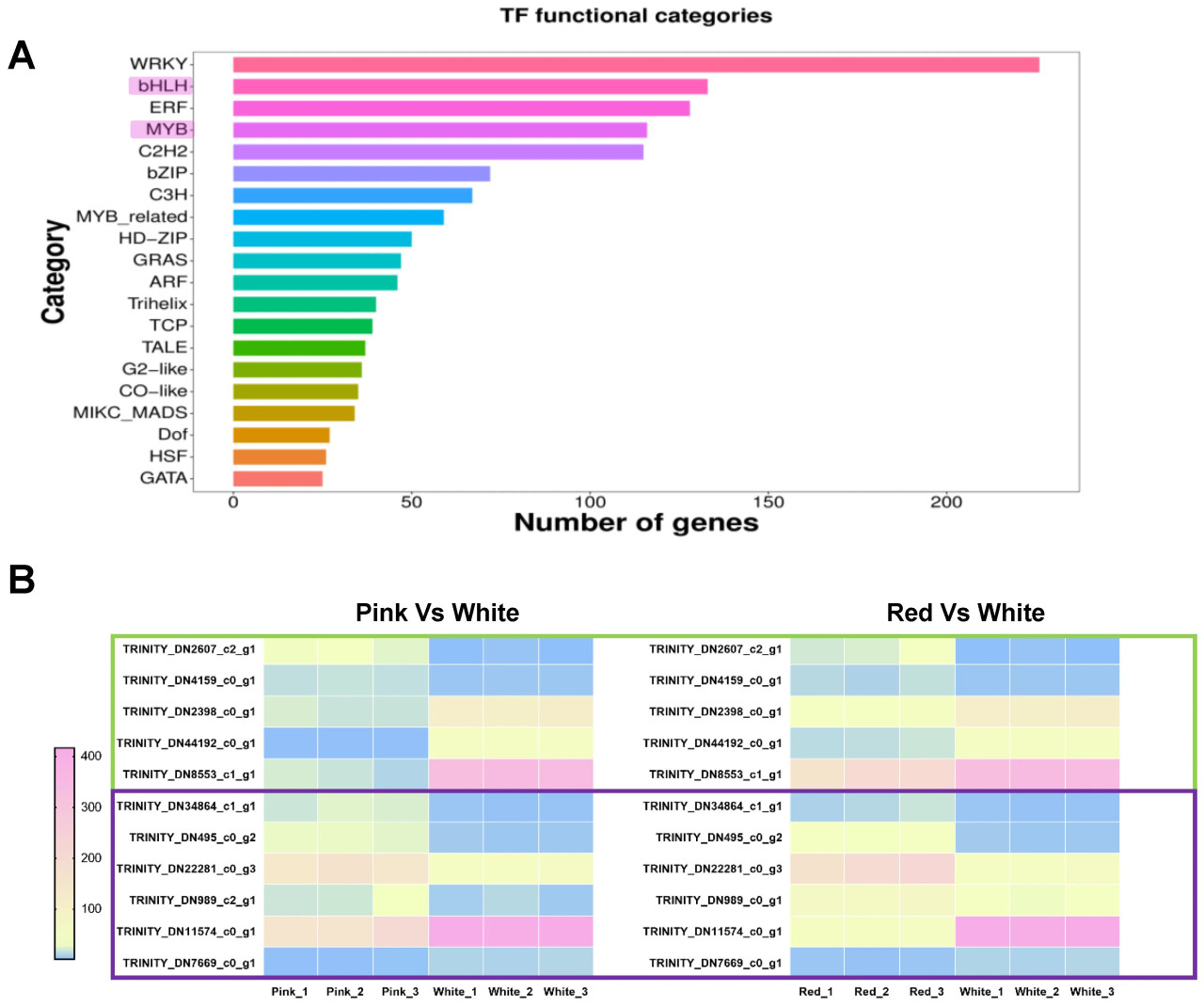
В предыдущих исследованиях регуляции метаболизма биосинтеза антоцианов было обнаружено, что путь биосинтеза антоцианов у растений регулируется белковым комплексом MBW, которым является MYB-bHLH-WD40 [34,35], причем MYB-bHLH играет ключевую роль [36,37,38]. Для дальнейшего изучения механизмов регуляции биосинтеза антоцианов у различно окрашенной космеи дваждыперистой мы дополнительно проанализировали дифференциально экспрессирующиеся транскрипционные факторы MYB и bHLH из данных транскриптомного секвенирования. Как показано на рисунке, мы получили в общей сложности 133 дифференциально экспрессирующихся транскрипционных фактора bHLH и 116 транскрипционных факторов MYB (Рисунок 6A). Для дальнейшего выявления ключевых регуляторных факторов, участвующих в регуляции биосинтеза антоцианов в различно окрашенных лепестках, мы отобрали транскрипционные факторы, которые были дифференциально экспрессированы как в группах красные против белых, так и розовые против белых, как показано на рисунке, включая пять TF bHLH, из которых два с повышенной регуляцией (TRINITY_DN2607_c2_g1, TRINITY_DN4159_c0_g1) и три с пониженной регуляцией (TRINITY_DN2398_c0_g1, TRINITY_DN44192_c0_g1, TRINITY_DN8553_c1_g1); и шесть TF MYB, из которых четыре с повышенной регуляцией (TRINITY_DN34864_c1_g1, TRINITY_DN495_c0_g2, TRINITY_DN22281_c0_g3, TRINITY_DN989_c2_g1) и два с пониженной регуляцией (TRINITY_DN11574_c0_g1, TRINITY_DN7669_c0_g1) (Рисунок 6B).
Рисунок 6. Анализ функциональных категорий транскрипционных факторов (TF) и паттернов экспрессии. (A) Столбчатая диаграмма, показывающая количество генов, связанных с различными функциональными категориями транскрипционных факторов (TF). Категории перечислены на оси Y, а количество генов представлено на оси X. (B) Тепловая карта иллюстрирует паттерны экспрессии транскрипционных факторов MYB и bHLH, которые дифференциально экспрессируются как в сравнениях групп красные против белых, так и розовые против белых. Цветовая градиентная шкала от синего к розовому представляет низкие и высокие уровни экспрессии. Гены обозначены их соответствующими идентификаторами Trinity, причем зеленые рамки указывают на транскрипционные факторы bHLH, а фиолетовые рамки — на транскрипционные факторы MYB.
Кроме того, чтобы изучить потенциальные функции вышеуказанных транскрипционных факторов в биосинтезе антоцианов у космеи дваждыперистой, мы построили и проанализировали филогенетическое дерево, результаты показаны в дополнительных материалах (Рисунки S1 и S2). На двух филогенетических деревьях красным цветом обозначены кандидатные положительные регуляторные факторы, полученные в результате анализа дифференциально экспрессирующихся транскрипционных факторов в транскриптомах цветков различной окраски, а синим цветом — кандидатные отрицательные регуляторные факторы.
На филогенетическом дереве bHLH (Рисунок S1), среди белков арабидопсиса, наиболее тесно связанных с нашими кандидатными транскрипционными факторами bHLH, подавляющее большинство еще не охарактеризованы в связи с метаболизмом флавоноидов растений. Только AtbHLH1, который наиболее тесно связан с Trinity DN2398 c0_g1, как было показано в многочисленных предыдущих исследованиях, является членом белкового комплекса MBW арабидопсиса, играющим положительную регуляторную роль в биосинтезе флавоноидов [14,39,40]. Это отличается от нашего идентифицированного Trinity DN2398 c0_g1 как кандидатного отрицательного регуляторного фактора в биосинтезе флавоноидов у космеи дваждыперистой, что предполагает, что гомологичные гены могут играть разные роли у разных видов и требуют дальнейшего изучения.
На филогенетическом дереве MYB (Рисунок S2) Trinity DN11574 c0_g1 наиболее тесно связан с MYB4 арабидопсиса, который охарактеризован как отрицательный регулятор антоцианов [41]. Однако биологическая функция у арабидопсиса гомологичных транскрипционных факторов Trinity DN7669 c0_g1 в отношении биосинтеза флавоноидов в настоящее время неясна. Белок Trinity DN989 c1_g1 наиболее тесно связан с MYB20 и MYB43 арабидопсиса, которые охарактеризованы как положительные регуляторы биосинтеза фенилаланина и лигнина [42]. Это предполагает, что наш кандидатный TF Trinity DN989 c1_g1 может быть вовлечен в регуляцию биосинтеза фенилаланина в вышестоящем пути биосинтеза флавоноидов. Два транскрипционных фактора арабидопсиса, наиболее тесно связанные с Trinity DN34864 c1 g1, MYB106 и MYB118, еще не были охарактеризованы как участвующие в метаболизме флавоноидов. Белки Trinity DN495 c0_g2 и DN2281 c0_g3 имеют наиболее близкую гомологию с транскрипционным фактором MYB57 арабидопсиса, который охарактеризован как стимулирующий накопление флавоноидов путем положительной регуляции экспрессии AtFLS1 [43]. Это предполагает, что наши два кандидатных транскрипционных фактора могут положительно регулировать путь ветвления метаболизма флавоноидов у различных цветков.
3.6. Регуляторная сеть предполагаемых путей биосинтеза флавоноидов и антоцианидинов
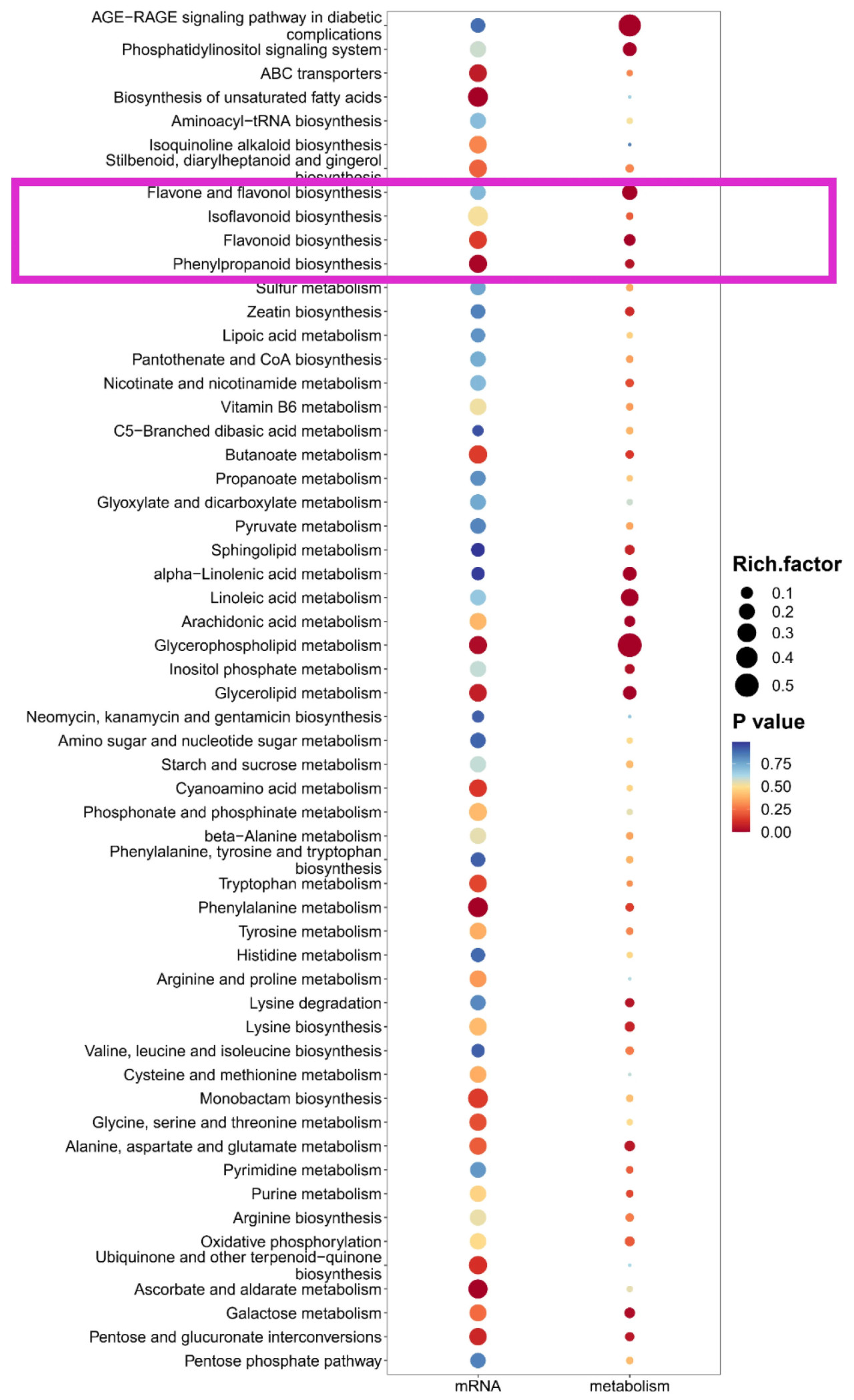
Чтобы обойти ограничения одноомиксного анализа, мы провели совместный анализ данных транскриптома и метаболома, полученных от цветков различной окраски. Результаты показаны на рисунке: при комбинированном анализе трех групп, а именно красные против белых, красные против розовых и розовые против белых, мы идентифицировали метаболические пути биосинтеза флавонов и флавонолов, биосинтеза изофлавоноидов, биосинтеза флавоноидов и биосинтеза фенилпропаноидов (Рисунок 7 и Рисунок S3). Среди четырех вышеуказанных путей, за исключением мРНК биосинтеза флавонов и флавонолов, другие пузырьки показывают красную цветовую гамму, указывая на значимое обогащение в соответствующих путях. Это дополнительно указывает на то, что формирование различной окраски лепестков цветков регулируется различиями в метаболизме фенилаланина и флавоноидов, а также связанными структурными генами и вышестоящими кандидатными транскрипционными факторами, которые предоставляют генетический резерв для последующего руководства направленной селекцией окраски цветков.
Рисунок 7. Интегрированный анализ обогащения транскриптомики и метаболомики между розовыми и белыми цветками. На оси X перечислены метаболические пути, причем p-значение представлено градиентом от синего к красному, где красный указывает на более значимое обогащение (более низкое p-значение), а размер каждого пузырька соответствует степени обогащения. Розовая рамка представляет метаболизм флавоноидов и связанные с ним метаболические пути.
4. Обсуждение
Изменчивость окраски цветков была предметом пристального интереса из-за ее важнейшей роли в селекции растений и ее коммерческой ценности. Среди них метаболизм флавоноидов важен в определении окраски растений. Однако у космеи дваждыперистой неясные метаболические пути флавоноидов и их молекулярная регуляция в значительной степени ограничили селекцию окраски цветков. Антоцианы являются важными продуктами в метаболическом пути флавоноидов, и они широко распространены у растений в природе. Антоцианы могут придавать цветкам и плодам яркие цвета, такие как красный, пурпурный и синий. В прошлых исследованиях было обнаружено, что пути биосинтеза антоцианов высококонсервативны в ходе эволюции растений [44], и было обнаружено, что биосинтез антоцианов у растений регулируется как эндогенными, так и экзогенными факторами [45,46]. Наше исследование объединило анализ метаболома и транскриптома цветков различной окраски, показав в некоторой степени метаболизм и регуляцию антоцианов у цветков различной окраски, заложив основу для последующей молекулярной направленной селекции. Конечно, с развитием омиксных технологий, дальнейшее включение таких областей, как протеомика и модификационная омика, и проведение более комплексных интегрированных анализов на основе омикса [47] может предоставить более точную и эффективную помощь в раскрытии молекулярных механизмов, лежащих в основе формирования окраски цветков.
В нашем исследовании с помощью метаболомного анализа мы обнаружили, что различная окраска лепестков космеи дваждыперистой тесно связана с содержанием продуктов в метаболическом пути флавоноидов, особенно антоцианов, что согласуется с предыдущими исследованиями, показывающими, что антоцианы определяют окраску растений [2,3,4]. Кроме того, при дифференциальном транскриптомном анализе мы обнаружили, что гены биосинтеза PAL и C4H на ранних стадиях метаболического пути флавоноидов были значительно повышены в окрашенных цветках (Рисунок 5), что предполагает, что ранние гены биосинтеза могут играть ключевую роль в формировании различной окраски цветков у космеи дваждыперистой. Аналогично, комбинированный анализ транскриптомики и метаболомики дополнительно указывает на метаболический путь флавоноидов как на ключевой для наблюдаемых различий в окраске цветков космеи дваждыперистой. Это сходно с механизмом, с помощью которого пути метаболизма флавоноидов и их регуляция влияют на окраску растений у других видов, таких как декоративная яблоня [48] и хризантема [49].
Кроме того, наше исследование идентифицировало кандидатные транскрипционные факторы, регулирующие метаболизм флавоноидов, и построило для них филогенетическое дерево. Среди транскрипционных факторов арабидопсиса, наиболее тесно связанных с ними, некоторые уже охарактеризованы с точки зрения их регуляторной роли в биосинтезе антоцианов, такие как AtMYB4 [41] и AtbHLH1 [14,39,40] и др., в то время как функции других остаются неясными. Это также вдохновляет на последующую характеристику биологических функций идентифицированных нами кандидатных транскрипционных факторов в регуляции биосинтеза антоцианов. На более глубоком уровне, хотя канонический комплекс MBW был описан как участвующий в регуляции биосинтеза флавоноидов у многих видов, таких как TTG1-GL3/TT8-PAP1 у арабидопсиса [50], MYB6-bHLH2 у хризантемы [19] и AN4-AN1-AN11 [51] у петунии, взаимодействуют ли MYB и bHLH с образованием комплекса MBW и молекулярные механизмы регуляции синтеза антоцианов после их взаимодействия, ожидают дальнейшей проверки и изучения с помощью экспериментов молекулярной биологии. Конечно, феномен, заключающийся в том, что гомологичные гены играют разные роли у разных видов, также требует дополнительного внимания, как это видно на примере Trinity DN2398 c0_g1 и AtbHLH1 (Рисунок S1), что может означать, что гомологичные гены имеют разные биологические функции у разных видов.
Интеграция данных транскриптома и метаболома предоставляет нам более комплексную аналитическую перспективу, показывая регуляторную сеть, которая включает не только структурные гены, но и транскрипционные факторы, контролирующие экспрессию этих генов. Это закладывает прочную основу для изучения молекулярных основ формирования окраски цветков у растений космеи дваждыперистой, предлагая понимание разнообразия окрасок цветков и последующей направленной селекции по признаку окраски цветков, тем самым повышая эстетическую и коммерческую ценность декоративных растений.
Дополнительные материалы
Следующие вспомогательные материалы можно загрузить по адресу: https://www.mdpi.com/article/10.3390/agriculture15030255/s1; Рисунок S1: Филогенетическое дерево семейства транскрипционных факторов bHLH; Рисунок S2: Филогенетическое дерево семейства транскрипционных факторов MYB; Рисунок S3: Интегрированный анализ обогащения транскриптомики и метаболомики между красными и розовыми (A) и красными и белыми (B) цветками; Таблица S1: Сводка данных транскриптомного секвенирования для лепестков космеи дваждыперистой (Cosmos bipinnatus Cav.) трех разных окрасок; Таблица S2: Сводка использованных пакетов R.
Ссылки
1. Gao, H.-N.; Jiang, H.; Cui, J.-Y.; You, C.-X.; Li, Y.-Y. The effects of hormones and environmental factors on anthocyanin biosynthesis in apple. Plant Sci. 2021, 312, 111024. [Google Scholar] [CrossRef] [PubMed]
2. Grotewold, E. The genetics and biochemistry of floral pigments. Annu. Rev. Plant Biol. 2006, 57, 761–780. [Google Scholar] [CrossRef] [PubMed]
3. Tanaka, Y.; Sasaki, N.; Ohmiya, A. Biosynthesis of plant pigments: Anthocyanins, betalains and carotenoids. Plant J. 2008, 54, 733–749. [Google Scholar] [CrossRef] [PubMed]
4. Zhao, D.; Tao, J. Recent advances on the development and regulation of flower color in ornamental plants. Front. Plant Sci. 2015, 6, 261. [Google Scholar] [CrossRef]
5. Lepiniec, L.; Debeaujon, I.; Routaboul, J.-M.; Baudry, A.; Pourcel, L.; Nesi, N.; Caboche, M. Genetics and biochemistry of seed flavonoids. Annu. Rev. Plant Biol. 2006, 57, 405–430. [Google Scholar] [CrossRef]
6. Lu, C.; Li, Y.; Wang, J.; Qu, J.; Chen, Y.; Chen, X.; Huang, H.; Dai, S. Flower color classification and correlation between color space values with pigments in potted multiflora chrysanthemum. Sci. Hortic. 2021, 283, 110082. [Google Scholar] [CrossRef]
7. Tanaka, Y.; Brugliera, F.; Chandler, S. Seeing is believing: Engineering anthocyanin and carotenoid biosynthetic pathways. Curr. Opin. Biotechnol. 2008, 19, 190–197. [Google Scholar] [CrossRef]
8. Tanaka, Y.; Brugliera, F. Flower colour and cytochromes P450. Philos. Trans. R. Soc. London. Ser. B Biol. Sci. 2013, 368, 20120432. [Google Scholar] [CrossRef]
9. Bakowska-Barczak, A. Acylated anthocyanins as stable, natural food colorants—A review. Pol. J. Food Nutr. Sci. 2005, 14, 55. [Google Scholar]
10. Yabuya, T.; Nakamura, M.; Iwashina, T.; Yamaguchi, M.; Takehara, T. Anthocyanin-flavone copigmentation in bluish purple flowers of Japanese garden iris (Iris ensata Thunb.). Euphytica 1997, 98, 163–167. [Google Scholar] [CrossRef]
11. Barnard, H.; Dooley, A.N.; Areshian, G.; Gasparyan, B.; Faull, K. Chemical evidence for wine production around 4000 BCE in the Late Chalcolithic Near Eastern highlands. J. Archaeol. Sci. 2011, 38, 977–984. [Google Scholar] [CrossRef]
12. Wang, Y.; Zhou, L.-J.; Wang, Y.; Liu, S.; Chen, F. Functional identification of a flavone synthase and a flavonol synthase genes affecting flower color formation in Chrysanthemum morifolium. Plant Physiol. Biochem. 2021, 166, 1109–1120. [Google Scholar] [CrossRef] [PubMed]
13. Dubos, C.; Stracke, R.; Grotewold, E.; Weisshaar, B.; Martin, C.; Lepiniec, L. MYB transcription factors in Arabidopsis. Trends Plant Sci. 2010, 15, 573–581. [Google Scholar] [CrossRef] [PubMed]
14. Gonzalez, A.; Zhao, M.; Leavitt, J.M.; Lloyd, A.M. Regulation of the anthocyanin biosynthetic pathway by the TTG1/bHLH/Myb transcriptional complex in Arabidopsis seedlings. Plant J. 2008, 53, 814–827. [Google Scholar] [CrossRef] [PubMed]
15. Albert, N.W.; Lewis, D.H.; Zhang, H.; Irving, L.J.; Jameson, P.E.; Davies, K.M. Light-induced vegetative anthocyanin pigmentation in Petunia. J. Exp. Bot. 2009, 60, 2191–2202. [Google Scholar] [CrossRef]
16. Jaakola, L.; Hohtola, A. Effect of latitude on flavonoid biosynthesis in plants. Plant Cell Env. 2010, 33, 1239–1247. [Google Scholar] [CrossRef] [PubMed]
17. Imène, H.; Heppel, S.C.; Jérémy, P.; Céline, L.; Stefan, C.; Serge, D.; Virginie, L.; Jochen, B. The Basic Helix-Loop-Helix Transcription Factor MYC1 Is Involved in the Regulation of the Flavonoid Biosynthesis Pathway in Grapevine. Mol. Plant 2010, 3, 509–523. [Google Scholar]
18. Petroni, K.; Tonelli, C. Recent advances on the regulation of anthocyanin synthesis in reproductive organs. Plant Sci. 2011, 181, 219–229. [Google Scholar] [CrossRef] [PubMed]
19. Xiang, L.-l.; Liu, X.-f.; Li, X.; Yin, X.-r.; Grierson, D.; Li, F.; Chen, K.-s. A Novel bHLH Transcription Factor Involved in Regulating Anthocyanin Biosynthesis in Chrysanthemums (Chrysanthemum morifolium Ramat.). PLoS ONE 2015, 10, e0143892. [Google Scholar] [CrossRef] [PubMed]
20. Xiang, L.; Liu, X.; Shi, Y.; Li, Y.; Li, W.; Li, F.; Chen, K. Comparative Transcriptome Analysis Revealed Two Alternative Splicing bHLHs Account for Flower Color Alteration in Chrysanthemum. Int. J. Mol. Sci. 2021, 22, 12769. [Google Scholar] [CrossRef]
21. Zhou, L.-J.; Geng, Z.; Wang, Y.; Wang, Y.; Liu, S.; Chen, C.; Song, A.; Jiang, J.; Chen, S.; Chen, F. A novel transcription factor CmMYB012 inhibits flavone and anthocyanin biosynthesis in response to high temperatures in chrysanthemum. Hortic. Res. 2021, 8, 248. [Google Scholar] [CrossRef]
22. Wang, Y.; Zhou, L.-J.; Wang, Y.; Geng, Z.; Liu, S.; Chen, C.; Chen, S.; Jiang, J.; Chen, F. CmMYB9a activates floral coloration by positively regulating anthocyanin biosynthesis in chrysanthemum. Plant Mol. Biol. 2022, 108, 51–63. [Google Scholar] [CrossRef]
23. Wang, Y.; Zhou, L.-J.; Wang, Y.; Geng, Z.; Ding, B.; Jiang, J.; Chen, S.; Chen, F. An R2R3-MYB transcription factor CmMYB21 represses anthocyanin biosynthesis in color fading petals of chrysanthemum. Sci. Hortic. 2022, 293, 110674. [Google Scholar] [CrossRef]
24. Xiang, L.; Liu, X.; Li, H.; Yin, X.; Grierson, D.; Li, F.; Chen, K. CmMYB#7, an R3 MYB transcription factor, acts as a negative regulator of anthocyanin biosynthesis in chrysanthemum. J. Exp. Bot. 2019, 70, 3111–3123. [Google Scholar] [PubMed]
25. Hu, Q.; Yang, L.; Liu, S.; Zhou, L.; Wang, X.; Wang, W.; Cai, L.; Wu, X.; Chang, Y.; Wang, S. A repressor motif-containing poplar R3 MYB-like transcription factor regulates epidermal cell fate determination and anthocyanin biosynthesis in Arabidopsis. J. Plant Biol. 2016, 59, 525–535. [Google Scholar] [CrossRef]
26. Shin, D.H.; Choi, M.; Kim, K.; Bang, G.; Cho, M.; Choi, S.-B.; Choi, G.; Park, Y.-I. HY5 regulates anthocyanin biosynthesis by inducing the transcriptional activation of the MYB75/PAP1 transcription factor in Arabidopsis. FEBS Lett. 2013, 587, 1543–1547. [Google Scholar] [CrossRef]
27. Zhou, L.-J.; Li, Y.-Y.; Zhang, R.-F.; Zhang, C.-L.; Xie, X.-B.; Zhao, C.; Hao, Y.-J. The small ubiquitin-like modifier E3 ligase MdSIZ1 promotes anthocyanin accumulation by sumoylating MdMYB1 under low-temperature conditions in apple. Plant Cell Environ. 2017, 40, 2068–2080. [Google Scholar] [CrossRef] [PubMed]
28. Kim, J.; Woo, H.R.; Nam, H.G. Toward systems understanding of leaf senescence: An integrated multi-omics perspective on leaf senescence research. Mol. Plant Pathol. 2016, 9, 813–825. [Google Scholar] [CrossRef] [PubMed]
29. Zhang, T.; Hu, Y.; Jiang, W.; Fang, L.; Guan, X.; Chen, J.; Zhang, J.; Saski, C.A.; Scheffler, B.E.; Stelly, D.M. Sequencing of allotetraploid cotton (Gossypium hirsutum L. acc. TM-1) provides a resource for fiber improvement. Nat. Biotechnol. 2015, 33, 531–537. [Google Scholar] [CrossRef]
30. Jordan, K.W.; Nordenstam, J.; Lauwers, G.Y.; Rothenberger, D.A.; Alavi, K.; Garwood, M.; Cheng, L.L. Metabolomic characterization of human rectal adenocarcinoma with intact tissue magnetic resonance spectroscopy. Dis. Colon Rectum 2009, 52, 520. [Google Scholar] [CrossRef] [PubMed]
31. Chen, S.; Zhang, L.; Xu, X.; Lv, H.; Yang, Y. Studies on factors influence UV-absorbance and color value of microencapsulated lutein. China Food Addit. 2013, 4, 100–102. [Google Scholar]
32. Gonnet, J.-F. Colour effects of co-pigmentation of anthocyanins revisited-1. A colorimetric definition using the CIELAB scale. Food Chem. 1998, 63, 409–415. [Google Scholar] [CrossRef]
33. Lyu, F.; Han, F.; Ge, C.; Mao, W.; Chen, L.; Hu, H.; Chen, G.; Lang, Q.; Fang, C. OmicStudio: A composable bioinformatics cloud platform with real-time feedback that can generate high-quality graphs for publication. iMeta 2023, 2, e85. [Google Scholar] [CrossRef] [PubMed]
34. Hong, Y.; Lv, Y.; Zhang, J.; Ahmad, N.; Li, X.; Yao, N.; Liu, X.; Li, H. The safflower MBW complex regulates HYSA accumulation through degradation by the E3 ligase CtBB1. J. Integr. Plant Biol. 2023, 65, 1277–1296. [Google Scholar] [CrossRef]
35. Lloyd, A.; Brockman, A.; Aguirre, L.; Campbell, A.; Bean, A.; Cantero, A.; Gonzalez, A. Advances in the MYB-bHLH-WD Repeat (MBW) Pigment Regulatory Model: Addition of a WRKY Factor and Co-option of an Anthocyanin MYB for Betalain Regulation. Plant Cell Physiol. 2017, 58, 1431–1441. [Google Scholar] [CrossRef]
36. Sun-Hyung, L.; Da-Hye, K.; Kim, J.K.; Jong-Yeol, L.; Sun-Hwa, H. A Radish Basic Helix-Loop-Helix Transcription Factor, RsTT8 Acts a Positive Regulator for Anthocyanin Biosynthesis. Front. Plant Sci. 2017, 8, 1917. [Google Scholar]
37. Liu, X.-F.; Yin, X.-R.; Allan, A.C.; Lin-Wang, K.; Shi, Y.-N.; Huang, Y.-J.; Ferguson, I.B.; Xu, C.-J.; Chen, K.-S. The role of MrbHLH1 and MrMYB1 in regulating anthocyanin biosynthetic genes in tobacco and Chinese bayberry (Myrica rubra) during anthocyanin biosynthesis. Plant Cell Tissue Organ Cult. 2013, 115, 285–298. [Google Scholar] [CrossRef]
38. Lai, B.; Du, L.-N.; Liu, R.; Hu, B.; Su, W.-B.; Qin, Y.-H.; Zhao, J.-T.; Wang, H.-C.; Hu, G.-B. Two LcbHLH transcription factors interacting with LcMYB1 in regulating late structural genes of anthocyanin biosynthesis in Nicotiana and Litchi chinensis during anthocyanin accumulation. Front. Plant Sci. 2016, 7, 106. [Google Scholar] [CrossRef] [PubMed]
39. Zhang, F.; Gonzalez, A.; Zhao, M.; Payne, C.T.; Lloyd, A. A network of redundant bHLH proteins functions in all TTG1-dependent pathways of Arabidopsis. Development 2003, 130, 4859–4869. [Google Scholar] [CrossRef]
40. Cominelli, E.; Gusmaroli, G.; Allegra, D.; Galbiati, M.; Wade, H.K.; Jenkins, G.I.; Tonelli, C. Expression analysis of anthocyanin regulatory genes in response to different light qualities in Arabidopsis thaliana. J. Plant Physiol. 2008, 165, 886–894. [Google Scholar] [CrossRef]
41. Wang, X.-C.; Wu, J.; Guan, M.-L.; Zhao, C.-H.; Geng, P.; Zhao, Q. Arabidopsis MYB4 plays dual roles in flavonoid biosynthesis. Plant J. 2020, 101, 637–652. [Google Scholar] [CrossRef]
42. Geng, P.; Zhang, S.; Liu, J.; Zhao, C.; Wu, J.; Cao, Y.; Fu, C.; Han, X.; He, H.; Zhao, Q. MYB20, MYB42, MYB43, and MYB85 regulate phenylalanine and lignin biosynthesis during secondary cell wall formation. Plant Physiol. 2020, 182, 1272–1283. [Google Scholar] [CrossRef] [PubMed]
43. Zhang, X.; He, Y.; Li, L.; Liu, H.; Hong, G. Involvement of the R2R3-MYB transcription factor MYB21 and its homologs in regulating flavonol accumulation in Arabidopsis stamen. J. Exp. Bot. 2021, 72, 4319–4332. [Google Scholar] [CrossRef]
44. Winkel Shirley, B. It takes a garden. How work on diverse plant species has contributed to an understanding of flavonoid metabolism. Plant Physiol. 2001, 127, 1399–1404. [Google Scholar] [CrossRef] [PubMed]
45. Liu, H.; Liu, Z.; Wu, Y.; Zheng, L.; Zhang, G. Regulatory mechanisms of anthocyanin biosynthesis in apple and pear. Int. J. Mol. Sci. 2021, 22, 8441. [Google Scholar] [CrossRef]
46. Xu, W.; Dubos, C.; Lepiniec, L. Transcriptional control of flavonoid biosynthesis by MYB–bHLH–WDR complexes. Trends Plant Sci. 2015, 20, 176–185. [Google Scholar] [CrossRef] [PubMed]
47. Yang, L.; Yang, Y.; Huang, L.; Cui, X.; Liu, Y. From single-to multi-omics: Future research trends in medicinal plants. Brief. Bioinform. 2023, 24, bbac485. [Google Scholar] [CrossRef] [PubMed]
48. Huang, B.; Rong, H.; Ye, Y.; Ni, Z.; Xu, M.; Zhang, W.; Xu, L.-A. Transcriptomic analysis of flower color variation in the ornamental crabapple (Malus spp.) half-sib family through Illumina and PacBio Sequel sequencing. Plant Physiol. Biochem. 2020, 149, 27–35. [Google Scholar] [CrossRef]
49. Geng, Z.; Wang, Y.; Wang, Y.; Wang, Y.; Sun, Y.; Wang, H.; Zhou, L.; Jiang, J.; Chen, S.; Chen, F. Transcriptomic and metabolomic analyses reveal CmMYB308 as a key regulator in the pink flower color variation of ‘Dante Purple’chrysanthemum. Plant Cell Rep. 2024, 43, 1–14. [Google Scholar] [CrossRef] [PubMed]
50. Shi, M.-Z.; Xie, D.-Y. Biosynthesis and metabolic engineering of anthocyanins in Arabidopsis thaliana. Recent Pat. Biotechnol. 2014, 8, 47–60. [Google Scholar] [CrossRef] [PubMed]
51. Albert, N.W.; Lewis, D.H.; Zhang, H.; Schwinn, K.E.; Davies, K.M. Members of an R2R3-MYB transcription factor family in Petunia are developmentally and environmentally regulated to control complex floral and vegetative pigmentation patterning. Plant J. 2011, 65, 771–784. [Google Scholar] [CrossRef] [PubMed]
Wang Y, Yang X, Zhou Q, Meng X, Peng J, Hu Y. Metabolomics Combined with Transcriptomics Reveals the Formation Mechanism of Different Colored Flowers of Cosmos bipinnata Cav. Agriculture. 2025; 15(3):255. https://doi.org/10.3390/agriculture15030255
Перевод статьи «Metabolomics Combined with Transcriptomics Reveals the Formation Mechanism of Different Colored Flowers ofCosmos bipinnataCav» авторов Wang Y, Yang X, Zhou Q, Meng X, Peng J, Hu Y., оригинал доступен по ссылке. Лицензия: CC BY. Изменения: переведено на русский язык













































































































Комментарии (0)