Какой миндаль выживет в соленой почве? Оценка четырех сортов для интенсивных садов
Повышение засоленности почвы угрожает мировому производству миндаля, что обусловливает необходимость разработки солеустойчивых сортов. В данном исследовании изучались механизмы солеустойчивости четырех самоукореняющихся генотипов миндаля (Виалфас, Гуара, Пента и Авихор) в контролируемых условиях. Молодые растения в течение 5 месяцев подвергались воздействию четырех уровней засоления (0, 25, 50 и 75 мМ NaCl). Анализировались параметры роста (диаметр ствола, длина побега, сырая и сухая масса), физиологические реакции (флуоресценция хлорофилла, газообмен, показатель SPAD) и минеральный состав.
Аннотация
Результаты показывают значительные генотип-специфичные реакции при критическом пороге засоления 50 мМ NaCl. В этих условиях Гуара и Виалфас сохраняли более высокую сырую массу стебля (31,4 г и 37 г соответственно), в то время как у Авихор наблюдалось значительное снижение. Измерения диаметра ствола выявили превосходные показатели Виалфас (7 мм) по сравнению с Гуара и Пента (оба около 6 мм), тогда как у Авихор отмечено наиболее сильное уменьшение (5 мм). Параметры флуоресценции хлорофилла указали на стрессовое воздействие: значения Fv/Fm снизились до 0,84 по сравнению с контрольными 0,87. Гуара сохранял более высокое отношение K⁺/Na⁺ в листьях (3,05) по сравнению с Авихор (1,95), в то время как Пента показал лучшую способность к исключению Na⁺ с самым низким содержанием Na⁺ в листьях (0,57%). Характер накопления Cl⁻ также различался между генотипами: у Авихор и Виалфас концентрация Cl⁻ в листьях была выше (0,74% и 0,73% соответственно) по сравнению с Пента (0,44%).
Реакция генотипов на всех уровнях засоления выявила различные модели устойчивости: Гуара сохранял рост и физиологические функции при всех обработках, в то время как Пента демонстрировал замечательную стабильность при высоком засолении. Виалфас проявлял активность при низком засолении, но резко снижал показатели при 75 мМ NaCl. Авихор показал наибольшую чувствительность к соли.
Эти результаты подчеркивают генетическую изменчивость солеустойчивости среди сортов миндаля и определяют потенциальные источники признаков солеустойчивости для селекционных программ. Исследование также дает представление для оптимизации отбора генотипов и стратегий управления в садах, пораженных засолением, способствуя более устойчивому производству миндаля в сложных условиях.
1. Введение
Миндаль (Prunus dulcis Mill. или Prunus amygdalus Batsch) представляет собой сельскохозяйственную культуру глобального значения, имеющую глубокие исторические корни в культивировании в Средиземноморье [1]. За последние десятилетия выращивание и производство миндаля стабильно росли, с темпом роста +196% [2]. Мировой рынок миндаля в 2022 году был оценен в 7397,62 млн долларов США, и, по прогнозам, будет расширяться со среднегодовым темпом роста 4,41%, достигнув 9583,6 млн долларов США к 2028 году [3]. Выращивание миндаля на богаре на маргинальных почвах распространено в средиземноморских странах, где эти сады исторически имели социально-экономическую ценность. В Испании богарные миндальные сады составляли примерно 67% от общей площади выращивания миндаля в сельскохозяйственном сезоне 2019–2020 годов [4]. Преобладали традиционные системы культивирования низкой и средней плотности [5]. Эти системы характеризуются менее чем 350 деревьями на гектар, расстоянием 6 × 6 м до 8 × 8 м, отсутствием механизации или орошения и использованием прямых сеянцев или сильнорослых подвоев [6]. Средняя продуктивность миндальных садов значительно выше в случае орошаемых культур: 1600–1800 кг/га против 400 кг/га для богарных культур [7].
Развитие орошаемых миндальных садов сверхвысокой плотности (СВП) с 2010 года произвело революцию в практике культивирования, опираясь на три десятилетия успеха с оливковыми рощами СВП [8]. Эти современные системы продемонстрировали высокую агрономическую [9,10], экономическую [11] и экологическую устойчивость [12]. Миндальные сады СВП используют карликовые подвои и самоукореняющиеся растения 'Smarttree', полученные с помощью культуры in vitro. Сорта включают Penta, Vialfas, Avijor и Guara [13]. Деревья высаживаются с расстоянием 4,0 × 1,5 м (1666 деревьев на гектар). Раннее вступление в плодоношение (к четвертому году) и полная механизация повышают рентабельность и устойчивость за счет снижения затрат ресурсов и расходов [5]. По состоянию на 2022 год в мире существует более 6500 га миндальных садов СВП, например, в таких странах, как Испания, Португалия, Италия, США, Марокко, Тунис, Чили и Турция [5]. Из-за недавнего внедрения СВП исследования этой системы ограничены. Исследования были направлены на биометрию сортов [14], влияние расстояния между деревьями на урожайность и перехват света [15,16], перехват света в системах СВП по сравнению с системами с открытым центром [17], а также влияние ориентации рядов и положения кроны [8].
Внедрение систем СВП сталкивается с серьезными проблемами из-за нехватки подходящей земли с полным водоснабжением для выращивания миндаля (5000–8000 м³/га). Это привело к созданию миндальных садов СВП на основе самоукореняющихся растений в районах с минимальным дополнительным орошением (500–700 м³/га). Эта концепция предлагает альтернативу как традиционным миндальным садам, так и зерновым культурам. Однако плохое качество воды во многих миндалеводческих регионах приводит к накоплению солей и стрессовым условиям [18]. Одних только осадков недостаточно для вымывания накопившихся солей, что делает необходимым использование солеустойчивых сортов для обеспечения рентабельности. К сожалению, исследования агрономических характеристик самоукореняющихся сортов миндаля остаются ограниченными. Только Casanova-Gascón и др. [19] оценивали показатели этих сортов в различных экологических ограничениях, включая лимитирующие почвенные условия, показывая некоторые различия в адаптируемости сортов. Учитывая ограниченность исследований по биотическим и абиотическим стрессам у самоукореняющихся растений миндаля, данное исследование ставит целью сравнить реакции четырех самоукореняющихся сортов (Vialfas, Guara, Penta и Avijor) на различные обработки соленой водой. Цель состоит в том, чтобы понять морфологические, физиологические и биохимические аспекты их солеустойчивости. Это исследование в контролируемых условиях оценит и ранжирует эти сорта на основе их реакции на солевой стресс.
2. Материалы и методы
2.1. Местоположение и дизайн эксперимента
Эксперимент был проведен в полиэтиленовой теплице, расположенной в Высшей политехнической школе Университета Сарагосы в Уэске, Испания (42°07′12,78″ с.ш., 0°26′49,04″ з.д.). В июне 2022 года были получены однородные 12-месячные укорененные деревья четырех сортов миндаля (Avijor, Guara, Penta, Vialfas) из питомника Agromillora Iberia (Испания) и пересажены в черные пластиковые горшки (15 × 15 × 20 см, 4,5 л), заполненные кварцевым песком (0,05–2,0 мм). Во время пересадки корни были промыты деионизированной водой для удаления остатков торфа.
Растения выращивались в течение 7 месяцев, а в феврале 2023 года их обрезали до высоты 60 см. Эксперимент начался 1 июня 2023 года, когда новый главный побег достиг высоты 50 см, и продолжался до 1 ноября 2023 года (5 месяцев). Растения выращивались в условиях естественного освещения в теплице, где поддерживалась дневная температура от 18 до 33 °C и дневная/ночная относительная влажность 55–85%. Автоматический мобильный экран был установлен при 27 °C для снижения дневной температуры, а вентиляционная система автоматически включалась для контроля температуры внутри теплицы ниже 35 °C.
Экспериментальный дизайн представлял собой полностью рандомизированный блок с общим количеством 64 дерева, по 4 дерева на каждую комбинацию обработки (4 уровня засоления) и генотипа (4 сорта).
2.2. Орошение
Питательный раствор, использованный в этом эксперименте, был раствором Хогланда 1/4 концентрации [20], добавленным к местной пресной воде с общей электропроводностью (ЭП) 0,8 дСм/м. Четыре генотипа подвергались воздействию четырех уровней соли (0, 25, 50 и 75 мМ NaCl) в течение 5 месяцев. Концентрации соли увеличивали на 25 мМ NaCl в неделю до достижения желаемых концентраций (1 июня).
Погодные условия определяли частоту и продолжительность орошения: 4-минутные сеансы происходили от одного до трех раз в день. Каждый горшок имел два капельницы с расходом 1,3 л/ч (Click Tip HD, Naandanjain, Джалгаон, Индия). Солевые растворы вводились объемным насосом MixRite E-300 (Tefen Flow and Dosing Technologies Ltd., кибуц Фарод, Израиль), а орошение контролировалось контроллером орошения Agronic 5500 (Sistemes Electrònics PROGRÉS, Барселона, Испания).
Уровни электропроводности и коэффициента адсорбции натрия для оросительной воды составили 0,8, 3,0, 6,0 и 9,0 дСм/м и 2, 30, 60 и 90 соответственно, со значениями pH в диапазоне 7,2–7,4. В ходе эксперимента дренажная вода из каждой обработки собиралась и анализировалась на вымытые растворенные вещества. Еженедельные измерения электропроводности в дренажном растворе проводились с использованием кондуктометра Hanna Instruments-HI 9033 (Вунсокет, Род-Айленд, США). Полученные значения составили 0,8, 3,2, 6,1 и 9,2 дСм/м, что соответствует концентрациям 0, 25, 50 и 75 мМ NaCl соответственно. Это подтвердило, что поддержание дренажной фракции 20–30% во время орошения обеспечивает постоянный уровень засоления в горшках на протяжении всего эксперимента [21].
2.3. Анализ растительного материала
Каждые 15 дней измеряли длину побега, диаметр ствола на высоте 10 см (с помощью цифрового штангенциркуля ABS, Hoffman Group, Мюнхен, Германия) и визуальные повреждения четырех растений на обработку. Индуцированный солью некроз листьев оценивали визуально на четырех растениях на обработку по шкале от 0 до 5, основанной на проценте пораженной общей площади листьев (0: нет симптомов; 1: 20%; 2: 40%; 3: 60%; 4: 80%; 5: более 80% кроны растения). Значения для каждой обработки представляют собой среднее значение четырех повторностей растений.
В конце эксперимента четыре растения из каждой обработки для каждого сорта были извлечены из субстрата и разделены на различные части (корни, древесина, новые побеги и листья). Надземные части растений были промыты дистиллированной водой, а корни — деионизированной водой. Была зафиксирована сырая масса всех частей растений, после чего они были высушены при 70 °C в течение 24 часов для определения их сухой массы.
Высушенный растительный материал был измельчен до частиц размером менее 2 мм с использованием электрической зерновой мельницы (модель HC400, CGoldenwall, Уси, Китай). Эти частицы затем были проанализированы с использованием как классической химии, так и портативного рентгенофлуоресцентного спектрометра Niton XL3t GOLDD+ (Thermo Scientific, Уолтем, Массачусетс, США). Размер частиц <2 мм был выбран для имитации физических условий обработанных почвенных образцов, которые могут быть измерены с помощью pXRF-зонда, в соответствии с выводами Sapkota и др. [22], Antonangelo и Zhang [23] и Towett и др. [24]. pXRF использовался для быстрого и эффективного измерения концентраций Ca²⁺, K⁺ и Cl⁻ без какой-либо предварительной обработки, с использованием «режима почвы» для Ca²⁺ и K⁺ и «горного режима» для Cl⁻ [25,26]. Измерения pXRF для катионов были откалиброваны с использованием атомно-абсорбционной спектрометрии в качестве эталонного метода для обеспечения точности элементного анализа. Для калибровки Cl⁻ образцы были проанализированы методом ионной хроматографии во внешней лаборатории (Eurofins Scientific, Сидамон, Льейда, Испания).
Для определения содержания натрия высушенные и измельченные растительные материалы были подвергнуты кислотному разложению с использованием азотной кислоты. Приблизительно 0,5 г каждого образца были предварительно разложены в течение 1 часа с 10 мл HNO₃ чистотой для анализа следов металлов. Затем разложенные образцы нагревали до 115 °C в течение 2 часов и разбавляли деионизированной водой до 50 мл [27]. Содержание натрия в разложенных образцах определяли атомно-абсорбционной спектрометрией (SpectrAA 10, Varian, Калифорния, США), как описано Калрой [28]. Все указанные значения представляют собой средние значения четырех повторных измерений.
2.4. Физиологические параметры
2.4.1. Хлорофилл листьев (SPAD)
Каждые две недели общее содержание хлорофилла определяли с использованием портативного хлорофилл-метра SPAD-502Plus (Konica Minolta, Осака, Япония), позволяющего проводить быстрые неразрушающие измерения. Значения SPAD были получены из полностью развернутых функциональных листьев, при этом оператор затенял измерительный прибор от прямого солнечного света во время каждого измерения. Пятнадцать листьев были случайным образом отобраны для каждого сорта и обработки, и их значения были усреднены для получения одного значения SPAD.
2.4.2. Флуоресценция хлорофилла
Параметры флуоресценции хлорофилла регистрировали каждые две недели с использованием портативного флуориметра Handy PEA (Hansatech Instruments Ltd., Норфолк, Великобритания). Регистрировались такие параметры, как начальная (F₀), максимальная (Fm), переменная (Fv = Fm − F₀) флуоресценция и максимальный квантовый выход фотосистемы II (Fv/Fm) в темно-адаптированных листьях, среди прочих. Параметры, полученные от флуориметра, были разделены на 3 группы: общая эффективность фотосистемы II, энергия и транспорт электронов, рассеяние энергии и повреждения [29,30,31].
2.4.3. Устьичная проводимость
Каждые две недели измеряли устьичную проводимость (gs, ммоль H₂O м⁻² с⁻¹) с использованием портативного порометра (SC-1 Meter Group, Вашингтон, округ Колумбия, США). Измерения проводились на двух хорошо освещенных и полностью развернутых листьях из средней части побега от четырех растений на обработку и сорт в период с 9:00 до 11:00 утра.
2.5. Статистический анализ
Все статистические анализы были выполнены с использованием программного обеспечения R (версия 4.4.1:2024) [32]. Был установлен полный 3-факторный факторный дизайн (генотип, обработка и орган) с 4 уровнями каждый и 4 повторностями, всего 4³ × 4 = 256 испытаний. Анализ образцов из каждого испытания позволил получить значения целевых переменных: Ca²⁺, Na⁺, K⁺, Cl⁻, сырая масса и сухая масса. Наряду с этими переменными анализировалось поведение наиболее важных соотношений между ними: Ca²⁺/Na⁺ и K⁺/Na⁺. Нормальность распределения данных была проверена для всех совокупностей с использованием критерия нормальности Колмогорова–Смирнова с поправкой Лилиефорса [33] или критерия Шапиро–Уилка [34] в зависимости от количества данных в группах, а также с использованием Q–Q графика нормальной вероятности. Этот критерий практически всегда не выполнялся. Требование гомоскедастичности было проверено с помощью теста Левена [35], которое во многих случаях не соблюдалось, поэтому обычный сравнительный анализ, предоставляющий линейную статистику (ANOVA), не может быть использован. Для решения этой проблемы были использованы два статистических метода: критерий Краскела–Уоллиса [36], когда распределение не было нормальным, но группы были гомоскедастичными; и гетероскедастичный F-тест Уэлча с усеченными средними и виндзоризованными дисперсиями, когда нельзя было предположить ни нормальность, ни гомоскедастичность. Эта последняя устойчивая процедура проверяет равенство средних, заменяя обычные средние и дисперсии на усеченные средние и виндзоризованные дисперсии [37,38]. Кроме того, были использованы методы бутстрапа для установления устойчивых доверительных интервалов для местоположения [39] и устойчивых однородных групп.
Были использованы модели отклика — модели естественных кубических сплайнов [40,41,42], анализирующие их показатели для каждой целевой переменной (диаметр ствола, длина побега, SPAD и устьичная проводимость), которые оценивались с помощью остаточного анализа, коэффициента корреляции (значение R²) [43], информационного критерия Акаике (AIC) [44] и байесовского информационного критерия (BIC) [45,46]. Эти значения вместе с критерием отношения правдоподобия и критерием Вальда позволяют установить качество соответствия модели.
3. Результаты
3.1. Параметры роста при солевом стрессе
3.1.1. Сырая и сухая масса
Рисунок S1 иллюстрирует структуру распределения сырой массы по обработкам и органам: стебли > древесина > корни > листья. Солевые эффекты различались в зависимости от органа, причем листья показывали самую высокую чувствительность, в частности у Avijor и Penta (Рисунок S2). Корни демонстрировали различные реакции, в то время как масса древесины оставалась относительно стабильной. Подробные статистические сравнения, включая группы значимости, предоставлены во вспомогательных материалах (столбец "Rob Groups" в прилагаемых таблицах).
Касательно влияния дозы на сырую массу, при 0 мМ NaCl все генотипы показывали сильный рост, причем Vialfas показал наилучшие результаты (Рисунок S3). При 25 мМ NaCl Vialfas и Guara сохранили или увеличили сырую массу стебля, в то время как Avijor и Penta показали значительные снижения (Рисунок S2). При 50 мМ NaCl Guara и Vialfas сохранили относительно высокую сырую массу стебля, в то время как Avijor показал дальнейшее снижение. При 75 мМ NaCl Avijor продемонстрировал частичное восстановление массы корней, древесины и стеблей по сравнению с 50 мМ NaCl.
Сухая масса показала схожую структуру распределения по органам: стебли имели самые высокие значения (11,67–19,32 г), за ними следовали древесина и корни (10,12–11,54 г и 8,88–10,71 г соответственно), а затем листья (4,33–5,82 г) по всем обработкам (Рисунок S4). Реакция органов на засоление различалась между генотипами, причем листья показывали самую высокую чувствительность, в частности у Avijor (Рисунок S5). При рассмотрении общих реакций генотипов на засоление Vialfas и Guara продемонстрировали более высокую толерантность по сравнению с другими генотипами (Рисунок S6). Vialfas показал самую высокую общую сухую массу в контрольных условиях (16,56 г) и сохранял высокие значения при умеренном засолении 25 мМ NaCl (15,79 г), хотя и снижаясь при более высоких уровнях засоления (11,65 г при 50 мМ и 9,00 г при 75 мМ NaCl). Guara сохранял стабильные значения сухой массы по всем обработкам (9,84–10,14 г, Рисунок S6). Avijor продемонстрировал значительную чувствительность к умеренному засолению: общая сухая масса снизилась с 9,76 г в контроле до 4,94 г при 25 мМ NaCl, хотя и показал восстановление при 75 мМ NaCl (10,04 г). Penta продемонстрировал промежуточную чувствительность, снизившись с 11,23 г в контроле до 7,97 г при самом высоком засолении (Рисунок S6).
3.1.2. Диаметр ствола
Таблица S1 предоставляет данные сплайнов, иллюстрирующие различия в диаметре ствола между генотипами и обработками. В контрольных условиях (Рисунок 1a) Vialfas продемонстрировал наиболее robustny рост (конечный диаметр 8 мм), за ним следовал Guara (7,5 мм), в то время как Avijor и Penta продемонстрировали схожие структуры роста (7 мм и 6,5 мм соответственно). При 25 мМ NaCl (Рисунок 1b) Vialfas сохранял превосходный рост, но Guara снизился до 6 мм, а Avijor и Penta показали небольшие снижения. При 50 мМ NaCl (Рисунок 1c) рост диаметра ствола снизился у всех генотипов, причем Vialfas показал лучшие результаты (7 мм), Guara и Penta показали схожий рост (6 мм), а Avijor продемонстрировал наиболее значительное снижение (5 мм). При 75 мМ NaCl (Рисунок 1d) Guara показал наилучшие показатели (6,5 мм); Penta и Avijor продемонстрировали схожие структуры роста (6 мм); в то время как Vialfas, который превосходно себя зарекомендовал при более низком засолении, показал наихудшие показатели (5,5 мм).
Рисунок 1. Эволюция диаметра ствола для четырех генотипов Prunus в зависимости от засоления: (a) контроль, (b) 25 мМ NaCl, (c) 50 мМ NaCl и (d) 75 мМ NaCl. Для каждого генотипа центральная линия представляет собой подобранную сплайн-кривую, а пунктирные линии выше и ниже представляют 95% доверительные интервалы.
3.1.3. Длина побега
Данные сплайнов о влиянии генотипа и обработки на длину побега представлены в Таблице S2. В контрольных условиях (Рисунок 2a) Vialfas продемонстрировал наиболее энергичный рост (конечная высота 160 см), за ним следовали Avijor и Guara (140 см и 135 см соответственно), а затем Penta (120 см). При 25 мМ NaCl (Рисунок 2b) Vialfas сохранял превосходный рост, причем Avijor почти сравнялся с Vialfas к концу периода, а Guara и Penta показывали более низкие темпы роста. При 50 мМ NaCl (Рисунок 2c) рост был значительно снижен у всех генотипов, при этом генотипические различия при более высоком стрессе уменьшились. При 75 мМ NaCl (Рисунок 2d) рост был сильно замедлен у всех генотипов, при этом Penta показал относительно лучшие результаты в условиях экстремального стресса, а Avijor продемонстрировал наихудшие показатели.
Рисунок 2. Эволюция длины побега для четырех генотипов Prunus в зависимости от засоления: (a) контроль, (b) 25 мМ NaCl, (c) 50 мМ NaCl и (d) 75 мМ NaCl. Для каждого генотипа центральная линия представляет собой подобранную сплайн-кривую, а пунктирные линии выше и ниже представляют 95% доверительные интервалы.
3.2. Физиологические реакции на солевой стресс
3.2.1. Параметры флуоресценции хлорофилла
Повышение засоления негативно повлияло на фотосинтетические параметры (φ(Po), PI_abs, PI_Inst и Fv/Fm) и параметры транспорта электронов (REo/RC и ψ(Eo)) у всех генотипов (Рисунок 3a,b). Penta и Avijor сохраняли относительно стабильную фотосинтетическую производительность и транспорт электронов, в то время как Guara и Vialfas показали значительные снижения, причем Guara испытал почти коллапс электронного потока при 75 мМ NaCl. Рассеяние энергии (DIo/RC и DIo/CSo; Рисунок 3c) увеличивалось с засолением, причем у толерантных генотипов наблюдался более контролируемый рост.
Рисунок 3. (a) Фотосинтетическая производительность, (b) поток электронов и (c) рассеяние энергии для различных генотипов Prunus в зависимости от засоления в конце эксперимента. 'Auto control Apr.' представляет собой среднее значение всех генотипов в апреле. Area представляет площадь над кривой индукции флуоресценции между минимальной флуоресценцией (F₀) и максимальной флуоресценцией (Fm) и связана с размером пула акцепторов электронов в фотосинтетической электрон-транспортной цепи. Fv/Fm — максимальный квантовый выход фотосистемы II (ФСII), когда все реакционные центры открыты. Vj представляет относительную переменную флуоресценцию на J-шаге OJIP-транзиента флуоресценции и предоставляет информацию о состоянии восстановления первичного акцептора электрона хинона (QA). Sm — нормализованная общая дополнительная площадь над OJIP-транзиентом и связана с энергией, необходимой для закрытия всех реакционных центров ФСII. N представляет число оборотов QA, то есть количество раз, когда QA восстанавливается и окисляется во время измерения. DIo/RC — энергия, рассеиваемая в виде тепла и флуоресценции на один реакционный центр. ETo/RC представляет скорость переноса электронов на один реакционный центр. REo/RC — скорость переноса электронов за пределы QA на один реакционный центр. φ(Po) — максимальный квантовый выход первичной фотохимии. ψ(Eo) представляет эффективность, с которой захваченный экситон может переместить электрон в электрон-транспортную цепь за пределы QA. DIo/CSo — энергия, рассеиваемая в виде тепла и флуоресценции на одно поперечное сечение. PI_abs — индекс производительности на основе абсорбции, который объединяет несколько параметров флуоресценции для предоставления общей меры производительности ФСII.
Ключевые измерения эффективности ФСII показали, что как сезонные изменения, так и солевой стресс негативно повлияли на показатели ФСII (Таблица S3 и Рисунок S7), что отразилось в снижении Fv/Fm и PI_abs. При 75 мМ NaCl фотосинтетический выход резко упал, хотя Penta и Avijor показали некоторое восстановление при 50 и 75 мМ NaCl (Рисунок 3a,b). Способность к переносу электронов снизилась при стрессе, на что указывает снижение REo/RC и ψ(Eo) (Рисунок S8). При 25 и 50 мМ NaCl корректировки параметров Area и Sm предполагали попытки компенсации, но при 75 мМ NaCl компенсационная способность была подавлена. Рассеяние энергии увеличивалось со стрессом, о чем свидетельствует повышение уровней DIo/RC и DIo/CSo (Рисунок S9), при этом параметр Vj показал накопление QA при 75 мМ NaCl.
3.2.2. Газообмен
Статистические данные по устьичной проводимости в зависимости от обработок и генотипов обобщены в Таблице S4. В контрольных условиях все генотипы демонстрировали схожие структуры (Рисунок 4a–d), причем Penta достиг самой высокой пиковой проводимости примерно на четвертой двухнеделе, а Vialfas сохранял наиболее стабильную проводимость на протяжении всего периода. При 25 мМ NaCl Penta сохранял самую высокую проводимость, особенно в начале, в то время как Vialfas показал заметное снижение. При 50 мМ NaCl проводимость снизилась у всех генотипов, причем Avijor показал самую низкую проводимость на протяжении всего периода. При 75 мМ NaCl Penta продемонстрировал наиболее значительное снижение, в то время как Vialfas сохранял наиболее стабильную структуру, хотя и на низких уровнях проводимости.
Рисунок 4. Эволюция устьичной проводимости (gs, ммоль H₂O м⁻² с⁻¹) для четырех генотипов Prunus в зависимости от засоления: (a) контроль, (b) 25 мМ NaCl, (c) 50 мМ NaCl и (d) 75 мМ NaCl. Для каждого генотипа центральная линия представляет собой подобранную сплайн-кривую, а пунктирные линии выше и ниже представляют 95% доверительные интервалы.
3.2.3. Анализ содержания хлорофилла с помощью SPAD
Статистические данные по SPAD в зависимости от обработок и генотипов обобщены в Таблице S5. В контрольных условиях все генотипы показывали увеличение значений SPAD с течением времени (Рисунок 5a–d), причем Guara демонстрировал самые высокие значения. При 25 мМ NaCl Guara сохранял высокие значения SPAD с сильным увеличением, в то время как Penta демонстрировал относительно стабильные значения. При 50 мМ NaCl Guara показал высокую вариабельность с резким снижением примерно на шестой двухнеделе с последующим восстановлением, в то время как Avijor демонстрировал стабильное увеличение. При 75 мМ NaCl Guara показал сильное увеличение значений SPAD с течением времени, в то время как Penta сохранял относительно низкие, но стабильные значения.
Рисунок 5. Эволюция SPAD для четырех генотипов Prunus в зависимости от засоления: (a) контроль, (b) 25 мМ NaCl, (c) 50 мМ NaCl и (d) 75 мМ NaCl. Для каждого генотипа центральная линия представляет собой подобранную сплайн-кривую, а пунктирные линии выше и ниже представляют 95% доверительные интервалы.
3.3. Визуальные симптомы солевого стресса
Все генотипы демонстрировали robustny рост в неосоленных условиях, характеризующийся избытком темно-зеленых листьев, равномерно распределенных вдоль стебля, хорошо развитыми корневыми системами и здоровой общей структурой растения (Рисунок 6). При 25 мМ NaCl симптомы стресса проявились в виде небольшого снижения густоты листвы, их размера и объема корневой системы. При 50 мМ NaCl появились симптомы стресса от умеренной до сильной степени, включая заметное уменьшение количества листьев с хлорозом и некрозом на краях листьев, более тонкие и короткие стебли, а также уменьшенный объем и ветвление корневой системы. При 75 мМ NaCl все генотипы показали серьезные симптомы стресса: значительное уменьшение количества листьев и обширный хлороз и некроз оставшихся листьев, заметно более тонкие и короткие стебли и сильно пораженные корневые системы с минимальным развитием и ветвлением.
Рисунок 6. Внешний вид четырех генотипов, подвергнутых различным обработкам засолением, в конце эксперимента. Показана только одна повторность на обработку.
Что касается повреждения листьев, как показано на шкале 0–5 на Рисунке 7a, Avijor и Guara продемонстрировали замечательную устойчивость при 25 мМ NaCl (Рисунок 7c), не показав измеримых повреждений, в то время как Penta и Vialfas проявили небольшую восприимчивость со значениями интегрированного повреждения за время (представленного площадью под кривыми прогрессирования повреждения) 5,49 и 3,30 соответственно. При 50 мМ NaCl (Рисунок 7d) Vialfas показал самое высокое накопленное повреждение (21,98), за ним следовали Guara (12,09) и Penta (8,79), в то время как Avijor сохранял относительно низкие уровни повреждения (3,30). При 75 мМ NaCl (Рисунок 7e) Penta продемонстрировал самое высокое интегрированное повреждение (30,77), за ним следовал Vialfas (29,67), в то время как Avijor (20,88) и Guara (19,78) показали сравнительно лучшую устойчивость.
Рисунок 7. (a) Шкала уровня повреждения листьев, (b–e) эволюция повреждения листьев для каждого из четырех генотипов Prunus в зависимости от засоления: (b) контроль, (c) 25 мМ NaCl, (d) 50 мМ NaCl и (e) 75 мМ NaCl. Значения на оси Y представляют мгновенные уровни повреждения по шкале 0–5, в то время как интегрированные значения, обсуждаемые в тексте, представляют площадь под этими кривыми прогрессирования повреждения за время. Для лучшей визуализации кривые прогрессирования повреждения были вертикально смещены там, где происходит перекрытие, при сохранении их относительных структур и фактических значений шкалы повреждения.
3.4. Изменения минерального состава при солевом стрессе
Учитывая структуру данных (Таблица S6), к зависимым переменным были применены логарифмические преобразования из-за отклонения от предположений нормальности. Этот подход облегчил построение общих факторных моделей для ANOVA-анализов (Таблица S7). Структура модели была определена как:
Все три фактора оказались значимыми во всех моделях. Для решения проблем гетероскедастичности и ненормальности были использованы устойчивые методы сравнения. Непреобразованные переменные использовались для этих сравнений (Таблица S8), поскольку это сочтено более подходящим, учитывая характеристики данных (Рисунок 8 и Рисунок 9).
Рисунок 8. Box-plot катионов и анионов для взаимодействий генотип × обработка засолением. S1, S2, S3 и S4 обозначают контроль, 25, 50 и 75 мМ NaCl соответственно. Различные буквы указывают на значительно различающиеся группы на основе статистического анализа устойчивых однородных групп (p < 0,05).
Рисунок 9. Box-plot катионов и анионов для взаимодействий орган × обработка засолением. S1, S2, S3 и S4 обозначают контроль, 25, 50 и 75 мМ NaCl соответственно. Различные буквы указывают на значительно различающиеся группы на основе статистического анализа устойчивых однородных групп (p < 0,05).
Статистическую значимость различий между обработками, генотипами и органами для всех минеральных анализов можно найти во вспомогательных материалах (Рисунки S10–S27, столбец "Rob Groups" в прилагаемых таблицах).
3.4.1. Содержание и распределение кальция
При изучении органоспецифических реакций (Рисунок S10) корни стабильно показывали самое высокое содержание Ca²⁺ у всех генотипов, с самым высоким содержанием в контроле (3,59%) и при обработке 25 мМ NaCl (3,58%), снижаясь при 50 мМ NaCl (2,69%) и увеличиваясь при 75 мМ NaCl (3,45%). Листья показывали второе по величине содержание Ca²⁺, постепенно снижающееся с повышением засоления. Древесина демонстрировала умеренное содержание Ca²⁺ с нелинейной реакцией на засоление, увеличиваясь с контроля (1,53%) до 25 мМ NaCl (1,93%), а затем постепенно снижаясь. Стебли показывали самое низкое содержание Ca²⁺ (1,20–1,26%).
Что касается генотип-специфичных реакций (Рисунки S11 и S12), Avijor продемонстрировал самое высокое среднее содержание Ca²⁺ в корнях (4,12%, что на 27–39% выше, чем у других генотипов), хотя и показывая вариабельную реакцию на засоление. Guara сохранял стабильно высокие уровни Ca²⁺ по всем обработкам засолением, показывая самое высокое среднее содержание Ca²⁺ в листьях (3,54%) и стеблях (1,37%). Penta демонстрировал более низкие уровни Ca²⁺ во всех органах и обработках. Vialfas показал умеренные уровни Ca²⁺ с меньшей вариабельностью, имея самое высокое содержание Ca²⁺ в древесине (1,92%).
3.4.2. Структуры накопления калия
Распределение калия также различалось по органам растений (Рисунок S13), причем листья показывали самое высокое содержание K⁺ (5,52–6,39%), за ними следовали стебли (1,48–1,82%), корни (1,01–1,19%) и древесина (0,66–0,78%). Содержание K⁺ в листьях снизилось с 9,23% в контроле до 3,47% при 75 мМ NaCl. Стебли продемонстрировали умеренное, но последовательное снижение (24% уменьшение), в то время как корни и древесина продемонстрировали сложные нелинейные реакции.
Генотип-специфичные реакции (Рисунки S14 и S15) показали у Avijor последовательное снижение среднего содержания K⁺ с 3,12% в контроле до 1,57% при 75 мМ NaCl. Penta сохранял несколько более высокие уровни K⁺ (2,78% при 25 мМ NaCl до 1,98% при 75 мМ NaCl). Vialfas продемонстрировал самое высокое содержание K⁺ в контроле (3,68%), но испытал значительные снижения с повышением засоления. Guara достиг самого низкого содержания K⁺ (1,51%) при 75 мМ NaCl.
3.4.3. Накопление и распределение хлорида
Органоспецифические структуры (Рисунок S16) показали, что листья имели самое высокое содержание Cl⁻ (0,64–1,24%), за ними следовали корни (0,45–0,66%), стебли (0,14–0,28%) и древесина (0,13–0,19%). Содержание Cl⁻ в контроле было низким (0,04–0,19%), значительно увеличиваясь при 25 мМ NaCl, в частности в листьях и корнях. При 50 мМ NaCl накопление Cl⁻ усилилось, причем ткань листьев продемонстрировала наиболее выраженное увеличение концентрации. При 75 мМ NaCl накопление Cl⁻ достигло своего пика: содержание Cl⁻ в листьях увеличилось в 18 раз от контроля до 75 мМ NaCl, в корнях — в 4,75 раза, в стеблях — в 7,9 раза, а в древесине — в 2,9 раза.
Что касается влияния генотипа, Avijor и Vialfas показали более крутое увеличение содержания Cl⁻ от контроля до 75 мМ NaCl, в то время как Penta показал более постепенное увеличение (Рисунки S17 и S18). При 50 мМ NaCl Avijor и Guara сгруппировались отдельно от Penta и Vialfas в статистических анализах. При 75 мМ NaCl Vialfas и Avijor накопили больше Cl⁻ в листьях (1,25 и 1,23% соответственно) по сравнению с Penta и Guara. Vialfas показал самое высокое содержание Cl⁻ в корнях (0,67%), в то время как Penta показал стабильно более низкое накопление Cl⁻.
3.4.4. Содержание и распределение натрия
Распределение натрия различалось по органам растений (Рисунок S19), причем листья показывали самое высокое содержание Na⁺ (1,05–1,59%), за ними следовали корни (0,45–0,73%), стебли (0,23–0,42%) и древесина (0,17–0,27%). Содержание Na⁺ в контроле было низким (0,11–0,22%), умеренно увеличиваясь при 25 мМ NaCl и значительно при 50 мМ NaCl (1,92% в листьях). Листья показали 9,7-кратное увеличение от контроля до 75 мМ NaCl, корни — 5,9-кратное, стебли — 2,9-кратное, а древесина — 2,5-кратное.
Относительно влияния генотипа (Рисунки S20 и S21), Avijor стабильно накапливал самые высокие уровни Na⁺, достигая 1,10% при 50 мМ NaCl и 1,19% при 75 мМ NaCl. Penta продемонстрировал превосходную способность к исключению Na⁺, в частности при 50 мМ NaCl. Guara и Vialfas продемонстрировали промежуточное накопление Na⁺. При 50 мМ NaCl генотипы распределились по различным статистическим группам, в то время как при 75 мМ NaCl все генотипы показали значительные различия по сравнению с обработками с более низким засолением, но не между собой.
3.4.5. Анализ соотношения калий/натрий
Органоспецифические структуры выявили последовательные тенденции у всех генотипов (Рисунок S22). Листья показывали самые высокие соотношения K⁺/Na⁺ (13,01–20,81), но они резко снизились с 43,44 в контроле до 1,93 при 75 мМ NaCl. Корни продемонстрировали умеренные соотношения K⁺/Na⁺ (2,88–4,24), снизившись с 8,54 в контроле до 1,02 при 75 мМ NaCl. Ткани древесины и стеблей показали промежуточные и относительно стабильные соотношения K⁺/Na⁺ по обработкам, снижаясь с 6,99 в контроле до 3,48 при 75 мМ NaCl и с 14,28 до 4,17 соответственно.
Что касается генотип-специфичных реакций (Рисунки S23 и S24), Guara продемонстрировал самое высокое среднее соотношение K⁺/Na⁺ (20,82) в контроле, за ним следовал Vialfas (18,98). Penta имел самые высокие соотношения K⁺/Na⁺ в стеблях (10,43) и древесине (6,21). При 75 мМ NaCl Penta сохранял относительно более высокие соотношения K⁺/Na⁺, в частности в корнях и стеблях, в то время как Avijor показал самое низкое соотношение K⁺/Na⁺ (1,65).
3.4.6. Анализ соотношения кальций/натрий
Корни сохраняли более высокие соотношения Ca²⁺/Na⁺ (6,75–10,17) по сравнению с другими органами у всех генотипов (Рисунок S25). Ткани древесины также продемонстрировали относительно высокие соотношения Ca²⁺/Na⁺, в частности у Penta (12,29) и Guara (11,28). Листья показали наиболее вариабельные соотношения Ca²⁺/Na⁺ между генотипами (4,42–9,45), в то время как стебли в целом продемонстрировали более низкие соотношения Ca²⁺/Na⁺ (4,46–5,85).
Что касается влияния генотипа, в контрольных условиях соотношения Ca²⁺/Na⁺ варьировались от 12,94 до 16,67 (Рисунки S26 и S27). Guara сохранял относительно более высокие соотношения Ca²⁺/Na⁺ по всем обработкам, в то время как Avijor показал наиболее драматическое снижение при 50 и 75 мМ NaCl. Penta и Vialfas продемонстрировали промежуточные реакции, причем Penta показал несколько лучшее поддержание соотношений Ca²⁺/Na⁺ при более высоких засолениях. При 75 мМ NaCl соотношения Ca²⁺/Na⁺ сошлись к более низким значениям у всех генотипов (2,69–5,99).
4. Обсуждение
4.1. Параметры роста при солевом стрессе
4.1.1. Сырая и сухая масса
Наши результаты подтверждают выводы Zrig и др. [47] и Sandhu и др. [48], которые сообщили о значительной вариабельности солеустойчивости среди подвоев миндаля (GFF 677, GN15, P. dulcis и 14 других коммерческих генотипов подвоев миндаля — включая персиковые гибриды и гибриды персика и миндаля). Vialfas продемонстрировал превосходную активность, в частности в контрольных условиях, что предполагает наличие врожденных признаков, способствующих robustny росту и потенциальной солеустойчивости. В свою очередь, Guara продемонстрировал наивысшую устойчивость по всем обработкам засолением, сохраняя рост в стрессовых условиях.
Способность Guara поддерживать высокую сырую и сухую массу при солевом стрессе — и даже увеличивать массу стебля при 25 мМ NaCl — предполагает потенциальные механизмы солеустойчивости. Этот индуцированный стрессом рост может быть обусловлен осмотической регуляцией или эффективной компартментацией ионов, как предполагают Munns и Tester [49] в своем обзоре механизмов солеустойчивости. Напротив, чувствительность Avijor, который испытал резкое снижение массы при умеренных уровнях засоления, подчеркивает генетическую основу солеустойчивости у Prunus. Подобная генетическая вариабельность была отмечена Toro и др. [50] в их исследовании подвоев Prunus с генетическим происхождением из подродов Prunus, Cerasus и Amygdalus.
Органоспецифические реакции предоставляют дополнительное понимание стратегий адаптации к солевому стрессу у Prunus. Приоритизация роста стебля и древесины над производством листьев при солевом стрессе согласуется с наблюдениями Zrig и др. [47] у подвоев миндаля. Эта структура распределения может служить адаптивной стратегией для поддержания структурной целостности в стрессовых условиях, как было предложено Tattini и др. [51] в их исследовании оливковых деревьев.
Различные реакции корней, в частности увеличение роста корней, наблюдаемое у Vialfas при умеренном засолении, предполагают адаптивные механизмы для улучшения приобретения ресурсов в стрессовых условиях. Подобная стимуляция роста корней при умеренном засолении была зарегистрирована у других древесных видов [52]. Эта реакция может быть ключевой для солеустойчивости, учитывая, что корни играют жизненно важную роль в исключении ионов и поглощении воды в соленой среде [53]. Нелинейные реакции на повышение засоления, в частности частичное восстановление некоторых генотипов при 75 мМ NaCl, могут указывать на активацию механизмов стрессового ответа при высоких уровнях засоления. Это явление, наблюдаемое у других видов растений, может включать индукцию антиоксидантных систем или накопление осмолитов [54].
4.1.2. Диаметр ствола
Превосходная солеустойчивость, проявленная Vialfas при 25 и 50 мМ NaCl, о чем свидетельствует сохраняющийся рост диаметра ствола, подтверждает предыдущие исследования солеустойчивых сортов Prunus. Например, Zrig и др. [55] сообщили о подобной вариабельности солеустойчивости среди различных подвоев Prunus, причем GN15 и GF677 показали лучшую толерантность, чем горький миндаль, хотя все подвои испытывали снижение роста при солевом стрессе. Однако значительное снижение показателей Vialfas при 75 мМ NaCl предполагает возможный пороговый эффект в его механизмах солеустойчивости. Эта структура напоминает двухфазную модель реакции на солевой стресс, описанную Munns и Tester [49], где растения сначала реагируют на осмотический компонент солевого стресса, за которым следует реакция на ионный стресс при более высоких уровнях засоления.
Замечательная структура устойчивости Guara, в частности его улучшенные показатели при 75 мМ NaCl после того, как он показал сниженный рост при 25 и 50 мМ NaCl, предполагает наличие индуцируемых механизмов солеустойчивости. Подобные явления наблюдались у других видов растений, например у некоторых галофитов, где высокое засоление запускает активацию специфических путей стрессового ответа [53]. Постепенное снижение роста диаметра ствола Avijor с повышением уровней засоления указывает на линейную реакцию на солевой стресс. Снижение роста при засолении, вероятно, обусловлено различными физиологическими реакциями и дополнительными энергетическими затратами, связанными со стрессом. Растения должны распределять энергию между поддержанием, ростом и механизмами защиты от стресса, при этом солевой стресс ограничивает общую доступную энергию из-за сниженного фотосинтеза [56]. Стабильные показатели Penta по всем обработкам засолением контрастируют с типичной реакцией растений, описанной Kozlowski и Pallardy [57], где стресс обычно снижает рост, поскольку растения перенаправляют энергию с роста на механизмы защиты от стресса.
4.1.3. Длина побега
Общая тенденция снижения темпов роста и увеличения вариабельности с повышением уровней засоления у всех генотипов соответствует общим эффектам солевого стресса на растения, как рассмотрено в обзоре Munns и Termaat [58].
Превосходные показатели Vialfas в контрольных условиях и при мягком стрессе предполагают сложный механизм стрессового ответа, который может отражать фенотипическую пластичность — признак, часто связанный с адаптивным потенциалом в изменчивых средах [59]. Значительное снижение при 75 мМ NaCl, наблюдаемое у Avijor, который продемонстрировал хороший рост в контрольных условиях и при мягком стрессе, иллюстрирует концепцию пороговой толерантности к засолению, описанную Munns и Tester [49]. Подобные пороговые реакции наблюдались у других видов Prunus, например, у различных подвоев миндаля [48], что указывает на общий, но вариабельный признак внутри рода. Последовательные промежуточные показатели Guara по обработкам с более низким засолением, наряду с его сниженной адаптируемостью к высокому засолению, отражают стратегию умеренной солеустойчивости. Стабильно более медленный рост Penta в контроле и при низком засолении, но его улучшенные показатели при стрессе высокого засоления предполагают компромисс между ростовым потенциалом и устойчивостью к стрессу. Это поддерживает гипотезу «синдрома устойчивости к стрессу», которая предполагает, что адаптивные к стрессу признаки достигаются ценой сниженного роста в благоприятных условиях [60]. Растения показывают вариабельные реакции на солевой стресс с первоначальными осмотическими корректировками, за которыми следуют негативные ионные эффекты после превышения порогов толерантности. Время наступления и серьезность этих порогов значительно различаются между видами и генотипами [61,62].
4.2. Физиологические реакции на солевой стресс
4.2.1. Параметры флуоресценции хлорофилла
По мере увеличения засоления от контроля до 75 мМ NaCl все генотипы продемонстрировали снижение параметров фотосинтеза и потока электронов, что соответствует известным эффектам солевого стресса на эффективность Фотосистемы II (ФСII) [49].
Наблюдаемое снижение максимального квантового выхода ФСII (Fv/Fm) при солевом стрессе указывает на повреждение реакционных центров ФСII, что согласуется с работой Ranjbarfordoei и др. [63] на миндальных деревьях (сладкий миндаль). Это снижение приписывается вмешательству ионов соли в осмотический баланс и генерации окислительного стресса. Эффективность захвата энергии (Fv/F₀) также снизилась, что предполагает повреждение реакционных центров и нарушение общей фотосинтетической способности, что соответствует выводам Jimenez и др. [64]. Максимальный квантовый выход первичной фотохимии ФСII (φ(Po)) снизился при солевом стрессе, что указывает на сниженную эффективность использования энергии света, что соответствует исследованиям Acosta-Motos и др. [65] на двух видах декоративных растений, Eugenia myrtifolia Cambess. и Myrtus communis L.
Способность к поглощению энергии, измеряемая параметром Area, показала значительные изменения между измерениями в апреле и сентябре, что указывает на физиологические корректировки к сезонным условиям или солевому стрессу [65]. Нормализованная площадь (Sm), которая указывает на размер пула акцепторов электронов ФСII, снизилась при высоком засолении, предполагая сниженную способность к потоку электронов [64]. Количество активных реакционных центров ФСII (N) снизилось при солевом стрессе, что указывает на меньшее количество функциональных центров, вероятно, из-за повреждения кислород-выделяющего комплекса и других компонентов ФСII [66].
Эффективность переноса электронов от ФСII к ФСI (REo/RC) снизилась при засолении, что предполагает, что солевой стресс влияет на конечную фазу транспорта электронов. Этот эффект подобен тем, которые наблюдали [67], отметившим подобное влияние на фотохимию ФСII при засухе у сортов черешни. Отношение F₀/Fm, которое измеряет долю энергии света, не используемой эффективно в ФСII, увеличилось при солевом стрессе, что указывает на большее рассеяние энергии в виде тепла [63]. Переменная J (Vj) на OJIP-кривой увеличилась при солевом стрессе, что указывает на проблемы в переносе электронов у сортов черешни [64].
Рассеяние энергии на один реакционный центр (DIo/RC) увеличилось в соленых условиях, что предполагает механизм защиты от избыточной энергии. Генотипы Penta и Avijor сохраняли относительно стабильную фотосинтетическую производительность (PI_abs) и поток электронов (REo/RC), в то время как Guara и Vialfas показали значительные снижения. Эта дифференциальная реакция согласуется с выводами Acosta-Motos и др. [65], которые наблюдали подобную вариабельность солеустойчивости среди декоративных растений.
Снижение PI_abs и Fv/Fm с повышением засоления, в частности у чувствительных сортов, указывает на снижение эффективности ФСII и общей фотосинтетической способности [68]. Почти коллапс потока электронов (REo/RC и ψ(Eo)) у Guara при 75 мМ NaCl предполагает серьезное нарушение электрон-транспортной цепи, что является распространенным следствием высокого засоления [69]. Частичное восстановление, продемонстрированное Penta и Avijor при умеренных засолениях (25–50 мМ NaCl) в сентябре, предполагает потенциальную сезонную адаптацию или процессы акклиматизации. Эта адаптивная способность, отсутствующая у чувствительных сортов, может включать механизмы осмотической регуляции или компартментации ионов [70].
4.2.2. Газообмен
В контрольных условиях генотипы продемонстрировали различные структуры устьичной проводимости, причем Penta показал самую высокую пиковую проводимость. Эта вариабельность базового устьичного поведения согласуется с выводами по другим видам Prunus. Например, Jimenez и др. [64] наблюдали значительные различия в устьичной проводимости среди различных подвоев Prunus в условиях отсутствия стресса, приписывая эти различия генетической вариабельности эффективности использования воды. Высокая проводимость, проявленная Penta в контрольных условиях, предполагает потенциал для более высокой фотосинтетической способности, что может быть преимуществом в оптимальных условиях выращивания.
По мере увеличения солевого стресса по обработкам (от 25 до 75 мМ NaCl) все генотипы продемонстрировали снижение устьичной проводимости, хотя и в разной степени. Эта реакция соответствует физиологической стратегии закрытия устьиц при солевом стрессе, которая помогает уменьшить потерю воды и предотвратить накопление ионов в тканях листьев [49,71].
Драматическое снижение устьичной проводимости Penta при сильном стрессе (75 мМ NaCl) после поддержания высокой проводимости в условиях более низкого стресса иллюстрирует концепцию порогов солеустойчивости. Эта структура напоминает выводы Läuchli и Grattan [72] в их исследовании различных видов растений и сельскохозяйственных культур, в частности однолетних культур и злаков. Vialfas, напротив, продемонстрировал более консервативную устьичную реакцию по всем обработкам, сохраняя относительно стабильные, хотя и более низкие, уровни проводимости. Хотя этот подход может ограничивать ростовой потенциал в оптимальных условиях, он может давать преимущество в постоянно стрессовых средах, как предполагают Hochberg и др. [73] в их работе над сортами винограда. Промежуточные реакции Guara и Avijor, причем Guara в целом сохранял более высокую устьичную проводимость при стрессе, предполагают различные стратегии осмотической регуляции. Способность Guara поддерживать относительно более высокий газообмен в соленых условиях может указывать на более эффективную компартментацию ионов или накопление осмолитов — механизмы, которые были связаны с повышенной солеустойчивостью подвоя горького миндаля по сравнению с Garnem [47].
4.2.3. Анализ содержания хлорофилла с помощью SPAD
Стабильно более высокие значения SPAD, продемонстрированные Guara в контрольной обработке, предполагают генотип-специфичный признак, который может быть связан с более высоким фотосинтетическим потенциалом или структурными различиями в ткани листьев. Различия в значениях SPAD между видами, по-видимому, зависят как от генетических, так и от экологических факторов. Atar и др. [74] продемонстрировали, что виды могут показывать характерные структуры содержания хлорофилла, со значительными вариациями среди различных видов деревьев и кустарников даже в идентичных экологических условиях.
По мере увеличения солевого стресса от 25 до 75 мМ NaCl генотип-специфичные реакции стали более выраженными, выявляя различные стратегии поддержания содержания хлорофилла в неблагоприятных условиях. Способность Guara сохранять высокие значения SPAD — и даже показывать увеличение при сильном стрессе (75 мМ NaCl) — особенно примечательна. Эта реакция параллельна выводам Acosta-Motos и др. [65] у E. myrtifolia, где увеличение значений SPAD при солевом стрессе было связано с морфологическими адаптациями листьев, такими как увеличенная толщина, что улучшало диффузию CO₂ к хлоропластам.
Стабильность значений SPAD, наблюдаемая у Penta по уровням стресса, в частности его более низкие значения при высоком стрессе (75 мМ NaCl), предполагает другую адаптивную стратегию. Эта структура напоминает выводы Munns и Tester [49], которые рассмотрели различные механизмы солеустойчивости и отметили, что некоторые растения поддерживают стабильные уровни хлорофилла как консервативную стратегию роста в стрессовых условиях. Однако важно отметить, что, хотя содержание хлорофилла может быть показателем фотосинтетической способности, связь между этими параметрами при солевом стрессе может зависеть от вида. Stepien и Johnson [75] обнаружили, что солеустойчивый Thellungiella сохранял как содержание хлорофилла, так и эффективность фотосинтеза при солевом стрессе, в то время как чувствительный к соли Arabidopsis показывал снижение обоих параметров.
Промежуточные реакции Avijor и Vialfas, характеризующиеся в целом увеличивающимися значениями SPAD с течением времени, даже при стрессе, указывают на некоторую степень устойчивости в поддержании содержания хлорофилла. Эта способность к накоплению хлорофилла в соленых условиях была связана с солеустойчивостью у других видов. Ashraf и Harris [76] отметили в своем обзоре физиологических маркеров солеустойчивости, что накопление хлорофилла как показатель солеустойчивости должно рассматриваться на видеспецифичной основе.
4.3. Визуальные симптомы солевого стресса
Все генотипы продемонстрировали прогрессирующее снижение высоты растений, количества листьев, здоровья листьев и развития корней по мере увеличения засоления, иллюстрируя кумулятивные негативные эффекты солевого стресса на рост и развитие растений. Эта структура соответствует выводам Dejampour и др. [77] в их исследовании подвоев персика.
Наблюдаемые различия в солеустойчивости среди изученных генотипов подтверждают выводы других исследований Prunus. Например, Zrig и др. [47] сообщили о значительной вариабельности солеустойчивости среди подвоев миндаля, причем некоторые генотипы сохраняли превосходные ростовые и физиологические параметры в соленых условиях. Аналогично, Rahneshan и др. [78] наблюдали дифференциальные реакции на солевой стресс среди генотипов фисташки, подчеркивая генетическую основу солеустойчивости у других многолетних древесных видов за пределами Prunus.
Превосходные показатели Guara и Penta при умеренных уровнях засоления (25–50 мМ NaCl) предполагают наличие эффективных механизмов солеустойчивости у этих генотипов. Это согласуется с выводами Momenpour и Imani [79], которые выявили вариабельность солеустойчивости среди сортов миндаля (Rabie, Perless, Super Nova, D99, 1–16 и 8–24), причем D99 сохранял более высокий рост и ионный гомеостаз в соленых условиях. Механизмы, лежащие в основе этой повышенной толерантности, могут включать более эффективное исключение Na⁺, улучшенную селективность K⁺/Na⁺ или усиленную компартментацию ионов, как предположили Munns и Tester [49].
Идентификация критического порога засоления около 50 мМ NaCl, при котором симптомы стресса стали более серьезными, соответствует наблюдениям в других исследованиях Prunus. Dejampour и др. [77] сообщили о значительном снижении эффективности фотосинтеза и ростовых параметров у подвоев персика (HS314, HS312, GF 677, HS 302) при уровнях засоления 6 и 9 дСм/м.
Серьезное воздействие при 75 мМ NaCl, особенно очевидное у Avijor, предполагает, что эта концентрация превышает порог толерантности этих генотипов Prunus. Этот вывод соответствует исследованию Toro и др. [50] по солевому стрессу у подвоев Prunus, которое показало, что Mariana 2624 и Garnem более устойчивы, чем Mazzard F12/1 и Cab6P при 120 мМ NaCl.
Наблюдаемые дифференциальные реакции в листьях, стеблях и корнях предоставляют понимание органоспецифических адаптаций к солевому стрессу. Высокая чувствительность листьев к солевому стрессу, о чем свидетельствует прогрессирующий хлороз и некроз, подчеркивает, что эти симптомы обычно вызываются избыточным содержанием Cl⁻ в листьях, в то время как Na⁺ имеет тенденцию накапливаться в корнях, стволе и ветвях, что согласуется с наблюдениями Zrig и др. [47] у сортов миндаля (Garnem и горький миндаль).
Эта чувствительность листьев, вероятно, отражает накопление токсичных ионов в фотосинтетических тканях; высокие концентрации как Na⁺, так и Cl⁻ в тканях листьев могут снижать фотосинтетическую способность. Деградация хлорофилла, специфически связанная с высоким накоплением Cl⁻, была описана Tavakkoli и др. [80].
Ухудшение корневой системы с повышением засоления было заметно у всех генотипов, особенно у Avijor, и напрямую влияло на поглощение воды и питательных веществ. Это наблюдение соответствует выводам Sandhu и др. [48], которые сообщили о значительно сниженных показателях выживаемости и биомассы корней у подвоев Prunus, подвергнутых солевому стрессу; обработка Na-Cl (120 мМ NaCl) вызвала наиболее серьезные снижения роста корней.
Поддержание лучшего развития корней у Guara и Penta при умеренном засолении предполагает более эффективные корневые механизмы солеустойчивости, возможно, включающие усиленные стратегии исключения или секвестрации ионов. Как описано Flowers и Colmer [81], виды различаются по своей способности ограничивать транспорт ионов от корней к побегам и различаются по своим способностям к компартментации ионов.
4.4. Изменения минерального состава при солевом стрессе
4.4.1. Содержание и распределение кальция
Распределение кальция различалось между органами растений и генотипами, причем корни стабильно показывали самые высокие уровни. Это согласуется с выводами Zrig и др. [47] и может смягчать токсичность Na⁺, поддерживая целостность мембраны и регулируя ионные каналы [82]. У некоторых растений поддержание высокого содержания Ca²⁺ при засолении связано с солеустойчивостью. Однако для подвоев миндаля не было найдено четкой ассоциации между концентрацией Ca²⁺ в тканях и солеустойчивостью [48]. Содержание Ca²⁺ в листьях снижалось с повышением засоления, однако Dejampour и др. [77] не обнаружили значительных изменений в концентрациях Ca²⁺ в листьях или соотношениях Na⁺/Ca²⁺ при солевом стрессе у подвоев P. dulcis. Уровни Ca²⁺ в древесине продемонстрировали сложную динамику, в то время как содержание Ca²⁺ в стеблях оставалось низким, что контрастирует с его ролью в солеустойчивости у других видов деревьев [83].
Что касается влияния генотипа, высокие уровни кальция в корнях Avijor предполагают потенциальный механизм солеустойчивости, так как Ca²⁺ помогает поддерживать целостность мембраны и регулировать ионный транспорт в соленых условиях [84]. Однако вариабельная реакция Avijor на засоление предполагает, что для его толерантности может существовать порог. Guara продемонстрировал стабильно высокие уровни Ca²⁺ по обработкам, особенно в листьях, что предполагает эффективную систему транспорта Ca²⁺ и robustny механизм гомеостаза, что может способствовать солеустойчивости. Эта структура аналогична выводам по фисташке, где высокие уровни Ca²⁺ связаны с повышенной солеустойчивостью [78].
Более низкие уровни Ca²⁺ у Penta могут указывать на менее эффективную систему поглощения или распределения, потенциально увеличивая восприимчивость к индуцированному солью дефициту кальция. Vialfas показал умеренные уровни Ca²⁺ с минимальной вариабельностью, особенно в ткани древесины, возможно, указывая на сбалансированную стратегию распределения, связанную с улучшенной солеустойчивостью. Rengel [82] продемонстрировал, что генотипическая вариация в управлении кальцием включает эффективность использования Ca²⁺, способность к поглощению и транспорту Ca²⁺ и поддержание гомеостаза Ca²⁺ во время солевого стресса.
4.4.2. Структуры накопления калия
Распределение калия значительно различалось по органам растений, при этом органоспецифические реакции на засоление наблюдались в терминах накопления ионов. Эта дифференциальная реакция по органам подчеркивает сложность целостного гомеостаза K⁺ в стрессовых условиях — концепцию, исследованную Anschütz и др. [85] в их исследовании механизмов регуляции калия.
Листья стабильно показывали самое высокое содержание K⁺, структура, соответствующая выводам Zrig и др. [47], отражающая важные роли калия в различных тканях растений, в частности в устьичной регуляции и фотосинтезе [86]. Значительное снижение содержания K⁺ в листьях при солевом стрессе согласуется с исследованиями, приписывающими это как сниженному поглощению K⁺, так и увеличенному выбросу K⁺ в соленых условиях [85]. Относительно высокие уровни K⁺, сохраняемые в корнях при 75 мМ NaCl, могут быть механизмом для поддержания гомеостаза K⁺/Na⁺, ключевого фактора солеустойчивости. Способность удерживать K⁺ внутри клеток может быть ключевой для солеустойчивости, как предположили Shabala и Cuin [87].
Avijor показал устойчивое снижение содержания K⁺ по обработкам, в то время как Penta сохранял несколько более высокие уровни K⁺, особенно при более высоких уровнях засоления. Это предполагает потенциальный механизм для лучшего удержания K⁺ в условиях высокого засоления [82]. Vialfas продемонстрировал самое высокое среднее содержание K⁺ в контрольных условиях, но показал значительные снижения по мере увеличения засоления. Guara продемонстрировал схожие тенденции, причем его содержание K⁺ достигло самого низкого уровня среди всех генотипов при 75 мМ NaCl. Эти различные реакции подчеркивают генетическое разнообразие в механизмах солеустойчивости внутри вида Prunus. Как отметили Shabala и Cuin [87], более 80% генетической вариабельности в солеустойчивости может быть связано с одним физиологическим признаком: способностью клетки предотвращать индуцированную NaCl утечку K⁺.
4.4.3. Накопление и распределение хлорида
Солеустойчивые генотипы цитрусовых и винограда с низкими концентрациями Cl⁻ в побегах имеют более высокие концентрации Cl⁻ в корнях по сравнению с чувствительными генотипами, что предполагает более эффективную компартментацию Cl⁻ в вакуолях корней. У некоторых подвоев авокадо более высокие концентрации Cl⁻ в листьях связаны с солеустойчивостью, потенциально указывая на эффективную секвестрацию Cl⁻ в вакуолях листьев [88].
Листья стабильно показывали самое высокое содержание Cl⁻, за ними следовали корни, стебли и древесина. Эта структура соответствует выводам Papadakis и др. [89] у Prunus cerasus L., где листья накапливали самые высокие уровни Cl⁻ при солевом стрессе. Такое значительное накопление Cl⁻ в листьях может приводить к ионной токсичности и нарушению эффективности фотосинтеза. Это предпочтительное накопление Cl⁻ в листьях может действовать как защитный механизм для более чувствительных органов или помогать поддерживать осмотический баланс, как предположили Munns и Tester [49] для гликофитов при солевом стрессе. Рассматривая генотип-специфичные реакции, Vialfas и Avijor накопили больше Cl⁻ в листьях, чем Penta и Guara. Эти различия могут быть обусловлены различиями в эффективности транспорта Cl⁻ от корней к побегам или способности к вакуолярной секвестрации, как предположили Teakle и Tyerman [88] в их исследовании транспорта Cl⁻ у растений.
Выраженные генотип-специфичные реакции при более высоких концентрациях соли, в частности отчетливая группировка Avijor и Guara отдельно от Penta и Vialfas при 50 мМ NaCl, предполагают дифференциальную активацию механизмов солеустойчивости. Это наблюдение согласуется с Sandhu и др. [48], которые сообщили о различных физиологических реакциях среди 14 коммерческих подвоев миндаля при различных уровнях засоления. При 75 мМ NaCl Avijor продемонстрировал самое высокое среднее содержание Cl⁻, за ним непосредственно следовал Vialfas, что предполагает, что эти генотипы могут быть аккумуляторами Cl⁻. Подобная вариабельность в накоплении Cl⁻ была отмечена Dejampour и др. [77] у подвоев Prunus в соленых условиях, где максимальное накопление Cl⁻ было зарегистрировано у генотипов Sahand и GF677. Стабильно более низкое накопление Cl⁻ у Penta по всем органам, в частности при более высоких уровнях засоления, предполагает возможные различия в механизмах солеустойчивости, аналогичные выводам, зарегистрированным у подвоев Prunus GF677 и MRS2, привитых на персик (cv. Armking) [90].
4.4.4. Содержание и распределение натрия
Распределение натрия значительно различалось по органам растений, причем листья показывали самое высокое содержание Na⁺, за ними следовали корни, стебли и древесина. Эта структура соответствует выводам Momenpour и Imani [79] у подвоев Prunus. Предпочтительное накопление Na⁺ в листьях может служить для защиты более чувствительных органов или помогать в поддержании осмотического баланса, как предложили Munns и Tester [49] и Hasegawa [84] для гликофитов при солевом стрессе. Такое предпочтительное накопление Na⁺ наблюдалось у других древесных видов, что предполагает, что это может быть общей стратегией у гликофитов [56,91].
Последовательная тенденция самых высоких уровней Na⁺ в листьях у всех генотипов может указывать на стратегию компартментации Na⁺ в листьях для защиты других органов или может отражать движение Na⁺ с транспирационным потоком к листьям. Однако значительное накопление Na⁺ в листьях может приводить к ионной токсичности и нарушению эффективности фотосинтеза, как наблюдали El Yamani и Cordovilla [92] на оливковых деревьях. Эти структуры накопления Na⁺ предполагают множественные стратегии управления солевым стрессом, включая селективный транспорт ионов, компартментацию Na⁺ в листьях и, возможно, исключение Na⁺ на уровне корней [53,93].
Генотипические различия в распределении Na⁺ наблюдались: Avijor накапливал больше Na⁺ в листьях, а Vialfas показывал более высокое содержание Na⁺ в корнях. Такие различия могут возникать из-за различий в эффективности транспорта Na⁺ от корней к побегам или способности к вакуолярной секвестрации [86,94]. У Avijor дифференциальное накопление Na⁺ в зависимости от обработки засолением согласуется с предыдущими исследованиями подвоев Prunus, где значительная вариабельность в накоплении ионов была отмечена среди сортов и подвоев [48]. Стабильно более низкое накопление Na⁺ у Penta, особенно при 50 мМ NaCl, предполагает потенциально уникальные механизмы солеустойчивости, о чем также сообщалось у других видов Prunus [89].
Примечательно, что генотип-специфичные реакции стали более выраженными при более высоком солевом стрессе, в частности при 50 мМ NaCl, что предполагает, что умеренное засоление может быть оптимальным для идентификации солеустойчивых генотипов. Однако схождение реакций при 75 мМ NaCl предполагает потенциальный пороговый эффект — явление, наблюдаемое в других исследованиях Prunus spp. [47,50].
4.4.5. Соотношение калий/натрий
Превосходная способность Guara и Penta поддерживать более высокие соотношения K⁺/Na⁺ при солевом стрессе заслуживает внимания и согласуется с наблюдениями Papadakis и др. [89] у сортов миндаля, где солеустойчивые генотипы продемонстрировали лучший гомеостаз K⁺/Na⁺.
Генетическая вариация влияет на способность поддерживать благоприятные соотношения K⁺/Na⁺, что является ключевым для солеустойчивости. Предпочтительное накопление K⁺ в листьях — это хорошо задокументированная стратегия у многих видов растений для смягчения пагубных последствий натрия для фотосинтетического аппарата [49]. Относительно стабильные соотношения K⁺/Na⁺, наблюдаемые в тканях древесины и стеблей, предполагают потенциальную буферную роль в ионном гомеостазе, как отмечено у оливковых деревьев El Yamani и Cordovilla [92]. Поддержание постоянных соотношений ионов в древесных тканях может быть важным для долгосрочной солеустойчивости у видов деревьев, потенциально защищая жизненно важные транспортные системы и меристематические области от ионных дисбалансов.
4.4.6. Соотношение кальций/натрий
Генотипические вариации в поддержании соотношения Ca²⁺/Na⁺ в соленых условиях, особенно сильные показатели Guara, указывают на различные механизмы солеустойчивости внутри вида Prunus. Эти различия, вероятно, происходят из-за вариаций в ионных транспортных системах, как предположили Shabala и Cuin [87]. Превосходные показатели Guara могут быть обусловлены более эффективными механизмами исключения Na⁺ или усиленными системами поглощения Ca²⁺, аналогичными тем, что обнаружены у солеустойчивых сортов других видов [49]. Стабильно более высокие соотношения Ca²⁺/Na⁺, наблюдаемые в корнях у всех генотипов, поддерживают идею о том, что корни служат ключевой первой линией защиты от солевого стресса. Эта структура предполагает наличие эффективных механизмов ионной селективности в тканях корней, возможно, включающих селективные ионные транспортеры, подобные описанным Shabala [95]. Резкое снижение соотношений Ca²⁺/Na⁺ в листьях с повышением засоления подчеркивает уязвимость фотосинтетических тканей к ионным дисбалансам. Этот вывод согласуется с Munns и Gilliham [56], которые подчеркивают важность поддержания благоприятных ионных соотношений в листьях для сохранения фотосинтетической способности при солевом стрессе. Генотипические различия в соотношениях Ca²⁺/Na⁺ в листьях, особенно более высокие соотношения, поддерживаемые Guara, могут быть связаны с различиями в стратегиях компартментации ионов или различиями в процессах загрузки и выгрузки ксилемы, как описано Rengel [82].
4.5. Сравнение показателей генотипов
Четыре генотипа миндаля продемонстрировали различные реакции на повышение засоления, выявляя различные уровни солеустойчивости.
Guara продемонстрировал наилучшие общие показатели в соленых условиях. Он сохранял рост и физиологические функции по уровням засоления, показывая особую устойчивость по диаметру ствола и сырой массе. Солеустойчивость Guara была подкреплена его способностью поддерживать высокие уровни Ca²⁺ и благоприятные ионные соотношения при стрессе. Penta занял близкое второе место по солеустойчивости. Хотя он не показывал самой высокой активности в контрольных условиях, Penta продемонстрировал замечательную стабильность по всем обработкам засолением. Он сохранял стабильную фотосинтетическую производительность и транспорт электронов при стрессе и показал эффективное исключение Na⁺ и регуляцию Cl⁻. Эта последовательная производительность предполагает robustny механизмы солеустойчивости. Vialfas показал хорошие показатели при низком и умеренном засолении, но более высокую чувствительность к сильному солевому стрессу. Он продемонстрировал превосходную активность в контрольных условиях и при низком засолении, в частности по ростовым параметрам. Однако Vialfas испытал значительные снижения при 75 мМ NaCl, что указывает на более низкий порог для сильного солевого стресса. Avijor оказался наиболее чувствительным к солевому стрессу среди четырех генотипов. Он показал значительные снижения ростовых параметров при умеренном и высоком уровнях засоления (25 и 50 мМ NaCl) и с трудом поддерживал физиологическую производительность при высоком засолении (75 мМ NaCl). Чувствительность Avijor была дополнительно подтверждена высоким накоплением Na⁺ в листьях, что предполагает менее эффективные механизмы исключения Na⁺.
С точки зрения общей солеустойчивости, генотипы могут быть ранжированы как Guara > Penta > Vialfas > Avijor. Этот рейтинг учитывает как абсолютные показатели при высоком засолении, так и стабильность реакции по уровням стресса.
4.6. Структура управления и практическое применение
4.6.1. Интегрированная структура управления солевым стрессом
Хотя наше исследование фокусируется на отборе генотипов, оптимизация производства миндаля в соленых условиях требует интегрированного подхода (Рисунок 10). Представленная структура иллюстрирует, как различные стратегии управления взаимодействуют для достижения улучшенных урожаев в соленых условиях. Генетическое управление через соответствующий отбор сортов — как исследовано в этом исследовании — формирует один из четырех ключевых столпов, наряду с управлением водными ресурсами, управлением почвой и непрерывным мониторингом.
Рисунок 10. Структура управления для выращивания миндаля в соленых условиях.
Оценка здоровья почвы играет ключевую роль в этом интегрированном подходе, в частности для управления солеными условиями. Она включает анализ физических, химических и биологических свойств почвы, при этом ключевые индикаторы, такие как электропроводность (ЭП), pH и коэффициент адсорбции натрия (SAR), используются для идентификации и мониторинга зон, пораженных солью. Хотя общие инструменты мониторинга здоровья почвы показали успех в управлении сельским хозяйством [96], управление миндальными садами в соленых условиях требует особого внимания к этим специфичным для засоления параметрам. Наши результаты демонстрируют, что мониторинг этих индикаторов предоставляет ключевую информацию для корректировки практик управления.
Стратегии управления, основанные на оценке почвы, включают внесение гипса для улучшения структуры почвы и усиления вымывания солей, оптимизацию методов орошения через капельные системы и соответствующие дренажные фракции, а также включение органического вещества для повышения микробной активности и доступности питательных веществ. Передовые инструменты мониторинга, такие как датчики и ГИС-технологии, обеспечивают непрерывную оценку почвы, гарантируя точные своевременные корректировки этих вмешательств. Этот целостный подход позволяет производителям максимизировать выгоды от солеустойчивых генотипов, сохраняя при этом здоровье почвы и обеспечивая долгосрочную устойчивость сада.
4.6.2. Генотип-специфичные применения
Дифференциальная солеустойчивость, наблюдаемая среди четырех генотипов миндаля, имеет значительные последствия для управления садами и селекционных программ, в частности в регионах, сталкивающихся с растущим засолением почвы.
Для районов с уровнями засоления до 50 мМ NaCl Guara становится оптимальным выбором из-за его последовательной производительности по различным уровням стресса. Его способность поддерживать рост и физиологические функции в соленых условиях делает его пригодным для широкого спектра сред, потенциально увеличивая устойчивость сада к колеблющемуся засолению почвы.
В регионах, подверженных более высоким уровням засоления или там, где засоление может увеличиваться со временем, Penta может быть предпочтительным вариантом. Его стабильная производительность по всем обработкам засолением, включая условия сильного стресса, предполагает, что он может быть лучше приспособлен к долгосрочному воздействию высокого засоления. Эффективные механизмы ионной регуляции Penta могут быть особенно ценны в этих сложных средах.
Vialfas, с его превосходной активностью в условиях низкого засоления, может быть отличным выбором для районов с мягкими проблемами засоления или в составе селекционной программы, направленной на объединение его признаков энергичного роста с механизмами солеустойчивости Guara или Penta.
Хотя Avijor показал самую высокую чувствительность к солевому стрессу, его признаки все еще могут быть ценны в селекционных программах. Понимание механизмов, лежащих в основе его чувствительности, может предоставить понимание ключевых генов или процессов, участвующих в солеустойчивости, потенциально приводя к разработке еще более устойчивых сортов.
Эти выводы также подчеркивают важность оценки и мониторинга засоления почвы и воды в управлении садами. Наблюдаемые генотип-специфичные пороги засоления могут определять стратегии орошения и практику внесения почвенных мелиорантов, помогая поддерживать оптимальные условия роста для каждого сорта.
Для селекционных программ эти результаты предоставляют основу для разработки новых солеустойчивых сортов миндаля. Скрещивание между Guara или Penta и другими высокоурожайными сортами может потенциально привести к появлению сортов, которые сочетают превосходную солеустойчивость с другими желательными агрономическими признаками.
Короче говоря, выбор генотипов миндаля должен быть адаптирован к конкретным экологическим условиям и целям управления. Это исследование предоставляет ценную информацию для такого принятия решений, потенциально способствуя более устойчивому и продуктивному выращиванию миндаля перед лицом растущего засоления почв.
5. Выводы
Это исследование четырех самоукореняющихся генотипов миндаля (Vialfas, Guara, Penta и Avijor) при различных уровнях засоления выявило генотип-специфичные реакции на солевой стресс по различным органам растений и физиологическим процессам. Все генотипы продемонстрировали критический порог засоления между 50 и 75 мМ NaCl, за которым происходит значительное ухудшение ростовых и физиологических параметров. Guara и Penta продемонстрировали превосходные общие показатели в соленых условиях, сохраняя лучший рост, физиологические функции и ионный гомеостаз по обработкам засолением. Эти генотипы показали более эффективные механизмы поддержания благоприятных соотношений K⁺/Na⁺ и Ca²⁺/Na⁺, в частности в листьях и корнях, что, по-видимому, было ключевым для их солеустойчивости.
Эти выводы имеют значительные последствия для выращивания миндаля в регионах, пораженных засолением почвы или воды. Наблюдаемые генотип-специфичные реакции предоставляют ценное руководство для выбора посадочного материала в сверхвысокой плотности самоукореняющихся миндальных садах — экономически эффективной альтернативе для регионов, сталкивающихся с нехваткой воды и проблемами засоления, будь то переход от традиционных миндальных садов или зерновых культур. Кроме того, идентифицированные солеустойчивые генотипы, в частности Guara и Penta, показывают значительные перспективы в качестве селекционного материала для разработки более устойчивых сортов миндаля.
Будущие исследования должны включать долгосрочные полевые исследования для оценки производительности этих генотипов в различных экологических условиях, так как солеустойчивость может зависеть от других абиотических факторов. Исследование молекулярной и генетической основы наблюдаемых различий в солеустойчивости могло бы облегчить маркер-ориентированную селекцию в селекционных программах. Оценка влияния солевого стресса на урожайность и качество плодов у этих генотипов также была бы ценна для коммерческого производства миндаля.
Вспомогательные материалы
Следующую вспомогательную информацию можно загрузить по адресу: https://www.mdpi.com/article/10.3390/agriculture15030254/s1; Рисунок S1. Box-plot и статистические данные для сырой массы в зависимости от взаимодействия обработка × орган, со значениями, объединенными по всем четырем генотипам для каждой комбинации обработка–орган; Рисунок S2. Box-plot для сырой массы в зависимости от взаимодействия обработка × орган × генотип; Рисунок S3. Box-plot и статистические данные для общей сырой массы растения в зависимости от взаимодействия генотип × обработка; Рисунок S4. Box-plot и статистические данные для сухой массы в зависимости от взаимодействия обработка × орган, со значениями, объединенными по всем четырем генотипам для каждой комбинации обработка–орган; Рисунок S5. Box-plot для сухой массы в зависимости от взаимодействия обработка × орган × генотип; Рисунок S6. Box-plot и статистические данные для общей сухой массы растения в зависимости от взаимодействия генотип × обработка; Рисунок S7. Общая эффективность фотосистемы II; Рисунок S8. Энергия и транспорт электронов; Рисунок S9. Рассеяние энергии и повреждения; Рисунок S10. Box-plot и статистические данные для Ca²⁺ в зависимости от взаимодействия обработка × орган; Рисунок S11. Box-plot и статистические данные для Ca²⁺ в зависимости от взаимодействия генотип × орган; Рисунок S12. Box-plot и статистические данные для Ca²⁺ в зависимости от взаимодействия генотип × обработка; Рисунок S13. Box-plot и статистические данные для K⁺ в зависимости от взаимодействия обработка × орган; Рисунок S14. Box-plot и статистические данные для K⁺ в зависимости от взаимодействия генотип × орган; Рисунок S15. Box-plot и статистические данные для K⁺ в зависимости от взаимодействия генотип × обработка; Рисунок S16. Box-plot и статистические данные для Cl⁻ в зависимости от взаимодействия обработка × орган; Рисунок S17. Box-plot и статистические данные для Cl⁻ в зависимости от взаимодействия генотип × орган; Рисунок S18. Box-plot и статистические данные для Cl⁻ в зависимости от взаимодействия генотип × обработка; Рисунок S19. Box-plot и статистические данные для Na⁺ в зависимости от взаимодействия обработка × орган; Рисунок S20. Box-plot и статистические данные для Na⁺ в зависимости от взаимодействия генотип × орган; Рисунок S21. Box-plot и статистические данные для Na⁺ в зависимости от взаимодействия генотип × обработка; Рисунок S22. Box-plot и статистические данные для K⁺/Na⁺ в зависимости от взаимодействия обработка × орган; Рисунок S23. Box-plot и статистические данные для K⁺/Na⁺ в зависимости от взаимодействия генотип × орган; Рисунок S24. Box-plot и статистические данные для K⁺/Na⁺ в зависимости от взаимодействия генотип × обработка; Рисунок S25. Box-plot и статистические данные для Ca²⁺/Na⁺ в зависимости от взаимодействия обработка × орган; Рисунок S26. Box-plot и статистические данные для Ca²⁺/Na⁺ в зависимости от взаимодействия генотип × орган; Рисунок S27. Box-plot и статистические данные для Ca²⁺/Na⁺ в зависимости от взаимодействия генотип × обработка; Таблица S1. Данные сплайнов для эффектов комбинаций генотип × обработка на диаметр ствола; Таблица S2. Данные сплайнов для эффектов комбинаций генотип × обработка на длину побега; Таблица S3. Описательная статистика измерений флуориметра; Таблица S4. Данные сплайнов для эффектов комбинаций генотип × обработка на устьичную проводимость; Таблица S5. Данные сплайнов для эффектов комбинаций генотип × обработка на значения SPAD; Таблица S6. Описательная статистика и анализ устойчивости концентраций ионов, параметров биомассы и ионных соотношений в образцах тканей растений; Таблица S7. ANOVA моделей log(переменная) p-значения каждого из факторов вместе с их взаимодействиями; Таблица S8. Устойчивые сравнения групповых p-значений каждого из факторов вместе с их взаимодействиями.
Ссылки
1. International Nut & Dried Fruit. Nuts & Dried Fruits Statistical Yearbook 2019/2020; International Nut & Dried Fruit: Reus, Spain, 2021; p. 80. [Google Scholar]
2. FAOSTAT. Food and Agricultural Commodities Production. Available online: http://www.fao.org/faostat/en/#data/QC/visualize (accessed on 20 January 2025).
3. Industry Research. Global Almond Industry Research Report 2023. Competitive Landscape, Market Size, Regional Status, and Prospect; Absolute Reports Pvt. Ltd.: Maharashtra, India, 2023; p. 111. [Google Scholar]
4. Spanish Ministry of Agriculture Fisheries and Food. Frutos Secos: Análisis de la Realidad Productiva 2021; Spanish Ministry of Agriculture, Fisheries and Food: Madrid, Spain, 2022; p. 60. [Google Scholar]
5. Felipe, A.J.; Rius, X.; Rubio-Cabetas, M.J. El Cultivo del Almendro. El Almendro II; Calidad Gráfica Araconsa SL: Zaragoza, Spain, 2022; p. 568. [Google Scholar]
6. Sottile, F.; Barone, E.; Barbera, G.; Palasciano, M. The Italian almond industry: New perspectives and ancient tradition. Acta Hortic. 2014, 1028, 401–407. [Google Scholar] [CrossRef]
7. Expósito, A.; Berbel, J. The economics of irrigation in almond orchards. Application to southern Spain. Agronomy 2020, 10, 796. [Google Scholar] [CrossRef]
8. Maldera, F.; Vivaldi, G.A.; Iglesias-Castellarnau, I.; Camposeo, S. Two almond cultivars trained in a super-high density orchard show different growth, yield efficiencies and damages by mechanical harvesting. Agronomy 2021, 11, 1406. [Google Scholar] [CrossRef]
9. Caruso, T.; Campisi, G.; Marra, F.P.; Camposeo, S.; Vivaldi, G.A.; Proietti, P.; Nasini, L. Growth and yields of ’Arbequina’ high-density planting systems in three different olive growing areas in Italy. Acta Hortic. 2014, 1057, 341–348. [Google Scholar] [CrossRef]
10. Connor, D.J.; Gómez-del-Campo, M.; Rousseaux, M.C.; Searles, P.S. Structure, management and productivity of hedgerow olive orchards: A review. Sci. Hortic. 2014, 169, 71–93. [Google Scholar] [CrossRef]
11. Pellegrini, G.; Sala, P.L.; Camposeo, S.; Contò, F. Economic sustainability of the olive oil high and super-high density cropping systems in Italy. Glob. Bus. Econ. Rev. 2017, 19, 553–569. [Google Scholar] [CrossRef]
12. Pellegrini, G.; Ingrao, C.; Camposeo, S.; Tricase, C.; Contò, F.; Huisingh, D. Application of water footprint to olive growing systems in the Apulia region: A comparative assessment. J. Clean. Prod. 2016, 112, 2407–2418. [Google Scholar] [CrossRef]
13. Agromillora. Super High-Density Almond Crops. Available online: https://www.agromillora.com/innovation/super-high-density-system/almonds-in-super-high-density/ (accessed on 20 January 2025).
14. Dias, A.B.; Caeiro, L.; Félix, G.; Falcão, J.M. Evaluation of biometric parameters of ‘Belona’, ‘Guara’ and ‘Lauranne’ cultivars in a superhigh density orchard. Acta Hortic. 2018, 1219, 73–78. [Google Scholar] [CrossRef]
15. Iglesias, I. Sistemas de plantación 2D: Una novedad en almendro, una realidad en frutales. Hacia una alta eficiencia. Rev. Frutic. 2019, 67, 22–44. [Google Scholar]
16. Ben Yahmed, J.; Ghrab, M.; Ben Mimoun, M. Eco-physiological evaluation of different scion-rootstock combinations of almond grown in Mediterranean conditions. Fruits 2016, 71, 185–193. [Google Scholar] [CrossRef]
17. Casanova-Gascón, J.; Figueras-Panillo, M.; Iglesias-Castellarnau, I.; Martín-Ramos, P. Comparison of SHD and open-center training systems in almond tree orchards cv. ‘Soleta’. Agronomy 2019, 9, 874. [Google Scholar] [CrossRef]
18. Phogat, V.; Mallants, D.; Cox, J.W.; Šimůnek, J.; Oliver, D.P.; Awad, J. Management of soil salinity associated with irrigation of protected crops. Agric. Water Manag. 2020, 227, 105845. [Google Scholar] [CrossRef]
19. Casanova-Gascón, J.; Martí-Dalmau, C.; Martín-Ramos, P. Comportamiento de variedades autorradicadas de almendro frente a factores limitantes del medio. Olint Rev. Plantaciones Superintensiv. Olivo 2020, 36, 31–34. [Google Scholar]
20. Hoagland, D.R.; Arnon, D.I. The Water-Culture Method for Growing Plants Without Soil; College of Agriculture-University of California; California Agricultural Experiment Station: Berkeley, CA, USA, 1950; p. 31. [Google Scholar]
21. Perica, S.; Goreta, S.; Selak, G.V. Growth, biomass allocation and leaf ion concentration of seven olive (Olea europaea L.) cultivars under increased salinity. Sci. Hortic. 2008, 117, 123–129. [Google Scholar] [CrossRef]
22. Sapkota, Y.; McDonald, L.M.; Griggs, T.C.; Basden, T.J.; Drake, B.L. Portable X-ray fluorescence spectroscopy for rapid and cost-effective determination of elemental composition of ground forage. Front. Plant Sci. 2019, 10, 317. [Google Scholar] [CrossRef]
23. Antonangelo, J.; Zhang, H. Soil and plant nutrient analysis with a portable XRF probe using a single calibration. Agronomy 2021, 11, 2118. [Google Scholar] [CrossRef]
24. Towett, E.K.; Shepherd, K.D.; Lee Drake, B. Plant elemental composition and portable X-ray fluorescence (pXRF) spectroscopy: Quantification under different analytical parameters. X-Ray Spectrom. 2016, 45, 117–124. [Google Scholar] [CrossRef]
25. McGladdery, C.; Weindorf, D.C.; Chakraborty, S.; Li, B.; Paulette, L.; Podar, D.; Pearson, D.; Kusi, N.Y.O.; Duda, B. Elemental assessment of vegetation via portable X-ray fluorescence (pXRF) spectrometry. J. Environ. Manag. 2018, 210, 210–225. [Google Scholar] [CrossRef]
26. Singh, V.K.; Sharma, N.; Singh, V.K. Application of X-ray fluorescence spectrometry in plant science: Solutions, threats, and opportunities. X-Ray Spectrom. 2021, 51, 304–327. [Google Scholar] [CrossRef]
27. Jones, J.B.; Case, V.W. Sampling, handling, and analyzing plant tissue samples. In Soil Testing and Plant Analysis, 3rd ed.; Westerman, R.L., Ed.; Soil Science Society of America: Madison, WI, USA, 2018; Volume 3, pp. 389–427. [Google Scholar]
28. Kalra, Y. Handbook of Reference Methods for Plant Analysis; CRC Press: Boca Raton, FL, USA, 1997; p. 320. [Google Scholar] [CrossRef]
29. Kalaji, H.M.; Schansker, G.; Ladle, R.J.; Goltsev, V.; Bosa, K.; Allakhverdiev, S.I.; Brestic, M.; Bussotti, F.; Calatayud, A.; Dąbrowski, P.; et al. Frequently asked questions about in vivo chlorophyll fluorescence: Practical issues. Photosynth. Res. 2014, 122, 121–158. [Google Scholar] [CrossRef] [PubMed]
30. Stirbet, A.; Govindjee. On the relation between the Kautsky effect (chlorophyll a fluorescence induction) and Photosystem II: Basics and applications of the OJIP fluorescence transient. J. Photochem. Photobiol. B 2011, 104, 236–257. [Google Scholar] [CrossRef] [PubMed]
31. Strasser, R.J.; Tsimilli-Michael, M.; Srivastava, A. Analysis of the chlorophyll a fluorescence transient. In Chlorophyll a Fluorescence: A Signature of Photosynthesis; Papageorgiou, G.C., Govindjee, Eds.; Springer: Dordrecht, The Netherlands, 2004; pp. 321–362. [Google Scholar] [CrossRef]
32. R Core Team. In R: A Language and Environment for Statistical Computing; R Foundation for Statistical Computing: Vienna, Austria, 2021.
33. Lilliefors, H.W. On the Kolmogorov-Smirnov test for normality with mean and variance unknown. J. Am. Stat. Assoc. 1967, 62, 399–402. [Google Scholar] [CrossRef]
34. Shapiro, S.S.; Wilk, M.B. An analysis of variance test for normality (complete samples). Biometrika 1965, 52, 591–611. [Google Scholar] [CrossRef]
35. Brown, M.B.; Forsythe, A.B. Robust tests for the equality of variances. J. Am. Stat. Assoc. 1974, 69, 364. [Google Scholar] [CrossRef]
36. Kruskal, W.H.; Wallis, W.A. Use of ranks in one-criterion variance analysis. J. Am. Stat. Assoc. 1952, 47, 583–621. [Google Scholar] [CrossRef]
37. Wilcox, R.R. Introduction to Robust Estimation and Hypothesis Testing, 5th ed.; Academic Press: London, UK, 2021. [Google Scholar]
38. Welch, B.L. On the comparison of several mean values: An alternative approach. Biometrika 1951, 38, 330–336. [Google Scholar] [CrossRef]
39. Mond, C.E.D.; Lenth, R.V. A robust confidence interval for location. Technometrics 1987, 29, 211. [Google Scholar] [CrossRef]
40. Harrell, F.E. Regression Modeling Strategies. With Applications to Linear Models, Logistic and Ordinal Regression, and Survival Analysis, 2nd ed.; Springer: Cham, Switzerland; New York, NY, USA, 2015; p. 582. [Google Scholar] [CrossRef]
41. Friedman, J.H. Multivariate adaptive regression splines. Ann. Stat. 1991, 19, 1–67. [Google Scholar] [CrossRef]
42. Durrleman, S.; Simon, R. Flexible regression models with cubic splines. Stat. Med. 2006, 8, 551–561. [Google Scholar] [CrossRef]
43. Krzanowski, W.J. An Introduction to Statistical Modelling; Wiley: London, UK, 2010; p. 272. [Google Scholar]
44. Akaike, H. Information theory and an extension of the maximum likelihood principle. In Selected Papers of Hirotugu Akaike; Parzen, E., Tanabe, K., Kitagawa, G., Eds.; Springer: New York, NY, USA, 1998; pp. 199–213. [Google Scholar] [CrossRef]
45. Schwarz, G. Estimating the dimension of a model. Ann. Stat. 1978, 6, 461–464. [Google Scholar] [CrossRef]
46. Chen, J.; Chen, Z. Extended Bayesian information criteria for model selection with large model spaces. Biometrika 2008, 95, 759–771. [Google Scholar] [CrossRef]
47. Zrig, A.; Ben Mohamed, H.; Tounekti, T.; Khemira, H.; Serrano, M.; Valero, D.; Vadel, A.M. Effect of rootstock on salinity tolerance of sweet almond (cv. Mazzetto). S. Afr. J. Bot. 2016, 102, 50–59. [Google Scholar] [CrossRef]
48. Sandhu, D.; Kaundal, A.; Acharya, B.R.; Forest, T.; Pudussery, M.V.; Liu, X.; Ferreira, J.F.S.; Suarez, D.L. Linking diverse salinity responses of 14 almond rootstocks with physiological, biochemical, and genetic determinants. Sci. Rep. 2020, 10, 21087. [Google Scholar] [CrossRef] [PubMed]
49. Munns, R.; Tester, M. Mechanisms of salinity tolerance. Annu. Rev. Plant Biol. 2008, 59, 651–681. [Google Scholar] [CrossRef]
50. Toro, G.; Pimentel, P.; Salvatierra, A. Effective categorization of tolerance to salt stress through clustering Prunus rootstocks according to their physiological performances. Horticulturae 2021, 7, 542. [Google Scholar] [CrossRef]
51. Tattini, M.; Gucci, R.; Coradeschi, M.A.; Ponzio, C.; Everard, J.D. Growth, gas exchange and ion content in Olea europaea plants during salinity stress and subsequent relief. Physiol. Plant. 2006, 95, 203–210. [Google Scholar] [CrossRef]
52. Rewald, B.; Leuschner, C.; Wiesman, Z.; Ephrath, J.E. Influence of salinity on root hydraulic properties of three olive varieties. Plant Biosyst. 2011, 145, 12–22. [Google Scholar] [CrossRef]
53. Flowers, T.J.; Colmer, T.D. Salinity tolerance in halophytes. New Phytol. 2008, 179, 945–963. [Google Scholar] [CrossRef]
54. Hasegawa, P.M.; Bressan, R.A.; Zhu, J.-K.; Bohnert, H.J. Plant cellular and molecular responses to high salinity. Annu. Rev. Plant Physiol. Plant Mol. Biol. 2000, 51, 463–499. [Google Scholar] [CrossRef]
55. Zrig, A.; Mohamed, H.B.; Tounekti, T.; Ennajeh, M.; Valero, D.; Khemira, H. A comparative study of salt tolerance of three almond rootstocks: Contribution of organic and inorganic solutes to osmotic adjustment. J. Agric. Sci. Technol. 2015, 17, 675–689. [Google Scholar]
56. Munns, R.; Gilliham, M. Salinity tolerance of crops–what is the cost? New Phytol. 2015, 208, 668–673. [Google Scholar] [CrossRef]
57. Kozlowski, T.T.; Pallardy, S.G. Acclimation and adaptive responses of woody plants to environmental stresses. Bot. Rev. 2002, 68, 270–334. [Google Scholar] [CrossRef]
58. Munns, R.; Termaat, A. Whole-plant responses to salinity. Funct. Plant Biol. 1986, 13, 143. [Google Scholar] [CrossRef]
59. Nicotra, A.B.; Atkin, O.K.; Bonser, S.P.; Davidson, A.M.; Finnegan, E.J.; Mathesius, U.; Poot, P.; Purugganan, M.D.; Richards, C.L.; Valladares, F.; et al. Plant phenotypic plasticity in a changing climate. Trends Plant Sci. 2010, 15, 684–692. [Google Scholar] [CrossRef] [PubMed]
60. Maggio, A.; Raimondi, G.; Martino, A.; De Pascale, S. Salt stress response in tomato beyond the salinity tolerance threshold. Environ. Exp. Bot. 2007, 59, 276–282. [Google Scholar] [CrossRef]
61. Isayenkov, S.V.; Maathuis, F.J.M. Plant salinity stress: Many unanswered questions remain. Front. Plant Sci. 2019, 10, 80. [Google Scholar] [CrossRef] [PubMed]
62. Rius-Garcia, X.; Videgain-Marco, M.; Casanova-Gascón, J.; Acuña-Rello, L.; Martín-Ramos, P. Comparative evaluation of salt tolerance in four self-rooted hazelnut (Corylus avellana L. and Corylus americana Walter) cultivars. Agronomy 2025, 15, 148. [Google Scholar] [CrossRef]
63. Ranjbarfordoei, A.; Samson, R.; Van Damme, P. Chlorophyll fluorescence performance of sweet almond [Prunus dulcis (Miller) D. Webb] in response to salinity stress induced by NaCl. Photosynthetica 2006, 44, 513–522. [Google Scholar] [CrossRef]
64. Jimenez, S.; Dridi, J.; Gutierrez, D.; Moret, D.; Irigoyen, J.J.; Moreno, M.A.; Gogorcena, Y. Physiological, biochemical and molecular responses in four Prunus rootstocks submitted to drought stress. Tree Physiol. 2013, 33, 1061–1075. [Google Scholar] [CrossRef]
65. Acosta-Motos, J.; Ortuño, M.; Bernal-Vicente, A.; Diaz-Vivancos, P.; Sanchez-Blanco, M.; Hernandez, J. Plant responses to salt stress: Adaptive mechanisms. Agronomy 2017, 7, 18. [Google Scholar] [CrossRef]
66. Stefanov, M.A.; Rashkov, G.D.; Borisova, P.B.; Apostolova, E.L. Changes in photosystem II complex and physiological activities in pea and maize plants in response to salt stress. Plants 2024, 13, 1025. [Google Scholar] [CrossRef] [PubMed]
67. Mihaljevic, I.; Viljevac Vuletic, M.; Tomas, V.; Horvat, D.; Zdunic, Z.; Vukovic, D. PSII photochemistry responses to drought stress in autochthonous and modern sweet cherry cultivars. Photosynthetica 2021, 59, 517–528. [Google Scholar] [CrossRef]
68. Baker, N.R. Chlorophyll fluorescence: A probe of photosynthesis in vivo. Annu. Rev. Plant Biol. 2008, 59, 89–113. [Google Scholar] [CrossRef] [PubMed]
69. Kalaji, H.M.; Jajoo, A.; Oukarroum, A.; Brestic, M.; Zivcak, M.; Samborska, I.A.; Cetner, M.D.; Łukasik, I.; Goltsev, V.; Ladle, R.J. Chlorophyll a fluorescence as a tool to monitor physiological status of plants under abiotic stress conditions. Acta Physiol. Plant 2016, 38, 102. [Google Scholar] [CrossRef]
70. Negrão, S.; Schmöckel, S.M.; Tester, M. Evaluating physiological responses of plants to salinity stress. Ann. Bot. 2017, 119, 1–11. [Google Scholar] [CrossRef] [PubMed]
71. Chaves, M.M.; Flexas, J.; Pinheiro, C. Photosynthesis under drought and salt stress: Regulation mechanisms from whole plant to cell. Ann. Bot. 2009, 103, 551–560. [Google Scholar] [CrossRef] [PubMed]
72. Läuchli, A.; Grattan, S.R. Plant responses to saline and sodic conditions. In Agricultural Salinity Assessment and Management, 2nd ed.; Wallender, W.W., Tanji, K.K., Eds.; American Society of Civil Engineers: Reston, VA, USA, 2011; pp. 169–205. [Google Scholar] [CrossRef]
73. Hochberg, U.; Degu, A.; Fait, A.; Rachmilevitch, S. Near isohydric grapevine cultivar displays higher photosynthetic efficiency and photorespiration rates under drought stress as compared with near anisohydric grapevine cultivar. Physiol. Plant. 2012, 147, 443–452. [Google Scholar] [CrossRef] [PubMed]
74. Atar, F.; Güney, D.; Bayraktar, A.; Yildirim, N.; Turna, İ. Seasonal change of chlorophyll content (SPAD value) in some tree and shrub species. Turk. J. For. Sci. 2020, 4, 245–256. [Google Scholar] [CrossRef]
75. Stepien, P.; Johnson, G.N. Contrasting responses of photosynthesis to salt stress in the glycophyte Arabidopsis and the halophyte Thellungiella: Role of the plastid terminal oxidase as an alternative electron sink. Plant Physiol. 2009, 149, 1154–1165. [Google Scholar] [CrossRef]
76. Ashraf, M.; Harris, P.J.C. Photosynthesis under stressful environments: An overview. Photosynthetica 2013, 51, 163–190. [Google Scholar] [CrossRef]
77. Dejampour, J.; Aliasgarzad, N.; Zeinalabedini, M.; Niya, M.R.; Hervan, E.M. Evaluation of salt tolerance in almond [Prunus dulcis (L.) Batsch] rootstocks. Afr. J. Biotechnol. 2012, 11, 11907–11912. [Google Scholar] [CrossRef]
78. Rahneshan, Z.; Nasibi, F.; Moghadam, A.A. Effects of salinity stress on some growth, physiological, biochemical parameters and nutrients in two pistachio (Pistacia vera L.) rootstocks. J. Plant Interact. 2018, 13, 73–82. [Google Scholar] [CrossRef]
79. Momenpour, A.; Imani, A. Effect of salinity stress on growth characteristics of selected almond (Prunus dulcis) genotypes. J. Plant Prod. Res. 2019, 26, 29–46. [Google Scholar]
80. Tavakkoli, E.; Rengasamy, P.; McDonald, G.K. High concentrations of Na+ and Cl− ions in soil solution have simultaneous detrimental effects on growth of faba bean under salinity stress. J. Exp. Bot. 2010, 61, 4449–4459. [Google Scholar] [CrossRef] [PubMed]
81. Flowers, T.J.; Colmer, T.D. Plant salt tolerance: Adaptations in halophytes. Ann. Bot. 2015, 115, 327–331. [Google Scholar] [CrossRef] [PubMed]
82. Rengel, Z. The role of calcium in salt toxicity. Plant Cell Environ. 1992, 15, 625–632. [Google Scholar] [CrossRef]
83. Läuchli, A.; Grattan, S.R. Plant growth and development under salinity stress. In Advances in Molecular Breeding Toward Drought and Salt Tolerant Crops; Jenks, M.A., Hasegawa, P.M., Jain, S.M., Eds.; Springer: Dordrecht, The Netherlands, 2007; pp. 1–32. [Google Scholar] [CrossRef]
84. Hasegawa, P.M. Sodium (Na+) homeostasis and salt tolerance of plants. Environ. Exp. Bot. 2013, 92, 19–31. [Google Scholar] [CrossRef]
85. Anschütz, U.; Becker, D.; Shabala, S. Going beyond nutrition: Regulation of potassium homoeostasis as a common denominator of plant adaptive responses to environment. J. Plant Physiol. 2014, 171, 670–687. [Google Scholar] [CrossRef] [PubMed]
86. Shabala, S.; Pottosin, I. Regulation of potassium transport in plants under hostile conditions: Implications for abiotic and biotic stress tolerance. Physiol. Plant. 2014, 151, 257–279. [Google Scholar] [CrossRef]
87. Shabala, S.; Cuin, T.A. Potassium transport and plant salt tolerance. Physiol. Plant. 2008, 133, 651–669. [Google Scholar] [CrossRef]
88. Teakle, N.L.; Tyerman, S.D. Mechanisms of Cl− transport contributing to salt tolerance. Plant Cell Environ. 2010, 33, 566–589. [Google Scholar] [CrossRef] [PubMed]
89. Papadakis, I.E.; Veneti, G.; Chatzissavvidis, C.; Therios, I. Physiological and growth responses of sour cherry (Prunus cerasus L.) plants subjected to short-term salinity stress. Acta Bot. Croat. 2018, 77, 197–202. [Google Scholar] [CrossRef]
90. Massai, R.; Remorini, D.; Tattini, M. Gas exchange, water relations and osmotic adjustment in two scion/rootstock combinations of Prunus under various salinity concentrations. Plant Soil 2004, 259, 153–162. [Google Scholar] [CrossRef]
91. Li, B.; Tester, M.; Gilliham, M. Chloride on the move. Trends Plant Sci. 2017, 22, 236–248. [Google Scholar] [CrossRef]
92. El Yamani, M.; Cordovilla, M.d.P. Tolerance mechanisms of olive tree (Olea europaea) under saline conditions. Plants 2024, 13, 2094. [Google Scholar] [CrossRef] [PubMed]
93. Malakar, P.; Chattopadhyay, D. Adaptation of plants to salt stress: The role of the ion transporters. J. Plant Biochem. Biotechnol. 2021, 30, 668–683. [Google Scholar] [CrossRef]
94. Mansour, M.M.F. Role of vacuolar membrane transport systems in plant salinity tolerance. J. Plant Growth Regul. 2022, 42, 1364–1401. [Google Scholar] [CrossRef]
95. Shabala, S. Learning from halophytes: Physiological basis and strategies to improve abiotic stress tolerance in crops. Ann. Bot. 2013, 112, 1209–1221. [Google Scholar] [CrossRef]
96. Reddy, A.A. The soil health card Scheme in India: Lessons learned and challenges for replication in other developing countries. J. Nat. Resour. Policy. Res. 2019, 9, 124–156. [Google Scholar] [CrossRef]
Rius-García X, Videgain-Marco M, Casanova-Gascón J, Acuña-Rello L, Zufiaurre-Galarza R, Martín-Ramos P. Evaluation of Salt Tolerance in Four Self-Rooted Almond Genotypes for Super-High-Density Orchards Under Varying Salinity Levels. Agriculture. 2025; 15(3):254. https://doi.org/10.3390/agriculture15030254
Перевод статьи «Evaluation of Salt Tolerance in Four Self-Rooted Almond Genotypes for Super-High-Density Orchards Under Varying Salinity Levels» авторов Rius-García X, Videgain-Marco M, Casanova-Gascón J, Acuña-Rello L, Zufiaurre-Galarza R, Martín-Ramos P., оригинал доступен по ссылке. Лицензия: CC BY. Изменения: переведено на русский язык
Фото: freepik
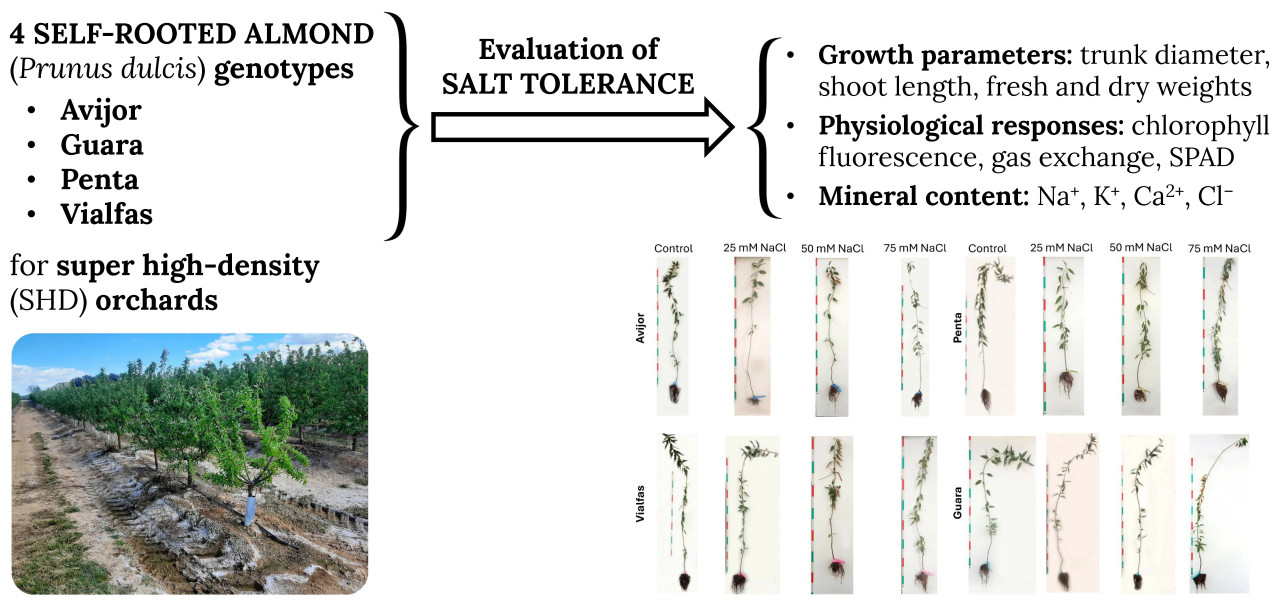
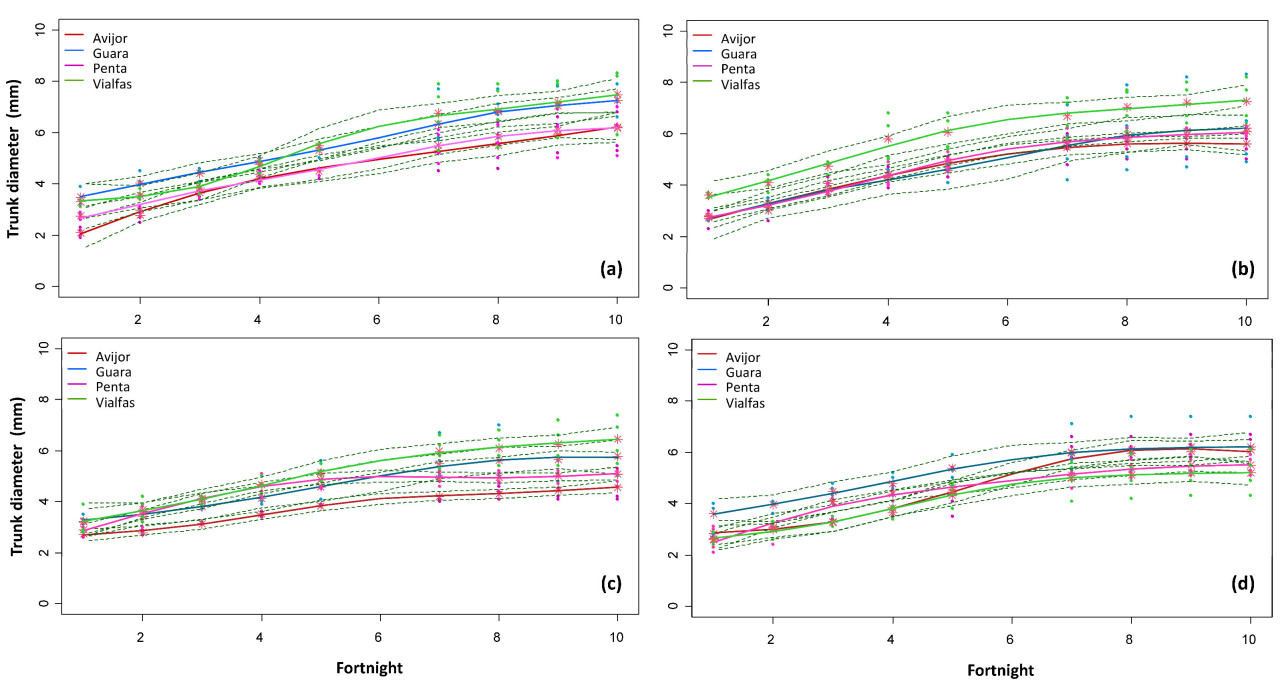
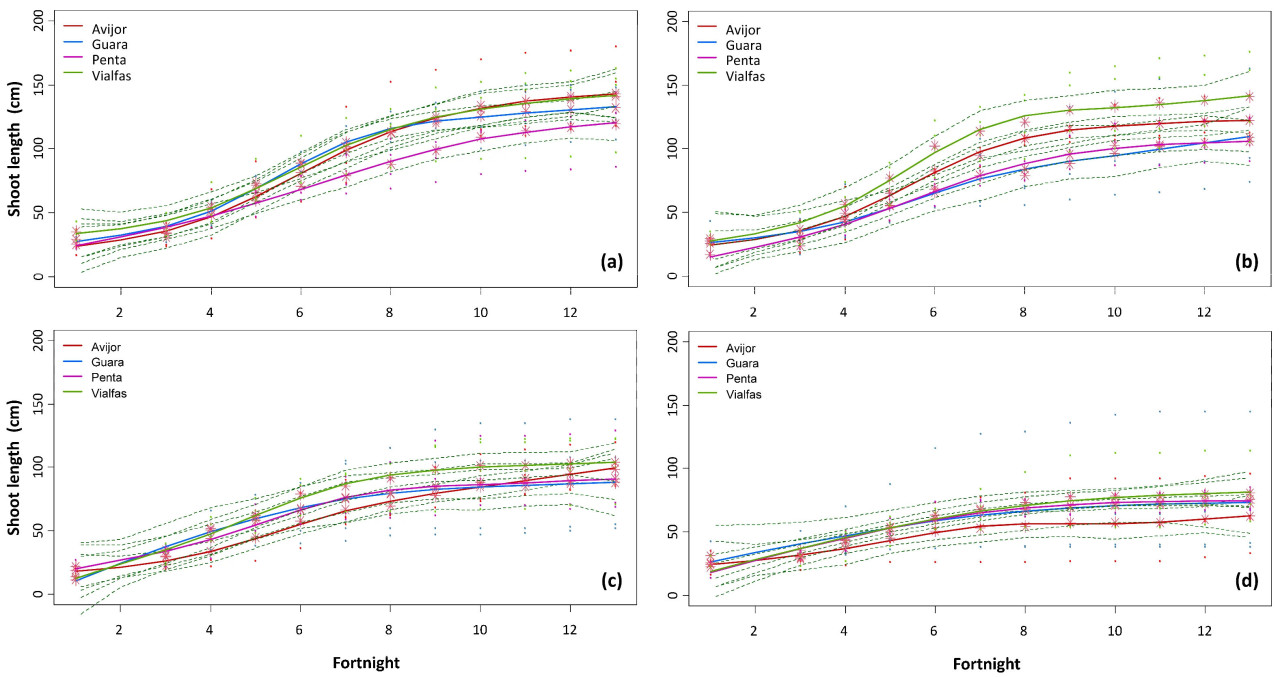
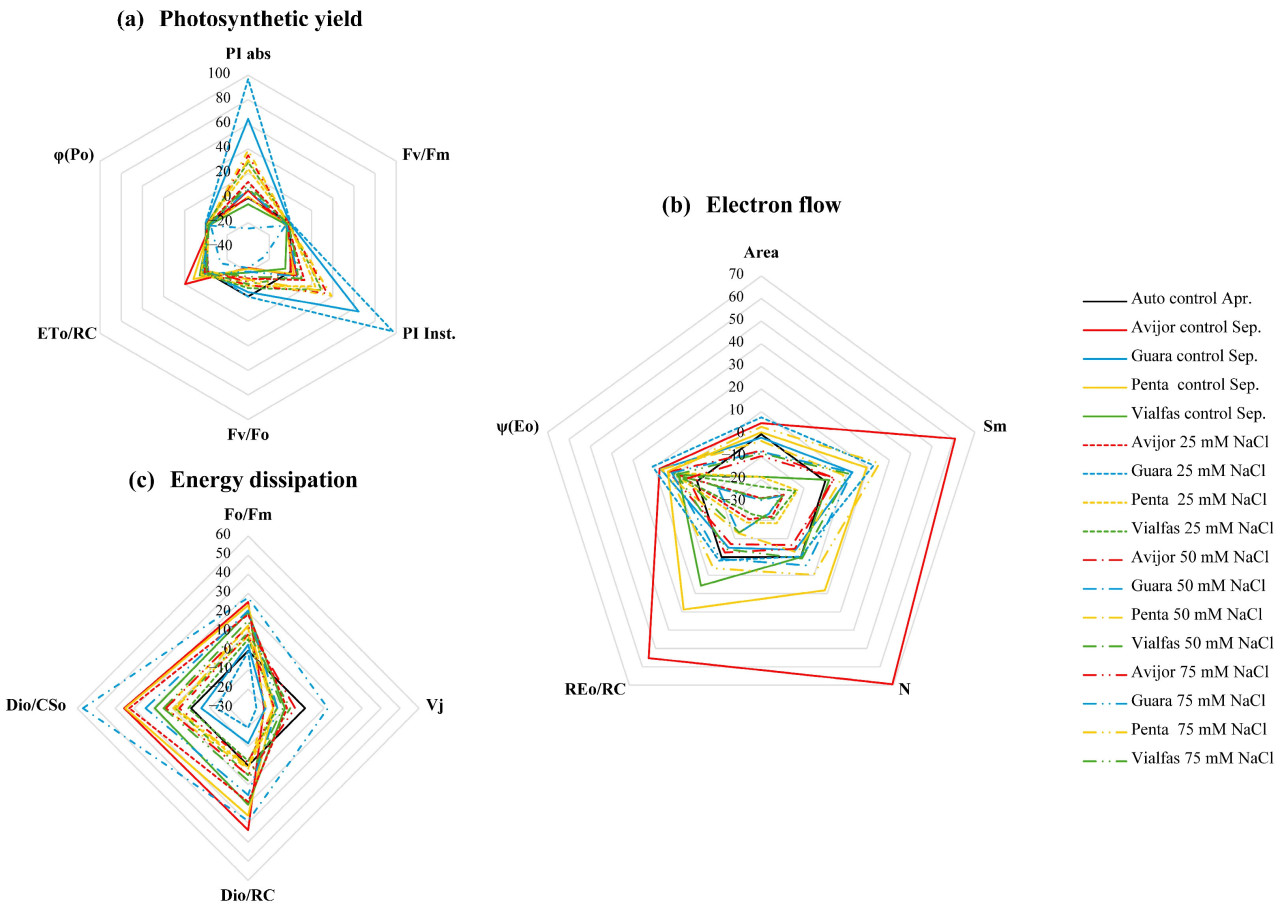
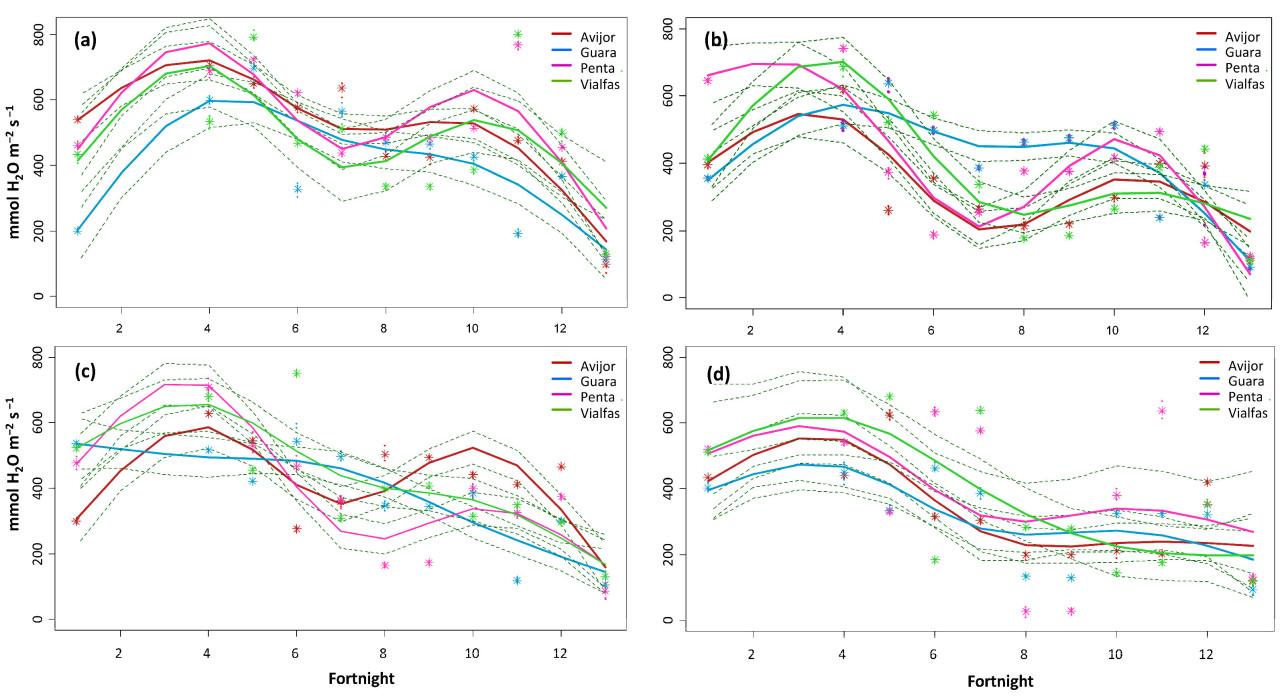
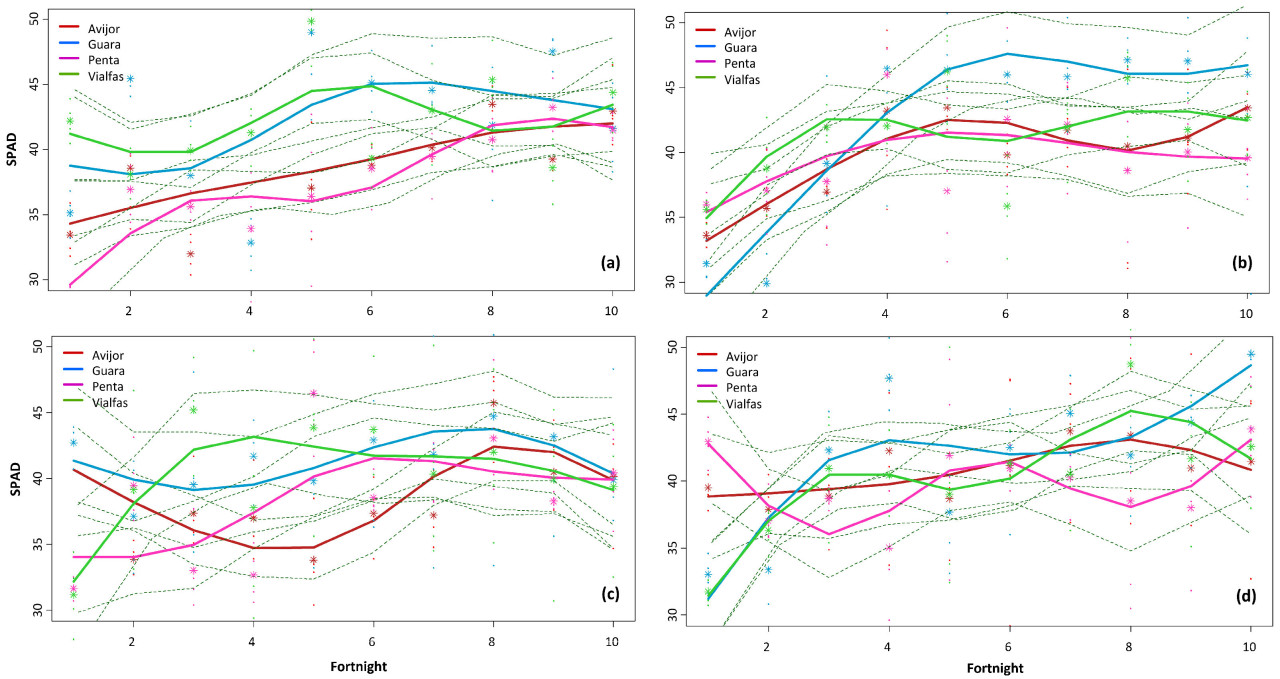

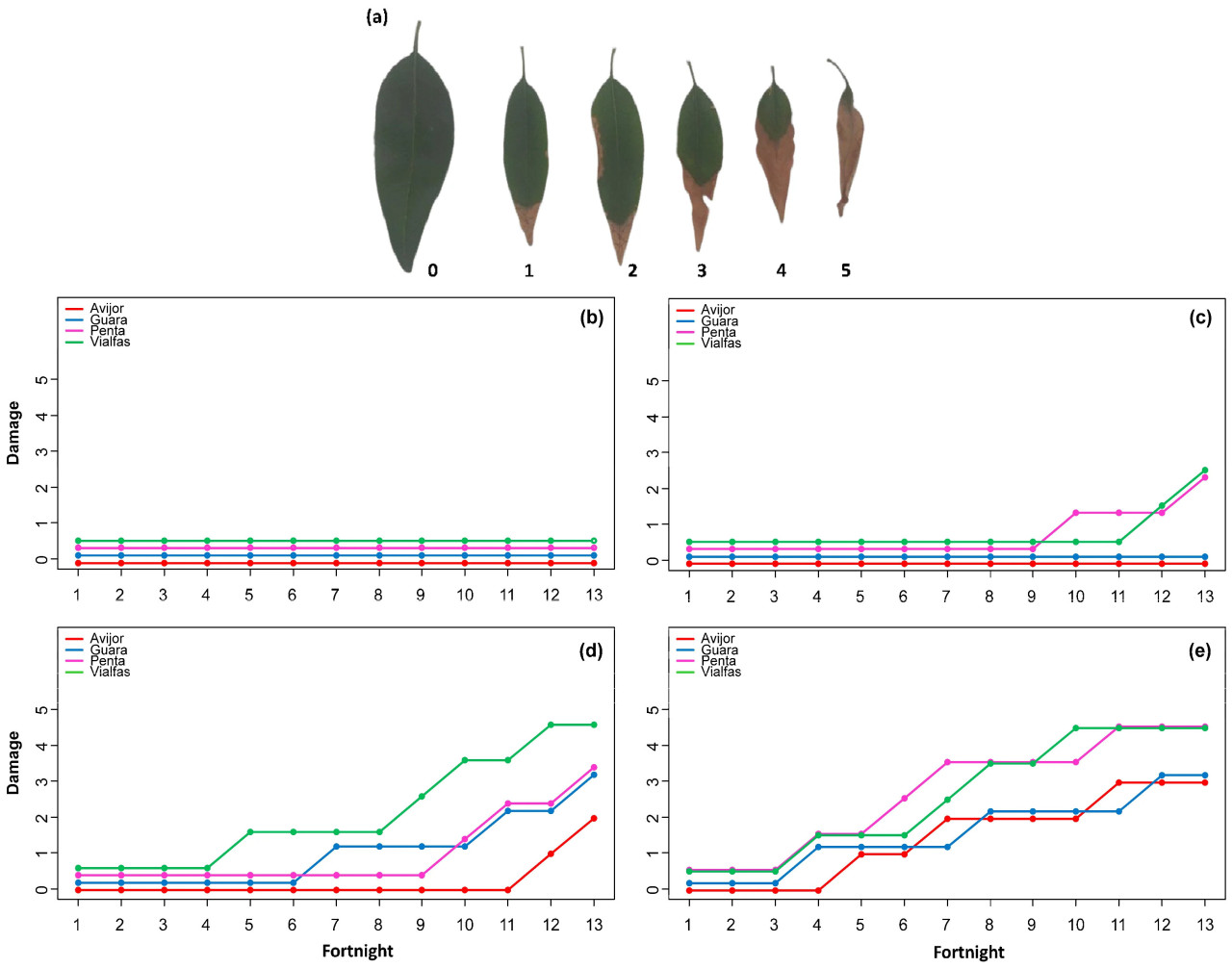
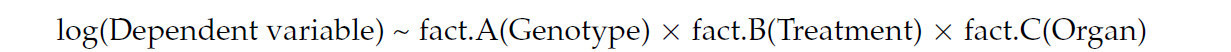
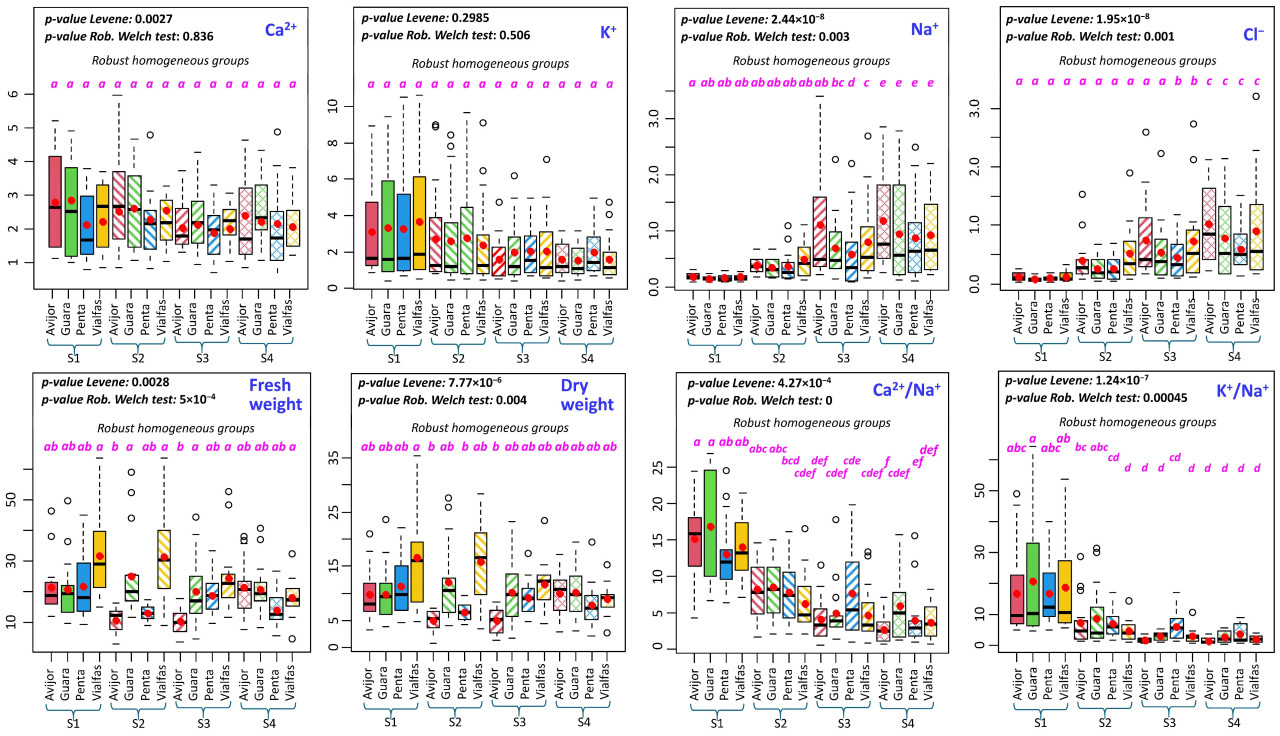
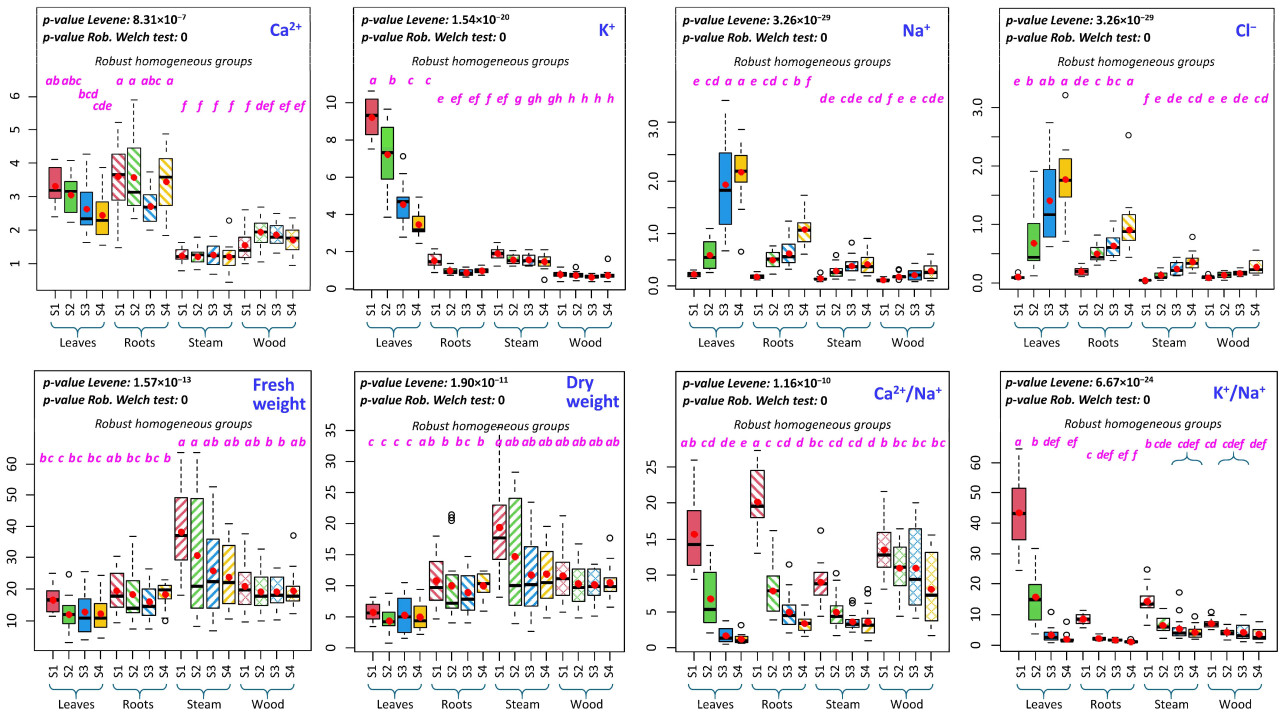
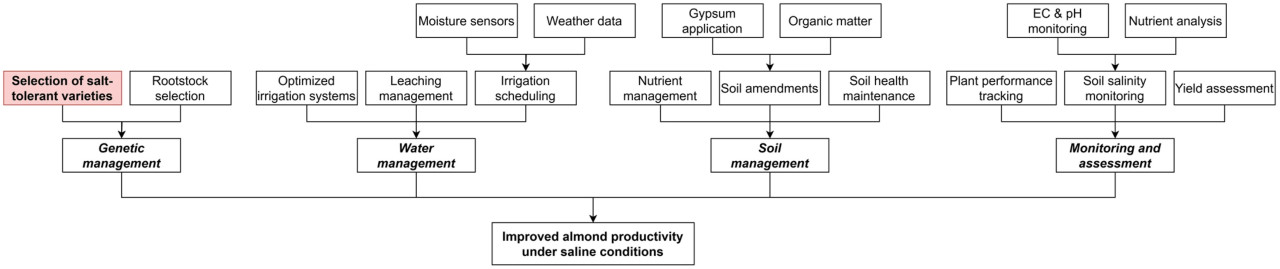













































































































Комментарии (0)