Кратковременная подкормка фосфором восстанавливает здоровую микрофлору в обеднённой жёлтой почве рисовых полей
Фосфор (P) в почве играет важную роль в процессе регуляции активности почвенных ферментов микробными сообществами. Цель данной работы — изучить, как кратковременное внесение фосфорных удобрений влияет на состав и функциональность сообщества почвенных грибов, что позволит глубже понять сложные реакции почвенных грибов на удобрение.
Аннотация
Для проведения вегетационного эксперимента были отобраны образцы почвы с многолетнего (длительного) опытного участка, где не вносились фосфорные удобрения. Вегетационный эксперимент включал четыре варианта обработки: без фосфорных удобрений (NK), с химическим фосфорным удобрением (NPK), 1/2 органического + 1/2 химического удобрения (MNP) и органическое удобрение (M). Для анализа состава, разнообразия и функциональности сообществ почвенных грибов использовалось высокопроизводительное секвенирование. Результаты показали, что кратковременное внесение фосфора значительно увеличило индексы Шеннона и Пьелу для почвенных грибов: прирост составил 34,48–59,00% и 29,79–53,19% соответственно. Наиболее обильными типами грибов были Ascomycota и Basidiomycota, тогда как среди родов доминировали Cladosporium и Emericellopsis. Основными факторами, влияющими на состав сообщества почвенных грибов, были общий азот (TN) и органическое вещество (OM). Анализ линейного дискриминантного анализа эффекта (LEfSe) показал, что при обработке NPK значительно обогащались грибы типа Mortierellomycota. Анализ FUNGuild выявил, что по сравнению с обработкой NK относительное обилие категории «Патоген животных – Эндофит – Паразит лишайников – Патоген растений – Древесный сапротроф» снизилось на 67,54%, 46,93% и 44,10% при обработках NPK, MNP и M соответственно. Относительное обилие «Патогенов растений» составило менее 1% в обработках NPK и MNP. Эти результаты указывают на то, что кратковременное внесение фосфора повысило уровень питательных веществ в почве и разнообразие сообщества почвенных грибов. Химическое фосфорное удобрение значительно улучшило структуру сообщества грибов в рисовых полях с желтым грунтом, способствуя развитию полезных грибов и подавлению патогенов.
1. Введение
Фосфор (P) является важнейшим элементом для роста растений и играет ключевую роль в прорастании семян, развитии корней и улучшении качества сельскохозяйственных культур [1,2,3]. Доступного фосфора в почвах часто недостаточно для удовлетворения потребностей растений в росте [4]. Фосфорные удобрения могут обеспечить фосфор, необходимый для роста сельскохозяйственных культур на полях, тем самым улучшая урожайность и качество [5,6]. Однако в сельскохозяйственном производстве Китая часто наблюдается неконтролируемое внесение P-удобрений, что привело ко всё более заметному проявлению низкой эффективности использования удобрений при высоких нормах их внесения, что оказало негативное воздействие на общее здоровье агроэкосистем [7,8]. Таким образом, корректировка стратегий удобрения и восполнение дефицита P в почвах, испытывающих его недостаток, с помощью различных удобрений важны для выяснения соответствующих методов удобрения почв, длительно испытывающих дефицит P, и для руководства практикой управления сельскохозяйственным удобрением. Почвенные грибы, как важная группа почвенных микроорганизмов, служат одними из основных индикаторов здоровья почвы и играют значимую роль в поддержании плодородия почвы, повышении продуктивности сельскохозяйственных культур и движении круговорота питательных веществ [9,10,11]. Грибы разлагают некоторые органические вещества в почве, которые трудно разлагаются бактериями, высвобождают углерод и питательные вещества в почвенный раствор, способствуют секвестрации почвенного органического углерода и являются важными регуляторами углеродного баланса почвы [12]. Таким образом, изучение восстановления и улучшения грибных сообществ и функциональных групп в почвах, длительно испытывающих дефицит P, после кратковременного внесения P-удобрений может углубить понимание механизма реакции почвенных грибных сообществ на удобрение и предоставить теоретическую основу для удобрения, безопасного производства риса и продвижения устойчивого развития почв на желтоземных рисовых полях Гуйчжоу.
Исследования показали, что по сравнению с отсутствием удобрения или несбалансированным удобрением, сбалансированное удобрение (NPK) может улучшить структуру микробного сообщества и увеличить микробное разнообразие [13,14]. Навоз значительно увеличил относительное обилие грибов, но снизил разнообразие грибов и видовое богатство. Химическое удобрение оказывает минимальное влияние на разнообразие грибов, но значительно увеличивает относительное обилие патогенных грибов (Fusarium и Colletotrichum) [15]. Кроме того, 38-летний длительный эксперимент по удобрению показал, что органическое удобрение оказывает более значительное влияние на бактериальные сообщества, чем химические удобрения, тогда как грибные сообщества были более чувствительны к внесению химических удобрений [16]. Wang [5] сообщил, что дефицит P увеличил относительное обилие Ascomycota, тогда как внесение P увеличило относительное обилие Basidiomycota и Mortierellomycota. По сравнению с химическим удобрением, комбинация P и органических удобрений была более эффективной для увеличения численности и разнообразия почвенных грибов. Другие исследования показали, что химические удобрения способствуют росту почвенных патогенных грибов, тогда как органические удобрения способствуют росту сапротрофных и микоризных грибов и подавляют почвенные патогены [17,18]. Эти исследования свидетельствуют о том, что внесение органических удобрений и сбалансированное удобрение оказывают положительное влияние на увеличение или поддержание разнообразия и относительного обилия микробного сообщества почвы. Отсутствие удобрения или несбалансированное удобрение в длительной перспективе приводит к нарушению баланса микробного сообщества, что негативно сказывается на здоровье почвы.
Большинство исследований реакции микробных сообществ на удобрение были сосредоточены на бактериях [19,20,21], при этом меньше внимания уделялось грибам [22]. Почвенные грибные сообщества обычно подвержены влиянию питательного статуса почвы и условий окружающей среды [23]. Внесение удобрений вводит питательные вещества, которые снижают зависимость микробного сообщества от углерода растений и активируют многочисленные дремлющие виды грибов. Однако внесение химических удобрений может привести к подкислению почвы и потере питательных веществ, ослабляя сеть взаимодействия растений и микроорганизмов в почве [24,25]. Некоторые исследования предполагают, что P-удобрения изменяют физико-химические свойства почвы (AP, OM и pH), тем самым перестраивая ризосферные грибные сообщества [5]. Другие исследования показали, что изменения в структуре грибных сообществ на альпийских лугах и плато-пастбищах более сильно связаны с содержанием почвенного органического углерода (SOC), азота и P, чем с pH почвы [26,27].
Длительное несбалансированное удобрение приводит к снижению плодородия почвы, уменьшению урожайности сельскохозяйственных культур и снижению микробного разнообразия. Поэтому улучшение структуры грибного сообщества в почвах при длительном несбалансированном удобрении является одной из главных проблем в исследованиях здоровья почвы, однако исследований по этой теме мало. Учитывая важную роль грибов в почвенных функциях и экосистемах, а также растущую обеспокоенность по поводу продолжающейся утраты биоразнообразия, становится всё более важным изучать влияние кратковременного внесения P-удобрений на почвенные грибные сообщества. На основе длительных экспериментов на Научной наблюдательной и экспериментальной станции по сохранению пахотных земель и сельскохозяйственной окружающей среды, мы сосредоточились на рисовых почвах, чтобы исследовать влияние кратковременного внесения P-удобрений на структуру грибного сообщества и функциональные группы в почвах с длительным дефицитом P. Кроме того, была проанализирована взаимосвязь между составом грибного сообщества и свойствами почвы, что предоставляет теоретическую основу для устойчивого управления желтоземами в Гуйчжоу.
2. Материалы и методы
2.1. Место исследования
Место исследования расположено на Гуйчжоуской сельскохозяйственной академии Научной наблюдательной и экспериментальной станции по сохранению пахотных земель и сельскохозяйственной окружающей среды (E: 106°39′52″, N: 26°29′49″) в районе Хуаси, город Гуйян, провинция Гуйчжоу. Экспериментальная зона находится в холмистой местности с желтыми почвами центральной части провинции Гуйчжоу, относится к субтропическому муссонному климату со средней высотой 1071 м. Среднегодовая температура в 2021 году составила 16,2 °C, а годовое количество осадков — 1335,6 мм. Почва образовалась из триасовых известняков и остатков песчаниковых сланцев, тип почвы классифицируется как Anthrosols, сформированные на материнской породе желтой почвы. Эксперимент был официально начат в 1995 году. До начала эксперимента были измерены физико-химические свойства почвы, которые показали pH 6,75, содержание органического вещества (OM), общего азота (TN), общего фосфора (TP), общего калия (TK), щелочного азота (AN), доступного фосфора (AP) и доступного калия (AK) составило 44,50 г·кг⁻¹, 1,96 г·кг⁻¹, 2,30 г·кг⁻¹, 13,8 г·кг⁻¹, 134 мг·кг⁻¹, 13,4 мг·кг⁻¹ и 294 мг·кг⁻¹ соответственно.
2.2. Экспериментальный дизайн
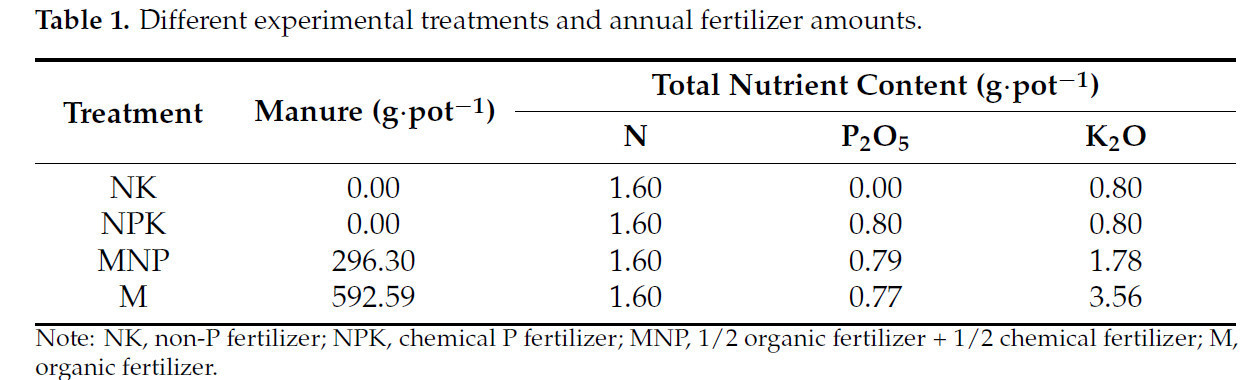
В этом исследовании желтая почва с рисовых полей, без длительного внесения P-удобрений, была отобрана в 2020 году для вегетационных опытов (опытов в горшках). Был проведен вегетационный опыт с четырьмя вариантами обработки: (1) без P-удобрения (NK), (2) химическое P-удобрение (NPK), (3) 1/2 органического удобрения + 1/2 химического удобрения (MNP) и (4) органическое удобрение (M). Эксперимент был проведен в рандомизированной полной блочной схеме с четырьмя повторностями на обработку, с двумя растениями риса, высаженными в 25 кг почвы на горшок. Перед высадкой риса фосфорные и калийные удобрения или органические удобрения вносились в качестве основного удобрения в соответствии с обработками (Таблица 1). Для обработок с химическими удобрениями мочевина вносилась дважды в течение вегетационного периода риса. Использованным органическим удобрением был коровий навоз (со средним содержанием C 10,4%; N 2,7 г·кг⁻¹; P₂O₅ 1,3 г·кг⁻¹; и K₂O 6,0 г·кг⁻¹), а химическими удобрениями были мочевина (N, 46%), суперфосфат (P₂O₅, 16%) и хлорид калия (K₂O, 60%). Помимо удобрения, другие меры управления в вегетационных опытах были одинаковыми.
Таблица 1. Различные экспериментальные обработки и годовые нормы удобрений.
2.3. Отбор почвенных образцов и измерения
2.3.1. Отбор почвенных образцов
Отбор почвенных образцов проводился после уборки риса в ноябре 2022 года. По одному почвенному образцу было случайным образом отобрано из каждого горшечного растения, и после удаления видимого органического вещества, камней и корней риса, образец был разделен на две части. Часть каждого свежего почвенного образца была просеяна через сито 2 мм и затем высушена на воздухе при комнатной температуре для определения физико-химических свойств почвы, в то время как другая часть была сохранена при температуре -80 °C для последующего выделения ДНК и анализа структуры грибного сообщества.
2.3.2. Определение физических и химических свойств почвы
pH почвы был измерен при соотношении почва/вода 1:2,5, содержание органического вещества (OM) почвы было определено с помощью метода объемного бихромата калия, общий азот (TN) почвы был определен методом Кьельдаля, доступный фосфор (AP) был определен с использованием метода Олсена с УФ-видимым спектрофотометром, а содержание доступного калия (AK) было определено с использованием пламенной фотометрии [28].
2.3.3. Выделение ДНК и секвенирование на платформе Illumina
Почвенная ДНК была выделена и протестирована на концентрацию и качество в соответствии с инструкциями производителя (Omega Bio-tek, Norcross, GA, США). После выделения ДНК концентрация и качество ДНК были измерены с помощью спектрофотометра NanoDrop NC2000 (Thermo Scientific, Waltham, MA, США) и электрофореза в агарозном геле. Область ITS рибосомальной РНК грибов была амплифицирована с использованием специфических праймеров ITS1F (5′-CTTGGTCATTTAGGAGATAA3′) и ITS2R (5′-GCTGGTTCTTCATCGATGC-3′). Была приготовлена реакционная смесь для ПЦР, после чего следовала начальная денатурация при 95 °C в течение 3 минут, затем 27 циклов амплификации. Каждый цикл начинался с денатурации при 95 °C в течение 30 секунд, затем следовал отжиг при 55 °C в течение 30 секунд и элонгация при 72 °C в течение 45 секунд для синтеза ДНК. Амплифицированный продукт был проанализирован с помощью 2% электрофореза в агарозном геле, целевой фрагмент был вырезан и очищен с помощью набора для очистки ПЦР (YuHua, Шанхай, Китай) в соответствии с инструкциями производителя. Концентрация ДНК была измерена с помощью Qubit 4.0 (Thermo Fisher Scientific, США). Платформа высокопроизводительного секвенирования Illumina MiSeq компании Majorbio Bio-Pharm Technology Co. Ltd. (Шанхай, Китай) была использована для секвенирования амплифицированных продуктов и завершения создания библиотеки.
2.4. Статистический анализ
Биоинформационный анализ почвы был выполнен с использованием облачной платформы Majorbio (https://cloud.majorbio.com, доступ 20 сентября 2024 года). Статистический анализ был проведен с использованием программного обеспечения SPSS (SPSS Inc., Чикаго, Иллинойс, США), и однофакторный дисперсионный анализ был использован для расчета значительных различий в физико-химических свойствах почвы и индексах альфа-разнообразия при различных условиях удобрения (тест LSD, p < 0.05 для значительных различий, p < 0.01 для высокозначительных различий). Анализ главных компонент (PCA) и избыточности (RDA) были проведены с использованием Canoco 5.0. PCA был использован для определения бета-разнообразия грибных сообществ, тогда как RDA был использован для определения взаимосвязей между свойствами почвы и структурой грибного сообщества. Для идентификации значительно обогащенных почвенных грибных сообществ при различных обработках удобрениями использовался метод анализа линейного дискриминантного анализа размера эффекта (LEfSe) [29]. Прогнозирование FunGuild [30] было использовано для анализа функциональной классификации и обилия грибов при различных обработках удобрениями.
3. Результаты
3.1. Изменения физико-химических свойств почвы после внесения фосфорного удобрения
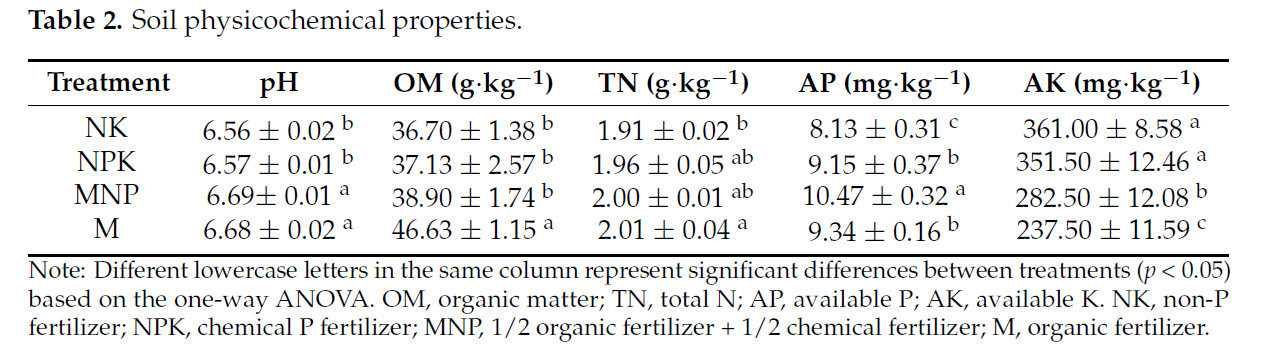
По сравнению с обработкой NK, обработки M и MNP значительно увеличили pH почвы на 1,83% и 1,98% соответственно (Таблица 2). Наиболее высокое содержание OM наблюдалось при обработке M — 46,63 г·кг⁻¹, что было значительно выше, чем при обработке NK на 27,06%, обработке NPK на 25,59% и обработке MNP на 19,87%. Содержание TN в почве при обработке M составило 2,01 г·кг⁻¹, что было значительно выше, чем при обработке NK, на 5,24%. Содержание AP в каждой обработке было следующим: MNP > M > NPK > NK. Значительной разницы между обработками M и NPK не наблюдалось. По сравнению с обработкой NK, содержание AK при обработках MNP и M было значительно ниже (на 21,75% и 34,21% соответственно).
Таблица 2. Физико-химические свойства почвы.
3.2. Влияние фосфорного удобрения на индексы α-разнообразия почвенных грибов
На основе результатов секвенирования мы проанализировали индекс Chao1, индекс Шеннона, индекс Симпсона и индекс Пьелу почвенных грибов. По сравнению с обработкой NK, индекс Шеннона и индекс Пьелу почвенных грибов значительно увеличились после кратковременного внесения P-удобрения, увеличившись на 34,48%~59,00% и 29,79%~53,19% соответственно. Индекс Chao1 значительно увеличился на 18,82% и 19,19% в обработках MNP и M соответственно по сравнению с обработкой NK. Индекс Симпсона почвенных грибов был самым низким при обработке NPK, что было значительно ниже, чем при обработке NK, на 78,95%, и значительной разницы по сравнению с обработками MNP и M не наблюдалось (Таблица 3).
Таблица 3. Индекс α-разнообразия почвенных грибов.
3.3. Влияние фосфорного удобрения на состав сообщества почвенных грибов
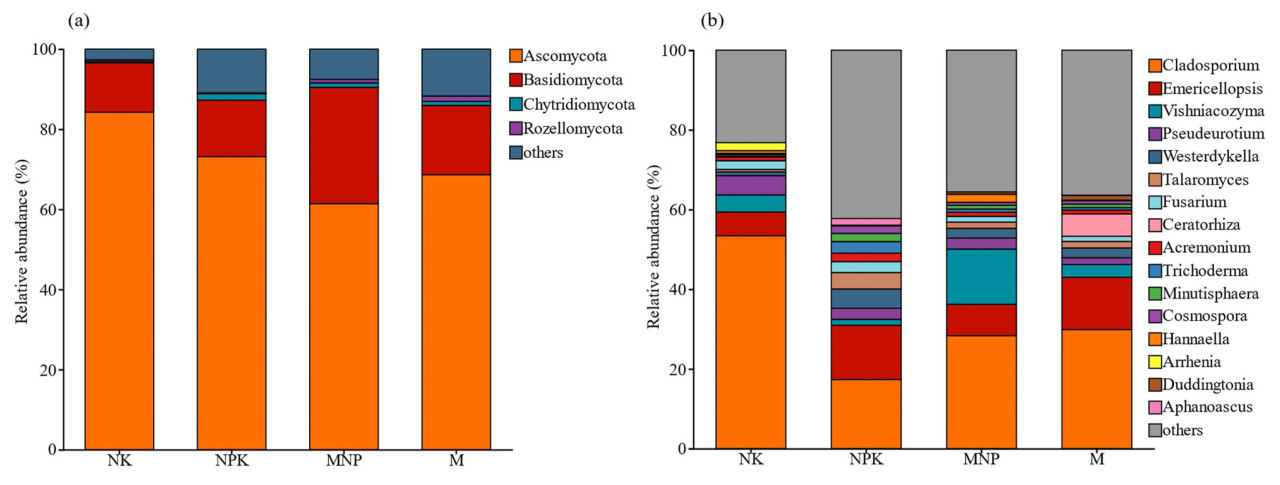
Мы сравнили состав сообщества почвенных грибов на уровнях типа и рода после добавления различных P-удобрений. В этом исследовании было 4 типа грибов и 16 родов грибов с относительным обилием > 1%. Ascomycota был наиболее обильным типом грибов, составляя от 61,43% до 84,26% всего грибного сообщества (Рисунок 1а). По сравнению с обработкой NK, относительное обилие Ascomycota снизилось на 13,16%, 27,09% и 18,53% в обработках NPK, MNP и M соответственно. Относительное обилие Basidiomycota, Chytridiomycota и Rozellomycota составляло 12,29%~29,01%, 0,39%~1,63% и 0,20%~1,33% соответственно. По сравнению с обработкой NK, относительное обилие трех типов почвенных грибов увеличилось в обработках MNP и M. Среди 16 наиболее обильных родов, Cladosporium и Emericellopsis имели наиболее высокое относительное обилие, варьирующееся от 17,34% до 53,42% и от 5,94% до 13,62% соответственно (Рисунок 1b). Относительное обилие Vishniacozyma было наиболее высоким — 13,86% в обработке MNP и наиболее низким — 1,48% в обработке NPK. Относительное обилие Arrhenia при обработке NK составило 1,98%, тогда как относительное обилие Ceratorhiza при обработке M составило 5,62%. По сравнению с обработкой NK, относительное обилие Fusarium при обработках органическими удобрениями (MNP и M) снизилось на 34,54% и 41,36% соответственно.
Рисунок 1. Относительное обилие почвенных грибов на уровне типа (a) и рода (b). NK — без P-удобрения; NPK — химическое P-удобрение; MNP — 1/2 органического удобрения + 1/2 химического удобрения; M — органическое удобрение.
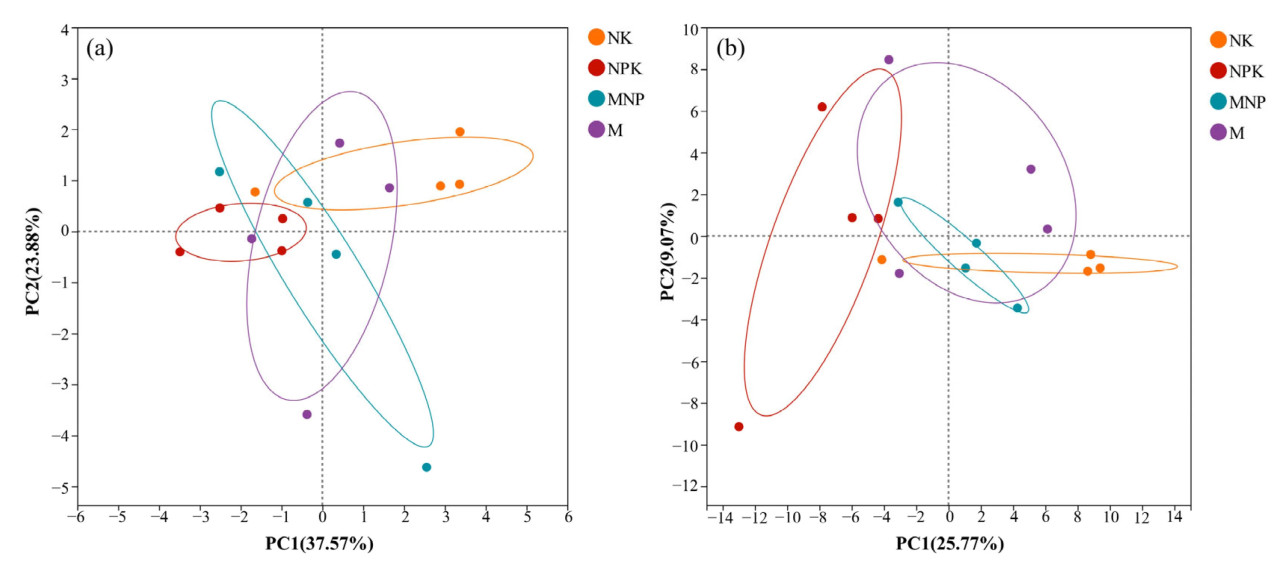
PCA показал, что первые две главные компоненты объясняли 37,57% и 23,88% вариации грибных сообществ на уровне типа (Рисунок 2а) и 25,77% и 9,07% вариации на уровне рода (Рисунок 2b) соответственно. Грибные сообщества значительно различались на уровне типа между обработками NK и NPK. Грибные сообщества значительно различались на уровне рода между обработками NPK, NK и MNP.
Рисунок 2. Анализ главных компонент (PCA) почвенных грибов на уровне типа (a) и рода (b). NK — без P-удобрения; NPK — химическое P-удобрение; MNP — 1/2 органического удобрения + 1/2 химического удобрения; M — органическое удобрение.
3.4. Реакция специфических грибных групп на различные фосфорные удобрения
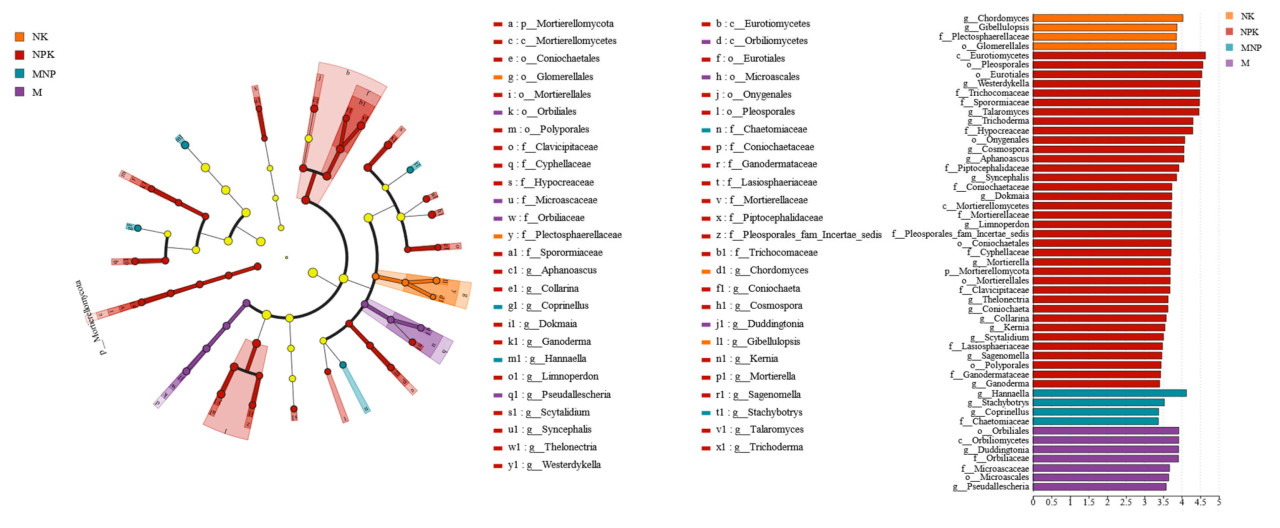
Почвенные грибные сообщества были проанализированы с помощью LEfSe от уровня типа до уровня рода, чтобы определить таксоны грибов, значительно обогащенные в почве после добавления различных P-удобрений. Результаты показали, что в различных обработках удобрениями было 51 значительно обогащенная грибная группа, причем наибольшее количество значительно обогащенных грибных групп (36) было в обработке NPK, а наименьшее количество значительно обогащенных грибных групп (4) — в обработках NK и MNP (Рисунок 3). Только почвенные грибы при обработке NPK, а именно Mortierellomycota, были значительно обогащены на уровне типа. Glomerellales были значительно обогащены на уровне порядка, Plectosphaerelaceae были значительно обогащены на уровне семейства, а Chordomyces и Gibellulosis были значительно обогащены на уровне рода в обработке NK. Chaetomiaceae были значительно обогащены на уровне семейства в обработке MNP, тогда как Hannella, Stachybotrys и Coprinellus были значительно обогащены на уровне рода. В обработке M Orbiliomycetes, Orbiliales, Orbiliaceae, Microasciale, Microascaceae, Seudomonas и Duddingtonia были значительно обогащены.
Рисунок 3. LEfSe-анализ почвенных грибных сообществ. Показаны только таксоны, соответствующие порогу значимости LDA 2 для грибных сообществ. Пять колец кладограммы представляют типы (самое внутреннее), классы, порядки, семейства и роды (самое внешнее). NK — без P-удобрения; NPK — химическое P-удобрение; MNP — 1/2 органического удобрения + 1/2 химического удобрения; M — органическое удобрение.
3.5. Функциональное прогнозирование сообщества почвенных грибов
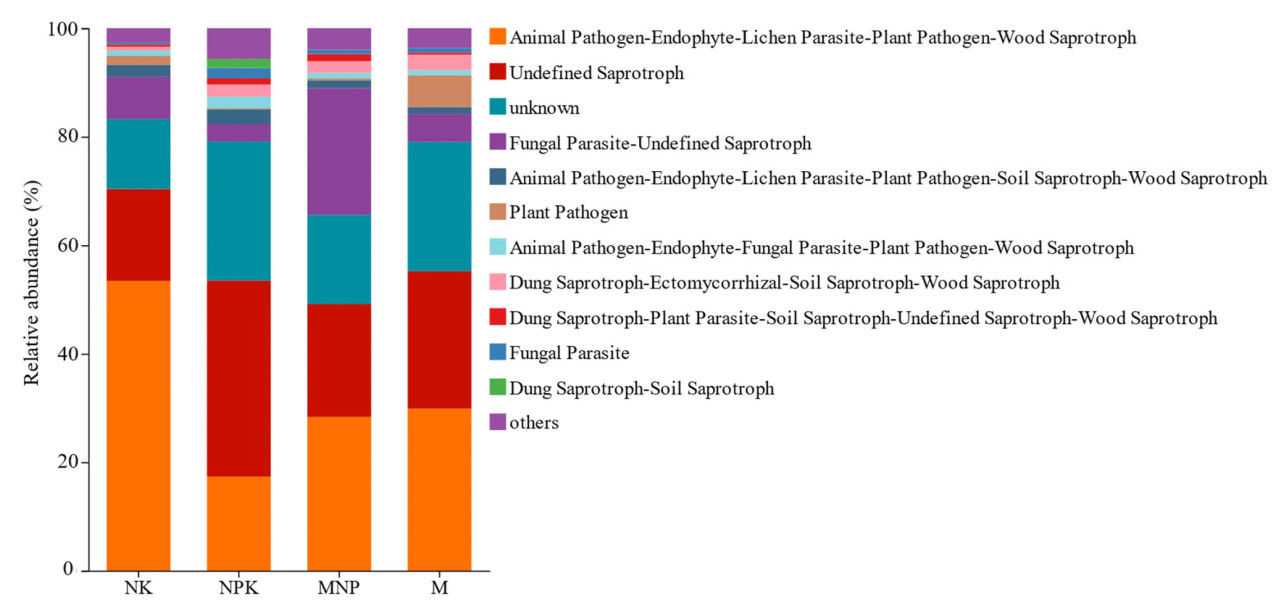
Мы использовали инструмент классификации грибов FunGuild для отнесения грибных OTU к специфическим питательным группам при различных обработках, а затем дополнительно подразделили их на специфические функциональные группы. Анализ показал 11 функциональных групп грибов с относительным обилием > 1%, среди которых функциональной группой с наиболее высоким относительным обилием была «Патоген животных – Эндофит – Паразит лишайников – Патоген растений – Древесный сапротроф». По сравнению с обработкой NK, относительное обилие «Патоген животных – Эндофит – Паразит лишайников – Патоген растений – Древесный сапротроф» снизилось на 67,54%, 46,93% и 44,10% соответственно в обработках NPK, MNP и M (Рисунок 4). Относительное обилие «Неопределенный сапротроф» в обработках NK, NPK, MNP и M составило 16,92%, 36,18%, 20,82% и 25,35% соответственно. Относительное обилие «Паразит грибов – Неопределенный сапротроф» было наиболее высоким — 23,35% в обработке MNP и наиболее низким — 3,22% в обработке NPK. Относительное обилие «Патоген растений» составило 5,84% в обработке M, 1,65% в обработке NK и <1% в обработках NPK и MNP. По сравнению с обработкой NK, относительное обилие «Сапротроф навоза – Эктомикоризный – Почвенный сапротроф – Древесный сапротроф» увеличилось на 194,67%, 188,00% и 284,00% в обработках NPK, MNP и M соответственно.
Рисунок 4. Прогнозирование функций FUNGuild почвенных грибных сообществ. NK — без P-удобрения; NPK — химическое P-удобрение; MNP — 1/2 органического удобрения + 1/2 химического удобрения; M — органическое удобрение.
3.6. Взаимосвязи между составом сообщества почвенных грибов и физико-химическими свойствами почвы
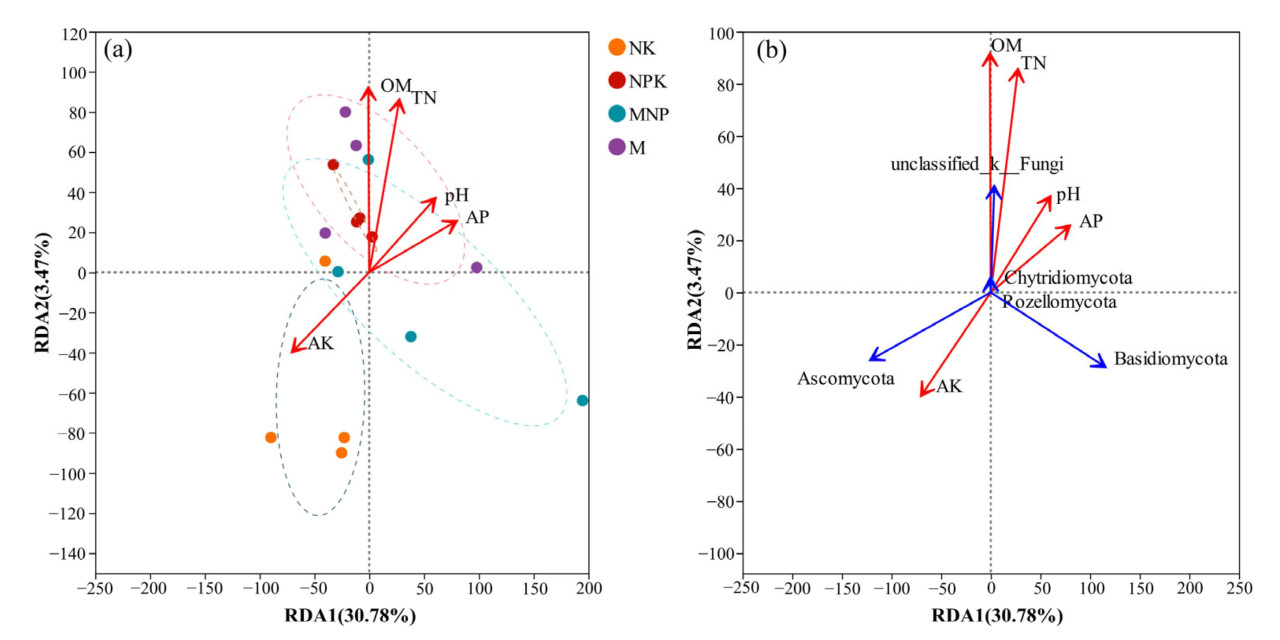
Анализ избыточности (RDA) был использован для исследования взаимосвязей между почвенными грибными сообществами и физико-химическими свойствами почвы на уровне типа. Результаты показали, что объясняющая способность первой и второй осей в анализе избыточности на уровне типа составила 30,78% и 3,47% соответственно, что указывает на то, что физико-химические свойства почвы вносят вклад в различия почвенных грибных сообществ. Органическое вещество почвы (OM, R² = 0,4346, p = 0,02) и общий азот (TN, R² = 0,4357, p = 0,031) были основными факторами, влияющими на состав грибного сообщества (Рисунок 5а). Относительные обилия Ascomycota и Basidiomycota были тесно связаны с углом между OM и TN, что указывает на значительную отрицательную корреляцию (Рисунок 5b).
Рисунок 5. Анализ избыточности физико-химических свойств почвы во взаимосвязи с различными группами образцов (a) и типами грибов (b). OM — органическое вещество; TN — общий N; AP — доступный P; AK — доступный K. NK — без P-удобрения; NPK — химическое P-удобрение; MNP — 1/2 органического удобрения + 1/2 химического удобрения; M — органическое удобрение.
4. Обсуждение
4.1. Внесение фосфорного удобрения может увеличить разнообразие почвенных грибов
Микробное разнообразие часто рассматривается как один из факторов, необходимых для устойчивого функционирования почвенных систем, и тесно связано с функцией, стабильностью и устойчивостью почвенной экосистемы [31,32]. Наши результаты показали, что по сравнению с обработкой NK, индекс Шеннона и индекс Пьелу почвенных грибов значительно увеличились после кратковременного внесения P-удобрения. Индекс Chao1 значительно увеличился в ответ на внесение органического удобрения (MNP и M) (Таблица 3). Эти результаты подчеркивают, что кратковременное внесение P-удобрений не только смягчает фосфорное ограничение, но и может улучшить разнообразие и богатство грибного сообщества за счет улучшения почвенной среды. Богатство почвенных грибов сильнее реагирует на органические удобрения, чем на химические. В почвах с дефицитом P внесение органических удобрений может эффективно увеличить богатство грибов, поскольку они обеспечивают дополнительный углерод и питательные вещества, улучшая почвенную микросреду [33,34]. Исследования показывают, что активность почвенных грибов тесно связана с доступностью углерода. В длительно испытывающих дефицит P почвах органическое удобрение активирует больше микробных популяций, которые используют углерод и питательные вещества из органических удобрений, значительно увеличивая богатство грибного сообщества [35,36,37].
4.2. Внесение химического фосфорного удобрения значительно улучшило структуру грибного сообщества
Доминирующие типы почвенных грибов при различных обработках включали в основном Ascomycota и Basidiomycota (Рисунок 1а). Относительное обилие Ascomycota было ниже после внесения P-удобрения, чем в обработке без P-удобрения, что указывает на то, что Ascomycota более чувствителен к реакции на дефицит P в почве. Этот результат согласуется с длительным исследованием Wang [3]. Напротив снижения обилия Ascomycota, Basidiomycota показал увеличение относительного обилия после внесения P-удобрения. Предыдущие исследования показали, что ограничение питательных веществ создает конкурентные отношения между Ascomycota и Basidiomycota, что приводит к отрицательной корреляции их относительных обилий [38].
Анализ главных компонент (PCA) показал значительное разделение грибных сообществ на уровне типа и рода между обработками NK и NPK (Рисунок 2), что указывает на то, что внесение химического P-удобрения играет значительную роль в изменении структуры грибного сообщества в желтой рисовой почве. Это может быть связано с тем, что структура грибных сообществ в длительно испытывающих дефицит P почвах является простой и нестабильной. Внесение химического P-удобрения нарушает исходный экологический баланс, вводя новые потоки вещества и энергии [39]. Различные таксоны грибов по-разному реагируют на фосфор; некоторые чувствительные к фосфору таксоны, которые эффективно используют фосфор, быстро размножаются, в то время как другие подавляются, что приводит к значительным изменениям грибных сообществ на уровне типа и рода [40].
LEfSe-анализ далее показал, что грибы, обогащенные в обработке NPK, были в основном полезными видами (Рисунок 3), такими как Trichoderma — важный биоконтрольный гриб, который подавляет почвенные патогены путем секреции антибиотиков или конкурентного исключения [41]. Кроме того, Mortierella, фосфатмобилизующий гриб, может преобразовывать нерастворимые соединения фосфора в растворимый фосфор, доступный для растений, улучшая обеспеченность почвы фосфором, а также может иметь потенциал для биоконтроля патогенов растений [42]. Orbiliomycetes, которые были обогащены в обработке M, играют значительную роль в здоровье почвы, поскольку исследования предполагают, что Orbiliomycetes вносят вклад в разложение органического вещества и влияют на здоровье почвы и рост растений [43]. Однако грибы, такие как Stachybotrys в группе обработки MNP и Pseudallescheria в группе обработки M, могут быть связаны с болезнями растений. Stachybotrys может подавлять развитие корней, производя микотоксины, повышая восприимчивость растений к другим патогенам за счет влияния на их устойчивость к стрессу [44]. Pseudallescheria может повреждать клеточные структуры растений, секретируя специфические ферменты и токсины, и может быстро распространяться в заболоченных рисовых почвах [45,46].
Сапротрофные грибы являются основными分解ителями в почве, ключевыми для разложения органического вещества [47]. Патогенные грибы получают питательные вещества, разрушая клетки хозяина, что оказывает негативное влияние на рост растений [48,49]. В этом исследовании кратковременное внесение P-удобрения снизило относительное обилие «Патоген животных – Эндофит – Паразит лишайников – Патоген растений – Древесный сапротроф», в то время как увеличило относительное обилие «Сапротроф навоза – Эктомикоризный – Почвенный сапротроф – Древесный сапротроф» (Рисунок 4). Эти результаты подчеркивают, что смягчение P-ограничения в рисовой почве может подавлять рост патогенных грибов в почве, способствовать росту сапротрофных грибов и улучшать структуру грибного сообщества. Эти результаты согласуются с результатами 9-летнего эксперимента по внесению P, проведенного Li [50]. Дальнейшее сравнение между различными обработками P-удобрениями показало, что относительное обилие патогенных грибов было самым низким в обработке NPK, в то время как относительное обилие «Паразит грибов – Неопределенный сапротроф» было самым высоким в обработке MNP, а относительное обилие «Патоген растений» было самым высоким в обработке M. Это может быть связано с значительным обогащением антагонистического патогенам гриба Mortierella в обработке NPK, который может обеспечивать источники P для полезных микроорганизмов, одновременно подавляя рост патогенных грибов [51,52]. С другой стороны, как микоризные, так и патогенные грибы нуждаются в питательных веществах для роста. Увеличение поступления питательных веществ из органических удобрений может способствовать росту патогенных грибов, и увеличение количества патогенных грибов также может быть связано с внесением экзогенных органических удобрений [22,53].
4.3. Содержание общего азота и органического вещества в почве являются ключевыми факторами, влияющими на состав грибных сообществ
Анализ избыточности (RDA) на основе состава грибного сообщества и физико-химических свойств почвы показал, что внесение P-удобрений значительно изменило содержание TN и OM, косвенно перестраивая структуру грибного сообщества. Liu [34] также сделал аналогичные выводы, дополнительно подчеркивая сложные взаимодействия между доступностью питательных веществ и динамикой грибного сообщества. Углубленный анализ показал, что Ascomycota и Basidiomycota были значительно отрицательно коррелированы с содержанием TN и OM (p < 0.05), что, вероятно, обусловлено несколькими механизмами. С одной стороны, избыток азота может изменить конкурентную динамику почвенных микробных сообществ [54]. В условиях богатого азотом Ascomycota и Basidiomycota могут оказаться в конкурентном невыгодном положении, что приводит к снижению их обилия. С другой стороны, высокий уровень азота может благоприятствовать грибным группам, которые могут эффективно использовать источники азота, подавляя рост Ascomycota и Basidiomycota, которые полагаются на другие питательные вещества, таким образом изменяя общую структуру грибного сообщества [55]. Содержание OM, как важный фактор, влияющий на грибные сообщества, также оказывает сложное влияние. Более высокое содержание OM обеспечивает обильные источники углерода для почвенных микроорганизмов, что в целом поддерживает более разнообразное грибное сообщество [56]. Однако избыточное OM может нарушить круговорот питательных веществ, влияя на состав таких грибных сообществ, как Ascomycota и Basidiomycota [57].
Ye [38] сообщил, что удобрение изменяет структуру грибного сообщества за счет изменения pH почвы. Однако наше исследование показало лишь незначительные вариации pH (0,01–0,13) в различных обработках, и на состав грибного сообщества pH влиял слабо, возможно, из-за более широкого оптимального диапазона pH для роста грибов [58]. Кратковременное внесение P-удобрений смягчило P-ограничение, но корреляция между содержанием AP и составом грибного сообщества не была значительной. Это может происходить потому, что рост определенных грибных сообществ более зависит от содержания других питательных веществ, таких как азот и углерод [10]. Кроме того, грибные сообщества могут использовать труднодоступные источники P в почве через различные механизмы (такие как секреция внеклеточных ферментов), которые напрямую не связаны с содержанием AP в почве [59]. Таким образом, влияние внесения P-удобрений на грибные сообщества включает не только прямые изменения содержания питательных веществ, но также может изменять структуру и функцию почвенного микробного сообщества через сложные экологические механизмы.
Кратковременное внесение P-удобрений не только улучшило структуру почвенного грибного сообщества, но и способствовало здоровью почвы за счет активации полезных микробов и подавления патогенов. Это открытие предоставляет ценные идеи для стратегий управления почвой, особенно в почвах с дефицитом P, где соответствующее внесение P может повысить плодородие почвы и поддержать стабильность и восстановление экосистемы. Будущие исследования должны изучить длительные последствия различных стратегий удобрения для микробных сообществ и то, как оптимизировать роль полезных микробов для разработки более устойчивых методов управления почвой.
5. Выводы
Кратковременное внесение P-удобрения значительно увеличивает индекс Шеннона и индекс Пьелу почвенных грибных сообществ, причем органическое удобрение дополнительно увеличивает индекс Chao1 грибов. Ascomycota и Basidiomycota были доминирующими типами грибов в желтой рисовой почве. При внесении химического P-удобрения Mortierellomycota были значительно обогащены, тогда как относительное обилие патогенных грибов значительно снизилось. Кроме того, результаты RDA показали, что почвенные TN и OM являются важными факторами для прогнозирования изменений в составе сообщества почвенных грибов. Эти результаты подчеркивают, что кратковременное внесение химического P-удобрения в почву с дефицитом P является более эффективным, чем внесение органического удобрения, для регуляции как полезных, так и патогенных грибов, предоставляя новые идеи для управления почвой в целях устойчивого производства сельскохозяйственных культур.
Ссылки
1. Veneklaas, E.J.; Lambers, H.; Bragg, J.; Finnegan, P.M.; Lovelock, C.E.; Plaxton, W.C.; Price, C.A.; Scheible, W.; Shane, M.W.; White, P.J.; et al. Opportunities for improving phosphorus-use efficiency in crop plants. New Phytol. 2012, 195, 306–320. [Google Scholar] [CrossRef] [PubMed]
2. Takahashi, Y.; Katoh, M. Root Response and Phosphorus Acquisition under Partial Distribution of Phosphorus and Water-soluble Organic Matter. Soil Use Manag. 2024, 40, e13038. [Google Scholar] [CrossRef]
3. Langhans, C.; Beusen, A.H.W.; Mogollón, J.M.; Bouwman, A.F. Phosphorus for sustainable development goal target of doubling smallholder productivity. Nat. Sustain. 2021, 5, 57–63. [Google Scholar] [CrossRef]
4. Vitousek, P.M.; Porder, S.; Houlton, B.Z.; Chadwick, O.A. Terrestrial phosphorus limitation: Mechanisms, implications, and nitrogen–phosphorus interactions. Ecol. Appl. 2010, 20, 5–15. [Google Scholar] [CrossRef]
5. Wang, J.; Yuan, J.; Wang, L.; Zhang, H.; Tang, Z.H.; Zhao, P.; Zhang, A.J.; Wang, J.D.; Zhang, Y.C. Effects of fertilizer application methods on fungal communities in sweet potato rhizosphere. J. Plant Nutr. Fertil. 2023, 29, 876–888. [Google Scholar]
6. Zhong, J.P.; Zheng, Z.C.; Li, T.X.; He, X.L. Effect of phosphorus fertilizer application rates on the loss of colloidal phosphorus on purple soil slopes. Sci. Agric. Sin. 2024, 57, 1547–1559. [Google Scholar]
7. Zou, T.; Zhang, X.; Davidson, E.A. Global trends of cropland phosphorus use and sustainability challenges. Nature 2022, 611, 81–87. [Google Scholar] [CrossRef]
8. Ducousso-Détrez, A.; Fontaine, J.; Lounès-Hadj Sahraoui, A.; Hijri, M. Diversity of phosphate chemical forms in soils and their contributions on soil microbial community structure changes. Microorganisms 2022, 10, 609. [Google Scholar] [CrossRef]
9. Li, J.; Delgado-Baquerizo, M.; Wang, J.-T.; Hu, H.-W.; Cai, Z.-J.; Zhu, Y.-N.; Singh, B.K. Fungal richness contributes to multifunctionality in boreal forest soil. Soil Biol. Biochem. 2019, 136, 107526. [Google Scholar] [CrossRef]
10. Tedersoo, L.; Bahram, M.; Põlme, S.; Kõljalg, U.; Yorou, N.S.; Wijesundera, R.; Ruiz, L.V.; Vasco-Palacios, A.M.; Thu, P.Q.; Suija, A.; et al. Global diversity and geography of soil fungi. Science 2014, 346, 1256688. [Google Scholar] [CrossRef]
11. Delgado-Baquerizo, M.; Maestre, F.T.; Reich, P.B.; Jeffries, T.C.; Gaitan, J.J.; Encinar, D.; Berdugo, M.; Campbell, C.D.; Singh, B.K. Microbial diversity drives multifunctionality in terrestrial ecosystems. Nat. Commun. 2016, 7, 10541. [Google Scholar] [CrossRef] [PubMed]
12. Nicolás, C.; Martin-Bertelsen, T.; Floudas, D.; Bentzer, J.; Smits, M.; Johansson, T.; Troein, C.; Persson, P.; Tunlid, A. The soil organic matter decomposition mechanisms in ectomycorrhizal fungi are tuned for liberating soil organic nitrogen. ISME J. 2019, 13, 977–988. [Google Scholar] [CrossRef] [PubMed]
13. Wang, J.L.; Liu, K.L.; Zhao, X.Q.; Zhang, H.Q.; Li, D.; Li, J.J.; Shen, R.F. Balanced fertilization over four decades has sustained soil microbial communities and improved soil fertility and rice productivity in red paddy soil. Sci. Total Environ. 2021, 793, 148664. [Google Scholar] [CrossRef] [PubMed]
14. Yang, Y.; Huang, X.; Li, Y.; Liu, Y.; Zhang, Y.; Zhu, H.; Xiong, H.; Zhang, S.; Jiang, T. Characteristics of the soil microbial community structure under long-term chemical fertilizer application in yellow soil paddy fields. Agronomy 2024, 14, 1186. [Google Scholar] [CrossRef]
15. Semenov, M.V.; Krasnov, G.S.; Semenov, V.M.; Van Bruggen, A. Mineral and organic fertilizers distinctly affect fungal communities in the crop rhizosphere. J. Fungi 2022, 8, 251. [Google Scholar] [CrossRef]
16. Pan, H.; Chen, M.; Feng, H.; Wei, M.; Song, F.; Lou, Y.; Cui, X.; Wang, H.; Zhuge, Y. Organic and inorganic fertilizers respectively drive bacterial and fungal community compositions in a fluvo-aquic soil in northern China. Soil Tillage Res. 2020, 198, 104540. [Google Scholar] [CrossRef]
17. Wang, Y.; Xu, Y.; Jiang, L.; Yang, Y.; Shi, J.; Guan, X.; Sun, T.; Zhao, H.; Wang, Y.; Liu, Y. Effect of Mild Organic Substitution on Soil Quality and Microbial Community. Agronomy 2024, 14, 888. [Google Scholar] [CrossRef]
18. Du, J.; Yu, Y.; Tang, C.; Zong, K.; Zhang, S.; Zhang, Q.; Fang, L.; Li, Y. Organic Fertilizers increase the proportion of saprotrophs favoring soil nitrification under medicinal plants Fritillaria thunbergii. Ind. Crops Prod. 2024, 219, 119129. [Google Scholar] [CrossRef]
19. Yang, Y.H.; Huang, X.C.; Zhu, H.Q.; LI, Y.; Zhang, S.; Zhang, Y.R.; Liu, Y.L.; Jiang, T.M. Bacterial community structure and composition under long-term combined application of organic and inorganic fertilizers in a yellow paddy soil. J. Plant Nutr. Fert. 2022, 28, 984–992. [Google Scholar]
20. Bo, H.; Li, Z.; Jin, D.; Xu, M.; Zhang, Q. Fertilizer Management Methods Affect Bacterial Community Structure and Diversity in the Maize Rhizosphere Soil of a Coal Mine Reclamation Area. Ann. Microbiol. 2023, 73, 24. [Google Scholar] [CrossRef]
21. Zhang, L.F.; Ma, L.; Li, Y.D.; Zheng, F.L.; Wei, J.L.; Tan, D.S.; Cui, X.M.; Li, Y. Effects of long-term synergistic application of organic materials and chemical fertilizers on bacterial community and enzyme activity in wheat-maize rotation fluvo-aquic soil. Scient. Agric. Sin. 2023, 56, 3843–3855. [Google Scholar]
22. Schlatter, D.C.; Gamble, J.D.; Castle, S.; Rogers, J.; Wilson, M. Abiotic and biotic drivers of soil fungal communities in response to dairy manure amendment. Appl. Environ. Microbiol. 2023, 89, e01931-22. [Google Scholar] [CrossRef] [PubMed]
23. Hu, X.; Liu, J.; Wei, D.; Zhu, P.; Cui, X.; Zhou, B.; Chen, X.; Jin, J.; Liu, X.; Wang, G. Effects of over 30-year of different fertilization regimes on fungal community compositions in the black soils of northeast China. Agric. Ecosyst. Environ. 2017, 248, 113–122. [Google Scholar] [CrossRef]
24. Paungfoo-Lonhienne, C.; Yeoh, Y.K.; Kasinadhuni, N.R.P.; Lonhienne, T.G.A.; Robinson, N.; Hugenholtz, P.; Ragan, M.A.; Schmidt, S. Nitrogen fertilizer dose alters fungal communities in sugarcane soil and rhizosphere. Sci. Rep. 2015, 5, 8678. [Google Scholar] [CrossRef]
25. Huang, R.; McGrath, S.P.; Hirsch, P.R.; Clark, I.M.; Storkey, J.; Wu, L.; Zhou, J.; Liang, Y. Plant-microbe networks in soil are weakened by century-long use of inorganic fertilizers. Microb. Biotechnol. 2019, 12, 1464–1475. [Google Scholar] [CrossRef]
26. He, D.; Xiang, X.; He, J.-S.; Wang, C.; Cao, G.; Adams, J.; Chu, H. Composition of the soil fungal community is more sensitive to phosphorus than nitrogen addition in the alpine meadow on the Qinghai-Tibetan Plateau. Biol. Fertil. Soils 2016, 52, 1059–1072. [Google Scholar] [CrossRef]
27. Jirout, J.; Šimek, M.; Elhottová, D. Inputs of nitrogen and organic matter govern the composition of fungal communities in soil disturbed by overwintering cattle. Soil Biol. Biochem. 2011, 43, 647–656. [Google Scholar] [CrossRef]
28. Lu, R.K. Methods of Soil Agricultural Chemistry Analysis; China Agriculture Press: Beijing, China, 1999; pp. 296–338. [Google Scholar]
29. Segata, N.; Izard, J.; Waldron, L.; Gevers, D.; Miropolsky, L.; Garrett, W.S.; Huttenhower, C. Metagenomic biomarker discovery and explanation. Genome Biol. 2011, 12, R60. [Google Scholar] [CrossRef]
30. Nguyen, N.H.; Song, Z.; Bates, S.T.; Branco, S.; Tedersoo, L.; Menke, J.; Schilling, J.S.; Kennedy, P.G. FUNGuild: An open annotation tool for parsing fungal community datasets by ecological guild. Fungal Ecol. 2016, 20, 241–248. [Google Scholar] [CrossRef]
31. Banerjee, S.; Van Der Heijden, M.G.A. Soil microbiomes and one health. Nat. Rev. Microbiol. 2023, 21, 6–20. [Google Scholar] [CrossRef]
32. Saleem, M.; Hu, J.; Jousset, A. More than the sum of its parts: Microbiome biodiversity as a driver of plant growth and soil health. Annu. Rev. Ecol. Evol. Syst. 2019, 50, 145–168. [Google Scholar] [CrossRef]
33. Zhou, W.J.; Chen, J.G.; Tan, Z.J.; Zhang, Y.Z.; Ceng, X.B. Response of paddy soil health to continuous amendments of organic fertilizer and lime separately under double-cropping rice fields. Scient. Agric. Sin. 2010, 29, 29–35. [Google Scholar]
34. Liu, H.; Xu, W.; Li, J.; Yu, Z.; Zeng, Q.; Tan, W.; Mi, W. Short-term effect of manure and straw application on bacterial and fungal community compositions and abundances in an acidic paddy soil. J. Soils Sediments 2021, 21, 3057–3071. [Google Scholar] [CrossRef]
35. Blagodatskaya, E.; Kuzyakov, Y. Active microorganisms in soil: Critical review of estimation criteria and approaches. Soil Biol. Biochem. 2013, 67, 192–211. [Google Scholar] [CrossRef]
36. He, M.; Tian, G.; Semenov, A.M.; Van Bruggen, A.H.C. Short-term fluctuations of sugar beet damping-off by pythium ultimum in relation to changes in bacterial communities after organic amendments to two soils. Phytopathology 2012, 102, 413–420. [Google Scholar] [CrossRef] [PubMed][Green Version]
37. Semenov, M.V.; Krasnov, G.S.; Semenov, V.M.; Ksenofontova, N.; Zinyakova, N.B.; Van Bruggen, A.H.C. Does fresh farmyard manure introduce surviving microbes into soil or activate soil-borne microbiota? J. Environ. Manage. 2021, 294, 113018. [Google Scholar] [CrossRef]
38. Ye, G.; Lin, Y.; Luo, J.; Di, H.J.; Lindsey, S.; Liu, D.; Fan, J.; Ding, W. Responses of soil fungal diversity and community composition to long-term fertilization: Field experiment in an acidic Ultisol and literature synthesis. Appl. Soil Ecol. 2020, 145, 103305. [Google Scholar] [CrossRef]
39. Ma, L.; Zhang, J.; Li, Z.; Xin, X.; Guo, Z.; Wang, D.; Li, D.; Zhao, B. Long-term phosphorus deficiency decreased bacterial-fungal network complexity and efficiency across three soil types in China as revealed by network analysis. Appl. Soil Ecol. 2020, 148, 103506. [Google Scholar] [CrossRef]
40. Ma, S.; Chen, X.; Su, H.; Xing, A.; Chen, G.; Zhu, J.; Zhu, B.; Fang, J. Phosphorus addition decreases soil fungal richness and alters fungal guilds in two tropical forests. Soil Biol. Biochem. 2022, 175, 108836. [Google Scholar] [CrossRef]
41. Yao, X.; Guo, H.; Zhang, K.; Zhao, M.; Ruan, J.; Chen, J. Trichoderma and its role in biological control of plant fungal and nematode disease. Front. Microbiol. 2023, 14, 1160551. [Google Scholar] [CrossRef]
42. Tayyab, M.; Islam, W.; Lee, C.G.; Pang, Z.; Khalil, F.; Lin, S.; Lin, W.; Zhang, H. Short-term effects of different organic amendments on soil fungal composition. Sustainability 2019, 11, 198. [Google Scholar] [CrossRef]
43. Zhang, F.; Yang, Y.-Q.; Zhou, F.-P.; Xiao, W.; Boonmee, S.; Yang, X.-Y. Multilocus Phylogeny and characterization of five undescribed aquatic carnivorous fungi (Orbiliomycetes). J. Fungi 2024, 10, 81. [Google Scholar] [CrossRef] [PubMed]
44. Wang, Y.; Hyde, K.D.; McKenzie, E.H.C.; Jiang, Y.-L.; Li, D.-W.; Zhao, D.-G. Overview of Stachybotrys (Memnoniella) and current species status. Fungal Divers. 2015, 71, 17–83. [Google Scholar] [CrossRef]
45. Pinto, M.R.; Mulloy, B.; Haido, R.M.T.; Travassos, L.R.; Barreto Bergter, E. A Peptidorhamnomannan from the mycelium of Pseudallescheria boydii is a potential diagnostic antigen of this emerging human pathogen. Microbiology 2001, 147, 1499–1506. [Google Scholar] [CrossRef]
46. Rougeron, A.; Schuliar, G.; Leto, J.; Sitterlé, E.; Landry, D.; Bougnoux, M.; Kobi, A.; Bouchara, J.; Giraud, S. Human-impacted areas of f rance are environmental reservoirs of the Pseudallescheria Boydii/Scedosporium apiospermum species complex. Environ. Microbiol. 2015, 17, 1039–1048. [Google Scholar] [CrossRef]
47. Eichlerová, I.; Baldrian, P. Ligninolytic enzyme production and decolorization capacity of synthetic dyes by saprotrophic white rot, brown rot, and litter decomposing basidiomycetes. J. Fungi 2020, 6, 301. [Google Scholar] [CrossRef]
48. Anthony, M.A.; Frey, S.D.; Stinson, K.A. Fungal community homogenization, shift in dominant trophic guild, and appearance of novel taxa with biotic invasion. Ecosphere 2017, 8, e01951. [Google Scholar] [CrossRef]
49. Xie, F.; Ma, A.; Zhou, H.; Liang, Y.; Yin, J.; Ma, K.; Zhuang, X.; Zhuang, G. Revealing fungal communities in alpine wetlands through species diversity, functional diversity and ecological network diversity. Microorganisms 2020, 8, 632. [Google Scholar] [CrossRef]
50. Yang, H.; Cheng, L.; Che, L.; Su, Y.; Li, Y. Nutrients addition decreases soil fungal diversity and alters fungal guilds and co-occurrence networks in a semi-arid grassland in northern China. Sci. Total Environ. 2024, 926, 172100. [Google Scholar] [CrossRef]
51. Xiong, W.; Li, R.; Ren, Y.; Liu, C.; Zhao, Q.; Wu, H.; Jousset, A.; Shen, Q. Distinct roles for soil fungal and bacterial communities associated with the suppression of vanilla Fusarium wilt disease. Soil Biol. Biochem. 2017, 107, 198–207. [Google Scholar] [CrossRef]
52. Zhu, R.; Jin, L.; Sang, Y.; Hu, S.; Wang, B.-T.; Jin, F.-J. Characterization of potassium-solubilizing fungi, Mortierella spp., isolated from a poplar plantation rhizosphere soil. Arch. Microbiol. 2024, 206, 157. [Google Scholar] [CrossRef] [PubMed]
53. Yan, Z.; Yang, S.; Chen, L.; Zou, Y.; Zhao, Y.; Yan, G.; Wang, H.; Wu, Y. Responses of soil fungal community composition and function to wetland degradation in the songnen plain, northeastern China. Front. Plant Sci. 2024, 15, 1441613. [Google Scholar] [CrossRef]
54. Zhang, H.; Chen, W.; Dong, L.; Wang, W. Grassland degradation amplifies the negative effect of nitrogen enrichment on soil microbial community stability. Glob. Change Biol. 2024, 30, e17217. [Google Scholar] [CrossRef]
55. Guo, W.; Wang, C.; Brunner, I.; Zhou, Y.; Tang, Q.; Wang, J.; Li, M.-H. Responses of soil fungi to long-term nitrogen-water interactions depend on fungal guilds in a mixed pinus Koraiensis forest. JGR Biogeosciences 2024, 129, e2023JG007826. [Google Scholar] [CrossRef]
56. Chen, Y.; Xu, T.; Fu, W.; Hu, Y.; Hu, H.; You, L.; Chen, B. Soil organic carbon and total nitrogen predict large-scale distribution of soil fungal communities in temperate and alpine shrub ecosystems. Eur. J. Soil Biol. 2021, 102, 103270. [Google Scholar] [CrossRef]
57. Lekberg, Y.; Arnillas, C.A.; Borer, E.T.; Bullington, L.S.; Fierer, N.; Kennedy, P.G.; Leff, J.W.; Luis, A.D.; Seabloom, E.W.; Henning, J.A. Nitrogen and phosphorus fertilization consistently favor pathogenic over mutualistic fungi in grassland soils. Nat. Commun. 2021, 12, 3484. [Google Scholar] [CrossRef]
58. Rousk, J.; Bååth, E.; Brookes, P.C.; Lauber, C.L.; Lozupone, C.; Caporaso, J.G.; Knight, R.; Fierer, N. Soil bacterial and fungal communities across a ph gradient in an arable soil. ISME J. 2010, 4, 1340–1351. [Google Scholar] [CrossRef]
59. Pang, F.; Li, Q.; Solanki, M.K.; Wang, Z.; Xing, Y.-X.; Dong, D.-F. Soil phosphorus transformation and plant uptake driven by phosphate-solubilizing microorganisms. Front. Microbiol. 2024, 15, 1383813. [Google Scholar] [CrossRef]
Yang H, Yang Y, Zhu H, Xiong H, Zhang Y, Liu Y, Huang X, Li Y, Jiang T. Short-Term Phosphorus Fertilization Alters Soil Fungal Community in Long-Term Phosphorus-Deprived Yellow Soil Paddy Fields. Agriculture. 2025; 15(3):280. https://doi.org/10.3390/agriculture15030280
Перевод статьи «Short-Term Phosphorus Fertilization Alters Soil Fungal Community in Long-Term Phosphorus-Deprived Yellow Soil Paddy Fields» авторов Yang H, Yang Y, Zhu H, Xiong H, Zhang Y, Liu Y, Huang X, Li Y, Jiang T., оригинал доступен по ссылке. Лицензия: CC BY. Изменения: переведено на русский язык
Фото: freepik














































































































Комментарии (0)