Почему нут не растет на щелочных почвах? Ответ кроется в корнях
Щелочной стресс создает значительные ограничения для сельского хозяйства, снижая доступность питательных веществ и ингибируя рост растений. В данном исследовании изучаются физиологические и биохимические реакции проростков нута (Cicer arietinum L.) на щелочной стресс, что имеет значение для повышения устойчивости культуры.
Аннотация
Проростки нута подвергались воздействию комбинации Na₂CO₃ и NaHCO₃, после чего оценивались изменения в росте, морфологии корней и усвоении питательных веществ. Щелочной стресс привел к значительному снижению ростовых показателей (длины побегов и корней, сырой и сухой массы), корне-побегового отношения и числа боковых корней, что указывает на выраженное повреждение корней. Это повреждение было связано с повышением уровня перекиси водорода (H₂O₂), усилением повреждения мембран и снижением жизнеспособности клеток. В ответ на щелочной стресс в корнях нута накапливались осмолиты (пролин, растворимые сахара) и повышалась активность антиоксидантных ферментов (каталазы, аскорбатпероксидазы) как адаптивная реакция для смягчения осмотического и окислительного стресса. Ионный гомеостаз был нарушен: снизилось поступление таких эссенциальных питательных элементов, как K, P, Mn, Fe и Zn, тогда как поглощение Na, Mg и Ca увеличилось, что привело к дисбалансу питательных веществ. Эти данные подчеркивают необходимость разработки стратегий, например, генетического улучшения, для повышения устойчивости нута к щелочному стрессу, что будет способствовать улучшению продуктивности культуры в сложных почвенных условиях.
Введение
К 2050 году ожидается, что численность мирового населения достигнет приблизительно 9,1 миллиарда, что потребует значительного увеличения производства продуктов питания. Согласно оценкам, производство продуктов питания должно вырасти на 70% по сравнению с уровнем 2009 года, чтобы адекватно удовлетворить потребности этого растущего населения (FAO, 2009). Повышение температуры, изменение характера выпадения осадков и экстремальные погодные явления, вызванные изменением климата, могут негативно влиять на урожайность сельскохозяйственных культур и производство продуктов питания (Rosenzweig et al., 2001). В дополнение к этим климатическим проблемам, абиотический стресс в виде засоления и защелачивания дополнительно ограничивает рост и продуктивность растений во всем мире (Fang et al., 2021). Солевой стресс возникает главным образом из-за присутствия нейтральных солей, таких как хлорид натрия (NaCl) и сульфат натрия (Na₂SO₄), тогда как щелочной стресс проистекает из присутствия щелочных солей, включая бикарбонат натрия (NaHCO₃) и карбонат натрия (Na₂CO₃) (Liu et al., 2022). Хотя обе формы стресса нарушают рост растений посредством различных механизмов, было показано, что защелачивание оказывает более пагубное воздействие на рост растений по сравнению с засолением (Paz et al., 2012; Gong et al., 2014; Fang et al., 2021; Liu et al., 2022).
Защелачивание служит ключевым ограничением для сельскохозяйственной деятельности, поскольку площадь возделывания щелочных почв (37%) превышает таковую для засоленных почв (23%) (Paz et al., 2012). Щелочные почвы, часто ассоциируемые с засушливыми и полузасушливыми регионами, встречаются в различных частях мира, влияя на сельскохозяйственную продуктивность. Почвы, богатые карбонатами, от природы являются щелочными, и такие почвы ограничивают рост кальцифобных растений. У двудольных растений, таких как горох, бобы или подсолнечник, ингибирование роста корней HCO₃⁻ проявляется в большей степени, чем у однодольных растений, таких как ячмень и овес (Poschenrieder et al., 2018). Щелочной стресс может приводить к многочисленным пагубным последствиям для роста растений, включая прорастание семян, морфологическое развитие и образование органов, что в конечном итоге приводит к снижению урожайности (Ma et al., 2023). Щелочной стресс препятствует росту и развитию растений, вызывая ионный и осмотический стрессы наряду с окислительным стрессом из-за повышенной выработки активных форм кислорода (ROS), которые нарушают физиологический и биохимический метаболизм растений (Wang et al., 2022a). Более того, щелочной стресс значительно снижает скорость фотосинтеза и уровень пигментов, оказывая более серьезное воздействие на фотосинтез, чем солевой стресс, что, в свою очередь, приводит к снижению накопления биомассы и урожайности, поскольку фотосинтез напрямую влияет на оба этих процесса (Yang et al., 2009). Активные формы кислорода (ROS) возникают как побочные продукты нормального метаболизма, и высокие концентрации ROS могут повреждать клеточные компоненты и мембраны. Абиотические стрессы, такие как жара, засуха и засоление, увеличивают выработку ROS, вызывая окислительный стресс (Dubey et al., 2022). Аналогично, щелочной стресс вызывает чрезмерное накопление активных форм кислорода (ROS), включая пероксид водорода (H₂O₂) и супероксидные радикалы, которые нарушают клеточные процессы и приводят к окислительному повреждению, в частности, через перекисное окисление липидов клеточных мембран в растительных тканях (Liu et al., 2022). Это окислительное повреждение подтверждается накоплением малонового диальдегида (MDA), побочного продукта перекисного окисления липидов, который служит надежным индикатором повреждения мембран в стрессовых условиях, как это было наблюдено у люцерны при щелочном стрессе (Song et al., 2017). Чтобы смягчить эти последствия, растения активируют ключевые антиоксидантные ферменты, такие как каталаза (CAT) и аскорбатпероксидаза (APX). Эти ферменты играют ключевую роль в детоксикации избыточного H₂O₂ и защите клеточных компонентов от окислительного повреждения. CAT быстро превращает H₂O₂ в воду и кислород в пероксисомах, тогда как APX, обладающая более высоким сродством к H₂O₂, функционирует в различных клеточных компартментах, используя аскорбат для снижения уровня H₂O₂ (Sofo et al., 2015). В дополнение к ферментативному удалению ROS, растения адаптируются к щелочному стрессу путем накопления осмолитов, включая пролин и растворимые сахара, которые способствуют осмотическому балансу и снижению ROS, а также поддерживают клеточные функции (Gong et al., 2014; Hou et al., 2023). Например, у пшеницы соле-щелочной стресс привел к повышению уровня пролина и растворимых сахаров для противодействия соле-щелочным условиям (Lin et al., 2012). Аналогично, у трансгенных проростков риса устойчивость к щелочному стрессу была связана со значительно более высоким накоплением пролина и растворимых сахаров по сравнению с контрольными растениями (Feng et al., 2024).
Корни, как основные органы, отвечающие за поглощение воды и питательных веществ, также играют ключевую роль в восприятии стресса и реагировании на него, в том числе в щелочных условиях. Было показано, что щелочной стресс оказывает значительное воздействие на корни растений, вызывая окислительный стресс, что приводит к снижению активности корней и гибели клеток корней (Guo et al., 2017; Zhang et al., 2017). Кроме того, щелочной стресс уменьшает площадь поверхности корней, общую длину корней и объем корней, ограничивая способность растения эффективно поглощать воду и питательные вещества. Например, у чувствительных сортов риса щелочные условия вызвали существенное снижение биомассы корней, площади поверхности и количества кончиков корней, что ключевой для эффективного поглощения воды и питательных веществ (Zhang et al., 2017; Fang et al., 2021). Повышенный уровень щелочных солей снижает содержание калия (K⁺), способствуя поглощению натрия (Na⁺), что приводит к выходу K⁺ из растительных клеток и нарушает гомеостаз Na⁺/K⁺, ухудшая ключевые клеточные функции (Wakeel, 2013). Кроме того, в ризосфере высокий pH вызывает осаждение множества ионов питательных веществ, препятствуя их доступности и поглощению, тем самым нарушая ионный гомеостаз (Guo et al., 2010, Guo et al., 2022).
Нут (Cicer arietinum L.), третья по значимости зернобобовая культура в мире, возделывается на приблизительно 12 миллионах гектаров, в основном в засушливых и полузасушливых регионах, где он подвергается различным абиотическим стрессам. Хотя воздействие засоления на рост, физиологию и ионный баланс нута было extensively изучено (Flowers et al., 2010), влияние щелочного стресса остается недостаточно изученным. В отличие от засоления, которое в первую очередь вызывает ионную токсичность, щелочной стресс включает высокие уровни pH, которые препятствуют поглощению эссенциальных питательных веществ и влияют на выведение натрия (Na⁺) (Zhang et al., 2023). Сочетанное воздействие ионной токсичности и повышенного pH делает щелочной стресс особенно вредным для роста растений, значительно нарушая ионный баланс, особенно гомеостаз Na⁺ и K⁺. В этом исследовании проростки нута подвергали щелочному стрессу с использованием смеси NaHCO₃ и Na₂CO₃, и анализировали такие параметры, как рост корней, биохимические изменения и концентрации ионов, чтобы показать механизмы, лежащие в основе повреждений, вызванных щелочным стрессом, и адаптивных реакций растений нута.
Материалы и методы
Растительный материал и условия выращивания
Мы отобрали здоровые семена нута (RVG 203) (любезно предоставлены KVK, IGNTU) и поверхностно стерилизовали их с помощью 70% этанола в течение 1 минуты, с последующим применением 0,5% гипохлорита натрия в течение 1 минуты. Затем семена промывали стерильной водой Milli-Q 5-6 раз. После этого семена инкубировали в стерильной воде Milli-Q в течение шести часов, а затем помещали на влажную фильтровальную бумагу для проращивания в темноте при 28°C.
Через два дня двадцать равномерно проросших проростков были отобраны и перенесены раздельно в контрольную и щелочную стрессовую среды. Им давали расти в течение 10 дней в контролируемой ростовой камере при 28°C с 12-часовым фотопериодом. После десяти дней обработки у проростков анализировали параметры роста, физиологические характеристики и биохимические реакции. Все эксперименты были проведены трижды, причем каждый эксперимент включал три биологические повторности.
Обработка щелочным стрессом
Щелочной стресс моделировали путем смешивания бикарбоната натрия (NaHCO₃) и карбоната натрия (Na₂CO₃) в молярном соотношении 9:1 и применения концентрации 20 мМ смеси в 0,5X растворе Хогланда (pH 9,1, EC 2650 мкСм/см). Эта концентрация была определена после оценки ингибирования роста растений в диапазоне концентраций от 0 до 40 мМ, с выбором наименьшей концентрации (20 мМ), при которой наблюдалось значительное повреждение корней и ингибирование роста растений в течение 10-дневного экспериментального периода. Контрольная обработка включала полив растений 0,5X раствором Хогланда (pH 6,5, EC 1200 мкСм/см) без добавления NaHCO₃ и Na₂CO₃. pH и EC гидропонных растворов контролировали ежедневно, и среду заменяли свежей средой каждые два дня.
Измерение роста проростков
После 10 дней роста как в контрольных, так и в щелочных стрессовых условиях проростки осторожно извлекали из ростовой среды и измеряли длину побега, длину корня, количество боковых корней, сырую массу как побега, так и корня. Затем после высушивания в духовке определяли сухую массу проростков. Корне-побеговое отношение рассчитывали как отношение сухой массы корня к сухой массе побега.
Измерение относительного содержания воды
Относительное содержание воды определяли в соответствии с методом, описанным Dubey et al. (2022). Изначально регистрировали сырую массу (FW) проростков. Затем проростки помещали в пластиковые пакеты, которые запечатывали после добавления воды для их погружения. Эти пакеты оставляли при комнатной температуре на 4 часа. После этого проростки промокали бумажными полотенцами для удаления лишней влаги и измеряли тургорную массу (TW). Затем проростки высушивали в духовке с горячим воздухом при 60°C в течение 4 дней и регистрировали сухую массу (DW). Относительное содержание воды (RWC) рассчитывали с использованием уравнения: RWC (%) = (FW – DW)/(TW – DW) x 100
Определение параметров корней
Параметры корней, включая общий объем, общую площадь поверхности, объем главного корня, площадь поверхности главного корня, объем боковых корней, площадь поверхности боковых корней, количество корневых кончиков и количество точек ветвления, как у контрольных, так и у обработанных растений, определяли с помощью RhizoVision Explorer (Seethepalli et al., 2021).
Определение содержания H₂O₂
Содержание пероксида водорода (H₂O₂) измеряли следующим образом: образцы корней (500 мг) гомогенизировали на льду в 5 мл 0,1% (мас./об.) трихлоруксусной кислоты (TCA). Гомогенат центрифугировали при 12 000 об/мин в течение 15 минут. Реакционная смесь включала 0,5 мл 10 мМ фосфатного буфера (pH 7,0), 1 мл 1 М йодида калия и 0,5 мл супернатанта. Эту смесь инкубировали в темноте в течение одного часа. Затем измеряли абсорбцию при 390 нм с помощью спектрофотометра. Содержание H₂O₂ определяли с использованием стандартной кривой и выражали в микромолях на грамм сырой массы (Dubey et al., 2022).
Оценка перекисного окисления липидов
Перекисное окисление липидов как в контрольных, так и в обработанных щелочью растениях оценивали путем измерения концентрации малонового диальдегида (MDA) в корневой ткани случайно выбранных растений из каждой группы. Определение MDA проводили в соответствии с методом, изложенным Heath and Packer (1968). Кратко: 200 мг корневой ткани гомогенизировали в 2 мл 0,1% TCA. Гомогенат затем центрифугировали при 10 000 g в течение 20 минут. Затем 0,5 мл супернатанта добавляли к реакционной смеси, содержащей 4 мл 0,5% TBA в 20% TCA. Реакционную смесь нагревали на водяной бане при 95°C в течение 30 минут, а затем немедленно охлаждали на льду. После охлаждения смесь центрифугировали при 10 000 g в течение 10 минут. Измеряли абсорбцию при 532 нм и 600 нм для супернатанта. Количество MDA оценивали, используя коэффициент экстинкции 155 мМ⁻¹ см⁻¹.
Оценка содержания пролина
Содержание пролина количественно определяли с использованием колориметрического метода, адаптированного из Abraham et al. (2010). Кратко: около 100 мг корневой ткани гомогенизировали в 3% сульфосалициловой кислоте. Гомогенат центрифугировали при 12 000 g в течение 5 минут при комнатной температуре. Аликвоту супернатанта (100 мкл) смешивали с 100 мкл 3% сульфосалициловой кислоты, 200 мкл ледяной уксусной кислоты и 200 мкл кислого нингидрина. Эту смесь инкубировали при 96°C в течение 60 минут, а затем быстро охлаждали на льду для остановки реакции. Образцы экстрагировали толуолом и измеряли абсорбцию при 520 нм, используя толуол в качестве эталона. Концентрацию пролина рассчитывали с использованием стандартной кривой.
Оценка общего содержания растворимых сахаров
Общее содержание растворимых сахаров определяли в соответствии с протоколом Irigoyen et al. (1992). Свежесобранную корневую ткань (200 мг) гомогенизировали в 2 мл 95% этанола. Гомогенат центрифугировали при 3500 g в течение 10 минут. Спиртовой супернатант (0,1 мл) смешивали с 3 мл свежеприготовленного раствора антрона (150 мг антрона, растворенного в 100 мл 72% H₂SO₄) и нагревали на кипящей водяной бане в течение 10 минут. Абсорбцию измеряли при 625 нм после охлаждения. Общее содержание растворимых сахаров количественно определяли с использованием стандартной кривой глюкозы.
Повреждение мембран
Для оценки целостности/повреждения мембран растительные образцы были случайным образом отобраны как из контрольной, так и из опытной групп. Корневые образцы тщательно промывали деионизированной водой для удаления любых прилипших к поверхности электролитов. Образцы корней (1 г) помещали в индивидуальные 50-мл пробирки Falcon, содержащие 20 мл деионизированной воды. Затем эти пробирки выдерживали при постоянной температуре 25°C в течение 1 часа. После этого периода инкубации измеряли электропроводность (EC) (обозначается как R1). После первоначального измерения образцы тканей подвергали кипячению на водяной бане в течение 40 минут. После кипячения образцам давали остыть до 25°C и снова измеряли EC (обозначается как R2). Повреждение мембран (MI) впоследствии рассчитывали с использованием следующей формулы: MI (%) = (R1/R2) × 100.
Анализ жизнеспособности клеток корней
Окрашивание и количественное определение Evans blue проводили, как описано ранее (Kumar and Kirti, 2012). Образцы погружали в 0,25% (мас./об.) раствор Evans blue при непрерывном перемешивании. После окрашивания сегменты корней тщательно промывали несколько раз водой Milli-Q для удаления избыточного и несвязанного красителя. Для количественного определения уровня Evans blue окрашенные образцы измельчали в 1% растворе SDS и затем центрифугировали при 12 000 g в течение 10 минут. Супернатант затем собирали и измеряли его оптическую плотность (OD) при 600 нм. Полученные значения OD затем использовали для расчета концентрации Evans blue в микрограммах на грамм сырой массы (мкг г⁻¹ FW), используя стандартную кривую, построенную с известными концентрациями Evans blue.
Оценка активности ферментов каталазы и аскорбатпероксидазы
Активность каталазы (CAT) и аскорбатпероксидазы (APX) измеряли в соответствии с методами Elavarthi and Martin (2010), как подробно описано Dubey et al. (2022). Кратко: активность CAT оценивали, отслеживая снижение абсорбции при 240 нм по мере разложения H₂O₂, тогда как активность APX определяли путем измерения снижения абсорбции аскорбата при 290 нм.
Измерение содержания ионов
Количественное определение содержания ионов проводили с использованием масс-спектрометрии с индуктивно связанной плазмой (ICP-MS) в Центральном исследовательском центре Индийского технологического института Дели. Образцы корней, каждый весом 200 мг, предварительно высушенные и измельченные, подвергали кислотному разложению с 8 мл концентрированной HNO₃ при 200°C и 60 бар в течение 30 минут в системе микроволнового разложения (производства Anton Paar, модель: Multiwave PRO). После разложения объем образца доводили до 40 мл деионизированной водой, и полученный раствор фильтровали с использованием мембраны 0,2 мкм. Элементный анализ проводили с использованием прибора ICP-MS (Модель: 7900, производство Agilent Technologies), откалиброванного в соответствии с инструкциями производителя с использованием холостых и мультиэлементных стандартов.
Данные и статистический анализ
Данные анализировали с использованием однофакторного дисперсионного анализа (ANOVA) с последующим сравнением средних с использованием критериев Тьюки и Бонферрони для определения уровней значимости. Статистический анализ выполняли с использованием программного обеспечения OriginPro 2021. Анализ главных компонент (PCA) ионома проводили с использованием программного обеспечения R.
Результаты и обсуждение
Влияние щелочного стресса на рост проростков нута
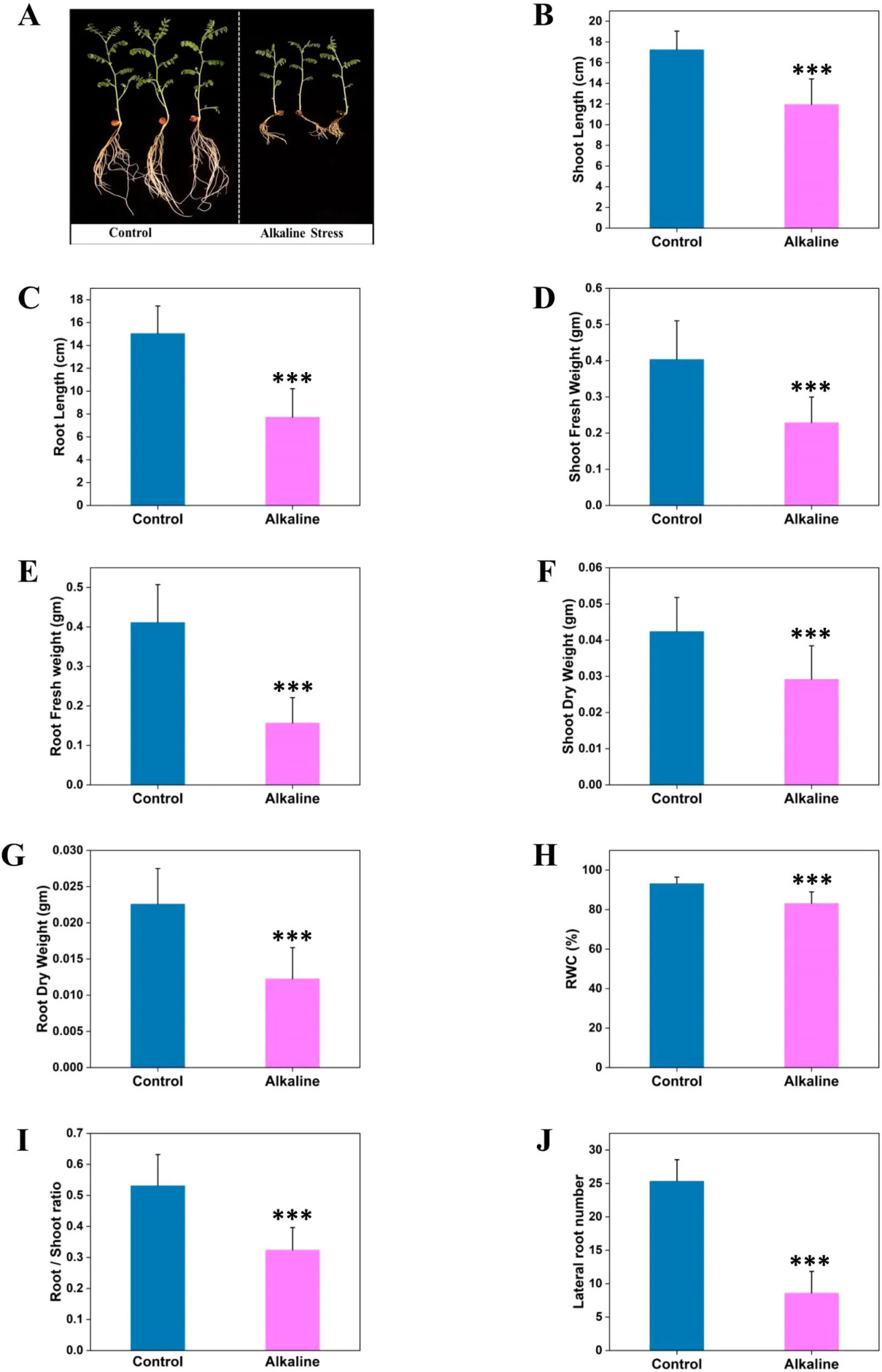
Щелочной стресс негативно влияет на рост и урожайность сельскохозяйственных культур, однако его воздействие на нут (Cicer arietinum L.), экономически и питательно важный бобовый, остается недостаточно изученным. Предыдущие несколько исследований показали пагубное воздействие щелочных условий как на однодольные, так и на двудольные культуры (Gong et al., 2014; Zhang et al., 2017). Щелочной стресс значительно ухудшал рост проростков нута, вызывая заметное снижение длины побега, длины корня, сырой массы побега, сырой массы корня, сухой массы побега, сухой массы корня и относительного содержания воды в проростках (RWC) (Рисунки 1A–H). Щелочной стресс снижал длину корня на 48% и длину побега на 30%. Сырая масса корня и сухая масса корня уменьшились на 62% и 45% соответственно, в то время как сырая масса побега и сухая масса побега уменьшились на 45% и 31%. Снижение роста было более выраженным у корней, о чем свидетельствует существенное снижение длины и биомассы корней. Дальнейший анализ корне-побегового отношения показал его снижение при щелочном стрессе, что указывает на повреждение корней (Рисунок 1I). Кроме того, общее количество боковых корней было сокращено на 66% (Рисунок 1J). Аналогичное снижение параметров роста при щелочном стрессе было сообщено для других видов растений, что указывает на общую реакцию в различных культурах (Guo et al., 2010; Wang et al., 2022b; Ma et al., 2023). Результаты подчеркивают пагубное воздействие щелочного стресса на проростки нута. Существенное снижение длины корней, биомассы и количества боковых корней указывает на негативное воздействие на корневую систему, ставящее под угрозу поглощение воды и питательных веществ и снижающее общую биомассу.
Рисунок 1 Влияние щелочного стресса на рост проростков нута. (A) Репрезентативные изображения десятидневных проростков нута, выращенных в контрольных и щелочных условиях. Количественно определены параметры роста, включая: длину побега (B), длину корня (C), сырую массу побега (D), сырую массу корня (E), сухую массу побега (F), сухую массу корня (G), относительное содержание воды (H), корне-побеговое отношение (I) и общее количество боковых корней (J). Данные представлены как средние значения с указанием погрешностей ± SD. Звездочки обозначают статистически значимые различия (P < 0,001).
Влияние щелочного стресса на морфологию корней и корневые признаки проростков нута
Архитектура корней значительно влияет на продуктивность растений, включая такие переменные, как топология, длина корней и ветвление, которые влияют на приобретение почвенных ресурсов и закрепление (Fitter and Stickland, 1991). Хотя воздействие засоления на развитие корней нута известно (Flowers et al., 2010; Kaur et al., 2022), нет исследований о влиянии защелачивания на морфологию корней нута, биохимические свойства и ионный гомеостаз. Учитывая, что щелочной стресс оказывает большее влияние на корни, мы проанализировали различные морфологические характеристики корней с использованием программного обеспечения RhizoVision (Seethepalli et al., 2021).
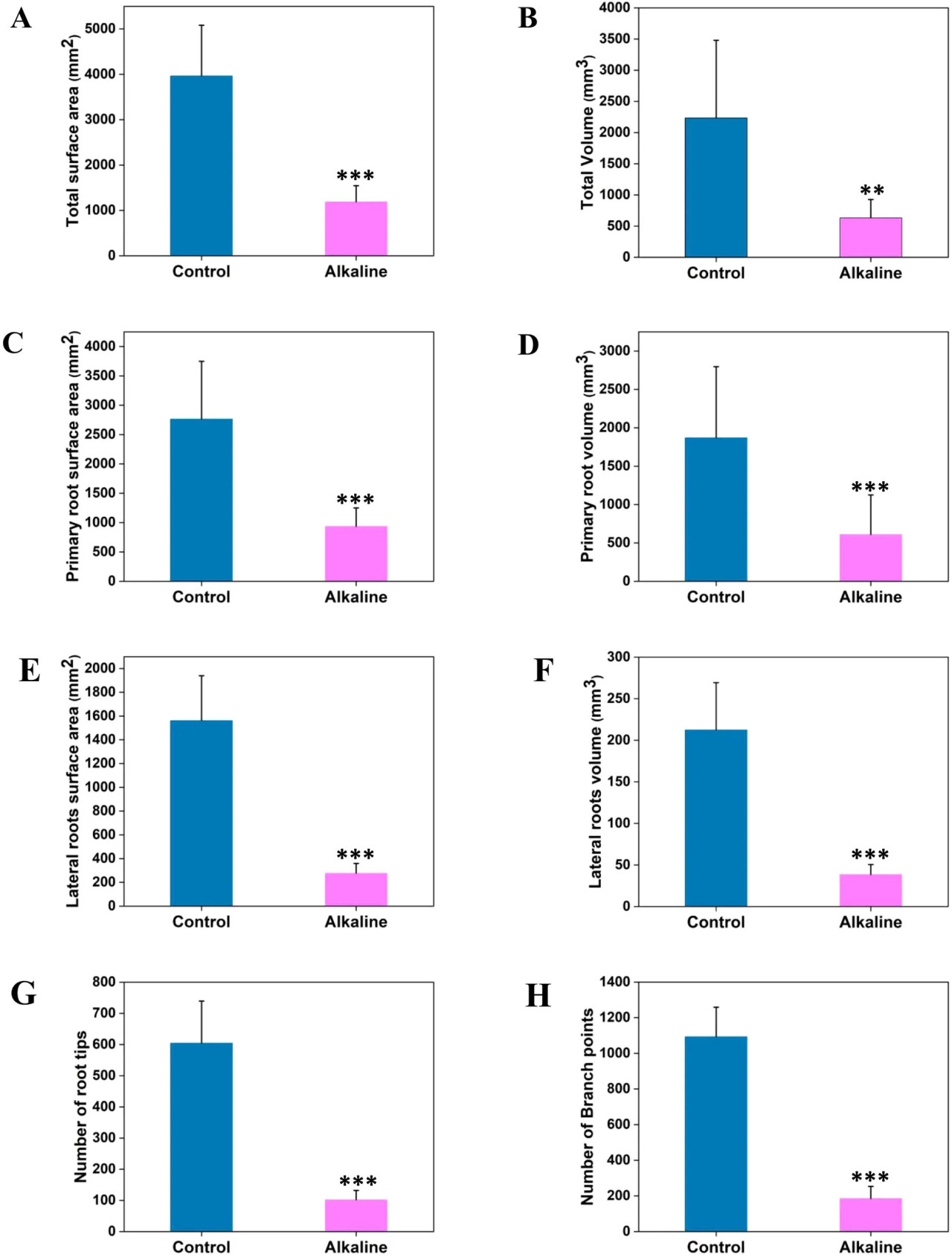
Значительные различия наблюдались в общей площади поверхности и общем объеме корней между контрольной группой и группой, подвергнутой щелочной обработке (Рисунки 2A, B). В то время как как признаки главного, так и боковых корней были негативно затронуты щелочным стрессом, признаки боковых корней демонстрировали более выраженное снижение (>80%) при щелочном стрессе (Рисунки 2E–H). Например, площадь поверхности и объем главного корня были уменьшены на 66,19% и 67,46% соответственно, тогда как площадь поверхности и объем боковых корней были уменьшены на 82,31% и 81,85% соответственно (Рисунки 2C–F). Кроме того, общее количество корневых кончиков и общее количество точек ветвления также показали значительное снижение (>80%) при щелочном стрессе по сравнению с контролем (Рисунки 2G, H), что указывает на нарушение роста главного и боковых корней у проростков нута в условиях щелочного стресса.
Рисунок 2 Анализ корневых признаков проростков нута в контрольных условиях и при щелочном стрессе с использованием RhizoVision Explorer. Корневые признаки проростков нута были проанализированы на полутоновых изображениях, полученных с помощью программного обеспечения RhizoVision Explorer, в контрольных и щелочных условиях. На рисунке представлены количественные определения следующих корневых признаков: общая площадь поверхности (A), общий объем (B), площадь поверхности главного корня (C), объем главного корня (D), площадь поверхности боковых корней (E), объем боковых корней (F), количество корневых кончиков (G) и количество точек ветвления (H). Данные выражены как средние значения ± SD (n = 25). Статистическая значимость указана звездочками (P < 0,01, P < 0,001).
Наблюдаемое снижение корне-побегового отношения у нута (Рисунок 1I) указывает на нарушение роста корней относительно роста побегов и на повреждение корней. Несколько исследований сообщили, что щелочной стресс ограничивает расширение корневой системы, тем самым снижая способность корневой структуры к эффективному поглощению питательных веществ и воды (Zhang et al., 2016; Lu et al., 2022; Wang et al., 2022b). Например, у риса воздействие щелочных условий значительно снижало площадь поверхности, длину и объем корней, что было связано с ограниченным расширением клеток и структурными повреждениями в корневых тканях (Lv et al., 2013). Аналогично, заметное снижение бокового ветвления и плотности корневых кончиков при щелочном стрессе по сравнению с контрольными условиями предполагает потерю ключевых адаптивных корневых признаков, необходимых для устойчивости в стрессовых условиях (Benjamin and Nielsen, 2006). Выраженное снижение корневых признаков по сравнению с побегами указывает на более высокую восприимчивость корней к щелочному стрессу.
Щелочной стресс вызывает повреждение мембран и снижает жизнеспособность клеток корней
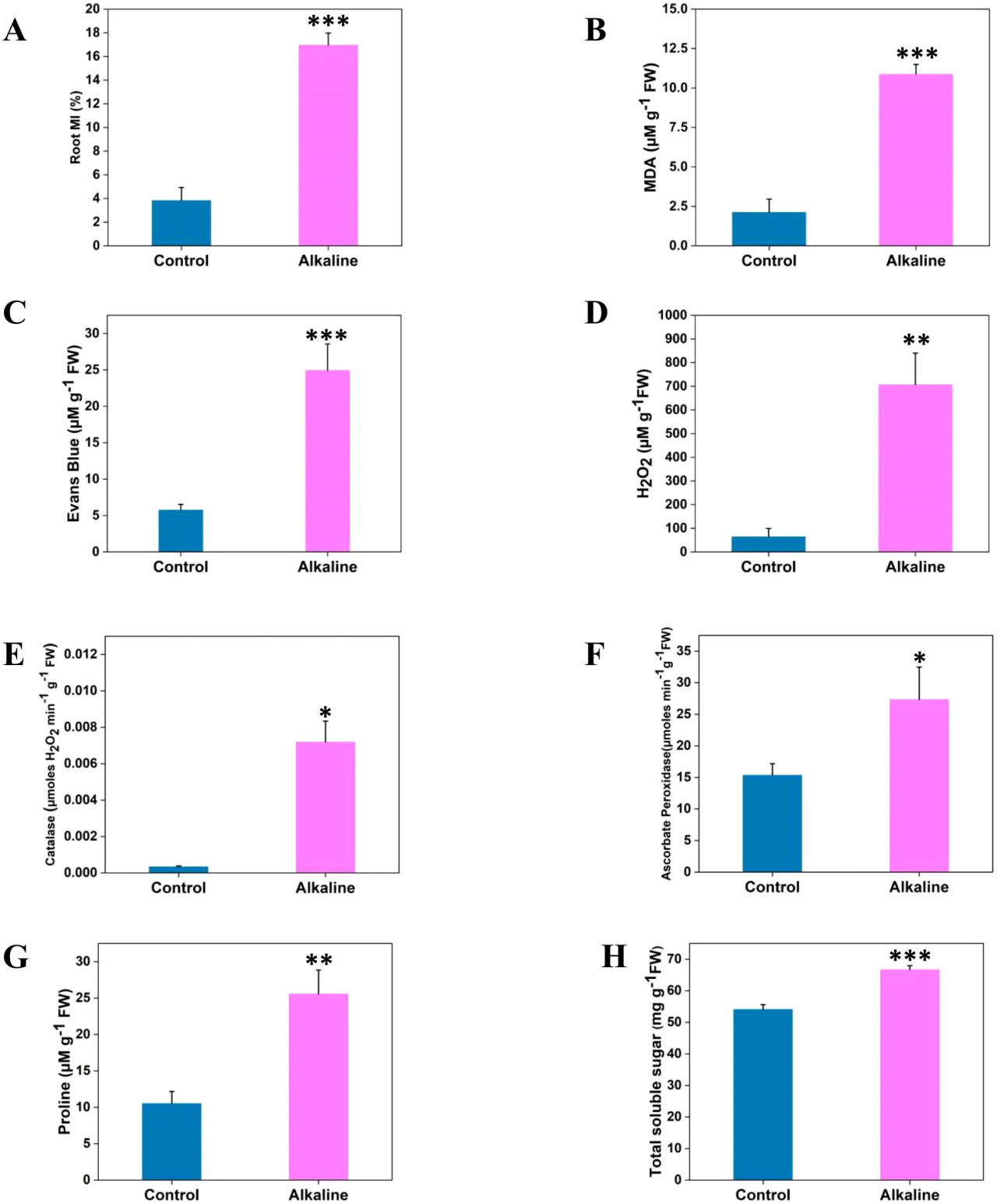
Щелочной стресс значительно влиял на клеточную мембрану корней, увеличивая утечку ионов более чем в 4 раза (Рисунок 3A) и концентрацию MDA в 5 раз (Рисунок 3B) по сравнению с контрольными растениями. Эти результаты четко указывают на повреждение мембран в корнях нута в щелочных условиях. Наблюдаемое увеличение утечки ионов предполагает существенную дестабилизацию мембран, вероятно, из-за нарушения ионного гомеостаза и окислительного стресса (Zhang et al., 2017). Аналогично, 5-кратное увеличение концентрации MDA указывает на повышенное перекисное окисление липидов, отражая окислительное повреждение, которое обычно усиливается в стрессовых условиях (Song et al., 2017). Жизнеспособность клеток корней в щелочных условиях оценивали с использованием окрашивания Evans blue, которое показало более чем 4-кратное увеличение поглощения красителя в стрессированных корнях по сравнению с контролем (Рисунок 3C). Повышенное поглощение Evans blue в стрессированных корнях нута наглядно показывает снижение жизнеспособности клеток, поскольку краситель избирательно проникает в нежизнеспособные клетки. Это сниженная жизнеспособность отражает гибель клеток и потерю функциональной корневой ткани, что, следовательно, ограничивает удлинение корней и образование боковых корней, о чем свидетельствует наблюдаемое снижение морфологии и ветвления корней (Рисунки 2A–H).
Рисунок 3 Физиологические и биохимические реакции корней нута на щелочной стресс. На рисунке представлен количественный анализ следующих физиологических и биохимических параметров: (A) Утечка электролитов, (B) Содержание малонового диальдегида (MDA), (C) Жизнеспособность клеток корней, (D) Содержание пероксида водорода (H₂O₂), (E) Активность каталазы (CAT), (F) Активность аскорбатпероксидазы (APX), (G) Содержание пролина и (H) Общее содержание растворимых сахаров. Данные выражены как средние значения ± SD из экспериментов, проведенных в трех повторностях. Статистическая значимость между контрольными и щелочными стрессовыми условиями обозначена как P < 0,05, P < 0,01, P < 0,001.
Накопление H₂O₂ и активность антиоксидантных ферментов в корнях в щелочных условиях
Чтобы исследовать основные причины повреждения мембран и гибели клеток в корнях нута при щелочном стрессе, мы изучили основные агенты, способствующие этому повреждению. Пероксид водорода (H₂O₂), тип активных форм кислорода (ROS), обычно образуется во время нормальных метаболических процессов. Однако, когда он присутствует в повышенных концентрациях, H₂O₂ может приводить к окислительному повреждению клеточных компонентов, включая мембранные липиды (Dubey et al., 2022). Количественное определение H₂O₂ в корнях нута в щелочных условиях показало, что его уровни увеличились в несколько раз по сравнению с контрольными корнями (Рисунок 3D). Кроме того, активности ферментов каталазы (CAT) и аскорбатпероксидазы (APX), ключевых антиоксидантов, были значительно повышены в стрессированных корнях (Рисунки 3E, F).
Чрезмерное накопление H₂O₂ было идентифицировано как ключевой фактор, способствующий чувствительности к щелочному стрессу, что было продемонстрировано в недавних исследованиях локуса Alkaline Tolerance 1 (AT1). У сорго и других однодольных функциональный AT1 негативно регулирует фосфорилирование аквапоринов, отвечающих за транспорт H₂O₂, что приводит к его накоплению и усилению окислительного повреждения в щелочных условиях. Нокауты AT1 у таких культур, как сорго, просо, рис и кукуруза, показали улучшенную устойчивость к щелочному стрессу за счет снижения накопления H₂O₂ и уменьшения окислительного стресса (Zhang et al., 2023).
Этот окислительный стресс вызывает повышение регуляции антиоксидантных ферментов, таких как каталаза (CAT) и аскорбатпероксидаза (APX), активируя врожденные механизмы защиты для противодействия окислительному стрессу. Как каталаза (CAT), так и аскорбатпероксидаза (APX) участвуют в удалении H₂O₂ (Dubey et al., 2022). Однако, хотя эти ферменты смягчают часть окислительного стресса, наблюдаемое повреждение корней и повышенные уровни H₂O₂ предполагают, что, несмотря на повышение активности CAT и APX, уровни ROS остаются высокими. Этот избыток ROS может перегружать защитные механизмы, приводя к окислительному повреждению, проявляющемуся в виде клеточных повреждений, гибели клеток и нарушении функции корней в щелочных условиях (Zhang et al., 2017). Баланс между продукцией ROS и антиоксидантной активностью в конечном итоге определяет степень клеточных и структурных повреждений при щелочном стрессе. Мощные антиоксиданты, такие как процианидины, могут смягчить повреждение корней и способствовать росту за счет снижения накопления ROS, что подчеркивает важность антиоксидантов в борьбе с окислительным стрессом (Zhang et al., 2017).
Накопление пролина и общих растворимых сахаров при щелочном стрессе
Накопление пролина и общих растворимых сахаров (TSS) является распространенной адаптивной реакцией растений на осмотический стресс, действуя как осмопротекторы в стрессовых условиях. Осмотический стресс, вызванный щелочным стрессом, привел к усилению накопления пролина и растворимых сахаров в корнях нута (Рисунки 3G, H). В частности, корни, обработанные щелочью, продемонстрировали заметное увеличение концентрации пролина на 59,53% и концентрации TSS на 18,8% по сравнению с контролем (Рисунки 3G, H).
Более высокие уровни неорганических ионов в почве повышают осмотическое давление, приводя к осмотическому стрессу и физиологической засухе у растений (Fang et al., 2021). Усиленное накопление пролина и общих растворимых сахаров (TSS) в корнях нута при щелочном стрессе указывает на осмопротекторную стратегию для смягчения этого стресса. В ответ на приток Na⁺ корни растений накапливают пролин и растворимые сахара, снижая осмотическое давление и улучшая удержание воды, ее поглощение и транспорт (Verma et al., 2016). Аналогичное увеличение пролина и TSS было сообщено для корней проса прутьевидного и сои при щелочном стрессе (Ma et al., 2023; Wang et al., 2022b). Эта адаптивная реакция соответствует более широким механизмам растений против абиотических стрессов, причем повышенные уровни пролина и TSS наблюдаются у растений в условиях теплового и солевого стресса (Dubey et al., 2022; Liu et al., 2022).
Щелочной стресс нарушает ионный баланс
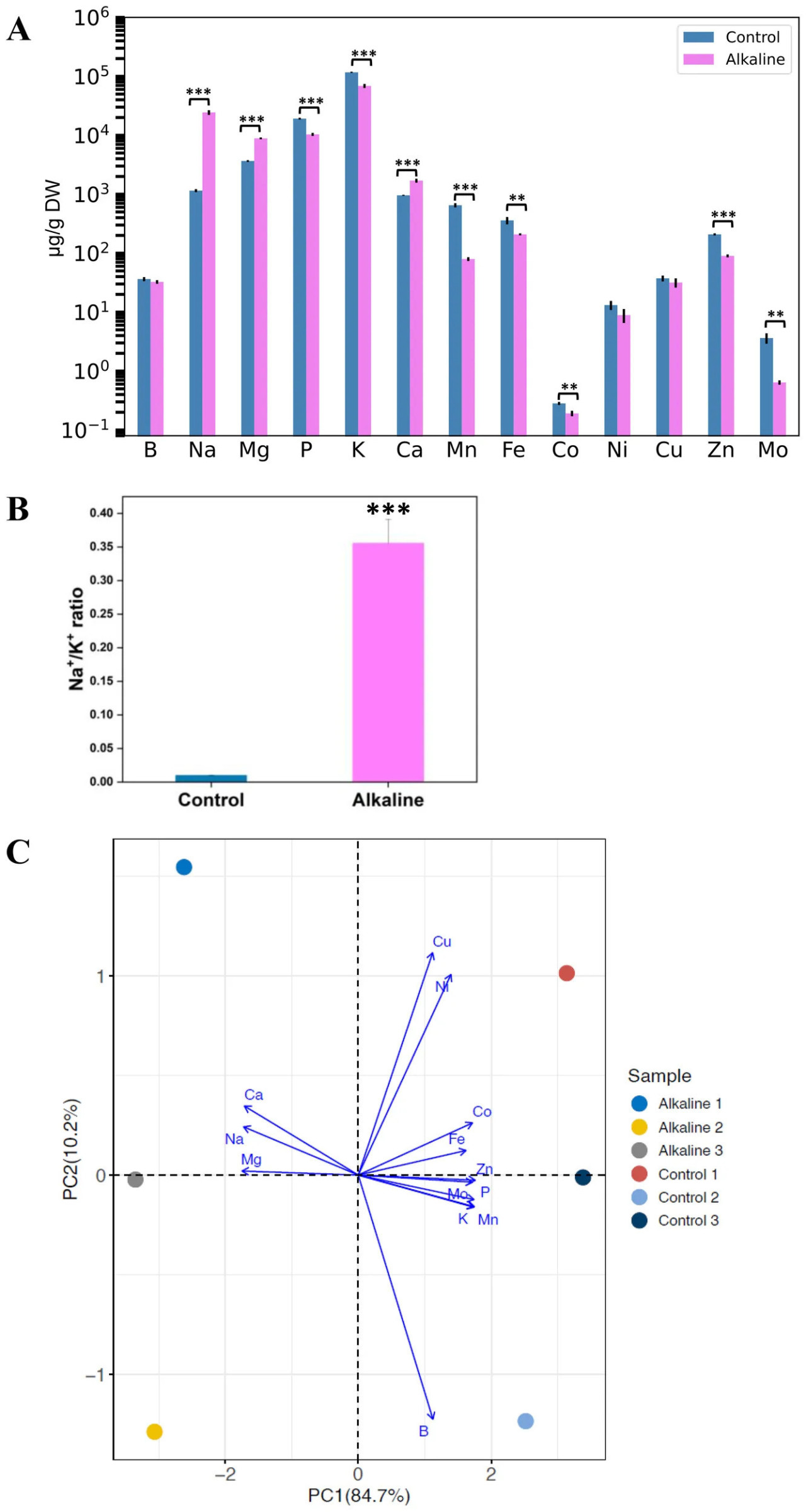
Щелочной стресс нарушает ионный баланс растений, что приводит к усилению накопления натрия (Na⁺), кальция (Ca²⁺) и магния (Mg²⁺) в корнях нута. И наоборот, уровни калия (K⁺), фосфора (P), марганца (Mn), железа (Fe), кобальта (Co), цинка (Zn) и молибдена (Mo) значительно снижаются в условиях щелочного стресса по сравнению с контролем. Уровни бора, никеля и меди показывают мало изменений между стрессированными и контрольными корнями (Рисунок 4A). Кроме того, отношение Na⁺/K⁺ существенно увеличивается при щелочном стрессе (Рисунок 4B). Анализ главных компонент (PCA) данных иономики показывает общие коэффициенты вариации для PC1 на уровне 84,72% и для PC2 на уровне 10,16% (Рисунок 4C). Повышенная щелочность из-за уровня бикарбоната снижает концентрации железа и калия у различных видов растений, включая ячмень, кукурузу и сорго (Alhendawi et al., 1997). Аналогично, щелочной стресс повышает уровни кальция и магния у пшеницы и люцерны, что соответствует нашим результатам на нуте (Guo et al., 2010; Wang et al., 2017).
Рисунок 4 Реакции концентрации ионов в корнях нута на щелочной стресс. (A) Концентрации элементов в корнях нута в контрольных и щелочных условиях, измеренные с помощью ICP-MS. Ось y представлена в логарифмическом масштабе для более четкой визуализации в различных диапазонах концентраций. (B) Отношение Na⁺/K⁺ в контрольных и щелочных условиях. (C) PCA, иллюстрирующая различия в иономных профилях между контрольными и обработанными щелочью корнями. Данные представлены как среднее значение ± SD (n = 3). Значимые различия указаны как P < 0,001, P < 0,01.
Щелочной стресс вызывает осмотический стресс и ионную токсичность, аналогичные солевому стрессу, дополнительно ухудшая поглощение питательных веществ при высоких значениях pH и приводя к дисбалансу питательных веществ, метаболическим нарушениям и расстройствам ионного гомеостаза (Guo et al., 2015; Lu et al., 2022). Калий (K⁺) имеет ключевое значение для активации ферментов, осмотической регуляции и клеточного ионного баланса, поддерживая общую метаболическую стабильность и многочисленные физиологические функции у растений. И наоборот, натрий (Na⁺) становится токсичным при повышенных концентрациях, нарушая метаболические процессы и активности ферментов. Таким образом, поддержание оптимального отношения Na⁺/K⁺ выжнейший для здоровья растений. В корнях нута щелочной стресс значительно повышает уровни Na⁺, одновременно снижая уровни K⁺, создавая дисбаланс Na⁺/K⁺, который негативно влияет на поглощение питательных веществ и клеточную функцию. Это вызванное стрессом повышение Na⁺ частично обусловлено конкуренцией с K⁺ за пути поглощения, поскольку Na⁺ часто заменяет K⁺ в неселективных каналах и высокоаффинных переносчиках, нарушая нормальное поглощение K⁺. Кроме того, вызванная щелочью деполяризация мембраны препятствует поглощению K⁺ и способствует его оттоку, дополнительно снижая уровни K⁺ в тканях растений (Wakeel, 2013).
Дальнейший, щелочной стресс негативно влияет на клубенькообразование у нута, о чем свидетельствует низкий процент клубенькообразования на щелочных почвах (Singh et al., 2015). Это снижение объясняется неблагоприятной средой для роста и размножения ризобий и дефицитом питательных веществ. В дополнение к макроэлементам, таким как фосфор, симбиоз бобовых и ризобий требует различных микроэлементов, включая бор, кобальт, медь, железо, марганец, молибден, никель и цинк, иногда в более высоких количествах, чем требуется самому растению или бактериям по отдельности (O’Hara, 2001). Например, молибден, ключевой для активности нитрогеназы, может снижать продуктивность бобовых, влияя на развитие и функцию клубеньков (O’Hara, 2001). Сниженные уровни молибдена и других микроэлементов в корнях нута в нашем исследовании предполагают, что щелочной стресс может препятствовать клубенькообразованию, затрудняя поглощение эссенциальных питательных веществ.
Выводы
Это исследование показывает, что щелочной стресс значительно подавляет рост нута за счет снижения биомассы побегов и корней, нарушения морфологии корней и ухудшения поглощения питательных веществ. Щелочной стресс также вызывает окислительное повреждение в корнях нута, о чем свидетельствуют повышенные уровни пероксида водорода (H₂O₂) и сниженная жизнеспособность клеток корней. Кроме того, щелочной стресс нарушает ионный баланс, что приводит к усилению поглощения натрия и снижению поглощения эссенциальных питательных веществ, таких как калий, фосфор и железо, которые имеют ключевое значение для здоровья и продуктивности растений. В ответ на стресс растения нута активируют адаптивные механизмы, включая накопление осмолитов, таких как пролин и растворимые сахара, и повышение активности антиоксидантных ферментов, что помогает частично смягчить клеточные повреждения. Однако сочетанные эффекты осмотического стресса, ионной токсичности и метаболических нарушений способствуют чрезмерной продукции активных форм кислорода (ROS), в конечном итоге подавляя защитные механизмы растения и вызывая повреждение корней.
Хотя это исследование предоставляет понимание реакций нута на щелочную среду, индуцированную комбинацией Na₂CO₃ и NaHCO₃, будущие исследования могли бы выиграть от изучения специфических эффектов каждой соли, чтобы лучше понять отдельные ионные и осмотические стрессовые реакции. Кроме того, изучение генетического разнообразия по устойчивости к щелочному стрессу у нута могло бы способствовать разработке устойчивых сортов, пригодных для этих сложных почвенных условий. В целом, эта работа вносит вклад в более широкое понимание физиологии стресса нута и подчеркивает необходимость инновационных подходов для повышения устойчивости сельскохозяйственных культур к щелочным почвам.
Ссылки
Kumar K, Jaiswal A, Koppolu UMK and Kumar KRR (2024) Alkaline stress disrupts growth, biochemistry, and ion homeostasis of chickpea (Cicer arietinum L.) roots. Front. Agron. 6:1497054. doi: 10.3389/fagro.2024.1497054
Перевод статьи «Alkaline stress disrupts growth, biochemistry, and ion homeostasis of chickpea (Cicer arietinumL.) roots» авторов Kumar K, Jaiswal A, Koppolu UMK and Kumar KRR., оригинал доступен по ссылке. Лицензия: CC BY. Изменения: переведено на русский язык
Фото: freepik

















































































































Комментарии (0)