Какая культура кормит почвенные микробы лучше? Ответ вас удивит
Экосистемные функции почвенных микробных сообществ критически важны для устойчивости агроэкосистем, обеспечивая сохранение окружающей среды и продовольственную безопасность. Долгосрочные эксперименты, сравнивающие контрастные севообороты, являются ценным инструментом для мониторинга микробных реакций, но они редко включают все фазы севооборота в рамках одного года. Следовательно, долгосрочное агрономическое воздействие может маскироваться непосредственным эффектом оцениваемой культуры. В этом исследовании мы сравнили различные севообороты на основе Индекса последовательности интенсификации (ISI), который учитывает время занятости почвы, и проанализировали влияние покровных культур и двух стратегий азотного удобрения.
Аннотация
Материал и методы: Мы использовали эксперимент, начатый в 2006 году, со следующими севооборотами: соя-соя, кукуруза-пшеница/соя и кукуруза-соя-пшеница/соя. Образцы почвы были отобраны после уборки каждой летней фазы (т.е. сои, кукурузы, пшеницы/сои), а прокариотическое сообщество почвы было проанализировано с использованием секвенирования гена 16S рРНК.
Результаты и обсуждение: Мы обнаружили, что ISI и фаза культуры были основными предикторами состава микробного сообщества, объясняя 14,7% и 13,0% вариации соответственно. Азотное удобрение оказало незначительный эффект (3,12%) и было обнаружено только после отбора проб кукурузы; покровные культуры не оказали значимого эффекта. Однако присутствие покровных культур показало более высокое альфа-разнообразие и повышенную численность Proteobacteria. Кукуруза обогащала численность определенных таксонов Planctomycetes и Verrucomicrobia, в то время как соя увеличивала численность Bacteroidetes и Proteobacteria. Сравнительно, соя обогащала *Mucilaginibacter* и Geobacter, а пшеница/соя — Brevundimonas и Roseimicrobium.
Заключение: Наши результаты демонстрируют, что фаза культуры так же важна, как и долгосрочное наследие севооборотов, в формировании микробного сообщества, и что реакция конкретных таксонов сильно зависит от фазы культуры, в которой проводился отбор проб.
1 Введение
Почва представляет собой сложнейшую биологическую систему, которая обеспечивает ключевые экосистемные функции, такие как среда обитания и поддержка жизни, регуляция климата, питательных веществ и воды, а также производство продуктов питания, топлива и волокна (Jónsson and Davíðsdóttir, 2016). Биологический компонент почвы, в частности микробиом (почвенные микроорганизмы), в последние годы привлекает значительное внимание (Hermans et al., 2020). Почвенные микробные сообщества могут улучшать здоровье почвы посредством накопления углерода (C), регуляции круговорота питательных веществ и содействия поддержанию или восстановлению почвенной структуры (Garnica et al., 2020; Kibblewhite et al., 2008). На почвенный микробиом могут влиять биотические и абиотические факторы, включая управление почвой и идентичность растений (Custódio et al., 2022; Chaparro et al., 2012; Hartman et al., 2018). В то же время почвенно-растительные взаимодействия, опосредованные почвенными микроорганизмами, могут влиять на здоровье растений, включая рост растений, ассоциации с патогенами и эффективность использования питательных веществ (Finzi et al., 2014; van der Heijden et al., 2008). Понимание непрерывных взаимосвязей между почвой, микробиомом и сельскохозяйственными культурами необходимо для создания устойчивых агроэкосистем.
Современное сельское хозяйство испытывает давление, вынуждающее производить больше продуктов питания для удовлетворения будущего роста мирового спроса в условиях дефицита ресурсов и изменения климата (Tilman et al., 2001). Аргентина является крупным мировым поставщиком сои, кукурузы и пшеницы (FAO, 2021). На плодородных аргентинских пампасах преобладание монокультуры сои (Glycine max L.), повсеместное чрезмерное использование пестицидов и заметный вынос питательных веществ с зерном, превышающий поступление азота, в последние двадцать лет создали угрозу устойчивости (Mazzilli et al., 2015). Предыдущие сообщения продемонстрировали, что неустойчивые методы ведения сельского хозяйства снижают биоразнообразие со значительными потерями эндемичных микробных видов (Figuerola et al., 2012). Такое воздействие на почвенный микробиом потенциально может привести к неблагоприятным последствиям для экосистемных функций, урожайности и общего здоровья почвы, тем самым влияя на глобальную продовольственную безопасность (Dubey et al., 2019). Следовательно, необходимы устойчивые методы ведения сельского хозяйства для обеспечения экологической устойчивости агроэкосистем (Miner et al., 2020). Эти методы включают использование нулевой обработки почвы для снижения нарушения почвы, севообороты, чередующие бобовые и злаковые культуры, включение покровных культур между товарными культурами, а также оптимальное восполнение питательных веществ, которые выводятся с зерном из агроэкосистем (Gaudin et al., 2015; Kleijn et al., 2019; Lupwayi et al., 2018; McDaniel et al., 2014; Novelli et al., 2017).
Одновременное достижение высоких урожаев сельскохозяйственных культур при сохранении здоровья почвы составляет основу парадигмы устойчивой интенсификации (SI) (Pretty and Bharucha, 2014). Эта парадигма основана на экологических принципах, которые предусматривают более интенсивное и эффективное использование ресурсов окружающей среды, включая воду, солнечную радиацию и питательные вещества, с конечной целью повышения общей продуктивности земель (Robledo et al., 2024). Сельскохозяйственные практики в рамках этого подхода стратегически разработаны для продления периодов покрытия почвы и сокращения фаз пара. Это достигается с помощью таких мер, как увеличение частоты выращивания злаков в севообороте за счет двойных посевов или использования покровных культур (Andrade et al., 2017; Caviglia and Andrade, 2010). Оптимизация питания культур достигается за счет дополнения применения неорганических удобрений и дополнительных источников питательных веществ, таких как бобовые культуры или органический навоз (Correndo et al., 2021; Enrico et al., 2020; Miner et al., 2020). Основными благотворными эффектами устойчивой интенсификации являются более высокие урожаи (Andrade et al., 2017; Cano et al., 2023; Stefan et al., 2021), увеличение запасов углерода в стабильных фракциях (Rodríguez et al., 2020; Romaniuk et al., 2018) и сокращение выбросов парниковых газов (Piccinetti et al., 2021). Однако существует критический баланс между необходимостью увеличения частоты выращивания злаков в последовательностях культур для повышения выгод от устойчивой интенсификации и большей зависимостью от азотных удобрений с пагубным воздействием азота на окружающую среду в богатых злаками агроэкосистемах.
Практики устойчивой интенсификации влияют на почвенный микробиом прямо и косвенно, что приводит к различным экологическим реакциям бактериальных групп (Frene et al., 2022). Например, увеличение живого покрова и разнообразия культур может генерировать постоянный поток углерода через ризодепозицию и благоприятствовать определенным копиотрофным группам, таким как Proteobacteria и Bacteroidetes, оказывая либо негативное, либо положительное воздействие на накопление углерода в почве и показатели здоровья почвы (Agomoh et al., 2020; Frene et al., 2022; Li et al., 2014; Novelli et al., 2011). Actinobacteria — тип, характеризующийся наличием множества представителей, стимулирующих рост растений, может увеличиваться в более разнообразных севооборотах, что положительно влияет на продуктивность культур (Stefan et al., 2021). Примечательно, что идентичность вида культуры может быть основным драйвером текущих почвенных микробных сообществ из-за химического состава тканей растений, корневых экссудатов, а также видоспецифических требований агрономических практик (Fang et al., 2022; Fox et al., 2020; Sasse et al., 2018). Например, зерновые культуры требуют высоких доз азотных удобрений и производят большое количество остатков с высоким соотношением C:N, в то время как бобовые могут частично удовлетворять потребность в азоте за счет биологической фиксации и производить небольшое количество остатков с низким соотношением C:N. Acidobacteria могут преобладать после возделывания зерновых, тогда как Actinobacteria и Proteobacteria могут доминировать после бобовых (Chamberlain et al., 2020; Feng et al., 2017; Stefan et al., 2021). Кроме того, азотное удобрение зерновых вызывает изменения pH почвы и изменяет численность ключевых бактериальных и архейных видов, участвующих в почвенном цикле азота, особенно в системах с нулевой обработкой (Viso et al., 2024).
Понимание взаимосвязи между почвенным микробиомом и агрономическими практиками необходимо для создания устойчивых, продуктивных и жизнеспособных агроэкосистем (Wall et al., 2019). Соотношение между зерновыми и бобовыми будет определять чистое поступление азота (Novelli et al., 2011), и как севообороты (Frene et al., 2022; Nivelle et al., 2016; Pinto et al., 2017), так и дополнительная азотная подкормка (Viso et al., 2024; Zhang et al., 2021) оказывают измеримое влияние на почвенный микробиом. Затем мы исследуем, в какой степени азотное удобрение и включение покровных культур модифицируют прокариотические сообщества в последовательностях культур с разной занятостью земель. Однако при анализе севооборотов неясно, являются ли эффекты на почвенную биоту следствием чистого эффекта долгосрочного севооборота или предшествующей культуры в конкретном севообороте (Fox et al., 2020; Ishaq et al., 2017). Чтобы избежать этого смешивающего эффекта, рекомендуется оценивать все фазы севооборота (т.е. все предшествующие культуры, входящие в этот севооборот, оцениваются одновременно), чтобы реакцию конкретной культуры на данный севооборот можно было сравнивать каждый год. В этом исследовании мы сравнили долгосрочный (13 лет) эффект последовательностей с разной занятостью земель, включая все товарные культуры в севообороте. Мы предположили, что: 1) фаза культуры в момент отбора проб окажет более сильное влияние на разнообразие прокариот, чем история севооборота; 2) для конкретной последовательности культур азотное удобрение зерновых и использование озимых покровных культур окажут меньшее влияние на почвенный микробиом по сравнению с долгосрочным управлением севооборотом.
2 Материалы и методы
2.1 Место исследования и экспериментальный дизайн
Эксперимент был проведен на исследовательской станции INTA Oliveros (32° 32' ю.ш., 60° 51' з.д.), Аргентина, на глубокой, хорошо дренированной, свободной от карбонатов типичной аргиудоли (USDA Soil Taxonomy) на глубину до 240 см, с суглинисто-пылеватой текстурой в поверхностном горизонте (глина 209 г кг−1, ил 708 г кг−1, песок 83 г кг−1) и преобладанием иллита в глинистой фракции, pH 6 (1/2,5 почва/вода), ЕКО 19,4 смольc кг−1. Климат влажный умеренный со среднегодовой температурой 17,6°C и среднегодовым количеством осадков 1042 мм. Осадки выпадают в основном осенью и весной, в то время как в летние месяцы обычно наблюдаются дефициты различной интенсивности в агроклиматическом балансе.
Долгосрочный эксперимент с нулевой обработкой почвы был заложен в 2006 году для оценки последовательностей культур с разной интенсивностью выращивания зерновых и сои. Территория находилась под возделыванием в течение последних 50 лет и под нулевой обработкой в течение последних 8 лет перед началом эксперимента. Эксперимент был организован по схеме рандомизированных полных блоков с тремя повторностями, каждая экспериментальная единица имела размер 13 м в ширину × 50 м в длину. Обработки включали комбинацию последовательностей культур и уровней азотного удобрения на зерновых. Каждая фаза со своей соответствующей практикой интенсификации (обработки азотными удобрениями или покровными культурами) возделывалась одновременно каждый год. Этот отличительный подход выделяет данное исследование среди других в этой области.
Последовательности культур были следующими: (i) монокультура сои (S-S); (ii) кукуруза-пшеница/соя (M-W/S) и (iii) кукуруза-соя-пшеница/соя (M-S-W/S). В обоих случаях (ii) и (iii) было протестировано включение озимой покровной культуры (CC): (iv) озимая покровная культура/кукуруза-пшеница/соя (CC/M-W/S) и (v) кукуруза-озимая покровная культура/соя-пшеница/соя (M-CC/S-W/S) и озимая покровная культура/кукуруза-соя-пшеница/соя (CC/M-S-T/S). Озимые покровные культуры включали вику мохнатую (Vicia villosa), высеваемую перед кукурузой и уничтожаемую в фазе середины цветения с помощью 3 л га−1 глифосата (48% действующего вещества).
Две нормы азотных удобрений были оценены в последовательностях, включающих зерновые (пшеницу или кукурузу). Эти нормы азотных удобрений были рассчитаны путем измерения содержания азота в почве при посеве как N-NO3 на глубине 60 см, которое вычиталось из порогового значения доступного азота (N-NO3 на 60 см + азот удобрений), установленного для двух целевых уровней урожайности зерна: порог 160 и 190 кг N га−1 для урожайности зерна выше и ниже 10000 кг га−1 для кукурузы (Salvagiotti et al., 2011; Correndo et al., 2021) и порог 92 и 135 кг N га−1 для урожайности зерна выше и ниже 5000 кг га−1 для пшеницы (Salvagiotti et al., 2004; Ferrari et al., 2010). Последовательности, которые получали низкие и высокие нормы азотных удобрений на зерновых, в дальнейшем обозначаются как LNF и HNF соответственно. Таким образом, эксперимент включал в общей сложности 4 последовательности, включающие зерновые, в сочетании с 2 рекомендациями по азотным удобрениям, а также монокультуру сои в качестве контроля.
Общее управление осуществлялось так, как обычно делают фермеры в регионе, для борьбы с вредителями и сорняками. Все фазы каждого севооборота присутствовали каждый год. При посеве соя была инокулирована Bradyrhizobium sp. и удобрена 70 кг га−1 тройного суперфосфата. Кукуруза и пшеница были удобрены при посеве 80 кг га−1 моноаммонийфосфата. Покровные культуры не получали удобрений.
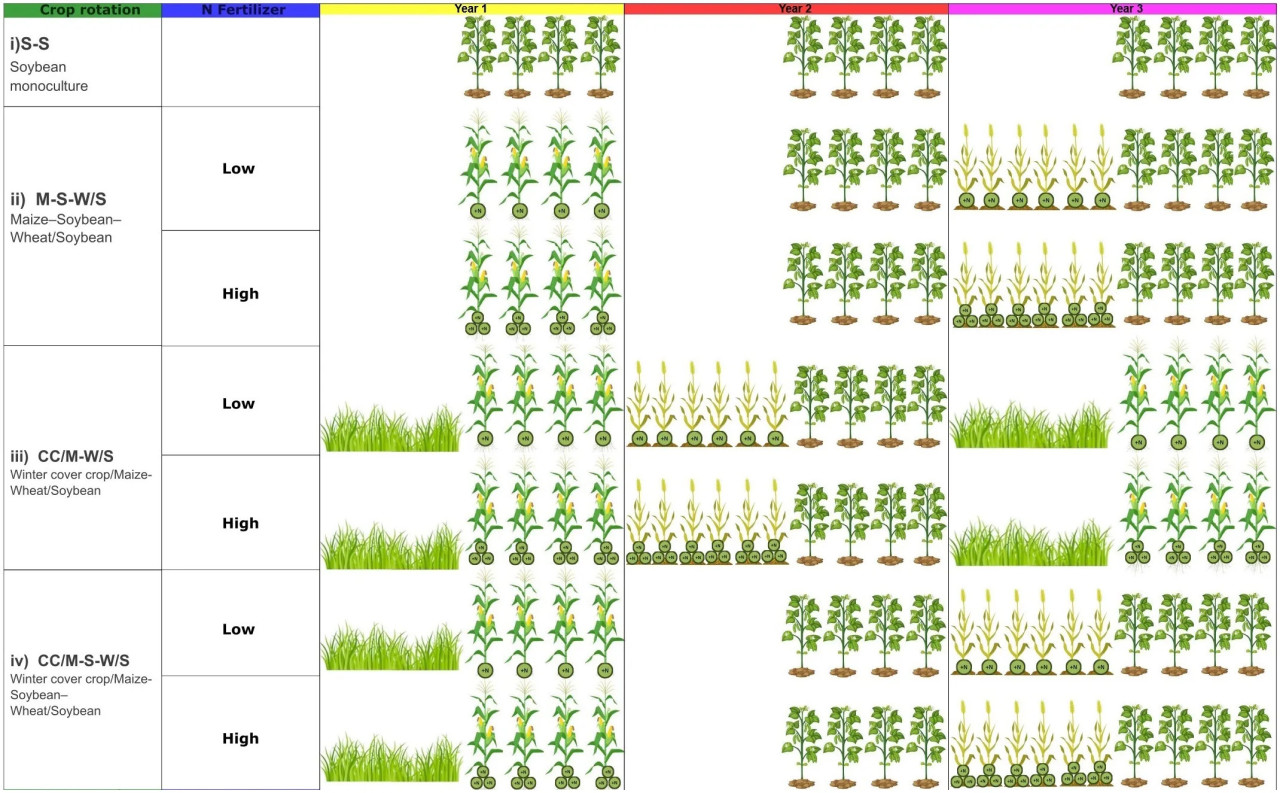
Индекс последовательности интенсификации (ISI), который выражает относительное количество дней в году, занятых культурами в данной последовательности культур, был рассчитан как отношение между количеством дней с культурами в каждой последовательности культур и продолжительностью последовательности (Caviglia and Andrade, 2010). С учетом реального времени, занятого культурами в каждой последовательности, были установлены следующие ISI: 0,39, 0,65, 0,55, 0,8 и 0,64 для S-S, M-W/S, M-S-W/S, CC/M-W/S и M-CC-S-W/S соответственно (Рисунок 1; Таблица 1).
Рисунок 1 Схема последовательности культур. При наличии зерновых культур два уровня азота, низкий и высокий, применялись к севообороту (LNF и HNF соответственно). Эксперимент начался в 2006 году, а отбор почвенных образцов был проведен после трех полных циклов севооборота в 2019 году после уборки летних культур: кукурузы, сои, пшеницы/сои. Поскольку самый длинный севооборот имеет продолжительность три года, графическая схема охватывает три года.
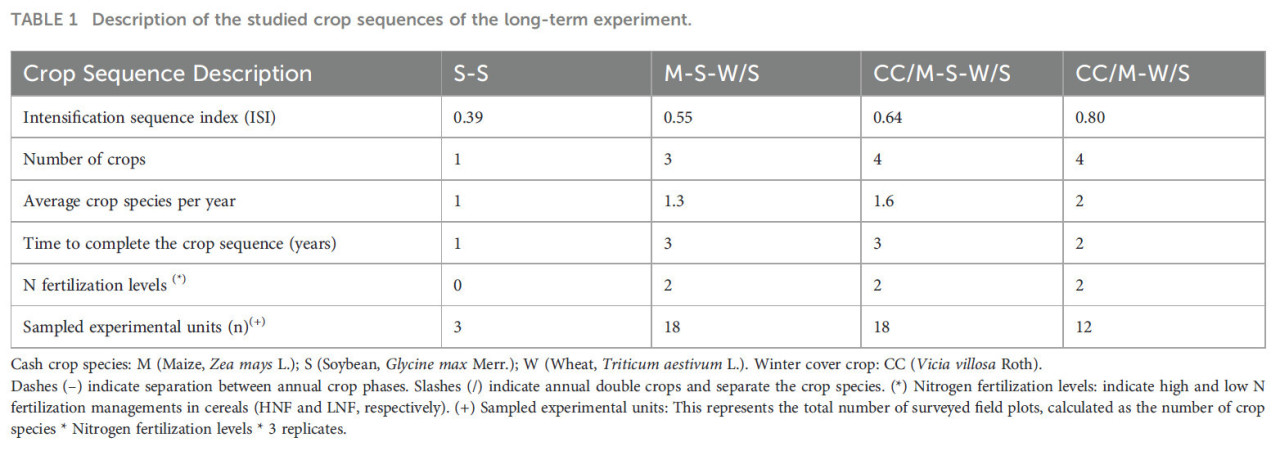
Таблица 1 Описание изученных последовательностей культур в долгосрочном эксперименте.
Виды товарных культур: M (кукуруза, Zea mays L.); S (соя, Glycine max Merr.); W (пшеница, Triticum aestivum L.). Озимая покровная культура: CC (Vicia villosa Roth).
Тире (–) указывает на разделение между годовыми фазами культур. Косые черты (/) указывают на годовые двойные посевы и разделяют виды культур. () Уровни азотного удобрения: указывают на высокий и низкий уровень управления азотными удобрениями на зерновых (HNF и LNF соответственно). (+) Обследованные экспериментальные единицы: Это представляет общее количество обследованных полевых делянок, рассчитанное как количество видов культур Уровни азотного удобрения 3 повторности.
2.2 Отбор почвенных образцов
В мае 2019 года (после окончания вегетационного сезона 2018-19) были отобраны почвенные образцы на глубине 0–5 см с тремя повторностями в каждой экспериментальной единице. Почвенные образцы были отобраны от летней товарной культуры в каждой фазе севооборотов, так что после уборки урожая были отобраны все культуры в каждом севообороте. Таким образом, кумулятивный эффект каждого севооборота был определен для летних товарных культур (кукуруза, соя и соя из фазы двойного посева пшеница/соя) (Рисунок 1). В дальнейшем мы используем термины «фаза культуры» и «идентичность культуры» как взаимозаменяемые для обозначения трех вышеупомянутых летних товарных культур. Аликвоты были смешаны и гомогенизированы в поле, высушены на воздухе и просеяны через сито с размером ячеек 2 мм. Часть почвенных образцов была сохранена при полевой влажности при -20°C до анализа для микробных измерений.
2.3 Выделение ДНК и секвенирование
Выделение ДНК было выполнено с использованием набора Power soil kit (MO BIO Laboratories, Inc. Carlsbad, CA) в соответствии с инструкциями производителя. Выделенная ДНК была отправлена в Европейскую молекулярно-биологическую лабораторию (EMBL, Гейдельберг, Германия) для секвенирования в 2019 году. Область V4 гена 16S рРНК, которая нацелена на бактериальные и архейные таксоны, была амплифицирована с использованием праймеров 515F (Parada et al., 2016) и 806R (Apprill et al., 2015) и платформы Illumina MiSeq. Сырые риды доступны в ENA под номером проекта PRJEB33480. Они также общедоступны на веб-сайте MGnify (https://www.ebi.ac.uk/metagenomics/) MGYS00005093.
2.4 Биоинформатический анализ
Биоинформатическая обработка ридов была выполнена с использованием QIIME 2 версии 2022.2 (Bolyen et al., 2019), адаптеры Illumina и праймеры были удалены с помощью функции 'cutadapt'. Затем была выполнена денуазированная обработка с использованием DADA2 в конвейере QIIME 2 (Callahan et al., 2016). Риды с качеством более 25 баллов и фрагменты длиннее 100 пар оснований были сохранены, и были сгенерированы ASV (варианты ампликонных последовательностей). Таксономическое присвоение каждой ASV было аннотировано с использованием модуля q2-classify-sklearn с использованием базы данных SILVA версии 13 (Quast et al., 2013), обученной для области V4 гена 16S рРНК, 515F-806R (Bokulich et al., 2018).
2.5 Статистический анализ
Данные были проанализированы и построены в R с использованием пакетов stat, agricolae, vegan, phyloseq, DESeq2 и ggplot2 (R Development Core Team, 2022). Перед анализом микробных данных каждый образец был разрежен до минимального количества ридов для коррекции усилия отбора проб с использованием подмножества бактериальных последовательностей. Индекс разнообразия Шеннона был оценен с использованием разреженных данных ASV. Пуассоновская регрессия была использована для моделирования взаимосвязи между ISI и индексом Шеннона и относительным обилием доминирующих типов. Матрицы расстояний были созданы на уровне ASV с использованием несходства Брея-Кертиса, и для этих матриц были построены ординации методом главных координат (PCoA). Влияние обработок на β-разнообразие было определено с использованием пермутационного дисперсионного анализа (PERMANOVA) с функцией adonis (Oksanen et al., 2015). Множественные сравнения с использованием PERMANOVA и поправки Бонферрони были использованы для определения различий в составе сообщества между интересующими контрастами. Для идентификации таксонов, ассоциированных с конкретным севооборотом, мы подобрали общую линейную модель (GLM) на основе отрицательного биномиального распределения с использованием функции DESeq из пакета DESeq2 в R (Love et al., 2014). DESeq2 идентифицировал таксоны (ASV), которые реагировали на каждую обработку, и какие таксоны были обогащены в каждой обработке. Мы использовали phyloseq версии 1.34.2 (McMurdie and Holmes, 2013) для визуализации относительного обилия таксонов, обусловливающих композиционные различия между обработками. Для оценки влияния интенсификации (ISI) на бактериальные типы мы использовали GLM на основе распределения Пуассона с делянкой как случайным эффектом. Когда данные были передиспергированы и условная дисперсия была выше условного среднего (т.е. обилие типов) (Bliss, 1953; Ross and Preece, 1985), мы выполнили отрицательную биномиальную регрессию с делянкой как случайным эффектом для обилия каждого типа, используя пакет MASS (Venables and Ripley, 2012).
3 Результаты
3.1 Анализ всего сообщества в ответ на идентичность культуры, интенсификацию и азотное удобрение
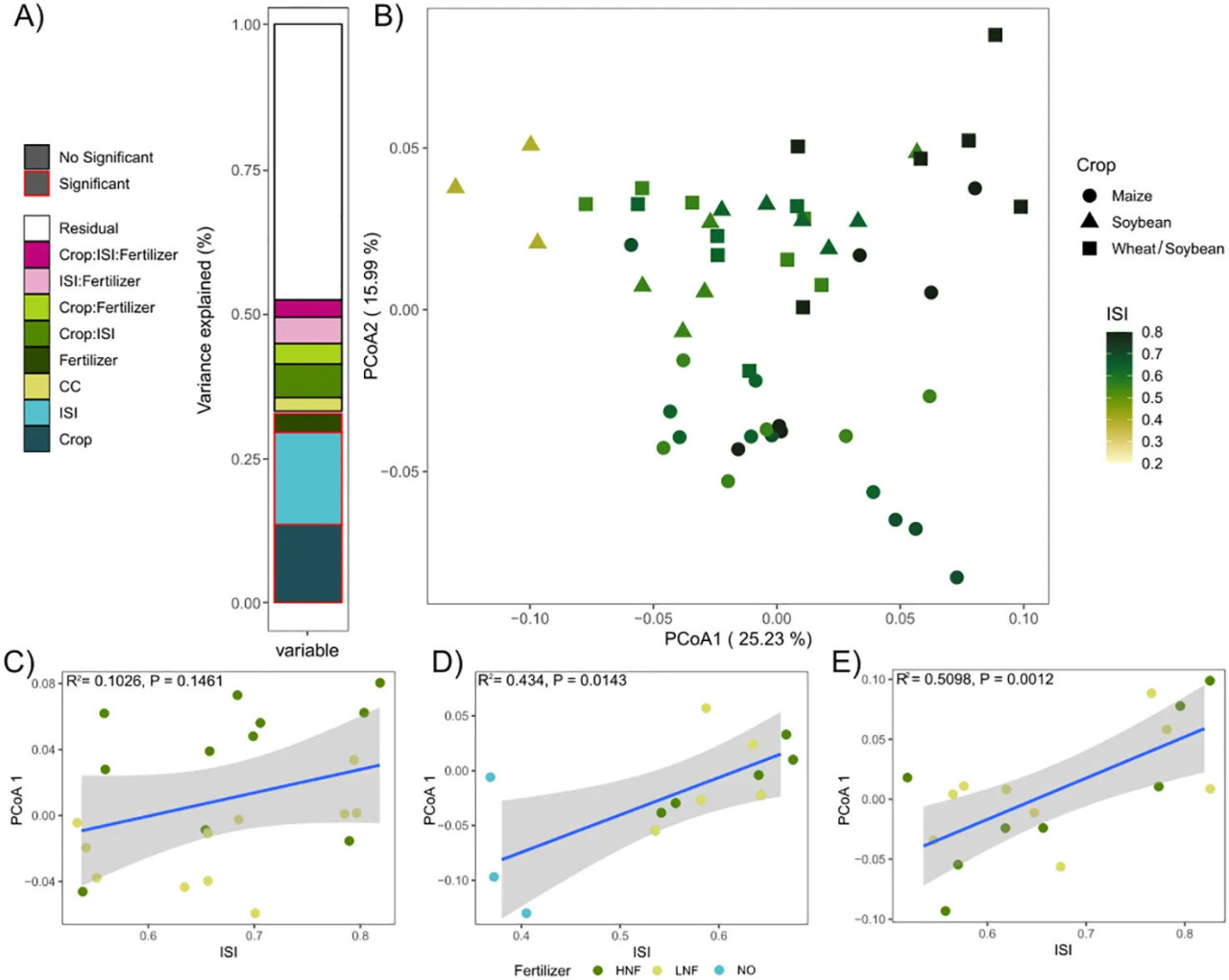
Анализ PERMANOVA показал, что ISI (P = 0,001) и идентичность культуры (P = 0,001) были наиболее сильными предикторами состава прокариотических сообществ, за которыми следовало азотное удобрение (P = 0,028), покровные культуры не были статистически значимы (Дополнительная таблица 1). Не было значимого взаимодействия между обработками (Дополнительная таблица 1; Рисунок 2A). ISI объяснял 14,7% вариации прокариотического сообщества, в то время как идентичность культуры объясняла 13,0% вариации. Не было взаимодействия между ISI и фазой культуры. Наконец, азотное удобрение и покровные культуры объясняли 3,12% и 2,33% соответственно (Дополнительная таблица 1; Рисунок 2A). Ординации методом главных координат (PCoA) на основе несходства Брея-Кертиса для структуры почвенного прокариотического сообщества показали, что фазы культур распределялись вдоль оси PCoA 2, при этом и соя, и соя из двойного посева пшеница/соя находились на положительных значениях, а кукуруза — на отрицательных значениях оси 2 (Рисунок 2B). Примечательно, что можно наблюдать влияние интенсификации на состав прокариотического сообщества вдоль оси PCoA 1: образцы с меньшей интенсификацией располагались на отрицательных значениях, а образцы с большей интенсификацией — на положительных значениях (Рисунок 2B). Не было обнаружено значимой ассоциации между осью PCoA 1 и ISI для кукурузы, но значимые взаимосвязи были показаны для фаз сои и пшеницы/сои (Рисунки 2C–E). Напротив, не было эффекта от покровных культур (Дополнительный рисунок 1A), и азотное удобрение оказало сильное влияние на фазу кукурузы, но не на фазы сои и пшеницы/сои (Дополнительный рисунок 1B; Дополнительная таблица 2).
Рисунок 2 (A) Дисперсия, проанализированная с помощью теста PERMANOVA. (B) Ординации методом главных координат (PCoA) на основе несходства Брея-Кертиса для состава почвенного прокариотического сообщества. График PCoA показывает характер распределения микробных сообществ среди различных культур и для индекса последовательности интенсификации (ISI). Взаимосвязь между ISI и осью PCoA1 в различных фазах культур (C) Кукуруза, (D) Соя и (E) Пшеница/Соя; окрашено по уровню удобрения.
3.2 α-разнообразие прокариот в ответ на интенсификацию культур
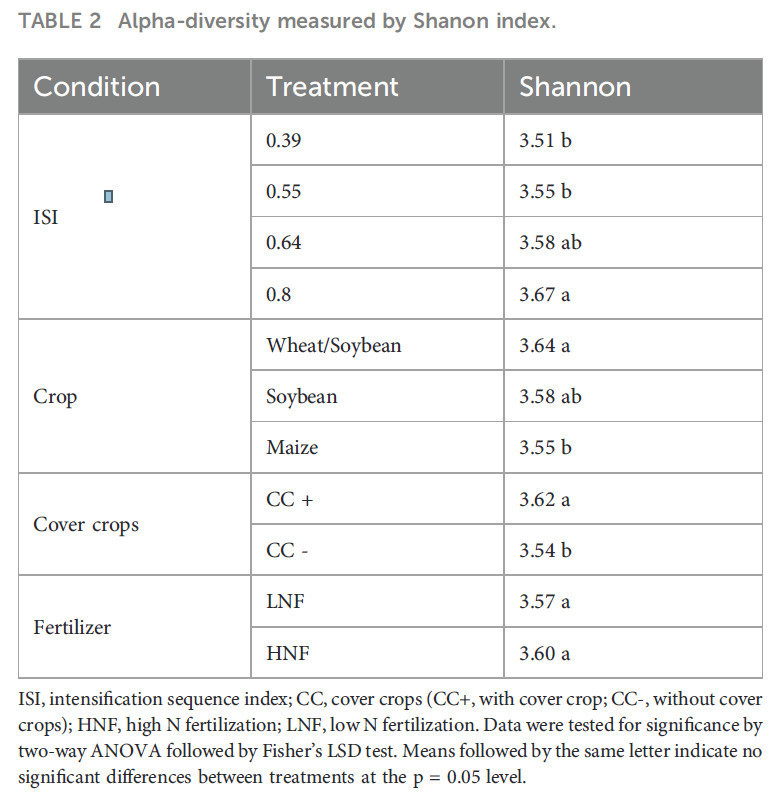
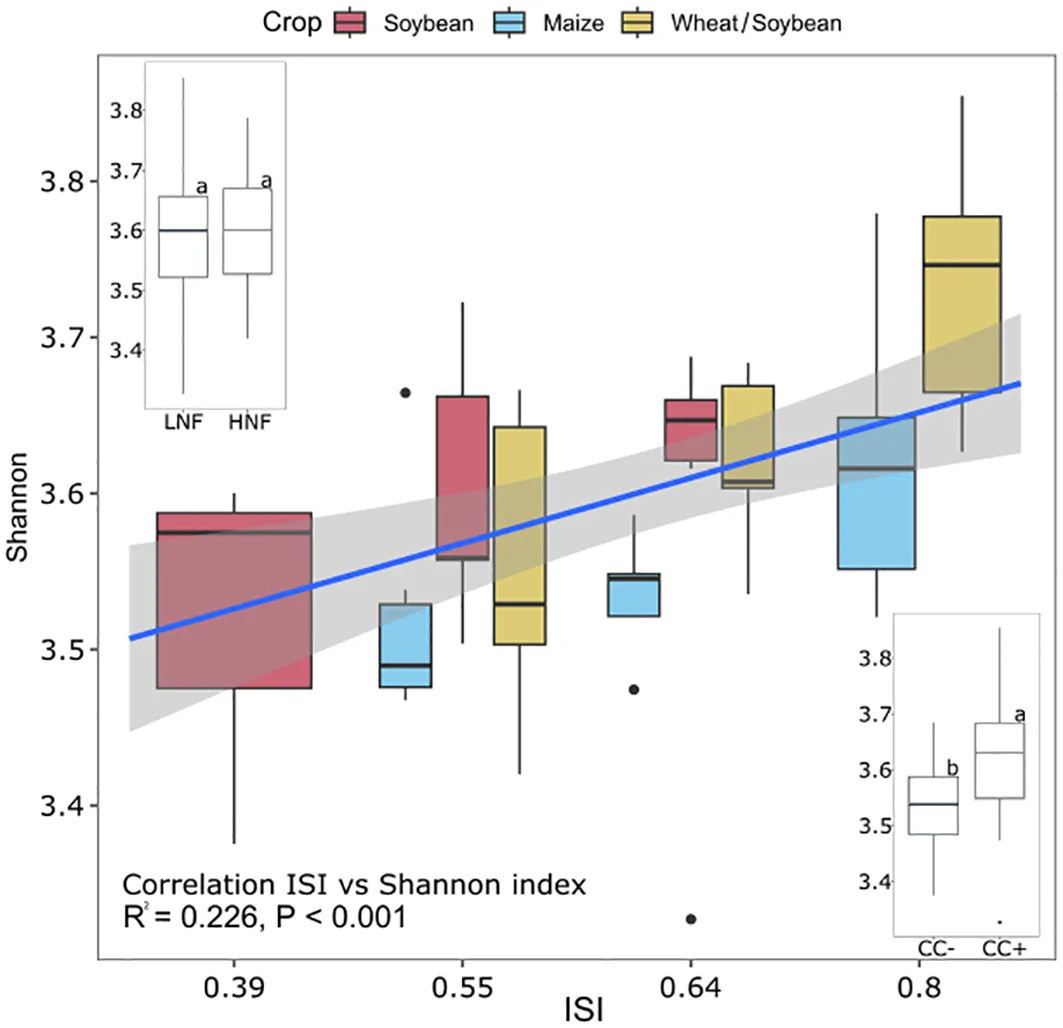
α-разнообразие для почвенного бактериального/архейного сообщества на основе индекса Шеннона показало различия для фазы культуры (P < 0,05) и покровных культур (P < 0,01) (Таблица 2), но не для азотного удобрения (P > 0,05) (Таблица 2). Двойные посевы пшеницы/сои в среднем составили 3,64 и были значительно выше, чем у кукурузы. При усреднении по всем севооборотам включение покровных культур увеличило α-разнообразие на 10% для трех культур (Рисунок 3, вставка). Наконец, разнообразие Шеннона увеличивалось с интенсификацией (ISI) для кукурузы (P = 0,039) и пшеницы/сои (P = 0,005) (Рисунок 3). Модель линейной регрессии между значением ISI и α-разнообразием показала значительную корреляцию (R2 = 0,226, P < 0,001) (Рисунок 3). В частности, мы обнаружили, что значение ISI и α-разнообразие были значительно скоррелированы для сои (R2 = 0,30, P = 0,002) и двойного посева пшеницы/сои (R2 = 0,24, P = 0,002), но не для кукурузы (R2 = 0,05, P = 0,162) (Рисунок 3).
Таблица 2 α-разнообразие, измеренное индексом Шеннона.
ISI, индекс последовательности интенсификации; CC, покровные культуры (CC+, с покровной культурой; CC-, без покровной культуры); HNF, высокое азотное удобрение; LNF, низкое азотное удобрение. Данные были проверены на значимость с помощью двухфакторного дисперсионного анализа (ANOVA) с последующим LSD-тестом Фишера. Средние значения, за которыми следует одна и та же буква, указывают на отсутствие значимых различий между обработками на уровне p = 0,05.
Рисунок 3 α-разнообразие микробного сообщества, измеренное индексом Шеннона для каждого индекса последовательности интенсификации (ISI), азотного удобрения и покровной культуры. Планки погрешностей указывают стандартную ошибку. Линия представляет линейную корреляцию между ISI и индексом Шеннона. Данные были проверены на значимость с помощью GLM ANOVA с последующим LSD-тестом Фишера. Буквы представляют значимые различия между обработками на уровне p = 0,05.
3.3 Структура прокариотического сообщества и реакция на интенсификацию культур и севооборот
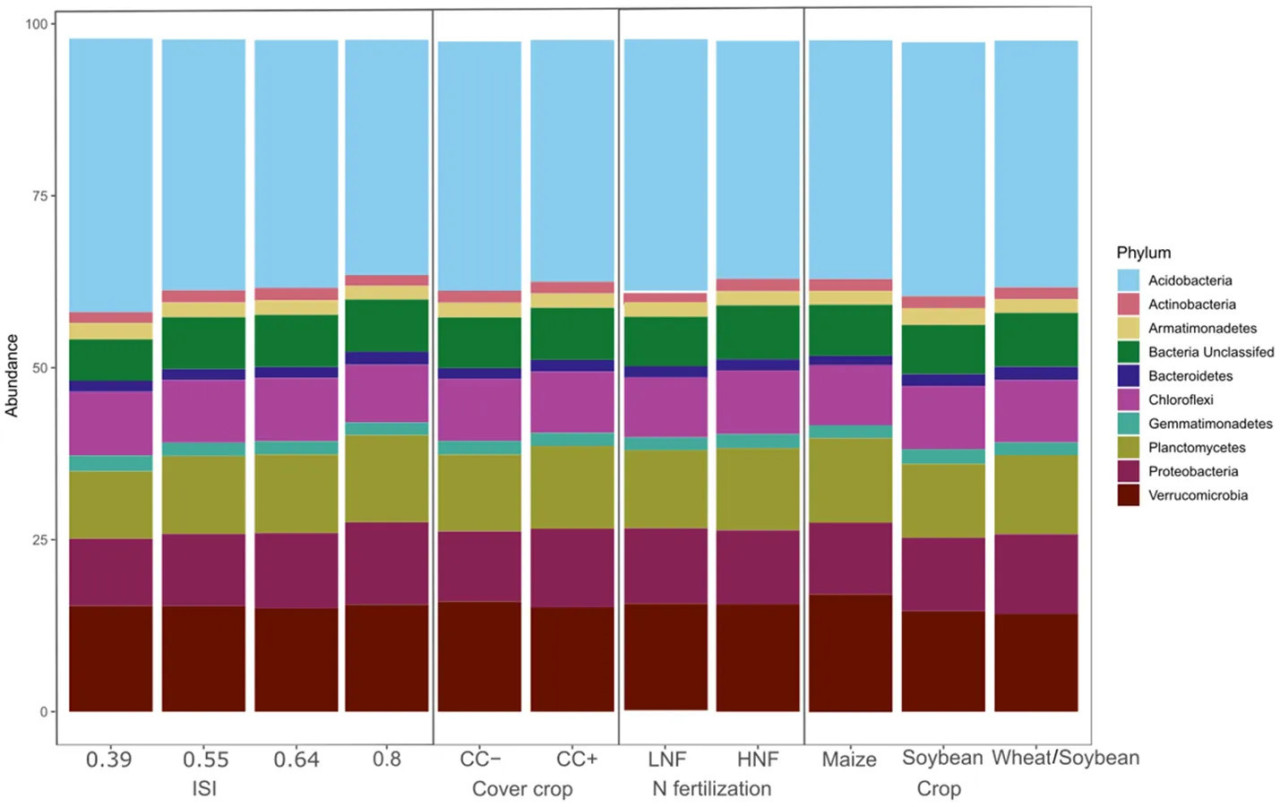
Из этой почвы было выделено в общей сложности 79 типов. Acidobacteria составляли большинство восстановленных ридов 16S рРНК (35,75% ± 3,11%), за ними следовали Verrucomicrobia (15,64% ± 2,37%), Planctomycetes (11,57% ± 1,45%), Proteobacteria (10,79% ± 1,36%) и Chloroflexi (8,90% ± 1,14%) (Рисунок 4). Вместе эти пять типов составляли более 80% последовательностей. Соя значительно увеличила обилие Acidobacteria (P = 0,037) и Armatimonadetes (P < 0,001), в то время как последовательности, содержащие сою, и двойной посев пшеницы/сои увеличили обилие Bacteroidetes (P < 0,001). Напротив, кукуруза значительно увеличила обилие Planctomycetes (P = 0,002) и Verrucomicrobia (P < 0,001). Наконец, Proteobacteria показали эффект взаимодействия между фазой культуры и азотным удобрением, будучи более обильными в двойном посеве пшеницы/сои в обоих случаях (P < 0,05). Мы отметили увеличение Chloroflexi, Gemmatimonadetes и Thaumarchaeota при HNF, в то время как Acidobacteria и Nitrospirae были более обильными при LNF (P < 0,05). Наконец, покровные культуры значительно увеличили обилие Proteobacteria (P < 0,05) (Рисунок 4).
Рисунок 4 Прокариотический состав на уровне типа в почве с различными севооборотами, покровными культурами, азотным удобрением и интенсификацией. Прокариотический состав на уровне типа (относительное обилие) в почве с различными индексом последовательности интенсификации (ISI), покровной культурой (CC-, CC+), азотным удобрением (LNF и HNF), культурой (кукуруза, соя, пшеница/соя).
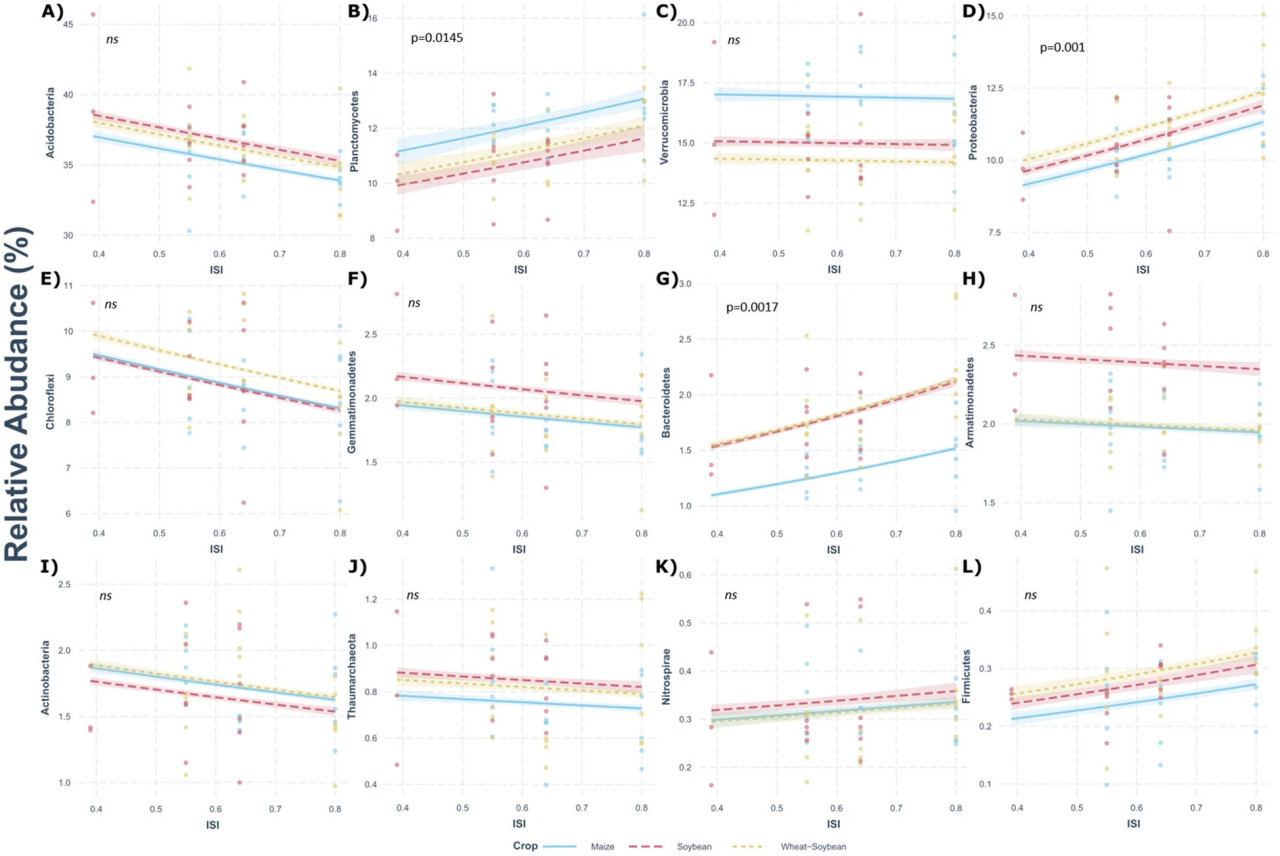
Мы проанализировали влияние IRI на различные типы с использованием модели пуассоновской регрессии для каждого севооборота и различных фаз каждого севооборота (Рисунок 5). Planctomycetes (R2 = 0,37, P = 0,0145), Proteobacteria (R2 = 0,51, P = 0,00108) и Bacteroidetes (R2 = 0,36, P = 0,0170) показали положительную взаимосвязь с ISI (Рисунки 5). Двойной посев пшеницы/сои показал высокое количество реагирующих на интенсификацию культур типов, демонстрируя положительную корреляцию с Planctomycetes (R2 = 0,27, P = 0,00168) и Bacteroidetes (R2 = 0,29, P = 0,0296), в то время как для кукурузы обилие Proteobacteria (R2 = 0,31, P = 0,00677) положительно коррелировало с ISI. Наконец, обилие Acidobacteria, Verrucomicrobia, Armatimonadetes, Chloroflexi, Gemmatimonadetes и Thaumarchaeota отрицательно коррелировало, но не значительно, с ISI, в то время как обилие Nitrospirae и Firmicutes положительно коррелировало, но не значительно, с ISI.
Рисунок 5 Взаимосвязь пуассоновской регрессии между относительным обилием (%) доминирующих типов для (A) Acidobacteria, (B) Planctomycetes, (C) Verrucomicrobia, (D) Proteobacteria, (E) Chloroflexi, (F) Gemmatimonadetes, (G) Bacteroidetes, (H) Armatimonadetes, (I) Actinobacteria, (J) Thaumarchaeota, (K) Nitrospirae и (L) Firmicutes и индексом последовательности интенсификации (ISI). Показаны значения значимости p регрессии; ns — не значимо.
3.4 Структура прокариотического сообщества и реакция на идентичность культуры
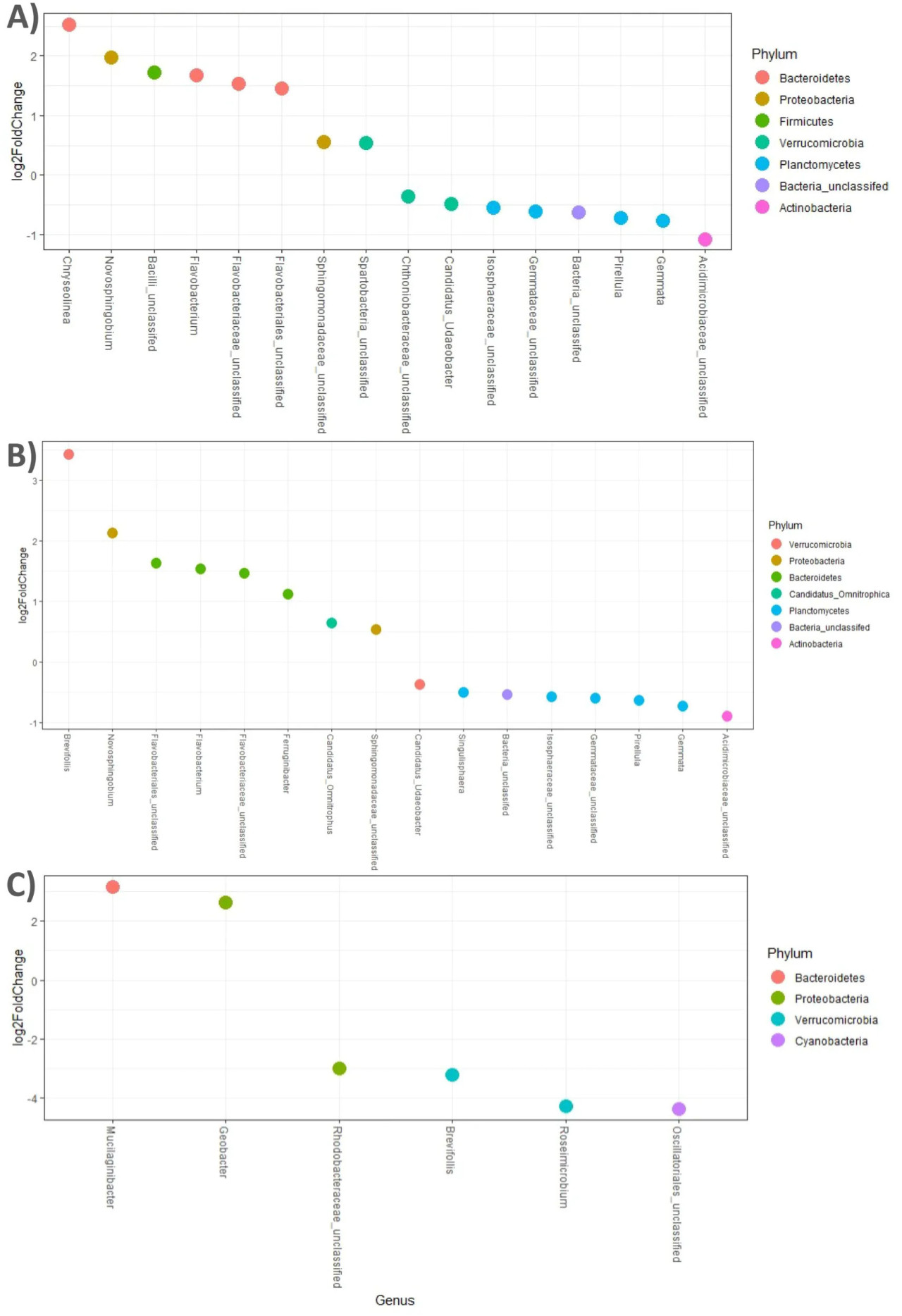
Мы использовали анализ дифференциального обилия DESeq2 (alpha = 0,001), чтобы определить, какие таксоны различались по присутствию и обилию среди почв, обусловленных различными видами растений, включенными в различные севообороты. Анализ DESeq2 показал, что кукуруза обогащала обилие Gemmata, Singulisphaera и Pirellula (оба Planctomycetes) и других неклассифицированных таксонов, принадлежащих к Planctomycetes (точки ниже 0 на графике представляют таксоны, обогащенные в кукурузе) по сравнению с соей и двойным посевом пшеницы/сои (Рисунки 6A, B). Двумя другими таксонами, обогащенными в кукурузе, были Acidimicrobiaceae неклассифицированные (тип: Actinobacteria) и Candidatus Udeobacter (тип: Verrucomicrobia). Напротив, соя обогащала обилие Flavobacterium и Chryseolinea (оба Bacteroidetes) и других неклассифицированных Bacteroidetes (точки выше 0 на графике) (Рисунки 6A, B). Другими таксонами, увеличенными в посевах сои, были Novosphingobium, Sphingomonadaceae неклассифицированные (тип: Proteobacteria; класс: Alpha-proteobacteria) и Spartobacteria неклассифицированные (Verrucomicrobia) (Рисунки 6A, B). Сравнение между соей и двойным посевом пшеницы/сои показало немного дифференциальных таксонов. Соя обогащала Mucilaginibacter (тип: Bacteroidetes) и Geobacter (тип: Proteobacteria, класс: Delta-proteobacteria) (оба выше 0 на графике), в то время как пшеница/соя обогащала Brevifollis и Roseimicrobium (тип: Verrucomicrobia) (ниже 0 на графике) (Рисунок 6C).
Рисунок 6 Дифференциальная представленность значимых ASV по обилию на уровне рода между севооборотами (A) Соя vs. Кукуруза, (B) Пшеница/Соя vs. Кукуруза и (C) Соя vs. Пшеница/Соя. Точки представляют значимо обильные ASV, окрашены по типу и обозначены по роду. Множественные точки на род представляют различные виды данного рода. Показаны только вероятности.
4 Обсуждение
Мы оценили прокариотическое сообщество с использованием высокопроизводительного секвенирования гена 16S рРНК в почвах, на которых выращивались три товарные культуры (пшеница, соя и кукуруза), в условиях контрастного управления интенсификацией в рамках долгосрочного экспериментального испытания. В этом исследовании непосредственный эффект трех товарных культур был оценен одновременно в каждом севообороте, что позволило нам оценить изолированное влияние каждой фазы в севообороте на микробные сообщества. Наши результаты показали, что как фаза культуры, так и интенсификация культур, измеряемая индексом последовательности интенсификации (ISI), оказали сходное влияние на структуру почвенного прокариотического микробиома. Кроме того, наши результаты показали небольшое, но значимое влияние азотного удобрения на прокариотическое сообщество. Между тем, покровные культуры показали незначимый эффект на структуру сообщества, но заметно увеличили α-разнообразие.
4.1 Влияние идентичности культуры на почвенное бактериальное сообщество
Почвенное биоразнообразие имеет ключевое значение для поддержания и улучшения экологических функций почвы (Bender et al., 2016). Бактериальное/архейное богатство, измеренное индексом Шеннона, показало значимые различия в зависимости от идентичности культуры (Ishaq et al., 2017). Несколько авторов показали, что пшеница увеличивает разнообразие по сравнению с другими культурами, такими как хлопок, рис и бобы (Wei et al., 2019; Granzow et al., 2017). Напротив, Ashworth et al. (2017) показали, что последовательность пшеница-соя имела значения богатства, сходные с теми, которые обнаружены либо в непрерывной монокультуре кукурузы, либо в непрерывной монокультуре сои.
Прокариотическое сообщество является ключевым компонентом почвенной экосистемы и может быть использовано для оценки здоровья почвы и растений (Sharma et al., 2010). В этом исследовании мы обнаружили явное и значимое различие в составе почвенного прокариотического сообщества между кукурузой, соей и пшеницей/соей, как ранее сообщалось Li et al. (2017). Это явление может быть в первую очередь обусловлено различной реакцией микроорганизмов на количество и качество корневых экссудатов или ризодепозиции, вызванных культурами (Costa et al., 2006). Мы обнаружили представителей Planctomycetes (Gemmata, Singulisphaera и Pirellula), Actinobacteria (Acidimicrobiaceae) и Verrucomicrobia (Candidatus Udeobacter), ассоциированных с кукурузой. Gemmata и Pirellula были ассоциированы с круговоротом азота, особенно с денитрификацией (Han et al., 2019). Однако Gemmata была связана с деградацией остатков пшеницы (Zhou et al., 2018). Напротив, как соя, так и двойной посев пшеницы/сои привели к активному увеличению Alpha-proteobacteria (Novosphingobium) и Bacteroidetes (Flavobacterium и Chryseolinea), оба из которых считаются копиотрофами (Fierer et al., 2007; İnceoğlu et al., 2011).
Соя была в основном обогащена Bacteroidetes, что может быть согласовано с тем, что соя имеет более высокую ризодепозицию, чем кукуруза (Qiao et al., 2017; Mazzilli et al., 2015). Ризодепозиты сои имеют более низкое соотношение C/N, чем у кукурузы, и быстро минерализуются микроорганизмами, что, вероятно, ответственно за больший сдвиг в бактериальном сообществе (Miao et al., 2021). Bacteroidetes обычно ассоциируются с почвами, богатыми азотом и легкодоступными питательными веществами (Liu et al., 2017). Например, роды Flavobacterium и Chryseobacterium были ассоциированы со стимуляцией роста растений и защитой от болезней (de Sousa Lopes et al., 2021). Двойной посев пшеницы/сои был обогащен Brevifollis и другими таксонами Verrucomicrobia, где этот тип чрезвычайно чувствителен к изменениям химических факторов, связанных с плодородием почвы, в коренных лесах или на лугах (Lupwayi et al., 2020; Stefan et al., 2021).
4.2 Влияние индекса интенсификации на почвенное бактериальное сообщество
Сельскохозяйственные практики в рамках парадигмы устойчивой интенсификации разработаны для сохранения почвы, повышения продуктивности культур и здоровья почвы (Bommarco et al., 2013). Предыдущие исследования показали положительный эффект этого сельскохозяйственного управления на экосистемные сервисы, такие как урожайность (Bowles et al., 2020; Gaudin et al., 2015), запасы органического углерода (Tamburini et al., 2020; Romaniuk et al., 2018; Beltrán et al., 2016), борьба с вредителями (Emery et al., 2021), обилие дождевых червей и мезофауны (Rodríguez et al., 2020) и выбросы закиси азота (Piccinetti et al., 2021). Исследования глобального масштаба показали, что почвенные микробиомы, особенно почвенные бактерии, формируются многими факторами (Fierer, 2017). Кроме того, Fan et al. (2020) наблюдали значимые, биологически значимые корреляции между урожайностью и обилием специфических ассоциированных с корнями микробных таксонов и функциональных генов, подчеркивая важность прокариотического сообщества в регуляции функционального потенциала почвы и продуктивности растений.
Интенсификация культур подразумевает увеличение числа культур в год и, следовательно, увеличение количества активных корней в течение года и количества углерода, поступающего в почву. Здесь увеличение индекса последовательности интенсификации (ISI) показало положительный эффект на биоразнообразие, измеренное индексом Шеннона, для всех трех культур, в основном для кукурузы и двойного посева пшеницы/сои. Venter et al. (2017) провели мета-анализ, который показал, что примерно 15,1% и 3,4% микробного богатства и разнообразия соответственно были увеличены в обработках с севооборотом по сравнению с монокультурами. Другие исследования показали, что интенсификация управления оказывает значимое влияние (Bender et al., 2016; Garland et al., 2020) или непостоянное влияние на биоразнообразие (Stefan et al., 2021). Увеличение числа бобовых культур каждый год улучшает поступление азота за счет биологической фиксации азота и растительных остатков (Lal, 2017). Кроме того, Romaniuk et al. (2018) и Beltrán et al. (2016) продемонстрировали, что восьми лет после принятия адекватной интенсификации было достаточно для накопления более лабильного углерода и макроэлементов в стабильных отложениях углерода. Как запасы углерода, так и запасы азота могут способствовать увеличению бактериального разнообразия почвы (Garland et al., 2021; Zak et al., 2003).
В этом исследовании мы обнаружили, что относительное обилие нескольких бактериальных и архейных типов было значительно изменено ISI. В целом, некоторые копиотрофные бактерии, такие как Proteobacteria, Firmicutes, Planctomycetes и Bacteroidetes, соответствовали экологической теории о том, что копиотрофное поведение (или r-стратегии) хорошо адаптировано к богатым питательными веществами условиям и положительно реагирует на интенсификацию (Li et al., 2014). Firmicutes и Bacteroidetes могут использовать аммоний или нитрат в качестве единственного источника азота (Ashworth et al., 2017; Frene et al., 2022). Напротив, Actinobacteria — это группа, которая была обнаружена в большей пропорции на лугах (Liao et al., 2023) и на которую негативно влияет нарушение почвы (Gou et al., 2024). Изменения в структуре микробного сообщества были ассоциированы с надземными процессами, связанными с разнообразием и составом культур (Delgado-Baquerizo et al., 2018).
В отличие от копиотрофных микроорганизмов, относительное обилие олиготрофных групп (например, Acidobacteria, Chloroflexi, Gemmatimonadetes и Armatimonadetes) значимо не реагировало на интенсификацию культур. Acidobacteria — это хорошо известная группа, которая процветает в кислых, бедных питательными веществами почвах и не реагирует эффективно на увеличение поступления углерода от дополнительной биомассы растений (Fierer et al., 2007; Kalam et al., 2020). Представители Chloroflexi были идентифицированы как патогенные бактерии (DeBruyn et al., 2011), которые не могут реагировать на интенсификацию культур из-за положительного влияния севооборота на здоровье культур (Custódio et al., 2022). Наконец, было сообщено, что Gemmatimonadetes и Armatimonadetes отрицательно реагируют на запасы углерода и фосфора в почве (Gou et al., 2024), и в настоящем исследовании оба типа отрицательно реагировали на интенсификацию культур. Эти результаты указывают на то, что интенсификация культур может вызвать сдвиг в стратегии жизненного цикла.
4.3 Влияние поступления азота на почвенное прокариотическое сообщество с помощью удобрений и покровных культур
Наши результаты выявили дифференциальный эффект между азотным удобрением и покровными культурами: хотя азотное удобрение значительно изменило структуру прокариотического сообщества, покровные культуры увеличили индекс α-разнообразия. Увеличение микробного разнообразия, ассоциированное с покровными культурами, было связано с более высокой активностью ферментов почвы и доступностью азота и фосфора, напрямую влияя на круговороты углерода и азота в почве (Chavarria et al., 2018; Kim et al., 2020; McClelland et al., 2021). Kim et al. (2020) обнаружили, что покровные культуры значительно увеличили биомассу, активность и разнообразие почвенных микробных сообществ. Однако наблюдаемый небольшой эффект озимых покровных культур на состав почвенного прокариотического сообщества в нашем исследовании может быть связан со временем отбора проб; наши образцы были собраны после уборки летних товарных культур. Согласно Liu et al. (2021), влияние покровных культур на состав микробного сообщества определяется не только идентичностью товарных и покровных культур, но и периодом сбора. Напротив, азотное удобрение показало незначительное, но существенное влияние на структуру состава сообщества (Li et al., 2018). Этот эффект наблюдался в основном на обработках с кукурузой, вероятно, потому что соя не получает азотных удобрений (Castle et al., 2021). Было документально подтверждено, что азотное удобрение изменяет обилие доминирующих бактериальных типов (Dai et al., 2018; Nguyen et al., 2018; Viso et al., 2024). Наши результаты выявили заметное снижение обилия Acidobacteria и Nitrospirae, которые, как известно, используют олиготрофную стратегию роста, менее благоприятную в удобренных почвах (Legrand et al., 2018; Ramirez et al., 2016).
5 Выводы
Наши результаты показали, что как интенсификация, так и фаза культуры влияли на состав почвенного прокариотического сообщества после тринадцати лет (2006-2019) интенсификации управления почвой. Кроме того, покровные культуры и азотные удобрения могли оказать ограниченное влияние на структуру и разнообразие почвенного бактериального/архейного сообщества. Бактериальные типы, ассоциированные с копиотрофными формами жизни, как оказалось, выигрывали от интенсификации, но некоторые олиготрофные типы — нет. Хотя копиотрофно/олиготрофная гипотеза является упрощенной, она предоставляет базовую основу для связывания реакции почвенных прокариотических сообществ на севообороты. Существует явная потребность в более понятных и сопоставимых данных о динамике почвенных микробиомов в агроэкосистемах, а также в их интеграции в общие модели с другими физическими, химическими и биологическими параметрами, чтобы лучше понять влияние различных и альтернативных сельскохозяйственных практик. Дальнейшие исследования определят, связана ли эта информация с продуктивностью культур и индексами здоровья почвы, способствуя оптимизации сельскохозяйственного управления и решению проблем, вызванных неподходящими практиками.
Ссылки
Frene JP, Bacigaluppo S, Maury M, Ortiz J, Rivarola M, Salvagiotti F and Faggioli V (2024) Crop-specific response of soil prokaryotic community to long-term intensification management: the importance of crop phase at sampling. Front. Agron. 6:1446404. doi: 10.3389/fagro.2024.1446404
Перевод статьи «Crop-specific response of soil prokaryotic community to long-term intensification management: the importance of crop phase at sampling» авторов Frene JP, Bacigaluppo S, Maury M, Ortiz J, Rivarola M, Salvagiotti F and Faggioli V., оригинал доступен по ссылке. Лицензия: CC BY. Изменения: переведено на русский язык
Фото: freepik






















































































































Комментарии (0)