Как севооборот и обработка фунгицидами влияют на микробы и ферменты в корнях пшеницы
Устойчивые системы растениеводства должны способствовать формированию большой и разнообразной микробной биомассы почвы для усиления биологических почвенных процессов, а не полагаться исключительно на химические меры, включая применение пестицидов. Севооборот увеличивает временное разнообразие надземной биоты, что, по сравнению с монокультурой, обычно способствует росту микробного разнообразия почвы. Однако сравнения между короткими и длинными севооборотами, учитывающие также воздействие пестицидов, встречаются редко.
Аннотация
Было проведено пятилетнее (2013–2017) полевое исследование для изучения влияния севооборота и фунгицидов на почвенный микробиом и его активность. Изучалось девять вариантов севооборота, с применением фунгицидов или без них, включая четыре двухлетних севооборота (пшеница после канолы, ячменя, гороха или льна), четыре трехлетних севооборота (к двухлетним добавлялись ячмень или канола) и один севооборот с последовательным выращиванием канолы и пшеницы (канола-канола-пшеница-пшеница). В 2017 году измеряли микробную биомассу почвы, состав, разнообразие и ферментативную активность в ризосфере последней культуры пшеницы в каждом севообороте. Фунгициды снижали видовое богатство грибов (количество различных таксонов грибов) в ризосфере пшеницы (например, индекс Chao1: 64,0 против 79,9), особенно в двухлетних севооборотах, но продолжительность/тип севооборота и предшествовавшие пшенице культуры по-разному влияли на разные таксоны. Два из трех наиболее распространенных филумов прокариот, Proteobacteriota и Actinobacteriota, по-разному реагировали на продолжительность севооборота: трехлетние севообороты обогащали первые (относительная численность 27,4% против 20,1%), тогда как двухлетние обогащали вторые (19,9% против 28,3%). По сравнению с масличными культурами, предшествовавшими анализируемой пшенице, предшествовавший горох обогащал Actinobacteriota (относительная численность 31,7% против 24,8%) и самый многочисленный класс грибов — Sordariomycetes (39,1% против 22,1%), а также увеличивал микробную биомассу углерода (МБУ) и активность арилсульфатазы на 33% и 57% соответственно. Корреляции относительной численности родов грибов или прокариот с активностью β-глюкозидазы и арилсульфатазы были одинаковыми (как положительные, так и отрицательные), но они были противоположны корреляциям с активностью кислотной фосфомоноэстеразы, что предполагает тесную связь между циклами углерода и серы. Помимо последствий этих характеристик почвенной микробиоты для круговорота питательных веществ, необходимо изучать их значение для биологической борьбы с болезнями.
1 Введение
Устойчивое производство сельскохозяйственных культур должно сочетать биологические процессы с химическими процессами для питания и защиты растений (борьба с вредителями), вместо того чтобы заменять первые последними. К химическим мерам, основанным на химических процессах, относятся применение неорганических удобрений и пестицидов. Биологические процессы в почве в основном опосредованы почвенными микроорганизмами и включают биологическую фиксацию азота клубеньковыми бактериями, поглощение питательных веществ микоризой, круговорот питательных веществ за счет микробной разложения органических веществ, вносимых в почву, биологическую борьбу с вредителями за счет микробного хищничества и конкуренции за ресурсы, а также детоксикацию агрохимикатов. Следовательно, устойчивые системы растениеводства должны поддерживать большие и разнообразные почвенные микробные сообщества. Севооборот увеличивает временное разнообразие надземной биоты, что должно трансформироваться в подземное разнообразие (Venter и др., 2016). В глобальном мета-анализе, проведенном на 76 исследованиях, Liu и др. (2023b) сообщили, что по сравнению с монокультурой севооборот увеличил микробную биомассу углерода (МБУ) почвы на 13,43% и индекс разнообразия Шеннона бактерий на 7,68%. Похожий мета-анализ использовал 20 исследований и показал увеличение выравненности и разнообразия микробов на 15,11% и 3,36% соответственно при севообороте (Venter и др., 2016).
Приведенные выше сравнения проводились между севооборотами и монокультурами. Однако сравнений влияния разной продолжительности севооборота на почвенный микробиом не так много, как сравнений севооборота с монокультурой. Некоторые исследования показывают, что длинные (разнообразные) севообороты приводят к большему микробному разнообразию почвы, чем короткие (простые) севообороты. В Огайо Huo и др. (2023) идентифицировали восемь вариантов ампликонной последовательности бактерий (ASVs) в севообороте кукуруза-соя-пшеница, которые отсутствовали в севообороте кукуруза-соя. На Северо-Китайской равнине Liu и др. (2023a) сообщили о значительно большей относительной численности Actinobacteriota и Ascomycota (на 15% и 20-23% соответственно) в севообороте батат-озимая пшеница-летняя кукуруза по сравнению с севооборотом озимая пшеница-летняя кукуруза. Один из выводов обзора влияния севооборота на экосистемные услуги и устойчивость агроэкосистем заключался в том, что диверсифицированные севообороты повышали устойчивость к заражению вредителями/болезнями и ускоряли восстановление после заражений (Liu и др., 2022). Причины, по которым севообороты (севооборот против монокультуры или длинные против коротких севооборотов) увеличивают микробное разнообразие почвы, включают физические, химические и биологические изменения почвы, создаваемые чередуемыми культурами, например, разные корневые действия последовательных культур, которые создают разные ниши для микробной экспансии, а также накопление разных корневых экссудатов и пожнивных остатков (Venter и др., 2016). На Среднем Западе США по сравнению с традиционным севооборотом кукуруза-соя 4-летний севооборот кукуруза-соя-овес-люцерна снизил сопротивление почвы росту корней на 8% и увеличил катионообменную способность, экстрагируемый солью почвенный C и МБУ на 16%, 157% и 62% соответственно (Baldwin-Kordick и др., 2022). Требуется больше исследований коротких и длинных севооборотов, чтобы развить существующие знания.
В то время как севообороты могут способствовать формированию большой и разнообразной микробной биомассы почвы, пестициды могут оказывать неблагоприятное воздействие на микробные сообщества почвы, поскольку по определению они токсичны. В обзоре воздействия сельскохозяйственных ресурсов на почвенные организмы Bünemann и др. (2006) сообщили, что порядок пестицидов по степени негативного воздействия на почвенный микробиом был следующим: фунгициды > инсектициды > гербициды. Фунгициды оказывают прямое негативное воздействие на почвенный микробиом, поскольку они токсичны для грибов, но они также могут оказывать косвенное воздействие на другие микроорганизмы через трофические связи, например, на бактерий, которые питаются грибами, убитыми фунгицидом, за счет использования ресурсов, ранее использовавшихся убитыми грибами, и за счет привлечения бактерий, разлагающих фунгициды (Han и др., 2021; Meyer и др., 2024). Han и др. (2021) сообщили об увеличении на 42-3500% родов бактерий, разлагающих тебуконазол, при обработке фунгицидом тебуконазол по сравнению с контролем. Однако в обзоре токсического воздействия тебуконазола на почвенную микробиоту Roman и др. (2021) отметили, что большинство исследований сообщали об умеренных, а иногда и преходящих, дозозависимых эффектах на микробную биомассу и разнообразие почвы. Riedo и др. (2023) сообщили о сходных результатах в микрокосмном эксперименте с оценкой трех фунгицидов в трех почвах. Необходимы исследования, сочетающие продолжительность севооборота и влияние фунгицидов на почвенный микробиом, чтобы выявить любые интерактивные эффекты.
Цель этого исследования была направлена на оценку того, как севообороты и применение фунгицидов влияют на микробную биомассу почвы, состав и разнообразие сообществ прокариот (бактерий и архей), а также на ферментативную активность в ризосфере пшеницы, которая была последней культурой в каждом севообороте. В отношении севооборотов мы в частности исследовали, как продолжительность севооборота и культуры, предшествовавшие конечной культуре пшеницы, повлияли на свойства почвенной микробиоты.
Схема эксперимента была инновационной, потому что (a) она не включала монокультуры, (b) она включала последовательный севооборот (канола-канола-пшеница-пшеница), и (c) культуры возделывались по технологии No-till. Все эти три аспекта севооборотов отражали распространенные методы в районе исследования.
2 Материалы и методы
2.1 Экспериментальный участок, схема и управление
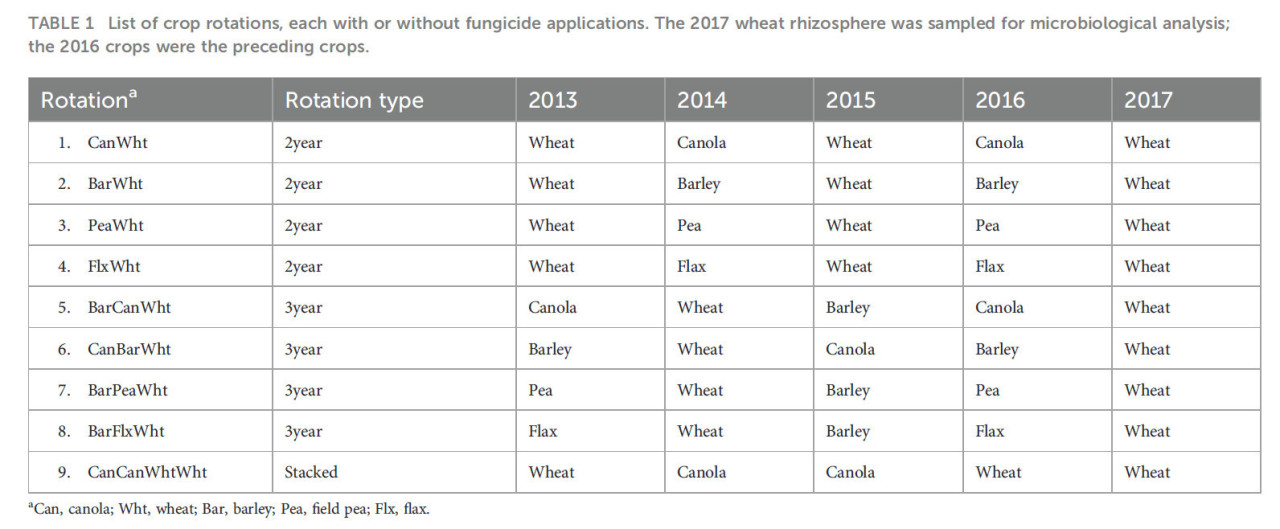
Пятилетнее полевое исследование проводилось с 2013 по 2017 год в Исследовательском и опытно-конструкторском центре Lacombe (113°45’ з.д., 52°27’ с.ш.), Альберта, Канада, с годовым количеством осадков 533 мм и среднегодовой температурой 3,5°C. Почва представляла собой суглинок (51% песка, 30% ила и 19% глины) чернозем (Typic Haplustoll в Таксономии почв) с pH 6,6 и содержанием органического C 45,2 г кг-1. Было девять севооборотов, с применением фунгицидов или без них, расположенных в рандомизированной полной блочной схеме с четырьмя повторностями (Таблица 1). Они включали четыре 2-летних севооборота (канола-пшеница, ячмень-пшеница, горох-пшеница и лен-пшеница), четыре 3-летних севооборота, где ячмень или канола были добавлены к 2-летним севооборотам (ячмень-канола-пшеница, канола-ячмень-пшеница, ячмень-горох-пшеница и ячмень-лен-пшеница), и один севооборот, где канола и пшеница были последовательно (канола-канола-пшеница-пшеница). В 2017 году во всех севооборотах была посеяна пшеница, конечная культура, которая была отобрана для оценки каждого севооборота. Таким образом, в дополнение к оценке севооборотов с точки зрения продолжительности/типа (2-летние, 3-летние или последовательные), также оценивалось влияние культуры, предшествующей пшенице (канола, ячмень, горох или лен) (Таблица 1).
Таблица 1 Список севооборотов, каждый с применением фунгицидов или без них. Для микробиологического анализа отбирали ризосферу пшеницы 2017 года; культуры 2016 года были предшествующими культурами.
Для обработки фунгицидами применяемые фунгициды зависели от культуры. На зерновых культурах применялся фунгицид protioconazole+tebucanzole для борьбы с фузариозом колоса в виде Prosaro 250 EC (Bayer, 125 г протиоконазола л-1 + 125 г тебуконазола л-1) в дозе 790 мл га-1 с объемом воды 100 л га-1. На ячмене фунгицид применяли на стадии выхода колоса на 70-100%, а на пшенице — между 75% выхода колоса на главном стебле и 50% цветения. Этот фунгицид также был направлен против листовых пятнистостей злаков (темно-бурая пятнистость и т.д.) и ржавчины. Оба действующих вещества относятся к химической группе триазолов в группе фунгицидов FRAC 3, и они влияют на биосинтез стеролов (https://www.frac.info/docs/default-source/publications/frac-code-list/frac-code-list-2024.pdf, проверено 12 сентября 2024 г.). На каноле применяли два фунгицида: один против черной ножки, а другой против склеротиниоза. Фунгицид против черной ножки — пираклостробин, применяли в виде Headline EC (250 г пираклостробина л-1) в баковой смеси с поддерживающими гербицидами для канолы на стадии 2-6 листьев в дозе 395 мл га-1, с объемом воды 100 л га-1. Фунгицид против склеротиниоза — протиоконазол, применяли в виде Proline 480 SC (480 г протиоконазола л-1) на стадии от раннего цветения до полного цветения канолы в дозе 363 мл га-1, с объемом воды 100 л га-1. Пираклостробин относится к химической группе метокси-карбаматов (ингибиторы хинон-оксидазы) в группе фунгицидов FRAC 11, и он влияет на митохондриальное дыхание. На полевом горохе фунгицидом был fluxapyroxad + pyraclostrobin, применяемый в виде Priaxor DS (250 г флуксапироксада л-1 и 250 г пираклостробина л-1) в начале цветения в дозе 296 мл л га-1, с объемом воды 100 л га-1. На льне фунгицидом был пираклостробин, применяемый в виде Headline EC (250 г пираклостробина л-1) через 7-10 дней после начала цветения в дозе 395 мл га-1, с объемом воды 100 л га-1. Флуксапироксад влияет на дыхание и относится к химической группе пиразол-4-карбоксамидов (ингибиторы сукцинатдегидрогеназы) в группе фунгицидов FRAC 7.
Посевы проводили в мае каждого года, и управляли ими в соответствии со стандартными агрономическими методами, включая нулевую обработку почвы. Удобрения вносили на основе результатов анализа почвы для небобовых культур, а полевой горох инокулировали инокулянтом Rhizobium.
2.2 Отбор почвенных образцов
В 2017 году мы отобрали почву из ризосферы пшеницы, конечной культуры каждого севооборота, на стадии флагового листа. Растения пшеницы извлекали из четырех случайных отрезков рядка длиной 0,5 м в каждой обработке, т.е. из четырех локаций на делянку. Мы удалили непрочно удерживающуюся почву с корней, встряхивая растения вручную, а оставшуюся почву, которая сильно прилипла к корням, осторожно счистили щеткой и собрали как ризосферную почву. Мы объединили четыре образца ризосферной почвы с каждой делянки, чтобы получить объединенный образец, и пропустили его через сито с ячейкой 2 мм. Образцы для экстракции ДНК были заморожены при -20°C, образцы для ферментного анализа были сохранены при 4°C, а образцы для анализа микробной биомассы C (МБУ) были высушены на воздухе и сохранены при 4°C.
2.3 Анализ микробной биомассы C
МБУ почвы измеряли с использованием метода субстрат-индуцированного дыхания (Horwath and Paul, 1994): 300 мг глюкозы растворяли в 9,0 мл воды и добавляли к 50 г воздушно-сухой почвы для доведения ее до 50% влагоемкости (определяемой путем измерения гравиметрической влажности после дренирования насыщенной водой почвенной колонны до прекращения капания воды). После перемешивания почву инкубировали в 1-литровой банке в течение 3 часов при 22°C, а количество CO2, накопившееся в надпочвенном пространстве, измеряли с помощью газовой хроматографии.
2.4 Анализ микробиома: экстракция ДНК, секвенирование и биоинформатика
Экстракцию ДНК почвы проводили с использованием набора Qiagen DNeasy Powerlyzer PowerSoil Kit (Quagen, Торонто, Онтарио) в соответствии с инструкциями производителя. Секвенирование проводили с использованием набора праймеров 515F/806R (515F: 5−ACACTGACGACATGG⊤CTACAGTGCAGCMGCGCGGT∀–3; 806R: 5−TACGGTAGCAGAGAC⊤GGTCTGGACTACHVGGGTWTCT∀T–3) для амплификации вариабельной области V4 гена 16S рРНК прокариот (бактерий и архей) (Caporaso и др., 2011). Образцы сначала штрихкодировали, а затем объединяли. Для характеристики почвенных грибов мы использовали ITS праймеры ITS1F/ITS2R (ITS1F: 5−C⊤GGTCA⊤TAGAGG∀GT∀–3; ITS2R: 5−GCTGCG⊤C⊤CATCGATGC–3) (Bellemain и др., 2010). Образцы снова сначала штрихкодировали, а затем объединяли. Полученные ампликонные библиотеки затем были очищены и количественно оценены отдельно. Каждую библиотеку секвенировали на платформе Illumina MiSeq в Центре инноваций Génome Québec при Университете Макгилла (Монреаль, Канада).
Данные последовательностей 16S были проанализированы с использованием пакета DADA2 (Callahan и др., 2016) (версия 3.14) языка статистических вычислений R. Сырые последовательности 16S были отфильтрованы на основе качества, были выведены ошибки, были отобраны варианты ампликонных последовательностей (ASVs), были удалены химеры, и выполнено таксономическое присвоение с использованием базы данных SILVA_NR99_v138.1. Для анализа ITS последовательностей мы использовали конвейер PIPITS (GitHub - hsgweon/pipits: Automated pipeline for analyses of fungal ITS from the Illumina) для создания таблиц относительной численности OTU и таксономического присвоения после присвоения последовательностей с помощью классификатора RDP против справочного набора данных UNITE fungal ITS (Gweon и др., 2015). Сырые последовательности были депонированы в репозитории NCBI Sequence Read Archive (SRA) под идентификатором BioProject ID PRJNA1175403. Как для 16S, так и для ITS, таблицы ASV, OTU и таксономического присвоения были экспортированы в модуль Marker-gene Data Profiling (MDP) онлайн-платформы MicrobiomeAnalyst для дальнейшего биоинформатического анализа (https://www.microbiomeanalyst.ca/) (Chong и др., 2020; Lu и др., 2023). Последовательности были отфильтрованы по низкому количеству и низкой вариантности перед анализом. Относительную численность микробов на различных уровнях классификации (от типа до рода) рассчитывали. Мы рассчитали следующие индексы α-разнообразия на уровне OTU: ACE (оценщик покрытия на основе численности), Chao1, Fisher и Shannon после рарификации данных до минимального размера библиотеки. β-разнообразие было визуализировано с использованием анализа главных координат (PCoA) на основе индекса несходства Брея-Кертиса, а групповые различия в структурах микробных сообществ были оценены на статистическую значимость с использованием перестановочного многомерного дисперсионного анализа (PERMANOVA), все в MicrobiomeAnalyst.
2.5 Ферментативный анализ
Активность β-глюкозидазы (цикл C), N-ацетил-β-глюкозаминидазы (NAG) (цикл N) и кислотной фосфомоноэстеразы (цикл P) измеряли с использованием микропланшетных флуориметрических анализов (Deng и др., 2011), как описано Lupwayi и др. (2019). Эти анализы были основаны на обнаружении 4-метил-умбеллиферона (MUF), высвобождаемого при ферментативном гидролизе меченных MUF субстратов (MUF-β-D-глюкозид, MUF-β-N-ацетил-глюкозаминид или MUF-фосфат), инкубированных с почвой при оптимальном pH для каждого фермента (pH 5,5 для NAG и pH 6,0 для двух других ферментов). Активность арилсульфатазы (цикл S) измеряли в настольном анализе для колориметрического измерения p-нитрофенола, высвобождаемого ферментом после инкубации 1 г почвы с буферным (pH 6,0) p-нитрофенил-β-D-сульфатом (Dick и др., 1996).
2.6 Статистический анализ
Данные по МБУ почвы, относительной численности микробиома на выбранных уровнях классификации, индексам α-разнообразия и ферментативной активности были статистически проанализированы с помощью дисперсионного анализа (ANOVA) как факториал севооборот x фунгицид в РПБС. Уровень значимости 5% использовался для определения статистической значимости, и средние значения были разделены с помощью критерия Тьюки HSD при обнаружении статистической значимости. Чтобы далее изучить, какие свойства севооборота повлияли на результаты, были построены следующие ортогональные контрасты:-
• 2-летние против 3-летних севооборотов: Севообороты 1-4 против Севооборотов 5-8.
• 2-летние против последовательных севооборотов: Севообороты 1-4 против Севооборота 9.
• Широколиственные культуры против ячменя в качестве предшествующих культур в 2-летних севооборотах: Севообороты 1, 3 и 4 против Севооборота 2.
• Горох против масличных культур в качестве предшествующих культур в 2-летних севооборотах: Севооборот 3 против Севооборотов 1 и 4.
Мы использовали только 2-летние севообороты для контрастов C и D, потому что включение 3-летних севооборотов в некоторых случаях смешало бы эффекты с теми самыми культурами, которые мы сравнивали.
Взаимосвязи между составом микробных родов и ферментативной активностью были оценены с помощью корреляционного анализа Пирсона, а некоторые взаимосвязи были смоделированы с помощью линейного регрессионного анализа, когда корреляции были значимыми на 5%-ном уровне значимости.
3 Результаты
3.1 Микробная биомасса C
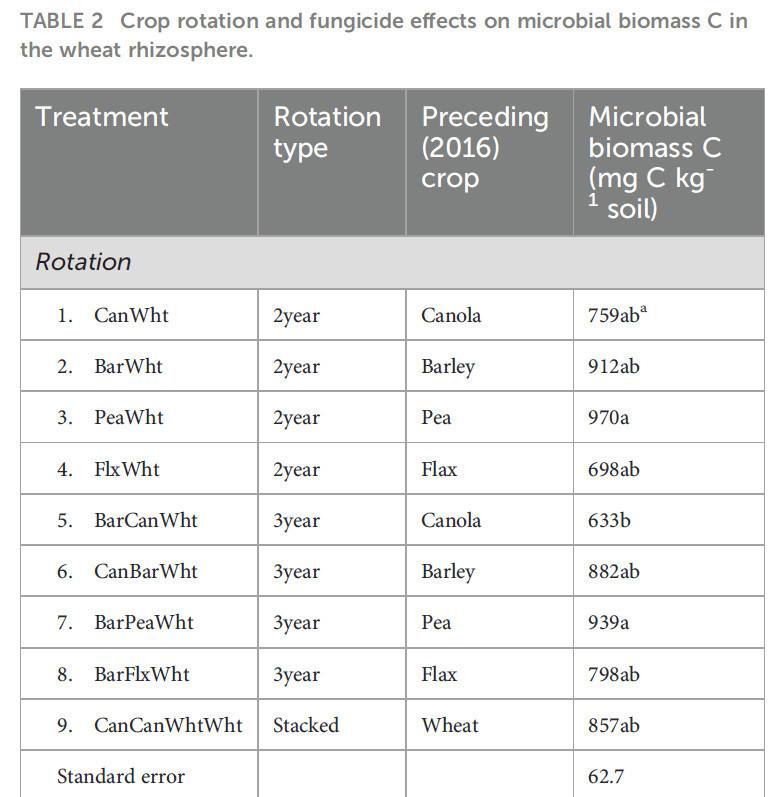
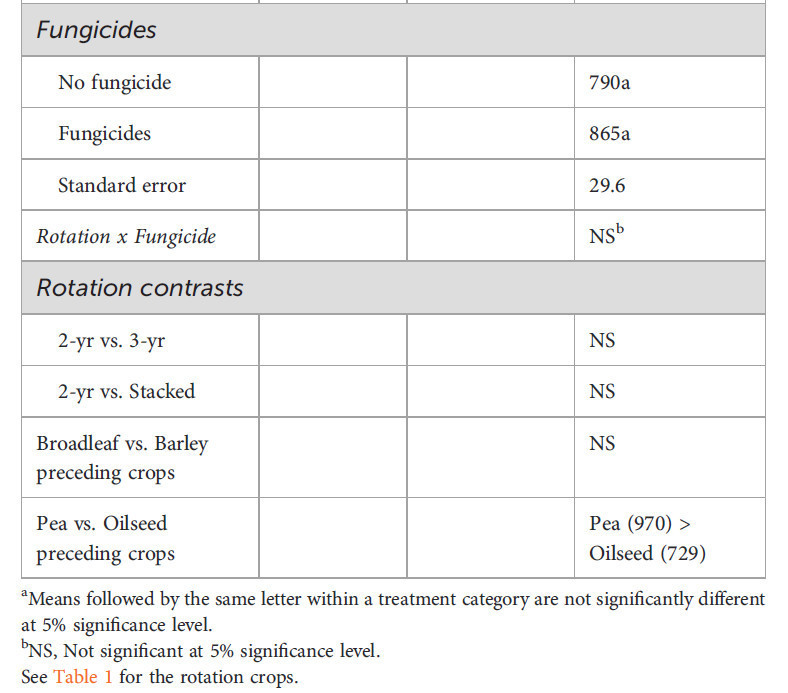
Микробная биомасса C в ризосфере пшеницы была самой высокой в севообороте горох-пшеница и самой низкой в севообороте ячмень-канола-пшеница, но продолжительность севооборота (2-летний против 3-летнего или 2-летний против последовательного) не оказала эффекта (Таблица 2). Хотя не было разницы в МБУ между широколиственными предшествующими культурами и предшествующей культурой ячменем, МБУ была на 33% выше в пшенице, предшествуемой горохом (970 мг C кг-1 почвы), чем в пшенице, предшествуемой масличными культурами (в среднем 729 мг C кг-1 почвы). Применение фунгицидов не повлияло на МБУ.
Таблица 2 Влияние севооборота и фунгицидов на микробную биомассу C в ризосфере пшеницы.
3.2 Грибной микробиом
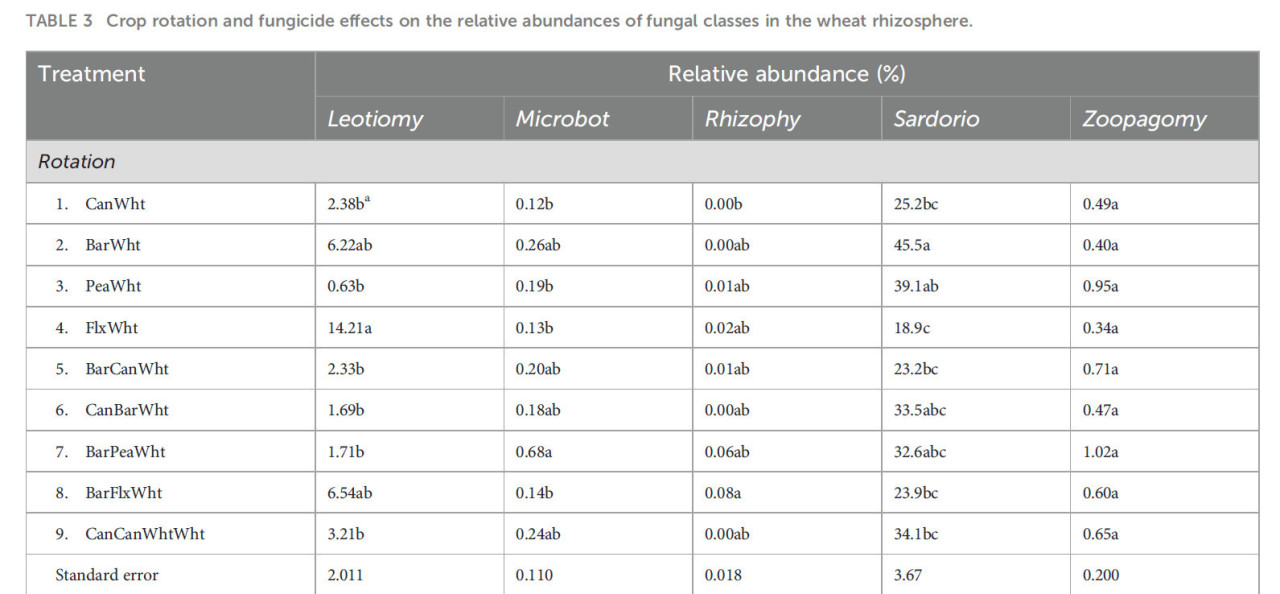
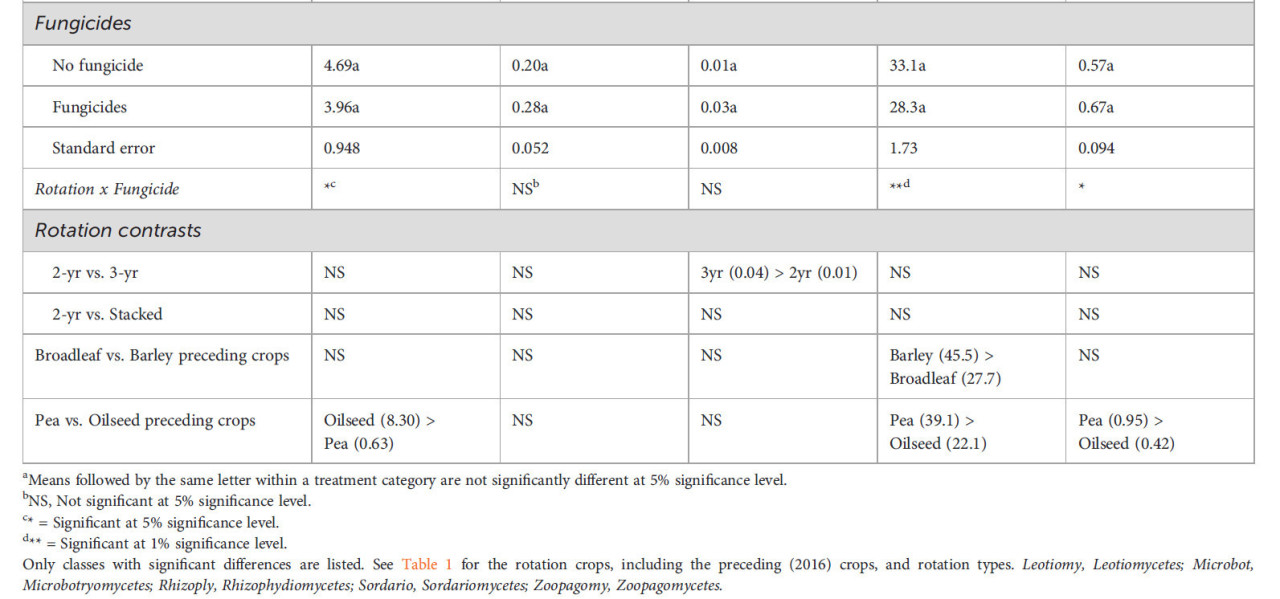
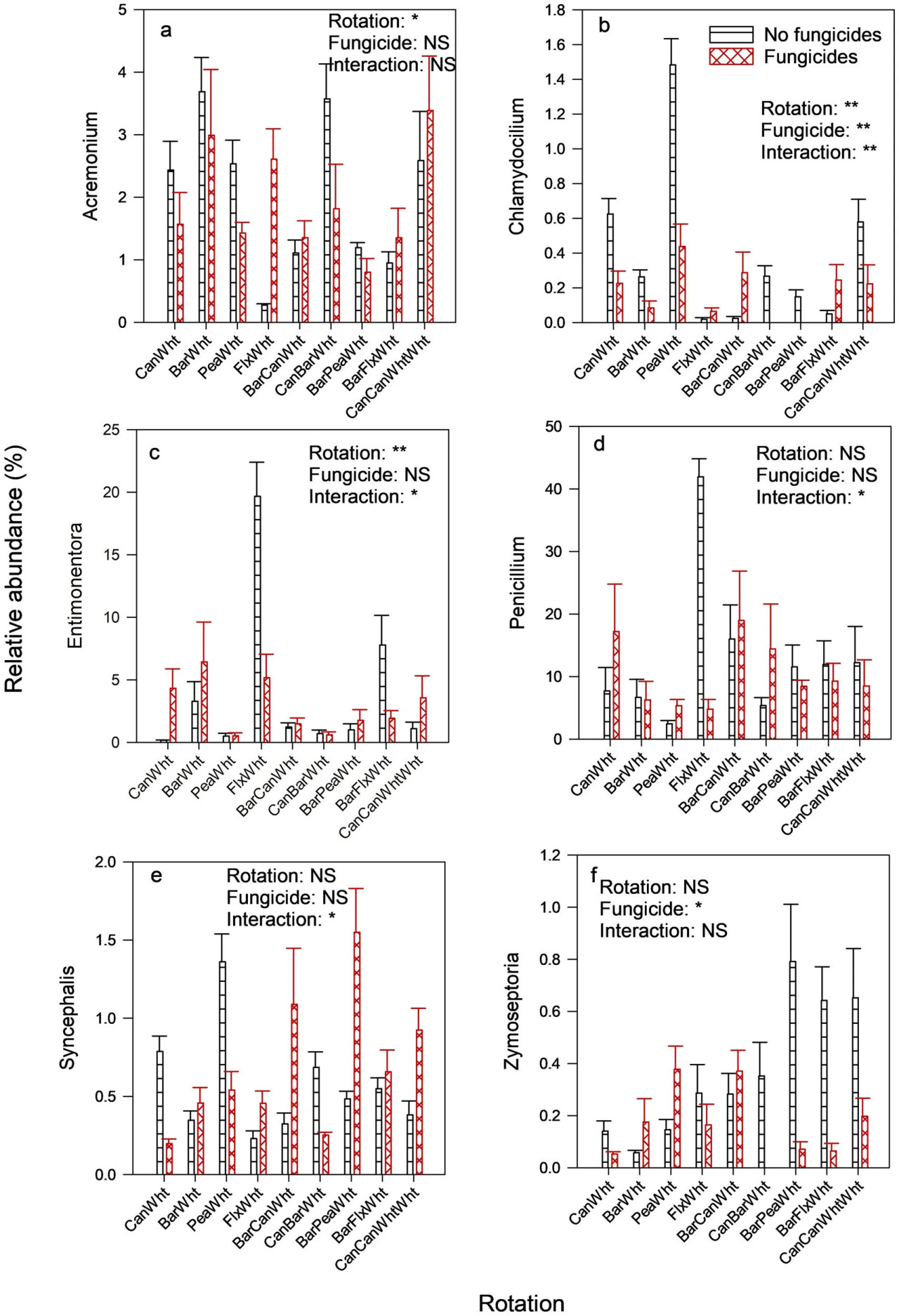
Наиболее многочисленным классом грибов был Sordariomycetes (Вспомогательный рисунок S1), и его относительная численность была выше, когда пшенице предшествовал ячмень, в частности в севообороте ячмень-пшеница без фунгицидов, чем широколиственные культуры (Таблица 3). На уровне рода этого грибного класса относительная численность рода Acremonium также была выше в севооборотах ячмень-пшеница и канола-ячмень-пшеница, чем в других севооборотах, но наблюдалось взаимодействие севооборот x фунгицид (Рисунок 1A). Sordariomycetes также были более многочисленны, когда предшествующей культурой был горох по сравнению с масличными предшествующими культурами (39,1% против 22,1% относительной численности) (Таблица 3), что иллюстрирует высокая относительная численность рода Clamydocillium в севообороте горох-пшеница без фунгицидов (Рисунок 1B). Относительная численность класса Leotiomycetes была самой высокой в севообороте лен-пшеница (Таблица 3), особенно там, где не применялись фунгициды. Этот эффект льна был основным фактором, способствовавшим большей относительной численности этого класса в пшенице, предшествуемой масличными культурами, по сравнению с предшествующей культурой горохом, как показано для рода Entimonentora (Рисунок 1C). Род Penicillium (из класса Eurotiomycetes), который был наиболее доминирующим родом грибов (Вспомогательный рисунок S2), также был обогащен в севообороте лен-пшеница (Рисунок 1D). Ни один конкретный тип севооборота или предшествующая культура не объясняли различия в относительной численности Microbotromycetes, и фунгициды не оказали эффекта (Таблица 3). 3-летние севообороты, в частности ячмень-лен-пшеница и ячмень-горох-пшеница, имели более высокую относительную численность Rhizophydiomycetes, чем 2-летние севообороты, и фунгициды не оказали эффекта. Однако фунгициды снизили относительную численность рода Zymoseptoria (из класса Dothideomycetes) (Рисунок 1F); этот род (Z. tritici) связан с септориозом листьев пшеницы. Zoopagomycetes были более многочисленны в пшенице, которой предшествовал горох, особенно в севообороте ячмень-горох-пшеница с фунгицидами и горох-пшеница без фунгицидов, чем масличные предшествующие культуры, как показано для рода Syncephalis (Рисунок 1E).
Таблица 3 Влияние севооборота и фунгицидов на относительную численность грибных классов в ризосфере пшеницы.
Перечислены только классы со значимыми различиями. См. Таблицу 1 для культур севооборота, включая предшествующие (2016) культуры, и типов севооборота. Leotiomy, Leotiomycetes; Microbot, Microbotryomycetes; Rhizoply, Rhizophydiomycetes; Sordario, Sordariomycetes; Zoopagomy, Zoopagomycetes.
Рисунок 1 Влияние севооборота и фунгицидов на относительную численность родов грибов в ризосфере пшеницы. Включены только роды (имевшие среднюю относительную численность не менее 0,20%) со значимыми различиями. Can, Канола; Wht, Пшеница; Bar, Ячмень; Pea, Горох полевой; Flx, Лен. Эффекты обработки: = значимо при 1%-ном уровне значимости; = значимо при 5%-ном уровне значимости; NS, не значимо при 5%-ном уровне значимости. Изображенные роды грибов включают (A) Acremonium, (B) Chlamydocilium, (C) Entimonentora, (D) Penicillium, (E) Syncephalis и (F) Zymoseptoria.
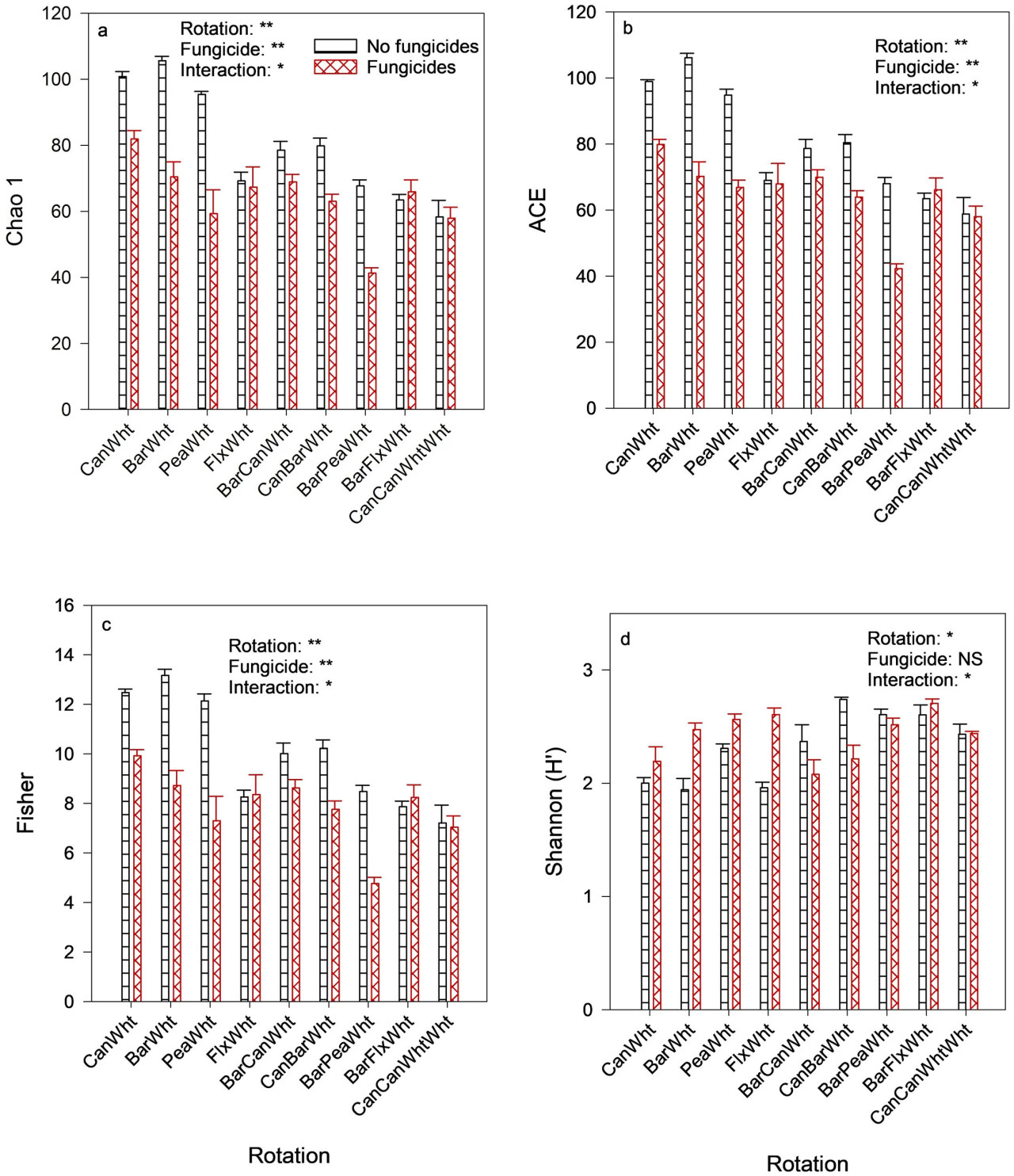
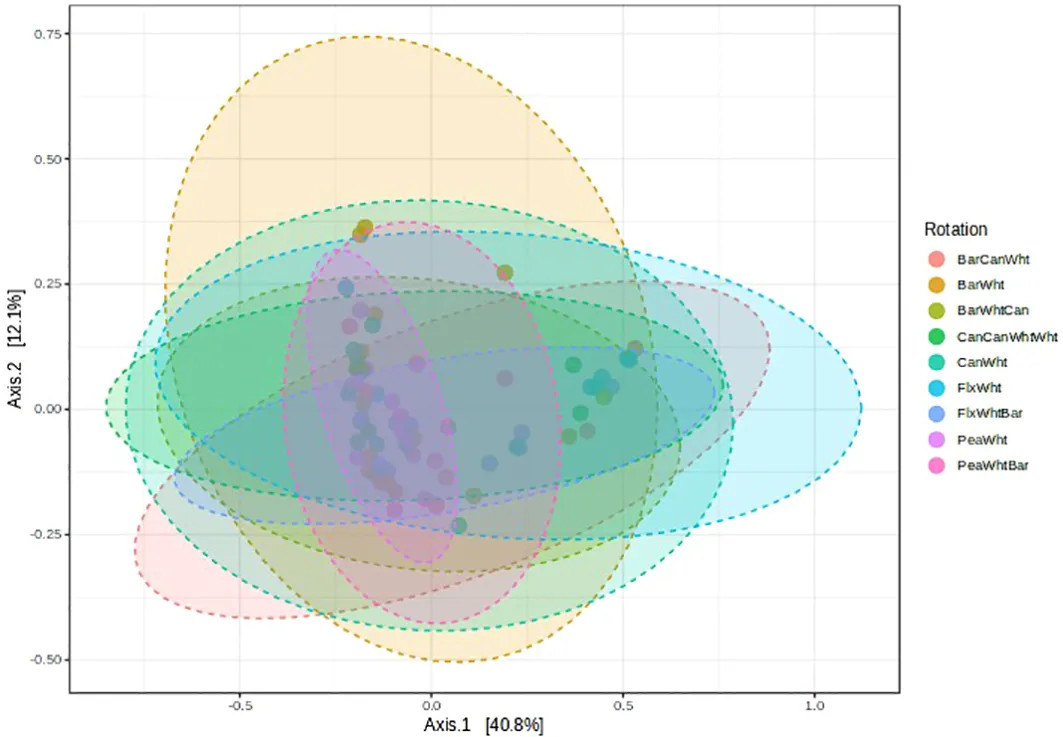
Индексы Chao 1, ACE и Fisher грибного α-разнообразия, которые все обозначают видовое богатство, были выше в 2-летних севооборотах, чем в 3-летних севооборотах или последовательном севообороте (Рисунки 2A–C). Эти индексы также были снижены применением фунгицидов (например, индексы Chao1: 64,0 против 79,9), особенно в 2-летних севооборотах. Однако индекс разнообразия Шеннона был выше в 3-летних севооборотах, чем в 2-летних, и применение фунгицидов увеличило этот индекс в 2-летних севооборотах (Рисунок 2D). Анализ главных координат (PCoA) показал, что грибное β-разнообразие зависело только от севооборота (PERMANOVA F-значение = 1,7801; R-квадрат = 0,18437; p-значение = 0,007), и Рисунок 3 показывает, что севообороты горох-пшеница, ячмень-пшеница и ячмень-горох-пшеница имели несколько отличные структуры грибного сообщества по сравнению с другими севооборотами. Фунгициды не повлияли на грибное β-разнообразие.
Рисунок 2 Влияние севооборота и фунгицидов на грибное α-разнообразие в ризосфере пшеницы. Can, Канола; Wht, Пшеница; Bar, Ячмень; Pea, Горох полевой; Flx, Лен; ACE, Оценщик покрытия на основе численности. Эффекты обработки: = значимо при 1%-ном уровне значимости; = значимо при 5%-ном уровне значимости; NS, не значимо при 5%-ном уровне значимости. Изображенные индексы включают (A) Chao 1, (B) Оценщик покрытия на основе численности (ACE), (C) Fisher и (D) Shannon.
Рисунок 3 Анализ главных координат (PCoA), показывающий влияние севооборота на грибное β-разнообразие в ризосфере пшеницы. Can, Канола; Wht, Пшеница; Bar, Ячмень; Pea, Горох полевой; Flx, Лен. PERMANOVA F-значение = 1,7801; R-квадрат = 0,18437; p-значение = 0,007.
3.3 Прокариотный микробиом
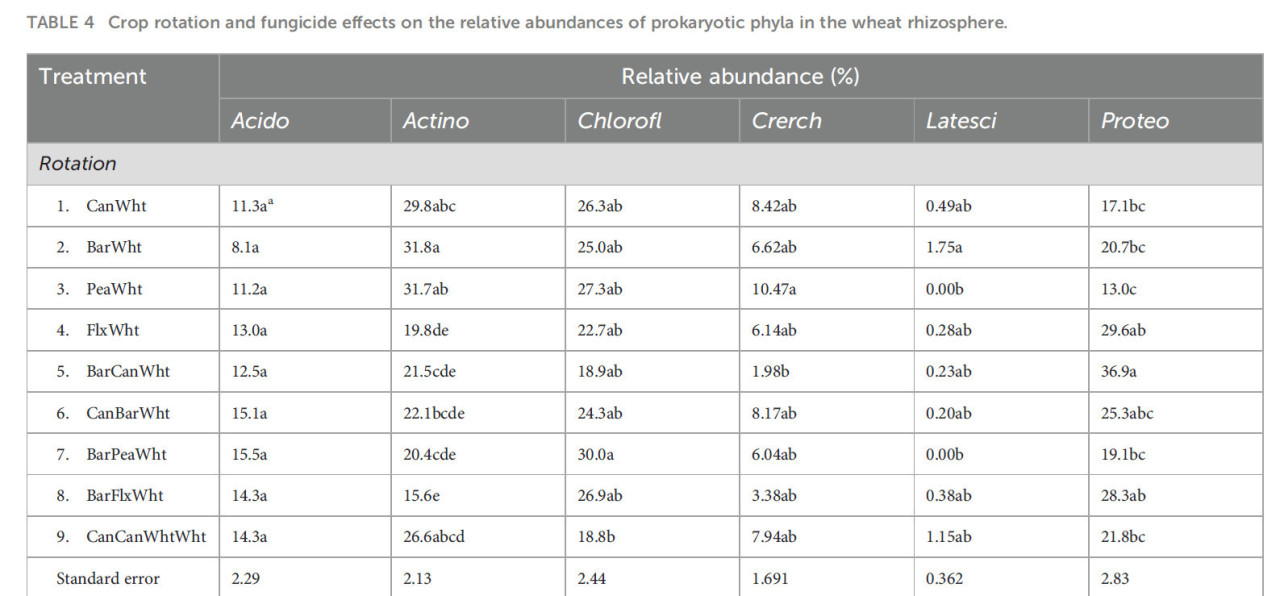
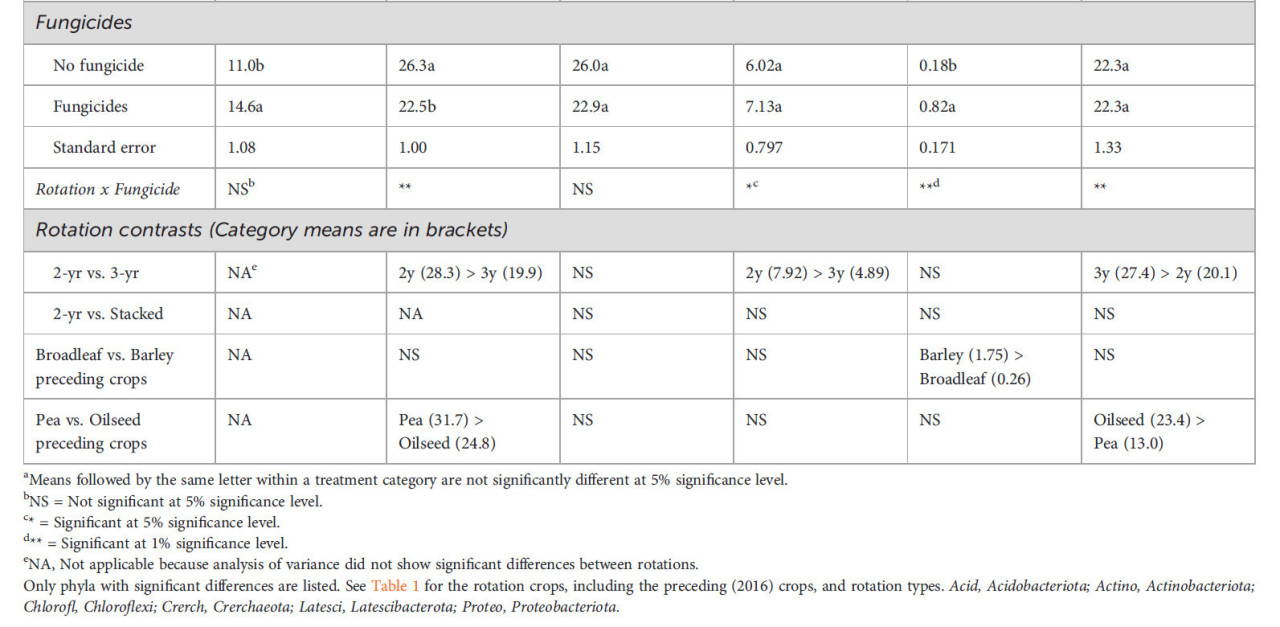
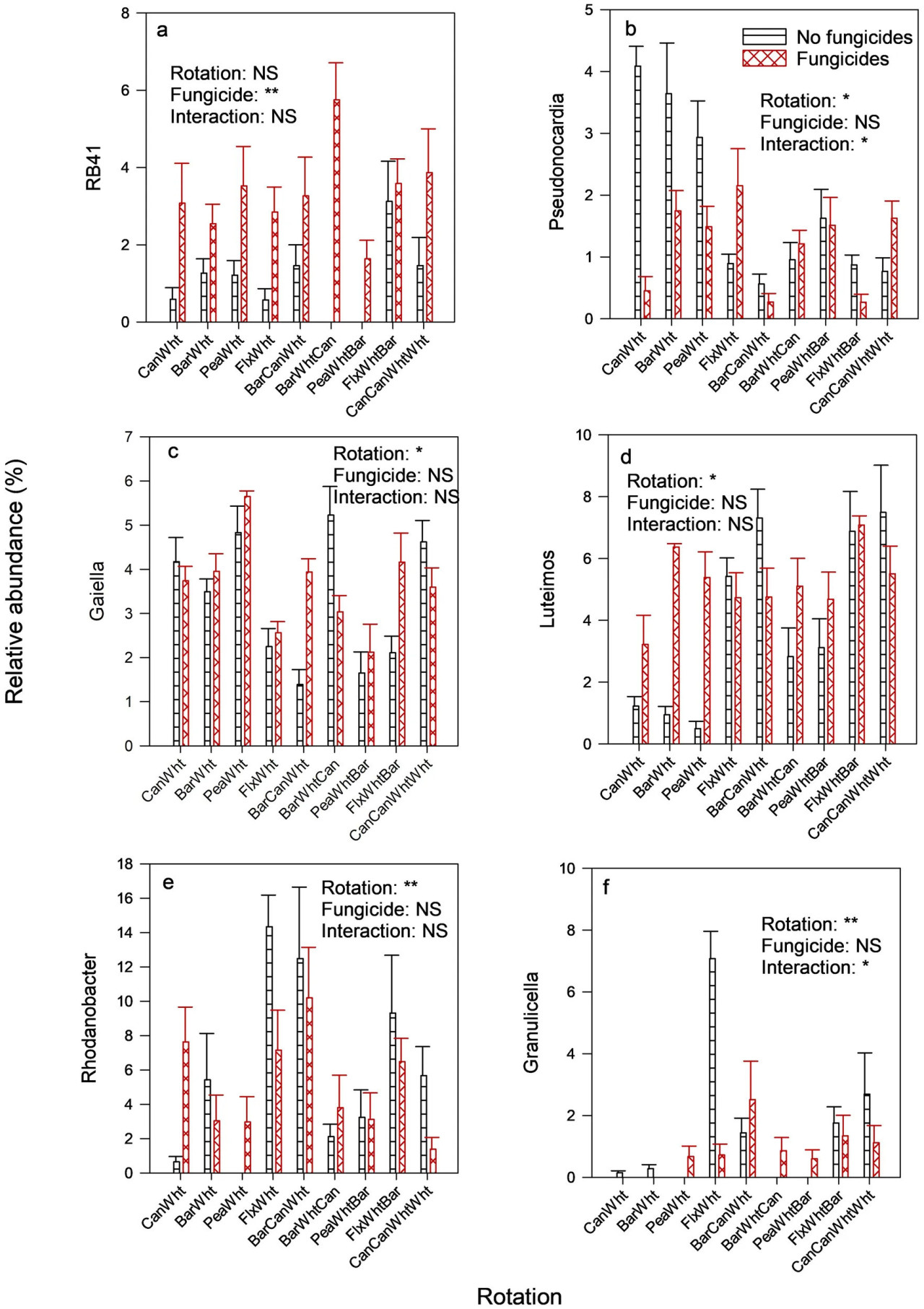
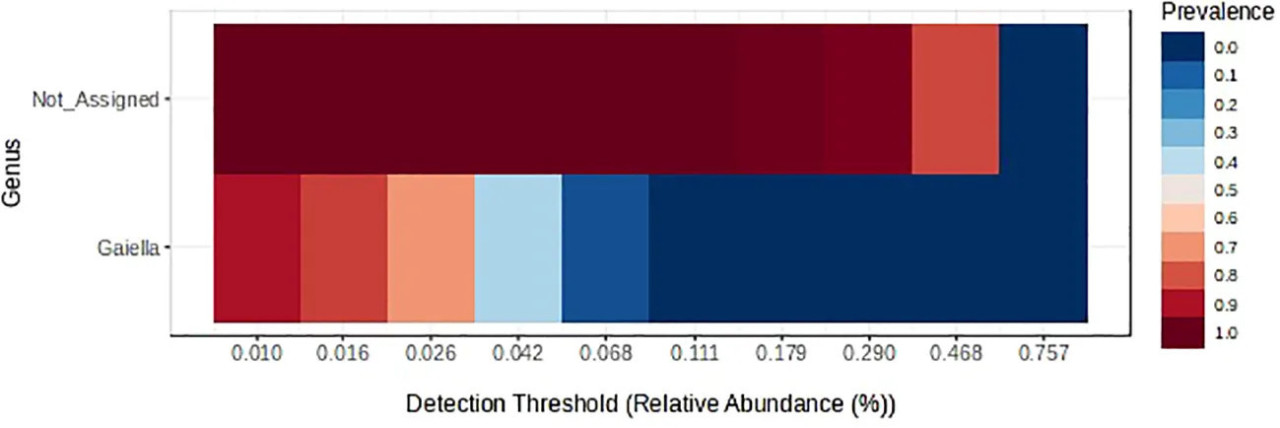
Наиболее доминирующими типами прокариот, каждый с примерно 24% относительной численности, были Chloroflexi, Actinobacteriota и Proteobacteriota (Вспомогательный рисунок S3). Севооборот не повлиял на относительную численность типа бактерий Acidobacteriota, которая была увеличена фунгицидами (Таблица 4). Эти эффекты также наблюдались на уровне рода, как показано относительной численностью рода RB41 (Рисунок 4A). Относительная численность Actinobacteriota была выше в 2-летних, чем в 3-летних севооборотах, и была снижена фунгицидами, особенно в 2-летних севооборотах (Таблица 4). Эти эффекты также наблюдались у рода Pseudonocardia (Рисунок 4B), но род Gaiella реагировал только на севооборот (Рисунок 4C). Влияние севооборота на тип Chloroflexi не могло быть категоризировано по типу севооборота, и фунгициды не оказали эффекта (Таблица 3). Относительная численность типа архей Crerchaeota была выше в 2-летних севооборотах, чем в 3-летних (Таблица 4), и фунгициды снизили ее численность в 2-летних севооборотах, увеличив в 3-летних. Latescibacterota были более многочисленны в пшенице, предшествуемой ячменем, чем той, которой предшествовали широколиственные культуры, и фунгициды увеличили их численность в севообороте ячмень-пшеница (Таблица 3). Proteobacteriota были более многочисленны в 3-летних, чем в 2-летних севооборотах (27,4% против 20,1% относительной численности, Таблица 4), что иллюстрируется родом Luteimonas (Рисунок 4D), и в пшенице, предшествуемой масличными культурами, чем предшествуемой горохом, что иллюстрируется родом Rhodanobacter (Рисунок 4E). Rhodanobacter (из типа Proteobacteriota) был наиболее доминирующим родом прокариот (Вспомогательный рисунок S4). Фунгициды увеличили относительную численность Proteobacteriota в 2-летних севооборотах (за исключением севооборота лен-пшеница). Хотя не было эффектов обработки на относительную численность типа Firmicutes, род Granulicella был обогащен в севообороте лен-пшеница без фунгицидов (Рисунок 4F). Неприсвоенный таксон и род Gaiella были основными таксонами прокариот, которые наблюдались по крайней мере в 85% образцов (Рисунок 5).
Таблица 4 Влияние севооборота и фунгицидов на относительную численность типов прокариот в ризосфере пшеницы.
Перечислены только типы со значимыми различиями. См. Таблицу 1 для культур севооборота, включая предшествующие (2016) культуры, и типов севооборота. Acid, Acidobacteriota; Actino, Actinobacteriota; Chlorofl, Chloroflexi; Crerch, Crerchaeota; Latesci, Latescibacterota; Proteo, Proteobacteriota.
Рисунок 4 Влияние севооборота и фунгицидов на относительную численность родов прокариот в ризосфере пшеницы. Включены только роды (имевшие среднюю относительную численность не менее 0,50%) со значимыми различиями. Can, Канола; Wht, Пшеница; Bar, Ячмень; Pea, Горох полевой; Flx, Лен. Эффекты обработки: = значимо при 1%-ном уровне значимости; = значимо при 5%-ном уровне значимости; NS, не значимо при 5%-ном уровне значимости. Изображенные роды прокариот включают (A) RB41, (B) Pseudonocardia, (C) Gaiella, (D) Luteimos, (E) Rhodanobacter и (F) Granulicella.
Рисунок 5 Основные таксоны прокариот, которые наблюдались по крайней мере в 85% образцов.
Ни α-разнообразие, ни β-разнообразие прокариотных сообществ не зависели от севооборотов или фунгицидов.
3.4 Ферментативная активность
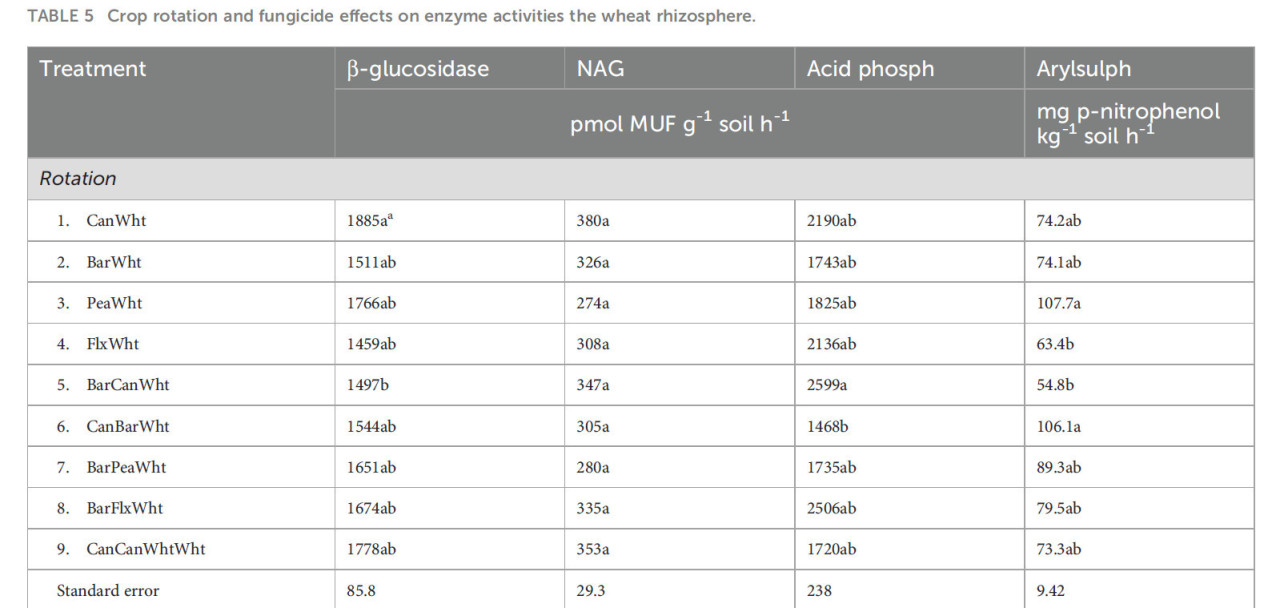
Не было эффектов севооборота или фунгицидов на активность N-ацетил-β-глюкозаминидазы (NAG), как и не было эффектов фунгицидов на активность любого другого фермента (Таблица 5). Активность β-глюкозидазы была самой высокой в севообороте канола-пшеница и самой низкой в севообороте ячмень-канола-пшеница, без четких указаний на эффекты типа севооборота или предшествующей культуры. Аналогично, активность кислотной фосфомоноэстеразы была самой высокой в севообороте ячмень-канола-пшеница и самой низкой в севообороте канола-ячмень-пшеница, что показывает влияние последовательности культур. Активность арилсульфатазы была на 57% выше, когда предшествующей культурой был горох (107,7 мг C кг-1 почвы), чем когда пшенице предшествовала масличная культура (68,8 мг C кг-1 почвы).
Таблица 5 Влияние севооборота и фунгицидов на ферментативную активность в ризосфере пшеницы.
3.5 Взаимосвязи между составом микробиома и ферментативной активностью
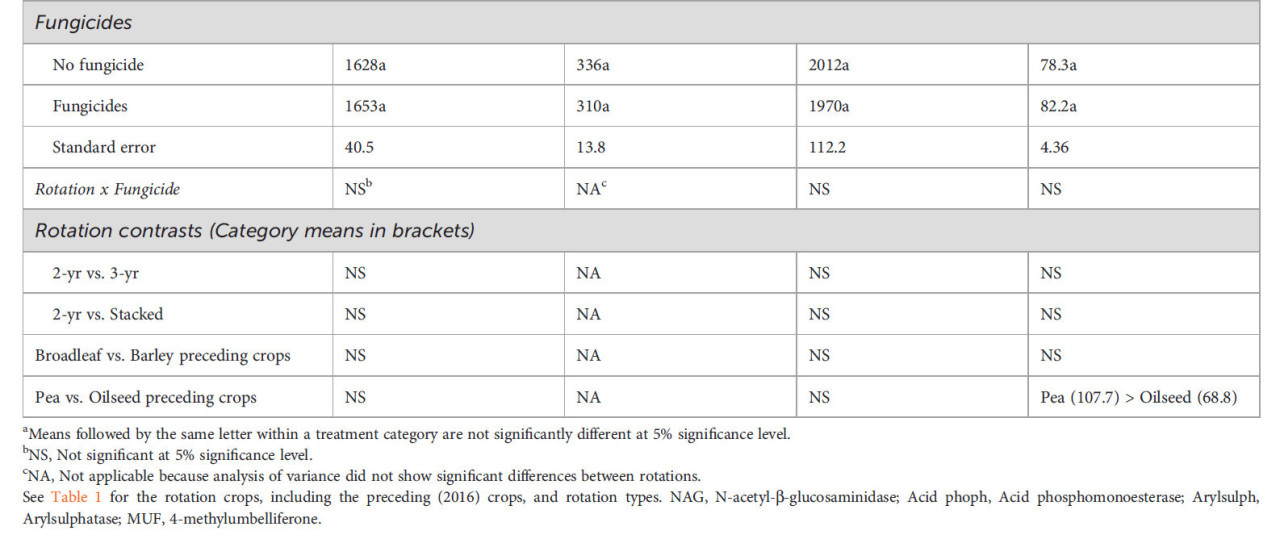
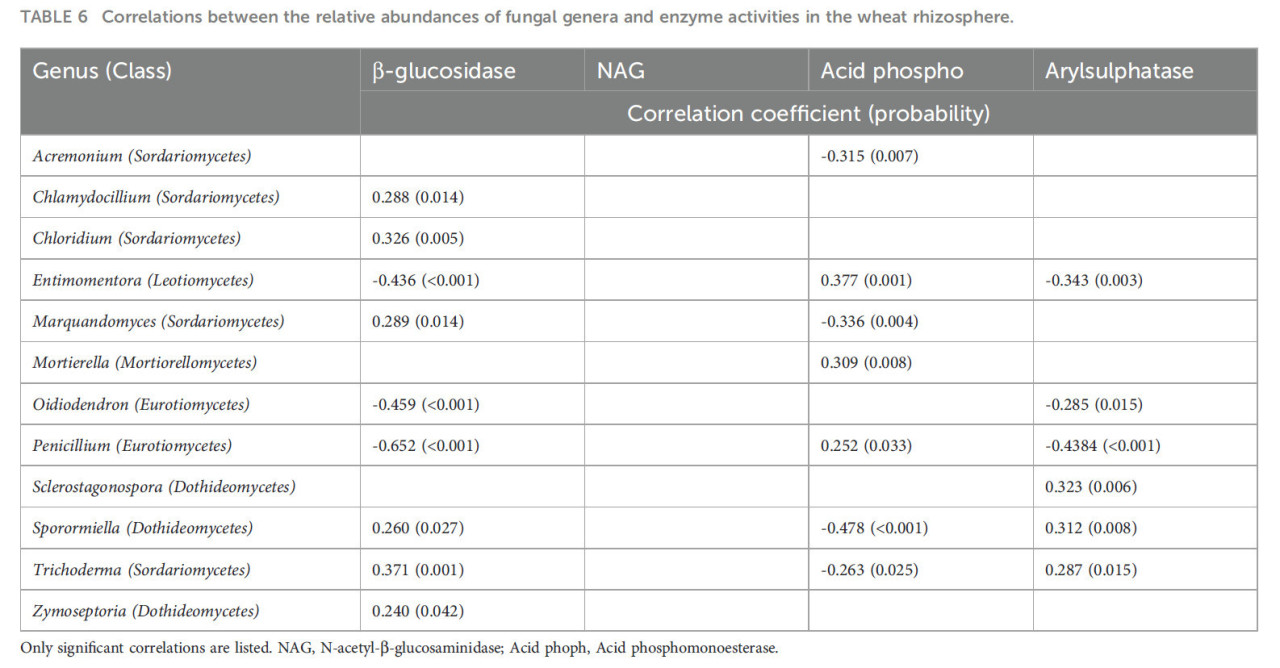
Ни одна из относительных численностей родов грибов не коррелировала с активностью N-ацетил-β-глюкозаминидазы, которая опосредует цикл N (Таблица 6). Относительная численность шести родов грибов, все из класса Sordariomycetes (роды Chlamydocillium, Chloridium, Marquandomycetes и Trichoderma) или Dothideomycetes (роды Sporormiella и Zymoseptoria), положительно коррелировала с активностью β-глюкозидазы; а три рода из классов Eurotiomycetes (роды Oidiodendron и Penicillium) или Leotiomycetes (род Entimomentora) имели отрицательные корреляции. Роды, которые были отрицательно коррелированы с активностью β-глюкозидазы, также были отрицательно коррелированы с арилсульфатазой, но положительно с кислотной фосфомоноэстеразой. Аналогично, отрицательные корреляции с кислотной фосфомоноэстеразой были противоположны корреляциям с активностью β-глюкозидазы или арилсульфатазы. Некоторые из этих взаимосвязей показаны с помощью линейной регрессии на Рисунке 6.
Таблица 6 Корреляции между относительной численностью родов грибов и ферментативной активностью в ризосфере пшеницы.
Перечислены только значимые корреляции. NAG, N-ацетил-β-глюкозаминидаза; Acid phoph, Кислотная фосфомоноэстераза.
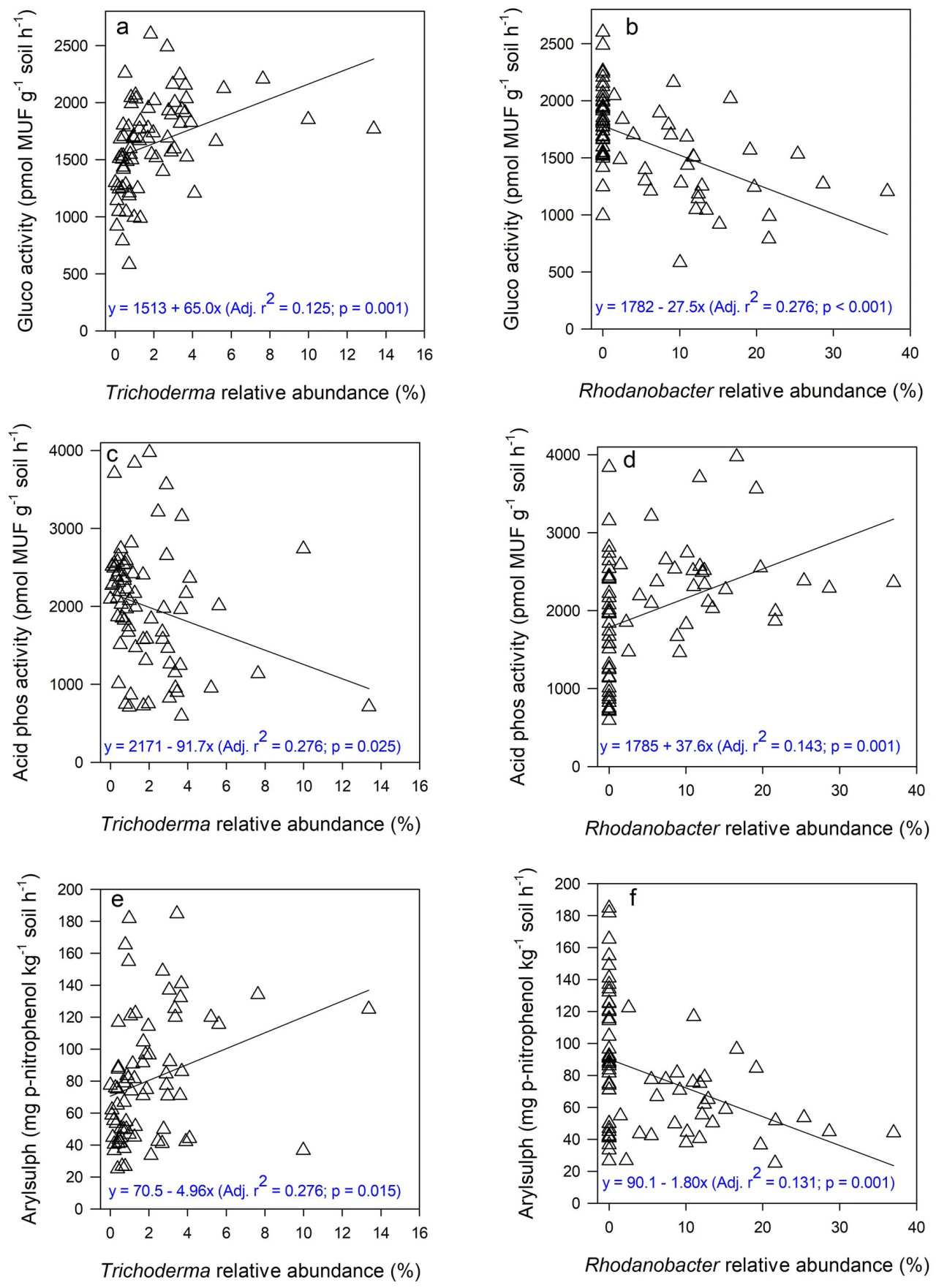
Рисунок 6 Взаимосвязи между относительной численностью рода грибов Trichoderma (класс Sordariomycetes) и активностью β-глюкозидазы (gluco), кислотной фосфомоноэстеразы (acid phos) и арилсульфатазы (arylsulph) (A, C, E) и между относительной численностью бактериального рода Rhodanobacter (тип Proteobacteriota) и активностью тех же ферментов (B, D, F).
Как и в случае с родами грибов, корреляции относительной активности родов прокариот с активностью β-глюкозидазы и арилсульфатазы были сходными (то есть обе положительные или отрицательные), но противоположными корреляциям с кислотной фосфомоноэстеразой. Относительная численность родов прокариот из типа Proteobacteriota (роды Masillia, Rhodonobacter и Sphingomonas), которая была отрицательно коррелирована с активностью β-глюкозидазы, также была отрицательно коррелирована с активностью арилсульфатазы, но положительно с активностью кислотной фосфомоноэстеразы (Вспомогательная таблица S1). Однако некоторые роды из типа Actinobacteria (например, Marmoricola) имели отрицательные корреляции, в то время как другие (например, Rubrobacter) — положительные, с активностью двух ферментов. Некоторые из этих взаимосвязей показаны с помощью линейной регрессии на Рисунке 6.
4 Обсуждение
4.1 Фунгициды
Наиболее стабильным эффектом фунгицидов было снижение индексов видового богатства грибов (α-разнообразие), особенно в 2-летних севооборотах (Рисунки 2A–C), но индекс разнообразия Шеннона в этих севооборотах увеличился (Рисунок 2D). Микробное разнообразие является функцией богатства (количество различных микробных таксонов) и выравненности (относительное распределение этих таксонов) (Bo-Ra и др., 2017). Наши результаты предполагают, что фунгициды сократили количество различных грибных таксонов в 2-летних севооборотах, но эти таксоны были более равномерно распределены в этих севооборотах, чем в 3-летних, т.е. не доминировали несколько таксонов. Возможно, что без фунгицидов в 2-летних севооборотах было больше грибных таксонов, чем в 3-летних, из-за грибных патогенов, на которые были направлены фунгициды. Однако примененные фунгициды были листовыми фунгицидами, которые не были направлены на почвенные грибные патогены. Следовательно, эти эффекты на грибное разнообразие, вероятно, были нецелевыми эффектами от фунгицидов, которые достигли почвы через несомкнутые пологи культур или стекая с листьев и стеблей культур. Поскольку различные фунгициды применялись к различным культурам в каждом севообороте, трудно приписать их эффекты конкретным фунгицидам. Однако 2-летние севообороты на основе пшеницы получали более высокую долю триазольных фунгицидов протиоконазола и тебуконазола (поскольку пшеница выращивалась каждый второй год), чем 3-летние севообороты (Таблица 1), что предполагает, что один или оба этих фунгицида могли снизить грибное богатство почвы. Lloyd и др. (2021) сообщили, что протиоконазол, примененный на голубике, снизил грибное богатство почвы. Напротив, Vasilchenko и др. (2023) сообщили, что фунгициды снизили индексы Шеннона как грибных, так и бактериальных сообществ в почве, но не повлияли на индексы Chao1 (богатства). Эффекты фунгицидов на почвенный микробиом оценивались только один раз в нашем исследовании из-за ограниченности ресурсов. При однократном отборе образцов невозможно узнать, были ли эффекты преходящими, о чем сообщалось в некоторых исследованиях (обзор Roman и др., 2021). Тем не менее, даже преходящие эффекты могут иметь последствия. Однако эти эффекты фунгицидов на грибное разнообразие не оказали заметного влияния на круговорот питательных веществ в нашем исследовании, поскольку ферментативная активность не изменилась.
Хотя фунгициды не повлияли на разнообразие прокариот в нашем исследовании, они снизили относительную численность Actinobacteriota, одновременно увеличив относительную численность Acidobacteriota и Latescibacterota (Таблица 4). Расходящиеся эффекты фунгицидов на различных почвенных прокариот также сообщались в других исследованиях, и увеличение относительной численности в основном приписывалось обогащению прокариот, которые детоксицируют фунгициды (Han и др., 2021; Vasilchenko и др., 2023).
4.2 Продолжительность/тип севооборота
Два из трех наиболее доминирующих типов прокариот, Actinobacteriota и Proteobacteriota, по-разному реагировали на продолжительность севооборота. По сравнению с 2-летними севооборотами 3-летние севообороты увеличили относительную численность Proteobacteriota (Таблица 3) и грибного класса Rhizophydiomycetes (Таблица 2), но обратное было верно для Actinobacteriota и типа архей Crerchaeota (Таблица 3). Liu и др. (2023a) также сообщили, что относительная численность Actinobacteriota была выше в 3-летнем севообороте (яровой батат-озимая пшеница-летняя кукуруза), чем в 2-летнем (озимая пшеница-летняя кукуруза).
Грибное α-разнообразие также по-разному реагировало на продолжительность севооборота: индексы видового богатства (Chao 1, ACE и Fisher) были выше в 2-летних севооборотах, чем в 3-летних или последовательном севообороте (Рисунки 2A–C), но обратное было верно для индекса (Шеннона), который сочетает богатство и выравненность (Рисунок 2D). Период исследования для этого полевого испытания, вероятно, был слишком коротким, чтобы 3-летние севообороты сформировали почвенный микробиом. В период с 2013 по 2017 год 2-летние севообороты завершили два цикла, но 3-летние севообороты завершили только один цикл. Идеальная продолжительность исследования была бы такой, при которой каждый севооборот завершает по крайней мере два цикла, как это было в 12-летнем исследовании почвозащиты с 1-летними и 6-летними севооборотами (Larney и др., 2017). В 16-летнем полевом испытании Yang и др. (2023) сообщили, что сложность микробной сети почвы увеличивалась с повышением разнообразия севооборота, и что сложность сети оказывала более сильное влияние на мультифункциональность почвы (характеризуемую с использованием функций, связанных со свойствами почвы, базальным дыханием, ферментативной активностью и циклом азота), чем состав и разнообразие микробных сообществ.
4.3 Предшествующие культуры
Наиболее многочисленный класс грибов, Sordariomycetes, и один из трех наиболее многочисленных типов прокариот, Actinobacteriota, были обогащены предшествующей культурой гороха по сравнению с масличными предшествующими культурами, как и МБУ (Таблица 2) и активность арилсульфатазы (Вспомогательная таблица S1). Borase и др. (2021) также сообщили, что добавление бобовой культуры маша в севооборот рис-пшеница увеличивает МБУ почвы и активность арилсульфатазы. Однако в нашем исследовании обратное было верно для грибного класса Leotiomycetes и бактериального типа Proteobacteriota из-за эффекта льна (Таблицы 3, 4). Причина обогащения Leotiomycetes льном неизвестна, но Tan и др. (2017) сообщили, что некоторые Leotiomycetes были потенциальными патогенами для лекарственной культуры санчи (Panax notoginseng) в Китае. Основное различие между горохом и масличными культурами заключается в биологической фиксации азота первыми и производстве масла последними. В полевых и тепличных исследованиях разложения пожнивных остатков Lupwayi и др. (2004a, b) сообщили, что МБУ почвы была выше при разложении остатков полевого гороха, чем остатков канолы, хотя их характер разложения не сильно различался. Многие исследования показали положительные эффекты севооборотов на основе бобовых на почвенный микробиом в отношении МБУ и разнообразия (обзор Lupwayi and Kennedy, 2007; Schaedel и др., 2021; Liu и др., 2023b), но другие показали, что добавление многих бобовых в севооборот может иметь отрицательные эффекты (Nayyar и др., 2009; Lupwayi и др., 2012; Bainard и др., 2017). Так, Bainard и др. (2017) сообщили, что добавление более двух бобовых фаз в 4-летний севооборот увеличило количество грибных патогенов, включая Fusarium avenaceum, F. redolens и Alternaria spp. Одна из масличных культур, канола, производит глюкозинолаты, которые высвобождают биоциды, действующие как почвенные фумиганты, тем самым воздействуя на почвенный микробиом (McCully и др., 2008). В зерновых системах на основе пшеницы в штате Вашингтон (США) Hansen и др. (2019) сообщили, что канола снизила количество почвенных грибов и грамположительных бактерий в некоторых местах. Следовательно, различные факторы могут объяснять различия между бобовыми и масличными культурами в их влиянии на почвенный микробиом.
По сравнению с масличными предшествующими культурами, предшествующая культура ячменя обогатила доминирующий класс грибов Sordariomycetes (Таблица 3) и один из наименее доминирующих типов прокариот, Latescibacterota (Таблица 4). Эти результаты предполагают, что эти таксоны процветают в условиях низкого содержания N в почве, поскольку Lupwayi и др. (2004b) сообщили о концентрациях N в остатках ячменя и канолы 4,9 и 10,9 мг г-1 соответственно, что приводит к соотношениям C/N 93 и 41 соответственно. Снижение относительной численности Sordariomycetes по отношению к пшенице не могло быть приписано эффектам фумигации почвы глюкозинолатами канолы, поскольку севооборот лен-пшеница имел несколько более низкую относительную численность Sordariomycetes, чем севооборот канола-пшеница (Таблица 3).
4.4 Взаимосвязи между составом микробиома и функционированием
Было две последовательные тенденции во взаимосвязях между составом микробиома и ферментативной активностью. Первая заключалась в том, что относительная численность ни одного из родов грибов не коррелировала с активностью N-ацетил-β-глюкозаминидазы, которая опосредует цикл N. Это наблюдение не обязательно предполагает, что грибы не были вовлечены в цикл N, а скорее то, что, вероятно, не было большой вариации в относительной численности родов грибов и/или активности N-ацетил-β-глюкозаминидазы, чтобы выявить взаимосвязи между ними. На самом деле, не было эффектов севооборота или фунгицидов на активность этого фермента (Таблица 5). Lupwayi и др. (2024) сообщили об отрицательной корреляции между относительной численностью Acremonium spp. и активностью N-ацетил-β-глюкозаминидазы. Это исследование включало инсектицид ивермектин, который убил некоторых почвенных микроартропод (но не других), которые, предположительно, увеличили содержание хитина в почве, субстрата для N-ацетил-β-глюкозаминидазы. Второе наблюдение заключалось в том, что корреляции относительной численности родов грибов или прокариот с активностью β-глюкозидазы и арилсульфатазы были сходными, но противоположными корреляциям с кислотной фосфомоноэстеразой. Это означает, что цикл P был менее зависим от почвенного органического C, чем цикл S, вероятно, потому, что почвенный P существует во многих химических формах в дополнение к органическим формам. В дополнение к микробной минерализации органического P (Raguet и др., 2023), почвенный P может стать доступным для растений из химических пулов за счет химического растворения или фосфатмобилизующих микроорганизмов (Islam и др., 2024).
Бактериальный род Gaiella был основным идентифицируемым (присвоенным) таксоном прокариот, который присутствовал в 85% образцов почвы (Рисунок 5), хотя его относительная численность была самой высокой в севообороте горох-пшеница и самой низкой в севообороте ячмень-горох-пшеница (Рисунок 4C). Однако роль этой бактерии в круговороте питательных веществ в этих севооборотах неясна, поскольку ее относительная численность не коррелировала ни с какой ферментативной активностью. В севооборотах рис-пшеница и сахарный тростник-пшеница в Индии этот род считался способствующим росту растений, поскольку его относительная численность положительно коррелировала с доступностью N, P, K, Fe и S (Ansari и др., 2024). Однако в севооборотах кукуруза-соя и монокультуре сои в Китае его относительная численность отрицательно коррелировала с урожайностью сои (Xu и др., 2024). Следовательно, экологические услуги, предоставляемые Gaiella spp. системам растениеводства, могут зависеть от контекста.
Относительная численность родов грибов и прокариот была связана с активностью ферментов, участвующих в круговороте питательных веществ, чтобы оценить их вклад в питательный потенциал почвы для здоровья сельскохозяйственных культур. Другие исследования связывали такое обилие с защитным потенциалом почвы для здоровья сельскохозяйственных культур (Mazzola and Gu, 2002; Stirling и др., 2012; Siegel-Hertz и др., 2018). В сравнении почв, подавляющих фузариозное увядание, с почвами, способствующими фузариозному увяданию, Siegel-Hertz и др. (2018) сообщили, что следующие роды грибов (также обнаруженные в нашем исследовании, Таблица 6) были обнаружены исключительно в почвах, подавляющих фузариоз: Acremonium, Mortierella и Penicillium. Роды прокариот, которые были более многочисленны в почвах, подавляющих фузариоз, чем в почвах, способствующих фузариозу (также в нашей Вспомогательной таблице S1), были: Massilia, Arthrobacter и Rubrobacter. Следовательно, некоторые из родов, идентифицированных в нашем исследовании, вероятно, были вовлечены в круговорот питательных веществ (N, P и S) и в биологическую борьбу с болезнями.
5 Выводы
Мы получили ценную информацию о влиянии севооборота и фунгицидов на микробную биомассу почвы, состав и разнообразие прокариотных сообществ, а также на ферментативную активность, даже несмотря на то, что период исследования, вероятно, был недостаточно длительным для того, чтобы 3-летние севообороты сформировали почвенный микробиом. В то время как применение фунгицидов снизило грибное богатство в ризосфере пшеницы (например, индексы Chao1: 64,0 против 79,9), особенно в 2-летних севооборотах, продолжительность/тип севооборота и культуры, предшествовавшие пшенице, оказали различное влияние на относительную численность различных таксонов. Два из трех наиболее доминирующих типов прокариот, Proteobacteriota и Actinobacteriota, по-разному реагировали на продолжительность севооборота: 3-летние севообороты обогатили первые (относительная численность 27,4% против 20,1%), но 2-летние севообороты обогатили вторые (19,9% против 28,3%). По сравнению с масличными культурами, предшествовавшими отобранной пшенице, предшествующая культура гороха обогатила Actinobacteriota (относительная численность 31,7% против 24,8%) и наиболее многочисленный класс грибов Sordariomycetes (39,1% против 22,1%), в дополнение к увеличению микробной биомассы углерода (МБУ) и активности арилсульфатазы на 33% и 57% соответственно. Корреляции относительной численности родов грибов или прокариот с активностью β-глюкозидазы и арилсульфатазы были как положительными, так и отрицательными, но противоположными корреляциям с кислотной фосфомоноэстеразой, что предполагает, что цикл S был более тесно связан с циклом C, чем цикл P. Помимо ключевого значения этих характеристик почвенной микробиоты для питания сельскохозяйственных культур (круговорот питательных веществ), необходимо изучить их аспекты, связанные с биологической борьбой с болезнями.
Вспомогательный материал
Вспомогательный материал к этой статье можно найти онлайн по адресу: https://www.frontiersin.org/articles/10.3389/fagro.2024.1455448/full#supplementary-material
Ссылки
1. Abdulridha J., Ampatzidis Y., Ehsani R., de Castro A. I. (2018). Evaluating the performance of spectral features and multivariate analysis tools to detect laurel wilt disease and nutritional deficiency in avocado. Comput. Electron. Agric. 155, 203–2011. doi: 10.1016/j.compag.2018.10.016. CrossRef Google Scholar
2. Ansari W. A., Kumar M., Krishna R., Singh A., Zeyad M. T., Tiwari P., et al. (2024). Influence of rice-wheat and sugarcane-wheat rotations on microbial diversity and plant growth promoting bacteria: Insights from high-throughput sequencing and soil analysis. Microbiol. Res. 278, 127533. doi: 10.1016/j.micres.2023.127533. CrossRef Google Scholar
3. Bainard L. D., Navarro-Borrell A., Hamel C., Braun K., Hanson K., Gan Y. (2017). Increasing the frequency of pulses in crop rotations reduces soil fungal diversity and increases the proportion of fungal pathotrophs in a semiarid agroecosystem. Agric. Ecosyst. Environ. 240, 206–214. doi: 10.1016/j.agee.2017.02.020. CrossRef Google Scholar
4. Baldwin-Kordick R., De M., Lopez M. D., Liebman M., Lauter N., Marino J., et al. (2022). Comprehensive impacts of diversified cropping on soil health and sustainability. Agroecol. Sustain. Food Syst. 46, 331–363. doi: 10.1080/21683565.2021.2019167. CrossRef Google Scholar
5. Bellemain E., Carlsen T., Brochmann C., Coissac E., Taberlet P., Kauserud H. (2010). ITS as an environmental DNA barcode for fungi: an in silico approach reveals potential PCR biases. BMC Microbiol. 10, 189. doi: 10.1186/1471-2180-10-189. CrossRef Google Scholar
6. Bo-Ra K., Jiwon S., Robin B. G., Jun Hyung L., Doo Wan K., Kuk-Hwan S., et al. (2017). Deciphering diversity indices for a better understanding of microbial communities. J. Microbiol. Biotechnol. 27, 2089–2093. doi: 10.4014/jmb.1709.09027. CrossRef Google Scholar
7. Borase D. N., Murugeasn S., Nath C. P., Hazra K. K., Singh S. S., Kumar N., et al. (2021). Long-term impact of grain legumes and nutrient management practices on soil microbial activity and biochemical properties. Arch. Agron. Soil Sci. 67, 2015–2032. doi: 10.1080/03650340.2020.1819532. CrossRef Google Scholar
8. Bünemann E. K., Schwenke G. D., Van Zwieten L. (2006). Impact of agricultural inputs on soil organisms - a review. Australian J. Soil Res. 44, 379–406. doi: 10.1071/SR05125. CrossRef Google Scholar
9. Callahan B. J., McMurdie P. J., Rosen M. J., Han A. W., Johnson A. J. A., Holmes S. P. (2016). DADA2: High-resolution sample inference from Illumina amplicon data. Nat. Methods 13, 581–583. doi: 10.1038/nmeth.3869. CrossRef Google Scholar
10. Caporaso J. G., Lauber C. L., Walters W. A., Berg-Lyons D., Lozupone C. A., Turnbaugh P. J., et al. (2011). Global patterns of 16S rRNA diversity at a depth of millions of sequences per sample. Proc. Natl. Acad. Sci. U.S.A. 108, 4516–4522. doi: 10.1073/pnas.1000080107. CrossRef Google Scholar
11. Chong J., Liu P., Zhou G., Xia J. (2020). Using MicrobiomeAnalyst for comprehensive statistical, functional, and meta-analysis of microbiome data. Nat. Protoc. 15, 799–821. doi: 10.1038/s41596-019-0264-1. CrossRef Google Scholar
12. Deng S., Kang H., Freeman C. (2011). "Microplate fluorometric assay for soil enzymes," in Methods in Soil Enzymology. Ed. Dick R. P. (Madison, WI: Soil Science Society of America), 311–318. Google Scholar
13. Dick R. P., Breakwell D. P., Turco R. F. (1996). "Soil enzyme activities and biodiversity measurements as integrative microbiological indicators," in Methods for assessing soil quality. Eds. Doran J. W., Jones A. J. (Madison, WI: Soil Science Society of America), 247–271. Special Publication Number 49. Google Scholar
14. Gweon H. S., Oliver A., Taylor J., Booth T., Gibbs M., Read D. S., et al. (2015). PIPITS: an automated pipeline for analyses of fungal internal transcribed spacer sequences from the Illumina sequencing platform. Methods Ecol. Evol. 6, 973–980. doi: 10.1111/mee3.2015.6.issue-8. CrossRef Google Scholar
15. Han L., Kong X., Xu M., Nie J. (2021). Repeated exposure to fungicide tebuconazole alters the degradation characteristics, soil microbial community and functional profiles. Environ. pollut. 287, 117660. doi: 10.1016/j.envpol.2021.117660. CrossRef Google Scholar
16. Hansen J. C., Schillinger W. F., Sullivan T. S., Paulitz T. C. (2019). Soil microbial biomass and fungi reduced with canola introduced into long-term monoculture wheat rotations. Front. Microbiol. 10, 1488. doi: 10.3389/fmicb.2019.01488. CrossRef Google Scholar
17. Horwath W. R., Paul E. A. (1994). "Microbial biomass," in Methods of Soil Analysis. Part 2. Microbiological and Biochemical Properties. Eds. Weaver R. W., Angle S., Bottomly P., Bezdicek D., Smith S., Tabatabai A., Wollum A. (Madison, WI: Soil Science Society of America), 753–773. Google Scholar
18. Huo D., Malacrinò A., Lindsey L. E., Benitez M.-S. (2023). Subtle responses of soil bacterial communities to corn-soybean-wheat rotation. Phytobiomes J. 7, 392–400. doi: 10.1094/PBIOMES-05-22-0032-R. CrossRef Google Scholar
19. Islam M., Siddique K. H. M., Padhye L. P., Pang J., Solaiman Z. M., Hou D., et al. (2024). A critical review of soil phosphorus dynamics and biogeochemical processes for unlocking soil phosphorus reserves. Adv. Agron. 185, 153–249. doi: 10.1016/bs.agron.2024.02.004. CrossRef Google Scholar
20. Larney F. J., Pearson D. C., Blackshaw R. E., Lupwayi N. Z. (2017). Soil changes over 12 yr of conventional vs. conservation management on irrigated rotations in southern Alberta. Can. J. Soil Sci. 97, 249–265. doi: 10.1139/cjss-2016-0141. CrossRef Google Scholar
21. Liu C., Plaza-Bonilla D., Coulter J. A., Kutcher H. R., Beckie H. J., Wang L., et al. (2022). Diversifying crop rotations enhances agroecosystem services and resilience. Adv. Agron. 173, 299–335. doi: 10.1016/bs.agron.2022.02.007. CrossRef Google Scholar
22. Liu Q., Li T., Chen L., Zhang S., Zhao Y., Chen Y., et al. (2023a). Taxonomic and functional diversity of the soil microbiome recruited from alternative crops in a rotation system. Eur. J. Soil Sci. 74, e13410. doi: 10.1111/ejss.13410. CrossRef Google Scholar
23. Liu Q., Zhao Y., Li T., Chen L., Chen Y., Sui P. (2023b). Changes in soil microbial biomass, diversity, and activity with crop rotation in cropping systems: A global synthesis. Appl. Soil Ecol. 186, 104815. doi: 10.1016/j.apsoil.2023.104815. CrossRef Google Scholar
24. Lloyd A. W., Percival D., Yurgel S. N. (2021). Effect of fungicide application on lowbush blueberries soil microbiome. Microorganisms 9, 1366. doi: 10.3390/microorganisms9071366. CrossRef Google Scholar
25. Lu Y., Zhou G., Ewald J., Pang Z., Shiri T., Xia J. (2023). MicrobiomeAnalyst 2.0: comprehensive statistical, functional and integrative analysis of microbiome data. Nucleic Acids Res. 51, W310–W318. doi: 10.1093/nar/gkad407. CrossRef Google Scholar
26. Lupwayi N. Z., Clayton G. W., O'Donovan J. T., Harker K. N., Turkington T. K., Rice W. A. (2004a). Decomposition of crop residues under conventional and zero tillage. Can. J. Soil Sci. 84, 403–410. doi: 10.4141/S03-082. CrossRef Google Scholar
27. Lupwayi N. Z., Clayton G. W., O'Donovan J. T., Harker K. N., Turkington T. K., Rice W. A. (2004b). Soil microbiological properties during decomposition of crop residues under conventional and zero tillage. Can. J. Soil Sci. 84, 411–419. doi: 10.4141/S03-083. CrossRef Google Scholar
28. Lupwayi N. Z., Floate K. D., Petri R. M. (2024). The veterinary parasiticide ivermectin increased the activity of an enzyme that mediates soil chitin degradation on a prairie grassland. Appl. Soil Ecol. 197, 105338. doi: 10.1016/j.apsoil.2024.105338. CrossRef Google Scholar
29. Lupwayi N. Z., Kennedy A. C. (2007). Grain legumes in Northern Great Plains: impacts on selected biological soil processes. Agron. J. 99, 1700–1709. doi: 10.2134/agronj2006.0313s. CrossRef Google Scholar
30. Lupwayi N. Z., Lafond G. P., May W. E., Holzapfel C. B., Lemke R. L. (2012). Intensification of field pea production: impact on soil microbiology. Agron. J. 104, 1189–1196. doi: 10.2134/agronj2012.0046. CrossRef Google Scholar
31. Lupwayi N. Z., Zhang Y., Hao X., Thomas B. W., Eastman A. H., Schwinghamer T. D. (2019). Linking soil microbial biomass and enzyme activities to long-term manure applications and their nonlinear legacy. Pedobiol 74, 34–42. doi: 10.1016/j.pedobi.2019.04.001. CrossRef Google Scholar
32. Mazzola M., Gu Y. H. (2002). Wheat genotype-specific induction of soil microbial communities suppressive to disease incited by Rhizoctonia solani anastomosis group AG-5 and AG-8. Phytopathol. 92, 1300–1307. doi: 10.1094/PHYTO.2002.92.12.1300. CrossRef Google Scholar
33. McCully M. E., Miller C., Sprague S. J., Huang C. X., Kirkegaard J. A. (2008). Distribution of glucosinolates and sulphur-rich cells in roots of field-grown canola (Brassica napus). New Phytol. 180, 193–205. doi: 10.1111/j.1469-8137.2008.02520.x. CrossRef Google Scholar
34. Meyer C., Jeanbille M., Breuil M.-C., Bru D., Höfer K., Screpanti C., et al. (2024). Soil microbial community fragmentation reveals indirect effects of fungicide exposure mediated by biotic interactions between microorganisms. J. Hazard. Mater. 470, 134231. doi: 10.1016/j.jhazmat.2024.134231. CrossRef Google Scholar
35. Nayyar A., Hamel C., Lafond G., Gossen B. D., Hanson K., Germida J. (2009). Soil microbial quality associated with yield reduction in continuous-pea. Appl. Soil Ecol. 43, 115–121. doi: 10.1016/j.apsoil.2009.06.008. CrossRef Google Scholar
36. Raguet P., Cade-Menun B., Mollier A., Abdi D., Ziadi N., Karam A., et al. (2023). Mineralization and speciation of organic phosphorus in a sandy soil continuously cropped and phosphorus-fertilized for 28 years. Soil Biol. Biochem. 178, 108938. doi: 10.1016/j.soilbio.2022.108938. CrossRef Google Scholar
37. Riedo J., Yokota A., Walther B., Bartolomé N., van der Heijden M. G. A., Bucheli T. D., et al. (2023). Temporal dynamics of total and bioavailable fungicide concentrations in soil and their effect upon nine soil microbial markers. Sci. Total Environ. 878, 162995. doi: 10.1016/j.scitotenv.2023.162995. CrossRef Google Scholar
38. Roman D. L., Voiculescu D. I., Filip M., Ostafe V., Isvoran A. (2021). Effects of triazole fungicides on soil microbiota and on the activities of enzymes found in soil: a review. Agriculture 11, 893. doi: 10.3390/agriculture11090893. CrossRef Google Scholar
39. Schaedel M., Hidrobo G., Grossman J. (2021). From microns to meters: exploring advances in legume microbiome diversity for agroecosystem benefits. Front. Sustain. Food Syst. 5, 668195. doi: 10.3389/fsufs.2021.668195. CrossRef Google Scholar
40. Siegel-Hertz K., Edel-Hermann V., Chapelle E., Terrat S., Raaijmakers J. M., Steinberg C. (2018). Comparative microbiome analysis of a fusarium wilt suppressive soil and a fusarium wilt conducive soil from the Châteaurenard Region. Front. Microbiol. 9, e568. doi: 10.3389/fmicb.2018.00568. CrossRef Google Scholar
41. Stirling G. R., Smith M. K., Smith J. P., Stirling A. M., Hamill S. D. (2012). Organic inputs, tillage and rotation practices influence soil health and suppressiveness to soilborne pests and pathogens of ginger. Aust. Plant Pathol. 41, 99–112. doi: 10.1007/s13313-011-0096-0. CrossRef Google Scholar
42. Tan Y., Cui Y., Li H., Kuang A., Li X., Wei Y., et al. (2017). Rhizospheric soil and root endogenous fungal diversity and composition in response to continuous Panax notoginseng cropping practices. Microbiol. Res. 194, 10–19. doi: 10.1016/j.micres.2016.09.009. CrossRef Google Scholar
43. Vasilchenko A. V., Poshvina D. V., Semenov M. V., Timofeev V. N., Iashnikov A. V., Stepanov A. A., et al. (2023). Triazoles and strobilurin mixture affects soil microbial community and incidences of wheat diseases. Plants 12, 660. doi: 10.3390/plants12030660. CrossRef Google Scholar
44. Venter Z. S., Jacobs K., Hawkins H.-J. (2016). The impact of crop rotation on soil microbial diversity: A meta-analysis. Pedobiologia 59, 215–223. doi: 10.1016/j.pedobi.2016.04.001. CrossRef Google Scholar
45. Xu L., Jin S., Su Y., Lyu X., Yan S., Wang C., et al. (2024). Combined metagenomics and metabolomic analysis of microbial community structure and metabolic function in continuous soybean cropping soils of Songnen Plain, China. Chem. Biol. Technol. Agric. 11, 46. doi: 10.1186/s40538-024-00569-x. CrossRef Google Scholar
46. Yang X., Hu H.-W., Yang G.-W., Cui Z.-L., Chen Y.-L. (2023). Crop rotational diversity enhances soil microbiome network complexity and multifunctionality. Geoderma. 436, 116562. doi: 10.1016/j.geoderma.2023.116562. CrossRef Google Scholar
Lupwayi NZ, Turkington TK, Tidemann BD, Kubota H and Polo RO (2024) Crop rotation and fungicides impact microbial biomass, diversity and enzyme activities in the wheat rhizosphere. Front. Agron. 6:1455448. doi: 10.3389/fagro.2024.1455448
Перевод статьи «Crop rotation and fungicides impact microbial biomass, diversity and enzyme activities in the wheat rhizosphere » авторов Lupwayi NZ, Turkington TK, Tidemann BD, Kubota H and Polo RO., оригинал доступен по ссылке. Лицензия: CC BY. Изменения: переведено на русский язык
Фото: freepik















































































































Комментарии (0)