Аромат, который сводит трипса с ума: идентификация аттрактантов лилейника
Цветочный трипс (Frankliniella intonsa Trybom) — широко распространённый вредитель, угрожающий овощным культурам по всему миру, с серьёзными вспышками численности в регионах выращивания лилейника (Hemerocallis citrina Baroni) в Китае.
Аннотация
Методы: Летучие соединения H. citrina на стадиях листообразования, стеблевания и цветения были идентифицированы с помощью газовой хроматографии-масс-спектрометрии (ГХ-МС). Поведенческие тесты с использованием Y-образного ольфактометра и полевые эксперименты с ловушками были проведены для оценки привлекательности ключевых летучих веществ.
Результаты: Всего было обнаружено 60 летучих соединений, причём ароматические соединения (особенно сесквитерпены) были наиболее распространены в период пиковой численности трипсов. E-β-фарнезен, нерол и линалоол привлекали трипсов в концентрациях 100 мг/мл и 10 мг/мл в поведенческих тестах. Полевые испытания показали, что нерол (160,0 ± 98,6 трипсов на ловушку) и смешанная приманка (182,5 ± 83,7 трипсов на ловушку) обладают превосходной привлекательностью; жёлтые клеевые ловушки превзошли по эффективности ловушки других цветов. Три активных компонента синергично увеличивали отлов трипсов на всех типах ловушек.
Обсуждение: Эти результаты создают теоретическую основу для экологически безопасных стратегий борьбы с цветочным трипсом с использованием летучих веществ растений-хозяев.
1 Введение
Цветочный трипс (Frankliniella intonsa Trybom) является многоядным вредителем, поражающим многие сельскохозяйственные культуры, включая пасленовые, бобовые, бахчевые и крестоцветные овощи (Jones, 2005). В Китае и других регионах этот вредитель наносит значительный ущерб как на стадии имаго, так и на стадии нимфы, питаясь цветочными органами и лепестками, что приводит к сильному побелению и потере урожайности. Кроме того, F. intonsa является переносчиком различных растительных вирусов, таких как вирус бронзовости томата (TSMV), что усугубляет повреждение культур (Inoue и др., 2004; Jones, 2005). Имея широкий круг хозяев и высокую репродуктивную способность, они представляют собой серьезную угрозу для различных растений (Lim и др., 2013; Yang и др., 2024).
Лилейник (Hemerocallis citrina Baroni) – многолетнее травянистое растение семейства Асфоделовые (Asphodelaceae), обладающее значительной экономической, пищевой и декоративной ценностью, особенно в Восточной Азии (Zhao и др., 2024). Его съедобные, лекарственные и декоративные свойства делают его важной культурой в Китае и Корее (Wang и др., 2024). Однако в последние годы Китай столкнулся с существенными вспышками численности цветочного трипса, которые сильно повлияли на культивирование лилейника (Zhang D. и др., 2021). Основной вред наносится, когда трипсы питаются на нижней стороне листьев, цветоносах и бутонах, что приводит к снижению качества и урожайности лилейника (Wu и др., 2018). Современные методы борьбы в значительной степени полагаются на химические инсектициды, которые, хотя и эффективны, ускоряют развитие устойчивости к пестицидам и представляют риск для здоровья человека (Lim и др., 2013; Zhao и др., 2016). Следовательно, существует острая необходимость в устойчивых стратегиях борьбы с вредителями.
Летучие вещества растений-хозяев имеют ключевое значение в агрегационном и пищевом поведении трипсов. Насекомые-фитофаги часто выбирают растения-хозяева на основе специфических летучих сигналов, которые могут проявлять сильные аттрактантные свойства (Bruce and Pickett, 2011; Cao и др., 2019). Предыдущие исследования показали аттрактивное действие растительных летучих веществ на различных вредителей, таких как восточная плодожорка (Cydia molesta) к летучим веществам персика (Lu and Qiao, 2020), β-кариофиллен и лимонен к Bactrocera dorsalis (Liu и др., 2024; Ranaweeera and Hee, 2024), белокрылки к летучим веществам баклажанов и томатов (Darshanee и др., 2017). Исследования трипсов и летучих веществ растений-хозяев в первую очередь сосредоточены на следующих аспектах. Летучие органические соединения, выделяемые растениями-хозяевами, включая бензоиды, пиридины, терпены и сложные эфиры, играют ключевую роль в модуляции поведения трипсов. Например, бензоидные соединения, такие как бензальдегид, коричный альдегид, эвгенол, салициловый альдегид, 4-этилбензальдегид, 2-ацетофеноновый этиловый эфир, эвгенол и геранилбромид, показали значительные аттрактантные эффекты для Frankliniella occidentalis, Thrips tabaci, Thrips obscurus и F. intonsa (Qu и др., 2024; Han и др., 2015; Koschier, 2008; Kogel and Koschier, 2002; Avellaneda и др., 2021; Zhang Z. и др., 2021). Метилизоникотинат из пиридиновых соединений проявляет аттрактивную активность не только по отношению к F. occidentalis, T. tabaci и T. obscurus, но и против Megalurothrips sjostedti, Thrips imaginis и Thrips major. Он был успешно разработан в коммерческие аттрактанты для трипсов, включая Lurem-TR (Koppert Biological Systems) и P178 (Chem Tica) (Nielsen и др., 2021; Andrews, 2011). Терпеновые соединения, такие как линалоол, нерол и β-кариофиллен, проявляют аттрактивную активность по отношению к F. occidentalis, Megalurothrips usitatus и F. intonsa (Cao и др., 2020; Avellaneda и др., 2021; Li и др., 2021). Кроме того, этилизовалерат, α-пинен и гераниаль показывают аттрактивные эффекты на Thrips palmi (Li и др., 2021; Qu и др., 2024).
Цветочный трипс (F. intonsa) является важным насекомым-опылителем. Предварительные полевые обследования показали, что цветочный трипс повреждает в основном бутоны и цветки лилейника. Уровень зараженности пораженных растений составил 100% в период цветения. В тяжелых случаях наблюдалось более 50 трипсов на цветок. Следовательно, зависит ли агрегация и повреждение F. intonsa на цветках лилейника от привлечения специфическими летучими веществами цветков-хозяев? В этом исследовании были идентифицированы и проанализированы летучие компоненты, которые специфически появлялись в период заражения цветочным трипсом, и проведен скрининг летучих веществ с аттрактивной активностью по отношению к цветочному трипсу. Результаты исследования не только способствуют пониманию взаимодействия между трипсами и их растениями-хозяевами, но и создают теоретическую основу для разработки более точных и эффективных технологий регуляции поведения трипсов.
2 Материалы и методы
2.1 Насекомые и полевая динамика популяции
Цветочные трипсы были собраны с растений лилейника, выращенных в районе Юньчжун, Датун, Китай (долгота 113°32’, широта 40°30’), и использованы для создания лабораторной колонии. Колония непрерывно разводилась в течение более двух поколений на фасоли обыкновенной (Phaseolus vulgaris Linn) в пробирках для сбора насекомых (85 мм × 25 мм). Они содержались в контролируемой камере окружающей среды (PRX-450C, Beijing Haitian Youcheng Technology Co., Ltd., Китай) в условиях 16-часового светового и 8-часового темнового цикла, при температуре 25 ± 1°C и относительной влажности 60 ± 5%.
Для оценки популяционной динамики F. intonsa на H. citrina проводился еженедельный мониторинг на том же поле лилейника в районе Юньчжун, Датун, Китай, с начала июня по октябрь 2023 года. Этот период охватывал весь фенологический цикл лилейника, включая стадии вегетативного роста, цветения и старения. Каждую неделю обследовалось 30 случайно выбранных растений лилейника. Трипсы отбирались с помощью тонкой кисточки и аспиратора, затем сохранялись в 70% этаноле. Идентификация и подсчет проводились под стереомикроскопом (Olympus SZX16, Olympus). Трипсы подсчитывались на трех различных частях растения H. citrina: листьях, стеблях и цветочных органах, чтобы оценить их распределение. Доля трипсов на каждой части растения (листья, стебли, цветочные органы) рассчитывалась как средний процент от общей популяции трипсов на растение.
2.2 Химические вещества
Растительные одоранты β-Пинен (≧ 98%), Линалоол (≧ 98%), Нерол (≧ 97%) были приобретены в компании Shanghai Aladdin Biochemical Technology Co. (Шанхай, Китай), (E)-β-Фарнезен (≧ 98%) был приобретен в компании Shanghai Bide Pharmaceutical Technology Co. (Шанхай, Китай), β-оцимен (≧ 98%) и α-Куркумен (≧ 98%) были приобретены в компании J&K Scientific Ltd. (Пекин, Китай). Все химические вещества разбавлялись н-гексаном (Sigma-Aldrich), а концентрации химических веществ для дозовых зависимостей составляли 100, 10, 1 и 0,1 мкг/мкл.
2.3 Экстракция и идентификация летучих веществ
Летучие вещества экстрагировались из проростков, бутонов и цветков H. citrina с использованием динамического хедспейс-отбора. Растительные ткани (листья, стебли, цветки) осторожно иссекались с помощью стерильных скальпелей для минимизации механических повреждений и собирались в течение 5 минут для уменьшения выбросов летучих веществ, индуцированных ранением. Растительные ткани (120 г) помещались в стеклянную банку (диаметр 20 см, высота 28 см) и соединялись с помощью тефлоновых трубок с трубками из нержавеющей стали, заполненными адсорбентом Tenax-TA (60/80 меш, Sigma-Aldrich, Сент-Луис, Миссури, США). Трипсы проявляли отчетливые обонятельные реакции на шесть летучих соединений, выделяемых лилейником. E-β-фарнезен, нерол и линалоол продемонстрировали значительную привлекательность для трипсов, тогда как α-куркумен, β-пинен и β-оцимен не вызывали заметной обонятельной реакции. Примечательно, что нерол в концентрации 100 мкг/мкл вызывал самую высокую скорость привлечения, достигающую 88%, значительно превосходя другие протестированные летучие вещества (Рисунок 3). Очищенный воздух, пропущенный через осушающую колонку и колонку с активированным углем, нагнетался в мешок для отбора проб с помощью атмосферного пробоотборника (TY-08A, Tianyu Instrument Co., Ltd., Китай) со скоростью потока 500 мл/мин. Каждый образец собирался в течение 8 часов, с тремя биологическими повторностями для каждого типа ткани. Привлекательность трипсов к одному и тому же соединению значительно варьируется в различных концентрациях. F. intonsa проявляет высокозначимое предпочтение к более высоким концентрациям нерола (100 мкг/мкл и 10 мкг/мкл) и линалоола (10 мкг/мкл), причем реакции заметно больше, чем в контрольной группе. Кроме того, этот вид проявляет значительно более сильное привлечение к более низкой концентрации E-β-фарнезена (1 мкг/мкл) по сравнению с контролем (Рисунок 4).
После сбора адсорбционные трубки подвергались термической десорбции с помощью TD-30 (Shimadzu, Киото, Япония), используя следующие настройки для десорбции трубки: 3 минуты при 250°C, температура холодной ловушки -10°C в течение 3 минут; температура десорбции холодной ловушки 280°C, бессплит-поток 20 мл/мин в ГХ-МС (QP-2020NX, Shimadzu, Киото, Япония). Летучие вещества разделялись при следующих условиях: гелий (чистота 99,999%) служил газом-носителем с температурой импульсного бессплитного инжектора 270°C, температурная программа печи начиналась с 45°C (удерживание 2 минуты), повышение на 6°C/мин до 240°C, а затем удерживание 5 минут, всего 40 минут. Для разделения использовалась капиллярная колонка Rtx-5 MS (30 м × 0,25 мм × 0,25 мкм, Restek Corporation, США). Для масс-спектрометрии температура интерфейса и ионного источника была установлена на 280°C, применялась электронная ионизация (EI) при 70 эВ, а спектры регистрировались в режиме полного сканирования в диапазоне масс 45–600 А.е.м. Индексы удерживания соединений рассчитывались относительно стандартов н-алканов (C8-18) и сравнивались с библиотекой NIST20 MS, соответствующей индексам удерживания на https://webbook.nist.gov/, относительное содержание этих соединений рассчитывалось по их площадям пиков.
2.4 Анализ активности летучих веществ растений-хозяев
Обонятельная реакция цветочных трипсов на летучие соединения лилейника: (E)-β-Фарнезен, Нерол, Линалоол, α-Куркумен, β-Пинен и β-оцимен была протестирована с использованием Y-образного ольфактометра (плечи 10 см, основание 22 см, диаметр 2,9 см, угол 60° между плечами), накрытого картонной коробкой (50 см × 48 см × 33 см), открытой сверху. Среди всех протестированных обработок комбинация желтой клеевой ловушки и смешанной приманки достигла самой высокой эффективности отлова, составив 203,2 ± 48,8 трипса (Рисунок 5, ANOVA, df = 2, F = 63,0, P < 0,05). Арена ольфактометра освещалась сверху источником света 40 люкс. Трипсы, использованные в эксперименте, были одного поколения, выращенного на стручках зеленой фасоли. После 2-часового голодания 30 трипсов по отдельности помещались в Y-трубку с помощью мягкой кисточки. Считалось, что трипс сделал выбор, когда он пересек 2/3 одного плеча в течение 5 минут. В противном случае трипс считался не реагирующим. Все биоанализы проводились между 8:00 и 10:00 утра в помещении при 26°C и 65% относительной влажности, в период, когда трипсы проявляли активное поведение. Воздушный поток поддерживался на уровне 250 мл/мин, и плечи менялись местами после каждого испытания для устранения потенциального смещения. Для плеча с обработкой 10 мкл тестируемого раствора наносилось на кусок фильтровальной бумаги Whatman® (длина 5 см, ширина 5 мм). Для контрольного плеча предоставлялась фильтровальная бумага, содержащая 10 мкл н-гексана.
2.5 Полевые испытания
Полевые испытания проводились на поле лилейника в районе Юньчжоу, Датун, Китай (40°30' с.ш., 113°32' в.д.) с 11 по 14 июля 2023 года. Летучие соединения, включая (E)-β-Фарнезен, Нерол, Линалоол, α-Куркумен, β-Пинен и β-оцимен, разводились до 10 мкг/мкл, и 100 мкл раствора наносились на колоколообразные зеленые резиновые септы (диаметр 0,7 см, Qinghe Dingye Rubber and Plastic Products Co., Хэбэй, Китай) в качестве приманки. Приманка подвешивалась в центре желтых клеевых ловушек.
Для дальнейшей проверки синергического эффекта трех активных компонентов на клеевых насекомых досках, обычно используемых в производстве, раствор (с соотношением (E)-β-фарнезен : нерол : линалоол = 4,8 : 21,3 : 73,9, что соответствует их пропорции в цветках H. annuus) был приготовлен тем же методом, что описан выше, а затем подвешен в центре желтых, синих и желто-черных полосатых клеевых ловушек (Caoxian Agricultural Production Materials Co., Ltd., Шаньдун, Китай). Клеевые насекомые доски трех цветов размещались случайным образом.
Для установки клеевых ловушек использовались деревянные колья высотой 1,2 м. Клеевые ловушки подвешивались на высоте 1 м и на расстоянии 5 м друг от друга вдоль рядов лилейника. Общее количество трипсов, пойманных на каждой ловушке, подсчитывалось, с 80 повторностями для каждого аттрактанта. Среднее количество трипсов на одну карточку, включая обе стороны, подсчитывалось каждые три дня, с 80 повторностями для летучих компонентов и 20 повторностями для клеевых карточек различных цветов.
2.6 Анализ данных
Различия в распределении трипсов между частями растений и эффективность различных комбинаций летучих соединений в привлечении цветочных трипсов в полевых условиях были проанализированы с использованием однофакторного дисперсионного анализа (ANOVA). Для поведенческих результатов рассчитывалась доля трипсов, выбравших обработку и контроль. Для определения значимых различий использовались критерии хи-квадрат. Трипсы, не сделавшие окончательного выбора, не использовались в статистическом анализе.
3 Результаты
3.1 Популяционная динамика цветочного трипса
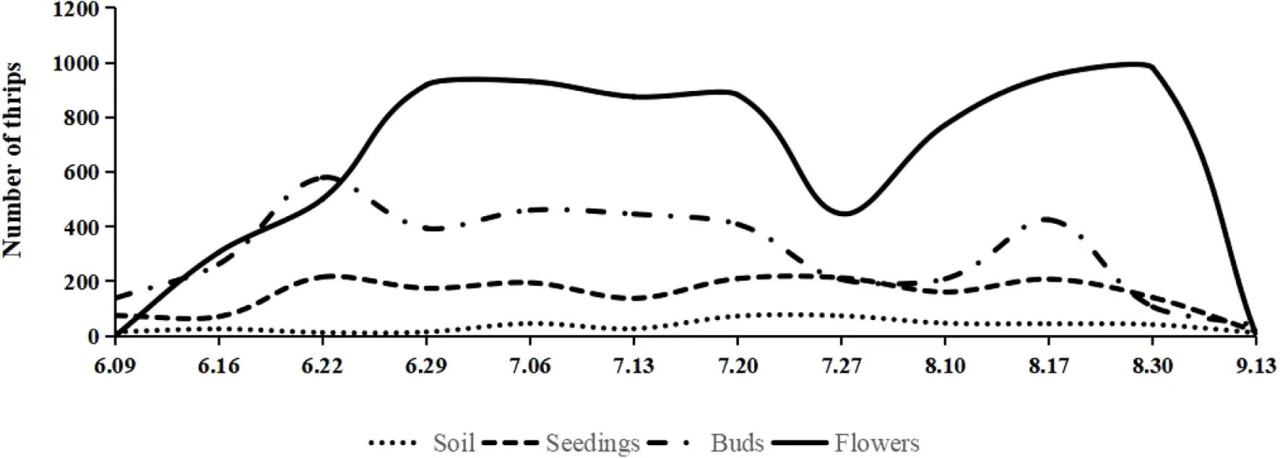
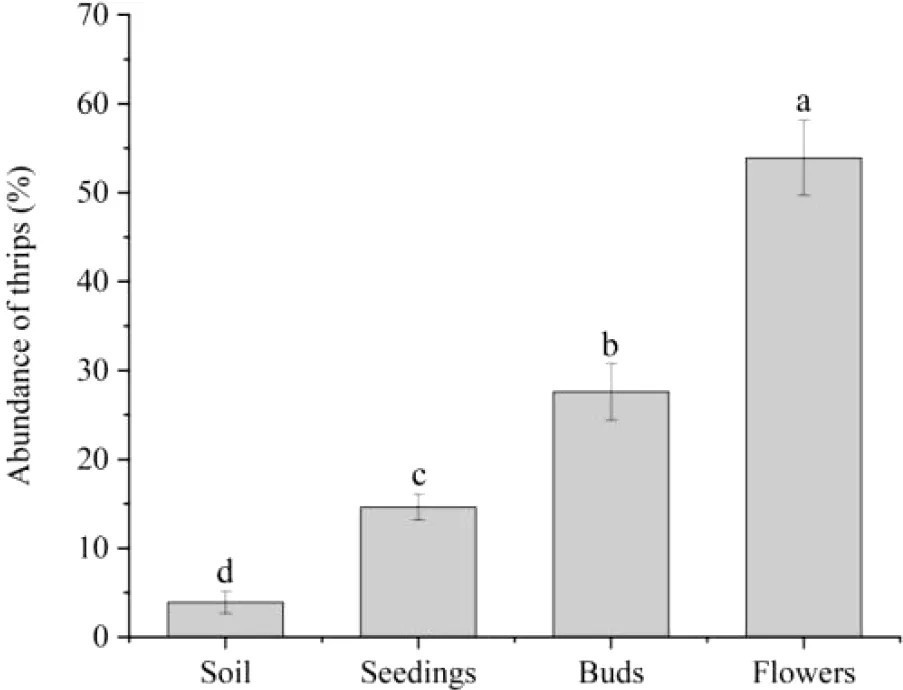
Цветочные трипсы впервые были обнаружены в начале июня в Датуне, Китай, что совпало с началом вегетационного сезона лилейника. По мере прохождения лилейником различных стадий развития, трипсы мигрировали на стебли к концу июня. С появлением цветочных бутонов с конца июня по начало июля трипсы сместили свои пищевые предпочтения на эти репродуктивные структуры. К концу сентября, по мере уменьшения количества цветков, трипсы рассеялись на альтернативных хозяев, включая Saussurea japonica. Зимовка начиналась в октябре, что означало конец их активного сезона на лилейнике (Рисунок 1). Распределение цветочных трипсов по различным частям лилейника было значимым (Рисунок 2, ANOVA df = 3, F = 48,4, P < 0,05). В течение вегетационного периода трипсы были наиболее многочисленны на цветочных органах, составляя 53,91 ± 4,25% популяции, затем на стеблях (27,58 ± 3,18%) и листьях (14,60 ± 1,46%), а наименьшее количество было в почве — 3,89 ± 1,26%.
Рисунок 1 Популяционная динамика цветочного трипса (Frankliniella intonsa) на лилейнике (Hemerocallis citrina). По мере роста лилейника трипсы мигрируют к бутонам и наносят повреждения в конце июня. После появления цветков с конца июня по начало июля вредители переключаются на цветки для питания; они входят в стадию зимовки в октябре.
Рисунок 2 Распределение цветочного трипса (Frankliniella intonsa) на частях лилейника (Hemerocallis citrina) в течение вегетационного сезона в Датуне, Китай. Обильность трипсов была самой высокой на цветочных органах (53,91 ± 4,25%), затем на стеблях (27,58 ± 3,18%) и листьях (14,60 ± 1,46%), самой низкой в почве (3,89 ± 1,26%). Обнаружены значительные различия в распределении трипсов между частями растений (df = 3, F = 58,4, P < 0,05).
3.2 Идентификация и анализ летучих веществ H. citrina
Было обнаружено шестьдесят летучих соединений, выделяемых из различных анатомических частей лилейника (листьев, стеблей и цветков), и они были классифицированы на восемь химических категорий: спирты, альдегиды, простые эфиры, фенолы, терпены, карбоновые кислоты, сложные эфиры, ароматические соединения и углеводороды. Примечательно, что шесть летучих соединений, а именно E-β-фарнезен, нерол, линалоол, α-куркумен, β-пинен и β-оцимен, присутствовали исключительно в бутонах и цветках. Значения LRT 31 соединения были сравнены с соответствующими индексами удерживания на https://webbook.nist.gov/chemistry/ для определения их химических структур (см. Дополнительную таблицу).
3.3 Обонятельная реакция трипсов на различные растительные летучие вещества
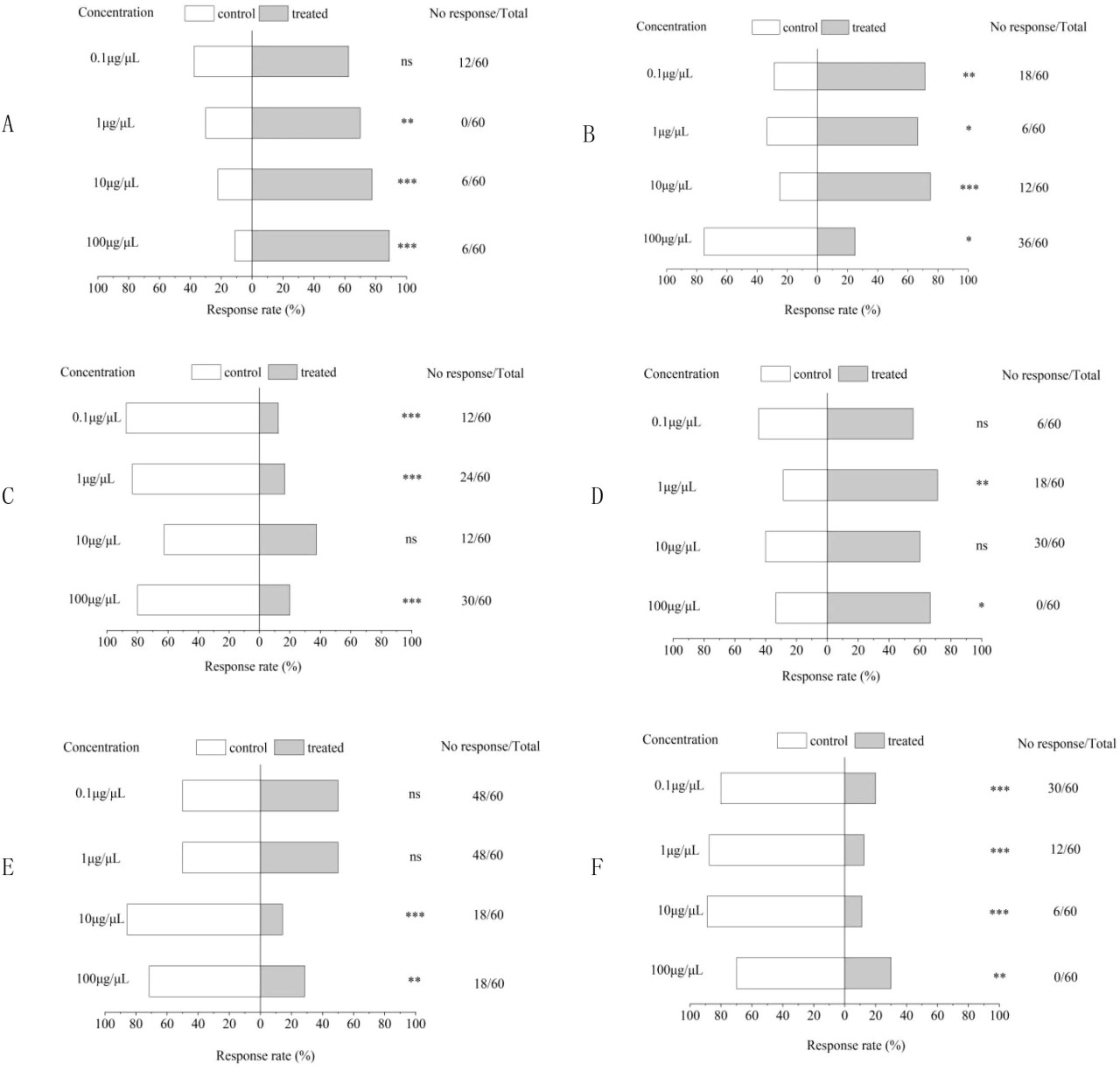
Трипсы проявляли отчетливые обонятельные реакции на шесть летучих соединений, выделяемых лилейником. E-β-фарнезен, нерол и линалоол продемонстрировали значительную привлекательность для трипсов, тогда как α-куркумен, β-пинен и β-оцимен не вызывали заметной обонятельной реакции. Примечательно, что нерол в концентрации 100 мкг/мкл вызывал самую высокую скорость привлечения, достигающую 88%, значительно превосходя другие протестированные летучие вещества.
Рисунок 3 Поведенческие реакции Frankliniella intonsa на шесть летучих соединений, выделяемых лилейником, в Y-образном ольфактометре. Столбцы представляют проценты выбора (n = 60) обработанного плеча [нерол (A), линалоол (B), β-оцимен (C), E-β-фарнезен (D), β-пинен (E) и α-куркумен (F) в четырех концентрациях] или контрольного плеча. Звездочки указывают на значительные различия (p < 0,05, p < 0,01, p < 0,001, критерий χ2; ns — не значимо).
Привлекательность трипсов к одному и тому же соединению значительно варьируется в различных концентрациях. F. intonsa проявляет высокозначимое предпочтение к более высоким концентрациям нерола (100 мкг/мкл и 10 мкг/мкл) и линалоола (10 мкг/мкл), причем реакции заметно больше, чем в контрольной группе. Кроме того, этот вид проявляет значительно более сильное привлечение к более низкой концентрации E-β-фарнезена (1 мкг/мкл) по сравнению с контролем.
3.4 Полевая привлекательность трипсов к различным растительным летучим веществам
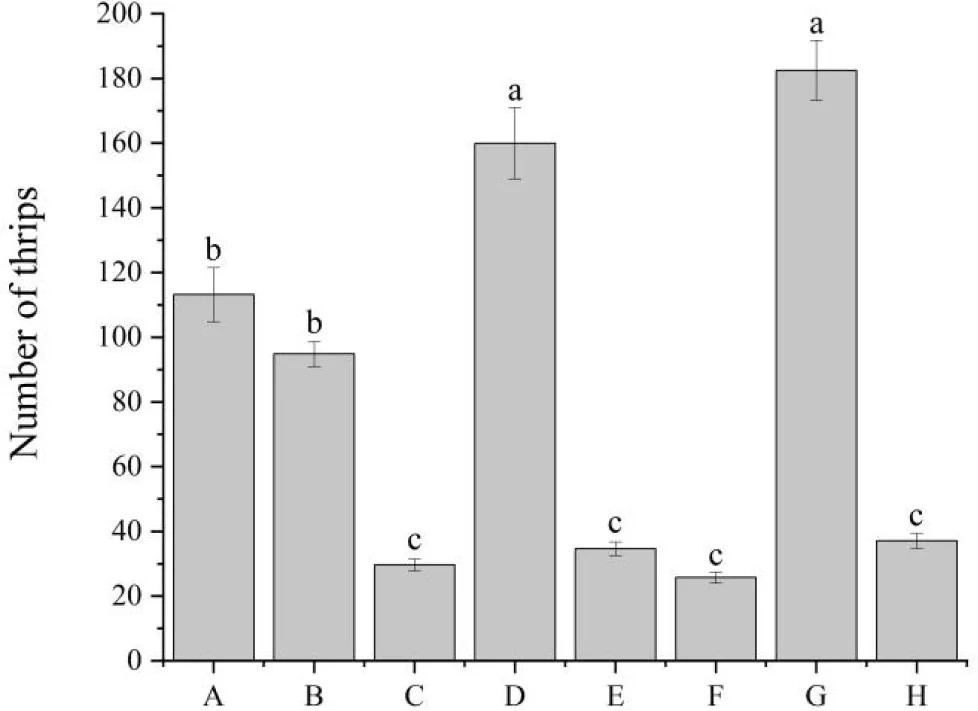
Полевой эксперимент показал, что нерол был наиболее эффективным аттрактантом, отлавливая в среднем 160,0 ± 98,6 трипсов на одну клеевую ловушку, хотя его превзошла смешанная приманка, которая отлавливала 182,5 ± 83,7 трипсов на ловушку. Однако разница между ними не является статистически значимой. Обе обработки значительно превзошли отдельные компоненты (E-β-фарнезен, линалоол, α-куркумен, β-пинен, β-оцимен) и контроль (ANOVA, df = 7, F = 100,7, P < 0,05).
Рисунок 4 Сравнительная полевая привлекательность Frankliniella intonsa к летучим компонентам. Смешанная приманка (G) отловила 182,5 ± 83,7 трипса на ловушку, превзойдя нерол (D), который отловил 160,0 ± 98,6 трипса на ловушку. Оба превзошли E-β-фарнезен (B), линалоол (A), α-куркумин (E), β-пинен (C), β-оцимен (F) и контроль (H). Статистический анализ (ANOVA, df = 7, F = 100,7, P < 0,05) подтвердил превосходную привлекательность нерола и смешанной приманки. Ось X: Обработка; Ось Y: Трипсов на ловушку.
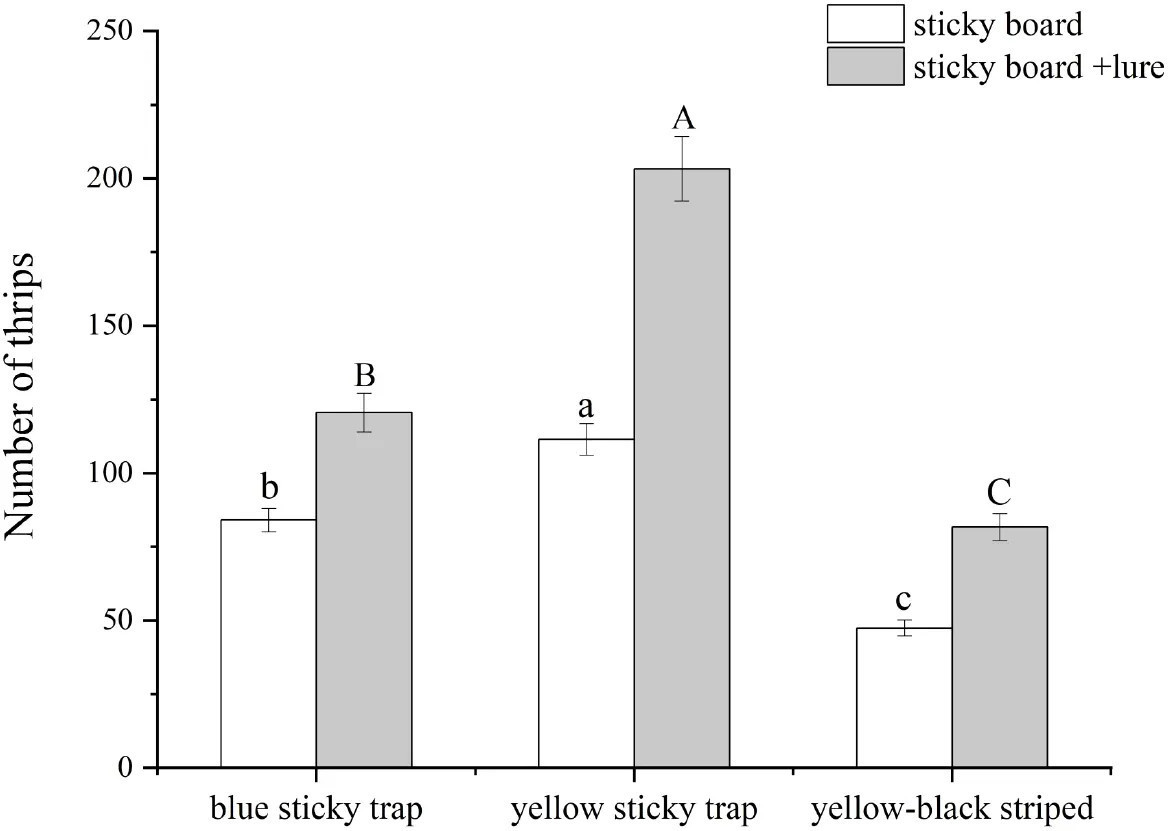
Клеевые ловушки различных цветов проявляют различную эффективность в привлечении F. intonsa. Желтая ловушка демонстрирует самую высокую эффективность привлечения, за ней следуют синие и желто-черные полосатые карточки (ANOVA, df = 2, F = 59,2, P < 0,05). В среднем, желтая клеевая ловушка отлавливала 111,5 ± 24,1 трипса, что примерно в 1,32 раза и 2,34 раза выше по сравнению с синими и желто-черными полосатыми карточками соответственно. При добавлении смешанной приманки привлекательность желтых, синих и желто-черных полосатых карточек для цветочных трипсов усиливалась. По сравнению с обработками без приманки, количество пойманных трипсов увеличилось на 82,3%, 43,3% и 72,1% для желтых, синих и желто-черных полосатых карточек соответственно. Среди всех протестированных обработок комбинация желтой клеевой ловушки и смешанной приманки достигла самой высокой эффективности отлова, составив 203,2 ± 48,8 трипса (ANOVA, df = 2, F = 63,0, P < 0,05).
Рисунок 5 Среднее количество Frankliniella intonsa, пойманных на желтые, синие и желто-черные полосатые ловушки с смешанным компонентом ((E)-β-фарнезен : нерол : линалоол = 4,8 : 21,3 : 73,9) и без него на поле лилейника. Желтые ловушки с смешанной приманкой отловили 203,2 ± 48,8 трипса на ловушку (ANOVA, df = 2, F = 63,0, P < 0,05).
4 Обсуждение
Цвет, морфология и летучие вторичные метаболиты растений играют важную роль в локализации хозяина трипсами (Teulon и др., 1993, 1999). Среди этих факторов летучие вторичные метаболиты, выделяемые листьями и цветками растений, играют ключевую роль в направлении поискового поведения хозяина трипсами (Lewis, 1997). Результаты обследования показывают, что популяция цветочных трипсов в почве остается стабильно низкой на протяжении всего периода роста лилейника, что указывает на то, что трипсы не размножаются локально, а скорее мигрируют с альтернативных растений-хозяев. В этом процессе летучие химические вещества, выделяемые растениями-хозяевами, играют ключевую роль в опосредовании дальних направленных перемещений трипсов. Распределение F. intonsa на лилейнике значительно выше на бутонах и цветках, чем на листьях и в почве, что предполагает, что вторичные метаболиты, присутствующие в цветочных структурах лилейника, оказывают аттрактивный эффект на популяции трипсов. В этом исследовании было обнаружено в общей сложности 60 летучих соединений в различных тканях лилейника. Среди них E-β-фарнезен, нерол, линалоол, α-куркумен, β-пинен и β-оцимен были обнаружены исключительно в основных местах скопления трипсов — бутонах и цветках. Дальнейшие поведенческие эксперименты продемонстрировали, что среди шести соединений E-β-фарнезен, нерол и линалоол проявляли сильную аттрактантную активность по отношению к цветочным трипсам в высокой концентрации (100 мкг/мкл и 10 мкг/мкл). Исследования показали, что низкие концентрации нерола оказывают значительные аттрактантные эффекты на F. occidentalis, Thrips hawaiiensis и Megalurothrips usitatus (Koschier и др., 2000; Han и др., 2015; Tang и др., 2015). Линалоол и его производные также проявляют аттрактантные свойства по отношению к различным видам трипсов. Например, 10% линалоол и линалоолоксид пиран значительно привлекают F. occidentalis (Hooper и др., 1999; Koschier и др., 2000), в то время как линалоол в объемной концентрации 10–6 привлекает T. hawaiiensis (Han и др., 2015), 10–2 привлекает M. usitatus (Tang и др., 2015), а в концентрации 10-3 мкл/мкл, как было показано, привлекает T. palmi (Cao и др., 2020). Кроме того, (E)-β-фарнезен в концентрациях 1% и 10% проявляет аттрактивную активность по отношению к F. occidentalis (Koschier и др., 2000; Katerinopoulos и др., 2005).
Дальнейшие полевые эксперименты продемонстрировали, что три соединения, (E)-β-фарнезен, нерол и линалоол в соотношении 4,8 : 21,3 : 73,9, а также каждое отдельное соединение, проявляли значительно большую привлекательность для цветочных трипсов по сравнению с другими отдельными компонентами. На сегодняшний день нет сообщений о применении этих трех соединений в полевой борьбе с трипсами. Однако нерол служит основным предшественником для искусственного синтеза агрегационного феромона цветочного трипса нер ил-(S)-2-метилбутаноата (Zhang и др., 2011), что предполагает, что нерол также может функционировать в качестве биосинтетического предшественника в естественном производстве этого феромона. Эта находка может предоставить основу для выяснения биосинтетического пути агрегационного феромона цветочного трипса.
Сообщалось, что синий цвет является самым привлекательным цветом для F. intonsa (Chen и др., 2017; Seo MiJa и др., 2006), за ним следуют по привлекательности белый (Mao и др., 2018) и розовый (Chen и др., 2025). В этом исследовании было обнаружено, что желтые карточки обладают значительно более сильной аттрактивной способностью, чем синие и желто-черные полосатые карточки для F. intonsa на поле лилейника. Результаты эксперимента показали, что цвет и материальный состав клеевых ловушек значительно различались в различных производителей. Следовательно, для точной оценки эффективности привлечения цветных пластин для трипсов необходимо определить значения RGB цветных пластин и их материальный состав (например, кукурузное волокно, полипропилен или бумага с полиэтиленовым покрытием) для всесторонней оценки.
Аттрактант проявляет синергический эффект на клеевых ловушках различных цветов, причем наиболее выраженное усиление наблюдается на желтых ловушках. Однако желтые клеевые ловушки не только отлавливают большое количество трипсов, но и привлекают полезных насекомых, таких как журчалки и божьи коровки. Более того, в практическом управлении вредителями их использование приводит к непреднамеренному удалению естественных врагов и требует значительных затрат труда и материалов для частой замены ловушек. Желто-черные полосатые ловушки, которые продемонстрировали сниженное неблагоприятное воздействие на естественных врагов и нецелевые организмы, в последние годы все чаще используются в грушевых садах для борьбы с такими вредителями, как тли и листоблошки (Zhao и др., 2018). Тем не менее, в этом исследовании желто-черные полосатые ловушки показали ограниченную эффективность в привлечении трипсов, что указывает на их непригодность для эффективного управления трипсами.
В заключение, E-β-фарнезен, нерол и линалоол предоставляют перспективные инструменты для мониторинга и контроля F. intonsa на H. citrina. Интегрируя растительные летучие вещества в IPM (комплексную борьбу с вредителями), данное исследование прокладывает путь к устойчивому управлению трипсами, снижая зависимость от пестицидов и повышая устойчивость сельского хозяйства. Будущие исследования должны быть направлены на оптимизацию летучих смесей, разработку формулировок с замедленным высвобождением инсектицидных адъювантов. Оценка воздействия на полезных насекомых также является ключевой для интеграции в IPM.
Дополнительный материал
Дополнительный материал к этой статье можно найти онлайн по адресу: https://www.frontiersin.org/articles/10.3389/fagro.2025.1699409/full#supplementary-material
Ссылки
1. Andrews P. (2011). Methyl isonicotinate-based attractants for thrips management. Pest Manage. Sci. 67, 1345–1350. doi: 10.1002/ps.2234. CrossRef Google Scholar
2. Avellaneda J., Díaz M., Coy-Barrera E., Rodríguez D., Osorio C. (2021). Rose volatile compounds allow the design of new control strategies for the western flower thrips (Frankliniella occidentalis). J. Pest Sci. 94, 129–142. doi: 10.1007/s10340-019-01131-7. CrossRef Google Scholar
3. Bruce T. J., Pickett J. A. (2011). Perception of plant volatile blends by herbivorous insects--finding the right mix. Phytochemistry 72, 1605–1611. doi: 10.1016/j.phytochem.2011.04.011. CrossRef Google Scholar
4. Cao Y., Li C., Yang H., Li J., Li S., Wang Y., et al. (2019). Laboratory and field investigation on the orientation of Frankliniella occidentalis (Thysanoptera: Thripidae) to more suitable host plants driven by volatiles and component analysis of volatiles. Pest Manage. Sci. 75, 598–606. doi: 10.1002/ps.5223. CrossRef Google Scholar
5. Cao Y., Wang J., Germinara G. S., Wang L., Yang H., Gao Y., et al. (2020). Behavioral responses of Thrips hawaiiensis (Thysanoptera: Thripidae) to volatile compounds identified from Gardenia jasminoides Ellis (Gentianales: Rubiaceae). Insects 11, 408. doi: 10.3390/insects11070408. CrossRef Google Scholar
6. Chen J., Niu L., Li L., Han D., Zhang F., Fu Y. (2017). Field trapping effect of different colors sticky cards to Frankliniella intonsa. J. Environ. Entomol. 39, 1169–1176. doi: 10.16380/j.kcxb.2017.06.013. CrossRef Google Scholar
7. Chen J., Wang Y., Li M. (2025). Color preference of Frankliniella intonsa in different cropping systems. J. Pest Sci. 98, 567–575. doi: 10.1007/s10340-024-01325-8. CrossRef Google Scholar
8. Darshanee H. L., Ren H., Ahmed N., Zhang Z.-F., Liu Y.-H., Liu T.-X. (2017). Volatile-mediated attraction of greenhouse whitefly Trialeurodes vaporariorum to tomato and eggplant. Front. Plant Sci. 8. doi: 10.3389/fpls.2017.01285. CrossRef Google Scholar
9. Han Y., Liu K., Wu J., Tang L. (2015). The Behavioral response of Frankliniella intonsa (Trybom) to eleven different chemicals. Chin. J. Trop. Crops 36, 1646–1649. Google Scholar
10. Hooper A. M., Bennison J. A., Luszniak M. C., Pickett J. A., Pow E. M., Wadhams L. J. (1999). Verbena× hybrida flower volatiles attractive to Western flower thrips, Frankliniella occidentalis. Pesticide. Sci. 55, 660–662. doi: 10.1002/(SICI)1096-9063(199906)55:6<660::AID-PS2>3.0.CO;2-V. CrossRef Google Scholar
11. Inoue T., Sakurai T., Murai T., Maeda T. (2004). Specificity of accumulation and transmission of tomato spotted wilt virus (TSWV) in two genera, Frankliniella and Thrips (Thysanoptera: Thripidae). Bull. Entomol. Res. 94, 501–507. doi: 10.1079/ber2004326. CrossRef Google Scholar
12. Jones D. R. (2005). Plant viruses transmitted by thrips. Eur. J. Plant Pathol. 113, 119–157. doi: 10.1007/s10658-005-2334-1. CrossRef Google Scholar
13. Katerinopoulos H. E., Pagona G., Afratis A., Stratigakis N., Roditakis N. (2005). Composition and insect attracting activity of the essential oil of Rosmarinus officinalis. J. Chem. Ecol. 31, 111–122. doi: 10.1007/s10886-005-0978-0. CrossRef Google Scholar
14. Kogel W. J., Koschier E. H. (2002). "Thrips responses to plant odors," in Thrips and Tospoviruses: Proceedings of the 7th international symposium on thysanoptera (Australian National Insect Collection, Canberra, Australia), p189–p190. Google Scholar
15. Koschier E. H. (2008). Essential oil compounds for thrips control--a review. Natural Product. Commun. 3, 1934578X0800300726. doi: 10.1177/1934578X0800300726. CrossRef Google Scholar
16. Koschier E. H., De Kogel W. J., Visser J. H. (2000). Assessing the attractiveness of volatile plant compounds to western flower thrips Frankliniella occidentalis. J. Chem. Ecol. 26, 2643–2655. doi: 10.1023/A:1026470122171. CrossRef Google Scholar
17. Lewis T. (1997). Thrips as crop pests (Wallingford, UK: CAB International). Google Scholar
18. Li X.-W., Zhang Z.-J., Hafeez M., Huang J., Zhang J.-M., Wang L.-K., et al. (2021). Rosmarinus officinialis L.(Lamiales: Lamiaceae), a promising repellent plant for thrips management. J. Econ. Entomol. 114, 131–141. doi: 10.1093/jee/toaa288. CrossRef Google Scholar
19. Lim U. T., Kim E., Mainali B. P. (2013). Flower model traps reduced thrips infestations on a pepper crop in field. J. Asia-Pac. Entomol. 16, 143–145. doi: 10.1016/j.aspen.2012.12.007. CrossRef Google Scholar
20. Liu L., Yang L., Yuan J., Zhang J., Liu C., Zhou H., et al. (2024). D-limonene is the active olfactory attractant in orange juice for Bactrocera dorsalis (Insecta: Diptera: Tephritidae). Life 14, 713. doi: 10.3390/life14060713. CrossRef Google Scholar
21. Lu P.-f., Qiao H.-l. (2020). Peach volatile emission and attractiveness of different host plant volatiles blends to Cydia molesta in adjacent peach and pear orchards. Sci. Rep. 10, 13658. doi: 10.1038/s41598-020-70685-9. CrossRef Google Scholar
22. Mao L., Chang Y., Yang F., Zhang L., Zhang Y., Jiang H. (2018). Attraction effect of different colored cards on thrips Frankliniella intonsa in cowpea greenhouses in China. Sci. Rep. 8, 13603. doi: 10.1038/s41598-018-32035-8. CrossRef Google Scholar
23. Nielsen H., Sigsgaard L., Kobro S., Jensen N. L., Jacobsen S. K. (2021). Species composition of thrips (Thysanoptera: Thripidae) in strawberry high tunnels in Denmark. Insects 12, 208. doi: 10.3390/insects12030208. CrossRef Google Scholar
24. Qu H., Chuai Z. R., Zhang W. B., Zhang J., Yun X. P., Liu J., et al. (2024). Host selection by thrips is affected by the floral volatile profile of sunflower. Plant. Cell Environ. 47, 4354–4368. doi: 10.1111/pce.15028. CrossRef Google Scholar
25. Ranaweeera P. H., Hee A. K. (2024). Attractancy of a sesquiterpene, β-caryophyllene to males of the oriental fruit fly, Bactrocera dorsalis (Diptera: Tephritidae). J. Chem. Ecol. 50, 1006–1009. doi: 10.1007/s10886-024-01480-3. CrossRef Google Scholar
26. Seo MiJa S. M., Kim SunJin K. S., Kang EunJin K. E., Kang MyongKi K. M., Yu YongMan Y. Y., Nam MyeongHyeon N. M., et al. (2006). Attraction of garden thrips, Frankliniella intonsa (Thysanoptera: Thripidae), to colored sticky cards in a Nonsan strawberry greenhouse. Crop Protection 25, 1011–1016. doi: 10.1016/S0261-2194(01)00119-3. CrossRef Google Scholar
27. Tang L., Han Y., Wu J., Fu B., Zhang R., Qiu H., et al. (2015). The effect of host plants and chemicals on behavioral response of Megalurothrips usitatus (Bagnall). J. Environ. Entomol. 37, 1024–1029. doi: 10.16380/j.kcxb.2015.05.015. CrossRef Google Scholar
28. Teulon D. A., Hollister B., Butler R. C., Cameron E. A. (1999). Color and odor responses of flying western flower thrips: wind tunnel and greenhouse experiments. Entomol. Experiment. Applicata. 93, 9–19. doi: 10.1046/j.1570-7458.1999.00557.x. CrossRef Google Scholar
29. Teulon D. A., Penman D. R., Ramakers P. M. (1993). Volatile chemicals for thrips (Thysanoptera: Thripidae) host finding and applications for thrips pest management. J. Econ. Entomol. 86, 1405–1415. doi: 10.1093/jee/86.5.1405. CrossRef Google Scholar
30. Wang L.-X., Wang Y.-H., Chen C., Liu J.-X., Li T., Li J.-W., et al. (2024). Advances in research on the main nutritional quality of daylily, an important flower vegetable of Liliaceae. PeerJ 12, e17802. doi: 10.7717/peerj.17802. CrossRef Google Scholar
31. Wu S., Tang L., Zhang X., Xing Z., Lei Z., Gao Y. (2018). A decade of a thrips invasion in China: lessons learned. Ecotoxicology 27, 1032–1038. doi: 10.1007/s10646-017-1864-6. CrossRef Google Scholar
32. Yang K., Han D., Wen J., Liang C., Zhan C., You Y., et al. (2024). Influence of temperature and host plant on the digestion of frankliniella intonsa (Trybom) revealed by molecular detection. Insects 15, 806. doi: 10.3390/insects15100806. CrossRef Google Scholar
33. Zhang Z., Hu H., Shang X. (2021). Identification of semiochemicals in cucumber leaves and their behavioral regulations on Western flower thrips Frankliniella occidentalis. J. Shanxi. Agric. Univ. (Natural. Sci. Edition). 41, 83–89. Google Scholar
34. Zhang D., Yao J., Huo Y. (2021). Practice and reflection on emergency control of yellow thrips in yunzhou district, datong city. China Plant Prot. Guide 11, 68–70. doi: 10.3969/j.issn.1672-6820.2021.11.028. CrossRef Google Scholar
35. Zhang Y., Li J., Wang Z. (2011). Biosynthesis of neryl-(S)-2-methylbutanoate, the aggregation pheromone of Frankliniella intonsa. J. Chem. Ecol. 37, 1215–1223. doi: 10.1007/s10886-011-0045-9. CrossRef Google Scholar
36. Zhao L., Li Q., Liu Z., Du H., Han F., Li J. (2018). State Intellectual Property Office of the People's Republic of China; Patent no. ZL201830550196.0. Google Scholar
37. Zhao R., Luo J., Xu B. (2024). Insights into secondary metabolites and health promoting effects of edible flower Hemerocallis citrina Baroni. J. Funct. Foods. 116, 106133. doi: 10.1016/j.jff.2024.106133. CrossRef Google Scholar
38. Zhao W., Wan Y., Xie W., Xu B., Zhang Y., Wang S., et al. (2016). Effect of spinosad resistance on transmission of tomato spotted wilt virus by the western flower thrips (Thysanoptera: Thripidae). J. Econ. Entomol. 109, 62–69. doi: 10.1093/jee/tov278. CrossRef Google Scholar
Liu H, Lv L, Su N, Wang J, Zhai X, Liu Z, Xing G and Li J (2026) Identification and characterization of volatile attractants for the flower thrips, (Frankliniella intonsa), from the host Hemerocallis citrina. Front. Agron. 7:1699409. doi: 10.3389/fagro.2025.1699409
Перевод статьи «Identification and characterization of volatile attractants for the flower thrips, (Frankliniella intonsa), from the host Hemerocallis citrina» авторов Liu H, Lv L, Su N, Wang J, Zhai X, Liu Z, Xing G and Li J., оригинал доступен по ссылке. Лицензия: CC BY. Изменения: переведено на русский язык










































































































Комментарии (0)