Опасно ли культивируемое мясо из рыбы, если клетки загрязнены микропластиком?
Культивируемое мясо, являющееся устойчивой альтернативой традиционному животноводству, привлекло внимание благодаря своим потенциальным экологическим и медицинским преимуществам. Однако опасения, связанные с загрязнением микропластиком, создают проблемы, особенно при получении клеток из морских организмов, склонных к биоаккумуляции микропластика. Кроме того, повсеместное присутствие микропластика в лабораторных условиях, в ингредиентах и в процессе производства повышает риск непреднамеренного загрязнения.
Аннотация
Данное исследование было сосредоточено на культурах клеток скелетной мускулатуры атлантической скумбрии (Scomber scombrus) для изучения воздействия микропластика, представленного флуоресцентными полиэтиленовыми микросферами (10–45 мкм), на функциональные свойства клеток, включая пролиферацию, жизнеспособность, экспрессию генов и процессы дифференцировки, критически важные для производства культивируемого мяса. Результаты показали значительное влияние на прикрепление и пролиферацию клеток при концентрациях микропластика 1 мкг/мл, 10 мкг/мл и 50 мкг/мл. Особенно заметно, что концентрация 10 мкг/мл оказывала наиболее выраженное воздействие на жизнеспособность клеток как на этапе прикрепления, так и на этапе пролиферации. Хотя результаты показали, что как концентрация, так и размер микропластика влияют на жизнеспособность клеток, дифференцировка клеток осталась неизменной, и требуются дальнейшие исследования дополнительных факторов. Эти выводы подчеркивают необходимость тщательного изучения взаимодействия микропластика с клетками для обеспечения безопасности пищевых продуктов и охраны здоровья в формирующейся индустрии культивируемого мяса.
1 Введение
Культивируемое мясо, полученное путем выращивания клеток животных, представляет собой инновационный сдвиг в производстве продуктов питания с потенциальными экологическими и медицинскими преимуществами (Rischer и др., 2020; Eibl и др., 2021; Dupuis и др., 2023; Jahir и др., 2023). Производимое в контролируемых условиях, этот подход не только минимизирует риски, связанные с загрязнителями традиционного животноводства, но и обещает более ресурсоэффективную методологию (Stephens и др., 2018). Недавние исследования показывают, что при интеграции возобновляемой энергии культивируемое мясо может обеспечить сокращение глобального потепления на 92%, загрязнения воздуха на 93%, использования земли на 95% и потребления воды на 78% по сравнению с традиционным выращиванием говядины (Vergeer и др., 2021; Kim и др., 2022; Sinke и др., 2023). По мере развития отрасли прогнозируется, что культивируемое мясо займет существенную долю рынка традиционного мяса и морепродуктов объемом 1,7 триллиона долларов, решая насущные проблемы, такие как вырубка лесов, утрата биоразнообразия и устойчивость к антибиотикам (Vergeer и др., 2021; Sinke и др., 2023).
В контролируемых лабораторных условиях культивируемое мясо производится из клеток, например, полученных от животных. Эти клетки проходят пролиферацию в специализированных средах для формирования мышечной ткани, представляя собой потенциально более безопасную, этичную и экологически устойчивую альтернативу традиционному производству мяса (Chriki и Hocquette, 2020; Ong и др., 2021). Однако потенциальной проблемой безопасности в этой инновации является загрязнение микропластиком. Один из путей потенциального загрязнения исходит от животных-доноров. Например, морские экосистемы являются известными резервуарами микропластика (Andrady, 2011; Cole и др., 2011; Ivar do Sul и Costa, 2014). Это приводит к биоаккумуляции в морских организмах, таких как рыбы и устрицы (Galloway и др., 2017; Sharma и Chatterjee, 2017; Bhuyan, 2022; Courtene-Jones и др., 2022). Когда такие морские организмы служат животными-донорами для извлечения клеток, необнаруженный микропластик может быть непреднамеренно внесен в процесс культивирования. Существующие аналитические методологии часто не позволяют обнаружить более мелкие частицы микропластика, что приводит к потенциальной недооценке их обилия в организмах-донорах (Huppertsberg и Knepper, 2018; Lv и др., 2021; Vivekanand и др., 2021; Adhikari и др., 2022). Другим значительным источником загрязнения является сама лабораторная среда. Исследования подчеркнули повсеместный характер микропластика в лабораторных условиях, возникающего в результате деградации повсеместно используемого пластикового оборудования, контейнеров и расходных материалов (Löder и др., 2017; Schymanski и др., 2018; Koelmans и др., 2019). Процесс производства культивируемого мяса требует использования различных пластиковых устройств, включая биореакторы, пипетки, флаконы для клеточных культур и другое оборудование, которое вступает в прямой контакт со средой и растущими клетками (Allan и др., 2019; Lee и др., 2022).
Микропластик — крошечные фрагменты пластика размером менее 5 мм — привлек значительное внимание из-за его вездесущности в окружающей среде и потенциальных рисков, которые он представляет для здоровья человека (Lim, 2021; Diamantidou и др., 2022; Leslie и др., 2022; Lwanga и др., 2022; Osman и др., 2023; Tsochatzis и др., 2023). При проглатывании эти частицы могут проходить через желудочно-кишечный тракт, и некоторые данные свидетельствуют о том, что более мелкие частицы микропластика и нанопластика могут даже проникать в ткани, попадая в кровеносную и лимфатическую системы (Campanale и др., 2020; Hirt и Body-Malapel, 2020; Jiang и др., 2020; Kannan и Vimalkumar, 2021; Yee и др., 2021; Diamantidou и др., 2022; Leslie и др., 2022; Fournier и др., 2023; Li и др., 2023; Ramsperger и др., 2023; Tsochatzis и др., 2023). Эти фрагменты могут действовать как переносчики различных токсикантов, включая тяжелые металлы, полициклические ароматические углеводороды и химические вещества, нарушающие работу эндокринной системы (Campanale и др., 2020; Abbasi и др., 2021; Amelia и др., 2021; Yee и др., 2021; Karla Lizzeth и др., 2023), тем самым вводя эти вредные агенты в организм человека. С клеточной точки зрения риски микропластика становятся более сложными. Прямое взаимодействие между клетками и микропластиком может приводить к физическим нарушениям, таким как повреждение мембраны (Fleury и Baulin, 2021; Dai и др., 2022; Wang и др., 2022), а химические вещества, входящие в состав этих пластиков или выщелачивающиеся из них, как известно, вызывают окислительный стресс, воспалительные реакции и генотоксические эффекты (Hirt и Body-Malapel, 2020; Goodman и др., 2021; Alqahtani и др., 2023; Cao и др., 2023; Herrala и др., 2023; Jeyavani и др., 2023; Mattioda и др., 2023). Потенциальные риски такого взаимодействия включают поражения ДНК, дисфункцию органов, метаболические нарушения, иммунологические аберрации, нейротоксичность и нарушения репродуктивных процессов и процессов развития (Galluzzi и др., 2018). Более того, предыдущие исследования показали потенциальную связь между воздействием микропластика и развитием или обострением некоторых хронических заболеваний, таких как сердечно-сосудистые заболевания, включая тромбоз, атеросклероз, рак и диабет (Lee и др., 2023; Wu и др., 2023). Учитывая документально подтвержденные неблагоприятные последствия микропластика при проглатывании, понимание и смягчение этих рисков имеет первостепенное значение для индустрии культивируемого мяса (EFSA Panel on Contaminants in the Food Chain CONTAM, 2016; Rubio-Armendáriz и др., 2022; Mamun и др., 2023; Ziani и др., 2023).
Хотя присутствие и потенциальная опасность микропластика все больше осознаются, понимание точных механизмов, с помощью которых он влияет на клеточные функции, остается критически важным направлением исследований (O'Neill и Lawler, 2021; Thornton Hampton и др., 2022). Чтобы более полно понять клеточные последствия воздействия микропластика, мы использовали культуры клеток скелетной мускулатуры атлантической скумбрии (Scomber scombrus), ранее созданные и охарактеризованные Saad и др. (2023), учитывая их значимость для производства культивируемого мяса. В этом исследовании использовались флуоресцентные полиэтиленовые микросферы (10–45 мкм) в качестве репрезентативного микропластика — диапазона размеров, ранее зафиксированного у рыб (Thiele и др., 2021; Makhdoumi и др., 2023). Наша работа была направлена на выяснение воздействия микропластика на клеточные функциональные свойства, с акцентом на жизнеспособность клеток на этапах прикрепления и роста, а также на клеточную дифференцировку, которые являются ключевыми процессами в производстве культивируемого мяса (O'Neill и др., 2021; Reiss и др., 2021). В исследовании использовались концентрации микропластика 1 мкг/мл, 10 мкг/мл и 50 мкг/мл. Предварительные результаты показали, что все обработки значительно повлияли на прикрепление клеток (на 2-й день) и пролиферацию (на 4-й день), при этом не было обнаружено различимых эффектов на дифференцировку клеток через 2 недели. Такие переменные, как размер микропластика и концентрация, потенциально влияли на эти результаты. Эти выводы, хотя и предварительные, предоставляют фундаментальные сведения для последующих исследований, подчеркивая важность понимания взаимодействия микропластика с клетками для обеспечения безопасности пищевых продуктов, защиты здоровья человека и смягчения воздействия на окружающую среду.
2 Материалы и методы
2.1 Приготовление и поддержание клеточных культур
Клеточные линии скумбрии (MACK2), использованные в этом исследовании, были получены из лаборатории доктора Дэвида Л. Каплана в Университете Тафтса. Приготовление клеток проводилось в соответствии с протоколом, описанным Saad и др. (2023). Кратко, замороженные клетки на 81-м пассаже были разморожены с использованием 9 мл полной ростовой среды, которая состояла из среды Лейбовица L-15 (Gibco™, Биллингс, МТ, США), дополненной 20% фетальной бычьей сывороткой (FBS, Gibco™, Биллингс, МТ, США), 1 нг/мл фактора роста FGF2-G3 (человеческий) (Defined Bioscience, Сан-Диего, Калифорния, США), 20 мМ HEPES (Gibco™, Биллингс, МТ, США) и 1% антибиотика-антимикотика (Gibco™, Биллингс, МТ, США). Клеточную суспензию затем центрифугировали при 500 RCF в течение 6 минут, и полученный осадок ресуспендировали в 10 мл ростовой среды. Клетки инкубировали в культуральном флаконе площадью 75 см² (Thermo Fisher Scientific, Уолтем, Массачусетс, США) при 27°C в инкубаторе без CO₂. Поддержание клеток включало регулярный пассаж при примерно 70% конфлюэнтности и посев с плотностью примерно 5000 клеток/см². Альтернативно, клетки хранили путем замораживания в ростовой среде, дополненной 10% диметилсульфоксида (DMSO, Sigma Aldrich, Сент-Луис, Миссури, США).
2.2 Приготовление микропластика и воздействие
В этом исследовании использовались флуоресцентные зеленые полиэтиленовые микросферы, полученные от Cospheric LLC (Голета, Калифорния, США). Микросферы имели размер в диапазоне 10–45 мкм. Перед экспериментами был проведен процесс стерилизации с использованием 91% изопропилового спирта (IPA), позволяя избыточной жидкости стекать по мере постепенного испарения сфер. Впоследствии стерилизованные микросферы были интегрированы в полную ростовую среду, дополненную 0,01% Твин 20. Микросферы вводили в экспериментальную установку в концентрациях 1, 10 и 50 мкг/мл на основе предыдущих исследований (Schirinzi и др., 2017; Hwang и др., 2020; Palaniappan и др., 2022). В исследование был включен экспериментальный контроль, состоящий из полной ростовой среды с 0,01% Твин 20, но без микросфер. Для достижения равномерного распределения микросфер в ростовой среде на предварительном этапе перед каждым экспериментом проводилась обработка среды с микросферами ультразвуком.
2.3 Влияние микропластика на прикрепление и жизнеспособность клеток
Клетки скумбрии высевали в трех повторностях в 6-луночные планшеты с плотностью посева примерно 5000 клеток/см². Клетки культивировали при постоянной температуре 27°C без CO₂. Для изучения влияния микропластика на разные стадии клеточного роста использовали два различных экспериментальных условия. В первом сценарии микропластик вносили в клеточную среду перед посевом для оценки его влияния на прикрепление клеток — ключевой начальный этап пролиферации клеток. Через 48 часов инкубации клетки достигли логарифмической фазы роста и были отсоединены от поверхности планшета с использованием 0,25% трипсина-ЭДТА (Thermo Fisher Scientific, Уолтем, Массачусетс, США). Жизнеспособность клеток оценивали с помощью теста с трипановым синим и автоматического счетчика клеток Countess 3 FL (Invitrogen™, Thermo Fisher Scientific, Уолтем, Массачусетс, США). Этот анализ использует дифференциальное поглощение клетками красителя трипанового синего для различения и подсчета жизнеспособных и нежизнеспособных клеток. Параметры прибора, включая пороги подсчета и коэффициенты разбавления красителя, были установлены в соответствии со спецификациями производителя для обеспечения точности и воспроизводимости показателей жизнеспособности. Во втором сценарии микропластик вносили в клеточную среду после достижения логарифмической фазы роста, при этом старую среду заменяли либо свежей средой, содержащей микропластик, либо контрольной свежей средой. После внесения микропластика клетки оставляли нетронутыми на 4 дня, что позволяло изучить потенциальные взаимодействия между микропластиком и клетками. После этого периода взаимодействия клетки отсоединяли и определяли количество жизнеспособных клеток, что позволило получить представление о влиянии микропластика на рост клеток после начальных этапов пролиферации.
2.4 Влияние микропластика на дифференцировку клеток
2.4.1 Анализ экспрессии генов методом RT-qPCR
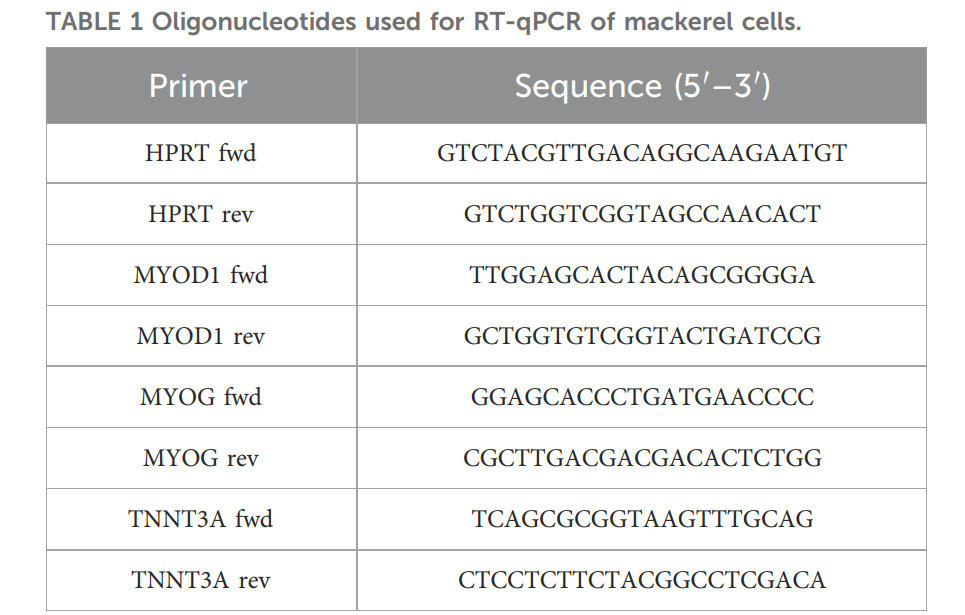
Клетки скумбрии на 82-м пассаже отсоединяли от 6-луночных планшетов с помощью трипсина в течение 3–4 минут и осаждали центрифугированием в течение 7,5 минут при 500 RCF. РНК экстрагировали из образцов с использованием набора NucleoSpin RNA (Mackerey-Nagel, Дюрен, Германия) и количественно определяли с помощью флуориметра Qubit 4 с использованием набора Qubit RNA High Sensitivity (HS) (Thermo Fisher Scientific, Уолтем, Массачусетс, США). Библиотеки кДНК для каждого образца были созданы из 100 нг РНК с использованием мастер-микса PrimeScript RT (Takara Bio, Кутацу, Япония) в соответствии со спецификациями производителя. Контроль без обратной транскриптазы (-RT) был приготовлен из образца с наиболее высоким выходом РНК путем недобавления мастер-микса к образцу. Мастер-микс PrimeScript RT содержит как случайные гексамеры, так и олиго-dT праймеры. RT-qPCR проводили в термоциклере CFX Opus 96 (Bio-Rad, Геркулес, Калифорния, США) с использованием премикса TB Green Advantage qPCR (Takara Bio, Кутацу, Япония) и олигонуклеотидов, указанных в Таблице 1. Праймеры были разработаны с использованием референсного генома южного голубого тунца (Thunnus maccoyii; NBCI RefSeq GCF_910596095.1) Saad и др. (2023). Было выполнено три технических повторности для каждого образца и гена, а также для контролей -RT и без матрицы (NTC). Условия амплификации были следующими: начальный этап 30 с при 95°C, затем 40 циклов по 5 с при 95°C и 30 с при 60°C, и финальный анализ диссоциации: 15 с при 65°C с увеличением на 0,5°C/с до достижения 95°C. Абсолютные значения экспрессии генов были рассчитаны как 2^(-ΔCt) с использованием гена гипоксантингуанинфосфорибозилтрансферазы (HPRT) в качестве домашнего гена. Относительные значения экспрессии генов были рассчитаны как 2^(-ΔΔCt) относительно контроля 0 нг/мл микропластика.
ТАБЛИЦА 1 Олигонуклеотиды, использованные для RT-qPCR клеток скумбрии.
2.4.2 Иммуноокрашивание
Чтобы наблюдать влияние микропластика на дифференцировку клеток, было проведено иммуноокрашивание на тяжелую цепь миозина в соответствии с протоколом, описанным Saad и др. (2023). Клетки скумбрии культивировали при 100% конфлюэнтности в ростовой среде и подвергали воздействию микропластика в различных концентрациях с последующим наблюдением в течение 14-дневного периода дифференцировки. После культивирования клетки фиксировали 4% параформальдегидом при комнатной температуре в течение 30 минут (Thermo Fisher Scientific, Уолтем, Массачусетс, США). Затем клетки промывали фосфатно-солевым буфером (PBS, Sigma Aldrich, Берлингтон, Массачусетс, США) и пермеабилизировали в течение 10 минут с использованием 0,1% Тритона-X (Sigma Aldrich, Берлингтон, Массачусетс, США). После пермеабилизации клетки блокировали в течение 30 минут с использованием 1× блокирующего буфера (Abcam, Кембридж, Великобритания), после чего следовала дополнительная промывка PBS. Раствор первичных антител, MF-20 (4 мкг/мл), наносили на клетки и инкубировали в течение ночи при 4°C. После последующей промывки PBS клетки проходили дополнительный 30-минутный этап блокировки с использованием 1× блокирующего буфера, а затем инкубировались в течение 1 часа со вторичными антителами — Goat Anti-Mouse IgG H&L (Alexa Fluor® 594, Abcam, Кембридж, Великобритания) и реагентом Phalloidin-iFluor 488 (Abcam, Кембридж, Великобритания) — каждое разведенное 1:1000 в 1× блокирующем буфере. После финальной промывки PBS ядра клеток окрашивали 4′,6-диамидино-2-фенилиндолом (DAPI, 1 мкг/мл, Thermo Fisher Scientific, Уолтем, Массачусетс, США) в PBS в течение 15 минут при комнатной температуре. Визуализацию проводили с использованием флуоресцентного микроскопа (DP27, Olympus Life Science, Токио, Япония), оснащенного светодиодной системой освещения (CoolLED, Андовер, Великобритания). Для оценки морфологии и структуры клеток на различных уровнях детализации использовались несколько объективов (4x, 10x, 20x). Изображения, полученные с объективами 4x и 10x, использовались для общей ориентации и обзоров с более низким разрешением, в то время как объектив 20x использовался для детальной визуализации, необходимой для выводов.
2.5 Статистический анализ
Статистический анализ проводился с использованием однофакторного дисперсионного анализа (ANOVA), при этом t-критерий использовался для сравнения между двумя параметрами с использованием статистического программного обеспечения Minitab.
3 Результаты и обсуждение
3.1 Жизнеспособность клеток
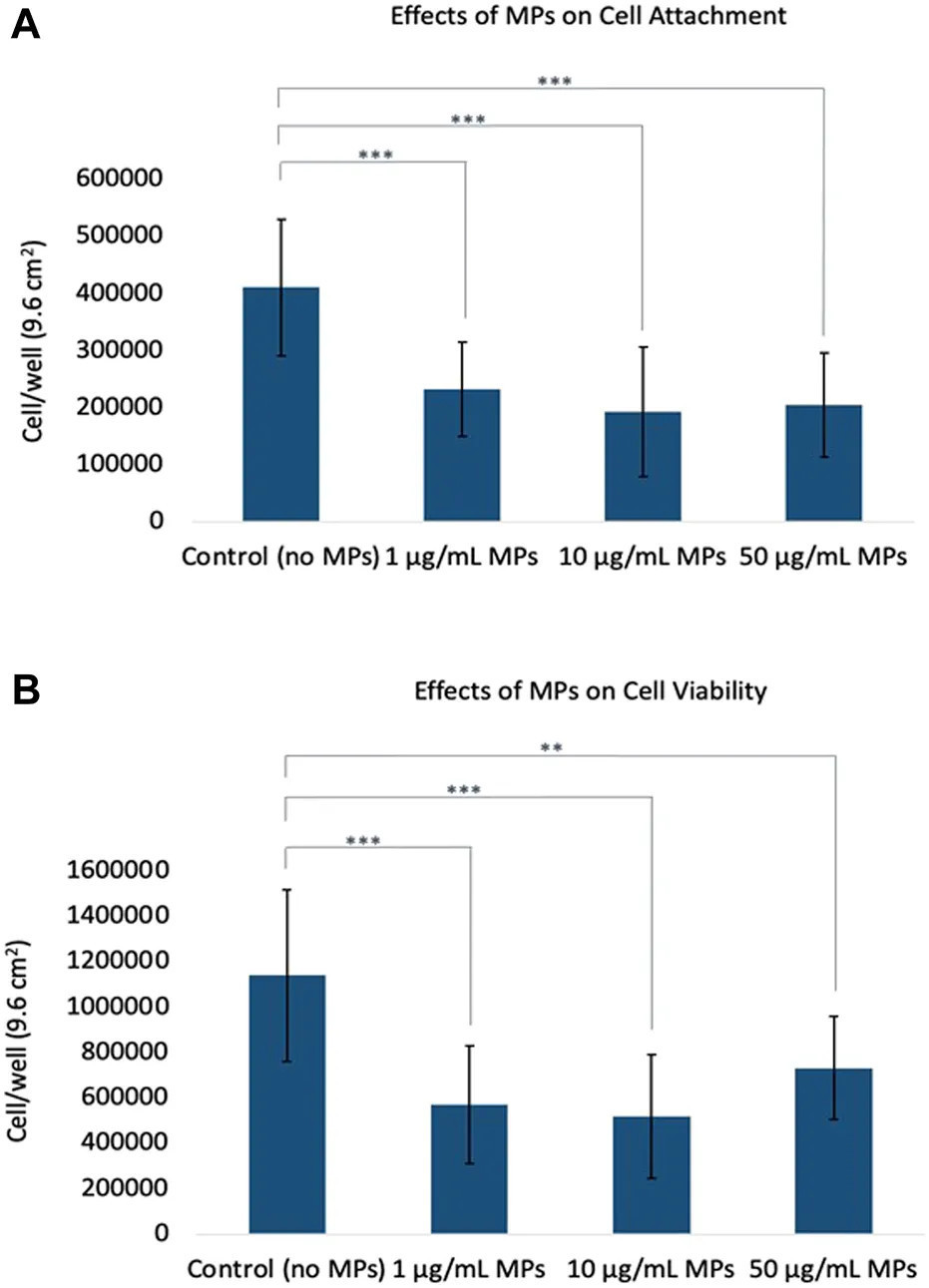
Жизнеспособность клеток как на этапе прикрепления, так и на этапе роста имеет первостепенное значение для производства мяса. На этапе прикрепления клетки должны успешно закрепиться на каркасе или матрице, чтобы предотвратить их потерю во время смены среды, создавая прочную основу для последующих этапов. После успешного прикрепления эти клетки должны эффективно пролиферировать, обеспечивая достаточную популяцию клеток для формирования мышечной ткани. Любая значительная гибель клеток или снижение пролиферации на этих этапах может подорвать общий выход и эффективность производства (Allan и др., 2019; Bodiou и др., 2020). Чтобы исследовать влияние микропластика на жизнеспособность клеток скумбрии на этапах прикрепления и роста, в этом исследовании микропластик вносили к клеткам в разное время. Рисунок 1A показал результаты воздействия микропластика на начальное прикрепление клеток при внесении в клеточную среду перед посевом, и статистический анализ выявил высокозначимую разницу в количестве клеток между группами (ANOVA, p < 0,001). И наоборот, Рисунок 1B показал влияние микропластика на пролиферацию клеток при добавлении после того, как клетки достигли логарифмической фазы роста, что также продемонстрировало статистически значимые изменения в скорости пролиферации (ANOVA, p < 0,001). Начальное количество клеток для посева составляло ~5000 клеток/см², а площадь поверхности 6-луночного планшета составляет 9,6 см². Сбор данных проводился на 2-й день для Рисунка 1A и на 4-й день для Рисунка 1B, что соответствовало заметному увеличению гибели клеток и отсоединению. На Рисунке 1A экспериментальная контрольная группа (без микропластика) показала количество клеток 410 000, тогда как у клеток, обработанных микропластиком, наблюдалось снижение примерно до половины этого числа. Аналогично, Рисунок 1B показал контрольное количество клеток 1 100 000, при этом у обработанных микропластиком оно составляло от 510 000 до 730 000. Примечательно, что присутствие микропластика привело к снижению количества клеток, причем концентрация 10 мкг/мл стабильно показывала самую низкую жизнеспособность. Основные причины и потенциальные механизмы, ответственные за эту тенденцию, подробно рассматриваются в следующих разделах.
РИСУНОК 1 Влияние микропластика на жизнеспособность клеток. (A) Влияние микропластика на начальное прикрепление клеток при внесении в клеточную среду перед посевом. (B) Воздействие микропластика на пролиферацию клеток после достижения клетками логарифмической фазы роста. Планки погрешностей представляют стандартное отклонение. Для оценки различий между каждой обработкой МП и экспериментальным контролем использовали t-критерий; звездочки указывают на значимое различие при p < 0,01 () и p < 0,001 ().
3.1.1 Влияние концентрации на жизнеспособность клеток
Это исследование выявляет сложную динамику воздействия микропластика (МП) и его влияние на жизнеспособность клеток скумбрии, обнаруживая потенциально нелинейную зависимость «доза-ответ». Методологически клетки подвергались воздействию МП в концентрациях 1, 10 и 50 мкг/мл. Примечательно, что наиболее выраженное снижение жизнеспособности клеток наблюдалось при промежуточной концентрации (10 мкг/мл), что бросает вызов общепринятой парадигме «доза-ответ», постулирующей повышение токсичности с увеличением концентрации. Это подтверждалось тенденциями жизнеспособности клеток, где для Рисунка 1A порядок был: контроль > 1 мкг/мл > 50 мкг/мл > 10 мкг/мл, а для Рисунка 1B: контроль > 50 мкг/мл > 1 мкг/мл > 10 мкг/мл. Эти результаты противоречат нескольким предыдущим исследованиям, в которых сообщалось о прямой дозозависимой токсичности МП. Например, Palaniappan и др. (2022) провели исследование с участием мышиных фибробластов L929 и эпителиальных клеточных линий MDCK и отметили дозозависимое снижение жизнеспособности клеток при воздействии 1, 10 или 20 мкг/мл ПЭ или ПС микросфер. Кроме того, их исследование показало усиление окислительного стресса при более высоких дозах МП, о чем свидетельствует повышенная экспрессия гена SOD3. В другом исследовании (Lee и др., 2021) клетки эндотелия пупочной вены человека (HUVEC) подвергались воздействию полистирольного микропластика (ПС-МП, 0–100 мкг/мл), что показало, что более высокие дозы заметно снижали жизнеспособность клеток и нарушали формирование ангиогенных трубок в краткосрочной перспективе, в то время как после длительного воздействия индуцировали аутофагическую и некротическую гибель клеток. Кроме того, в другом исследовании, сосредоточенном на среде кишечника человека (Herrala и др., 2023), исследователи оценили токсикологические последствия частиц сверхвысокомолекулярного полиэтилена (250–1000 мкг/мл) на клетки колоректальной аденокарциномы человека Caco-2 и HT-29. 48-часовая экспозиция этих полиэтиленовых частиц привела к дозозависимому снижению жизнеспособности клеток и сопутствующему повышению окислительного стресса. Окислительное повреждение было особенно выражено в митохондриях, что проливает свет на более широкие проблемы со здоровьем.
Сложное взаимодействие между концентрацией МП и его потенциальными цитотоксическими эффектами очевидно. Хотя значительная часть литературы подтверждает дозозависимое снижение жизнеспособности клеток, существуют определенные исключения. В недавнем исследовании in vitro, изучающем влияние микропластика (ПВХ и ПЭ) на лейкоциты головной почки средиземноморского дорада и европейского морского окуня (HKL) (Espinosa и др., 2018), было обнаружено, что воздействие различных концентраций микропластика в течение 1 и 24 часов не оказывало значительного влияния на жизнеспособность клеток HKL. Кроме того, высокие дозы микропластика приводили к минимальным изменениям ключевых клеточных функций врожденного иммунитета, включая снижение фагоцитоза и повышение активности респираторного взрыва. Эти расходящиеся результаты подчеркивают значение дальнейших исследований с учетом типа микропластика, размера и конкретной клеточной среды для окончательных выводов о более широком влиянии МП на клеточное здоровье. Наши результаты вносят вклад в этот развивающийся нарратив, предполагая, что взаимодействие между МП и биологическими системами может быть более сложным, чем считалось ранее.
3.1.2 Влияние размера микропластика и агрегации
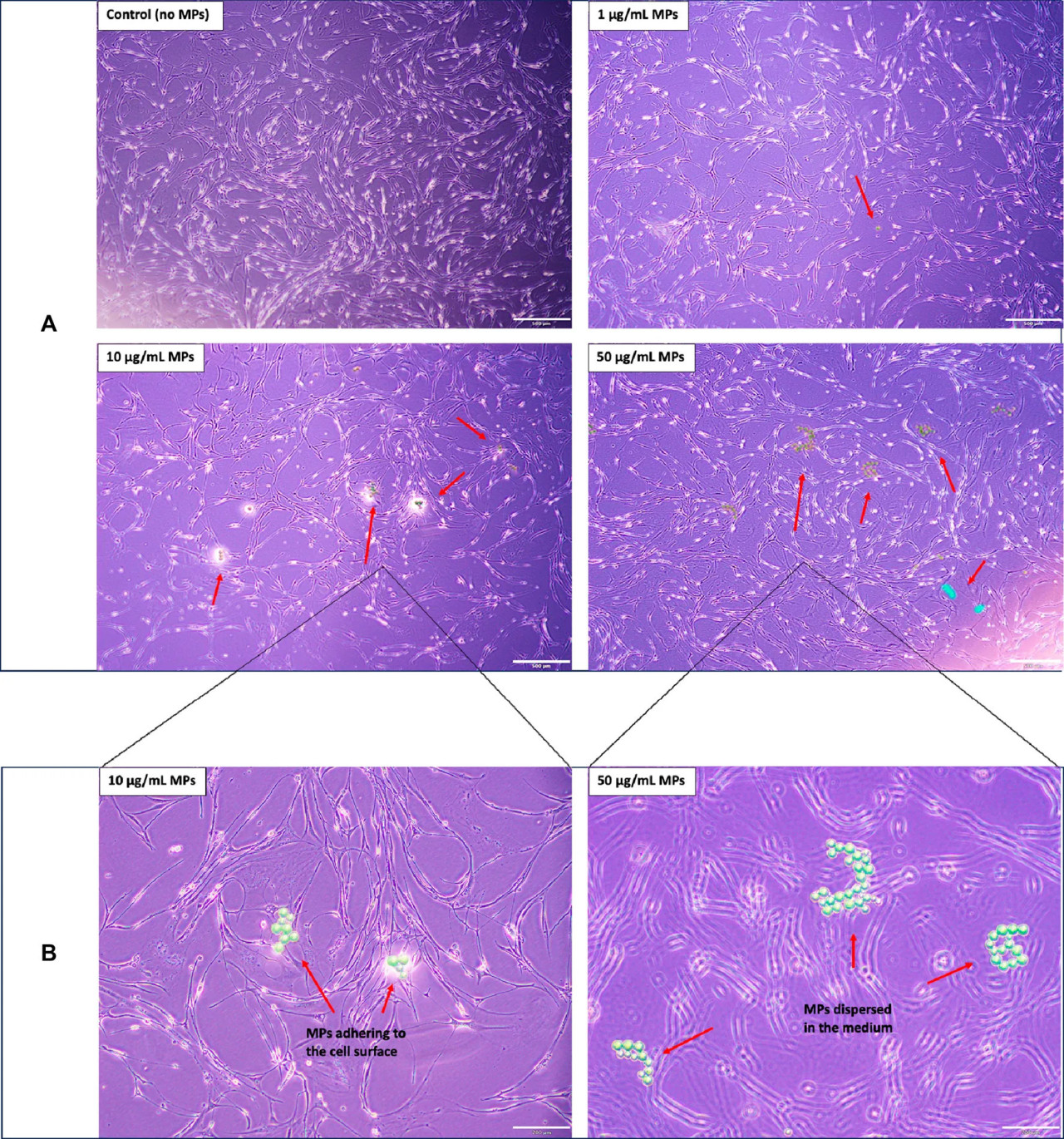
В дополнение к концентрации, мы наблюдали, что размер и состояние агрегации МП играют ключевую роль в опосредовании их взаимодействия с клетками скумбрии. В частности, при концентрации 10 мкг/мл МП были склонны прилипать к поверхности клеток, либо по отдельности, либо в виде небольших агрегатов, что приводило к наиболее значительному снижению жизнеспособности клеток. И наоборот, концентрация 50 мкг/мл приводила к образованию более крупных агрегатов МП, которые оставались в суспензии в культуральной среде, ограничивая их контакт с клетками, как показано на Рисунке 2. Это отсутствие клеточного взаимодействия, особенно в сценариях, где МП вносились после прикрепления клеток, соответствует минимальному влиянию на жизнеспособность клеток, наблюдаемому при этой более высокой концентрации (тенденция количества клеток на Рисунке 1B: контроль > 50 мкг/мл > 1 мкг/мл > 10 мкг/мл). Таким образом, выраженные эффекты при 10 мкг/мл подчеркивают потенциал специфических размеров МП, которые поддерживают тесный клеточный контакт, нарушать жизнеспособность клеток. Размышляя о роли размера и агрегации микропластика в жизнеспособности клеток, наши результаты согласуются с появляющимися исследованиями, которые изучают сложные воздействия микропластика на клеточное здоровье. Систематический обзор оценил взаимосвязи «доза-ответ» в отношении микропластика и жизнеспособности клеток путем анализа исследований вплоть до марта 2021 года (Danopoulos и др., 2022). Из 17 рассмотренных исследований 8 были включены в мета-регрессионный анализ. В обзоре были определены четыре эффекта, связанных с МП: цитотоксичность, иммунный ответ, окислительный стресс и барьерные свойства, при этом генотоксичность не показала эффекта. Ключевыми предикторами гибели клеток были неправильная форма МП, продолжительность воздействия и концентрация МП. Примечательно, что клетки Caco-2 проявляли повышенную восприимчивость к МП. Концентрации всего 10 мкг/мл (5–200 мкм) влияли на жизнеспособность клеток, в то время как 20 мкг/мл (0,4 мкм) влияли на высвобождение цитокинов. Эти результаты согласуются с нашими наблюдениями, в частности, со значительным снижением жизнеспособности клеток при 10 мкг/мл, что предполагает, что не только концентрация, но и физическая форма МП модулирует их цитотоксичность.
РИСУНОК 2 Морфологический анализ клеток скумбрии с обработкой МП и без нее: (A) Изображения с малым увеличением (объектив 4X), показывающие морфологию клеток скумбрии после 4 дней инкубации с различными концентрациями МП. Красные стрелки указывают на наблюдаемые МП или агрегаты МП. Масштабная линейка соответствует 500 мкм. (B) Изображения с большим увеличением (объектив 10X), предоставляющие детальные виды морфологии клеток для обработок МП 10 мкг/мл и 50 мкг/мл, соответствующих образцам, показанным на Рисунке 2A. Масштабная линейка соответствует 200 мкм.
В подробном исследовании Zhang и др. (2022) были изучены воздействия полистирольных микросфер (ПС-МП) и наносфер (ПС-НП) четырех различных размеров: 0,1, 0,5, 1 и 5 мкм. Это исследование выявило явное предпочтение клеточного поглощения более мелкими наночастицами по сравнению с их более крупными аналогами. Примечательно, что ПС-МП оказывали минимальное влияние на жизнеспособность клеток и апоптоз. Однако в группах с высокой концентрацией были заметны тонкие признаки окислительного стресса. Поразительное различие наблюдалось в повреждении мембраны: ПС-МП вызывали значительно большее повреждение, чем ПС-НП, что подчеркивает зависимость клеточных ответов от размера при воздействии МП. Развивая тему влияния размера микропластика на клетки, исследование токсичности полистирольных (ПС) частиц дополнительно прояснило эти сложные взаимосвязи (Hwang и др., 2020). Исследователи обнаружили, что ПС-частицы действуют как потенциальные иммунные стимуляторы, вызывая продукцию цитокинов и хемокинов в зависимости от размера и концентрации. Более крупные ПС-частицы (диаметром 10–100 мкм) демонстрировали незначительную цитотоксичность. Напротив, более мелкие частицы, особенно размером 460 нм и 1 мкм, отрицательно влияли на эритроциты. Их увеличенная площадь поверхности, которая облегчает более сильные взаимодействия, такие как силы Ван-дер-Ваальса, была определена как причина гемолиза. Кроме того, воздействие этих более мелких ПС-частиц приводило к повышению секреции IL-6, что указывает на потенциальное воспаление на ранней стадии. Однако исследование также показало отсутствие существенного повышения секреции гистамина, что снижает опасения по поводу гистамин-индуцированного воспаления или аллергических реакций. Поглощение частиц происходило в основном посредством эндоцитоза и фагоцитоза фагоцитирующими клетками, что приводило к локальному воспалению через высвобождение провоспалительных цитокинов, а не к прямой цитотоксичности (Hwang и др., 2020). В дополнение к описанным примерам, другие исследования стабильно указывают на то, что размер частиц микропластика значительно влияет на клеточные взаимодействия. Примечательно, что более мелкие частицы связаны с повышенным клеточным поглощением, более выраженными воспалительными реакциями, повышенной скоростью апоптоза и усиленными клеточными стрессовыми реакциями (Wright и Kelly, 2017; Revel и др., 2018; Yong и др., 2020). Эти результаты подчеркивают потенциальные риски для здоровья, связанные с более мелкими частицами микропластика.
3.1.3 Потенциальные взаимодействия и другие вовлеченные факторы
Взаимодействие между клетками и микропластиком представляет собой многогранный процесс, на который влияет совокупность факторов, таких как физико-химические свойства микропластика, клеточные характеристики, токсичность мономеров, добавок и олигомеров в частицах, а также преобладающие условия окружающей среды (Revel и др., 2018; Smith и др., 2018; Campanale и др., 2020; Leslie и др., 2022). Эта динамичная взаимосвязь приобретает значение при рассмотрении потенциальных последствий микропластика для клеточного здоровья (Lee и др., 2023; Li и др., 2023). Хотя в этом исследовании в основном иллюстрировалось влияние размера и дозы микропластика на жизнеспособность клеток, важно вписать эти выводы в расширенную систему факторов, модулирующих взаимодействия микропластика с клетками. Полимерный состав микропластика (например, тип полимера, наличие добавок и потенциал микропластика поглощать другие загрязнители окружающей среды), например, часто ассоциируется с дискретными цитотоксическими эффектами (Duis и Coors, 2016; Revel и др., 2018; Hwang и др., 2020). Форма микропластика дополнительно уточняет этот спектр взаимодействий. Сообщалось, что волокнистый микропластик может вызывать физические повреждения, дополнительно воздействовать на ткани или вызывать закупорки (Wright и др., 2013; Watts и др., 2015; Diamantidou и др., 2022; Leslie и др., 2022; Tsochatzis и др., 2023), тогда как сферические микрогранулы, распространенные в средствах личной гигиены, могут облегчать более гладкую клеточную интернализацию (Wright и др., 2013). Выцветание добавок в полимерных материалах, таких как пластификаторы, смазочные материалы, стабилизаторы, антиоксиданты, которые добавляются производителем для улучшения свойств полимеров, может мигрировать на поверхность полимеров из-за разделения фаз (Nouman и др., 2017). Как правило, эти добавки представляют собой незамещенные амиды, полученные из длинноцепочечных жирных кислот. Сообщалось, что цитотоксичность, связанная с этими добавками, может возникать из-за выщелачивания выцветших материалов в растворимой форме или из-за прямого контакта между выцветшими веществами и клетками (Kim и др., 2003).
Наномасштабный микропластик может приводить к образованию активных форм кислорода (ROS), что предполагает, что он может вызывать стресс у клеток, способствуя окислительным реакциям (Campanale и др., 2020; Paul и др., 2020; Yee и др., 2021). Сопутствующие воспалительные реакции могут дестабилизировать клеточный гомеостаз, возможно, знаменуя начало апоптоза (Elmore, 2007; Wright и др., 2013; Lamichhane и др., 2023). Также могут быть прямые физические эффекты, такие как потенциальное повреждение или закупорка тканей, особенно у организмов с несколькими типами клеток (Bhagat и др., 2021; Yee и др., 2021). Некоторые клеточные сигналы стресса, в частности p-JNK и p-p38, подчеркивают, что микропластик можно рассматривать как агенты, вызывающие стресс (Jeong и др., 2016; Jeong и др., 2017; Scopetani и др., 2020). Также стоит отметить, что разные организмы и типы клеток могут по-разному реагировать на эти пластики (Jeong и Choi, 2019; Bhagat и др., 2021). Понимание этих многогранных взаимодействий имеет решающее значение для выяснения воздействия микропластика на клеточную жизнеспособность и разработки стратегий смягчения их потенциальных неблагоприятных последствий.
3.2 Дифференцировка клеток
Дифференцировка клеток имеет первостепенное значение в процессе производства культивируемого мяса, служа незаменимым фактором, определяющим органолептические и питательные характеристики конечного продукта. Это включает направление плюрипотентных или мультипотентных клеток, преимущественно стволовых клеток, через специфические пути дифференцировки для получения необходимых специализированных типов клеток, составляющих мясо, таких как миоциты, адипоциты и фибробласты (Allan и др., 2019; Zakrzewski и др., 2019; Reiss и др., 2021). Тщательная оркестровка дифференцировки миоцитов является ключевой для формирования миофибрилл, придающих уникальную текстуру и ощущение во рту, характерные для мяса (Listrat и др., 2016; Lee и др., 2021). Параллельно с этим, направленная дифференцировка адипоцитов имеет решающее значение для отложения внутримышечного жира, который является ключевым фактором вкусового профиля и мраморности (Li и др., 2020). Кроме того, дифференцировка фибробластов и последующее образование соединительной ткани обеспечивают важную структурную целостность и влияют на нежность мяса (Purslow, 2020). Поэтому глубокое понимание и точный контроль этих процессов дифференцировки необходимы для оптимизации и масштабируемости культивируемого мяса, обеспечивая как его коммерческую жизнеспособность, так и соответствие ожиданиям потребителей (Reiss и др., 2021; Bomkamp и др., 2023).
3.2.1 Дифференциальная экспрессия генов
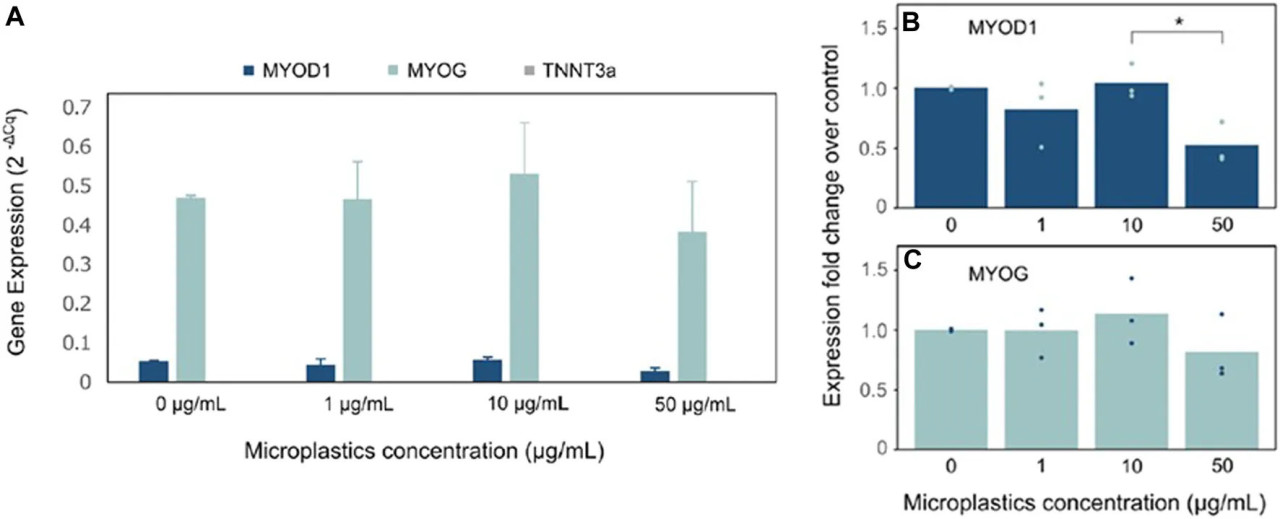
В этом исследовании мы оценили влияние микропластика на дифференцировку мышечных клеток путем измерения уровней экспрессии трех ключевых миогенных маркеров: MYOD1, MYOG и TNNT3A. MYOD1 характерен для миогенных предшественников (миобластов) на ранних фазах дифференцировки мышечных клеток, MYOG экспрессируется на стадии миоцитов, а TNNT3A действует как поздний маркер, связанный с функцией скелетных мышц. Рисунок 3A иллюстрирует абсолютные значения экспрессии генов MYOD1, MYOG и TNNT3A клеток скумбрии, культивируемых в различных концентрациях микропластика (0, 1, 10 и 50 мкг/мл). Примечательно, что наблюдалась повышенная экспрессия MYOG по сравнению с MYOD1, что означает, что клетки находились в хорошо дифференцированном состоянии миоцитов. Однако отсутствие экспрессии TNNT3A предполагает, что полного созревания до функционирующих мышечных волокон не произошло. Рисунки 3B и 3C показывают экспрессию генов MYOD1 и MYOG в виде кратности изменения (fold-change), представленной как 2^(-ΔΔCt), относительно контрольной обработки без микропластика. HPRT служил домашним геном для нормализации экспрессии. Примечательно, что общее отсутствие статистической разницы наблюдалось между обработками в экспрессии генов при различных концентрациях микропластика, согласно расчетам однофакторного дисперсионного анализа. Исключением было одно заметное различие в экспрессии MYOD1 между концентрациями 10 мкг/мл и 50 мкг/мл; однако это наблюдение было слабо подтверждено p-значением на границе 0,05, что указывает на слабую статистическую значимость.
РИСУНОК 3 Экспрессия маркеров генов мышечной дифференцировки в клетках скумбрии, растущих с МП и без МП: (A) Абсолютные значения экспрессии генов MYOD1, MYOG и TNNT3A клеток MACK. Экспрессия гена представлена как 2^(-ΔCt). (B и C) Экспрессия генов MYOD1 и MYOG в виде кратности изменения относительно контрольной обработки. Точки указывают на отдельные точки данных для каждой биологической повторности, а планки указывают на их среднее значение (n = 3 экспериментальных, n = 3 технических). HPRT использовался в качестве домашнего гена для нормализации экспрессии. Статистическая значимость, рассчитанная с помощью однофакторного дисперсионного анализа (ANOVA), обозначена звездочками, где p < 0,05 ().
Наблюдаемое увеличение экспрессии MYOG в сочетании с отсутствием экспрессии TNNT3A указывало на состояние хорошо дифференцированных клеток, которые еще не достигли поздних стадий мышечного развития. Это наблюдение может быть связано с потенциальным началом клеточного старения или снижением жизнеспособности клеток, особенно учитывая, что используемая клеточная линия скумбрии находилась на пассаже #82 — стадии, на которой клетки часто демонстрируют измененные паттерны дифференцировки из-за накопленных генетических и эпигенетических изменений (Di Micco и др., 2021). Несмотря на различия в концентрациях микропластика, общая экспрессия генов демонстрировала минимальные статистически значимые различия, что подчеркивает необходимость дальнейшего изучения взаимодействий между микропластиком и процессами дифференцировки клеток.
3.2.2 Иммуноцитохимический анализ
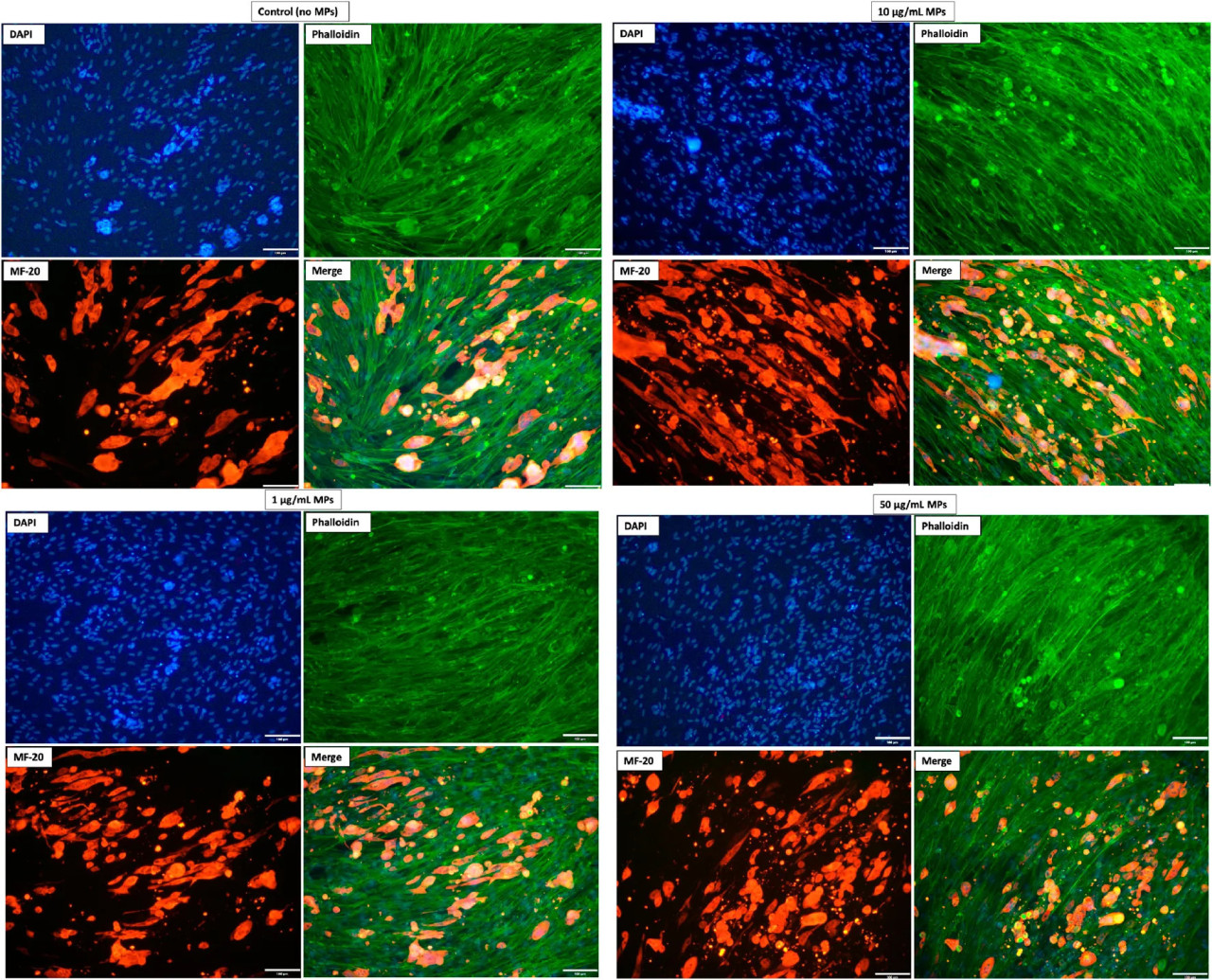
В дополнение к нашим результатам ПЦР в реальном времени, иммуноцитохимические анализы обеспечили визуальное подтверждение процессов дифференцировки клеток. Клетки, подвергнутые воздействию различных концентраций микропластика (0, 1, 10, 50 мкг/мл) в течение 14 дней, были затем исследованы с использованием MF20, DAPI и Фаллоидина, нацеленных соответственно на миозин, клеточные ядра и актиновые филаменты. Как показано на Рисунке 4, каждое экспериментальное условие демонстрировало характерные паттерны окрашивания для всех трех молекулярных маркеров. Примечательно, что удлиненные структуры, положительные по миозину, специфически окрашенные MF20, были очевидны во всех условиях. Этот согласованный паттерн окрашивания подчеркивает дифференцировку клеток скумбрии в мышечные клетки. Важно, что сходства, наблюдаемые между группами, подвергшимися воздействию МП, и контролем, позволяют предположить, что тестируемые концентрации МП оказали незначительное влияние на дифференцировку клеток скумбрии.
РИСУНОК 4 Репрезентативные изображения иммуноокрашивания клеток скумбрии с воздействием МП и без него. DAPI (синий) метит ядра, Фаллоидин (зеленый) выделяет актиновые филаменты, а MF20 (красный) детектирует дифференцировку мышечных волокон. Снято с использованием объектива 20X; масштабная линейка = 100 мкм.
Наблюдаемая минимальная вариация в экспрессии генов при разных концентрациях МП позволяет предположить, что дифференцировка мышечных клеток может обладать врожденной устойчивостью к стрессу, индуцированному микропластиком. Такая устойчивость была зафиксирована в различных клеточных системах, которые поддерживают гомеостаз и продолжают дифференцировку, несмотря на воздействия окружающей среды (Gugliuzza и Crist, 2022). Альтернативно, согласованная экспрессия генов может указывать на пороговый эффект, когда только концентрации или размеры частиц микропластика выше/ниже определенного уровня достаточно разрушительны, чтобы нарушить клеточные процессы (Campanale и др., 2020). Например, литература свидетельствует о том, что клеточные реакции на стресс могут зависеть от размера при взаимодействии с наночастицами, что будет подробно рассмотрено в следующем разделе.
3.2.3 Влияние микропластика на дифференцировку клеток
Хотя наши результаты продемонстрировали дифференцировку клеток, влияние микропластика на этот процесс оставалось неразличимым; все группы обработки и контроля давали аналогичные результаты. Напротив, более ранние исследования выявили явные последствия микропластика для дифференцировки клеток. Например, Najahi и др. (2022) изучали влияние микропластика полиэтилентерефталата (МП-ПЭТ, <1 мкм и <2,6 мкм) на мезенхимальные стромальные клетки человека, выявив 30% снижение пролиферации клеток и изменения потенциала дифференцировки адипозных клеток и клеток костного мозга. Одновременно Han и др. (2020) обнаружили, что микропластик из поливинилхлорида (ПВХ) и акрилонитрилбутадиенстирола (АБС) влиял на неадгезивные мононуклеарные клетки периферической крови (PBMC), заставляя их дифференцироваться в дендритные клетки, что предполагает, что такие воздействия пластика могут запускать иммунные реакции человека. В другом исследовании Hua и др. (2022) подчеркнули, что ПС-микропластик может нарушать дифференцировку кортикальных слоев в церебральных сфероидах, что указывает на потенциальные нейротоксические последствия. Аналогично, Im и др. (2022) сообщили, что полистирольные наночастицы, особенно с пониженной плотностью сшивки, влияли на активность активных форм кислорода и заметно способствовали адипогенной дифференцировке мезенхимальных стволовых клеток. Более того, сообщалось, что стадия дифференцировки клеток может влиять на взаимодействие клетки с микропластиком, особенно в отношении поглощения этих частиц (Peng и др., 2023). В том исследовании исследователи показали, что полистирольный (ПС) микропластик размером 2 мкм по-разному влияет на клеточные линии человека в зависимости от их состояния дифференцировки, причем недифференцированные клетки Caco-2 демонстрировали значительное поглощение ПС, в то время как дифференцированные клетки проявляли сниженную способность к интернализации ПС. В совокупности эти результаты подчеркивают многогранные воздействия микро/нанопластика на дифференцировку клеток различных типов, акцентируя необходимость всестороннего понимания и бдительного мониторинга. Кроме того, такие переменные, как конкретный тип пластика, продолжительность воздействия и концентрация пластика, остаются важнейшими факторами, которые могут дополнительно модулировать эти эффекты (Smith и др., 2018).
Чтобы распутать сложную динамику между микропластиком и дифференцировкой мышечных клеток, крайне важно, чтобы будущие исследования изучали молекулярные взаимодействия, которые поддерживают этот процесс. Исследования должны выходить за рамки традиционных миогенных маркеров, включая ряд молекулярных мишеней, на которые потенциально влияет воздействие микропластика. Комплексный подход, охватывающий изучение клеточного старения, эпигенетических модификаций и широкого спектра связанных с дифференцировкой биомаркеров, будет иметь важное значение для углубления нашего понимания последствий воздействия микропластика. Крайне необходимо, чтобы будущие исследования включали эти аспекты для выяснения клеточных и молекулярных механизмов, на которые влияет микропластик, что в конечном итоге уточнит наше понимание их воздействия на определение судьбы клеток и развитие тканей.
4 Заключение
В заключение, в этом исследовании было оценено влияние микропластика на клеточные линии скелетной мускулатуры атлантической скумбрии (S. scombrus) с использованием флуоресцентных полиэтиленовых микросфер (10–45 мкм) в качестве модельного микропластика. Основное внимание уделялось пониманию влияния воздействия микропластика на важнейшие клеточные процессы, а именно на жизнеспособность клеток на этапах прикрепления и роста, а также на дифференцировку клеток, которые имеют первостепенное значение в производстве культивируемого мяса. Используя концентрации микропластика 1 мкг/мл, 10 мкг/мл и 50 мкг/мл, наряду с контролем, не содержащим микропластика, в исследовании был принят тест с трипановым синим для оценки жизнеспособности клеток. Полученные данные показали заметную разницу в жизнеспособности клеток между обработками, подвергшимися воздействию микропластика, по сравнению с контролем. Параллельно дифференцировка клеток исследовалась с помощью ПЦР в реальном времени для анализа экспрессии генов и методологии иммуноокрашивания. Несмотря на наблюдаемую дифференцировку клеток, исследование не выявило явного влияния микропластика на дифференцировку клеток.
Результаты этого исследования выявляют взаимосвязь между микропластиком и клеточными механизмами, подчеркивая потенциальные последствия для клеточных процессов. Будучи предварительными данными, это исследование закладывает основу для последующих, более детальных исследований. Учитывая повсеместное присутствие микропластика в современной окружающей среде, необходимо изучить его более широкое воздействие на клеточные системы. Понимание этих последствий жизненно важно не только для продвижения биотехнологических приложений, но и для выявления потенциальных долгосрочных последствий в более широком контексте экологии и здоровья человека.
Ссылки
1. Abbasi S., Moore F., Keshavarzi B. (2021). PET-microplastics as a vector for polycyclic aromatic hydrocarbons in a simulated plant rhizosphere zone. Environ. Technol. Innovation 21, 101370. doi: 10.1016/j.eti.2021.101370. CrossRef Google Scholar
2. Adhikari S., Kelkar V., Kumar R., Halden R. U. (2022). Methods and challenges in the detection of microplastics and nanoplastics: a mini-review. Polym. Int. 71 (5), 543–551. doi: 10.1002/pi.6348. CrossRef Google Scholar
3. Allan S. J., De Bank P. A., Ellis M. J. (2019). Bioprocess design considerations for cultured meat production with a focus on the expansion bioreactor. Front. Sustain. Food Syst. 3. doi: 10.3389/fsufs.2019.00044. CrossRef Google Scholar
4. Alqahtani S., Alqahtani S., Saquib Q., Mohiddin F. (2023). Toxicological impact of microplastics and nanoplastics on humans: understanding the mechanistic aspect of the interaction. Front. Toxicol. 5, 1193386. doi: 10.3389/ftox.2023.1193386. CrossRef Google Scholar
5. Amelia T. S. M., Khalik W. M. A. W. M., Ong M. C., Shao Y. T., Pan H.-J., Bhubalan K. (2021). Marine microplastics as vectors of major ocean pollutants and its hazards to the marine ecosystem and humans. Prog. Earth Planet. Sci. 8 (1), 12. doi: 10.1186/s40645-020-00405-4. CrossRef Google Scholar
6. Andrady A. L. (2011). Microplastics in the marine environment. Mar. Pollut. Bull. 62 (8), 1596–1605. doi: 10.1016/j.marpolbul.2011.05.030. CrossRef Google Scholar
7. Bhagat J., Nishimura N., Shimada Y. (2021). Toxicological interactions of microplastics/nanoplastics and environmental contaminants: current knowledge and future perspectives. J. Hazard. Mater. 405, 123913. doi: 10.1016/j.jhazmat.2020.123913. CrossRef Google Scholar
8. Bhuyan M. S. (2022). Effects of microplastics on fish and in human health. Front. Environ. Sci. 10. doi: 10.3389/fenvs.2022.827289. CrossRef Google Scholar
9. Bodiou V., Moutsatsou P., Post M. J. (2020). Microcarriers for upscaling cultured meat production. Front. Nutr. 7, 10. doi: 10.3389/fnut.2020.00010. CrossRef Google Scholar
10. Bomkamp C., Musgrove L., Marques D. M. C., Fernando G. F., Ferreira F. C., Specht E. A. (2023). Differentiation and maturation of muscle and fat cells in cultivated seafood: lessons from developmental biology. Mar. Biotechnol. 25 (1), 1–29. doi: 10.1007/s10126-022-10174-4. CrossRef Google Scholar
11. Campanale C., Massarelli C., Savino I., Locaputo V., Uricchio V. F. (2020). A detailed review study on potential effects of microplastics and additives of concern on human health. Int. J. Environ. Res. Public Health 17 (4), 1212. doi: 10.3390/ijerph17041212. CrossRef Google Scholar
12. Cao J., Xu R., Wang F., Geng Y., Xu T., Zhu M., et al. (2023). Polyethylene microplastics trigger cell apoptosis and inflammation via inducing oxidative stress and activation of the NLRP3 inflammasome in carp gills. Fish Shellfish Immunol. 132, 108470. doi: 10.1016/j.fsi.2022.108470. CrossRef Google Scholar
13. Chriki S., Hocquette J. F. (2020). The myth of cultured meat: a Review. Front. Nutr. 7, 7. doi: 10.3389/fnut.2020.00007. CrossRef Google Scholar
14. Cole M., Lindeque P., Halsband C., Galloway T. S. (2011). Microplastics as contaminants in the marine environment: a review. Mar. Pollut. Bull. 62 (12), 2588–2597. doi: 10.1016/j.marpolbul.2011.09.025. CrossRef Google Scholar
15. Courtene-Jones W., Clark N. J., Fischer A. C., Smith N. S., Thompson R. C. (2022). Ingestion of microplastics by marine animals. Plastics Ocean, 349–366. doi: 10.1002/9781119768432.ch12. CrossRef Google Scholar
16. Dai S., Ye R., Huang J., Wang B., Xie Z., Ou X., et al. (2022). Distinct lipid membrane interaction and uptake of differentially charged nanoplastics in bacteria. J. Nanobiotechnology 20 (1), 191. doi: 10.1186/s12951-022-01321-z. CrossRef Google Scholar
17. Danopoulos E., Twiddy M., West R., Rotchell J. M. (2022). A rapid review and meta-regression analyses of the toxicological impacts of microplastic exposure in human cells. J. Hazard. Mater. 427, 127861. doi: 10.1016/j.jhazmat.2021.127861. CrossRef Google Scholar
18. Diamantidou D., Mastrogianni O., Tsochatzis E., Theodoridis G., Raikos N., Gika H., et al. (2022). Liquid chromatography-mass spectrometry method for the determination of polyethylene terephthalate and polybutylene terephthalate cyclic oligomers in blood samples. Anal. Bioanal. Chem. 414 (4), 1503–1512. doi: 10.1007/s00216-021-03741-6. CrossRef Google Scholar
19. Di Micco R., Krizhanovsky V., Baker D., d'Adda di Fagagna F. (2021). Cellular senescence in ageing: from mechanisms to therapeutic opportunities. Nat. Rev. Mol. Cell Biol. 22 (2), 75–95. doi: 10.1038/s41580-020-00314-w. CrossRef Google Scholar
20. Duis K., Coors A. (2016). Microplastics in the aquatic and terrestrial environment: sources (with a specific focus on personal care products), fate and effects. Environ. Sci. Eur. 28 (1), 2. doi: 10.1186/s12302-015-0069-y. CrossRef Google Scholar
21. Dupuis J. H., Cheung L. K. Y., Newman L., Dee D. R., Yada R. Y. (2023). Precision cellular agriculture: the future role of recombinantly expressed protein as food. Compr. Rev. Food Sci. Food Saf. 22 (2), 882–912. doi: 10.1111/1541-4337.13094. CrossRef Google Scholar
22. EFSA Panel on Contaminants in the Food Chain (CONTAM) (2016). Presence of microplastics and nanoplastics in food, with particular focus on seafood. EFSA J. 14 (6), e04501. doi: 10.2903/j.efsa.2016.4501. CrossRef Google Scholar
23. Eibl R., Senn Y., Gubser G., Jossen V., van den Bos C., Eibl D. (2021). Cellular agriculture: opportunities and challenges. Annu. Rev. Food Sci. Technol. 12, 51–73. doi: 10.1146/annurev-food-063020-123940. CrossRef Google Scholar
24. Elmore S. (2007). Apoptosis: a review of programmed cell death. Toxicol. Pathol. 35 (4), 495–516. doi: 10.1080/01926230701320337. CrossRef Google Scholar
25. Espinosa C., García Beltrán J. M., Esteban M. A., Cuesta A. (2018). In vitro effects of virgin microplastics on fish head-kidney leucocyte activities. Environ. Pollut. 235, 30–38. doi: 10.1016/j.envpol.2017.12.054. CrossRef Google Scholar
26. Fleury J.-B., Baulin V. A. (2021). Microplastics destabilize lipid membranes by mechanical stretching. Proc. Natl. Acad. Sci. 118 (31), e2104610118. doi: 10.1073/pnas.2104610118. CrossRef Google Scholar
27. Fournier E., Leveque M., Ruiz P., Ratel J., Durif C., Chalancon S., et al. (2023). Microplastics: what happens in the human digestive tract? First evidences in adults using in vitro gut models. J. Hazard. Mater. 442, 130010. doi: 10.1016/j.jhazmat.2022.130010. CrossRef Google Scholar
28. Galloway T. S., Cole M., Lewis C. (2017). Interactions of microplastic debris throughout the marine ecosystem. Nat. Ecol. Evol. 1 (5), 0116. doi: 10.1038/s41559-017-0116. CrossRef Google Scholar
29. Galluzzi L., Vitale I., Aaronson S. A., Abrams J. M., Adam D., Agostinis P., et al. (2018). Molecular mechanisms of cell death: recommendations of the nomenclature committee on cell death 2018. Cell Death Differ. 25 (3), 486–541. doi: 10.1038/s41418-017-0012-4. CrossRef Google Scholar
30. Goodman K. E., Hare J. T., Khamis Z. I., Hua T., Sang Q.-X. A. (2021). Exposure of human lung cells to polystyrene microplastics significantly retards cell proliferation and triggers morphological changes. Chem. Res. Toxicol. 34 (4), 1069–1081. doi: 10.1021/acs.chemrestox.0c00486. CrossRef Google Scholar
31. Gugliuzza M. V., Crist C. (2022). Muscle stem cell adaptations to cellular and environmental stress. Skelet. Muscle 12 (1), 5. doi: 10.1186/s13395-022-00289-6. CrossRef Google Scholar
32. Han S., Bang J., Choi D., Hwang J., Kim T., Oh Y., et al. (2020). Surface pattern analysis of microplastics and their impact on human-derived cells. ACS Appl. Polym. Mater. 2 (11), 4541–4550. doi: 10.1021/acsapm.0c00645. CrossRef Google Scholar
33. Herrala M., Huovinen M., Järvelä E., Hellman J., Tolonen P., Lahtela-Kakkonen M., et al. (2023). Micro-sized polyethylene particles affect cell viability and oxidative stress responses in human colorectal adenocarcinoma Caco-2 and HT-29 cells. Sci. Total Environ. 867, 161512. doi: 10.1016/j.scitotenv.2023.161512. CrossRef Google Scholar
34. Hirt N., Body-Malapel M. (2020). Immunotoxicity and intestinal effects of nano- and microplastics: a review of the literature. Part Fibre Toxicol. 17 (1), 57. doi: 10.1186/s12989-020-00387-7. CrossRef Google Scholar
35. Hua T., Kiran S., Li Y., Sang Q.-X. A. (2022). Microplastics exposure affects neural development of human pluripotent stem cell-derived cortical spheroids. J. Hazard. Mater. 435, 128884. doi: 10.1016/j.jhazmat.2022.128884. CrossRef Google Scholar
36. Huppertsberg S., Knepper T. P. (2018). Instrumental analysis of microplastics — benefits and challenges. Anal. Bioanal. Chem. 410 (25), 6343–6352. doi: 10.1007/s00216-018-1210-8. CrossRef Google Scholar
37. Hwang J., Choi D., Han S., Jung S. Y., Choi J., Hong J. (2020). Potential toxicity of polystyrene microplastic particles. Sci. Rep. 10 (1), 7391. doi: 10.1038/s41598-020-64464-9. CrossRef Google Scholar
38. Im G.-B., Kim Y. G., Jo I.-S., Yoo T. Y., Kim S.-W., Park H. S., et al. (2022). Effect of polystyrene nanoplastics and their degraded forms on stem cell fate. J. Hazard. Mater. 430, 128411. doi: 10.1016/j.jhazmat.2022.128411. CrossRef Google Scholar
39. Ivar do Sul J. A., Costa M. F. (2014). The present and future of microplastic pollution in the marine environment. Environ. Pollut. 185, 352–364. doi: 10.1016/j.envpol.2013.10.036. CrossRef Google Scholar
40. Jahir N. R., Ramakrishna S., Abdullah A. A. A., Vigneswari S. (2023). Cultured meat in cellular agriculture: advantages, applications and challenges. Food Biosci. 53, 102614. doi: 10.1016/j.fbio.2023.102614. CrossRef Google Scholar
41. Jeong C.-B., Kang H.-M., Lee M.-C., Kim D.-H., Han J., Hwang D.-S., et al. (2017). Adverse effects of microplastics and oxidative stress-induced MAPK/Nrf2 pathway-mediated defense mechanisms in the marine copepod Paracyclopina nana. Sci. Rep. 7 (1), 41323. doi: 10.1038/srep41323. CrossRef Google Scholar
42. Jeong C.-B., Won E.-J., Kang H.-M., Lee M.-C., Hwang D.-S., Hwang U.-K., et al. (2016). Microplastic size-dependent toxicity, oxidative stress induction, and p-JNK and p-p38 activation in the monogonont rotifer (brachionus koreanus). Environ. Sci. Technol. 50 (16), 8849–8857. doi: 10.1021/acs.est.6b01441. CrossRef Google Scholar
43. Jeong J., Choi J. (2019). Adverse outcome pathways potentially related to hazard identification of microplastics based on toxicity mechanisms. Chemosphere 231, 249–255. doi: 10.1016/j.chemosphere.2019.05.003. CrossRef Google Scholar
44. Jeyavani J., Sibiya A., Stalin T., Vigneshkumar G., Al-Ghanim K. A., Riaz M. N., et al. (2023). Biochemical, genotoxic and histological implications of polypropylene microplastics on freshwater fish oreochromis mossambicus: an aquatic eco-toxicological assessment. Toxics 11 (3), 282. doi: 10.3390/toxics11030282. CrossRef Google Scholar
45. Jiang B., Kauffman A. E., Li L., McFee W., Cai B., Weinstein J., et al. (2020). Health impacts of environmental contamination of micro- and nanoplastics: a review. Environ. Health Prev. Med. 25 (1), 29. doi: 10.1186/s12199-020-00870-9. CrossRef Google Scholar
46. Kannan K., Vimalkumar K. (2021). A review of human exposure to microplastics and insights into microplastics as obesogens. Front. Endocrinol. 12, 724989. doi: 10.3389/fendo.2021.724989. CrossRef Google Scholar
47. Karla Lizzeth M.-C., Leandro H.-C., Carlos M. A.-A., Luis Alberto Peralta P., Carolina P.-M. (2023). "Micro(Nano) Plastics as carriers of toxic agents and their impact on human health," in Advances and challenges in microplastics. Editor El-Sayed S. (London, UK: IntechOpen). Ch. 10. doi: 10.5772/intechopen.111889. CrossRef Google Scholar
48. Kim S., Beier A., Schreyer H. B., Bakshi B. R. (2022). Environmental life cycle assessment of a novel cultivated meat burger patty in the United States. Sustainability 14 (23), 16133. doi: 10.3390/su142316133. CrossRef Google Scholar
49. Kim Y. H., Han D. K., Park K. D., Kim S. H. (2003). Enhanced blood compatibility of polymers grafted by sulfonated PEO via a negative cilia concept. Focus Biomaterials Sci. Asia 24, 2213–2223. doi: 10.1016/S0142-9612(03)00023-1. CrossRef Google Scholar
50. Koelmans A. A., Mohamed Nor N. H., Hermsen E., Kooi M., Mintenig S. M., De France J. (2019). Microplastics in freshwaters and drinking water: critical review and assessment of data quality. Water Res. 155, 410–422. doi: 10.1016/j.watres.2019.02.054. CrossRef Google Scholar
51. Lamichhane G., Acharya A., Marahatha R., Modi B., Paudel R., Adhikari A., et al. (2023). Microplastics in environment: global concern, challenges, and controlling measures. Int. J. Environ. Sci. Technol. 20 (4), 4673–4694. doi: 10.1007/s13762-022-04261-1. CrossRef Google Scholar
52. Lee D. Y., Lee S. Y., Jung J. W., Kim J. H., Oh D. H., Kim H. W., et al. (2022). Review of technology and materials for the development of cultured meat. Crit. Rev. Food Sci. Nutr. 63, 8591–8615. doi: 10.1080/10408398.2022.2063249. CrossRef Google Scholar
53. Lee H.-S., Amarakoon D., Wei C.-i., Choi K. Y., Smolensky D., Lee S.-H. (2021). Adverse effect of polystyrene microplastics (PS-MPs) on tube formation and viability of human umbilical vein endothelial cells. Food Chem. Toxicol. 154, 112356. doi: 10.1016/j.fct.2021.112356. CrossRef Google Scholar
54. Lee K. Y., Loh H. X., Wan A. C. A. (2021). Systems for muscle cell differentiation: from bioengineering to future food. Micromachines (Basel) 13 (1), 71. doi: 10.3390/mi13010071. CrossRef Google Scholar
55. Lee Y., Cho J., Sohn J., Kim C. (2023). Health effects of microplastic exposures: current issues and perspectives in South Korea. Yonsei Med. J. 64 (5), 301–308. doi: 10.3349/ymj.2023.0048. CrossRef Google Scholar
56. Leslie H. A., Van Velzen M. J., Brandsma S. H., Vethaak A. D., Garcia-Vallejo J. J., Lamoree M. H. (2022). Discovery and quantification of plastic particle pollution in human blood. Environ. Int. 163, 107199. doi: 10.1016/j.envint.2022.107199. CrossRef Google Scholar
57. Li X., Fu X., Yang G., Du M. (2020). Review: enhancing intramuscular fat development via targeting fibro-adipogenic progenitor cells in meat animals. Animal 14 (2), 312–321. doi: 10.1017/S175173111900209X. CrossRef Google Scholar
58. Li Y., Tao L., Wang Q., Wang F., Li G., Song M. (2023). Potential health impact of microplastics: a review of environmental distribution, human exposure, and toxic effects. Environ. Health 1, 249–257. doi: 10.1021/envhealth.3c00052. CrossRef Google Scholar
59. Lim X. (2021). Microplastics are everywhere - but are they harmful? Nature 593 (7857), 22–25. doi: 10.1038/d41586-021-01143-3. CrossRef Google Scholar
60. Listrat A., Lebret B., Louveau I., Astruc T., Bonnet M., Lefaucheur L., et al. (2016). How muscle structure and composition influence meat and flesh quality. ScientificWorldJournal 2016, 3182746. doi: 10.1155/2016/3182746. CrossRef Google Scholar
61. Löder M. G. J., Imhof H. K., Ladehoff M., Löschel L. A., Lorenz C., Mintenig S., et al. (2017). Enzymatic purification of microplastics in environmental samples. Environ. Sci. Technol. 51 (24), 14283–14292. doi: 10.1021/acs.est.7b03055. CrossRef Google Scholar
62. Lv L., Yan X., Feng L., Jiang S., Lu Z., Xie H., et al. (2021). Challenge for the detection of microplastics in the environment. Water Environ. Res. 93 (1), 5–15. doi: 10.1002/wer.1281. CrossRef Google Scholar
63. Lwanga E. H., Beriot N., Corradini F., Silva V., Yang X., Baartman J., et al. (2022). Review of microplastic sources, transport pathways and correlations with other soil stressors: a journey from agricultural sites into the environment. Chem. Biol. Technol. Agric. 9 (1), 20. doi: 10.1186/s40538-021-00278-9. CrossRef Google Scholar
64. Makhdoumi P., Hossini H., Pirsaheb M. (2023). A review of microplastic pollution in commercial fish for human consumption. Rev. Environ. Health 38 (1), 97–109. doi: 10.1515/reveh-2021-0103. CrossRef Google Scholar
65. Mamun A. A., Prasetya T. A. E., Dewi I. R., Ahmad M. (2023). Microplastics in human food chains: food becoming a threat to health safety. Sci. Total Environ. 858, 159834. doi: 10.1016/j.scitotenv.2022.159834. CrossRef Google Scholar
66. Mattioda V., Benedetti V., Tessarolo C., Oberto F., Favole A., Gallo M., et al. (2023). Pro-Inflammatory and cytotoxic effects of polystyrene microplastics on human and murine intestinal cell lines. Biomolecules 13 (1), 140. doi: 10.3390/biom13010140. CrossRef Google Scholar
67. Najahi H., Alessio N., Squillaro T., Conti G. O., Ferrante M., Di Bernardo G., et al. (2022). Environmental microplastics (EMPs) exposure alter the differentiation potential of mesenchymal stromal cells. Environ. Res. 214 (4), 114088. doi: 10.1016/j.envres.2022.114088. CrossRef Google Scholar
68. Nouman M., Saunier J., Jubeli E., Yagoubi N. (2017). Additive blooming in polymer materials: consequences in the pharmaceutical and medical field. Polym. Degrad. Stab. 143, 239–252. doi: 10.1016/j.polymdegradstab.2017.07.021. CrossRef Google Scholar
69. O'Neill E. N., Cosenza Z. A., Baar K., Block D. E. (2021). Considerations for the development of cost-effective cell culture media for cultivated meat production. Compr. Rev. Food Sci. Food Saf. 20 (1), 686–709. doi: 10.1111/1541-4337.12678. CrossRef Google Scholar
70. O'Neill S. M., Lawler J. (2021). Knowledge gaps on micro and nanoplastics and human health: a critical review. Case Stud. Chem. Environ. Eng. 3, 100091. doi: 10.1016/j.cscee.2021.100091. CrossRef Google Scholar
71. Ong K. J., Johnston J., Datar I., Sewalt V., Holmes D., Shatkin J. A. (2021). Food safety considerations and research priorities for the cultured meat and seafood industry. Compr. Rev. Food Sci. Food Saf. 20 (6), 5421–5448. doi: 10.1111/1541-4337.12853. CrossRef Google Scholar
72. Osman A. I., Hosny M., Eltaweil A. S., Omar S., Elgarahy A. M., Farghali M., et al. (2023). Microplastic sources, formation, toxicity and remediation: a review. Environ. Chem. Lett. 21, 2129–2169. doi: 10.1007/s10311-023-01593-3. CrossRef Google Scholar
73. Palaniappan S., Sadacharan C. M., Rostama B. (2022). Polystyrene and polyethylene microplastics decrease cell viability and dysregulate inflammatory and oxidative stress markers of MDCK and L929 cells in vitro. Expo. Health 14 (1), 75–85. doi: 10.1007/s12403-021-00419-3. CrossRef Google Scholar
74. Paul M. B., Stock V., Cara-Carmona J., Lisicki E., Shopova S., Fessard V., et al. (2020). Micro- and nanoplastics - current state of knowledge with the focus on oral uptake and toxicity. Nanoscale Adv. 2 (10), 4350–4367. doi: 10.1039/D0NA00539H. CrossRef Google Scholar
75. Peng M., Vercauteren M., Grootaert C., Rajkovic A., Boon N., Janssen C., et al. (2023). Cellular and bioenergetic effects of polystyrene microplastic in function of cell type, differentiation status and post-exposure time. Environ. Pollut. 337, 122550. doi: 10.1016/j.envpol.2023.122550. CrossRef Google Scholar
76. Purslow P. P. (2020). The structure and role of intramuscular connective tissue in muscle function. Front. Physiology 11, 495. doi: 10.3389/fphys.2020.00495. CrossRef Google Scholar
77. Ramsperger A., Bergamaschi E., Panizzolo M., Fenoglio I., Barbero F., Peters R., et al. (2023). Nano- and microplastics: a comprehensive review on their exposure routes, translocation, and fate in humans. NanoImpact 29, 100441. doi: 10.1016/j.impact.2022.100441. CrossRef Google Scholar
78. Reiss J., Robertson S., Suzuki M. (2021). Cell sources for cultivated meat: applications and considerations throughout the production workflow. Int. J. Mol. Sci. 22 (14), 7513. doi: 10.3390/ijms22147513. CrossRef Google Scholar
79. Revel M., Châtel A., Mouneyrac C. (2018). Micro(nano)plastics: a threat to human health? Curr. Opin. Environ. Sci. Health 1, 17–23. doi: 10.1016/j.coesh.2017.10.003. CrossRef Google Scholar
80. Rischer H., Szilvay G. R., Oksman-Caldentey K.-M. (2020). Cellular agriculture — industrial biotechnology for food and materials. Curr. Opin. Biotechnol. 61, 128–134. doi: 10.1016/j.copbio.2019.12.003. CrossRef Google Scholar
81. Rubio-Armendáriz C., Alejandro-Vega S., Paz-Montelongo S., Gutiérrez-Fernández ÁJ., Carrascosa-Iruzubieta C. J., Hardisson-de la Torre A. (2022). Microplastics as emerging food contaminants: a challenge for food safety. Int. J. Environ. Res. Public Health 19 (3), 1174. doi: 10.3390/ijerph19031174. CrossRef Google Scholar
82. Saad M. K., Yuen J. S. K., Joyce C. M., Li X., Lim T., Wolfson T. L., et al. (2023). Continuous fish muscle cell line with capacity for myogenic and adipogenic-like phenotypes. Sci. Rep. 13 (1), 5098. doi: 10.1038/s41598-023-31822-2. CrossRef Google Scholar
83. Schirinzi G. F., Pérez-Pomeda I., Sanchís J., Rossini C., Farré M., Barceló D. (2017). Cytotoxic effects of commonly used nanomaterials and microplastics on cerebral and epithelial human cells. Environ. Res. 159, 579–587. doi: 10.1016/j.envres.2017.08.043. CrossRef Google Scholar
84. Schymanski D., Goldbeck C., Humpf H.-U., Fürst P. (2018). Analysis of microplastics in water by micro-Raman spectroscopy: release of plastic particles from different packaging into mineral water. Water Res. 129, 154–162. doi: 10.1016/j.watres.2017.11.011. CrossRef Google Scholar
85. Scopetani C., Esterhuizen M., Cincinelli A., Pflugmacher S. (2020). Microplastics exposure causes negligible effects on the oxidative response enzymes glutathione reductase and peroxidase in the oligochaete Tubifex tubifex. Toxics 8 (1), 14. doi: 10.3390/toxics8010014. CrossRef Google Scholar
86. Sharma S., Chatterjee S. (2017). Microplastic pollution, a threat to marine ecosystem and human health: a short review. Environ. Sci. Pollut. Res. 24 (27), 21530–21547. doi: 10.1007/s11356-017-9910-8. CrossRef Google Scholar
87. Sinke P., Swartz E., Sanctorum H., van der Giesen C., Odegard I. (2023). Ex-ante life cycle assessment of commercial-scale cultivated meat production in 2030 (vol 28, pg 234, 2023). Int. J. Life Cycle Assess. 28 (9), 1225–1228. doi: 10.1007/s11367-023-02183-9. CrossRef Google Scholar
88. Smith M., Love D. C., Rochman C. M., Neff R. A. (2018). Microplastics in seafood and the implications for human health. Curr. Environ. Health Rep. 5 (3), 375–386. doi: 10.1007/s40572-018-0206-z. CrossRef Google Scholar
89. Stephens N., Di Silvio L., Dunsford I., Ellis M., Glencross A., Sexton A. (2018). Bringing cultured meat to market: technical, socio-political, and regulatory challenges in cellular agriculture. Trends Food Sci. Technol. 78, 155–166. doi: 10.1016/j.tifs.2018.04.010. CrossRef Google Scholar
90. Thiele C. J., Hudson M. D., Russell A. E., Saluveer M., Sidaoui-Haddad G. (2021). Microplastics in fish and fishmeal: an emerging environmental challenge? Sci. Rep. 11 (1), 2045. doi: 10.1038/s41598-021-81499-8. CrossRef Google Scholar
91. Thornton Hampton L. M., Bouwmeester H., Brander S. M., Coffin S., Cole M., Hermabessiere L., et al. (2022). Research recommendations to better understand the potential health impacts of microplastics to humans and aquatic ecosystems. Microplastics Nanoplastics 2 (1), 18. doi: 10.1186/s43591-022-00038-y. CrossRef Google Scholar
92. Tsochatzis E. D., Theodoridis G., Corredig M. (2023). Analysis of oligomers to assess exposure to microplastics from foods. A perspective. Front. Nutr. 10, 1186951. doi: 10.3389/fnut.2023.1186951. CrossRef Google Scholar
93. Vergeer R., Sinke P., Odegard I. (2021). TEA of cultivated meat, Future projections of different scenarios - corrigendum. C. Delft. 21. Google Scholar
94. Vivekanand A. C., Mohapatra S., Tyagi V. K. (2021). Microplastics in aquatic environment: challenges and perspectives. Chemosphere 282, 131151. doi: 10.1016/j.chemosphere.2021.131151. CrossRef Google Scholar
95. Wang W., Zhang J., Qiu Z., Cui Z., Li N., Li X., et al. (2022). Effects of polyethylene microplastics on cell membranes: a combined study of experiments and molecular dynamics simulations. J. Hazard. Mater. 429, 128323. doi: 10.1016/j.jhazmat.2022.128323. CrossRef Google Scholar
96. Watts A. J. R., Urbina M. A., Corr S., Lewis C., Galloway T. S. (2015). Ingestion of plastic microfibers by the crab carcinus maenas and its effect on food consumption and energy balance. Environ. Sci. Technol. 49 (24), 14597–14604. doi: 10.1021/acs.est.5b04026. CrossRef Google Scholar
97. Wright S. L., Kelly F. J. (2017). Plastic and human health: a micro issue? Environ. Sci. Technol. 51 (12), 6634–6647. doi: 10.1021/acs.est.7b00423. CrossRef Google Scholar
98. Wright S. L., Rowe D., Thompson R. C., Galloway T. S. (2013). Microplastic ingestion decreases energy reserves in marine worms. Curr. Biol. 23 (23), R1031–R1033. doi: 10.1016/j.cub.2013.10.068. CrossRef [Google Scholar](http://scholar.google.com/scholar_lookup?author=S.%2BL..%2BWright&author=D..%2BRowe&author=R.%2BC..%2BThompson&author=T.%2BS..%2BGalloway&publication_year=2013&title=Microplastic%2 Bingestion%2Bdecreases%2Benergy%2Breserves%2Bin%2Bmarine%2Bworms&journal=Curr.+Biol.&volume=23&pages=R1031-R1033)
99. Wu D., Feng Y., Wang R., Jiang J., Guan Q., Yang X., et al. (2023). Pigment microparticles and microplastics found in human thrombi based on Raman spectral evidence. J. Adv. Res. 49, 141–150. doi: 10.1016/j.jare.2022.09.004. CrossRef Google Scholar
100. Yee M. S., Hii L. W., Looi C. K., Lim W. M., Wong S. F., Kok Y. Y., et al. (2021). Impact of microplastics and nanoplastics on human health. Nanomater. (Basel) 11 (2), 496. doi: 10.3390/nano11020496. CrossRef Google Scholar
101. Yong C. Q. Y., Valiyaveettil S., Tang B. L. (2020). Toxicity of microplastics and nanoplastics in mammalian systems. Int. J. Environ. Res. Public Health 17 (5), 1509. doi: 10.3390/ijerph17051509. CrossRef Google Scholar
102. Zakrzewski W., Dobrzyński M., Szymonowicz M., Rybak Z. (2019). Stem cells: past, present, and future. Stem Cell Res. Ther. 10 (1), 68. doi: 10.1186/s13287-019-1165-5. CrossRef Google Scholar
103. Zhang Y., Wang S., Olga V., Xue Y., Lv S., Diao X., et al. (2022). The potential effects of microplastic pollution on human digestive tract cells. Chemosphere 291, 132714. doi: 10.1016/j.chemosphere.2021.132714. CrossRef Google Scholar
104. Ziani K., Ioniță-Mîndrican C.-B., Mititelu M., Neacșu S. M., Negrei C., Moroșan E., et al. (2023). Microplastics: a real global threat for environment and food safety: a state of the art review. Nutrients 15 (3), 617. doi: 10.3390/nu15030617. CrossRef Google Scholar
Sun T, Timoneda A, Banavar A and Ovissipour R (2024) Enhancing food safety and cultivated meat production: exploring the impact of microplastics on fish muscle cell proliferation and differentiation. Front. Food. Sci. Technol. 4:1309884. doi: 10.3389/frfst.2024.1309884
Перевод статьи «Enhancing food safety and cultivated meat production: exploring the impact of microplastics on fish muscle cell proliferation and differentiation» авторов Sun T, Timoneda A, Banavar A and Ovissipour R., оригинал доступен по ссылке. Лицензия: CC BY. Изменения: переведено на русский язык
Фото: magnific.com












































































































Комментарии (0)