Уксусные бактерии против гниения: новый метод силосования сорго
Целью данного исследования было выделение, характеристика и идентификация молочнокислых бактерий, продуцирующих уксусную кислоту, из свежих растений сорго и силоса, а также оценка влияния выделенных изолятов, используемых в качестве микробных инокулянтов, на таксономическое разнообразие и качество ферментации силоса.
Аннотация
На первом этапе эксперимента было подготовлено восемь опытных силосных хранилищ, а также был отобран образец свежего растения сорго сорта BRS Ponta Negra (Sorghum bicolor (L.) Moench.) для характеристики и идентификации бактерий. Для второго этапа эксперимента было отобрано пять штаммов, которые были внесены в силос по схеме 7 × 2 (факторный дизайн): семь вариантов обработки и два срока вскрытия, в четырех повторностях. Было идентифицировано четыре типа видов, при этом преобладал Lactiplantibacillus plantarum (72,73%). Было выявлено влияние взаимодействия между вариантами обработки и сроками вскрытия на потери от выделения жидкости, газообразные потери, популяцию молочнокислых бактерий, дрожжей и содержание молочной кислоты. По аэробной стабильности выделились варианты с Lactiplantibacillus plantarum (GML 66) и Weissella cibaria, которые показали стабильность в течение 71,75 и 68,87 часа соответственно. Использование Lactiplantibacillus plantarum (GML 66) в качестве микробного инокулянта в силосе из сорго увеличило содержание сухого вещества, снизило потери от выделения жидкости и повысило выход сухого вещества. Это также привело к снижению популяции дрожжей в силосе, что способствовало большей аэробной стабильности силоса.
1. Введение
Кормовое сорго имеет профиль ферментации, считающийся подходящим для процесса силосования, при котором оно подвергается молочнокислому брожению. Однако основная проблема в исследованиях, связанных с силосом из этих кормовых растений, возникает после вскрытия хранилища из-за его низкой аэробной стабильности, связанной с высоким содержанием молочной кислоты и остаточных растворимых углеводов и низкой концентрацией конечных продуктов брожения с противогрибковой активностью [1].
Таким образом, несмотря на быстрое подкисление среды и большую выработку молочной кислоты в период ферментации, одна молочная кислота не может ингибировать рост плесени и дрожжей после вскрытия силоса. Плесень и дрожжи потребляют молочную кислоту и остаточные растворимые углеводы, вызывая порчу силосной массы. Одновременно происходит повышение температуры, pH, продукции CO2, воды и тепла [2]. В результате, из-за повышения pH, действие других нежелательных микроорганизмов, таких как энтеробактерии, приводит к аэробной порче силоса.
Поэтому очень трудно контролировать эпифитную популяцию микроорганизмов, присутствующих на кормовом растении в момент силосования. Следовательно, штаммы гетероферментативных молочнокислых бактерий используются в качестве микробных инокулянтов для повышения аэробной стабильности силоса за счет выработки органических кислот с высокой противогрибковой активностью, таких как уксусная и пропионовая кислота.
Некоторые штаммы гетероферментативных молочнокислых бактерий, такие как Lentilactobacillus buchneri, могут преобразовывать молочную кислоту в уксусную кислоту и 1,2-пропандиол в фазе ферментации процесса силосования [3]. Однако исследования, проведенные с использованием облигатных и факультативных гетероферментативных штаммов Lentilactobacillus в качестве микробной добавки в силосе из кормового сорго в тропических и полузасушливых условиях, остаются неубедительными [4,5,6,7,8,9,10,11,12]. Эти результаты могут быть связаны с эпифитными популяциями микроорганизмов, обнаруживаемыми на растениях, выращиваемых в тропическом и полузасушливом климате.
Колонизация поверхностей растений эпифитными бактериями зависит от многих факторов, включая вид растения в регионе, климат, почву, вегетативную стадию растения, географическое положение, интенсивность солнечной радиации и тип используемого удобрения [13,14]. Ding и др. [15] оценили эпифитное бактериальное сообщество растения in natura и динамику бактериального сообщества в процессе ферментации силоса Elymus nutans, выращенного в четырех различных регионах Цинхай-Тибетского плато. Авторы наблюдали, что качество ферментации силоса варьировалось в зависимости от районов выращивания Elymus nutans, а изменения бактериального разнообразия в процессе ферментации были обусловлены эпифитными бактериями Elymus nutans.
Следовательно, селективное культивирование и поиск молочнокислых бактерий позволяют понять динамику доминирующих видов в растении и на каждом этапе процесса силосования, что позволяет отобрать наиболее хорошо адаптированные для использования в качестве микробных инокулянтов. Исследования такого характера являются начальными для некоторых кормовых растений, а в полузасушливых регионах нет записей в литературе об исследованиях такого рода.
Таким образом, молочнокислые бактерии, способные преобразовывать молочную кислоту в уксусную кислоту и 1,2-пропандиол, выделенные из кормового сорго, выращенного в полузасушливом климате, могут использоваться в качестве более конкурентных инокулянтов, чем коммерческие штаммы, представленные на рынке. Следовательно, данное исследование было направлено на выделение, характеристику и идентификацию молочнокислых бактерий, продуцирующих уксусную кислоту, из свежего и силосованного кормового сорго, выращенного в полузасушливом регионе, а также на оценку эффектов применения выделенных изолятов в качестве микробных инокулянтов на таксономическое разнообразие, качество ферментации, потери в процессе силосования, химический состав и аэробную стабильность силосов из кормового сорго.
2. Материалы и методы
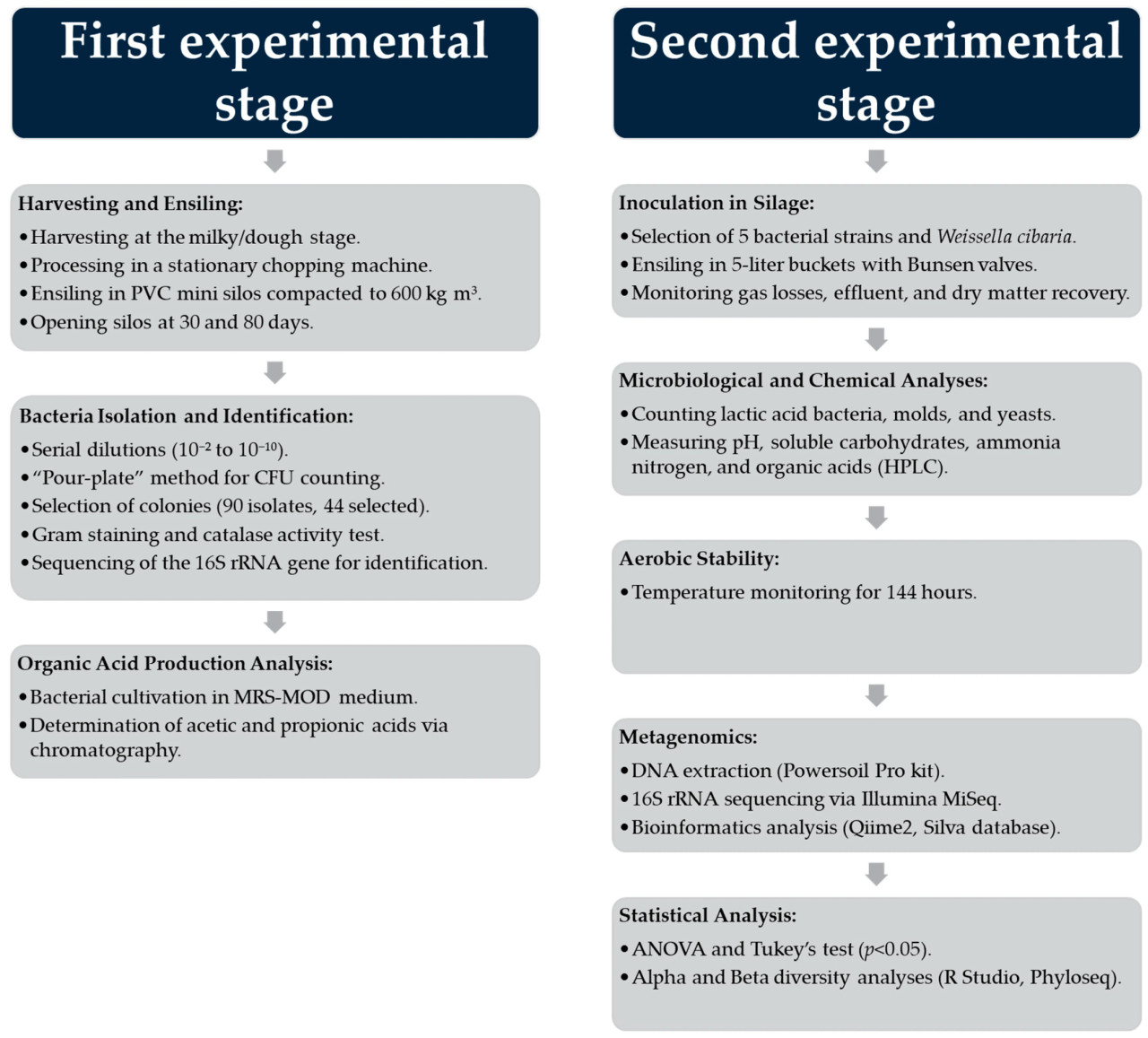
Блок-схема деятельности, проведенной в ходе исследования, показывает Рисунок 1.
Рисунок 1. Блок-схема экспериментальных этапов.
2.1. Место проведения и варианты обработки
Первое испытание было проведено в период с сентября по декабрь 2021 года в Лаборатории кормовых культур, принадлежащей Центру сельскохозяйственных наук Федерального университета Параибы, Арея, PB, который расположен в микрорегионе Брежу-Параибано, по географическим координатам 6°58′12″ южной широты, 35°42′15″ западной долготы (Гринвич), на высоте 619 м над уровнем моря.
Сорго было посажено на частной территории, расположенной по координатам 7°23′26″ южной широты, 36°48′30″ западной долготы и 529 м над уровнем моря, в городе Сан-Жозе-дус-Кордейрус, мезорегион Борборема и микрорегион Западный Карири, известный как Карири-Параибано. Он представляет климат Bsh (жаркий полузасушливый), согласно классификации Кёппена, с осадками с февраля по июнь, годовым количеством осадков и средней температурой около 551,7 мм и 23 °C соответственно. После анализа почва была подвергнута корректировке для удовлетворения потребностей культуры и засеяна вручную, с использованием семян сорго cv. BRS Ponta Negra (Sorghum bicolor (L.) Moench.) в сахарозе на глубину приблизительно 1,0 см на площади около 0,5 га, с расстоянием между растениями 0,7 м между рядами, всего 10 растений на погонный метр, и убрано, когда зерна достигли молочно-восковой спелости.
После уборки сорго было переработано в стационарной измельчающей машине, а затем засилосовано в экспериментальные мини-силосы из поливинилхлорида (ПВХ) диаметром 15 см × высотой 30 см. Материал уплотняли с помощью деревянных палок до достижения плотности 600 кг/м³ по сырой массе (СМ) в каждом мини-силосе. В процессе были собраны репрезентативные образцы растения in natura, затем было построено 8 экспериментальных силосов, которые были вскрыты через 30 и 80 дней после силосования.
2.2. Культивирование, выделение, характеристика и идентификация бактерий
Штаммы молочнокислых бактерий, сбраживающих молочную кислоту, были выделены из образцов растения сорго, выращенного в полузасушливом регионе, и в оба срока вскрытия. Образец материала был использован для последующих разведений (10⁻²–10⁻¹⁰), которые были использованы для посева методом «глубинного агара», и чашки со значениями от 30 до 300 колониеобразующих единиц (КОЕ) считались поддающимися подсчету и выделению [16].
Для проверки использования анаэробной молочной кислоты бактерии выращивали в соответствии с методологией, описанной Oude Elferink и др. [17], с использованием модифицированной среды MRS-бульон (среда MRS-MOD) следующего состава (на литр дистиллированной воды): пептон (5,0 г), дрожжевой экстракт (2,0 г), Tween 80 (0,5 мл), фосфат калия — K₂HPO₄ (1,0 г), фосфат мононатрия — NaH₂PO₄·H₂O (3,0 г), ацетат натрия (0,6 г), сульфат магния — MgSO₄·7H₂O (0,2 г), сульфат марганца — MnSO₄·H₂O (0,04 г), агар (15 г), молочная кислота (4,8 мл), глюкоза (1 г) и уксусная кислота (1,5 мл).
Изоляты были собраны с растений перед силосованием и в каждый срок вскрытия силоса (30 и 80 дней). Колонии отбирали из чашек с наибольшими разведениями, применяя критерий отбора квадратного корня из общего количества колоний на каждой отобранной чашке. Было отобрано девяносто колоний из различных чашек и в разные сроки вскрытия.
После отбора колоний 44 были выбраны и подвергнуты окраске по Граму и процедуре определения каталазной активности, идентифицированы в соответствии с их происхождением. После этого грамположительные и каталазоотрицательные бактерии были культивированы в пробирках, содержащих стерильную среду AGAR MRS, и отправлены в GoGenetic — Куритиба/PR, компанию, ответственную за экстракцию ДНК из изолятов, которые были оценены с помощью секвенирования по Сэнгеру кодирующей области 16S рРНК, путем сравнения полученных последовательностей каждого изолята с последовательностями, доступными в базе данных GenBank. Последовательности гена 16S рРНК, показавшие сходство, равное или превышающее 97%, рассматривались как принадлежащие к одной операционной таксономической единице (OTU) [18].
Аликвота (2 мл) бульонной культуры выделенных бактерий была подкислена 0,15 мл 50% раствора серной кислоты через три дня после роста в бульоне и отправлена в Лабораторию инструментальной хроматографии Химического департамента Федерального университета Пернамбуку – Ресифи, Пернамбуку, для определения содержания органических кислот (уксусной и пропионовой кислот) [19].
2.3. Использование бактерий, продуцирующих уксусную кислоту, в качестве инокулянтов в силосе из сорго
После селективного культивирования, идентификации и оценки продукции органических кислот было выбрано пять бактериальных штаммов на основе продукции уксусной кислоты для использования в качестве микробных инокулянтов на втором экспериментальном этапе, который проводился с февраля по май 2022 года в Лаборатории кормовых культур, принадлежащей Центру сельскохозяйственных наук Федерального университета Параибы, Арея, PB, расположенном в микрорегионе Брежу-Параибано, по географическим координатам 6°58′12″ южной широты, 35°42′15″ западной долготы (Гринвич) и 619 м над уровнем моря. Посев был выполнен на том же участке, с соблюдением тех же процедур, что и при выполнении первого экспериментального этапа, что обеспечило использование сорго с теми же исходными условиями окружающей среды.
Экспериментальный дизайн был полностью рандомизированным, расположенным по факторной схеме 7 × 2, с 7 вариантами обработки и 2 сроками вскрытия (30 и 80 дней), в 4 повторностях, всего 56 экспериментальных силосов. Из семи вариантов обработки пять представляли собой штаммы молочнокислых бактерий, выделенные из растения сорго in natura и силоса с первого экспериментального этапа, на основе продукции уксусной кислоты, дополнительно к контрольному варианту (без инокулянта) и варианту с Weissella cibaria.
Weissella cibaria была выделена из кактуса груши (опунции) Pereira и др. [20], и, как сообщается, оказала положительное влияние на аэробную стабильность силосов из кактуса груши и проса [21]. Таким образом, она была использована в качестве положительного контроля.
Следовательно, варианты обработки представляли собой:
1. Контроль — без инокулянта.
2. GML 09 — Lactiplantibacillus plantarum.
3. GML 11 — Pediococcus pentosaceus.
4. GML 51 — Lactiplantibacillus plantarum.
5. GML 66 — Lactiplantibacillus plantarum.
6. GML 68 — Lactiplantibacillus plantarum.
7. Weissella cibaria.
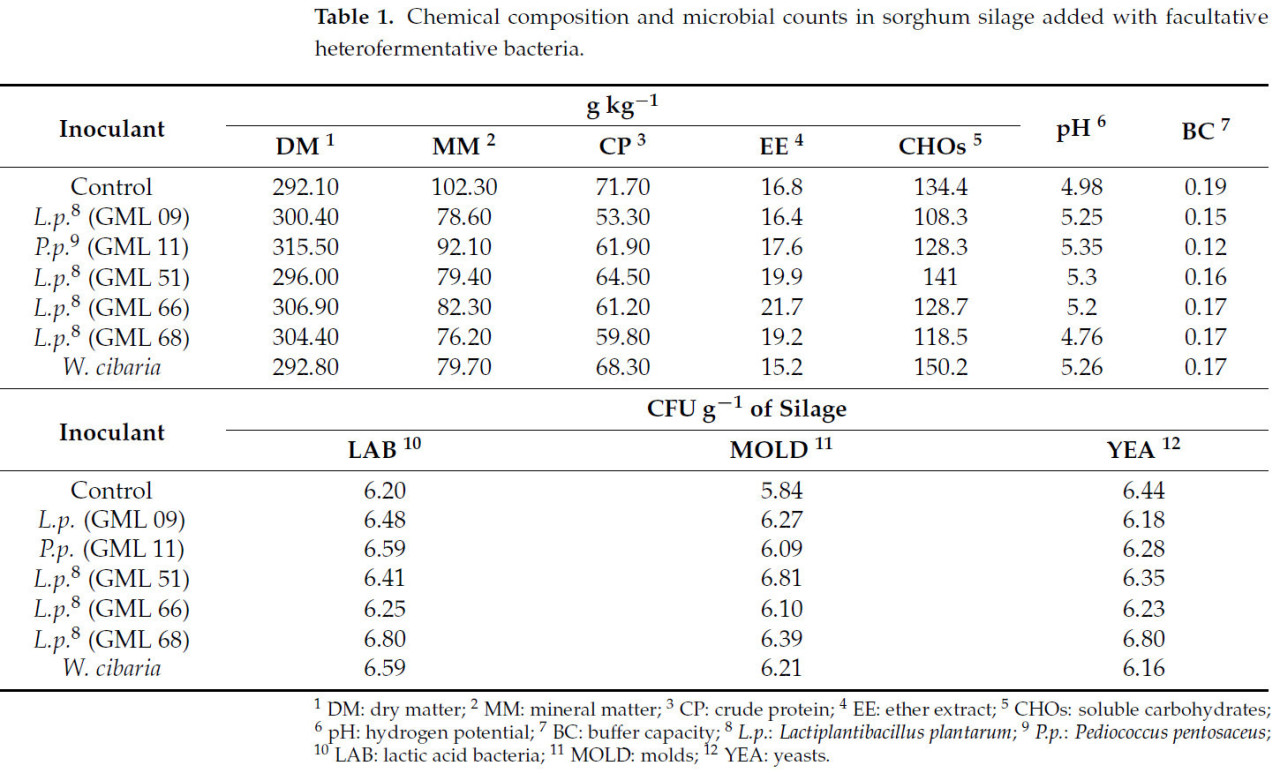
Перед силосованием пять выделенных штаммов, а также Weissella cibaria, инкубировали в MRS-бульоне при 37 °C в трех последовательных активациях каждые 24 ч. Разведения были скорректированы с целью внесения 10⁶ колониеобразующих единиц на грамм силосуемого корма. В контрольном варианте (без инокуляции) добавляли такое же количество дистиллированной воды, как и в смесь инокулянта, чтобы исключить эффект добавления раствора инокулянта. Химический и микробиологический состав вариантов обработки в день силосования можно увидеть в Таблице 1.
Таблица 1. Химический состав и микробные показатели в силосе из сорго с добавлением факультативных гетероферментативных бактерий.
Силосование проводили в ведрах емкостью 5 л, уплотняя до плотности 600 кг/м³, оснащенных клапаном Бунзена для выхода газа, добавляя на дно силосов один килограмм мелкого сухого песка, отделенного от силосуемого материала нетканым полотном, что позволяло улавливать и количественно определять выделившуюся жидкость, произведенную силосом.
Для количественной оценки микробных популяций использовали селективные питательные среды для каждой микробной группы. Десять граммов свежего силоса взвешивали и добавляли к 90 мл дистиллированной воды с ручным встряхиванием с последующими серийными разведениями в диапазоне от 10⁻² до 10⁻⁷. После этого проводили посев каждой экспериментальной повторности в двух экземплярах для каждой питательной среды. Для культивирования молочнокислых бактерий (МКБ) использовали среду Man, Rogosa и Sharpe (MRS Agar) и инкубировали в течение 48 ч в термостате с биохимическим потреблением кислорода (БПК) при 35 °C; для популяций плесени и дрожжей (YEA) использовали картофельно-декстрозный агар (PDA), подкисленный 1% винной кислотой (10%), после 72 ч, оба инкубировали в БПК при 30 °C. После периода инкубации для каждой микробной популяции подсчитывали чашки с КОЕ в диапазоне от 30 до 300, согласно Kung Jr. [16], дифференцируя колонии плесени и дрожжей по морфологическим характеристикам.
Значения pH, буферную емкость и растворимые углеводы измеряли в образцах вариантов обработки перед силосованием, в то время как для образцов в сроки вскрытия выполняли другие анализы, описанные далее. Значения pH измеряли с помощью pH-метра в соответствии с методологией, описанной Bolsen и др. [22]. Уровни аммиачного азота (NH₃-N) в силосах определяли в соответствии с методологией, описанной Chaney и др. [23]. Буферную емкость (БЕ) определяли в соответствии с методологией, предложенной Playne и McDonald [24], в адаптации Mizubuti и др. [25]. Содержание растворимых углеводов определяли в соответствии с методологией DuBois и др. [26]. Для количественного определения уровней молочной кислоты (МК), уксусной кислоты (УК) и пропионовой кислоты (ПК) в силосе использовали высокоэффективную жидкостную хроматографию (ВЭЖХ), модель SPD-10A VP, сопряженную с ультрафиолетовым (УФ) детектором. Анализ выполняли при длине волны 210 нм, скорости потока в колонке 0,6 мл/мин, давлении в колонке 87 кгс и объеме инъекции 10 мкл. Образцы готовили с использованием 10 г материала, разведенного в 90 мл дистиллированной воды, и впоследствии фильтровали через фильтровальную бумагу Whatman перед анализом [19].
Для определения газообразных потерь, потерь с выделившейся жидкостью и выхода сухого вещества экспериментальные силосы взвешивали, учитывая их вес, согласно Jobim и др. [27], используя следующие уравнения:
где GL = газообразные потери (%СВ); SWc = вес силоса при силосовании (закрытый) (кг); SWo = вес силоса при вскрытии (закрытый) (кг); FMc = масса корма при силосовании (кг); DMc = сухое вещество корма при силосовании (%).
где EL = потери с выделившейся жидкостью; SEWo = вес пустого силоса + песок при вскрытии (кг); SEWc = вес пустого силоса + песок при силосовании (кг); S = вес силоса (кг); FMc = масса корма при силосовании (кг).
где DMR = выход сухого вещества (%); FMo = масса корма при вскрытии (кг); DMo = содержание СВ при вскрытии (%); FMc = масса корма при силосовании (кг); DMc = содержание СВ при силосовании (%).
Анализы химического состава выполняли в соответствии с методологиями, описанными AOAC [28], для содержания сухого вещества (СВ) (метод 934.01), минеральных веществ (МВ) (метод 930.05), сырого протеина (СП) (метод 920.87) и сырого жира (СЖ) (метод 920.39).
Оценку аэробной стабильности проводили из 2 кг репрезентативных образцов силосов, которые были повторно упакованы в те же экспериментальные силосы без уплотнения, на 144 часа. Термометр вставляли в геометрический центр каждого экспериментального силоса для мониторинга температуры каждые тридцать минут, контролируя температуру в помещении на уровне 25 °C, и определяли момент нарушения аэробной стабильности, согласно Kung Jr. и Ranjit [19], когда температура силоса превышала температуру окружающей среды более чем на 2 °C.
Оценку метагеномного разнообразия проводили в Лаборатории продуктов животного происхождения, принадлежащей Центру сельскохозяйственных наук Федерального университета Параибы. Три повторности каждого варианта обработки были отобраны во время силосования и в срок вскрытия 80 дней, а затем немедленно заморожены при −80 °C для секвенирования ДНК гена 16S рРНК. Для экстракции геномной ДНК 25 г каждого образца разводили в 225 мл стерильного 0,85% раствора хлорида натрия (100 мл дистиллированной воды на 0,85 г растворенного вещества NaCl), помещали в автоматический гомогенизатор на 3 минуты, и весь раствор фильтровали. Весь профильтрованный раствор центрифугировали (6000 об/мин в течение 10 мин при 4 °C) в пробирке Falcon, сохраняя осадок и отбрасывая весь супернатант. Геномную ДНК экстрагировали с использованием коммерческого набора (Powersoil Pro DNA, Qiagen, Хильден, Германия). Целостность ДНК оценивали с помощью электрофореза в 1% агарозном геле и количественно определяли с помощью флуорометрии (Qubit, Thermo Fisher, Уолтем, MA, USA). Области V3–V4 микробного гена 16S рРНК амплифицировали с помощью ПЦР (95 °C в течение 3 мин, затем 25 циклов при 95 °C в течение 30 с, 55 °C в течение 30 с, 72 °C в течение 30 с и финальная элонгация при 72 °C в течение 5 мин) с использованием праймеров: 5′-TCG TCG GCA GCG TCA GAT GTG TAT AAG AGA CAG CCT ACG GGN GGC WGCAG-3′ и R: 5′-GTC TCG TGG GCT CGG AGA TGT GTA TAA GAG ACA GGA CTA CHV GGG TAT CTA ATCC-3′. Библиотеку ампликонов готовили с использованием набора Nextera XT Index Kit Set A (Illumina Inc., Сан-Диего, CA, USA), и для очистки и промывки использовали магнитные шарики (Agencourt AMPureXP, Beckman Coulter, Индианаполис, IN, USA). Секвенирование парных концов проводили на платформе Illumina MiSeq с использованием набора для 500 циклов V2 (Illumina Inc., Сан-Диего, CA, USA).
Прочтения были обработаны с использованием платформы Qiime2. Прямые и обратные последовательности были импортированы объединенными, и прочтения с низким качеством были удалены, применяя показатель качества Q > 20 в качестве контроля качества с помощью программы Dada2. Химерные и неклассифицированные последовательности были удалены из анализов. Таксономическая идентификация была выполнена с использованием баз данных Silva (https://www.arb-silva.de/ , доступ 19 марта 2023 г.).
2.4. Статистический анализ
Полученные результаты были оценены с помощью дисперсионного анализа для проверки значимости эффектов инокулянта и срока вскрытия, а также взаимодействия между факторами, и средние значения были сравнены с помощью критерия Тьюки, принимая 0,05 в качестве критического уровня вероятности. Процедуры выполнялись с использованием программного обеспечения SAS 9.4 (SAS Institute, 2015, Кари, CN, USA). Данные были проанализированы с использованием следующей модели:
где Yijk — наблюдение, касающееся комбинации выделенных штаммов молочнокислых бактерий и срока вскрытия, μ — общее среднее, Ti — изолированный эффект выделенных штаммов молочнокислых бактерий, Aj — изолированный эффект срока вскрытия, (T × A)ij — эффект взаимодействия между штаммами выделенных молочнокислых бактерий и сроком вскрытия, а εijk — случайная ошибка, связанная с наблюдением.
Анализы альфа- и бета-разнообразия выполнялись с использованием программного обеспечения R Studio версии 4.2.2 (Posit PBC, Бостон, MA, USA), с пакетом анализа Phyloseq (https://joey711.github.io/phyloseq/ , доступ 19 марта 2023 г.). Статистические критерии Тьюки были применены для индексов разнообразия, считая p-значение < 0,05 статистическим различием. Три образца на вариант обработки были стандартизированы на основе анализа кривых разрежения и глубины секвенирования.
3. Результаты
3.1. Идентификация и характеристика бактерий
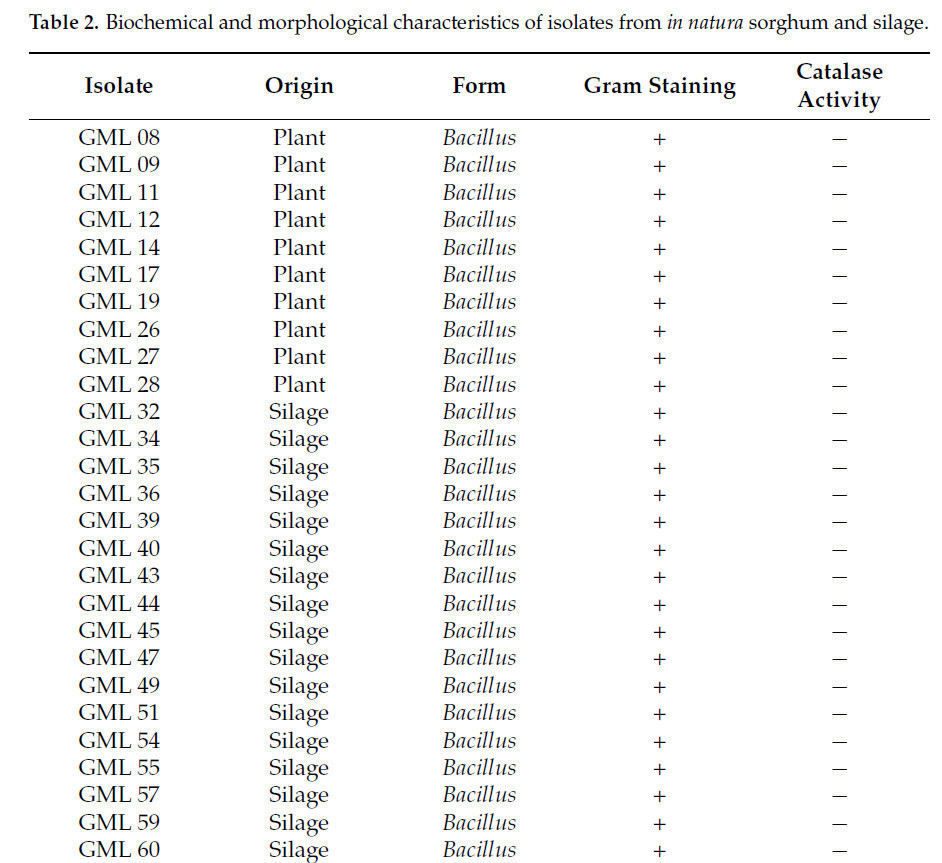
Все выделенные бактерии, независимо от того, происходили ли они из растения сорго in natura или из силоса, были классифицированы как грамположительные и каталазоотрицательные (Таблица 2).
Таблица 2. Биохимические и морфологические характеристики изолятов из сорго in natura и силоса.
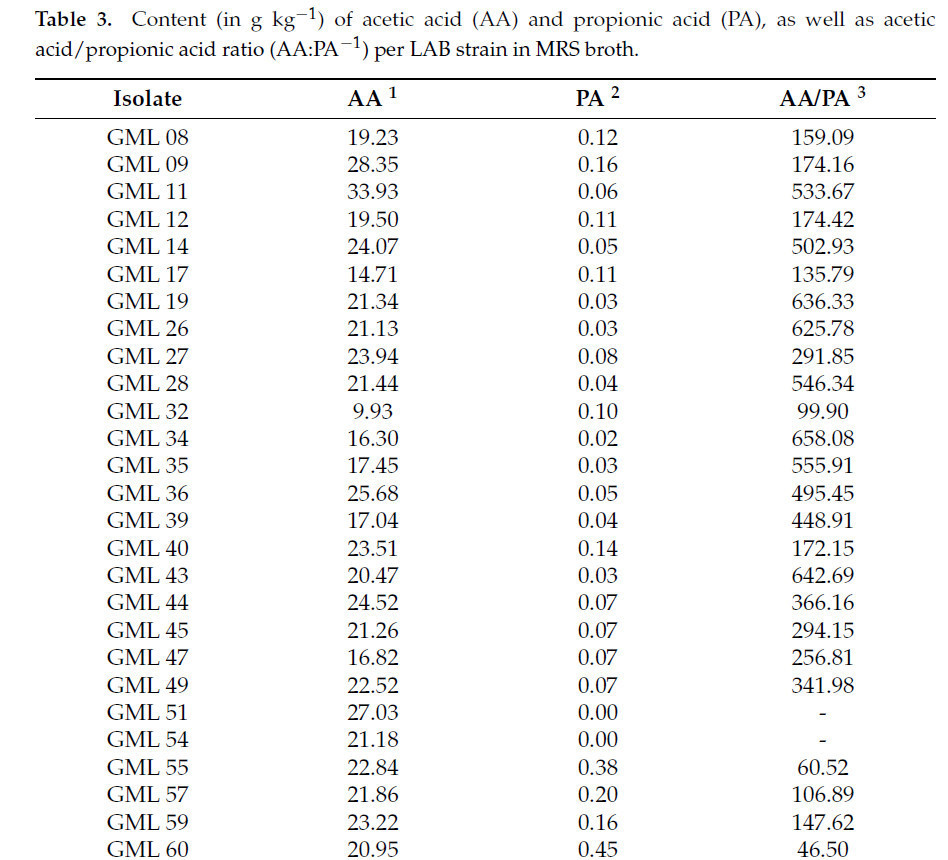
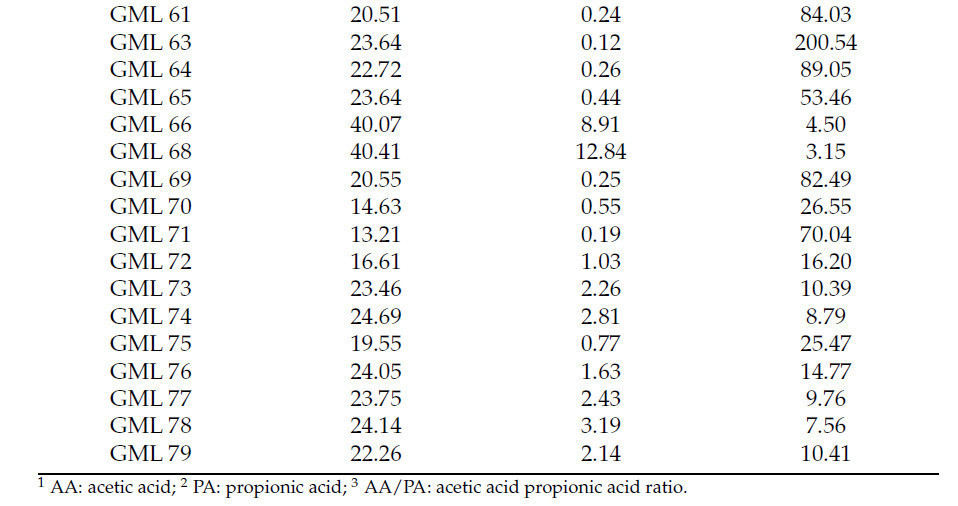
Концентрации органических кислот варьировались в зависимости от каждого штамма, в диапазоне от 9,93 до 40,41 г кг⁻¹ уксусной кислоты и от 0 до 12,84 г кг⁻¹ пропионовой кислоты (Таблица 3).
Таблица 3. Содержание (в г кг⁻¹) уксусной кислоты (УК) и пропионовой кислоты (ПК), а также соотношение уксусная кислота/пропионовая кислота (УК:ПК⁻¹) на штамм МКБ в MRS-бульоне.
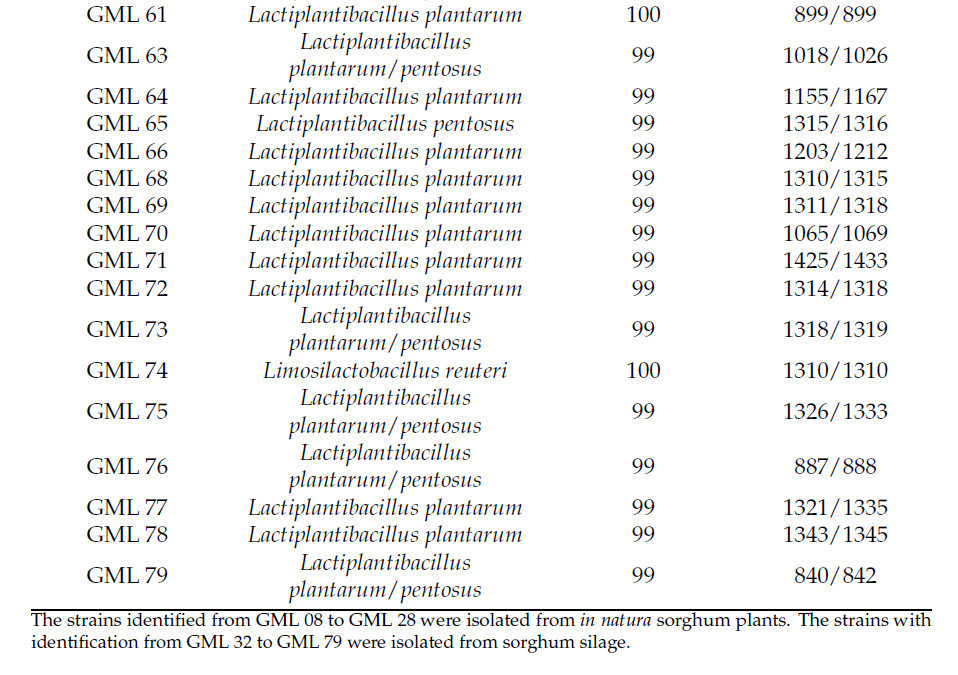
Все выделенные штаммы показали сходство последовательностей пар оснований, равное или превышающее 99%, по сравнению с базой данных GenBank через алгоритм BLAST (Национальный центр биотехнологической информации, Бетесда, MD, USA). Среди 44 изолятов было идентифицировано четыре типа видов бактерий: Lactiplantibacillus plantarum, Pediococcus pentosaceus, Lactiplantibacillus plantarum/pentosus и Limosilactobacillus reuteri. Наблюдалось преобладание Lactiplantibacillus plantarum среди 44 выделенных штаммов, независимо от их происхождения (растение сорго in natura или силос), что соответствовало 72,73% от общего числа (Таблица 4).
Таблица 4. Изоляты, сходство видов бактерий и количество оснований изолятов из сорго in natura и силоса.
3.2. Использование бактерий в качестве инокулянтов в силосе из сорго
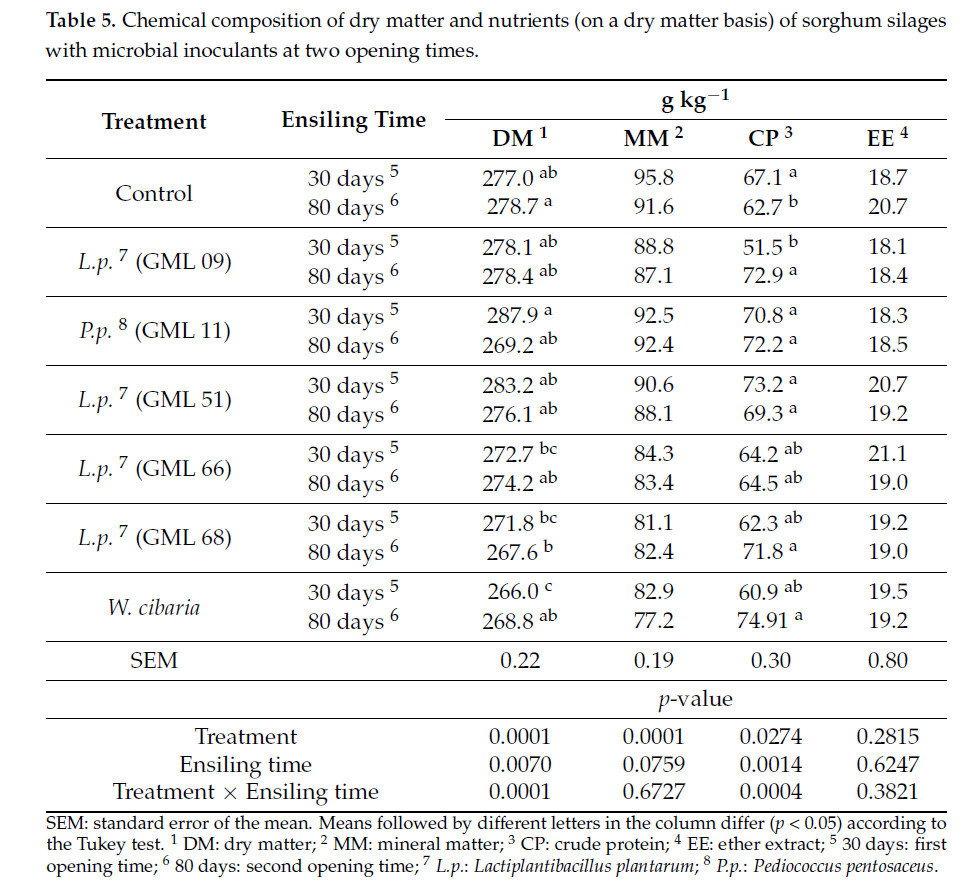
Было обнаружено влияние взаимодействия (p < 0,05) на содержание СВ (p = 0,0001) и СП (p = 0,0004) в силосах в зависимости от использования штаммов в качестве микробных инокулянтов и сроков вскрытия экспериментальных силосов. Наблюдалось различие (p < 0,05) по содержанию СВ, выраженному в г кг⁻¹, причем наиболее высокое значение наблюдалось через 30 дней в силосе, инокулированном штаммом GML 11, а наиболее низкое — в силосе, инокулированном W. cibaria. Через 80 дней после силосования наиболее высокое содержание СВ наблюдалось в контрольном силосе, а наиболее низкое — в силосе, инокулированном штаммом GML 68 (Таблица 5).
Таблица 5. Химический состав сухого вещества и питательных веществ (в пересчете на сухое вещество) силосов из сорго с микробными инокулянтами в два срока вскрытия.
Наблюдалось различие (p < 0,05) по содержанию СП, выраженному в г кг⁻¹ СВ, причем наиболее высокое содержание наблюдалось через 30 дней в контрольных силосах и силосах, инокулированных штаммами GML 11 и GML 51, без различий между ними, а наиболее низкое — в силосе, инокулированном штаммом GML 09. Через 80 дней после силосования наиболее высокое содержание СП наблюдалось в силосах, инокулированных штаммами GML 09, GML 11, GML 51, GML 68 и W. cibaria, без различий между ними, а наиболее низкое содержание — в контрольном силосе (Таблица 5).
Влияния взаимодействия (p > 0,05) на содержание золы (p = 0,6727) и СЖ (p = 0,3821) обнаружено не было. Однако был обнаружен изолированный эффект штамма на содержание золы, выраженное в г кг⁻¹ СВ (p = 0,0001), с наиболее высокими показателями в контрольном силосе и силосе, инокулированном штаммом GML 11, без различий между ними, и наиболее низким в силосе, инокулированном W. cibaria. Однако не было обнаружено различий (p > 0,05) по содержанию СЖ (p = 0,2815) в силосах, с общим средним значением 19,28 г кг⁻¹ СВ. Что касается сроков вскрытия после силосования, не было обнаружено различий (p > 0,05) по переменным зола (p = 0,0759) или СЖ (p = 0,6247), с общими средними значениями 87,00 и 19,25 г кг⁻¹ СВ соответственно (Таблица 5).
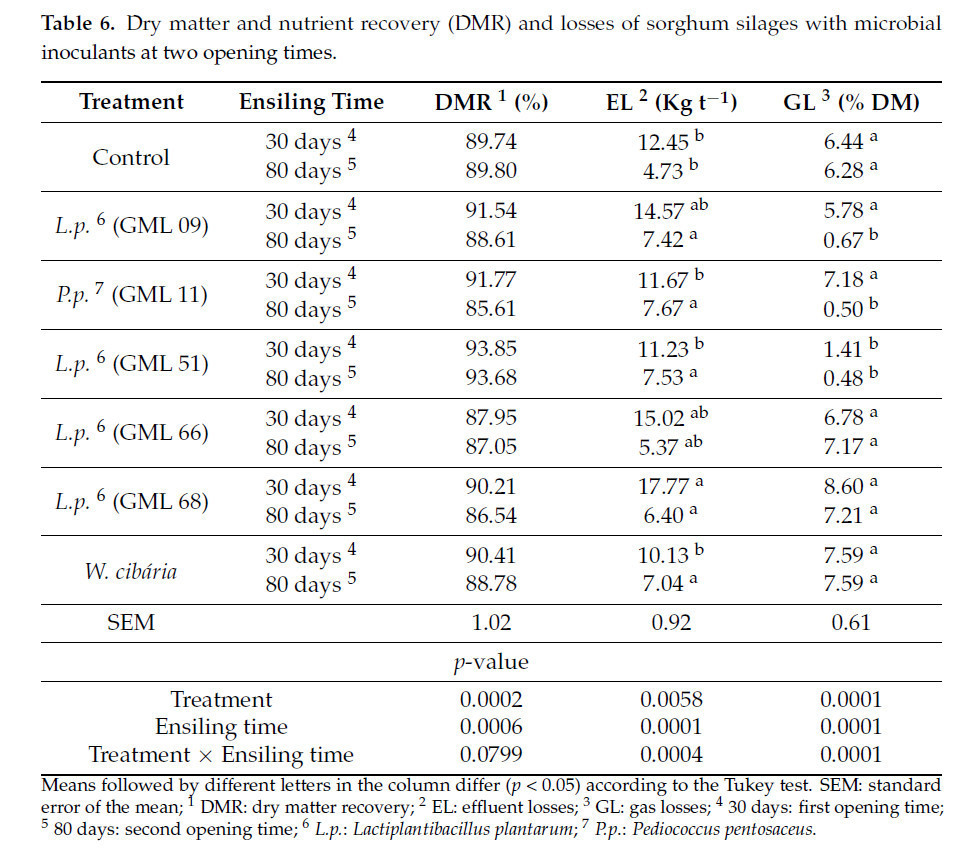
Существовало взаимодействие (p < 0,05) между штаммами, использованными в качестве микробных инокулянтов, и сроками вскрытия экспериментальных силосов для EL (p = 0,001) и GL (p = 0,0004). Наблюдалось различие (p < 0,05) для EL, выраженной в кг т⁻¹, причем наиболее высокое значение EL наблюдалось через 30 дней в силосе, инокулированном штаммом GML 68, а наиболее низкое — в неинокулированном (контрольном) силосе и силосах, инокулированных штаммами GML 11, GML 51 и W. cibaria, без различий между ними (Таблица 6).
Таблица 6. Выход сухого вещества и питательных веществ (ВСВ) и потери силосов из сорго с микробными инокулянтами в два срока вскрытия.
Наблюдалось различие (p < 0,05) для GL, выраженной в % СВ, причем наиболее высокие потери GL наблюдались через 30 дней в контрольном силосе и силосах, инокулированных штаммами GML 09, GML 11, GML 66, GML 68 и W. cibaria, без различий между ними, а наиболее низкие — в силосе, инокулированном штаммом GML 51. Через 80 дней после силосования наиболее высокие значения GL наблюдались в контрольном силосе. Силосы, инокулированные штаммами GML 66, GML 68 и W. cibaria, не имели различий между собой, а наиболее низкие значения наблюдались в силосах, инокулированных штаммами GML 09, GML 11 и GML 51, без различий между ними (Таблица 6).
Влияния взаимодействия (p = 0,0799) на ВСВ силосов обнаружено не было. Однако был обнаружен изолированный эффект штаммов (p = 0,0002), использованных в качестве микробных инокулянтов в силосах, с наиболее высоким ВСВ, наблюдаемым в силосе, инокулированном штаммом GML 51, и наиболее низким — в контрольном силосе и силосах, инокулированных штаммами GML 09, GML 11, GML 66, GML 68 и W. cibaria, без различий между ними. Что касается сроков вскрытия после силосования, наблюдалось различие (p = 0,0006), с наиболее высоким средним значением, наблюдаемым в срок вскрытия 30 дней, и наиболее низким — через 80 дней после силосования (Таблица 6).
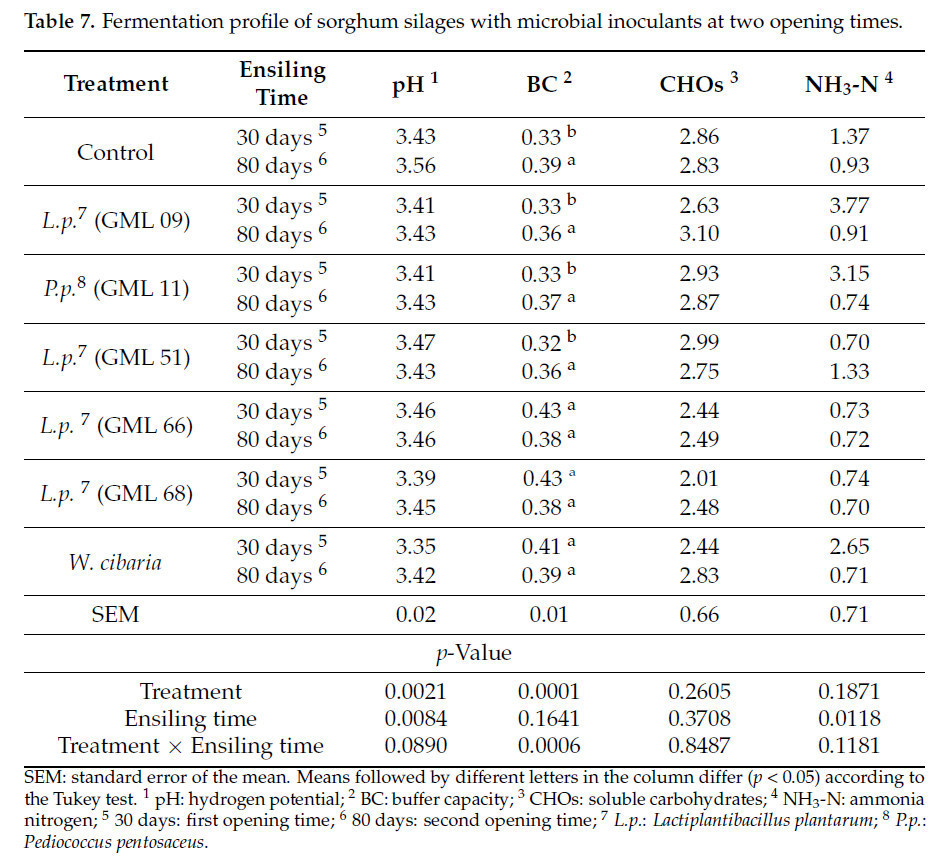
Существовало влияние взаимодействия (p < 0,05) между штаммами, использованными в качестве микробных инокулянтов, и сроками вскрытия экспериментальных силосов для БЕ (p = 0,0006). Наблюдалось различие (p < 0,05) для БЕ (экв. мг HCl 100 г⁻¹ СВ), с наиболее высокими средними значениями, наблюдаемыми через 30 дней в силосах, инокулированных штаммами GML 66, GML 68 и W. cibaria, без различий между ними, и наиболее низкими — в контрольном силосе и силосах, инокулированных штаммами GML 09, GML 11 и GML 51, без различий между ними. Однако средние значения вариантов обработки не различались через 80 дней после силосования (Таблица 7).
Таблица 7. Профиль ферментации силосов из сорго с микробными инокулянтами в два срока вскрытия.
Влияния взаимодействия (p > 0,05) на pH (p = 0,0890), CHOs (p = 0,8487) или NH₃-N (p = 0,1181) обнаружено не было. Был обнаружен изолированный эффект штамма (p < 0,05) для переменных pH (p = 0,0021), с наиболее высоким средним значением, наблюдаемым в контрольном силосе, и наиболее низким — в силосе, инокулированном W. cibaria. Однако не было обнаружено различий (p > 0,05) для CHOs (p = 0,2605) или NH₃-N (p = 0,1871), с общими средними значениями 2,68 и 1,36 соответственно (Таблица 7).
Что касается сроков вскрытия после силосования, было обнаружено различие (p < 0,05) для pH (p = 0,0084) и NH₃-N (p = 0,0118), с наиболее высокими средними значениями, наблюдаемыми в сроки вскрытия 80 и 30 дней, и наиболее низкими через 30 и 80 дней после силосования соответственно. Однако не было выявлено влияния (p = 0,3708) сроков вскрытия на CHOs, с общим средним значением 2,68 г кг⁻¹ СВ (Таблица 7).
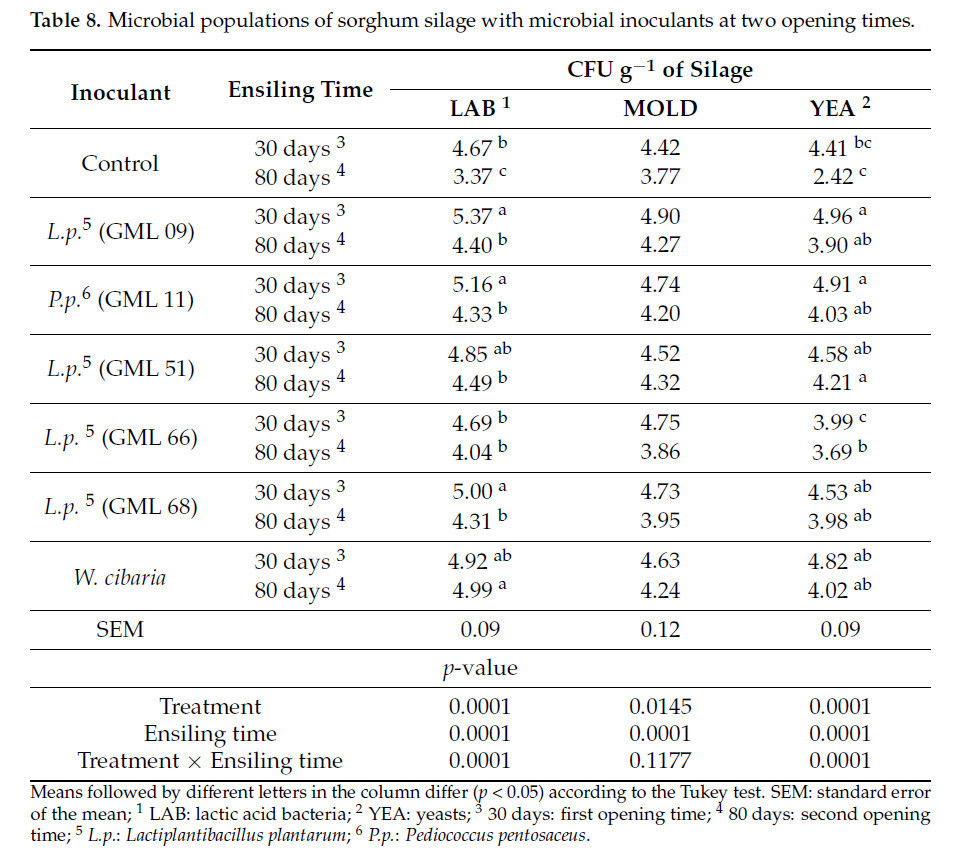
Наблюдалось влияние взаимодействия (p < 0,05) на популяции МКБ (p = 0,0001) и YEA (p = 0,0001) в зависимости от использования штаммов в качестве микробных инокулянтов и сроков вскрытия экспериментальных силосов. Наблюдалось различие (p < 0,05) для популяции МКБ (КОЕ г силоса), причем наиболее высокие популяции наблюдались через 30 дней в силосах, инокулированных штаммами GML 09, GML 11 и GML 68, без различий между ними, а наиболее низкие — в контрольных силосах и силосе, инокулированном штаммом GML 66. Через 80 дней после силосования наиболее высокая популяция МКБ наблюдалась в силосе, инокулированном W. cibaria, а наиболее низкая — в контрольном силосе (Таблица 8).
Таблица 8. Микробные популяции силоса из сорго с микробными инокулянтами в два срока вскрытия.
Наблюдалось различие (p < 0,05) для популяции YEA (КОЕ г силоса), причем наиболее высокие популяции наблюдались через 30 дней в силосах, инокулированных штаммами GML 09 и GML 11, без различий между ними, а наиболее низкие — в силосе, инокулированном штаммом GML 66. Через 80 дней после силосования наиболее высокая популяция YEA наблюдалась в силосе, инокулированном штаммом GML 51, а наиболее низкая — в контрольном силосе (Таблица 8).
Влияния взаимодействия (p > 0,05) на популяцию MOLD (плесени) (p = 0,1177) в силосах (КОЕ г силоса) обнаружено не было. Однако был обнаружен изолированный эффект штамма (p = 0,0145), с наиболее высокими популяциями плесени, обнаруженными в силосах, инокулированных штаммами GML 09 и GML 11, и наиболее низкой — в контрольном силосе. Что касается сроков вскрытия, наблюдалось различие (p = 0,0001), с наиболее высокой популяцией, наблюдаемой в срок вскрытия 30 дней, и наиболее низкой — через 80 дней после силосования (Таблица 8).
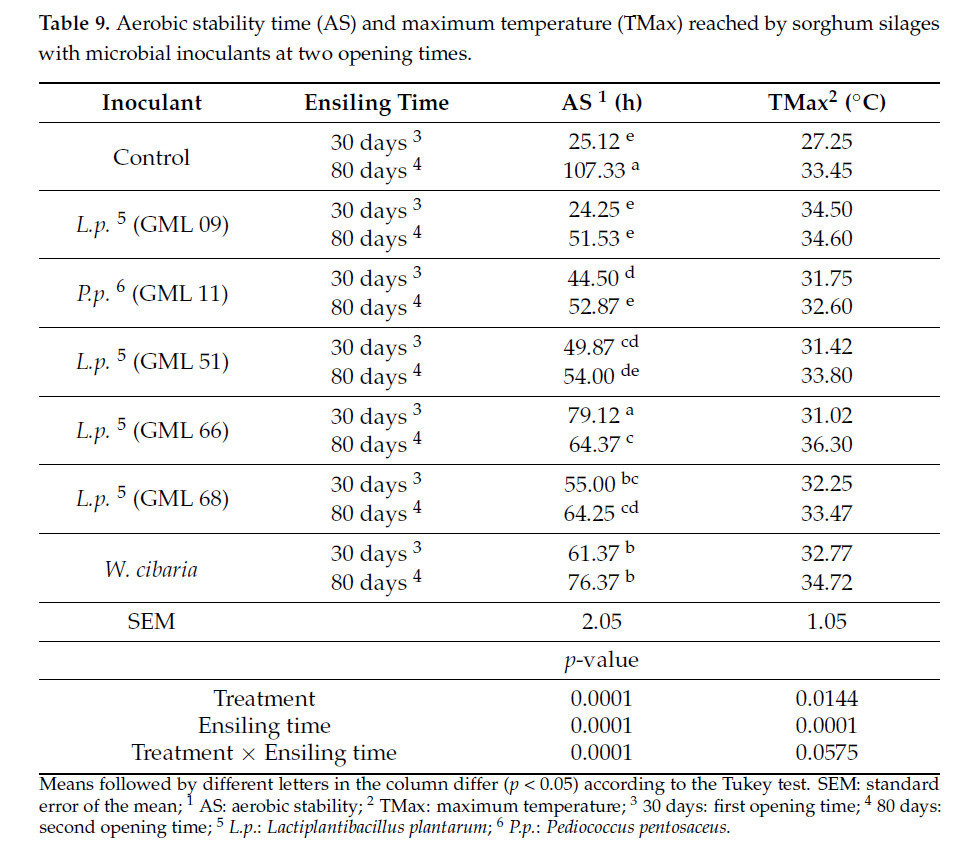
Существовало взаимодействие (p < 0,05) между штаммами, использованными в качестве микробных инокулянтов, и сроками вскрытия экспериментальных силосов для AS (аэробной стабильности) (p = 0,0001), выраженной в часах. Наблюдалось различие (p < 0,05) для AS силосов, с наиболее длительным временем, наблюдаемым через 30 дней в силосе, инокулированном штаммом GML 66, и наиболее коротким — в контрольном силосе и силосе, инокулированном штаммом GML 09. Через 80 дней после силосования наиболее длительное время AS наблюдалось в контрольном силосе, а наиболее короткое — в силосах, инокулированных штаммами GML 09 и GML 11 (Таблица 9).
Таблица 9. Время аэробной стабильности (AS) и максимальная температура (TMax), достигнутая силосами из сорго с микробными инокулянтами в два срока вскрытия.
Влияния взаимодействия (p > 0,05) на Tmax (p = 0,0575) силосов (°C) обнаружено не было. Однако был обнаружен изолированный эффект штамма (p = 0,0144) микробных инокулянтов, с наиболее высокими температурами, наблюдаемыми в силосах, инокулированных штаммами GML 09, GML 66 и W. cibaria, и наиболее низкой — в контрольном силосе. Что касается сроков вскрытия, наблюдалось различие (p = 0,0001), с наиболее высокой температурой, зарегистрированной в срок вскрытия 80 дней, и наиболее низкой — через 30 дней после силосования (Таблица 9).
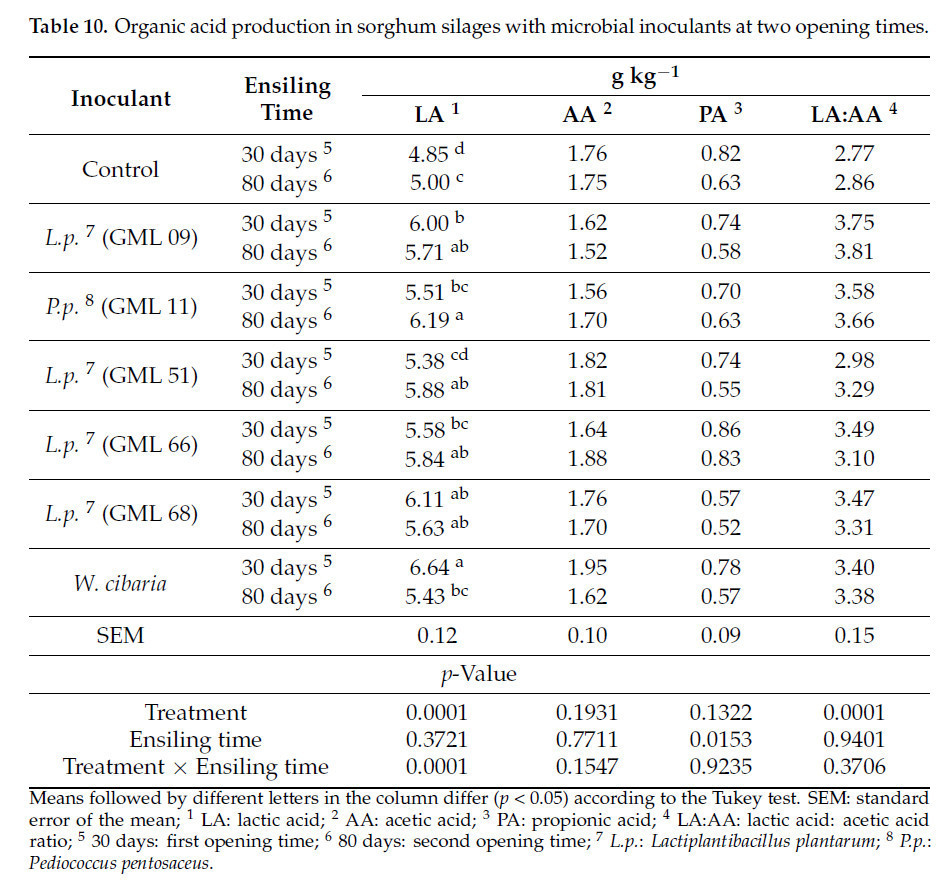
Существовало взаимодействие (p < 0,05) между штаммами, использованными в качестве микробных инокулянтов, и сроками вскрытия экспериментальных силосов для AL (молочной кислоты) (p = 0,0001). Наблюдалось различие (p < 0,05) в содержании МК в силосах, с наиболее высокой концентрацией, наблюдаемой через 30 дней в силосе, инокулированном W. cibaria, и наиболее низкой — в контрольном силосе и силосе, инокулированном штаммом GML 09. Через 80 дней после силосования наиболее высокое содержание МК наблюдалось в силосе, инокулированном штаммом GML 11, а наиболее низкое — в контрольном силосе (Таблица 10).
Таблица 10. Продукция органических кислот в силосах из сорго с микробными инокулянтами в два срока вскрытия.
Влияния взаимодействия (p > 0,05) на УК (p = 0,1547), ПК (p = 0,9235) или соотношение МК:УК (p = 0,3706) обнаружено не было. Был обнаружен изолированный эффект штамма (p < 0,05) для соотношения МК:УК (p = 0,0001), с наиболее высоким соотношением, наблюдаемым в силосе, инокулированном GML 09, и наиболее низким — в контрольном силосе. Однако не было обнаружено различий (p > 0,05) для УК (p = 0,1931) или ПК (p = 0,7711), с общими средними значениями 1,72 и 0,68 г кг⁻¹ соответственно (Таблица 10).
Что касается сроков вскрытия после силосования, наблюдалось различие (p < 0,05) для содержания ПК (p = 0,0153), с наиболее высокой концентрацией, наблюдаемой в срок вскрытия 30 дней, и наиболее низкой — через 80 дней после силосования. Однако не было обнаружено различий (p > 0,05) для УК (p = 0,7711) или соотношения МК:УК (p = 0,9401) в зависимости от сроков вскрытия, с общими средними значениями 1,72 и 3,34 г кг⁻¹ соответственно (Таблица 10).
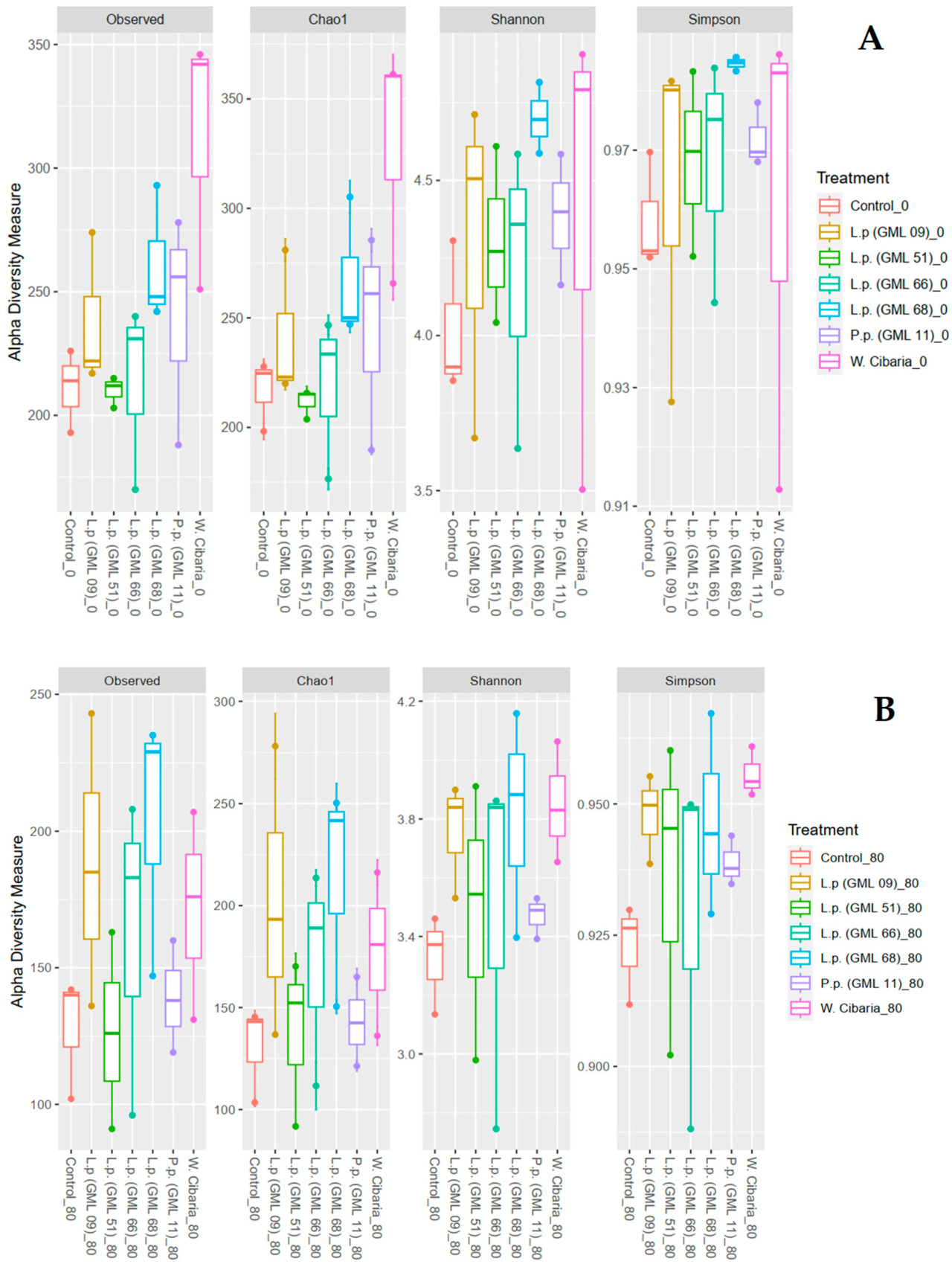
Что касается индексов альфа-разнообразия, наблюдалось более высокое разнообразие для варианта с Weissella cibaria по сравнению с контрольным вариантом перед силосованием, согласно индексам разнообразия Observed и Chao1, но не было статистических различий между сообществами для индексов Shannon и Simpson (Рисунок 2A). В конце 80-дневного периода ферментации не наблюдалось различий в разнообразии между сообществами по индексам альфа-разнообразия (Рисунок 2B).
Рисунок 2. Анализ альфа-разнообразия метагеномов по всем вариантам обработки в нулевой момент времени (A) и через 80 дней после силосования (B), основанный на индексах Chao1, Shannon и Simpson.
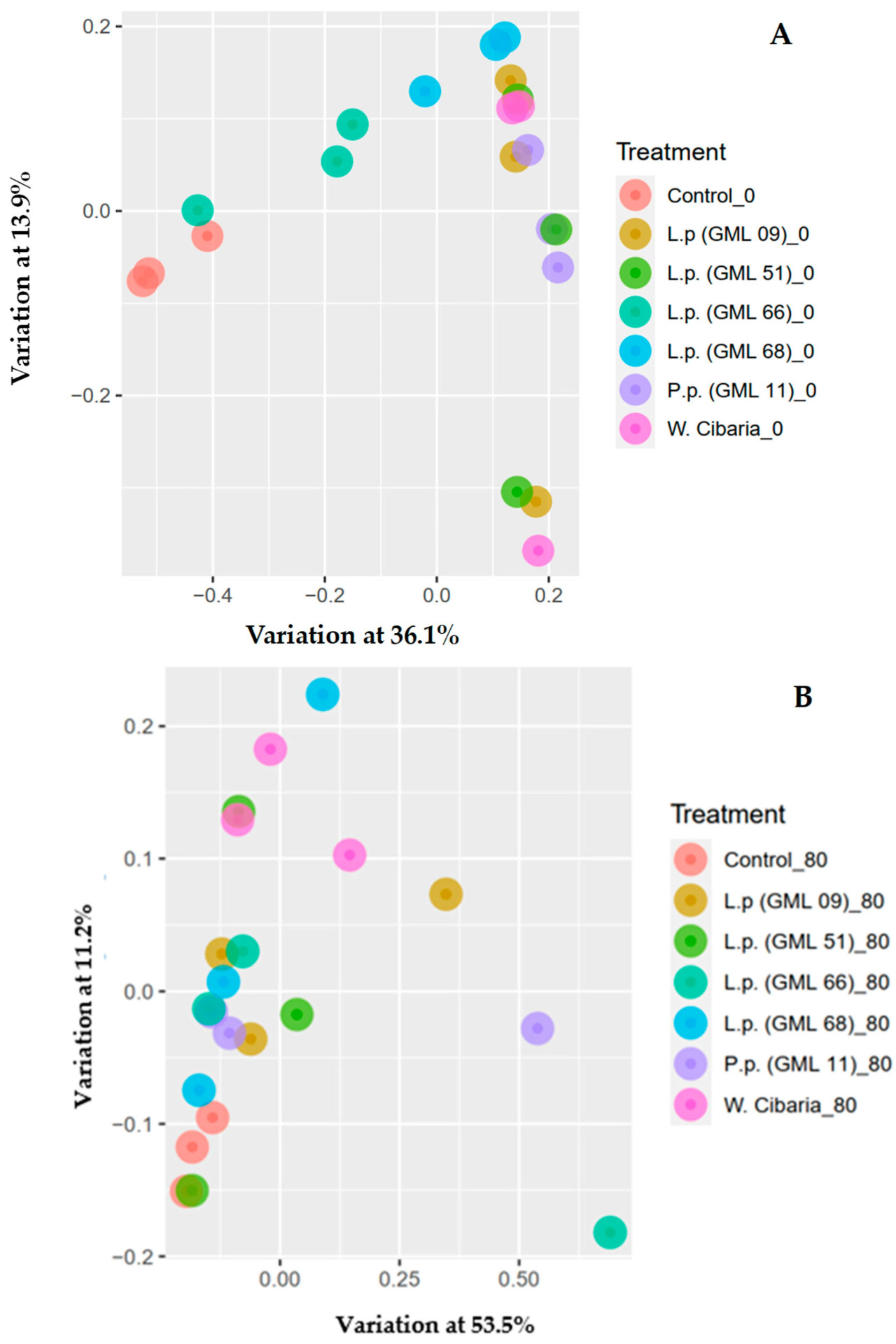
Индекс бета-разнообразия показал, что перед силосованием контрольный вариант обработки был более обильным, представляя таксономический состав, в разной степени отличающийся от других вариантов обработки (Рисунок 3A). Сообщества вариантов обработки не показали больших различий в своем составе после 80 дней ферментации при анализе с помощью индекса бета-разнообразия (Рисунок 3B).
Рисунок 3. Анализ бета-разнообразия метагеномов по всем вариантам обработки в нулевой момент времени (A) и через 80 дней после силосования (B), представленный графиками анализа главных координат (PCoA).
4. Обсуждение
Молочнокислые бактерии классифицируются как грамположительные, с каталазоотрицательной активностью, не образующие спор, продуцирующие молочную кислоту и факультативные анаэробы (Zheng и др.) [29]. Однако эти бактерии могут продуцировать другие типы органических кислот помимо молочной кислоты и могут быть охарактеризованы как гомоферментативные или гетероферментативные.
Микроорганизмы, идентифицированные в этом исследовании, принадлежат к семейству Lactobacillaceae. Это семейство молочнокислых микроорганизмов включает гомоферментативные и гетероферментативные бактерии, как обнаружили Zheng и др. [29], которые заявили, что Pediococcus и бактерии, принадлежащие к группе Lactiplantibacillus plantarum, имеют эволюционную связь между собой (Таблица 4). Согласно тем же авторам, несмотря на метаболические характеристики, ориентированные на гомоферментацию, то есть производство молочной кислоты, эти бактерии филогенетически взаимосвязаны с гетероферментативными бактериями.
Штаммы, идентифицированные в этом исследовании, продуцировали уксусную и пропионовую кислоты, что выделяет Lactiplantibacillus plantarum (GML 66) и Lactiplantibacillus plantarum (GML 68) (Таблица 3). Хотя эти бактерии считаются гомоферментативными, они были способны продуцировать другие органические кислоты, что подтверждает утверждения Zheng и др. [29] о том, что они филогенетически взаимосвязаны с гетероферментативными бактериями.
Наблюдаемые значения СВ, СЖ и СП (Таблица 5) сходны со значениями, найденными Rodrigues и др. [30] и Santos и др. [31], которые работали с силосами из сорго с микробными инокулянтами. Исследования силоса из жома сахарного сорго с коммерческими микробными инокулянтами, состоящими из Lactiplantibacillus plantarum и Lentilactobacillus buchneri, показали более высокое содержание СВ в вариантах с этими инокулянтами, чем в варианте без инокуляции бактерий [32], что подтверждает настоящее исследование, где варианты обработки, инокулированные Lactiplantibacillus plantarum (GML 09), Pediococcus pentosaceus (GML 11) и Lactiplantibacillus plantarum (GML 51), вскрытые через 30 дней, остались статистически сходными с контрольным вариантом.
Только Lactiplantibacillus plantarum (GML 09) отличался от других вариантов по значениям СП (Таблица 5) в наиболее короткий срок вскрытия. Этот результат связан со значением NH₃-N (Таблица 7) для того же варианта в тот же срок вскрытия, что указывает на то, что наблюдалась несколько более интенсивная протеолитическая активность, чем в других вариантах, что привело к более низкому содержанию СП (Таблица 5) по сравнению с различными вариантами и, следовательно, к более высокому содержанию NH₃-N (Таблица 7) в этом силосе. Согласно Sun и др. [33] и Li и др. [34], протеолитическая активность, происходящая в процессе ферментации, приводит к образованию азотистых соединений, аминокислот, аммиака и биоактивных пептидов, демонстрируя пробиотические характеристики, связанные с Lactiplantibacillus plantarum.
Более низкое содержание СП (Таблица 5) наблюдалось в контрольном силосе по сравнению с другими вариантами, которые различались в наиболее длительный срок вскрытия. На это прямо повлияло более высокое значение pH (3,56) (Таблица 7) в тот же срок вскрытия, что указывает на то, что могла произойти протеолиз.
Инокуляция Lactiplantibacillus plantarum (GML 09) в наиболее короткий срок вскрытия привела к необычной реакции, как указали Silva и др. [35], получившие более низкое содержание СП для инокулированных силосов из сорго и кукурузы (54,8 и 70,0 г кг⁻¹ СВ соответственно) по сравнению с теми же силосами без инокуляции микроорганизмов (55,8 и 72,2 г кг⁻¹ СВ соответственно). Michel и др. [36] изучали инокулированные силосы из сорго и наблюдали, что инокулированные силосы получили более высокое содержание СП (67,7 г кг⁻¹ СВ) по сравнению с силосом без инокулянтов (64,7 г кг⁻¹ СВ), ведя себя сходно с контрольным вариантом, вскрытым через 80 дней в настоящем исследовании (Таблица 5).
Силос, инокулированный Lactiplantibacillus plantarum (GML 51), привел к более высокому ВСВ (Таблица 6), что было отнесено на счет гомоферментативного брожения, производящего гораздо больше молочной кислоты, чем уксусной (Таблица 10). Несмотря на различие в процессе ферментации силоса, этих изменений было недостаточно, чтобы изменить ВСВ.
Через 30 дней после силосования силос, инокулированный W. cibaria, выделялся среди других, показывая наиболее низкие EL среди них (10,13 кг т⁻¹). Напротив, через 80 дней после силосования силосы из контрольного варианта и Lactiplantibacillus plantarum (GML 66) показали наиболее низкие EL: 4,73 и 5,73 кг т⁻¹ соответственно (Таблица 6). Dos Santos и др. [37] также обнаружили более высокие EL в кукурузном силосе без инокулянта и с лиофилизированным инокулянтом, тогда как более низкие EL (0,45 кг т⁻¹) были получены при оценке кукурузного силоса с активированным инокулянтом.
Инокуляция Lactiplantibacillus plantarum (GML 51) привела к наиболее низким GL (1,41% СВ) при первом вскрытии. Что касается второго вскрытия, варианты контроль, Lactiplantibacillus plantarum (GML 66), Lactiplantibacillus plantarum (GML 68) и Weissella cibaria привели к наиболее высоким GL, в диапазоне от 6,28 до 7,59% СВ (Таблица 6).
Coelho и др. [38] наблюдали, что газообразные потери не подверглись влиянию эффекта совместной инокуляции Lactobacillus plantarum и Propionibacterium acidipropionici в перемещенных кукурузных силосах. С другой стороны, в исследованиях Dos Santos и др. [37], GL были значительно выше для силосов с активным инокулянтом (5,55% СВ), результат, который был выше, чем в контрольных силосах и силосах с лиофилизированным инокулянтом, которые показали 2,67 и 3,17% СВ соответственно.
Для данных, относящихся к БЕ силоса (Таблица 7), силосы, инокулированные Lactiplantibacillus plantarum (GML 66), Lactiplantibacillus plantarum (GML 68) и Weissella cibaria, показали большую устойчивость среди других вариантов в первый срок вскрытия, и не было обнаружено различий между вариантами для второго срока вскрытия. Yin и др. [39] изучали Lentilactobacillus buchneri в кукурузных силосах и наблюдали, что инокулированный силос получил более высокую концентрацию общих кислот, хотя и не очень значительную по сравнению с кукурузным силосом без инокулянта. Согласно Yin и др. [39], химические реакции могут происходить внутри силоса с участием произведенных органических кислот, что приводит к увеличению газообразования и снижению буферной емкости. Варианты с Lactiplantibacillus plantarum (GML 66), Lactiplantibacillus plantarum (GML 68) и Weissella cibaria показали более высокие GL, чем другие, в первый срок вскрытия, что подтверждает Yin и др. [39], которые указали, что произошла химическая реакция, снижающая БЕ этих вариантов к следующему сроку вскрытия.
Наблюдалось снижение всех микробных популяций (Таблица 8) через 80 дней, в фазе стабильности ферментации. В этой фазе наблюдается, что ферментация протекает более мягко (Таблица 10).
Было видно, что в оба срока вскрытия контрольный вариант представлял наиболее низкие показатели МКБ. Из-за инокуляции бактерий в другие варианты этот результат был уже ожидаем (Таблица 8). Rabelo и др. [40], Chen и др. [41] и Soundharrajan и др. [42] подтвердили данные по МКБ настоящего исследования, так как в их исследованиях также были обнаружены более высокие показатели МКБ в силосах, инокулированных молочнокислыми бактериями, по сравнению с контрольным вариантом.
Тот же результат наблюдался для популяции YEA (Таблица 8). Это могло произойти из-за более высокой продукции молочной кислоты в других вариантах (Таблица 10), которая может служить субстратом для развития YEA, а также из-за их более низких значений pH (Таблица 7), что дополнительно благоприятствовало росту популяции YEA (Таблица 8). Dos Santos и др. [37] также нашли сходные результаты для микробной популяции YEA при вскрытии силосов через 70 дней, где вариант с активным инокулянтом получил 5,17 КОЕ г⁻¹ силоса, а контрольный вариант получил 4,86 КОЕ г⁻¹ силоса, что представляет снижение на 0,31 КОЕ г⁻¹ силоса.
Что касается результатов AS среди вариантов, было обнаружено, что Lactiplantibacillus plantarum (GML 09), Pediococcus pentosaceus (GML 11), Lactiplantibacillus plantarum (GML 51) и Lactiplantibacillus plantarum (GML 68) способствовали снижению времени AS силосов, влияя на них негативно. Lactiplantibacillus plantarum (GML 66) и Weissella cibaria продлили время AS силосов.
Можно наблюдать, что произошло увеличение AS и TMax для сроков вскрытия, когда силосы были вскрыты позднее. Это увеличение означает, что, несмотря на продление времени стабильности после вскрытия силосов и воздействия кислорода, также произошло повышение температуры этих силосов во время вторичной микробной активности, повысив их внутреннюю температуру.
Когда силосы были вскрыты через 30 дней, за исключением Lactiplantibacillus plantarum (GML 09), который был ниже контрольного варианта, все варианты получили более высокие результаты, что выделяет Lactiplantibacillus plantarum (GML 66). Эта длительная стабильность объясняется микробиологическими данными популяции YEA этого же варианта в тот же срок вскрытия (Таблица 8), и эти микроорганизмы ответственны за ускорение порчи силоса, используя как остаточные растворимые углеводы, так и произведенную молочную кислоту.
Что касается второго срока вскрытия, наилучшее время AS было получено контрольным вариантом, за которым следовали Weissella cibaria и Lactiplantibacillus plantarum (GML 66). Несмотря на способность продуцировать уксусную кислоту в больших количествах, более быстрое подкисление среды и более высокое содержание молочной кислоты (Таблица 10) привели к более высокому количеству YEA (Таблица 8) в инокулированных силосах за 80-дневный период, где контрольный вариант выделялся наиболее низким количеством микробной популяции YEA для этого срока вскрытия (Таблица 8). Этот результат подтверждает Ferrero и др. [43], которые обнаружили обратно пропорциональную зависимость между временем до нарушения аэробной стабильности и популяцией дрожжей.
Dos Santos и др. [37] наблюдали более короткое время AS для контрольного варианта по сравнению с инокулированными силосами из сорго. Nkosi и др. [44] оценили силосы, инокулированные Lactiplantibacillus plantarum и Lentilactobacillus buchneri, и наблюдали, что силосы с Lactiplantibacillus plantarum получили наихудшую AS, всего 46 ч, что было ниже, чем в контрольном варианте (53 ч) и с Lentilactobacillus buchneri (72 ч). Эти данные подтверждают настоящее исследование для результатов срока вскрытия 80 дней, поскольку использованные штаммы были Lactiplantibacillus plantarum, и он также получил более низкие значения AS по сравнению с контролем. Исследование Michel и др. [36] также подтвердило эти данные, также наблюдая лучшее время AS для силосов, которые не были инокулированы. Таким образом, изоляты настоящего исследования могут быть эффективны в комбинациях с гетероферментативными молочнокислыми бактериями, поскольку по отдельности они не эффективны в контроле аэробной стабильности силосов.
Обычно кислые силосы могут способствовать превращению этанола в уксусную кислоту под действием уксуснокислых бактерий, что объясняет, что могло произойти в увеличении времени AS в этом исследовании (Таблица 9). С точки зрения краткосрочного вскрытия силоса, силос без инокуляции оказался не очень эффективным, показывая, что в этом случае инокуляция необходима.
В оба срока вскрытия силос без микробного инокулянта получил наиболее низкие значения продукции молочной кислоты (Таблица 10). Этот результат подтверждает более высокую продукцию молочной кислоты в силосах, которые были инокулированы. Инокуляция Weissella cibaria привела к более высокой продукции молочной кислоты, статистически отличаясь только от контрольного варианта и от Lactiplantibacillus plantarum (GML 51). Этот результат показывает, что другие штаммы, инокулированные в силосы, несмотря на то, что считаются гомоферментативными, вели себя сходно с Weissella cibaria, которая является гетероферментативной.
В целом, за исключением контрольного варианта, все инокулированные силосы получили результаты между 4,36 КОЕ г⁻¹ силоса (Lactiplantibacillus plantarum GML 66) и 4,95 КОЕ г⁻¹ силоса (Weissella cibaria). Эти результаты напрямую связаны с продукцией молочной кислоты, которая получила наиболее высокие концентрации для силосов с более высокими микробными показателями молочнокислых бактерий (Таблица 10).
Эти данные также связаны со значениями pH (Таблица 7). Согласно Xu и др. [45], молочнокислые бактерии могут быстро преобразовывать растворимые углеводы в органические кислоты, вызывая резкое падение pH до более кислых уровней. Такое поведение pH происходило обратно пропорционально продукции молочной кислоты, поскольку увеличение концентрации органических кислот, особенно молочной кислоты, вызывает более кислый pH в силосе (Таблица 7 и Таблица 10). Кроме того, Dos Santos и др. [37] обнаружили такое же обратное поведение для силосов, вскрытых через 70 дней, где контрольный силос и силос, инокулированный активным инокулянтом, получили 46,61 и 38,56 г кг⁻¹ СВ соответственно, причем контрольный силос получил более кислый pH (3,52), а силос с активным инокулянтом получил менее кислое значение (3,66), статистически отличаясь друг от друга.
Между сроками вскрытия наблюдалась более высокая продукция пропионовой кислоты, когда силос был вскрыт раньше (Таблица 10). Этот результат может быть связан с более высокой доступностью молочной кислоты в первый период вскрытия (Chen и др. [41]), служащей субстратом для метаболизма бактерий и преобразования ее в другие кислоты, такие как пропионовая кислота.
На соотношение молочная кислота:уксусная кислота прямо повлияла разница между вариантами в продукции молочной кислоты, поскольку чем больше вариация одной из двух кислот, тем больше разница в соотношении молочная кислота:уксусная кислота. Среди вариантов, поскольку контроль получил наиболее низкую продукцию молочной кислоты, он, следовательно, получил наиболее низкое соотношение молочная кислота:уксусная кислота (Таблица 10).
Данные альфа-разнообразия показали, что существовала более высокая численная концентрация для варианта с Weissella cibaria по сравнению с контролем перед периодом ферментации (Рисунок 2A). После периода ферментации наблюдалось снижение этой бактериальной популяции в силосах, поэтому между ними не было различий. Согласно Du и др. [46], ферментированные силосы имеют более низкое альфа-разнообразие по сравнению с тем же материалом до периода ферментации. Это происходит из-за преобладания МКБ, которые вызывают снижение pH силоса из-за продукции органических кислот, будучи способными ингибировать и снижать бактериальное разнообразие, присутствующее в силосе. Как наблюдается в Таблице 8, произошло снижение всех микробных популяций, количественно определенных в этом исследовании (МКБ, плесени и дрожжи). Эти результаты микробной популяции связаны со значениями pH (Таблица 7) и органических кислот (Таблица 10), подтверждая это снижение альфа-разнообразия.
Результаты бета-разнообразия показали, что использование инокуляции бактерий, независимо от использованного штамма, способствовало дифференциации среди всех вариантов по сравнению с контролем перед силосованием. После периода ферментации не наблюдалось различий между ними (Рисунок 3B). Это могло произойти из-за большего обилия некоторых доминирующих видов бактерий, способных развиваться и расти в больших количествах, способствуя снижению диверсификации присутствующего бактериального сообщества. Подтверждая это исследование, Muraro и др. [47] также наблюдали снижение бета-разнообразия, преобладание которого происходило среди четырех основных видов, где авторы объяснили, что не было значительных различий между вариантами из-за низкого разнообразия в этом индексе.
Таким образом, можно наблюдать, что продвижение периода ферментации силосов, помимо способствования численному снижению микробной популяции (также наблюдаемому в альфа-разнообразии) (Таблица 8 и Рисунок 2B), приводит к большей конкуренции между доминирующими видами, пока они не достигнут своего наибольшего обилия, чтобы они могли сократить и даже устранить другие менее конкурентоспособные виды.
В силосах из сорго, которые считаются кислыми силосами, может происходить превращение этанола уксуснокислыми бактериями, преобразуясь в уксусную кислоту, что объясняет увеличение аэробной стабильности с течением времени. Однако, когда силос вскрывают через короткий интервал времени без использования микробных инокулянтов, это может привести к менее стабильному силосу.
Инокулянты Lactiplantibacillus plantarum (GML 66), Lactiplantibacillus plantarum (GML 68) и Weissella cibaria выделялись среди использованных штаммов. Их производительность наблюдалась в оба срока вскрытия, через 30 и 80 дней ферментации, что делает возможным их включение в состав инокулянтов в сочетании друг с другом или с другими бактериями, такими как Lentilactobacillus buchneri, способными способствовать более высокому выходу сухого вещества из силосов, продукции органических кислот и большей устойчивости к воздействию кислорода в стабильной форме силосов из сорго.
Таким образом, штаммы Lactiplantibacillus plantarum (GML 66) и Lactiplantibacillus plantarum (GML 68) должны быть применены в будущих исследованиях для проверки их эффективности в сочетании с другими бактериями и на других кормовых культурах.
5. Выводы
Использование модифицированной селективной среды (MRS-MOD) и молекулярных методов повышает точность отбора новых штаммов в качестве микробных инокулянтов и, следовательно, усиливает их влияние на процесс ферментации силосов. Кроме того, это позволит более детально охарактеризовать микробиоту, присутствующую в силосах, облегчая понимание процессов, которые все еще плохо изучены в тропических условиях.
Таким образом, поиск эпифитных бактерий из сорго in natura и силосованного, в разные сроки его вскрытия, привел почти полностью к видам Lactiplantibacillus plantarum и Pediococcus pentaseus. По мере того как период ферментации продвигался, доминирующие виды достигали своего наибольшего обилия, способствуя численному снижению, наблюдаемому в альфа-сообществе. Несмотря на это, Lactiplantibacillus plantarum (GML 66) показал наилучшую производительность в качестве инокулянта в силосе из сорго.
Несмотря на достижения, достигнутые в поиске и выделении новых штаммов молочнокислых бактерий из кормового сорго, культивируемого в засушливых и полузасушливых регионах, все еще существуют ограничения в охвате полной степени микробного разнообразия, присутствующего в образцах, в частности в отношении редких видов, из-за ограниченной глубины секвенирования. В этом контексте будущие исследования должны быть проведены с целью идентификации новых микробных штаммов, интегрируя дополнительные подходы, такие как метаболомный анализ, для достижения более полной и функциональной характеристики микробиома.
Ссылки
1. Muck, R.E. Silage Microbiology and Its Control through Additives. Rev. Bras. Zootec. 2010, 39, 183–191. [Google Scholar] [CrossRef]
2. da Silva, T.C.; da Silva, L.D.; Santos, E.M.; Oliveira, J.S.; Perazzo, A.F. Importance of the Fermentation to Produce High-Quality Silage. Ferment. Process. 2017, 8, 1–20. [Google Scholar]
3. Muck, R.E.; Nadeau, E.M.G.; McAllister, T.A.; Contreras-Govea, F.E.; Santos, M.C.; Kung, L., Jr. Silage Review: Recent Advances and Future Uses of Silage Additives. J. Dairy Sci. 2018, 101, 3980–4000. [Google Scholar] [CrossRef]
4. Tabacco, E.; Piano, S.; Cavallarin, L.; Bernardes, T.F.; Borreani, G. Clostridia Spore Formation during Aerobic Deterioration of Maize and Sorghum Silages as Influenced by Lactobacillus Buchneri and Lactobacillus Plantarum Inoculants. J. Appl. Microbiol. 2009, 107, 1632–1641. [Google Scholar] [CrossRef] [PubMed]
5. Tabacco, E.; Piano, S.; Revello-Chion, A.; Borreani, G. Effect of Lactobacillus Buchneri LN4637 and Lactobacillus Buchneri LN40177 on the Aerobic Stability, Fermentation Products, and Microbial Populations of Corn Silage under Farm Conditions. J. Dairy Sci. 2011, 94, 5589–5598. [Google Scholar] [CrossRef]
6. Lima, R.; Díaz, R.F.; Castro, A.; Hoedtke, S.; Fievez, V. Multifactorial Models to Assess Responses to Sorghum Proportion, Molasses and Bacterial Inoculant on in Vitro Quality of Sorghum–Soybean Silages. Anim. Feed Sci. Technol. 2011, 164, 161–173. [Google Scholar] [CrossRef]
7. Lima, R.; Lourenço, M.; Diaz, R.F.; Castro, A.; Fievez, V. Effect of Combined Ensiling of Sorghum and Soybean with or without Molasses and Lactobacilli on Silage Quality and in Vitro Rumen Fermentation. Anim. Feed Sci. Technol. 2010, 155, 122–131. [Google Scholar] [CrossRef]
8. Abdelhadi, L.O.; Tricarico, J.M. Effects of Stage of Maturity and Microbial Inoculation at Harvest on Nutritive Quality and Degradability of Grain Sorghum Whole-Plant and Head-Chop Silages. Anim. Feed Sci. Technol. 2009, 152, 175–185. [Google Scholar] [CrossRef]
9. Thomas, M.E.; Foster, J.L.; McCuistion, K.C.; Redmon, L.A.; Jessup, R.W. Nutritive Value, Fermentation Characteristics, and in Situ Disappearance Kinetics of Sorghum Silage Treated with Inoculants. J. Dairy Sci. 2013, 96, 7120–7131. [Google Scholar] [CrossRef] [PubMed]
10. Rêgo, A.C.d.; Siqueira, G.R.; Almeida, G.B.D.E.S.; Signoretti, R.D.; Resende, F.D.d. Effect of Particle Size and Bacterial Inoculant on the Temperature, Density and PH of Pearl Millet Silages. Rev. Caatinga 2016, 29, 984–995. [Google Scholar] [CrossRef]
11. Hassanat, F.; Mustafa, A.F.; Seguin, P. Effects of Inoculation on Ensiling Characteristics, Chemical Composition and Aerobic Stability of Regular and Brown Midrib Millet Silages. Anim. Feed Sci. Technol. 2007, 139, 125–140. [Google Scholar] [CrossRef]
12. Srigopalram, S.; Ilavenil, S.; Park HyungSoo, P.H.; Kim DaHye, K.D.; Choi KiChoon, C.K. Effect of Combined Lactobacillus Plantarum Inoculants on Improving Fermentation Quality and Aerobic Stability of Japanese Barnyard Millet Silage; CABI Digital Library: Wallingford, UK, 2018. [Google Scholar]
13. Pang, H.; Qin, G.; Tan, Z.; Li, Z.; Wang, Y.; Cai, Y. Natural Populations of Lactic Acid Bacteria Associated with Silage Fermentation as Determined by Phenotype, 16S Ribosomal RNA and RecA Gene Analysis. Syst. Appl. Microbiol. 2011, 34, 235–241. [Google Scholar] [CrossRef]
14. McGarvey, J.A.; Franco, R.B.; Palumbo, J.D.; Hnasko, R.; Stanker, L.; Mitloehner, F.M. Bacterial Population Dynamics during the Ensiling of Medicago Sativa (Alfalfa) and Subsequent Exposure to Air. J. Appl. Microbiol. 2013, 114, 1661–1670. [Google Scholar] [CrossRef] [PubMed]
15. Ding, Z.; Bai, J.; Xu, D.; Li, F.; Zhang, Y.; Guo, X. Microbial Community Dynamics and Natural Fermentation Profiles of Ensiled Alpine Grass Elymus Nutans Prepared from Different Regions of the Qinghai-Tibetan Plateau. Front. Microbiol. 2020, 11, 855. [Google Scholar] [CrossRef] [PubMed]
16. Kung, L., Jr. Preparation of Silage Water Extracts for Chemical Analyses. Standard Operating Procedure–001 2.03.96; University of Delaware, Ruminant Nutrition Laboratory: Newark, DE, USA, 1996; pp. 1–309. [Google Scholar]
17. Oude Elferink, S.J.W.H.; Krooneman, J.; Gottschal, J.C.; Spoelstra, S.F.; Faber, F.; Driehuis, F. Anaerobic Conversion of Lactic Acid to Acetic Acid and 1, 2-Propanediol by Lactobacillus Buchneri. Appl. Environ. Microbiol. 2001, 67, 125–132. [Google Scholar] [CrossRef] [PubMed]
18. Altschul, S.F.; Gish, W.; Miller, W.; Myers, E.W.; Lipman, D.J. Basic Local Alignment Search Tool. J. Mol. Biol. 1990, 215, 403–410. [Google Scholar] [CrossRef] [PubMed]
19. Kung, L., Jr.; Ranjit, N.K. The Effect of Lactobacillus Buchneri and Other Additives on the Fermentation and Aerobic Stability of Barley Silage. J. Dairy Sci. 2001, 84, 1149–1155. [Google Scholar] [CrossRef] [PubMed]
20. Pereira, G.A.; Santos, E.M.; Araújo, G.G.L.; Oliveira, J.S.; Pinho, R.M.A.; Zanine, A.d.M.; Souza, A.F.N.; Macedo, A.J.S.; Neto, J.M.C.; Nascimento, T.V.C. Isolation and Identification of Lactic Acid Bacteria in Fresh Plants and in Silage from Opuntia and Their Effects on the Fermentation and Aerobic Stability of Silage. J. Agric. Sci. 2019, 157, 684–692. [Google Scholar] [CrossRef]
21. Santana, L.P.; Santos, E.M.; Oliveira, J.S.; Santos, B.R.C.; Carvalho, G.G.P.; Cavalcanti, J.V.F.L.; Cruz, G.F.L.; Pereira, D.M.; Cavalcanti, H.S.; Santos, F.N.S. Microbial Inoculant and Cottonseed Cake as Additives for Millet Silage at Different Fermentation Times. N. Z. J. Agric. Res. 2024, 67, 223–239. [Google Scholar] [CrossRef]
22. Bolsen, K.K.; Lin, C.; Brent, B.E.; Feyerherm, A.M.; Urban, J.E.; Aimutis, W.R. Effect of Silage Additives on the Microbial Succession and Fermentation Process of Alfalfa and Corn Silages. J. Dairy Sci. 1992, 75, 3066–3083. [Google Scholar] [CrossRef]
23. Chaney, A.L.; Marbach, E.P. Modified Reagents for Determination of Urea and Ammonia. Clin. Chem. 1962, 8, 130–132. [Google Scholar] [CrossRef] [PubMed]
24. Playne, M.J.; McDonald, P. The Buffering Constituents of Herbage and of Silage. J. Sci. Food Agric. 1966, 17, 264–268. [Google Scholar] [CrossRef]
25. Mizubuti, I.Y.; Pinto, A.P.; Pereira, E.S.; Ramos, B.M.O. Métodos Laboratoriais de Avaliação de Alimentos Para Animais. Londrina Eduel 2009, 1. [Google Scholar]
26. DuBois, M.; Gilles, K.A.; Hamilton, J.K.; Rebers, P.A.t.; Smith, F. Colorimetric Method for Determination of Sugars and Related Substances. Anal. Chem. 1956, 28, 350–356. [Google Scholar] [CrossRef]
27. Jobim, C.C.; Nussio, L.G.; Reis, R.A.; Schmidt, P. Avanços Metodológicos Na Avaliação Da Qualidade Da Forragem Conservada. Rev. Bras. Zootec. 2007, 36, 101–119. [Google Scholar] [CrossRef]
28. AOAC. Official Methods of Analysis of AOAC International, 20th ed.; George, W., Latimer, Jr., Eds.; AOAC Int.: Gaithersburg, MD, USA, 2016; ISBN 0935584870. [Google Scholar]
29. Zheng, J.; Wittouck, S.; Salvetti, E.; Franz, C.M.A.P.; Harris, H.M.B.; Mattarelli, P.; O’toole, P.W.; Pot, B.; Vandamme, P.; Walter, J. A Taxonomic Note on the Genus Lactobacillus: Description of 23 Novel Genera, Emended Description of the Genus Lactobacillus Beijerinck 1901, and Union of Lactobacillaceae and Leuconostocaceae. Int. J. Syst. Evol. Microbiol. 2020, 70, 2782–2858. [Google Scholar] [CrossRef]
30. Rodrigues, P.H.M.; Senatore, A.L.; de Sousa Lucci, C.; de Andrade, S.J.T.; de Lima, F.R.; Melotti, L. Valor Nutritivo Da Silagem de Sorgo Tratada Com Inoculantes Enzimo-Microbianos. Acta Sci. 2002, 24, 1141–1145. [Google Scholar] [CrossRef]
31. Santos, A.P.M.d.; Santos, E.M.; Oliveira, J.S.d.; Ribeiro, O.L.; Perazzo, A.F.; Martins Araújo Pinho, R.; Macêdo, A.J.d.S.; Pereira, G.A. Effects of Urea Addition on the Fermentation of Sorghum (Sorghum bicolor) Silage. Afr. J. Range Forage Sci. 2018, 35, 55–62. [Google Scholar] [CrossRef]
32. Dong, M.; Li, Q.; Xu, F.; Wang, S.; Chen, J.; Li, W. Effects of Microbial Inoculants on the Fermentation Characteristics and Microbial Communities of Sweet Sorghum Bagasse Silage. Sci. Rep. 2020, 10, 837. [Google Scholar] [CrossRef]
33. Sun, W.; Shahrajabian, M.H.; Lin, M. Research Progress of Fermented Functional Foods and Protein Factory-Microbial Fermentation Technology. Fermentation 2022, 8, 688. [Google Scholar] [CrossRef]
34. Li, J.; Yuan, X.; Dong, Z.; Mugabe, W.; Shao, T. The Effects of Fibrolytic Enzymes, Cellulolytic Fungi and Bacteria on the Fermentation Characteristics, Structural Carbohydrates Degradation, and Enzymatic Conversion Yields of Pennisetum Sinese Silage. Bioresour. Technol. 2018, 264, 123–130. [Google Scholar] [CrossRef]
35. Silva, A.V.; Pereira, O.G.; Valadares Filho, S.d.C.; Garcia, R.; Cecon, P.R.; Ferreira, C.L.d.L.F. Consumo e Digestibilidades Dos Nutrientes Em Bovinos Recebendo Dietas Contendo Silagens de Milho e Sorgo, Com e Sem Inoculante Microbiano. Rev. Bras. Zootec. 2006, 35, 2469–2478. [Google Scholar] [CrossRef]
36. Michel, P.H.F.; Gonçalves, L.C.; Rodrigues, J.A.S.; Keller, K.M.; Raposo, V.S.; Lima, E.M.; Santos, F.P.C.; Jayme, D.G. Re-ensiling and Inoculant Application with Lactobacillus Plantarum and Propionibacterium Acidipropionici on Sorghum Silages. Grass Forage Sci. 2017, 72, 432–440. [Google Scholar] [CrossRef]
37. Dos Santos, A.P.M.; Santos, E.M.; de Araújo, G.G.L.; Oliveira, J.S.; Zanine, A.M.; Pinho, R.M.A.; Cruz, G.F.L.; Ferreira, D.J.; Perazzo, A.F.; Pereira, D.M.; et al. Effect of Inoculation with Preactivated Lactobacillus Buchneri and Urea on Fermentative Profile, Aerobic Stability and Nutritive Value in Corn Silage. Agriculture 2020, 10, 335. [Google Scholar] [CrossRef]
38. Coelho, M.M.; Gonçalves, L.C.; Rodrigues, J.A.S.; Keller, K.M.; Anjos, G.V.d.S.d.; Ottoni, D.; Michel, P.H.F.; Jayme, D.G. Chemical Characteristics, Aerobic Stability, and Microbiological Counts in Corn Silage Re-Ensiled with Bacterial Inoculant. Pesqui. Agropecu. Bras. 2018, 53, 1045–1052. [Google Scholar] [CrossRef]
39. Yin, H.; Zhao, M.; Pan, G.; Zhang, H.; Yang, R.; Sun, J.; Yu, Z.; Bai, C.; Xue, Y. Effects of Bacillus Subtilis or Lentilactobacillus Buchneri on Aerobic Stability, and the Microbial Community in Aerobic Exposure of Whole Plant Corn Silage. Front. Microbiol. 2023, 14, 1177031. [Google Scholar] [CrossRef] [PubMed]
40. Rabelo, C.H.S.; Basso, F.C.; Lara, E.C.; Jorge, L.G.O.; Härter, C.J.; Mari, L.J.; Reis, R.A. Effects of Lactobacillus Buchneri as a Silage Inoculant or Probiotic on in Vitro Organic Matter Digestibility, Gas Production and Volatile Fatty Acids of Low Dry-matter Whole-crop Maize Silage. Grass Forage Sci. 2017, 72, 534–544. [Google Scholar] [CrossRef]
41. Chen, L.; Yuan, X.J.; Li, J.F.; Dong, Z.H.; Wang, S.R.; Guo, G.; Shao, T. Effects of Applying Lactic Acid Bacteria and Propionic Acid on Fermentation Quality, Aerobic Stability and in Vitro Gas Production of Forage-Based Total Mixed Ration Silage in Tibet. Anim. Prod. Sci. 2019, 59, 376–383. [Google Scholar] [CrossRef]
42. Soundharrajan, I.; Muthusamy, K.; Han, O.-K.; Lee, H.J.; Purushothaman, S.; Kim, D.; Choi, K.C. Effects of Microbial Inoculants on the Fermentation and Preservation of Triticale Silages at High and Low Moisture Levels. Appl. Sci. 2020, 10, 7855. [Google Scholar] [CrossRef]
43. Ferrero, F.; Piano, S.; Tabacco, E.; Borreani, G. Effects of Conservation Period and Lactobacillus Hilgardii Inoculum on the Fermentation Profile and Aerobic Stability of Whole Corn and Sorghum Silages. J. Sci. Food Agric. 2019, 99, 2530–2540. [Google Scholar] [CrossRef]
44. Nkosi, B.D.; Vadlani, P.V.; Brijwani, K.; Nanjunda, A.; Meeske, R. Effects of Bacterial Inoculants and an Enzyme on the Fermentation Quality and Aerobic Stability of Ensiled Whole-Crop Sweet Sorghum. S. Afr. J. Anim. Sci. 2012, 42, 232–240. [Google Scholar] [CrossRef]
45. Xu, Z.; He, H.; Zhang, S.; Kong, J. Effects of Inoculants Lactobacillus Brevis and Lactobacillus Parafarraginis on the Fermentation Characteristics and Microbial Communities of Corn Stover Silage. Sci. Rep. 2017, 7, 13614. [Google Scholar] [CrossRef]
46. Du, Z.; Sun, L.; Chen, C.; Lin, J.; Yang, F.; Cai, Y. Exploring Microbial Community Structure and Metabolic Gene Clusters during Silage Fermentation of Paper Mulberry, a High-Protein Woody Plant. Anim. Feed Sci. Technol. 2021, 275, 114766. [Google Scholar] [CrossRef]
47. Muraro, G.B.; de Almeida Carvalho-Estrada, P.; de Oliveira Pasetti, M.H.; Santos, M.C.; Nussio, L.G. Bacterial Dynamics of Sugarcane Silage in the Tropics. Environ. Microbiol. 2021, 23, 5979–5991. [Google Scholar] [CrossRef]
Leite GM, Santos EM, de Oliveira JS, Pereira DM, de Oliveira CJB, Cavalcanti JVFL, de Lima VMR, de Lima JPVdMF, Gomes PGB, Edvan RL, et al. Isolation of Acetic Acid-Producing Bacterial Strains and Utilization as Microbial Inoculants in Sorghum Silages. Agriculture. 2025; 15(3):241. https://doi.org/10.3390/agriculture15030241
Перевод статьи «Isolation of Acetic Acid-Producing Bacterial Strains and Utilization as Microbial Inoculants in Sorghum Silages» авторов Leite GM, Santos EM, de Oliveira JS, Pereira DM, de Oliveira CJB, Cavalcanti JVFL, de Lima VMR, de Lima JPVdMF, Gomes PGB, Edvan RL, et al., оригинал доступен по ссылке. Лицензия: CC BY. Изменения: переведено на русский язык
Фото: shutterstock
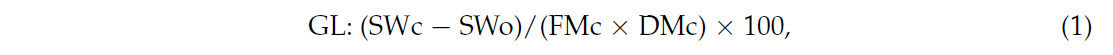
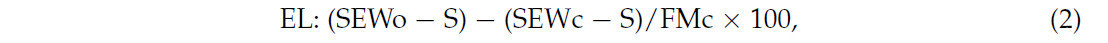
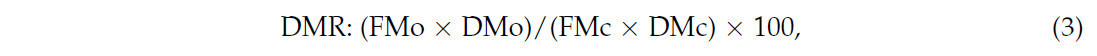
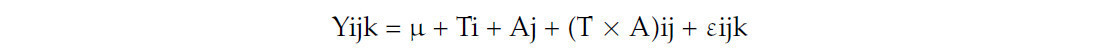















































































































Комментарии (0)