Когда азот вредит, а вода спасает: сезонные хитрости степной почвы
Изучение влияния добавления азота и воды на динамику N₂O имеет критическое значение, поскольку N₂O является ключевым фактором изменения климата (включая азотное осаждение и изменения режима осадков) и разрушения стратосферного озона. Умеренная степь служит заметным природным источником этого мощного парникового газа. В данном исследовании используются полевые наблюдения и отбор почвенных образцов для анализа сезонной динамики эмиссии N₂O в умеренной степи Внутренней Монголии и механизма, с помощью которого добавление азота и воды, как двух различных типов факторов, изменяет эту сезонную динамику. В работе рассматривается регуляторная роль экологических факторов, физико-химических свойств почвы, структуры микробного сообщества и численности функциональных генов, влияющих на эмиссию N₂O.
Аннотация
Полученные результаты показывают, что эффекты добавления азота и воды на механизмы эмиссии N₂O различаются на протяжении вегетационного сезона. Внесение азота стабильно увеличивает выбросы N₂O. Напротив, добавление воды подавляет эмиссию N₂O в начале вегетационного периода, но стимулирует выбросы в период пика и в конце сезона.
В начале вегетационного сезона добавление азота в первую очередь повышало уровень растворённого органического азота (DON), что обеспечивало матрицу для нитрификации и способствовало эмиссии N₂O. В то же время добавление воды увеличивало влажность почвы, повышая численность гена nosZ (редуктазы закиси азота), одновременно снижая содержание нитратного азота (NO₃⁻-N), а также экспрессию генов AOA (архей-аммонийокислителей) amoA и AOB (аммонийокисляющих бактерий) amoA, тем самым уменьшая выбросы N₂O.
В период пика вегетации роль азота в регулировании pH и аммонийного азота (NH₄⁺-N), а также усиление экспрессии AOB amoA, приводили к резкому росту эмиссии N₂O. Добавление воды влияет на баланс между нитрификацией и денитрификацией, изменяя аэробные и анаэробные условия в почве, что в конечном итоге увеличивает выбросы N₂O за счёт подавления nosZ. По мере затухания вегетационного сезона и снижения количества осадков температура также становилась драйвером эмиссии N₂O.
Моделирование структурными уравнениями показывает, что влияние азота и воды на изменения потоков N₂O через нитрификацию и денитрификацию более значительно в период пика вегетации. Данное исследование раскрывает новые аспекты того, как добавление азота и воды по-разному влияет на динамику N₂O на различных этапах вегетационного сезона в умеренной степи, обеспечивая научную основу для прогнозирования и регулирования выбросов N₂O в этих экосистемах.
1. Введение
Закись азота (N₂O) является мощным и долгоживущим парниковым газом, который играет критическую роль в изменении климата и разрушении стратосферного озона [1,2,3,4]. В 2020 году средний глобальный коэффициент эмиссии N₂O достиг 4,3% [5]. Луга, которые покрывают приблизительно 49% поверхности суши Земли [6], особенно чувствительны к глобальному изменению климата (азотному осаждению и изменению режима осадков) из-за их расположения в основном в экологически хрупких зонах. В Китае луга ежегодно выделяют в среднем 76,5 ± 12,8 Gg N в виде N₂O, причём 57% приходится на почвы умеренных степей [7]. В связи с глобальным потеплением, усилением антропогенного азотного осаждения и изменением режима выпадения осадков [8,9] точное прогнозирование и моделирование эмиссии N₂O становится всё более важным [10,11,12].
Потоки N₂O обычно регулируются климатическими факторами, почвенной матрицей и микроорганизмами [13,14,15]. Добавление азота напрямую увеличивает субстраты для нитрификации и денитрификации, тем самым способствуя эмиссии N₂O [16]. Содержание NH₄⁺-N в почве является критическим фактором, влияющим на эмиссию N₂O [11,17]. Состав органического вещества почвы также значительно влияет на гетеротрофную микробную активность. Высокий уровень органического углерода способствует микробному дыханию, изменяя баланс между нитрификацией и денитрификацией, что влияет на продукцию N₂O [18]. Добавление азота может приводить к подкислению почвы через такие процессы, как нитрификация NH₄⁺ и выщелачивание NO₃⁻, которые снижают активность редуктазы N₂O в процессе денитрификации и увеличивают выбросы [19,20]. Более низкий pH почвы, который влияет на микробную биомассу и структуру сообщества, может значительно снижать скорость нитрификации и денитрификации [21,22]. Осадки являются ещё одним ключевым фактором, поскольку они влияют на влажность почвы, которая регулирует геохимические циклы и эмиссию N₂O [23,24]. В хорошо аэрируемых сухих почвах N₂O в основном образуется в процессе нитрификации [25]. Однако когда содержание воды в почве достигает насыщения, возникающие анаэробные условия благоприятствуют денитрификации, что дополнительно способствует эмиссии N₂O [26]. Эта вариабельность того, как влажность почвы влияет на нитрификацию и денитрификацию, вносит вклад в неопределённость влияния осадков на поток N₂O [27,28]. Хотя многие исследования сообщают, что добавление азота и воды может напрямую или косвенно влиять на потоки N₂O, изменяя регулирующие факторы [12,29], результаты противоречивы. Связь между добавлением азота и потоком N₂O может быть линейной, экспоненциальной или нелинейной в зависимости от местных экологических условий и других ограничений, связанных с питательными веществами [11,12,30,31]. Более того, добавление азота и подкисление почвы по-разному влияют на численность и активность функциональных генов аммонийокисляющих микроорганизмов [32]. В кислых почвах доминируют аммонийокисляющие археи (AOA), тогда как в нейтральных почвах доминируют аммонийокисляющие бактерии (AOB) [33,34]. И наоборот, некоторые исследования показывают, что AOB более устойчивы к подкислению почвы [35], что свидетельствует о том, что высокая численность AOA не обязательно доминирует в нитрификационной активности. Некоторые исследования также показывают, что численность генов денитрификации не всегда зависит от добавления азота [36]. Добавление воды смещает источник N₂O между процессами нитрификации и денитрификации, стимулируя или подавляя эмиссию N₂O в умеренной степи [37,38]. Тем не менее, исследований по совместному влиянию азотного осаждения и осадков на потоки N₂O остаётся недостаточно, несмотря на то, что взаимодействия между азотом и водой варьируют в зависимости от количества осадков. В засушливые годы их влияние на поток N₂O может быть аддитивным, тогда как в нормальные годы они могут проявлять синергетические эффекты [39]. Некоторые исследования также показали, что выпадение осадков может снижать усиливающий эффект азотных добавок на поток N₂O [40]. Наконец, сезонное распределение осадков играет решающую роль в эмиссии N₂O; однако исследования того, как добавление воды влияет на N₂O на разных этапах вегетационного сезона, всё ещё ограничены. Таким образом, необходимы дополнительные исследования для изучения сезонных взаимодействий между поступлением азота и воды и их влиянием на эмиссию N₂O, в частности через их воздействие на почвенные условия и микробные процессы.
Учитывая отсутствие консенсуса относительно реакции потоков N₂O в умеренной степи на азотное осаждение и осадки, а также то, что лишь несколько исследований количественно оценили сезонные закономерности эмиссии N₂О in situ в условиях изменений азотного осаждения и осадков и факторов, контролирующих её на разных этапах вегетационного сезона, данное исследование провело полевые эксперименты по добавлению азота и воды в типичной умеренной степи Внутренней Монголии, Китай. В нём измерялись годовые колебания эмиссии N₂O и рассматривалось влияние долгосрочных обработок азотом и водой в течение нескольких дат отбора проб на протяжении вегетационного сезона на закономерности сезонной изменчивости N₂O. Другая цель — оценить важность экологических факторов, физико-химических свойств почвы, структуры и функции микробного сообщества почвы как контролирующих факторов в регуляции эмиссии N₂О in situ в полевых условиях путём моделирования атмосферного азотного осаждения и режимов осадков. Мы предполагаем, что добавление азота и воды по-разному связано с эмиссией N₂O в разное время в экосистемах полузасушливых лугов, в то время как другие факторы, такие как микробная активность и доступность матрицы в почве, могут изменять эффекты добавления азота и воды на протяжении сезонных изменений. Наше исследование предоставляет научную основу для прогнозирования тенденций изменений почвенной матрицы и микробного сообщества в лугах на фоне будущих глобальных изменений, а также для точной оценки почвенных потоков N₂O.
2. Материалы и методы
2.1. Район исследования и экспериментальный дизайн
Исследовательская станция расположена в уезде Дуолунь, аймак Шилин-Гол, Автономный район Внутренняя Монголия, с географическими координатами от 115°50′ в.д. до 116°55′ в.д. и от 41°46′ с.ш. до 42°39′ с.ш. Район исследования был организован на базе Тринадцатимильного пляжа, Дуолуньской экспериментально-демонстрационной исследовательской станции восстановительной экологии Института ботаники Китайской академии наук. Этот район имеет типичный континентальный климат с переходом от умеренно полузасушливого к полувлажному, со среднегодовым количеством осадков 385,5 мм за период с 1953 по 2004 год [41], сосредоточенных в основном с июня по сентябрь. Тип почвы — в основном каштаново-кальциевая почва с низким плодородием и рыхлой структурой, а текстура почвы представлена в основном супесью. Естественные растения в уезде Дуолунь включают ковыль Крылова (Stipa krylovii), житняк гребенчатый (Agropyron cristatum), колосняк китайский (Leymus chinensis) и полевую полынь (Artemisia frigida) [42].
Месячные изменения температуры воздуха, осадков, влажности почвы и температуры почвы в районе исследования за 2018–2020 годы показаны на Рисунке 1. Данные об осадках и температуре воздуха регистрировались с помощью флюкс-вышки на Дуолуньской исследовательской станции восстановительной экологии. Общее количество осадков в 2020 году составило 270,9 мм, при этом в течение шести месяцев подряд до мая выпадало менее 10 мм осадков в месяц. Большая часть осадков выпала в период с мая по август, что составило 83,54% от годового итога, с максимальным количеством в июле и августе. Среднемесячная температура воздуха в 2020 году варьировалась от −14,88 °C до 17,98 °C, следуя одновершинной закономерности, с наименьшим значением в январе и наибольшим в июле. Среднемесячная температура почвы колебалась от −8,21 °C до 19,37 °C, в то время как влажность почвы варьировалась от 5,56% до 15,91%. Из-за выраженной сезонной цикличности эмиссии N₂O из лугов [43] с наибольшими выбросами в июле [44] и пиком осадков и азотного осаждения летом, временные рамки данного исследования охватывали период с мая по сентябрь.
Рисунок 1. Месячная изменчивость осадков, температуры воздуха, а также температуры и влажности почвы на глубине 0–10 см в районе исследования с 2018 по 2020 год.
Экспериментальный участок состоял из 16 небольших делянок, каждая размером 4 м × 4 м, с 1-метровой буферной зоной между соседними делянками. Эксперимент был разделен на четыре группы обработок: CK (0 мм yr⁻¹), N4 (4 г N m⁻² yr⁻¹), W1 (56,25 мм yr⁻¹, что эквивалентно 15% от нормы осадков) и комбинированное добавление азота и воды (W1N4), по четыре повторности каждая. ПВХ-кольца (диаметром 19,00 см, высотой 10,00 см) были случайным образом заглублены на 5 см в каждой делянке для измерений потока N₂O. Эксперимент по добавлению азота и воды начался в 2017 году, с использованием NH₄NO₃ в качестве источника азота. Твердый NH₄NO₃ растворяли в 10 л воды (что эквивалентно 0,625 мм осадков, менее 1% от среднемноголетнего месячного количества осадков с июня по август) и вносили на делянки в три отдельных приема в начале июня, июля и августа, избегая периодов дождей. Конкретные нормы внесения показаны в Таблице S1.
2.2. Отбор почвенных образцов и физико-химический анализ
Почвенные образцы отбирались ежемесячно с мая по сентябрь 2020 года. В каждой из четырех повторностей экспериментальных обработок с помощью почвенного бура диаметром 3 см отбирались керны почвы с глубины 0–10 см. Каждая маленькая делянка отбиралась методом пяти точек, после чего образцы тщательно перемешивались и просеивались через сито с ячейкой 2 мм. Почвенные образцы с каждой делянки были разделены на две части: одна хранилась при −80 °C для молекулярно-биологического анализа и определения активности ферментов, а другая хранилась при −20 °C для измерения физико-химических свойств почвы и микробной биомассы. pH почвы измеряли с помощью pH-метра (PB-10), а содержание воды в почве определяли гравиметрическим методом. 10 г почвенного образца экстрагировали 40 мл 0,5 M раствора K₂SO₄, и фильтрат использовали для определения концентраций аммонийного азота (NH₄⁺-N) и нитратного азота (NO₃⁻-N) с помощью проточного анализатора AA3 (CFA, Bran Luebbe, Гамбург, Германия). Затем содержание растворенного органического углерода (DOC) измеряли с помощью анализатора общего органического углерода (TOC-L CPN, Shimadzu, Киото, Япония).
В полевых условиях поток N₂O измеряли с помощью портативного анализатора N₂O (Model 909-0025, LGR, USA), основанного на технологии внеосевой интегральной полостной выходной спектроскопии (Off-Axis ICOS), при этом поток выражали в nmol N₂O m⁻² s⁻¹. Это устройство использовалось совместно с автоматической многоканальной системой длительных измерений почвенных потоков SF-3000, что обеспечивало наблюдение за каждой делянкой в течение примерно 1 часа 19 минут для получения одного значения потока. Используя систему мультиплексора, данные о потоке N₂O для 16 делянок измерялись последовательно через автоматическое открытие и закрытие камер, причем каждое измерение в камере длилось приблизительно 200 с. Ежедневное значение потока N₂O для каждой делянки рассчитывалось как среднее из этих измерений. В этом исследовании контролировался весь период 2020 года, и аномальные данные из-за неисправности прибора были исключены. Был длительный период пропущенных данных с 10 по 28 июня, что было связано с тем, что солнечные батареи испытывали недостаток энергии, из-за чего насосы мультиплексора не работали. Поэтому прибор был отправлен в сервис для обеспечения точности последующих данных и регулярного обслуживания. После ручного полива в период наблюдения измерения проводились повторно с интервалом в один день. Температура и объемная влажность почвы на глубине 0–10 см измерялись с помощью датчиков температуры и влажности, подключенных к камере SR-21.
2.3. Экстракция ДНК и микробиологический анализ
Микробный биомассовый углерод (MBC) и азот (MBN) анализировали методом хлороформного фумигирования с последующей экстракцией 0,5 M K₂SO₄, с использованием анализатора общего органического углерода для измерений (TOC-L CPN, Shimadzu, Киото, Япония). Активность почвенных ферментов измеряли с помощью многомодового планшетного ридера Synergy H1. Выбранные для исследования ферменты включали N-ацетил-β-D-глюкозаминидазу (NAG), β-глюкозидазу (BG), кислую фосфатазу (AP), полифенолоксидазу (POX) и пероксидазу (PER) для анализа взаимосвязи между круговоротом углерода и азота в почве и активностью ферментов. 96-луночный планшет для гидролаз был черным непрозрачным планшетом (флуоресцентный метод), а 96-луночный планшет для оксидаз был прозрачным планшетом (метод поглощения света), и оба были колориметрически сравнены при спектре возбуждения 360 нм и спектре поглощения 450 нм в планшетном ридере для получения количественных результатов анализа, а активность ферментов выражалась в единицах µmol g⁻¹ h⁻¹. Структура микробного сообщества определялась методом биомаркеров фосфолипидных жирных кислот (PLFA), а состав фосфолипидных жирных кислот анализировался с помощью газовой хроматографии с тройной квадрупольной масс-спектрометрией (GC) для анализа структуры микробного сообщества.
Количественная ПЦР (полимеразная цепная реакция) использовалась для определения численности выбранных в этом исследовании функциональных генов нитрификации AOA amoA, AOB amoA и генов денитрификации nirK, nirS и nosZ. Общую почвенную ДНК экстрагировали с помощью набора FastDNA TM SPIN Kit (MP Biomedicals, Санта-Ана, Калифорния, США); концентрацию и чистоту проверяли в микро-УФ-спектрофотометре (Nanodrop Technologies, Уилмингтон, Делавэр, США), а индекс микробного биомассового углерода почвы определяли по концентрации ДНК. Численность микробных функциональных генов определяли с помощью системы детекции ПЦР в реальном времени. Серийные 10-кратные разведения плазмид для каждого целевого гена были обнаружены с помощью qПЦР (Система детекции количественной ПЦР в реальном времени) для получения стандартной кривой со значением R² > 0,997 [45]. Отрицательные контроли, образцы и стандартные серии выполнялись в трех повторностях на 48-луночном планшете. 20 мкл ПЦР-реакционной смеси содержали 10 мкл премикса от TaKaRa, 0,2 мкл каждого праймера (20 мМ) и 1 мкл матрицы ДНК. Бычий сывороточный альбумин также был включен для обеспечения устойчивости к ингибиторам почвы. Праймеры для амплификации и условия реакции для пяти выбранных генов нитрификации и денитрификации показаны в Таблице S2 [46].
2.4. Статистический анализ
Данные о потоке N₂O, а также физико-химических и микробных свойствах почвы были проверены на нормальность и показали нормальное распределение. Однофакторный и двухфакторный дисперсионный анализ (ANOVA) были выполнены с использованием SPSS версии 26 для изучения влияния добавления азота и воды, а также их взаимодействий на различные параметры. Последующие множественные сравнения проводились с использованием критерия LSD (при равных дисперсиях) и Даннетта-T3 (при неравных дисперсиях) для оценки значимости различий. Корреляционный анализ Пирсона и пошаговая регрессия использовались для изучения взаимосвязей между численностью микроорганизмов, физико-химическими свойствами почвы и потоками N₂O, а также для выявления факторов, определяющих изменения потоков N₂O. Метод главных компонент (PCA) был применен для анализа характеристик почвы при обработках азотом и водой. Наконец, модель структурных уравнений (SEM) Amos 24 была применена для исследования механизма влияния обработки добавлением азота и воды на поток N₂O. Графики были созданы с использованием программного обеспечения Origin 2021.
3. Результаты
3.1. Влияние факторов окружающей среды на поток N₂O
Как показано на Рисунке 2, поток N₂O в 2020 году колебался от −0,208 до 0,192 nmol m⁻² s⁻¹ в течение года. В невегетационный период потоки показывали минимальную изменчивость, варьируясь от −0,081 до 0,143 nmol m⁻² s⁻¹ и составляя 20,31% от годового итога. Потоки N₂O в контрольных делянках оставались практически стабильными с марта по июль после начала весны, колебались и снижались за тот же период в делянках с добавлением воды и продолжали увеличиваться после начала весны до сентября в делянках с добавлением азота и совместным добавлением азота и воды (Рисунок 2). Примечательно, что потоки N₂O в целом увеличивались в месяц, следующий за обработкой добавлением азота (Рисунок 2).
Рисунок 2. Изменения почвенных потоков N₂O при добавлении азота и воды в разные месяцы 2020 года. Обработки: контроль (CK), добавление азота (N4), добавление воды (W1) и комбинированное добавление азота и воды (W1N4).
Распределение осадков в течение вегетационного сезона увеличивалось от начала к середине сезона. Высокие выбросы N₂O происходили при высоких температурах почвы (ST), при этом N₂O в это время в основном регулировался влажностью почвы (SM) (Рисунок 3). В начале вегетационного сезона выбросы N₂O немного увеличивались с повышением ST и снижались со снижением ST и SM в конце вегетационного сезона (Рисунок 3). В невегетационный период потоки N₂O в основном зависели от изменений температуры (Рисунок 3). Когда влажность почвы была низкой в начале вегетационного сезона, поток N₂O из почвы достигал минимума между 8 и 13 часами и максимума между 17 и 20 часами (Рисунок 4), показывая значительную отрицательную корреляцию между температурой почвы и потоками N₂O. В период пика вегетационного сезона, когда влажность почвы была наибольшей, суточная динамика N₂O не зависела от температуры почвы, и потоки N₂O были положительными (Рисунок 4).
Рисунок 3. Месячная изменчивость потоков N₂O под влиянием температуры и влажности почвы в 2020 году. Различные обведенные цифры на диаграмме представляют разные месяцы. ①: Январь; ②: Февраль; ③: Март; ④: Апрель; ⑤: Май; ⑥: Июнь; ⑦: Июль; ⑧: Август; ⑨: Сентябрь; ⑩: Октябрь; ⑪: Ноябрь; ⑫: Декабрь. Красный цвет означает высокий поток N₂O, а синий — низкий поток N₂O.
Рисунок 4. (a) Суточная динамика почвенных потоков N₂O, температуры и влажности почвы в мае 2020 года. (b) Суточная динамика почвенных потоков N₂O, температуры и влажности почвы в августе 2020 года. Обработки: контроль (CK), добавление азота (N4), добавление воды (W1) и комбинированное добавление азота и воды (W1N4).
Значения Q10 показали значительные сезонные различия между обработками (Таблица S3). В начале вегетационного сезона значения Q10 были относительно высокими для всех обработок, что указывает на повышенную температурную чувствительность в этот период. Например, CK имел Q10, равный 2,251, в то время как добавление азота показало немного более высокое значение 2,291. Добавление воды также привело к высокому Q10, равному 2,358. Напротив, в период пика вегетационного сезона значения Q10 были заметно ниже во всех обработках, причем значения N4 и W1 снизились до 0,419 и 0,687 соответственно. В конце вегетационного сезона комбинированная обработка добавлением азота и воды (W1N4) показала наибольшее значение Q10, равное 4,135. В невегетационный сезон значения Q10 были в целом умеренными, от 0,793 (W1) до 1,604 (N4), что предполагает стабильное, но сниженное влияние температуры на поток N₂O.
3.2. Влияние добавления азота и воды на поток N₂O
В течение вегетационного сезона 2020 года на эмиссию N₂O влияли добавление азота и воды (p < 0,01, Таблица S4), но не было взаимодействий между этими двумя факторами. Однако совокупная эмиссия N₂O значительно зависела от добавления азота, добавления воды и их взаимодействий (p < 0,01, Таблица S4). В частности, добавление воды в июне значительно снижало поток N₂O (p < 0,05, Рисунок 5), в то время как обработки добавлением азота и комбинированным добавлением азота и воды в августе показали значительно более высокие потоки по сравнению с контролем и обработкой водой (p < 0,05, Рисунок 5). В мае на делянках с добавлением воды был значительно более низкий поток N₂O из почвы по сравнению с контролем и добавлением азота (p < 0,05, Рисунок 5). В остальные месяцы значительных различий в потоках N₂O между обработками не наблюдалось. На протяжении всего вегетационного сезона контроль, добавление азота и комбинированная обработка азотом и водой находились в состоянии эмиссии, в то время как добавление воды было практически в равновесии. По сравнению с контролем, добавление азота увеличило выбросы N₂O на 109,38% (p < 0,01, Таблица S4), тогда как добавление воды снизило их примерно в 1,5 раза (p < 0,01, Таблица S4). Результаты показали, что добавление воды снижало выбросы N₂O в начале вегетационного сезона, увеличивало их в период пика и в конце сезона, а обработки азотом увеличивали выбросы N₂O на протяжении всего вегетационного сезона.
Рисунок 5. Месячная изменчивость эмиссии N₂O из почвы при добавлении азота и воды. Обработки: контроль (CK), добавление азота (N4), добавление воды (W1) и комбинированное добавление азота и воды (W1N4). Разные строчные буквы указывают на значительные различия между обработками в один и тот же месяц, а разные прописные буквы указывают на значительные различия между месяцами при одной и той же обработке (p < 0,05).
3.3. Влияние добавления азота и воды на физико-химические свойства почвы
Метод главных компонент (PCA) показал, что первые две компоненты объясняли 63,2% изменчивости физико-химических свойств почвы в умеренной степи (Рисунок S1). Добавление азота значительно влияло на pH почвы, растворенный органический азот (DON) и содержание неорганического азота, в то время как добавление воды значительно влияло на SM, pH, растворенный органический углерод (DOC) и содержание неорганического азота (Таблица 1). По сравнению с контролем, добавление азота значительно снижало pH почвы (p < 0,01, Таблица 1), но влияние добавления воды на pH почвы было значительно усилено (p < 0,01, Таблица 1). Значительных различий в содержании воды в почве (SWC) между обработками не было (Таблица 1). Добавление воды значительно увеличило DOC на 24,53% (p < 0,01, Таблица 1), а комбинированное добавление азота и воды также увеличило DOC. Добавление азота значительно увеличило DON на 20,57% (p < 0,05, Таблица 1). Добавление азота также привело к увеличению аммонийного азота (NH₄⁺-N) и нитратного азота (NO₃⁻-N), причем содержание NH₄⁺-N было выше при добавлении азота, чем при добавлении воды, в то время как добавление воды значительно снижало содержание NO₃⁻-N (p < 0,01, Таблица 1). Не было обнаружено взаимодействующих эффектов комбинированного добавления азота и воды на физико-химические свойства почвы. Добавление воды значительно увеличило влажность почвы на 29,92% (p < 0,05, Таблица 1), но значительных различий во влажности почвы между различными обработками не было. Добавление азота и воды не оказало значительного влияния на температуру почвы.
Таблица 1. Влияние добавления азота и воды на физико-химические свойства почвы и микробную биомассу.
3.4. Влияние добавления азота и воды на почвенные микробные факторы
Микробный биомассовый углерод почвы (MBC) не показал значительных изменений между обработками. Добавление азота значительно снизило микробный биомассовый азот почвы (MBN) (p < 0,05, Таблица 1), в то время как добавление воды показало незначительную тенденцию к увеличению MBN (Таблица 1). Что касается активности гидролитических ферментов почвы в разные месяцы, активность β-глюкозидазы (BG) в мае была выше, чем в другие месяцы (p < 0,05, Рисунок 6c), в то время как в августе активность BG при обработке водой была значительно выше, чем в контроле и при комбинированной обработке азотом и водой (p < 0,05, Рисунок 6c). Не было обнаружено значительного влияния добавления азота и воды на активность N-ацетил-β-D-глюкозаминидазы (NAG) и кислой фосфатазы (AP) (Таблица S5). Что касается активности оксидаз почвы, добавление воды оказало значительное влияние на активность пероксидазы (POX) (p < 0,01, Таблица S5). В июне и июле добавление воды и комбинированное добавление азота и воды не увеличивали значимо активность POX; однако в сентябре активность POX в этих двух обработках была значительно выше, чем в группе только с азотом и в контрольной группе (p < 0,05, Рисунок 6a). Кроме того, добавление азота в июле значительно увеличило активность пероксидазы (PER) на 23,83% (p < 0,05, Рисунок 6b), а в сентябре все обработки оказывали стимулирующее влияние на активность PER. Результаты показывают, что добавление азота ингибирует активность оксидазы POX в почве, в то время как добавление воды смягчает ингибирование микробной активности, вызванное подкислением почвы при добавлении азота (p < 0,01, Таблица S5).
Рисунок 6. Изменения активности гидролитических и оксидазных ферментов почвы при добавлении азота и воды. (a) Изменения POX почвы в условиях добавления азота и воды; (b) Изменения PER почвы в условиях добавления азота и воды; (c) Изменения BG почвы в условиях добавления азота и воды; (d) Изменения AP почвы в условиях добавления азота и воды; (e) Изменения NAG почвы в условиях добавления азота и воды. Обработки: контроль (CK), добавление азота (N4), добавление воды (W1) и комбинированное добавление азота и воды (W1N4). Разные строчные буквы указывают на значительные различия между обработками в один и тот же месяц, а разные прописные буквы указывают на значительные различия между месяцами при одной и той же обработке (p < 0,05).
Микробное сообщество почвы варьировалось, как показано на Рисунке 7, и его содержание увеличивалось с увеличением месяца. Общее содержание фосфолипидных жирных кислот (PLFA) значительно увеличилось на 33,10% в июне при комбинированной обработке и значительно снизилось на 25,05% в июле при обработке водой (p < 0,05, Рисунок 7a). Содержание грибных PLFA в контрольной группе в сентябре было значительно выше по сравнению с маем, показав увеличение на 115,62% (p < 0,05, Рисунок 7b). Добавление воды значительно снизило содержание грибных PLFA в июле, но показало тенденцию к увеличению в другие месяцы (p < 0,05, Рисунок 7b). Содержание актинобактерий (Ac) в контрольной группе в сентябре было значительно выше по сравнению с маем на 110,88% (p < 0,05, Рисунок 7e), в то время как содержание арбускулярных микоризных грибов (AMF) при обработке азотом было значительно ниже в сентябре по сравнению с контрольной группой на 42,19% (p < 0,05, Рисунок 7f). Напротив, добавление воды увеличивало содержание AMF в мае, июне и августе, но снижало его на 21,05% и 5,84% в июле и сентябре соответственно (Рисунок 7f). Для грамположительных бактерий (G+) и грамотрицательных бактерий (G−) контрольная группа в сентябре была значительно выше на 89,42% и 76,66% соответственно по сравнению с маем (p < 0,05, Рисунок 7c,d).
Рисунок 7. Изменения содержания фосфолипидных жирных кислот (PLFA) в почве при добавлении азота и воды. (a) Изменения общего содержания PLFA в почве в условиях добавления азота и воды; (b) Изменения содержания грибных PLFA в почве в условиях добавления азота и воды; (c) Изменения содержания G+ PLFA в почве в условиях добавления азота и воды; (d) Изменения содержания G− PLFA в почве в условиях добавления азота и воды; (e) Изменения содержания PLFA актинобактерий в почве в условиях добавления азота и воды; (f) Изменения содержания PLFA арбускулярных микоризных грибов в почве в условиях добавления азота и воды. Обработки: контроль (CK), добавление азота (N4), добавление воды (W1) и комбинированное добавление азота и воды (W1N4). Разные строчные буквы указывают на значительные различия между обработками в один и тот же месяц, а разные прописные буквы указывают на значительные различия между месяцами при одной и той же обработке (p < 0,05).
Что касается функциональных генов нитрификации в почве, добавление воды оказало значительное влияние на численность генов AOA amoA и AOB amoA (p < 0,01, Таблица S6), тогда как добавление азота в основном влияло на численность генов AOB amoA (p < 0,01, Таблица S6). Взаимодействующих эффектов между добавлением азота и воды на численность этих генов не наблюдалось (Таблица S6). В умеренной степи добавление азота привело к значительно более высокой численности генов AOA amoA по сравнению с добавлением воды. И наоборот, численность генов AOB amoA была заметно ниже при обработке водой и комбинированной обработке, чем в контрольной группе и при добавлении азота (p < 0,05, Таблица S6). Однако на численность генов денитрификации эти обработки не оказали значительного влияния (Таблица S6).
3.5. Взаимосвязи между N₂O и влияющими факторами
Многофакторный пошаговый регрессионный анализ показал ключевые факторы, влияющие на эмиссию N₂O на разных этапах вегетационного сезона (Таблица 2). В начале вегетационного сезона (май и июнь) SM и DON имели наибольшую объясняющую способность для вариаций потока N₂O, объясняя 34,6% дисперсии (p < 0,01, Таблица 2). Это указывает на то, что DON является важным предиктором, даже когда нет значительных различий в содержании влаги в почве. В период пика вегетационного сезона (июль и август) pH и NH₄⁺-N объясняли 46,6% вариаций потока N₂O (p < 0,001; Таблица 2), в течение которого N₂O в основном зависел от субстратов. В конце вегетационного сезона (сентябрь) pH, ST и NH₄⁺-N вместе объясняли 51,9% вариаций N₂O (p < 0,001, Таблица 2), причем добавление NH₄⁺-N дополнительно указывает на то, что сезонная изменчивость эмиссии N₂O в первую очередь обусловлена субстратами, а не непосредственно температурой. Корреляционный анализ показал, что DON и NH₄⁺-N были значительно положительно связаны с ST и SM (p < 0,01, Рисунок 8) и значительно отрицательно связаны с pH (p < 0,01, Рисунок 8). В начале вегетационного сезона SM была значительно положительно связана с DON и nirK (p < 0,01, Рисунок 8) и значительно отрицательно связана с AOA amoA (p < 0,01, Рисунок 8), в то время как pH не показал значимой корреляции с численностью функциональных генов нитрификации-денитрификации. В период пика вегетационного сезона pH показал значительную отрицательную корреляцию с AOB amoA (p < 0,01, Рисунок 8) и значительную положительную корреляцию с микробным биомассовым углеродом и азотом почвы (p < 0,05, Рисунок 8). DON, NH₄⁺-N и ST были положительно связаны с nirK и nosZ (p < 0,01, Рисунок 8), в то время как NH₄⁺-N показал отрицательную корреляцию с nirS (p < 0,05, Рисунок 8). Кроме того, SM была отрицательно связана с численностью гена AOB amoA (p < 0,05, Рисунок 8), но не показала значимой корреляции с численностью генов AOA amoA.
Рисунок 8. График корреляции между численностью функциональных генов и физико-химическими свойствами почвы. Значимо при уровне вероятности 0,05. Значимо при уровне вероятности 0,01.
Таблица 2. Основные модели объясняющих факторов для месячного потока N₂O в течение вегетационного сезона.
Модель структурных уравнений (SEM) показала ключевые пути, влияющие на эмиссию N₂O. В более сухой ранний вегетационный сезон добавление азота увеличивало поток N₂O за счет повышения содержания неорганического азота (IN) и DON. И наоборот, добавление воды снижало выбросы N₂O, отрицательно влияя на NO₃⁻-N и экспрессию гена AOB, в то же время положительно влияя на экспрессию nosZ (Рисунок 9a). Кроме того, добавление азота снижало pH почвы, что ингибировало гены нитрификации. Эти пути объясняли примерно 51% вариаций потока N₂O в этот период (Рисунок 9a). Во влажный пик вегетационного сезона добавление воды ингибировало нитрификацию за счет снижения численности гена AOB amoA. Однако вода также стимулировала выбросы N₂O за счет повышения SM и подавления экспрессии гена nosZ (Рисунок 9b). Добавление азота и воды оказало значительное влияние на pH, причем добавление воды смягчало подкисление почвы, вызванное добавлением азота. Более низкий pH оказывал значительное отрицательное влияние на численность гена AOB amoA, в то время как экспрессия гена AOB amoA сильно способствовала выбросам N₂O (Рисунок 9b). Было обнаружено, что гены nirK и nirS оказывают значительное отрицательное влияние на поток N₂O (Рисунок 9b). Результаты SEM показывают, что прямые и косвенные пути могут объяснить около 45% вариаций потока N₂O (Рисунок 9b).
Рисунок 9. Модели структурных уравнений потока N₂O и его влияющих факторов в (a) начале вегетационного сезона с меньшим количеством осадков и (b) в период пика вегетационного сезона с высокой температурой и влажностью. Синие линии обозначают значимые положительные корреляции, красные линии — значимые отрицательные корреляции, а пунктирные линии — незначимые корреляции. Значимо при уровне вероятности 0,05. Значимо при уровне вероятности 0,01. Значимо при уровне вероятности 0,001.
4. Обсуждение
4.1. Сезонная динамика эмиссии N₂O в умеренной степи
Изменения N₂O в умеренной степи в этом исследовании показали четкую сезонную закономерность, с пиками месячного динамического поглощения весной и пиками эмиссии летом. Выбросы N₂O были относительно стабильными в невегетационный период, но колебания выбросов увеличивались с повышением температуры после начала весны (март), и вегетационный сезон (с мая по сентябрь) составлял большую часть годовых выбросов N₂O, что согласуется с результатами предыдущих исследований [47]. В невегетационный период почвы в районе исследования зимой замерзают, что приводит к слабой микробной активности и медленным изменениям выбросов N₂O [48]. По мере повышения температуры во время весеннего оттаивания почвенные микроорганизмы становятся активными, что приводит к значительным выбросам N₂O за короткий период [49].
Распределение осадков в течение вегетационного сезона влияет на выбросы N₂O. Распределение осадков за вегетационный сезон 2020 года постепенно увеличивалось от начала к середине сезона (Рисунок 1), что задержало пик осадков по сравнению с предыдущими годами [50]. В начале вегетационного сезона повышение температуры стимулирует микробно-опосредованные процессы круговорота азота, увеличивая скорость нитрификации и денитрификации в почве и приводя к увеличению выбросов N₂O [51,52,53]. В период пика вегетационного сезона наблюдается значительная положительная корреляция между осадками и скоростями нитрификации и денитрификации, что указывает на то, что когда температура не является ограничивающим фактором, осадки и доступность воды в почве ограничивают микробный круговорот азота, который варьируется во времени [54,55]. Таким образом, при максимальных значениях влажности почвы суточная динамика N₂O не зависит от температуры почвы и находится в состоянии эмиссии (Рисунок 4). Напротив, в начале вегетационного сезона, когда влажность почвы низкая, суточная динамика потоков N₂O из почвы образует одновершинную кривую между 8 и 13 часами, значительно отрицательно коррелируя с температурой почвы, что сходно с результатами, полученными на люцерновых лугах в восточной Ганьсу с использованием тех же методов мониторинга [56]. Среда со сниженным содержанием O₂ из-за достаточной влажности почвы и отсутствия интенсивности фотосинтеза растений способствует восстановлению N₂O, что переводит N₂O в состояние поглощения [57]. По мере того как интенсивность солнечного света повышает температуру почвы, усиленная транспирация способствует потреблению воды растениями, а усиленный фотосинтез обеспечивает больше O₂ для микробной активности [58], выбросы N₂O постепенно увеличиваются. Более высокие значения Q10 в начале и конце вегетационного сезона показывают, что выбросы N₂O более чувствительны к изменениям температуры в эти периоды, вероятно, из-за повышенной микробной активности в благоприятных условиях влажности и субстрата. И наоборот, более низкие значения Q10 для N₂O в период пика вегетации указывают на сниженную температурную чувствительность, и в этот период вариации потока N₂O в основном зависят от pH и NH₄⁺-N.
Помимо сезонных закономерностей эмиссии N₂O, наблюдаемых в умеренной степи, важно учитывать потенциальные эффекты временной задержки между обработками и микробными реакциями. Исследования показали, что микробные сообщества и почвенные процессы могут демонстрировать отсроченные реакции на изменения условий окружающей среды [59,60]. Хотя наше исследование было сосредоточено на прямой сезонной динамике эмиссии N₂O, возможность эффектов временной задержки требует дальнейшего изучения.
4.2. Реакция потоков N₂O в разные периоды вегетационного сезона в умеренной степи на добавление азота и воды
Добавление азота значительно способствовало эмиссии N₂O в этом исследовании, что сходно с результатами предыдущих исследований [15,61,62]. В лесных экосистемах азотное осаждение обычно приводит к увеличению выбросов N₂O, что согласуется с закономерностями, наблюдаемыми в этом исследовании для умеренных лугов, с вариациями в зависимости от содержания органического вещества почвы и динамики микробного сообщества. Например, лесные почвы с высоким содержанием органического углерода имеют тенденцию проявлять более сильные реакции эмиссии N₂O из-за усиленной денитрификационной активности [63]. Интегративный анализ глобальных парниковых газов также показал, что современное азотное осаждение значительно увеличивает выбросы N₂O из почвы [64]. Недавние исследования показали, что вклад органического вещества в эмиссию N₂O после добавления нитратов непропорционален праймированию почвенного углерода, индуцированному субстратом [31]. Это открытие предполагает, что индуцированные нитратами выбросы N₂O могут не зависеть исключительно от доступности углеродных субстратов, но также зависеть от динамики эффективности использования азота микроорганизмами и путей денитрификации. Добавление азота изначально не оказывало значительного влияния на потоки N₂O из почвы из-за поглощения и использования эффективного азота растениями [65]. Однако по мере увеличения добавления азота потребность растений в азоте удовлетворялась, конкуренция между растениями и нитрифицирующими микроорганизмами снижалась, концентрации матрицы для нитрификации и денитрификации увеличивались, а микроорганизмы, использующие остаточный неорганический азот, способствовали превращению почвенного азота в газообразные формы, тем самым усиливая выбросы N₂O из почвы [38,66,67,68]. Таким образом, влияние добавления азота на N₂O не было значительным в начале вегетационного сезона, но значительно способствовало выбросам N₂O в период пика вегетации.
Исследования показывают, что уменьшение количества осадков подавляет выбросы N₂O, в то время как увеличение осадков способствует им [24,53], поскольку соответствующие условия влажности напрямую изменяют содержание O₂ в почве и, таким образом, влияют на активность микробных ферментов, что согласуется с закономерностью пика вегетационного сезона в этом исследовании. Добавление воды увеличивает влажность почвы, снижает скорость диффузии кислорода из атмосферы в почву, способствует разложению остаточного органического вещества и позволяет высвобождать как органические, так и неорганические вещества в почву [69]. Таким образом, добавление воды может способствовать выбросу N₂O за счет повышения доступности азота и углерода в почве, которые служат субстратами для денитрификации [70]. Однако наше исследование показало, что добавление воды в начале вегетационного сезона подавляло выбросы N₂O, возможно, из-за того, что избыточная влажность почвы снижает уровень O₂, ускоряет восстановление редуктазы закиси азота, а ограниченная доступность азотных субстратов вынуждает денитрифицирующие бактерии использовать атмосферный N₂O в качестве альтернативного акцептора электронов вместо нитрата [57], тем самым снижая выбросы N₂O из почвы. Водно-болотные экосистемы в основном регулируются колебаниями уровня грунтовых вод, где высокое водонасыщение способствует полному восстановлению N₂O до N₂, тем самым снижая чистую эмиссию [71]. Однако добавление воды в начале вегетационного сезона ограничивало нитрификацию, подавляя численность AOA amoA и AOB amoA, тем самым ингибируя выбросы N₂O. Это приводит к различным закономерностям влияния добавления воды на потоки N₂O в разные периоды вегетационного сезона. Примечательно, что комбинированное добавление азота и воды значительно увеличило выбросы N₂O в период пика вегетации (Рисунок 5). Это может быть связано с тем, что добавление воды способствует быстрому переносу добавленного азота из поверхностной почвы в минеральный азот в слое почвы 0–10 см, тем самым обеспечивая обильные субстраты как для нитрификации, так и для денитрификации [37,72].
Сосуществование AOA amoA и AOB amoA в нашем исследовании позволяет предположить, что их присутствие обусловлено комплементарной нишевой дифференциацией, а не прямой конкуренцией. AOA amoA процветают в условиях низкого содержания аммиака и кислой среде, в то время как AOB amoA лучше приспособлены к богатым питательными веществами щелочным средам [73,74]. В начале вегетационного сезона микробная активность и превращение азота в N₂O были медленнее из-за более низких температур почвы, причем AOA amoA играли ключевую роль. Напротив, AOB amoA доминировали в период пика вегетации, когда более высокие температуры почвы и концентрации аммиака, обусловленные внесением удобрений и орошением, создавали более благоприятные условия [75].
4.3. Механизмы влияния добавления азота и воды на изменчивость потоков N₂O в разные периоды вегетационного сезона
Выбросы N₂O из почвы в основном происходят в результате микробно-опосредованных процессов нитрификации, денитрификации и их сопряженных процессов [76]. В полузасушливых лугах Внутренней Монголии нитрификация является основным путем продукции N₂O, причем азотные субстраты и доступность O₂ являются доминирующими регулирующими факторами [77]. В условиях увеличения азотных субстратов и сопряженных водо-азотных условий субстраты, способствующие продукции N₂O, и численность функциональных генов нитрификации и денитрификации являются основными факторами, влияющими на выбросы N₂O [39,78,79].
Это исследование показало, что динамические изменения потока N₂O значительно связаны с почвенными субстратами и численностью микроорганизмов. В начале вегетационного сезона добавление азота увеличивало содержание DON и NH₄⁺-N в почве, усиливая субстраты нитрификации и приводя к увеличению численности функциональных генов нитрификации, особенно AOB amoA (Таблица S6, Рисунок 9a), что согласуется с предыдущими исследованиями [41,79,80]. В этот период DON-опосредованное гетеротрофное аммонийное окисление является основным драйвером образования N₂O [81,82,83]. Однако NH₄⁺-N оказывал отрицательное влияние на выбросы N₂O (Таблица 2), возможно, из-за того, что усиленное почвенное дыхание потребляет больше O₂ и создает более анаэробные условия, благоприятные для денитрификации, таким образом способствуя полному восстановлению N₂O до N₂. В период пика вегетации, по мере увеличения степени превращения NH₄⁺-N в NO₃⁻-N, NO₃⁻-N, образующийся в процессе нитрификации, напрямую используется денитрифицирующими микроорганизмами, присутствующими в анаэробном или гипоксическом пространстве, в качестве матрицы [84], что обеспечивает подходящие условия реакции для денитрификации и, следовательно, стимулирует сопряжение нитрификации и денитрификации, стимулируя продукцию N₂O [85]. Хотя NO₃⁻-N значительно увеличивал численность гена nirK (Рисунок 9b), его экспрессия была отрицательно связана с выбросами N₂O и положительно связана с влажностью почвы (Рисунок 8). Это может быть связано с экологической чувствительностью генов nirK и nirS, в результате чего их роль в денитрификации зависит от влажных условий в течение вегетационного периода [46], что предполагает, что денитрификация более полная в условиях высокой влажности, что способствует восстановлению N₂O до N₂. Высокая численность гена nosZ дополнительно способствовала этому процессу (Таблица S6), указывая на то, что повышенная экспрессия генов nirK и nirS снижала выбросы N₂O. Кроме того, pH также влияет на процессы нитрификации и денитрификации [86]. Вызванное добавлением азота подкисление почвы значительно подавляет микробные сообщества, особенно арбускулярные микоризные грибы [87,88,89]. В сильно кислых условиях вклад грибов в выбросы N₂O увеличивается [90,91]. Добавление воды в некоторой степени смягчает засуху, тем самым способствуя микробной активности и усиливая обогащение азотом. Следовательно, содержание MBC и MBN было значительно ниже при добавлении азота, чем при добавлении воды (Таблица 1), что сходно с предыдущими исследованиями [92,93].
Влажность почвы может влиять на изменения численности функциональных генов и, таким образом, контролировать потоки N₂O, модулируя концентрацию O₂ в почве и содержание NO₃⁻-N [18,94,95]. Гипоксические условия, вызванные добавлением воды, очень благоприятны для пути денитрификации [96], который включает последний этап восстановления N₂O до N₂ в сильно насыщенных почвах [97]. Таким образом, условия влажности способствуют восстановлению N₂O до N₂, тем самым увеличивая поглощение N₂O [98]. Наше исследование показало, что в начале вегетационного сезона добавление воды подавляло выбросы N₂O (Рисунок 5). Добавление воды снижало уровень NO₃⁻-N, ингибируя процесс денитрификации и тем самым снижая выбросы N₂O (Рисунок 9). Исследования показали, что AOB и AOA проявляют различный вклад в процесс аммонийного окисления в зависимости от влажности почвы, тем самым влияя на выбросы N₂O [73]. В период пика вегетации, когда воды в изобилии, активность AOB обычно выше, что приводит к увеличению выбросов N₂O. Напротив, в условиях относительно низкой влажности почвы в начале вегетационного сезона активность AOA имеет тенденцию доминировать, что потенциально может привести к снижению выбросов N₂O. Однако аноксическая среда, вызванная добавлением воды, стимулировала гены nirK и nosZ, делая процесс денитрификации более полным. Исследования показывают, что ген nosZ проявляет большую чувствительность к колебаниям влажности почвы по сравнению с nirK и nirS, что коррелирует с усилением восстановления N₂O при более высокой влажности почвы [99]. Поглощение N₂O зависит от численности nosZ [98]. Таким образом, в пик вегетационного сезона моделирование структурными уравнениями показало, что добавление воды увеличивало влажность почвы, подавляло численность гена nosZ и снижало превращение N₂O в N₂, тем самым увеличивая выбросы N₂O (Рисунок 9). Это противоречит результатам начала вегетационного сезона, доказывая, что различное содержание влаги в почве по-разному действует на ген nosZ и что nosZ имеет потенциал выступать в качестве гена-индикатора выбросов N₂O из почвы (Рисунок 9). В целом, добавление азота и воды оказало значительное влияние на численность генов AOB amoA и AOA amoA, но не на функциональные гены денитрификации (Таблица S6), что указывает на то, что нитрификация играет доминирующую роль в луговых экосистемах [79]. Добавление азота значительно увеличило численность аммонийокисляющих бактерий (AOB) (Таблица S6), что позволяет предположить, что реакция численности AOB на азотное осаждение более чувствительна, чем AOA [78,100].
Это исследование показало, что добавление азота значительно увеличивало выбросы N₂O, в то время как добавление воды подавляло выбросы в начале вегетационного сезона, но способствовало им в период пика вегетации. Эти результаты подчеркивают важность рационального управления азотными и водными ресурсами в экосистемах умеренных лугов для снижения выбросов парниковых газов и поддержания здоровья экосистем. Учитывая, что добавление азота значительно снижает pH почвы и влияет на структуру микробных сообществ [101], необходимо изучить методы снижения азотного осаждения, такие как использование низкоазотных удобрений или применение улучшенных методов внесения удобрений, чтобы смягчить негативные последствия для подкисления почвы и микробной функциональности. Поскольку эффекты добавления воды на выбросы N₂O значительно различаются в разные периоды, рекомендуется отдавать приоритет водоснабжению в засушливые сезоны, избегая при этом чрезмерного орошения в период пика вегетации для снижения выбросов парниковых газов. Интегрированная стратегия управления азотными и водными ресурсами может эффективно оптимизировать циклы углерода и азота в луговых экосистемах, уравновешивая продуктивность экосистемы и выбросы парниковых газов [102], тем самым способствуя устойчивому развитию экосистем.
Хотя это исследование предоставляет предварительные данные о краткосрочных эффектах обработок на микробные сообщества и выбросы N₂O, несколько областей требуют дальнейшего изучения. Будущие исследования должны быть направлены на следующие направления: (1) изучение долгосрочных (многолетних) эффектов обработок на адаптацию микробных сообществ для лучшего понимания сукцессии и стабильности микробных сообществ во времени; (2) интеграция изотопных методов для лучшего разделения источников N₂O, в частности различения биологических и небиологических источников, что улучшит наше понимание микробного вклада в выбросы N₂O; и (3) изучение взаимодействий растений и микроорганизмов в опосредовании реакций N₂O, поскольку корневые экссудаты растений могут играть решающую роль в регуляции микробных сообществ и влиять на выбросы N₂O.
5. Выводы
Выбросы N₂O из умеренной степи Внутренней Монголии показали сезонные изменения, причем выбросы в вегетационный сезон (май-сентябрь) были выше, чем в невегетационный, под влиянием температуры и влажности. В этот период добавление азота способствовало выбросам N₂O, в то время как добавление воды подавляло их в начале вегетационного сезона и способствовало выбросам в пиковый период, причем между ними наблюдалось взаимодействие. В начале вегетационного сезона, при меньшем количестве осадков, основными драйверами были DON и SM; в теплый и влажный пик вегетации основными факторами стали pH и NH₄⁺-N. По мере постепенного уменьшения осадков важными факторами в конце вегетационного сезона были pH, NH₄⁺-N и ST. Добавление азота и воды влияет на поток N₂O из почвы, изменяя почвенную матрицу и численность микроорганизмов. Добавление азота обеспечивает матрицу для нитрификации и денитрификации, тем самым стимулируя выбросы N₂O. В начале вегетационного сезона добавление воды снижает матрицу денитрификации и способствует экспрессии nosZ, что уменьшает поток N₂O. Однако в период пика вегетации добавление воды подавляет nosZ и AOB amoA, одновременно увеличивая доступность органического вещества, что приводит к более высокому потоку N₂O. Примечательно, что гены нитрификации более чувствительны к добавлению азота и воды, чем гены денитрификации, причем AOB amoA играет доминирующую роль в процессе аммонийного окисления. Добавление азота значительно снижало содержание микробной биомассы и подавляло активность оксидаз, в то время как добавление воды помогало смягчить ингибирование микроорганизмов, вызванное подкислением при добавлении азота. В целом, на выбросы N₂O из умеренной степи по-разному влияют добавление азота и воды, и они определяются почвенной матрицей и реакцией микроорганизмов на изменения почвенных условий. Изучение этих факторов и их механизмов имеет решающее значение для снижения выбросов N₂O в условиях глобального изменения климата и предоставляет научную основу для адаптации и защиты луговых экосистем. Будущие исследования должны глубже изучать взаимосвязи в системе почва-растение-микроорганизмы и их долгосрочное влияние на выбросы N₂O, учитывать численность функциональных генов при амплификации как ДНК, так и РНК, получить более полное представление о путях изменчивости потока N₂O и процессах круговорота азота в экосистемах и предоставить более эффективные стратегии управления для устойчивого экологического развития.
Вспомогательные материалы
Следующие вспомогательные материалы можно загрузить по адресу: https://www.mdpi.com/article/10.3390/agriculture15030283/s1, Таблица S1: Детали добавления твердого азота и воды на делянках; Таблица S2: Праймеры для количественной ПЦР и условия реакции; Таблица S3: Температурная чувствительность (Q10) эмиссии N₂O по сезонам и обработкам; Таблица S4: Влияние добавления азота и воды на поток N₂O; Таблица S5: Влияние добавления азота и воды на активность почвенных ферментов; Таблица S6: Влияние добавления азота и воды на функциональные гены почвы; Рисунок S1: Анализ главных компонент (PCA) свойств почвы при различных обработках.
Ссылки
1. Prather, M.J.; Hsu, J.; DeLuca, N.M.; Jackman, C.H.; Oman, L.D.; Douglass, A.R.; Fleming, E.L.; Strahan, S.E.; Steenrod, S.D.; Søvde, O.A. Measuring and modeling the lifetime of nitrous oxide including its variability. J. Geophys. Res. Atmos. 2015, 120, 5693–5705. [Google Scholar] [CrossRef] [PubMed]
2. Tian, H.Q.; Xu, R.T.; Canadell, J.G.; Thompson, R.L.; Winiwarter, W.; Suntharalingam, P.; Davidson, E.A.; Ciais, P.; Jackson, R.B.; Janssens-Maenhout, G. A comprehensive quantification of global nitrous oxide sources and sinks. Nature 2020, 586, 248–256. [Google Scholar] [CrossRef] [PubMed]
3. Feng, R.; Li, Z.H. Current investigations on global N2O emissions and reductions: Prospect and outlook. Environ. Pollut. 2023, 338, 122664. [Google Scholar] [CrossRef]
4. Bouwman, A.; Beusen, A.; Griffioen, J.; Van Groenigen, J.; Hefting, M.; Oenema, O.; Van Puijenbroek, P.; Seitzinger, S.; Slomp, C.; Stehfest, E. Global trends and uncertainties in terrestrial denitrification and N2O emissions. Philos. Trans. R. Soc. B Biol. Sci. 2013, 368, 20130112. [Google Scholar] [CrossRef]
5. Harris, E.; Yu, L.; Wang, Y.P.; Mohn, J.; Henne, S.; Bai, E.; Barthel, M.; Bauters, M.; Boeckx, P.; Dorich, C.; et al. Warming and redistribution of nitrogen inputs drive an increase in terrestrial nitrous oxide emission factor. Nat. Commun. 2022, 13, 4310. [Google Scholar] [CrossRef] [PubMed]
6. Bardgett, R.D.; Bullock, J.M.; Lavorel, S.; Manning, P.; Schaffner, U.; Ostle, N.; Chomel, M.; Durigan, G.; Fry, E.L.; Johnson, D. Combatting global grassland degradation. Nat. Rev. Earth Environ. 2021, 2, 720–735. [Google Scholar] [CrossRef]
7. Zhang, F.; Qi, J.; Li, F.M.; Li, C.S.; Li, C.B. Quantifying nitrous oxide emissions from Chinese grasslands with a process-based model. Biogeosciences 2010, 7, 2039–2050. [Google Scholar] [CrossRef]
8. IPCC. Climate change 2013: The physical science basis. In Contribution of Working Group I to the Fifth Assessment Report of the Intergovernmental Panel on Climate Change; Cambridge University Press: Cambridge, UK; New York, NY, USA, 2013. [Google Scholar] [CrossRef]
9. Galloway, J.N.; Townsend, A.R.; Erisman, J.W.; Bekunda, M.; Cai, Z.; Freney, J.R.; Martinelli, L.A.; Seitzinger, S.P.; Sutton, M.A. Transformation of the nitrogen cycle: Recent trends, questions, and potential solutions. Science 2008, 320, 889–892. [Google Scholar] [CrossRef]
10. Li, Y.; Wang, G.; Shurpali, N.J.; Shen, Y.Y. Nitrogen addition affects nitrous oxide emissions of rainfed lucerne grassland. Int. J. Environ. Res. Public Health 2022, 19, 7789. [Google Scholar] [CrossRef] [PubMed]
11. Du, Y.G.; Ke, X.; Li, J.M.; Wang, Y.Y.; Cao, G.M.; Guo, X.W.; Chen, K.L. Nitrogen deposition increases global grassland N2O emission rates steeply: A meta-analysis. Catena 2021, 199, 105105. [Google Scholar] [CrossRef]
12. Gu, X.Y.; Wang, Y.H.; Laanbroek, H.J.; Xu, X.F.; Song, B.; Huo, Y.W.; Chen, S.P.; Li, L.H.; Zhang, L.H. Saturated N2O emission rates occur above the nitrogen deposition level predicted for the semi-arid grasslands of Inner Mongolia, China. Geoderma 2019, 341, 18–25. [Google Scholar] [CrossRef]
13. Xu, W.L.; Zhao, M.M.; Ren, R.R.; Song, W.Z.; Gao, W.F.; Henry, H.A.; Sun, W. Grazing amplifies the stimulating effects of N addition on N2O emissions in a temperate meadow steppe. Agric. Ecosyst. Environ. 2022, 339, 108143. [Google Scholar] [CrossRef]
14. Li, Z.L.; Zeng, Z.Q.; Tian, D.S.; Wang, J.S.; Fu, Z.; Zhang, F.Y.; Zhang, R.Y.; Chen, W.N.; Luo, Y.Q.; Niu, S. Global patterns and controlling factors of soil nitrification rate. Glob. Change Biol. 2020, 26, 4147–4157. [Google Scholar] [CrossRef] [PubMed]
15. Wu, Y.F.; Gao, X.P.; Cao, D.C.; Li, L.; Li, X.Y.; Zeng, F.J. Nitrous oxide emissions from an alpine grassland as affected by nitrogen addition. Atmosphere 2021, 12, 976. [Google Scholar] [CrossRef]
16. Li, Z.L.; Zeng, Z.Q.; Song, Z.P.; Tian, D.S.; Huang, X.Z.; Nie, S.; Wang, J.; Jiang, L.F.; Luo, Y.Q.; Cui, J. Variance and main drivers of field nitrous oxide emissions: A global synthesis. J. Clean. Prod. 2022, 353, 131686. [Google Scholar] [CrossRef]
17. Chen, S.; Hao, T.X.; Goulding, K.; Misselbrook, T.; Liu, X.J. Impact of 13-years of nitrogen addition on nitrous oxide and methane fluxes and ecosystem respiration in a temperate grassland. Environ. Pollut. 2019, 252, 675–681. [Google Scholar] [CrossRef] [PubMed]
18. Senbayram, M.; Chen, R.; Budai, A.; Bakken, L.; Dittert, K. N2O emission and the N2O/(N2O + N2) product ratio of denitrification as controlled by available carbon substrates and nitrate concentrations. Agric. Ecosyst. Environ. 2012, 147, 4–12. [Google Scholar] [CrossRef]
19. Obia, A.; Cornelissen, G.; Mulder, J.; Dorsch, P. Effect of soil pH increase by biochar on NO, N2O and N2 production during denitrification in acid soils. PloS ONE 2015, 10, e0138781. [Google Scholar] [CrossRef] [PubMed]
20. Wang, Y.J.; Guo, J.H.; Vogt, R.D.; Mulder, J.; Wang, J.G.; Zhang, X.S. Soil pH as the chief modifier for regional nitrous oxide emissions: New evidence and implications for global estimates and mitigation. Glob. Change Biol. 2018, 24, E617–E626. [Google Scholar] [CrossRef] [PubMed]
21. Schleuss, P.M.; Widdig, M.; Biederman, L.A.; Borer, E.T.; Crawley, M.J.; Kirkman, K.P.; Seabloom, E.W.; Wragg, P.D.; Spohn, M. Microbial substrate stoichiometry governs nutrient effects on nitrogen cycling in grassland soils. Soil Biol. Biochem. 2021, 155, 108168. [Google Scholar] [CrossRef]
22. Bergaust, L.; Mao, Y.; Bakken, L.R.; Frostegard, A. Denitrification response patterns during the transition to anoxic respiration and posttranscriptional effects of suboptimal pH on nitrogen oxide reductase in Paracoccus denitrificans. Appl. Environ. Microbiol. 2010, 76, 6387–6396. [Google Scholar] [CrossRef] [PubMed]
23. Yang, J.Y.; Jia, X.Y.; Ma, H.Z.; Chen, X.; Liu, J.; Shangguan, Z.P.; Yan, W.M. Effects of warming and precipitation changes on soil GHG fluxes: A meta- analysis. Sci. Total Environ. 2022, 827, 154351. [Google Scholar] [CrossRef]
24. Li, L.F.; Hao, Y.B.; Zheng, Z.Z.; Wang, W.J.; Biederman, J.A.; Wang, Y.F.; Wen, F.Q.; Qian, R.Y.; Xu, C.; Zhang, B.; et al. Heavy rainfall in peak growing season had larger effects on soil nitrogen flux and pool than in the late season in a semiarid grassland. Agric. Ecosyst. Environ. 2021, 326, 107785. [Google Scholar] [CrossRef]
25. Verhoeven, E.; Decock, C.; Barthel, M.; Bertora, C.; Sacco, D.; Romani, M.; Sleutel, S.; Six, J. Nitrification and coupled nitrification-denitrification at shallow depths are responsible for early season N2O emissions under alternate wetting and drying management in an Italian rice paddy system. Soil Biol. Biochem. 2018, 120, 58–69. [Google Scholar] [CrossRef]
26. Wang, X.; Bai, X.Y.; Ma, L.; He, C.G.; Jiang, H.B.; Sheng, L.X.; Luo, W.B. Snow depths’ impact on soil microbial activities and carbon dioxide fluxes from a temperate wetland in Northeast China. Sci. Rep. 2020, 10, 8709. [Google Scholar] [CrossRef]
27. Kou, Y.P.; Li, C.N.; Li, J.B.; Tu, B.; Wang, Y.S.; Li, X.Z. Climate and soil parameters are more important than denitrifier abundances in controlling potential denitrification rates in Chinese grassland soils. Sci. Total Environ. 2019, 669, 62–69. [Google Scholar] [CrossRef] [PubMed]
28. Shi, Y.J.; Wang, J.F.; Ao, Y.N.; Han, J.Y.; Guo, Z.H.; Liu, X.Y.; Zhang, J.W.; Mu, C.S.; Le Roux, X. Responses of soil N2O emissions and their abiotic and biotic drivers to altered rainfall regimes and co-occurring wet N deposition in a semi-arid grassland. Glob. Change Biol. 2021, 27, 4894–4908. [Google Scholar] [CrossRef]
29. Guo, Y.; Dong, Y.S.; Peng, Q.; Li, Z.L.; He, Y.L.; Yan, Z.Q.; Qin, S.Q. Effects of nitrogen and water addition on N2O emissions in temperate grasslands, northern China. Appl. Soil Ecol. 2022, 177, 104548. [Google Scholar] [CrossRef]
30. Shcherbak, I.; Millar, N.; Robertson, G.P. Global metaanalysis of the nonlinear response of soil nitrous oxide (N2O ) emissions to fertilizer nitrogen. Proc. Natl. Acad. Sci. USA 2014, 111, 9199–9204. [Google Scholar] [CrossRef]
31. Li, Y.; Moinet, G.Y.; Clough, T.J.; Whitehead, D. Organic matter contributions to nitrous oxide emissions following nitrate addition are not proportional to substrate-induced soil carbon priming. Sci. Total Environ. 2022, 851, 158274. [Google Scholar] [CrossRef] [PubMed]
32. Ying, J.Y.; Li, X.X.; Wang, N.N.; Lan, Z.C.; He, J.Z.; Bai, Y.F. Contrasting effects of nitrogen forms and soil pH on ammonia oxidizing microorganisms and their responses to long-term nitrogen fertilization in a typical steppe ecosystem. Soil Biol. Biochem. 2017, 107, 10–18. [Google Scholar] [CrossRef]
33. He, W.Y.; Zhang, M.M.; Jin, G.Z.; Sui, X.; Zhang, T.; Song, F.Q. Effects of nitrogen deposition on nitrogen-mineralizing enzyme activity and soil microbial community structure in a korean pine plantation. Microb. Ecol. 2020, 81, 410–424. [Google Scholar] [CrossRef]
34. Li, Y.Y.; Chapman, S.J.; Nicol, G.W.; Yao, H.Y. Nitrification and nitrifiers in acidic soils. Soil Biol. Biochem. 2018, 116, 290–301. [Google Scholar] [CrossRef]
35. Sun, R.; Myrold, D.D.; Wang, D.Z.; Guo, X.S.; Chu, H.Y. AOA and AOB communities respond differently to changes of soil pH under long-term fertilization. Soil Ecol. Lett. 2019, 1, 126–135. [Google Scholar] [CrossRef]
36. Wang, Y.; Ji, H.F.; Wang, R.; Guo, S.L. Responses of nitrification and denitrification to nitrogen and phosphorus fertilization: Does the intrinsic soil fertility matter? Plant Soil 2019, 440, 443–456. [Google Scholar] [CrossRef]
37. Liu, X.C.; Dong, Y.S.; Qi, Y.C.; Peng, Q.; He, Y.T.; Sun, L.J.; Jia, J.Q.; Guo, S.F.; Cao, C.C.; Yan, Z.Q. Response of N2O emission to water and nitrogen addition in temperate typical steppe soil in Inner Mongolia, China. Soil Tillage Res. 2015, 151, 9–17. [Google Scholar] [CrossRef]
38. Liu, W.; Lü, X.T.; Yang, Y.; Hou, L.Y.; Shao, C.L.; Yuan, W.P.; Pan, Q.M.; Li, L.H. Hot moments of N2O emission under water and nitrogen management in three types of steppe. J. Geophys. Res. Biogeosciences 2022, 127, e2022JG006877. [Google Scholar] [CrossRef]
39. Zhang, L.H.; Hou, L.Y.; Guo, D.F.; Li, L.H.; Xu, X.F. Interactive impacts of nitrogen input and water amendment on growing season fluxes of CO2, CH4, and N2O in a semiarid grassland, Northern China. Sci. Total Environ. 2017, 578, 523–534. [Google Scholar] [CrossRef]
40. Du, Y.G.; Guo, X.W.; Cao, G.M.; Li, Y.K. Increased nitrous oxide emissions resulting from nitrogen addition and increased precipitation in an alpine meadow ecosystem. Pol. J. Environ. Stud. 2016, 25, 447–451. [Google Scholar] [CrossRef] [PubMed]
41. Shen, X.Y.; Zhang, L.M.; Shen, J.P.; Li, L.H.; Yuan, C.L.; He, J.Z. Nitrogen loading levels affect abundance and composition of soil ammonia oxidizing prokaryotes in semiarid temperate grassland. J. Soils Sediments 2011, 11, 1243–1252. [Google Scholar] [CrossRef]
42. Sun, J.; Liu, M.; Li, S.G.; Hu, Z.M.; Sun, X.M.; Wen, X.F.; Zhang, L.M. Survival strategy of Stipa krylovii and Agropyron cristatum in typical steppe of Inner Mongolia. Acta Ecol. Sin. 2011, 31, 2148–2158. [Google Scholar]
43. Bai, Y.X.; Li, X.B.; Wen, W.Y.; Mi, X.; Li, R.H.; Huang, Q.; Zhang, M. CO2, CH4 and N2O flux changes in degraded grassland soil of Inner Mongolia, China. J. Arid. Land 2018, 10, 347–361. [Google Scholar] [CrossRef]
44. Zhang, K.R.; Zhu, Q.A.; Liu, J.X.; Wang, M.; Zhou, X.L.; Li, M.X.; Wang, K.F.; Ding, J.H.; Peng, C.H. Spatial and temporal variations of N2O emissions from global forest and grassland ecosystems. Agric. For. Meteorol. 2019, 266, 129–139. [Google Scholar] [CrossRef]
45. Tang, Y.Q.; Yu, G.R.; Zhang, X.Y.; Wang, Q.F.; Tian, D.S.; Tian, J.; Niu, S.L.; Ge, J.P. Environmental variables better explain changes in potential nitrification and denitrification activities than microbial properties in fertilized forest soils. Sci. Total Environ. 2019, 647, 653–662. [Google Scholar] [CrossRef]
46. Zhang, J.Q.; He, P.; Liu, Y.H.; Du, W.; Jing, H.C.; Nie, C. Soil properties and microbial abundance explain variations in N2O fluxes from temperate steppe soil treated with nitrogen and water in Inner Mongolia, China. Appl. Soil Ecol. 2021, 165, 103984. [Google Scholar] [CrossRef]
47. Gao, W.F.; Gao, D.W.; Song, L.Q.; Sheng, H.C.; Cai, T.J.; Liang, H. Contribution of the nongrowing season to annual N2O emissions from the permafrost wetland in Northeast China. Environ. Sci. Pollut. Res. 2022, 29, 61470–61487. [Google Scholar] [CrossRef] [PubMed]
48. Li, K.H.; Gong, Y.M.; Song, W.; Lv, J.L.; Chang, Y.H.; Hu, Y.K.; Tian, C.Y.; Christie, P.; Liu, X.J. No significant nitrous oxide emissions during spring thaw under grazing and nitrogen addition in an alpine grassland. Glob. Change Biol. 2012, 18, 2546–2554. [Google Scholar] [CrossRef]
49. Gao, W.F.; Yao, Y.L.; Gao, D.W.; Wang, H.; Song, L.Q.; Sheng, H.C.; Cai, T.J.; Liang, H. Responses of N2O emissions to spring thaw period in a typical continuous permafrost region of the Daxing’an Mountains, northeast China. Atmos. Environ. 2019, 214, 116822. [Google Scholar] [CrossRef]
50. Dong, Q.; Liu, Y.H.; He, P.; Du, W. Belowground biomass changed the regulatory factors of soil N2O funder N and water additions in a temperate steppe of Inner Mongolia. J. Soil Sci. Plant Nutr. 2023, 24, 606–617. [Google Scholar] [CrossRef]
51. Dobbie, K.; Smith, K. The effects of temperature, water-filled pore space and land use on N2O emissions from an imperfectly drained gleysol. Eur. J. Soil Sci. 2001, 52, 667–673. [Google Scholar] [CrossRef]
52. Wang, Y.S.; Xue, M.; Zheng, X.H.; Ji, B.M.; Du, R.; Wang, Y.F. Effects of environmental factors on N2O emission from and CH4 uptake by the typical grasslands in the Inner Mongolia. Chemosphere 2005, 58, 205–215. [Google Scholar] [CrossRef]
53. Li, L.F.; Zheng, Z.Z.; Wang, W.J.; Biederman, J.A.; Xu, X.L.; Ran, Q.W.; Qian, R.Y.; Xu, C.; Zhang, B.; Wang, F.; et al. Terrestrial N2O emissions and related functional genes under climate change: A global meta-analysis. Glob. Change Biol. 2020, 26, 931–943. [Google Scholar] [CrossRef]
54. Wang, N.N.; Li, L.; Dannenmann, M.; Luo, Y.K.; Xu, X.H.; Zhang, B.W.; Chen, S.P.; Dong, K.H.; Huang, J.H.; Xu, X.F.; et al. Seasonality of gross ammonification and nitrification altered by precipitation in a semi-arid grassland of Northern China. Soil Biol. Biochem. 2021, 154, 108146. [Google Scholar] [CrossRef]
55. Bhandari, J.; Pan, X.B.; Bijaya, G. Spatial and seasonal variation in rain use efficiency in semiarid grasslands of Inner Mongolia. Adv. Meteorol. 2015, 2015, 917415. [Google Scholar] [CrossRef]
56. Wang, G.; Yang, X.L.; Li, Y. Characteristics of N2O emission from Medicago sativa stands and its response to nitrogen fertilizers in the Longdong dryland plateau. Chin. J. Appl. Environ. Biol. 2018, 24, 450–456. [Google Scholar] [CrossRef]
57. Majumdar, D. Biogeochemistry of N2O uptake and consumption in submerged soils and rice fields and implications in climate change. Crit. Rev. Environ. Sci. Technol. 2013, 43, 2653–2684. [Google Scholar] [CrossRef]
58. Li, F.D.; Du, K.; Zhang, Q.Y.; Gu, C.K.; Leng, P.F.; Qiao, Y.F.; Zhu, N.; Hao, S.; Huang, Y.B.; Shi, S.J. High-frequency dynamic observation of N2O emission flux from cropland in the North China Plain. Chin. J. Eco-Agric. 2018, 26, 195–202. [Google Scholar] [CrossRef]
59. Yang, J.; Blondeel, H.; Boeckx, P.; Verheyen, K.; De Frenne, P. Responses of the soil microbial community structure to multiple interacting global change drivers in temperate forests. Lant Soil 2023, 496, 641–656. [Google Scholar] [CrossRef]
60. Luo, X.S.; Qian, H.; Wang, L.; Han, S.; Wen, S.L.; Wang, B.; Huang, Q.Y.; Chen, W.L. Fertilizer types shaped the microbial guilds driving the dissimilatory nitrate reduction to ammonia process in a Ferralic Cambisol. Soil Biol. Biochem. 2020, 141, 107677. [Google Scholar] [CrossRef]
61. Liu, X.R.; Zhang, Q.W.; Li, S.G.; Zhang, L.M.; Ren, J.Q. Simulated NH4+-N deposition inhibits CH4 uptake and promotes N2O emission in the meadow steppe of Inner Mongolia, China. Pedosphere 2017, 27, 306–317. [Google Scholar] [CrossRef]
62. Yang, Y.; Xiao, Y.M.; Li, C.B.; Wang, B.; Gao, Y.H.; Zhou, G.Y. Nitrogen addition, rather than altered precipitation, stimulates nitrous oxide emissions in an alpine steppe. Ecol. Evol. 2021, 11, 15153–15163. [Google Scholar] [CrossRef] [PubMed]
63. Cen, X.Y.; Mueller, C.; Kang, X.Y.; Zhou, X.H.; Zhang, J.B.; Yu, G.R.; He, N.P. Nitrogen deposition contributed to a global increase in nitrous oxide emissions from forest soils. Commun. Earth Environ. 2024, 5, 532. [Google Scholar] [CrossRef]
64. Deng, L.; Huang, C.B.; Kim, D.G.; Shangguan, Z.P.; Wang, K.B.; Song, X.Z.; Peng, C.H. Soil GHG fluxes are altered by N deposition: New data indicate lower N stimulation of the N2O flux and greater stimulation of the calculated C pools. Glob. Change Biol. 2020, 26, 2613–2629. [Google Scholar] [CrossRef] [PubMed]
65. Zhang, C.J.; Yang, Z.L.; Shen, J.P.; Sun, Y.F.; Wang, J.T.; Han, H.Y.; Wan, S.Q.; Zhang, L.M.; He, J.Z. Impacts of long-term nitrogen addition, watering and mowing on ammonia oxidizers, denitrifiers and plant communities in a temperate steppe. Appl. Soil Ecol. 2018, 130, 241–250. [Google Scholar] [CrossRef]
66. Geng, F.Z.; Li, K.H.; Liu, X.J.; Gong, Y.M.; Yue, P.; Li, Y.G.; Han, W.X. Long-term effects of N deposition on N2O emission in an alpine grassland of Central Asia. Catena 2019, 182, 104100. [Google Scholar] [CrossRef]
67. Chen, J.H.; Zhang, Y.J.; Yang, Y.; Tao, T.T.; Sun, X.; Guo, P. Effects of increasing organic nitrogen inputs on CO2, CH4, and N2O fluxes in a temperate grassland. Environ. Pollut. 2021, 268, 115822. [Google Scholar] [CrossRef] [PubMed]
68. Ma, L.N.; Lü, X.T.; Liu, Y.; Guo, J.X.; Zhang, N.Y.; Yang, J.Q.; Wang, R.Z. The effects of warming and nitrogen addition on soil nitrogen cycling in a temperate grassland, northeastern China. PLoS ONE 2011, 6, e27645. [Google Scholar] [CrossRef] [PubMed]
69. Chen, W.W.; Zheng, X.H.; Chen, Q.; Wolf, B.; Butterbach-Bahl, K.; Brüggemann, N.; Lin, S. Effects of increasing precipitation and nitrogen deposition on CH4 and N2O fluxes and ecosystem respiration in a degraded steppe in Inner Mongolia, China. Geoderma 2013, 192, 335–340. [Google Scholar] [CrossRef]
70. Yan, G.Y.; Mu, C.C.; Xing, Y.J.; Wang, Q.G. Responses and mechanisms of soil greenhouse gas fluxes to changes in precipitation intensity and duration: A meta-analysis for a global perspective. Can. J. Soil Sci. 2018, 98, 591–603. [Google Scholar] [CrossRef]
71. Zhang, W.T.; Hu, Z.Y.; Audet, J.; Davidson, T.A.; Kang, E.; Kang, X.M.; Li, Y.; Zhang, X.D.; Wang, J.Z. Effects of water table level and nitrogen deposition on methane and nitrous oxide emissions in an alpine peatland. Biogeosciences 2022, 19, 5187–5197. [Google Scholar] [CrossRef]
72. Kim, D.-G.; Mishurov, M.; Kiely, G. Effect of increased N use and dry periods on N2O emission from a fertilized grassland. Nutr. Cycl. Agroecosyst. 2010, 88, 397–410. [Google Scholar] [CrossRef]
73. Lin, Y.P.; Ansari, A.; Wunderlich, R.F.; Lur, H.-S.; Thanh Ngoc-Dan, C.; Mukhtar, H. Assessing the influence of environmental niche segregation in ammonia oxidizers on N2O fluxes from soil and sediments. Chemosphere 2022, 289, 133049. [Google Scholar] [CrossRef] [PubMed]
74. Hink, L.; Gubry-Rangin, C.; Nicol, G.W.; Prosser, J.I. The consequences of niche and physiological differentiation of archaeal and bacterial ammonia oxidisers for nitrous oxide emissions. ISME J. 2018, 12, 1084–1093. [Google Scholar] [CrossRef]
75. Hu, L.; Dong, Z.X.; Wang, Z.; Xiao, L.W.; Zhu, B. The contributions of ammonia oxidizing bacteria and archaea to nitrification-dependent N2O emission in alkaline and neutral purple soils. Sci. Rep. 2022, 12, 19928. [Google Scholar] [CrossRef] [PubMed]
76. Castro-Barros, C.M.; Rodríguez-Caballero, A.; Volcke, E.; Pijuan, M. Effect of nitrite on the N2O and NO production on the nitrification of low-strength ammonium wastewater. Chem. Eng. J. 2016, 287, 269–276. [Google Scholar] [CrossRef]
77. Jiang, C.M.; Yu, G.R.; Fang, H.J.; Cao, G.M.; Li, Y.N. Short-term effect of increasing nitrogen deposition on CO2, CH4 and N2O fluxes in an alpine meadow on the Qinghai-Tibetan Plateau, China. Atmos. Environ. 2010, 44, 2920–2926. [Google Scholar] [CrossRef]
78. Sun, Y.F.; Shen, J.P.; Zhang, C.J.; Zhang, L.M.; Bai, W.M.; Fang, Y.; He, J.Z. Responses of soil microbial community to nitrogen fertilizer and precipitation regimes in a semi-arid steppe. J. Soils Sediments 2017, 18, 762–774. [Google Scholar] [CrossRef]
79. Long, X.E.; Shen, J.P.; Wang, J.T.; Zhang, L.M.; Di, H.J.; He, J.Z. Contrasting response of two grassland soils to N addition and moisture levels: N2O emission and functional gene abundance. J. Soils Sediments 2016, 17, 384–392. [Google Scholar] [CrossRef]
80. Verhamme, D.T.; Prosser, J.I.; Nicol, G.W. Ammonia concentration determines differential growth of ammonia-oxidising archaea and bacteria in soil microcosms. ISME J. 2011, 5, 1067–1071. [Google Scholar] [CrossRef] [PubMed]
81. Xu, P.D.; Shi, L.; Yang, X.; Yang, H.M.; Dong, K.H.; Wang, C.H. Influence mechanisms of N addition on the concentration of soil dissolved organic matter in China. Land Degrad. Dev. 2023, 34, 4690–4698. [Google Scholar] [CrossRef]
82. Zhang, J.B.; Wang, J.; Zhong, W.H.; Cai, Z.C. Organic nitrogen stimulates the heterotrophic nitrification rate in an acidic forest soil. Soil Biol. Biochem. 2015, 80, 293–295. [Google Scholar] [CrossRef]
83. Huang, R.; Wang, Y.Y.; Liu, J.; Li, J.C.; Xu, G.X.; Luo, M.; Xu, C.; Ci, E.; Gao, M. Variation in N2O emission and N2O related microbial functional genes in straw-and biochar-amended and non-amended soils. Appl. Soil Ecol. 2019, 137, 57–68. [Google Scholar] [CrossRef]
84. Wrage, N.; Velthof, G.L.; van Beusichem, M.L.; Oenema, O. Role of nitrifier denitrification in the production of nitrous oxide. Soil Biol. Biochem. 2001, 33, 1723–1732. [Google Scholar] [CrossRef]
85. Fan, K.K.; Yan, Y.C.; Xu, D.W.; Li, S.Z.; Zhao, Y.; Wang, X.; Xin, X.P. Methane and nitrous oxide fluxes with different land uses in the temperate meadow steppe of Inner Mongolia, China. Agronomy 2022, 12, 2810. [Google Scholar] [CrossRef]
86. Zhang, C.; Song, Z.L.; Zhuang, D.H.; Wang, J.; Xie, S.S.; Liu, G.B. Urea fertilization decreases soil bacterial diversity, but improves microbial biomass, respiration, and N-cycling potential in a semiarid grassland. Biol. Fertil. Soils 2019, 55, 229–242. [Google Scholar] [CrossRef]
87. Yang, Y.; Li, T.; Wang, Y.Q.; Cheng, H.; Chang, S.X.; Liang, C.; An, S.S. Negative effects of multiple global change factors on soil microbial diversity. Soil Biol. Biochem. 2021, 156, 108229. [Google Scholar] [CrossRef]
88. Han, Y.F.; Feng, J.G.; Han, M.G.; Zhu, B. Responses of arbuscular mycorrhizal fungi to nitrogen addition: A meta-analysis. Glob. Change Biol. 2020, 26, 7229–7241. [Google Scholar] [CrossRef] [PubMed]
89. Zeng, J.; Liu, X.J.; Song, L.; Lin, X.G.; Zhang, H.Y.; Shen, C.C.; Chu, H.Y. Nitrogen fertilization directly affects soil bacterial diversity and indirectly affects bacterial community composition. Soil Biol. Biochem. 2016, 92, 41–49. [Google Scholar] [CrossRef]
90. Huang, Y.; Xiao, X.; Long, X.E. Fungal denitrification contributes significantly to N2O production in a highly acidic tea soil. J. Soils Sediments 2017, 17, 1599–1606. [Google Scholar] [CrossRef]
91. Aldossari, N.; Ishii, S. Fungal denitrification revisited–Recent advancements and future opportunities. Soil Biol. Biochem. 2021, 157, 108250. [Google Scholar] [CrossRef]
92. Peng, Y.; Chen, G.S.; Chen, G.T.; Li, S.; Peng, T.C.; Qiu, X.R.; Luo, J.; Yang, S.S.; Hu, T.X.; Hu, H.L. Soil biochemical responses to nitrogen addition in a secondary evergreen broad-leaved forest ecosystem. Sci. Rep. 2017, 7, 2783. [Google Scholar] [CrossRef] [PubMed]
93. Yang, S.; Li, X.B.; Wang, R.Z.; Cai, J.P.; Xu, Z.W.; Zhang, Y.G.; Li, H.; Jiang, Y. Effects of nitrogen and water addition on soil bacterial diversity and community structure in temperate grasslands in northern China. J. Appl. Ecol. 2015, 26, 739–746. [Google Scholar] [CrossRef]
94. Morley, N.; Baggs, E.M. Carbon and oxygen controls on N2O and N2 production during nitrate reduction. Soil Biol. Biochem. 2010, 42, 1864–1871. [Google Scholar] [CrossRef]
95. Juhanson, J.; Hallin, S.; Soderstrom, M.; Stenberg, M.; Jones, C.M. Spatial and phyloecological analyses of nosZ genes underscore niche differentiation amongst terrestrial N2O reducing communities. Soil Biol. Biochem. 2017, 115, 82–91. [Google Scholar] [CrossRef]
96. Khalil, K.; Mary, B.; Renault, P. Nitrous oxide production by nitrification and denitrification in soil aggregates as affected by O2 concentration. Soil Biol. Biochem. 2004, 36, 687–699. [Google Scholar] [CrossRef]
97. Wu, D.M.; Dong, W.X.; Oenema, O.; Wang, Y.Y.; Trebs, I.; Hu, C.S. N2O consumption by low-nitrogen soil and its regulation by water and oxygen. Soil Biol. Biochem. 2013, 60, 165–172. [Google Scholar] [CrossRef]
98. Liu, H.S.; Zheng, X.Z.; Li, Y.F.; Yu, J.H.; Ding, H.; Sveen, T.R.; Zhang, Y.S. Soil moisture determines nitrous oxide emission and uptake. Sci. Total Environ. 2022, 822, 153566. [Google Scholar] [CrossRef]
99. Qin, H.L.; Xing, X.Y.; Tang, Y.F.; Zhu, B.L.; Wei, X.M.; Chen, X.B.; Liu, Y. Soil moisture and activity of nitrite- and nitrous oxide-reducing microbes enhanced nitrous oxide emissions in fallow paddy soils. Biol. Fertil. Soils 2020, 56, 53–67. [Google Scholar] [CrossRef]
100. Carey, C.J.; Dove, N.C.; Beman, J.M.; Hart, S.C.; Aronson, E.L. Meta-analysis reveals ammonia-oxidizing bacteria respond more strongly to nitrogen addition than ammonia-oxidizing archaea. Soil Biol. Biochem. 2016, 99, 158–166. [Google Scholar] [CrossRef]
101. Ren, J.L.; Wang, C.L.; Wang, Q.X.; Song, W.Z.; Sun, W. Nitrogen addition regulates the effects of variation in precipitation patterns on plant biomass formation and allocation in a Leymus chinensis grassland of northeast China. Front. Plant Sci. 2024, 14, 1323766. [Google Scholar] [CrossRef] [PubMed]
102. Peng, Q.; Qi, Y.C.; Yin, F.H.; Guo, Y.; Dong, Y.S.; Liu, X.R.; Yuan, X.J.; Lv, N. The seasonal response of N2O emissions to increasing precipitation and nitrogen deposition and its driving factors in temperate semi-arid grassland. Agronomy 2024, 14, 1153. [Google Scholar] [CrossRef]
Ren S, Liu Y, He P, Zhao Y, Wang C. Nitrogen and Water Additions Affect N2O Dynamics in Temperate Steppe by Regulating Soil Matrix and Microbial Abundance. Agriculture. 2025; 15(3):283. https://doi.org/10.3390/agriculture15030283
Перевод статьи «Nitrogen and Water Additions Affect N2O Dynamics in Temperate Steppe by Regulating Soil Matrix and Microbial Abundance» авторов Ren S, Liu Y, He P, Zhao Y, Wang C., оригинал доступен по ссылке. Лицензия: CC BY. Изменения: переведено на русский язык
фото: wikipedia
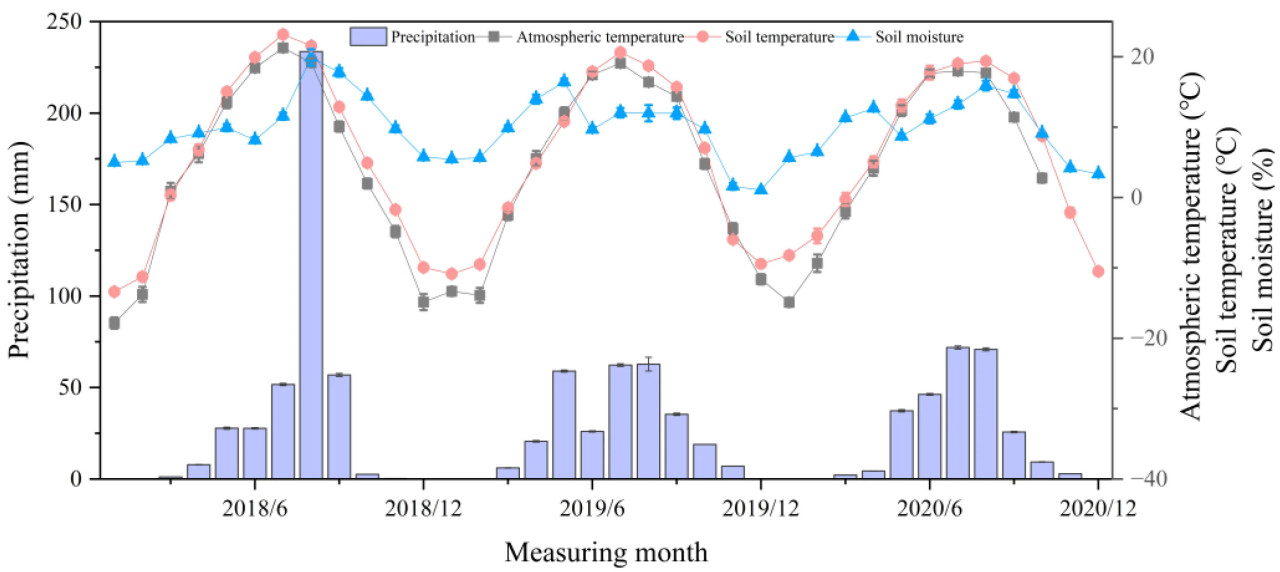
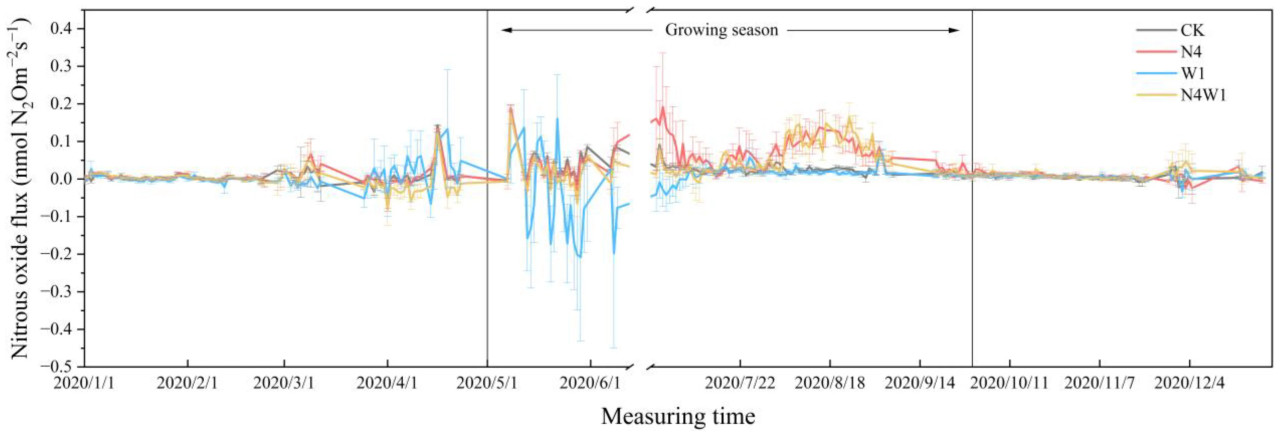
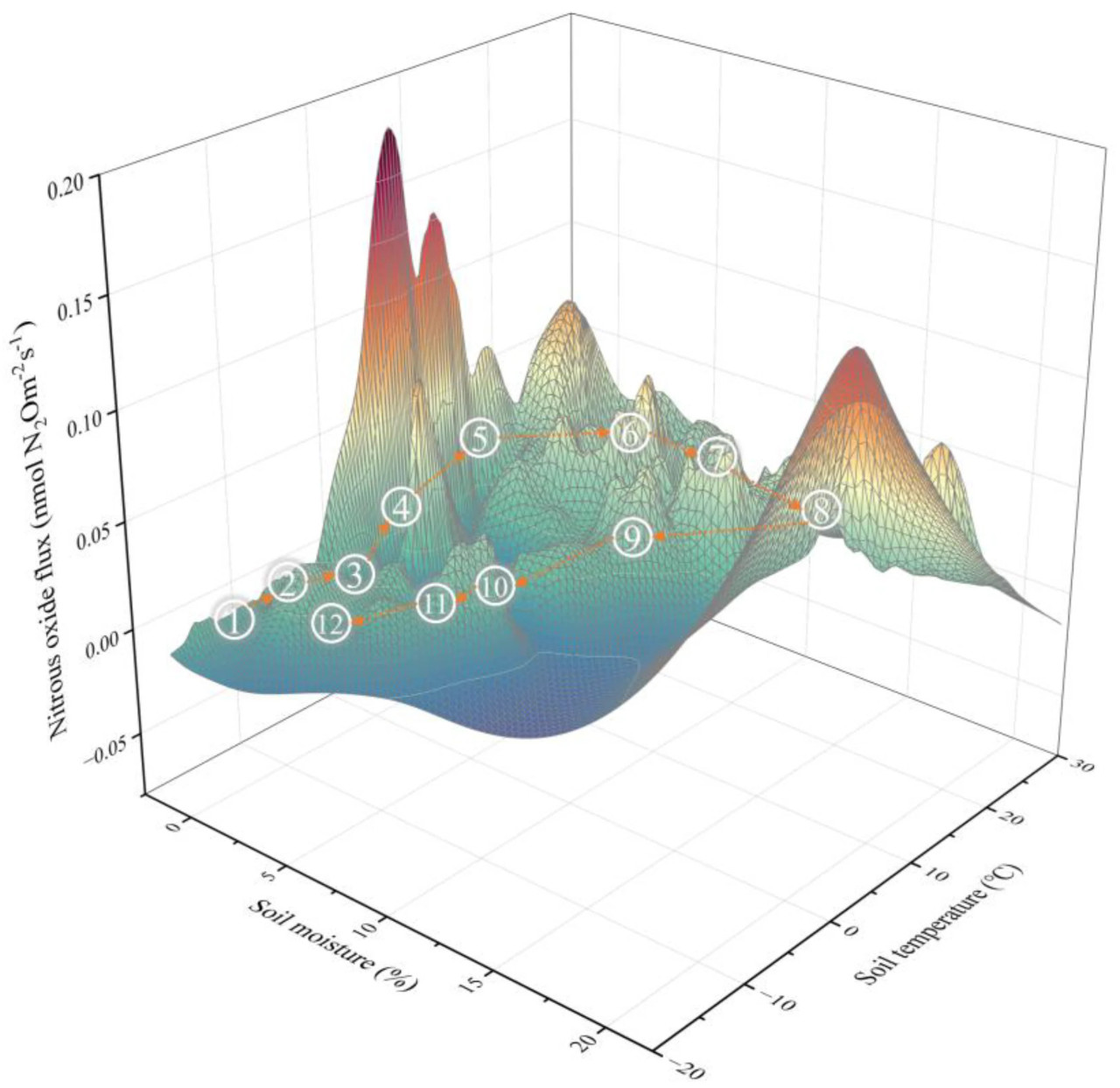
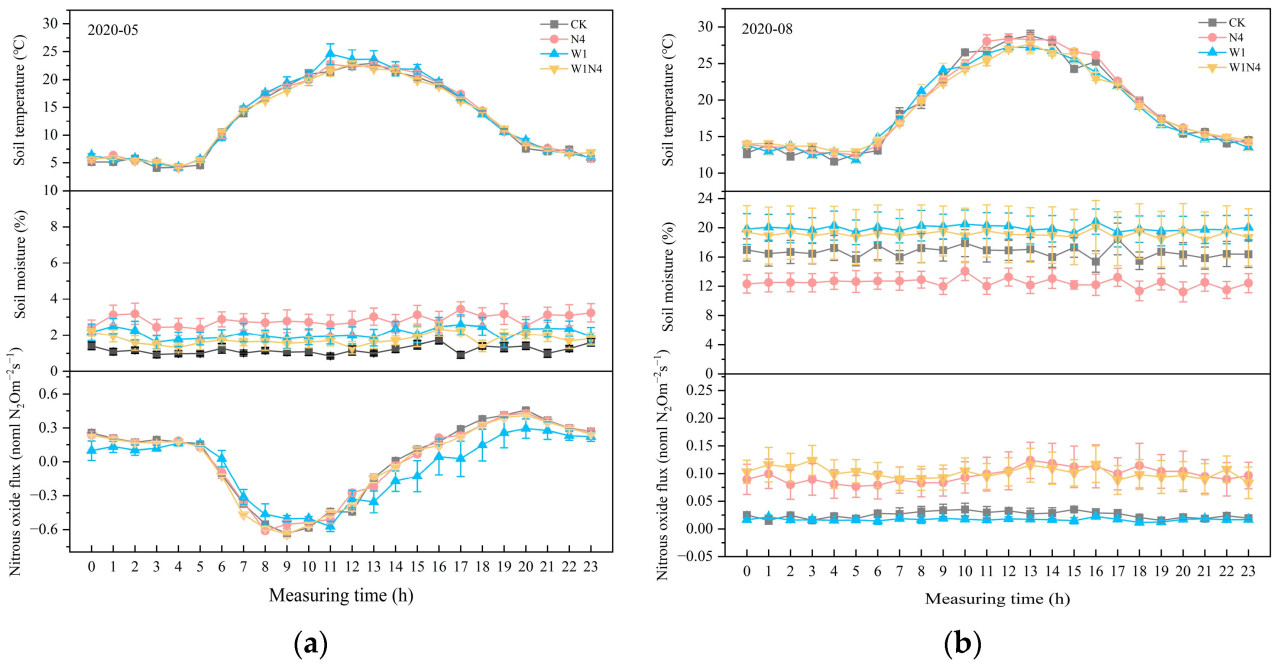
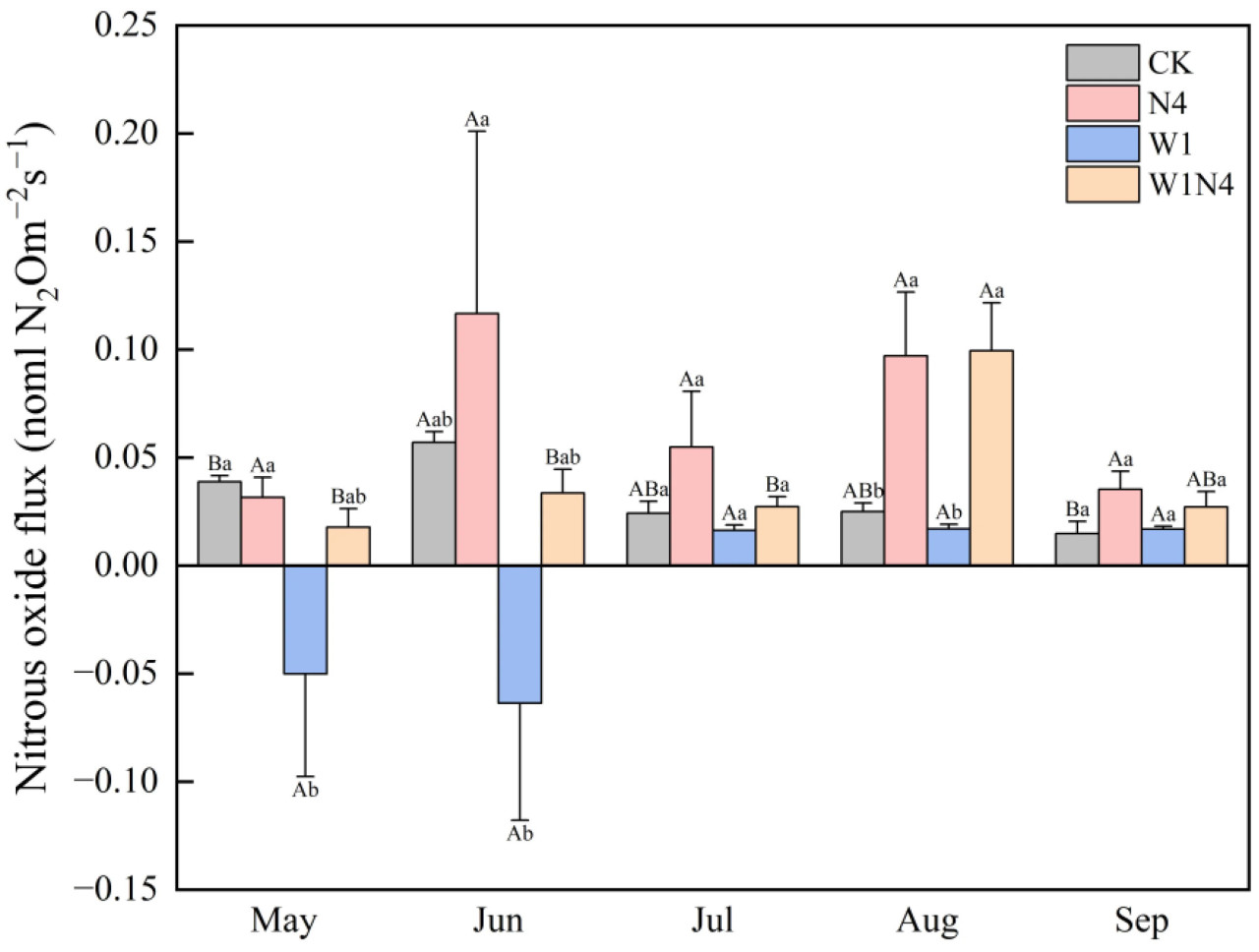
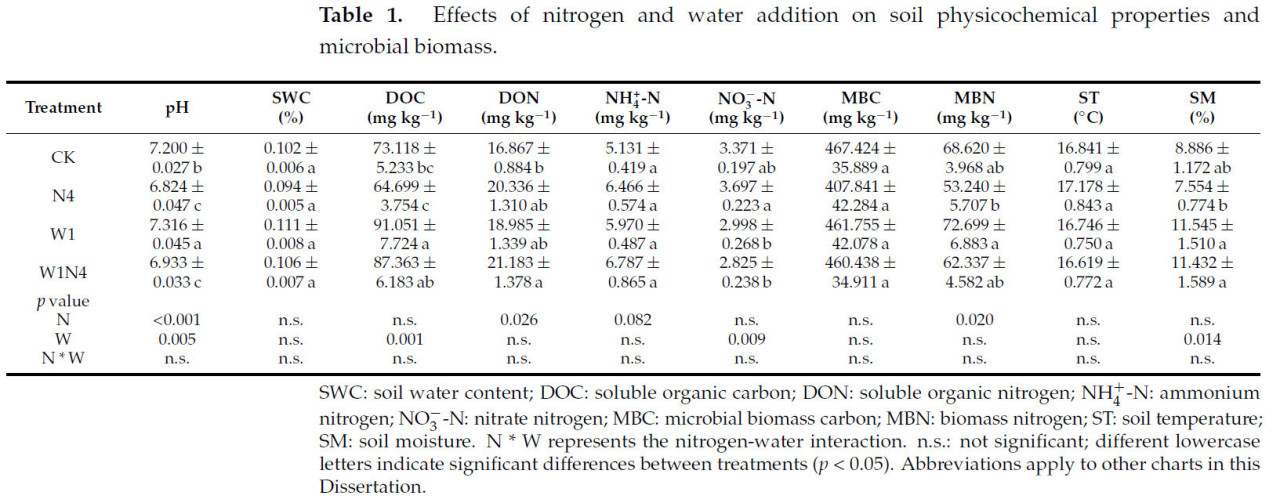
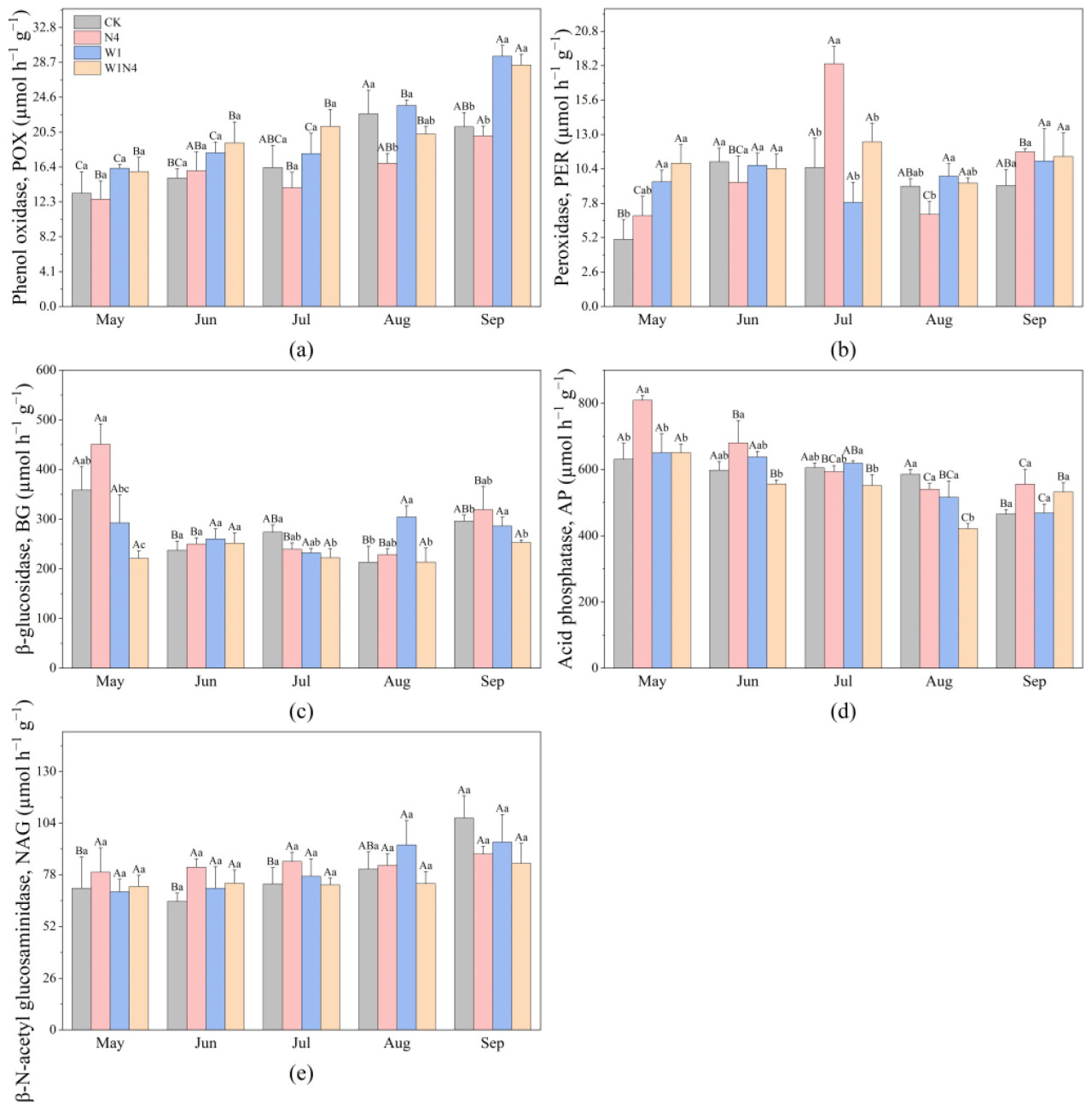
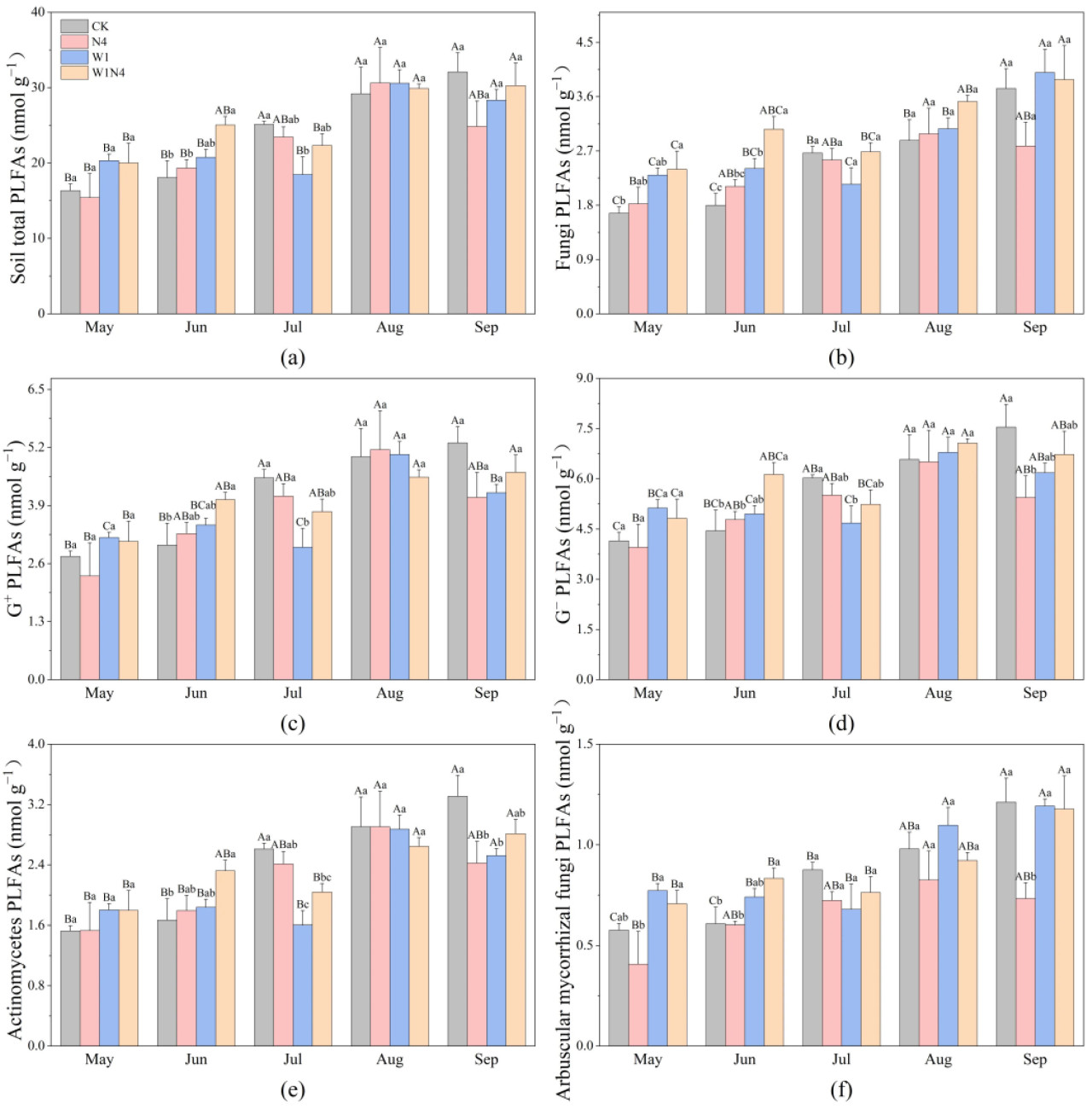
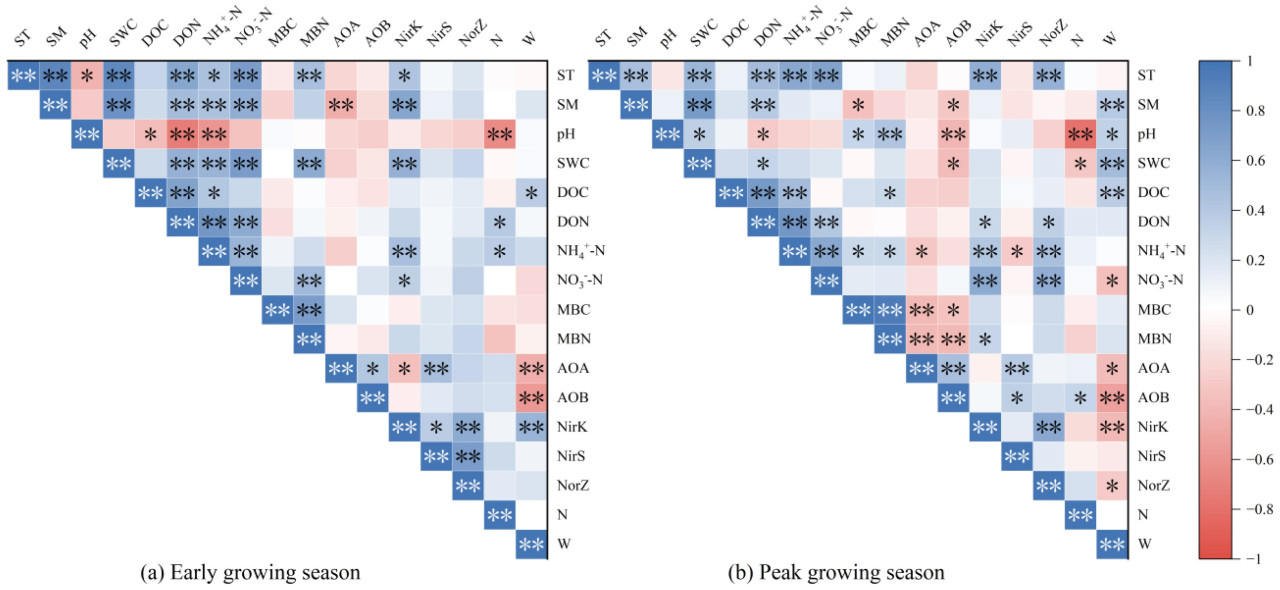

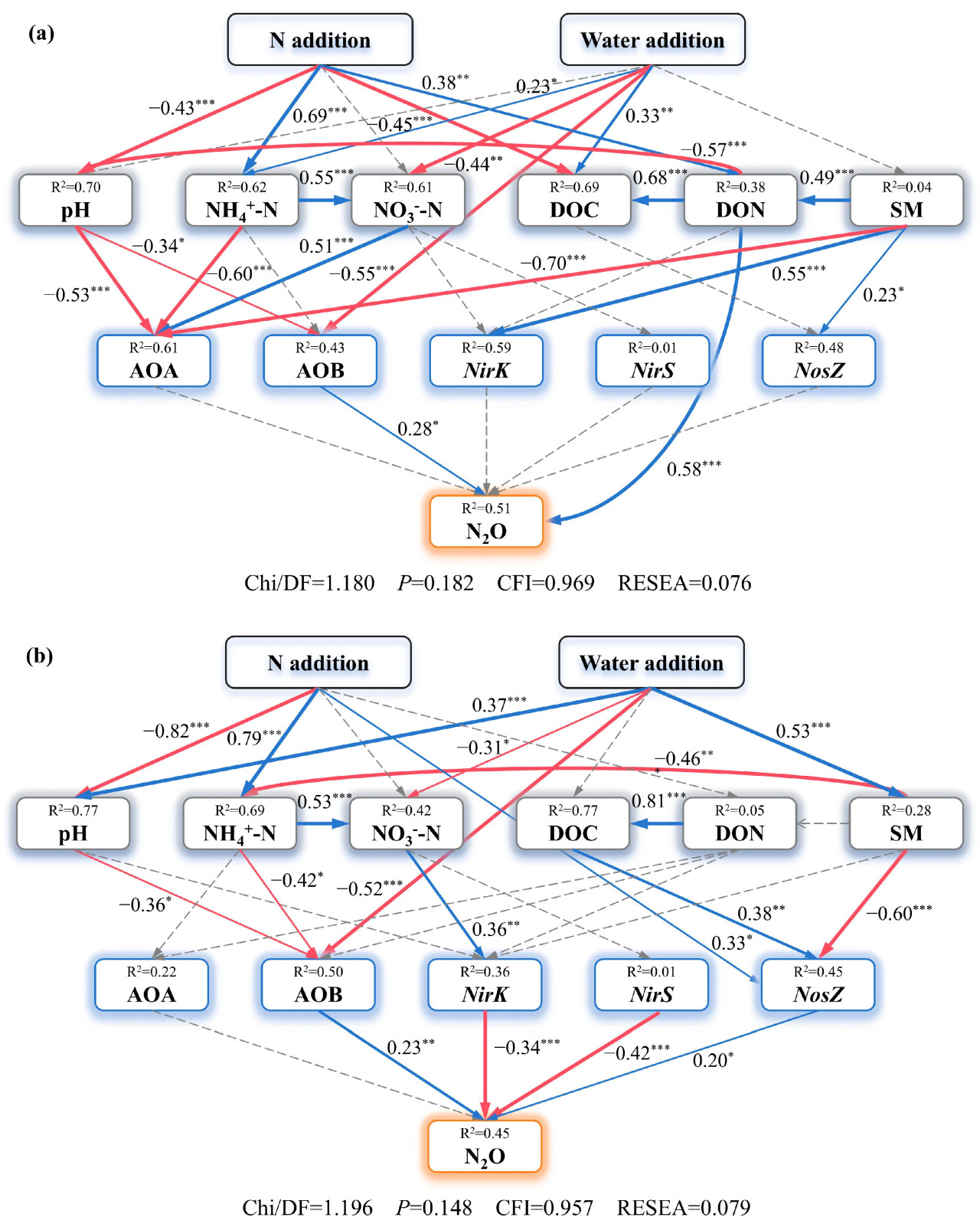















































































































Комментарии (0)